Изобретение относится к медицине, а именно к новым лекарственным препаратам, и может найти применение при лечении заболеваний, связанных с гипертонусом парасимпатической нервной системы, в частности язвенной болезни, бронхиальной астмы, аритмии.
В настоящее время для снижения тонуса парасимпатической нервной системы используются соединения двух фармакологических классов: ганглиоблокаторы (Н-холинолитики) и атропиноподобные средства (М-холинолитики). Известные ганглиоблокаторы имеют тот недостаток, что наряду с блокадой парасимпатических ганглиев они блокируют также и симпатические ганглии, что ведет к таким побочным эффектам, как гипотония, ортостатический коллапс, импотенция. Для атропиноподобных средств характерны такие побочные эффекты, как сухость во рту, гортани, нарушение зрения и аккомодации, тахикардия, затруднение мочеиспускания, запоры, атония кишечника. Довольно узок диапазон терапевтического эффекта такого популярного М-холинолитика, как атропина, у которого соотношение лечебной и токсической доз (терапевтический индекс) составляет всего (1:3) - (1:5). Избавиться от побочных эффектов М-холиноблокаторов подбором доз не удается, так как согласно наблюдениям клиницистов эффективность М-холиноблокаторов, используемых при лечении гастроэнтерологических больных, проявляется только в тех дозах, которые начинают вызывать и побочные эффекты (для атропина это доза 0,5-1 мг и выше). Все вышесказанное относится и к пирензепину (гастрозепину). Приписываемая ему способность избирательно блокировать мускариновые рецепторы на клетках желудочных желез подвергается сомнению. При использовании пирензепина в эффективных дозах он вызывает те же побочные реакции, что и атропин и метацин.
Таким образом, как ганглиоблокаторы, так и атропиноподобные средства, используемые в целях снижения тонуса парасимпатических нервов, имеют существенные недостатки. Ганглиоблокаторы обладают перед М-холинолитиками тем преимуществом, что, вызывая децентрализацию интрамуральной нервной системы, они не влияют на сами ткани гладкомышечных органов и секреторных клеток, которые содержат М-, но не содержат Н-холинорецепторов. В связи с этим, уровень побочных эффектов ганглиоблокаторов по сравнению с М-холинолитиками более низкий, что отмечается клиницистами. В месте с тем подчеркивается, что следует учитывать гипотензивное действие ганглиоблокаторов, которое является главной помехой для использования ганглиоблокаторов в целях защиты от парасимпатических влияний. Ганглиоблокаторы, по сравнению с М-холинолитиками, обеспечивают более полный блок центральных влияний, поскольку через М-холинорецепторы реализуется лишь часть той информации, которая проходит через парасимпатический ганглий. Например, было отмечено, что блокирование периферических М-холинорецепторов не вполне защищает желудочно-кишечный тракт от чрезмерного потока центральных импульсов, которые могут быть причиной заболевания. В этом отношении более эффективными могут быть вещества, которые, наряду с сильными М-холинолитическими свойствами, обладают и некоторым ганглиоблокирующим действием.
В пользу сказанного можно привести следующие данные. Известно, что вагусное освобождение гастрина осуществляется двумя способами: атропиночувствительным механизмом с участием М-холинорецепторов постганглионарных нейронов и атропинорезистентным - путем освобождения бомбензина, являющегося, в свою очередь, сильнейшим стимулятором выхода гастрина. Бомбензиновый механизм освобождения гастрина угнетается ганглиоблокаторами. Следовательно, блок парасимпатической передачи через ганглий должен приводить к более полному блоку желудочной секретации по сравнению с атропином и другими М-холинолитиками.
Утверждают, что в конечном счете дискутабельна не сама целесообразность блокады нервной импульсации к желудке на уровне вегетативных ганглиев. В оправданности такой цели нет поводов сомневаться. Недоказанной остается лишь возможность достигнуть этого без ненужного риска для больного. Излишняя многосторонность эффекта ганглиоблокаторов будет во многом преодолена, если появятся вещества, избирательно действующие на парасимпатические ганглии. Подобных препаратов пока нет.
Целью изобретения является получение веществ, избирательно блокирующих парасимпатические ганглии.
Цель достигается путем применения третичнобутилдециламмоний хлорида (ИЭМ-1678) в качестве средства, снижающего тонус парасимпатической нервной системы
ИЭМ-1678 CH3-(CH2)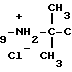 H3 , что может дать возможность использовать его для лечения язвенной болезни, гастрита, пилороспазма, холецистита, желчно-каменной болезни, спазмов кишечника и мочевых путей, бронхиальной астмы, сердечно-сосудистых заболеваний, связанных с усилением парасимпатических влияний на проводящую систему сердца. Возможно также использование его в качестве противоядия при отравлении холиномиметическими и антихолинэстеразными веществами.
H3 , что может дать возможность использовать его для лечения язвенной болезни, гастрита, пилороспазма, холецистита, желчно-каменной болезни, спазмов кишечника и мочевых путей, бронхиальной астмы, сердечно-сосудистых заболеваний, связанных с усилением парасимпатических влияний на проводящую систему сердца. Возможно также использование его в качестве противоядия при отравлении холиномиметическими и антихолинэстеразными веществами.
В отличие от известных ганглиоблокаторов, ИЭМ-1678 способен избирательно снижать тонус парасимпатической нервной системы и тем самым избежать таких побочных эффектов, как гипотония, ортостатический коллапс и импотенция, опасность которой, как показала клиника, особенно велика при курсовом лечении. В отличие от М-холиноблокаторов, ИЭМ-1678 способен обеспечить более полный блок центральных влияний и меньший уровень побочных эффектов.
Имеется только одно сообщение о третичнобутилдециламине (его хлоргидрат, ИЭМ-1678, в литературе не описан), в котором ничего не сообщается о его биологических и физико-химических свойствах и излагается только метод синтеза и выход (23% от теоретического). Соединение получено путем N-алкилирования дециламина сложным металлоорганическим комплексом, содержащим третичнобутил, медь и литий, в тетрагидрофуране при -20оС и продувке кислородом. Такой метод синтеза совершенно неприемлем для промышленного производства, не говоря о низком выходе продукта.
Был разработан простой и пригодный для крупномасштабного заводского производства метод синтеза ИЭМ-1678 по следующей схеме:
Десу1_Br+т-BuNH2___→ Десу1-NHBu-т 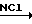 Де
Де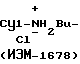 т
т
Данный метод позволяет осуществить производство ИЭМ-1678 из отечественного сырья.
Синтез третичнобутилдециламмоний хлорида (ИЭМ-1678).
Смесь 100 мл (106,8 г, 0,486 моль) бромистого децила, 100 мл (69,6 г, 0,955 моль) третичнобутиламина и 300 мл н-пропанола кипятят 4 ч, охлаждают, подкисляют соляной кислотой, смесь упаривают, остаток подщелачивают, верхний слой амина отделяют, сушат КОН и разгоняют. Сначала отгоняется избыток исходного амина, затем третичнобутилдециламин, выход 94 г (91%), так как 122-126оС /7 мм рт.ст., nд20 1,4335.
Из 94 г амина после подкисления НСl упаривания смеси и перекристаллизации остатка из воды получают 100 г (92% в расчете на исходный амин) третичнобутилдециламмоний хлорида (ИЭМ-1678), белый кристаллический продукт, т. пл. 147-149о.
Вычислено, %: С 67,45; Н 12,82; Сl 14,23; N 5,62.
Найдено, %: С 67,75; Н 12,62; Сl 14,04;
67,80. 12,45. 13,94. N 5,80.
5,94.
Фармакологические методы исследования.
Чтобы оценить способность препарата ИЭМ-1678 снижать тонус парасимпатической нервной системы путем блокирования передачи в парасимпатических ганглиях, был использован ряд известных фармакологических методик на изолированных ганглиях, изолированных органах и на целом животном, где ганглиоблокирующий эффект на различных ганглиях определяли по способности препарата уменьшать на 50% физиологические ответы, вызванные электрической или химической (субехолин) стимуляцией (величины ЕС50 и ЕД50 в опытах in vitro и in vivo, соответственно). Активность ИЭМ-1678 сопоставляли в одном и том же опыте с активностью гексония, наиболее известного и применяемого в клинике ганглиоблокатора. Это сопоставление проводили по способности препарата блокировать проведение как в парасимпатических, так и в симпатических ганглиях. Цель сопоставления состояла в том, чтобы, во-первых, сравнить ИЭМ-1678 с гексонием по способности блокировать проведение через парасимпатические ганглии, и во-вторых, показать избирательность блокирующего действия ИЭМ-1678 на проведение в парасимпатических ганглиях по сравнению с симпатическими, поскольку известные ганглиоблокаторы такой избирательностью не обладают. Данное сопоставление было проведено на морской свинке, крысе, кошке и собаке.
В этих опытах влияние препарата на проведение через парасимпатические (интрамуральные) ганглии, расположенные в стенках таких органов, как желудок, кишка и сердце, изучали по влиянию их на соответствующие функции - сокращение моторику, секрецию, частоту сердечных сокращений. Влияние препарата на проведение через симпатические ганглии изучали по влиянию на сокращение мигательной перепонки кошки, на сокращение семявыносящего протока, по влиянию на артериальное давление и рефлекс Горнера. Сопоставление активности препаратов на парасимпатических и симпатических ганглиях было проведено также в опытах на изолированных ганглиях (цилиарном и верхнем шейном симпатическом ганглии кошки). Механизм ганглиоблокирующего действия ИЭМ-1678 изучали в опытах на одиночных нейронах симпатического ганглия крысы и лягушки.
Снижение тонуса парасимпатической нервной системы является важным фактором при лечении язвенной болезни. Если ИЭМ-1678 способен эффективно блокировать парасимпатическую гиперимпульсацию, то он должен устранять связанную с этим гиперсекрецию желудочного сока, одного из ведущих патогенных факторов при гастрите и язвенной болезни. Поэтому в хронических опытах на собаках было исследовано влияние ИЭМ-1678 (а также гексония, атропина и пирензепина) на желудочную секрецию, вызванную гипертонусом парасимпатического нерва, стимулированного инсулиновой гипогликемией, причем блокирующий эффект ИЭМ-1678 сопоставлен с эффектами гексония и М-холинолитиков - атропина и пирензепина.
В опытах на крысах было также исследовано влияние ИЭМ-1678 на экспериментальные модели поражений слизистой оболочки желудка, в которых существенную роль играет парасимпатическая гиперимпульсация, вызванная нервно-психическим ("социальным") стрессом или иммобилизацией животных на холоду ("холодовой стресс").
После изложения фармакологических опытов на животных приведены данные по острой токсичности и широте фармакологического эффекта в сравнении с гексонием. Затем следуют выводы.
Опыты на морской свинке.
На парасимпатических ганглиях тонкой кишки морской свинки в опытах in vitro величина ЕС50 для ИЭМ-1678 составила 0,1 мкМ, тогда как для гексония 4,5 мкМ, т.е. ИЭМ-1678 в 45 раз активнее гексония. На симпатических ганглиях семявыносящего протока морской свинки ЕС50 для ИЭМ-1678 равно 6,4 мкМ, для гексония - 12 мкМ, т.е. здесь ИЭМ-1678 всего в 2 раза активнее гексония. Таким образом, в опытах на свинке парасимпатическая блокирующая активность ИЭМ-1678 в 22,5 раза выше его симпатической блокирующей активности.
Опыты на крысе.
Опыты in vitro. На парасимпатических ганглиях тонкой кишки крысы величина ЕС50 для ИЭМ-1678 равна 0,4 мкМ, тогда как для гексония 12 мкМ, т.е. ИЭМ-1678 в 30 раз активнее гексония. На парасимпатических ганглиях желудка крысы ЕС50 для ИЭМ-1678 равно 0,38 мкМ, для гексония 11 мкм, т.е. здесь ИЭМ-1678 активнее гексония в 29 раз.
В опытах на изолированной тонкой кишке крысы ИЭМ-1678 неконкурентно угнетает сокращения кишки, вызванные метилфурметидом и хлористым барием, в концентрации ЕС50 = 1,3 ˙ 10-6 М, которая примерно на порядок превышает те, в которых он блокирует интрамуральные ганглии кишечника, т.е. ИЭМ-1678 обладает миотропным спазмолитическим действием. Прямое мышечное релаксирующее действие ИЭМ-1678 может вносить определенный вклад в его противоязвенный эффект, дополняя и углубляя фармакологическую денервацию, вызванную ганглиоблокирующим действием препарата. Гексоний и атропин не обладают сколько-нибудь существенным прямым миотропным действием на гладкую мышцу. ИЭМ-1678 по силе и длительности спазмолитического эффекта в 5-10 раз превосходит такие известные спазмолитики, как папаверин или ношпа. Это может оказаться важным положительным фактором при лечении длительно незаживающих и часто рецидивирующих язв желудка и двенадцатиперстной кишки.
Опыты in vivo. На парасимпатических ганглиях тонкой кишки крысы величина ЕД50 для ИЭМ-1678 равна 0,18 мкм, а для гексония 3,7 мкМ, т.е. ИЭМ-1678 активнее гексония в 20 раз. На парасимпатических ганглиях желудка крысы ЕС50 для ИЭМ-1678 равно 0,2 мкМ, для гексония 4,4 мкМ, т.е. ИЭМ-1678 в 22 раза активнее гексония. Таким образом, в опытах на крысе in vivo ИЭМ-1678 по способности блокировать парасимпатические ганглии кишки и желудка превосходит гексоний в 20-22 раза, а в опытах in vitro - в 29-30 раз.
В то же время, на парасимпатических ганглиях сердца крысы в опытах in vivo ИЭМ-1678 сильнее гексония всего в 1,9 раза. Если сравнить приведенные цифры в опытах in vivo (20-22 для кишки и желудка и 1,9 для сердца), то видно, что блокирующая активность ИЭМ-1678 на желудочно-кишечном тракте примерно на порядок превышает блокирующую активность на сердце, т.е. препарат обладает избирательным действием на желудочно-кишешчный тракт (ЖКТ). Если сравнить не относительные (по гексонию) активности ИЭМ-1678, а прямые значения действующих концнетраций (дозы ЕД50 0,2 и 1,7 мкМ/кг для желудка и сердца крысы, соответственно), то ИЭМ-1678 на ЖКТ в 8,5 раз активнее, чем на сердце.
Блокирующую активность препарата на симпатических ганглиях крысы можно оценить по уменьшению прессорной реакции, вызванной введением субехолина (в/в). В этом тесте величина блокирующей активности (ЕД50) для ИЭМ-1678 составила 2,4 мкМ, для гексония 3 мкМ. Отсюда видно, что если по симпатической блокирующей активности ИЭМ-1678 близок к гексонию (2,4 и 3 мкМ, соответственно), то по парасимпатической блокирующей активности в опытах на крысах он превосходит гексоний в 20-30 раз. Это хорошо коррелирует с данными по гипотензивной активности: если для гексония доза ЕД30, вызывающая гипотензию, превыает дозу ЕД50, вызывающую блок парасимпатических ганглиев желудка, всего в 3 раза (13,9 и 4,4 мкМ/кг, соответственно), то для ИЭМ-1678 - в 112 раз (22,5 и 0,2 мкМ/кг соответственно).
Опыты на кошке.
Опыты на изолированных ганглиях кошки.
Определяли концентрацию ганглиоблокатора, которая снижала на 50% (ЕС50) амплитуду потенциалов действия, вызванных преганглионарной стимуляцией. Величины ЕС50 для парасимпатического (цилиарного) и симпатического (верхнего шейного) ганглиев кошки составили для ИЭМ-1678 1,8 ˙ 10-6 М и 3,8 ˙ 10-6 М, а для гексония - 385 ˙ 10-6 и 116 ˙ 10-6 М, соответственно, т.е. на изолированном парасимпатическом ганглии ИЭМ-1678 в 214 раз сильнее гексония, а на симпатическом - 30 раз. Если избирательность оценивать путем прямого сопоставления блокирующих доз ЕС50 для обоих типов ганглиев, то она составит для ИЭМ-1678 3,8 ˙ 10-6(1,8 ˙ 10-6 = 2,1 раза, а для гексония 116 ˙ 10-6) 385 ˙ 10-6 = 0,3 раза. Т.е. если гексоний в 3,3 раза сильнее блокирует симпатические ганглии кошки по сравнению с парасимпатическими (цилиарными), то ИЭМ-1678, наоборот, в 2,1 раза сильнее блокирует парасимпатические ганглии по сравнению с симпатическими. Относительно меньшая избирательность действия ИЭМ-1678 на изолированных ганглиях по сравнению с той, что получена в опытах на кишке крысы и свинки, возможно, связана со структурно-функциональными отличиями цилиарных ганглиев от интрамуральных ганглиев кишечника.
Опыты на кошке in situ.
Способность препарата блокировать верхний шейный симпатический ганглий (ВШСГ) кошки определяли по способности уменьшать на 50% (ЕД50) сокращение мигательной перепонки кошки в ответ на преганглионарное раздражение. При внутриартериальном введении непосредственно к ВШСГ активность ИЭМ-1678 составила 0,08 от активности гексония, при внутривенном введении - 0,05-0,07. Таким образом, ИЭМ-1678 блокировал ВШСГ наркотизированной кошки в 12-20 раз слабее гексония как при внутривенном, так и при внутриартериальном введении.
В другой постановке опытов о способности препарата блокировать симпатические ганглии судили по гипотензивному эффекту, о способности блокировать парасимпатические ганглии сердца - по ослаблению урежения сердечного ритма, вызванного раздражением блуждающего нерва, а о способности блокировать парасимпатические ганглии двенадцатиперстной кишки - по ослаблению двигательной реакции, вызванной раздражением блуждающего нерва.
Для ИЭМ-1678 величина ЕД50, характеризующая блок парасимпатических ганглиев сердца и кишки, составила в среднем 0,46 и 0,58 мг/кг, а для гексония - 0,19 и 0,18 мг/кг, соответственно. ИЭМ-1678 при указанных дозах ЕД50 не уменьшал артериальное давление, тогда как гексоний в дозе 0,19 мг/кг уменьшал давление на 10%. Устойчивый и длительный гипотензивный эффект (снижение артериального давления на 20 мм рт.ст.) ИЭМ-1678 вызывал лишь начиная с дозы 2 мг/кг, а блок проведения в верхнем шейном симпатическом ганглии - в дозах 2,5-4 мг/кг. Таким образом, ИЭМ-1678 блокирует парасимпатические ганглии сердца и кишки в дозах, которые в 4-8 раз меньше доз, снижающих артериальное давление и блокирующих проведение в верхнем шейном симпатическом ганглии кошки.
ИЭМ-1678 отличается от гексония более плавным наступлением ганглиоблокирующего эффекта и большей его длительностью. Так, время достижения максимального эффекта и длительность действия на сердце в дозе ЕД50 составили для ИЭМ-1678, соответственно 22 мин и 65 мин (для гексония 5 мин и 22 мин), на артериальное давление - 10 мин и 86 мин (для гексония 5 мин и 18 мин).
Никакого влияния на дыхание ИЭМ-1678 не оказывал вплоть до 5 мкМ/кг. В дозах 20-30 мкМ/кг он вызывал кратковременное усиление дыхания. Нервно-мышечное проведение не блокировалось в дозах до 30 мкМ/кг.
ИЭМ-1678 не проявил мускаринолитического действия в отношении мускариновых рецепторов подтипа М1. В опытах на наркотизированной кошке в дозах до 4 мкМ/кг внутриартериально он не предупреждал сокращения мигательной перепонки, вызваного внутриартериальным введением к ганглию МсN-А-343, избирательно активирующего М1-рецепторы ганглионарных нейронов. В то же время уже в дозе 1 мкМ/кг (0,25 мг/кг) он на 80% подавлял ответ, вызванный никотиновым агонистом субехолином или электрическим раздражением преганглионарного ствола. Отсутствие мускаринолитического действия у ИЭМ-1678 на мускариновые рецепторы подтипа М1 было также подтверждено в опытах на изолированных симпатических ганглиях лягушки: он не предупреждал деполяризацию ганглионарных нейронов (при внутриклеточном отведении), вызванную мускариновым агонистом метилфурметидом.
Таким образом, ИЭМ-1678 является ганглиоблокатором, избирательно действующим на парасимпатические ганглии, причем для его эффекта характерно постепенное развитие и большая продолжительность. В дозах, блокирующих проведение в парасимпатических ганглиях, он не влияет на артериальное давление, дыхание, нервно-мышечную передачу и на мускариновые М1-рецепторы. Дыхание и нервно-мышечную передачу он не угнетает даже в дозе 30 мкМ/кг (7,5 мг/кг), которая в 15 раз превышает дозу ЕД50, блокирующую проведение в парасимпатических ганглиях кишки и сердца.
Опыты на собаке.
Влияние ИЭМ-1678 на моторику желудка.
В хронических опытах на собаке величина ЕД50, тормозящая инсулиновую моторику желудка, равна мг/кг, : в/в 0,07; п/к 0,2; в/киш. 0,3, а ЕД50, тормозящая пищевую моторику желудка, равна, мг/кг,: в/в 0,3; п/к 0,6; в/киш 1,2. Разница в дозах ИЭМ-1678, угнетающих инсулиновую и пищевую моторику, свидетельствует о способности ИЭМ-1678 в определенном интервале доз вызывать фармакологическую ваготомию, при которой достигается децентрализация ауэрбаховского сплетения без нарушения межнейронных отношений в самом сплетении. При этом сохраняется способность автономной интрамуральной регуляции функций желудочно-кишечного тракта.
Гексоний, вследствие блокады им симпатических ганглиев, в дозе 0,25-0,5 мг/кг углубляет инсулиновую гипогликемию до уровня, вызывающего кому и быструю смерть собаки. Это делает невозможным испытание гексония на фоне инсулиновой моторики и секреции. Пищевую моторику гексоний тормозит в дозе ЕД50 3 мг/кг, в/в, т.е. в 10 раз слабее по сравнению с ИЭМ-1678.
Способность ИЭМ-1678, в отличие от гексония, тормозить инсулиновую моторику и секрецию без заметных побочных эффектов говорит о том, что он является избирательным парасимпатическим блокатором. Это же подтверждается отсутствием у данного препарата способности вызывать гипотенсивный эффект и синдром Горнера (тест на симпатическую блокирующую активность) вплоть до дозы 2 мг/кг, в/в.
Влияние ИЭМ-1678 на секрецию желудка.
Для ИЭМ-1678 величина ЕД50, блокирующая инсулиновую секрецию желудочного сока, равна 0,02 мг/кг (в/в), 0,15 мг/кг (п/к) и 0,25 мг/кг (в/киш.). Соответствующие значения для атропина - 0,02 мг/кг (в/в). 0,03 мг/кг (п/к) и 0,06 мг/кг (в/киш.), для пирензепина - 0,2 мг/кг (в/в), 0,3 мг/кг (п/к), 2 мг/кг (в/киш.).
Таким образом, ИЭМ-1678 в данном тесте не уступает атропину по активности при в/в введении и превосходит по активности пирензепин при в/в - в 10 раз, при п/к - в 2 раза и при в/киш. - в 8 раз. Из этих данных, а также с учетом известных исследований следует, что ИЭМ-1678 является первым ганглиоблокатором, способным эффективно блокировать инсулиновую секрецию. Это достигается благодаря тому, что при данных дозах ИЭМ-1678 не блокирует симпатические ганглии и не уменьшает артериальное давление. Кроме того, это первый ганглиоблокатор, активность которого по определенным антисекреторным тестам находится на уровне наиболее активных М-холинолитиков.
Гексоний неспособен тормозить инсулиновую секрецию из-за присущего ему симпатического блокирующего эффекта.
ИЭМ-1678 обладает также способностью угнетать пентагастриновую секрецию желудка (пентагастрин 6 мкг/кг, п/к). Дозы ЕД50, блокирующие пентагастриновую секрецию, для ИЭМ-1678, атропина и пирензепина равны, соответственно: в/в 0,01, 0,03 и 0,3 мг/кг и п/к 1,3, 0,4 и 0,4 мг/кг. При подкожном введении ИЭМ-1678 в дозе 2 мг/кг количество желудочного сока уменьшается от 120 до 40 мл, дебит кислоты от 17 до 5,1 ммоль/л, дебит пепсина от 17,6 до 8,8 мг (усредненные данные). Никаких видимых побочных эффектов при этом не наблюдалось.
Опыты на одиночных нейронах симпатического ганглия крысы.
Исследовали влияние ИЭМ-1678 на трансмембранный ток, вызываемый ацетилхолином (АХ) в нейронах верхнего шейного ганглия крысы. Обнаружено, что ИЭМ-1678 обладает каналоблокирующим действием, поскольку действие ИЭМ-1678 на АХ-ток усиливается при гиперполяризации мембраны и после предварительной активации холинорецепторов.
По постоянной времени восстановления второго ответа при парной аппликации АХ в присутствии блокатора определено значение константы скорости деблокирования открытых каналов к-в, которая для ИЭМ-1678 при 20-23оС и 50 мВ составила в среднем 0,022 с-1, тогда как для гексония к-в >10 c-1. Таким образом, длительность существования комплекса ИЭМ-1678 с открытым каналом холинорецептора составляет 45 с, тогда как для гексония менее 0,1 с. Различие длительности существования комплекса с открытым каналом более чем в 450 раз означает, что ИЭМ-1678 связывается с открытым каналом намного сильнее, чем гексоний. Величина к-в для ИЭМ-1678 зависит от потенциала: 0,022 с-1 при -50 мВ и 0,2 с-1при +10 мВ.
Установлено, что процесс блокирования-деблокирования открытых каналов холинорецепторов соединением ИЭМ-1678 может многократно воспроизводиться в условиях парной аппликации АХ даже после полного удаления блокатора из раствора. При этом кинетика деблокирования каналов и ее потенциалозависимость являются приблизительно такими же, как и в присутствии блокатора. Предполагается, что блокирование открытого канала холинорецептора соединением ИЭМ-1678 происходит после необратимой фиксации последнего на молекуле рецептора, которая осуществляется с помощью децильного радикала. В пользу такой роли децильного радикала говорит тот факт, что процесс многократного блокирования-деблокирования после удаления блокатора из раствора имеет место также для дециламмоний хлорида (аналога ИЭМ-1678 с N+H3-группой при дециле), с тем лишь отличием, что длительность существования комплекса с открытым каналом составляет для него около 0,5 с, т.е. в 90 раз меньше, чем в случае ИЭМ-1678. Это также свидетельствует о значительном вкладе в связывание с каналом третичнобутильной группы при N-атоме молекулы ИЭМ-1678.
Отмеченные особенности блокирования соединением ИЭМ-1678 говорят о том, что это - представитель нового класса каналоблокирующих агентов. Большая длительность и эффективность действия ИЭМ-1678 в опытах на животных связана, по-видимому, с необычно длительным существованием комплекса ИЭМ-1678 с открытым каналом холинорецептора, в 450 раз превышающим гексоний, и с необратимой фиксацией препарата на рецепторе.
Опыты на крысах по предупреждению и лечению поражений слизистой оболочки желудка.
На модели экспериментального ульцерогенеза ("социальный стресс") ИЭМ-1678 проявил выраженную способность защищать слизистую оболочку желудка крыс от эрозивно-язвенных и геморрагических поражений, вызываемых действием стресса. В дозе 4 мг/кг препарат проявил примерно такой же защитный эффект от эрозивно-язвенных поражений, как бензогексоний в дозе 10 мг/кг, пирензепин (гастрозепин) в дозе 12,5 мг/кг и Н2-блокатор циметидин (тагамет) в дозе 15 мг/кг (все тесты здесь и далее - при внутрибрюшинном введении, в/б). Из соотношения доз видно, что ИЭМ-1678 в 2,5-3 раза активнее гексония, пирензепина и циметидина.
Важным показателем антиязвенной активности является защита от геморрагических поражений (массивных кровоизлияний) слизистой оболочки желудка. Здесь ИЭМ-1678 в дозе 1 мг/кг проявил очень высокий защитный эффект, тогда как бензогексоний, пирензепин и циметидин даже в больших (на порядок) дозах оказались практически неэффективными.
Так, количество геморрагических поражений в контроле составило, в среднем 2,8, а при введении ИЭМ-1678 (1 мг/кг) 0,2, т.е. уменьшилось в 14 раз. Размер одного поражения (в среднем) на одно животное составил: в контроле 4,7 мм2, а в присутствии ИЭМ-1678 0,2 мм2, т.е. в 23 раза меньше.
ИЭМ-1678 проявил также способность защищать слизистую оболочку желудка от эрозивно-язвенных и геморрагических поражений, вызываемых серотонином.
Противоязвенный эффект препаратов оценивается с помощью индекса Паулса ( индекс изъязвления) и индекса площади изъязвления:
Индекс Паулса = 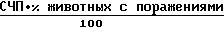 ,
,
ИНдекс площади изъявления = 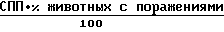 , где СЧП - среднее число поражений на одно животное в группе;
, где СЧП - среднее число поражений на одно животное в группе;
СПП - средняя площадь поражения.
Чем меньше величина индекса, тем активнее защитный эффект препарата. Индекс Паулса на модели "социального стресса" составил: в контроле 2,4, для ИЭМ-1678 0,54 (1 мг/кг) и 0,75 (4 мг/кг), для бензогексония 1,2 (10 мг/кг), для пирензепина 2,7 (12,5 мг/кг). Индекс площади изъязвления составил: в контроле 4,7, для ИЭМ-1678 1,2 (1 мг/кг) и 0,9 (4 мг/кг). Из полученных результатов видно, что ИЭМ-1678 проявляет противоязвенный эффект в несколько раз больший, чем гексоний и пирензепин, хотя дозы двух последних препаратов были на порядок выше.
На модели генерализованного стресса (иммобилизация животных при 4-6оС) ИЭМ-1678 проявил выраженную способность защищать слизистую оболочку желудка крыс от эрозивных и геморрагических поражений, вызываемых стрессом, при профилактическом (предупреждающем) действии. При применении ИЭМ-1678 с лечебной целью препарат вводили сразу после стресса и последующие двое суток 2 раза в день.
При профилактическом действии ИЭМ-1678 в дозе 4 мг/кг проявил примерно такое же защитное действие, как и бензогексоний в дозе 10 мг/кг. Индекс Паулса составил: в контроле 13,4; для ИЭМ-1678 9,6; для бензогексония 9,0. Таким образом, по соотношению доз ИЭМ-1678 в 2,5 раза активнее гексония.
При оценке лечебного эффекта препарата индекс площади изъязвления для ИЭМ-1678 в дозе 4 мг/кг составил 8, а для бензогексония в дозе 10 мг/кг 20,3. Следовательно, даже в меньшей дозе, чем гексоний, ИЭМ-1678 в 2,5 раза активнее бензогексония по способности уменьшать площадь изъязвлений.
Определение токсичности.
Острая токсичность ИЭМ-1678, определенная в опытах на мышах, характеризуется величиной ЛД50, равной 26 мг/кг при в/в введении и 85 мг/кг при внутрибрюшинном введении. Для гексония дибромида в тех же условиях эксперимента 82,8 мг/кг (в/в) и 180 мг/кг (в/бр).
Широту фармакологического эффекта можно оценить отношением ЛД50 к ЕД50. Если для сравнения использовать ЕД50, которая отражает способность препарата блокировать парасимпатическую иннервацию желудка крысы в опытах in vivo, то ее величина для гексония дибромида равна 1,59 мг/кг, а для ИЭМ-1678 0,05 мг/кг. Тогда широта фармакологического эффекта для ИЭМ-1678 и гексония при в/в введении составит, соответственно, 520 (26/0,05) и 52 (82,8/1,59), а при в/бр введении 1700 (85/0,05) и 113 (180/1,59). Таким образом, широта фармакологического эффекта для ИЭМ-1678 больше, чем у гексония, в 10 раз при в/в введении (520/52), и в 15 раз при в/бр введении (1700/113).
Таким образом, препарат ИЭМ-1678 в качестве средства для снижения тонуса парасимпатической нервной системы обладает следующими преимуществами перед известными ганглиоблокаторами и М-холиноблокаторами, используемыми для этой цели:
в отличие от известных ганглиоблокаторов, ИЭМ-1678 в дозах, блокирующих проведение в парасимпатических ганглиях, не вызывает побочных эффектов, связанных с блокадой симпатических ганглиев, таких, как гипотензия, ортостатический коллапс, импотенция;
по сравнению с М-холинолитиками, ИЭМ-1678 обеспечивает более полный блок центральных влияний и меньший уровень побочных эффектов, поскольку ИЭМ-1678, в отличие от М-холинолитиков, не блокирует М-холинорецепторы гладких мышц и способен вызывать фармакологическую ваготомию, при которой сохраняется автономная саморегуляция внутренних органов, тогда как М-холинолитики ее полностью подавляют;
ИЭМ-1678 значительно активнее гексония по способности блокировать передачу в парасимпатических ганглиях: в 214 раз на изолированном цилиарном ганглии, в 29-45 раз в опытах на кишке крысы in vitro и в 20-22 раза - в опытах на кишке крысы in vivo;
преимуществом ИЭМ-1678 перед гексонием и другими ганглиоблокаторами является медленное развитие ганглиоблокирующего эффекта, что уменьшает опасность ортостатического коллапса даже при сильном превышении лечебной дозы. Так, в опытах на кошках максимум ганглиоблокирующего эффекта гексония (в дозе ЕД50) наступает через 3-5 мин, тогда как при действии ИЭМ-1678 через 22 мин;
по длительности действия ИЭМ-1678 превосходит гексоний. Если блокирующий эффект гексония в опытах на кошке (в дозе ЕД50) прекращается через 22 мин после введения, то ИЭМ-1678 - через 65 мин.;
ИЭМ-1678 более эффективно, чем гексоний и пирензепин, подавляет желудочную секрецию, вызванную инсулином или пентагастрином. При инсулиновой секреции ИЭМ-1678 превосходит по активности пирензепин при в/в введении в 10 раз, при п/к в 2 раза, при в/киш в 8 раз, не уступая атропину по активности при в/в введении, тогда как гексоний неспособен тормозить инсулиновую секрецию из-за присущего ему симпатического блокирующего эффекта;
ИЭМ-1678 в 2,5-3 раза активнее гексония, пирензепина и Н2-блокатора циметидина по способности защищать слизистую оболочку желудка крыс от эрозивно-язвенных поражений. Особенно эффективным ИЭМ-1678 оказался при защите от геморрагических поражений (массивных кровоизлияний) слизистой оболочки желудка, тогда как гексоний, пирензепин и циметидин практически не проявили защитного эффекта в данном тесте. ИЭМ-1678 проявил здесь не только предупреждающее, но и лечебное действие;
широта фармакологического эффекта ИЭМ-1678 в 10-15 раз больше по сравнению с гексонием;
ИЭМ-1678 удовлетворительно всасывается в желудочно-кишечном тракте и может назначаться внутрь. Так, в хронических опытах на собаке дозы ЕД50, тормозящие моторику желудка, различались при в/в и в/киш введении всего в 4 раза, тогда как для пирензепина - в 10 раз;
ИЭМ-1678 может использоваться для снижения парасимпатического тонуса у больных диабетом (вынужденных постоянно принимать инсулин), тогда как гесоний, блокируя симпатические ганглии, усиливает гипогликемию и, следовательно, создает угрозу гипогликемического шока;
препарат ИЭМ-1678 отличается уникальной простотой промышленного синтеза, получается из доступных и дешевых полупродуктов, с высоким выходом и очень простой процедурой очистки (кристаллизация из воды);
ИЭМ-1678 может оказаться перспективным для замены ряда дорогих дефицитных импортных препаратов;
вся совокупность свойств ИЭМ-1678 позволяет отнести его к новому классу фармакологически активных веществ - избирательным блокаторам парасимпатических ганглий.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-АЛКИЛ-ТРОПИНЫ И N-АЛКИЛ-НОРТРОПИНЫ С н-ЛИТИЧЕСКОЙ, ПРОТИВОПАРКИНСОНИЧЕСКОЙ, ПРОТИВОЭПИЛЕПТИЧЕСКОЙ, АНАЛЬГЕЗИРУЮЩЕЙ И АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2597616C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЯЗВЕННОЙ БОЛЕЗНИ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2000 |
|
RU2179439C1 |
| СПОСОБ ЗАЩИТЫ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ В ПРОЦЕССЕ ОПЕРАЦИИ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА НА РАБОТАЮЩЕМ СЕРДЦЕ | 2001 |
|
RU2200552C1 |
| СПОСОБ СИМПАТИЧЕСКОЙ ГАНГЛИОНАРНОЙ БЛОКАДЫ | 1991 |
|
RU2069559C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕВРИТА СЛУХОВОГО НЕРВА | 2001 |
|
RU2195272C1 |
| СПОСОБ КОНСЕРВАТИВНОГО ЛЕЧЕНИЯ ПАРЕЗА И ПАРАЛИЧА КИШЕЧНИКА ПРИ РАЗЛИТОМ ГНОЙНОМ ПЕРИТОНИТЕ У ДЕТЕЙ | 1992 |
|
RU2038078C1 |
| ПРИМЕНЕНИЕ ГИДРОХЛОРИДА 1-ФЕНИЛ-1-(1`-МЕТИЛЦИКЛОПЕНТИЛ)-4-ПИПЕРИДИНО-2-БУТИН-1-ОЛА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО М1 ХОЛИНОБЛОКИРУЮЩЕЙ АКТИВНОСТЬЮ | 2004 |
|
RU2273478C2 |
| СПОСОБ ЛЕЧЕНИЯ ДВИГАТЕЛЬНЫХ НАРУШЕНИЙ ГОРТАНИ | 2002 |
|
RU2236223C2 |
| Миорелаксант теркуронии | 1975 |
|
SU685289A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГИПОЛИПИДЕМИЧЕСКИМИ СВОЙСТВАМИ | 2008 |
|
RU2392933C2 |
Изобретение относится к медицине, в частности к фармакологии, к новым лекарственным препаратам, и может быть использовано для лечения заболеваний, связанных с гепертонусом парасимпатического нерва, таких, как язвенная болезнь, бронхиальная астма, аритмия. Средство представляет собой третичнобутилдециламмоний хлорид, который по своим фармакологическим свойствам является избирательным блокатором парасимпатических ганглиев и в отличие от известных ганглиоблокаторов не вызывает побочных эффектов, связанных с блокадой симпатических ганглиев, таких, как гипотензия, ортостатический коллапс, импотенция. По сревнению с M-холинолитиками, данное средство обеспечивает более полный блок центральных явлений и меньший уровень побочных эффектов: препарат не блокирует M-холинорецепторы гладких мышц и способен вызывать фармакологическую ваготонию, при которой сохраняется автономная саморегуляция внутренних органов, тогда как M-хилинолитики ее полностью подавляют. По сравнению с известным ганглиоблокатором гексонием данное средство в 20 - 40 раз активнее по способности подавлять передачу в парасимпатических ганглиях кишки крысы, отличается большей (в 10 раз) широтой фармакологического эффекта, большей длительностью действия, более плавным и медленным развитием ганглиоблокирующего эффекта и высокой способностью защищать слизистую оболочку желудка крыс от эрозивно-язвенных и геморрагических поражений.
Применение третичнобутилдециламмоний хлорида в качестве холинолитического средства.
Авторы
Даты
1994-06-15—Публикация
1987-12-30—Подача