Изобретение относится к химии, конкретно к улучшенному способу получения бензамида.
Известны способы получения бензамида из метилового эфира бензойной кислоты взаимодействием с аммиаком в присутствии катализатора типа хлористого алюминия [Заявка Японии 79 76501, кл. C 07 C 103/00] или при большом избытке аммиака при температуре выше 100оС под давлением [Дормидонтова Н.В., Уставщиков Б.Ф., Фарберов М.И., Ученые записки Ярославского технологического института, 1971, т. 22, вып.1, стр.77-82. Скорость реакции аммонолиза эфиров α -оксикислот и их корреляции по уравнению Тафта].
Известны способы получения бензамида из этилового эфира бензойной кислоты взаимодействием с водным аммиаком при нагревании до 100оС [Сompt. rend. Acad. Sci., 1847, v.25, p.734] или при нагревании со спиртовым аммиаком; при этом бензамид выделен с низким выходом [Fischer E., Dilthey A., Ber., 1902, B. 35 (1), N 3, S.844-856. Einwirkung von Ammiak auf die Alkylmalonester.]
Наиболее близок предлагаемому способу способ получения бензамида, заключающийся в том, что этиловый эфир бензойной кислоты подвергают взаимодействию с аммиаком в растворе метанола в присутствии катализатора. В качестве катализатора используют цианистый натрий. При этом в закрытом сосуде при 50оС при экспозиции 50 ч конверсия эфира составляла 79%, а реальный выход 64% . В отсутствии цианистого натрия конверсия не превышает 57% [Hogberg T. , Strom P., Ebner M., Ransby S., J. Org. Chem., 1987, v.52, N 10, p.2033-2036, Cyanide as an Efficient and Mild Cataiyst in the Aminolysis of Esters] (прототип).
Недостатком способа-прототипа является низкий выход целевого продукта и использование ядовитого катализатора.
Целью изобретения является упрощение процесса, повышение его экологической безопасности и повышение выхода целевого продукта. Поставленная цель достигается способом получения бензамида, заключающимся в том, что метиловый эфир бензойной кислоты подвергают взаимодействию с аммиаком в водном метаноле в присутствии катализатора, которым в данном способе является вода, при массовом соотношении метиловый эфир бензойной кислоты:метанол:водный аммиак (25%-ный) 1:(5-10):(4,5-7), обычно при комнатной температуре.
Для выделения целевого продукта целесообразно удалить избыточное количество аммиака и метанола, непрореагировавший метилбензоат отогнать с паром и кристаллизовать целевой продукт из воды с добавлением небольшого количества аммиака.
Таким образом, по предлагаемому способу все непрореагировавшие реагенты могут быть регенерированы и использованы в последующих циклах. Следовательно, предлагаемый способ экологически безопасен.
Хотя амидирование эфиров карбоновых кислот является обычным методом получения амидов в органической химии неоднократно осуществлялись попытки его применения к эфирам бензойной кислоты, низкая скорость реакций и обратимость процессов не позволяли надеяться на его практическое осуществление для синтеза бензамида. Это иллюстрируется работами Гордона с соавторами (Gordon M. , Miller J.G., Day A.R. J. Am. Chem. Soc., 1948, v.70, N 5, p. 1946-1953. Effect of structure on reactivity. I.; Gordon M., Miller J.G., Day A.R. ibid., 1949, v.71, N 4, p.1245-1250. ibid. II.) по изучению кинетики аммонолиза различных сложных эфиров. В отличие от эфиров кислот жирного ряда эфиры ароматических кислот и, в частности бензойной, оказываются практически инертными в реакциях аммонолиза. В одинаковых условиях относительная скорость аммонолиза метилбензоата составляет всего 8% от скорости аммонолиза метилацетата (табл. 6, Gordon M., Miller J.G., Day A.R. ibid., 1949, v.71, N 4, p.1245-1250. Effect of structure on reactivity. II.)
Сравнение скоростей аммонолиза эфиров бензойной кислоты показывает, что спиртовой остаток мало влияет на реакционную способность в реакции аммонолиза эфиров бензойной кислоты (табл.4, Gordon M., Miller J.G., Day A.R. ibid. , 1949, v.71, N 4, p.1245-1250. Effect of structure on reactivity. II.)
Эмилем Фимером [Fischer E., Dilthey A., Ber., 1902, B. 35 (I), N 3, S. 844-856. Einwirkung von Ammiak auf die Alkylmalonester.] показано, что многочасовое нагревание этилбензоата с большим избытком насыщенного при 0оС спиртового аммиака при 25оС приводит к образованию бензамида с выходом 5%, а при 175оС - 1,7%. В силу изложенного достижение положительного эффекта по предлагаемому способу является неожиданным, а способ получения бензамида аммонолизом метилбензоата в водном аммиака при комнатной температуре не мог быть предложен a priori.
Подбор оптимальных условий проведения процесса неожиданно позволил получить бензамид с высоким выходом и высокого качества экологически чистым и по существу безотходным способом.
На стадии аммонолиза повышение температуры процесса безусловно приводит к повышению скорости аммонолиза, однако при этом еще более существенно увеличиваются скорости побочных реакций и получить чистый целевой продукт сразу не удается, а требуются дополнительные операции по его очистке.
Увеличение количества аммиака способствует увеличению выхода бензамида, однако для сохранения реакционной массы гомогенной приходится увеличивать количество метанола, что разбавляет реакционную массу и приводит к увеличению необходимой длительности процесса.
Отличительными особенностями предлагаемого способа являются использование в качестве исходного соединения метилового эфира бензойной кислоты, а в качестве катализатора воды, при массовом соотношении бензойная кислота: метанол:водный аммиак (25%-ный) 1:(5-10):(4,5-7).
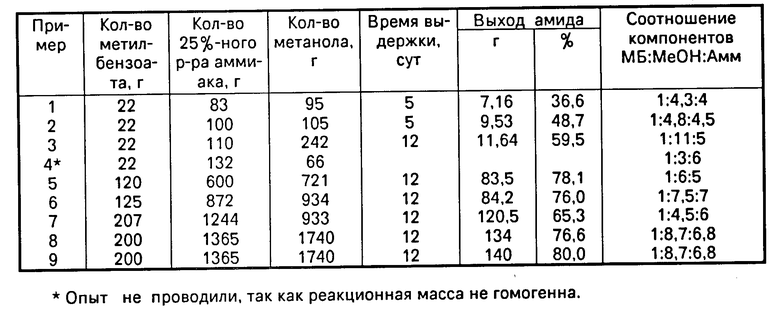
П р и м е р ы 1-9. К метиловому эфиру бензойной кислоты добавляют 25% -ный водный раствор аммиака и метиловый спирт в количестве, необходимом для образования гомогенной реакционной массы. Смесь выдерживают при комнатной температуре в течение указанного в таблице времени. Аммиак и метанол удаляют, непрореагировавший метилбензоат отгоняют с водяным паром до тех пор, пока отгон не станет абсолютно прозрачным. При охлаждении бензамид выкристаллизовывается. Получают амид бензойной кислоты с т.пл. 128-129оС.
Сущность изобретения: продукт-бензамид, т.пл. 128-129°С. Реагент 1: метиловый эфир бензойной кислоты. Реагент 2: NH3 в CH3OH . Условия реакции: в присутствии воды при массовом соотношении метиловый эфир бензойной кислоты: CH3OH в NH3 водн. 25%-ном 1:(5-10):(4,5-7) преимущественно при комнатной температуре. 1 з.п. ф-лы, 1 табл.
| Day A.R | |||
| tbid., 1949, v.71, N 4, р.1245-1250. |
Авторы
Даты
1994-09-15—Публикация
1992-06-25—Подача