Изобретение касается применения магний-пиридоксаль-5'- фосфатглютамината для предупреждения болезней, вызываемых связанными пероксидами и приводящих к повреждению сосудов.
В последние четыре десятилетия в западных индустриальных странах наблюдается быстрый рост нарушений обмена веществ, главным образом, нарушений жирового обмена веществ. Основная причина этого в чрезмерной пище и/или употреблении жирных продуктов при одновременном ограничении движения. При этих условиях увеличивается содержание холестерина и липида в крови, в результате возрастает вероятность атеросклеротических сердечных и периферийных сосудистых заболеваний. Известно, что повышенные уровни холестерина в крови вызывают появление артериальных сосудистых склерозов. Гиперхолестеромия нарушение обмена веществ, которое всегда сопровождает гиперлипидемию. Патогенетически различные, но симптоматически сходные клинические картины гиперлипидемии (замутнение сыворотки хилус-микронами) и гиперхолестеремии (увеличение содержания холестерина в плазме крови до уровня более 200 мг%) суммированы в общие понятия гиперлипопротеинемия или гиперлипидемия.
Для лечения гиперхолестеремии преимущественно используются производные арилоксиуксусной кислоты, в особенности этиловые эфиры альфа-(n-хлорфенокси)-изомасляной кислоты, а также производные никотиновой кислоты. Кроме этого, используют для лечения и профилактики гиперхолестерамии глютаминовые эфиры пиридоксин-5-фосфорной кислоты.
При характеристике клинической картины гиперхолестерамии или гиперлипидемии необходимо учесть, что сосудистые заболевания вероятны для подвергающейся опасности группы лиц группы "риска", а именно: курильщиков, диабетиков, престарелых с высоким кровяным давлением, лиц, испытывающих сильные волнения (стрессы). Это является следствием присутствия в крови повышенной концентрации пероксидов, связанных с LDL (липопротеин низкой плотности). Эти LDL связанные пероксиды вызывают и ускоряют образование стеромы и атеросклеротических "бляшек" в сосудах и могут рассматриваться, как случай диабетической ангиопатии.
Известно, что атеросклеротические изменения в сосудах являются результатом эндотелиальных повреждений и патогеназ продолжается следующим образом: эндотелийное повреждение пластинчатая адгезия размножение клеток одинаковой силы отложение липида.
Первая стадия эндотелийное повреждение может иметь множество случаев, а именно: механическое повреждение рассекающими силами, а случае гипертонии; химическое повреждение холестерином при гиперхолестеремии, в частности токсическое повреждение (отравление) из-за заражений крови. Полагают, что другие направления почти идентичны с тремя указанными типами поражений.
Результат эндотелийного повреждения, так же, как последующего жирового отложения между (и в) клетками артериальной системы: повышенное скопление тромбоклеток, сопровождаемое размножением клеток одинаковой силы, приводящее к дальнейшему увеличенному накоплению липопротеинов в соединительной ткани основного вещества, образованию комплекса с амино-глиценом глюкозы в соединительной ткани и нарушением обмена веществ на клеточном уровне. Затем образование кальция в пораженных зонах завершает все изменения, которые в конечном счете, вызывают сужение сосудов.
Исследования, выполненные на гиперхолестеромичных кроликах и крысах В. Шнейдером в его диссертации (завершенной в 1987 г.) в Университете Йоханна Гутенберга, Мейнц, показали, что при введении относительно высоких концентраций магний-пиридоксаль-5-фосфат-глютамината (МПФГ) снижаются концентрации липида в аорте. Но эта работа не дает каких-либо сведений по механизму, который приводит к образованию сосудистой атеромы в группах "риска" (согласно результатам В. Шнейдера), и нельзя заключить, что образование атеромы может быть предупреждено исключением имеющихся в крови загрязнений.
В прошлом предполагали, что пероксиды в крови могут инициировать нарушения обмена веществ У.П.Шнейберг и др. в I.Biol.Chem. vol.264, N 26 pages 15216 to 15223 (1989) указали на наличие окислительно-модифицированных LDL в качестве рецепторов этого. Изобретением доказы- вается (на основании целеустремленных опытов), что это вызвано LDL-связанными пероксидами. Опытами, прове- денными in vitro, могла быть внесена ясность в один из механизмов, лежащий в основе токсического эндотелийного повреждения, и было показано, что можно вводить эти пероксиды, а их применение безвредно.
Предмет изобретения фармацевтическое обеспечение LDL-связанных пероксидов для того, чтобы избежать и/или замедлить сосудистые повреждения, в частности образование атером или артериосклеротических образований в артериальных сосудах, так же как ангиопатических заболеваний в случае диабета. Предметом настоящего изобретения при этом, в частности, является фармацевтическое обеспечение указанных случаев при отсутствии диагнозов гиперлипидемии или гиперхолестерамии.
Это достигается использованием магний-пиридоксаль-5'-фосфат- глютамината с получением лекарственного препарата, пригодного для профилактики болезней, вызываемых сосудистыми повреждениями, в частности, согласно изобретению, предотвращаются атероматоз, так же как и ангиопатические болезни у подверженных заболеваниям групп лиц, включающих диабетиков, курильщиков, престарелых, гипертоников и лиц, испытывающих стрессы.
Магний-пиридоксаль-5'-фосфат-глю- таминат вещество, которое предпочтительно было использовано для снижения повышенного содержания жира в крови. Вещество (МПФГ) известно под торговым названием СедалипидRи распространяется фирмой Steigerwald Arzneimittelwerk. До сих пор было известно, что магний-пиридоксаль-5-фосфат-глюминат действует как радикальный интерцептор в крови и поэтому возможно предотвращение цепной реакции, вызванной пероксидом липида. На основе этого эффекта (как радикального интерцептора) использование МПФГ пригодно для профилактики сосудистых повреждений, в особенности при отсутствии гиперлипидемии и/или гиперхолестерамии.
МПФГ является производным пиридоксина и имеет следующую формулу:
Mg 1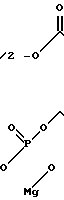
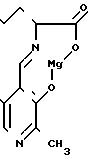
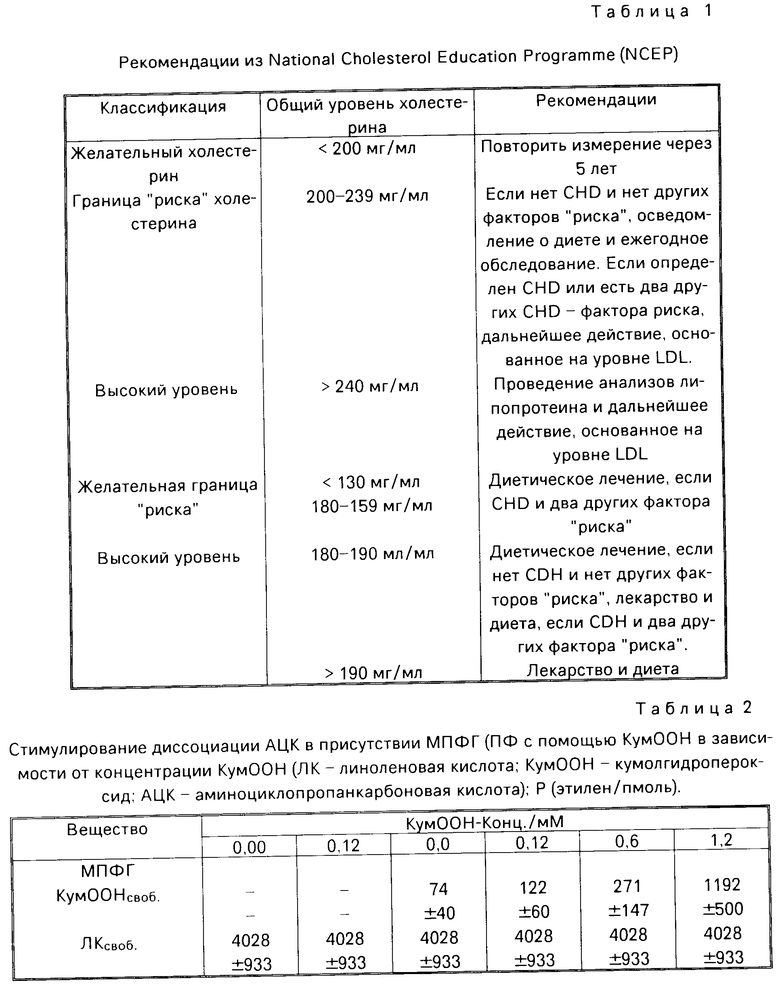
Соединение МПФГ вводится лицам "риска", имеющим высокую концентрацию LDL-связанных пероксидов, однако не испытывающим симптомы гиперлипидемии и/или гиперхолестерамии. Эти симптомы обычно определяются на основе уровней холестерина и триглицерида. В Европе, так же, как и в США, существуют рекомендации по уровням холестерина и триглицерида, которые могут считаться нормальными. Эта ссылка относится к рекомендациям National Cholesterol Education Programme (NCEP) США и указаниям The European Atherosclerosis Society Study Graep.
В табл. 1 и 2 приведены значения нормальных уровней холестерина и триглицерида, а также рекомендации по лечению.
Рекомендации
The Europen Atherosclerosis Society Study Graep
Тип А:Холестерин: 200 250 мг/мл (5,2-5 ммоль/л)
Триглицериды: < 200 мг/мл (2,3 ммоль/л)
Оценить общий "риск" CHD, принимая во внимание наследственность на CHD, повышенное кровяное давление, диабет, мужской пол, молодость, курение, низкий HDL холестерина (< 35 мг/дл)
Ограничить калорийность пищи при избыточном весе: дать консультации по питанию и нейтрализовать другие присутствующие факторы "риска".
Тип В: Холестерин 250 300 мг/мл (6,5-7,8 ммоль/л)
Триглицерид < 200 мг/мл (< 2,3 ммоль/
/л) Оценить общий "риск" CHD, как указано для типа А. Ограничить калорийность пищи (при избытке веса), предписать липидпонижающую диету, проверить ее выполнение и последствия. Если холестерин остается высоким, следует использовать липидснижающее лекарство.
Тип С: Холестерин 200 мг/мл (5,2 ммоль/л)
Триглицерид 200 500 мг/мл (2,3-5,6 ммоль/л) Искать лежащие в основе причины гипертриглицеридемии, например ожирение, избыточное потребление алкоголя, мочегонных средств, диабет "бета-блокадники" эксогенный эстроген. Ограничить калорийность диеты (при избытке веса), рассмотреть лежащие в основе причины. Предписать и контролировать липидпонижающую диету. Контролировать уровни холестерина и триглицерида.
Тип D: Холестерин 200- 300 мг/дл (5,2-7,8 ммоль/л)
Триглицерид 200- 500 мг/дл (2,8-5,6 ммоль/л) Оценить общий "риск" CHD, как в типе А. Искать причины гипертриглицеридемии, как в типе С. Ограничить калорийность диеты (при избыточном весе), рассмотреть причины гипертриглицеридемии согласно типу А или В. Предписать и контролировать липидпонижающую диету, если реакция сыворотки липида неадекватна и общий "риск" CHD высок, следует использовать липидснижающее лекарство.
Тип Е: Холестерин > 300 мг/мл (7,8 ммоль/
/ л)
и/или
Триглицерид > 500 мг/мл (5,6 ммоль/л) Следует направить в "липидную" клинику или к врачу-специалисту для обследования и назначения лечения диетой и, если необходимо, лекарствами.
Существуют также подобные опубликованные рекомендации British Cardiac Society Working Group on Coronary Prevention, the British Hyperlipidaemia Association ant the Canadian Consensus Conference of Cholesterol.
Из приведенных данных ясно, что имеются незначительные отличия в значениях уровня "вредного" холестерина. Тем не менее полезно достижение уровней ниже пограничных или в средней зоне между еще нормальным и повышенным уровнями с помощью введения МПФГ согласно изобретению, что благотворно сказывается для всех групп лиц, подверженных заболеванию, имеющих высокий уровень LDL-связанных пероксидов.
Хотя не определена граница уровня холестерина, вызывающего гиперлипидемию, предполагают, согласно общему подходу, что примерно 240 мг/мл (в соответствии с рекомендациями США) или 250 мг/мл (в соответствии с рекомендациями EG) могут быть приняты как начало гиперлипидемии. Следовательно, при введении МПФГ достигаются значения ниже указанных уровней холестерина.
Заявителем выполнены исследования, ясно показывающие, что у группы лиц "риска" наблюдаются высокие уровни LDL-связанных пероксидов. Было также показано, что при добавлении МПФГ исчезают симптомы, характерные для LDL-связанных пероксидов. Таким образом, было выявлено, что применение МПФГ пациентами, отнесенными к группе "риска", является оправданным и полезным.
При ускорении образования атеромы, особенно у указанной выше группы лиц, предполагают следующий механизм, который подтверждается описанными ниже опытами in vitro: LDL окисляется кислородсодержащим реагентом (перекисный радикал О2-, гидроксил радикал ОН), в частности пероксидом, который присутствует в крови, с образованием LDL-пероксида. Этот LDL-пероксид в основном не абсорбируется макрофагами, но связывает отработанный рецептор, который отлагается в эндотелийных клетках, В этом случае LDL-отложения образуются на эндотелийных клетках, которые затем притягивают дальнейшие липидные отложения.
Дальнейшее повреждение сосудов эндотелийных клеток вызывается окислением глютатиона пероксида и/или LDL-связанными пероксидом. Это окисление может привести к гибели клеток, так как клетка не может больше поддерживать окислительно-восстановительный потенциал.
Исследования, проведенные на основе насыщенной кислоты, связанной пероксидами, показывают, что последняя разлагается в присутствии МПФГ и становится поэтому вредной.
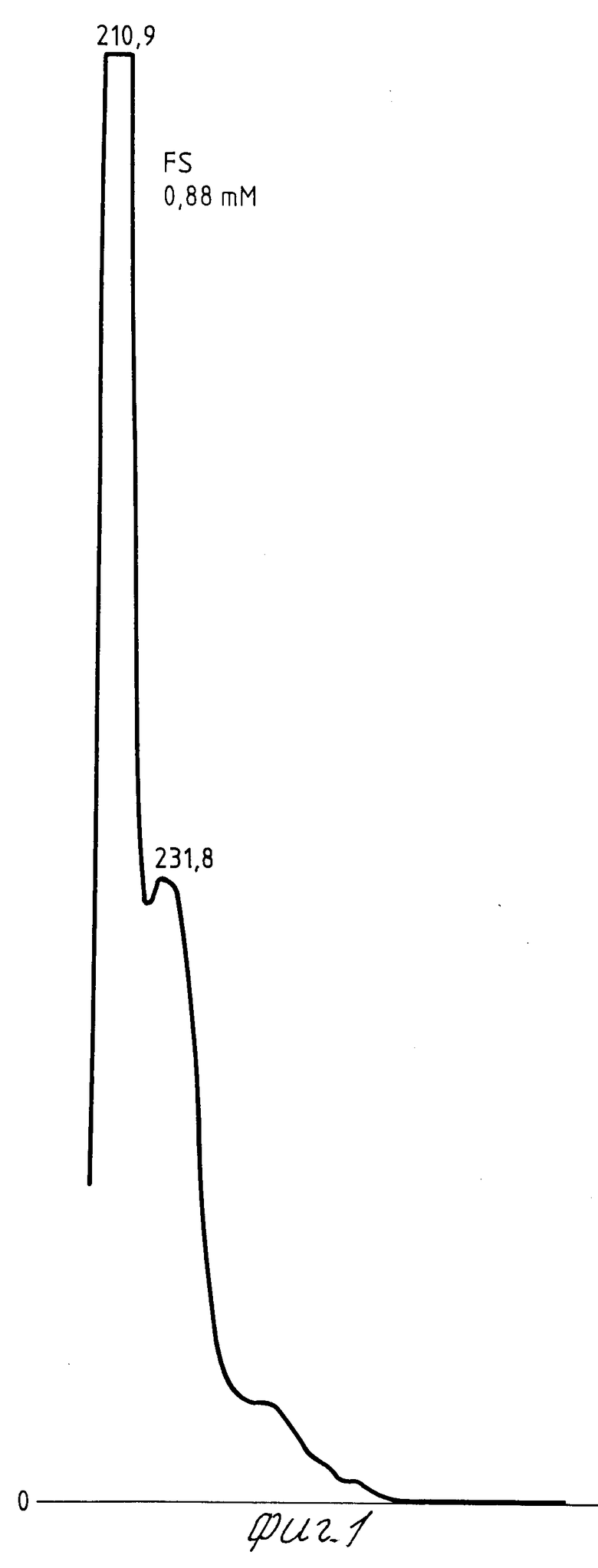
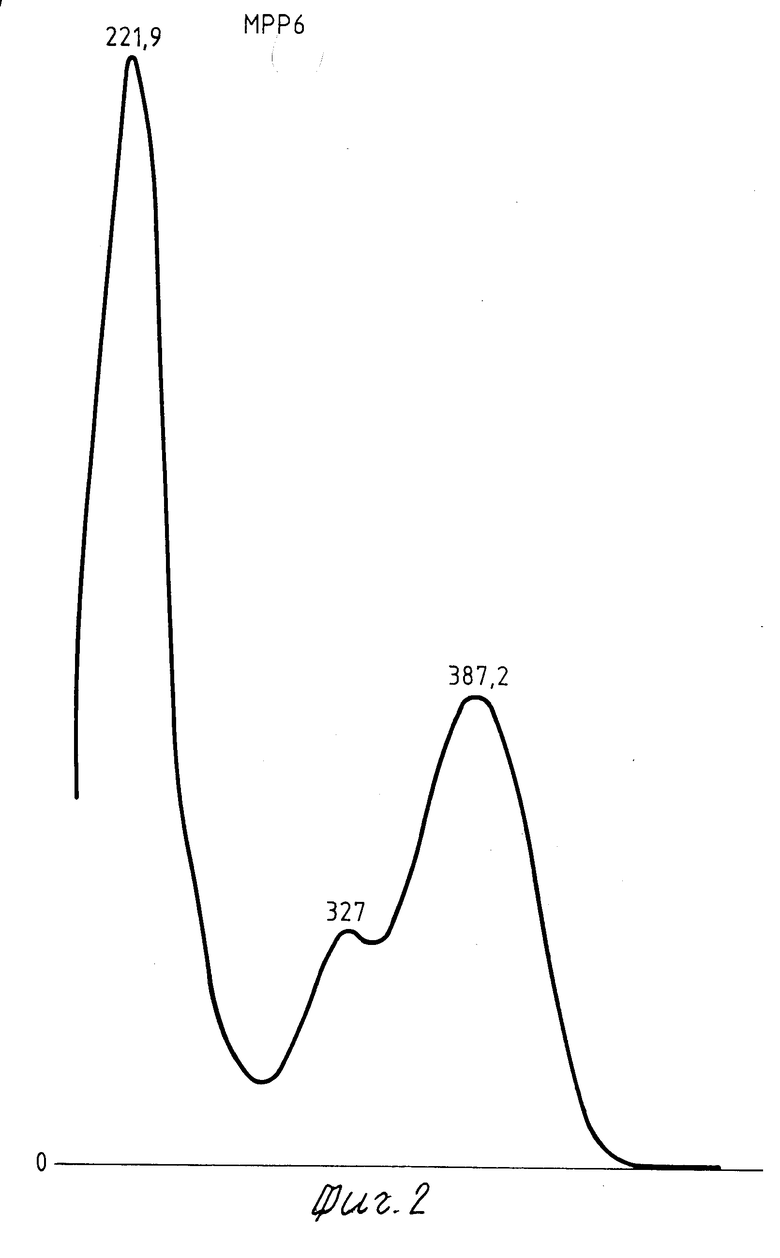
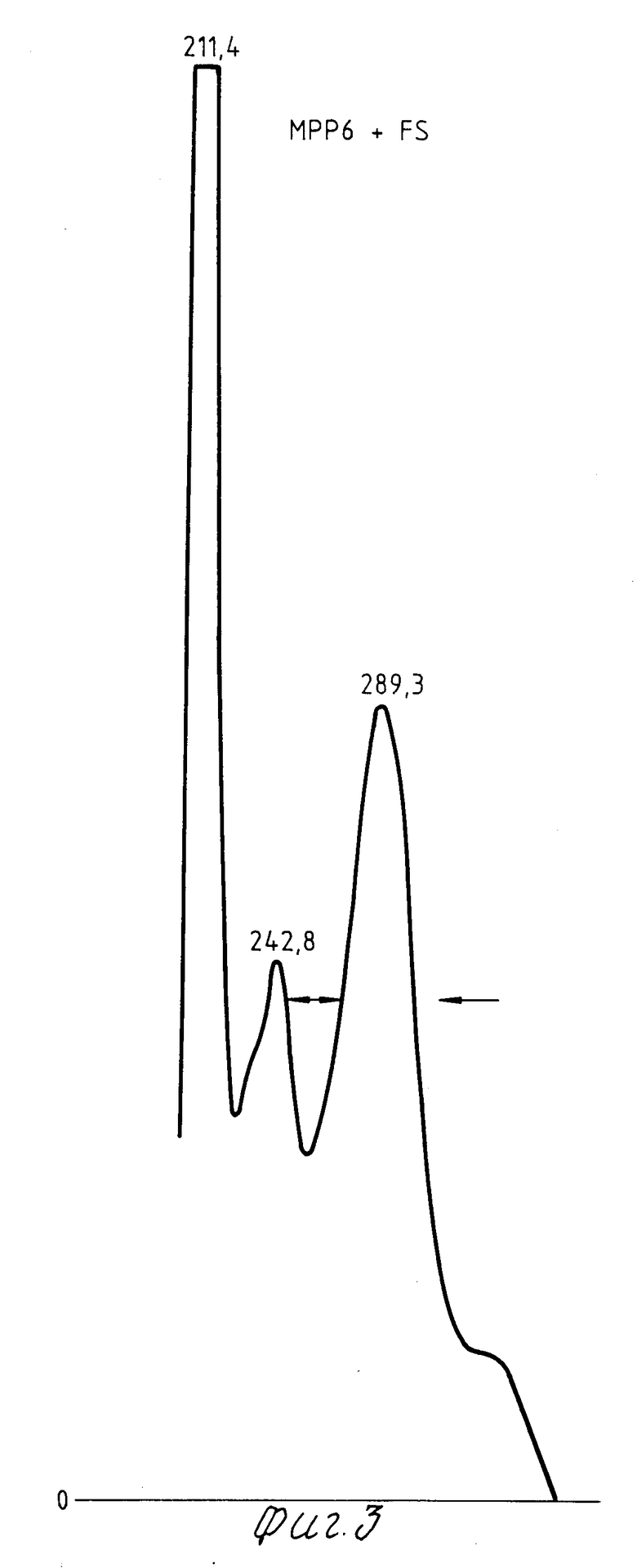
На фиг.1 показан спектр линоленовой кислоты (0,88 мМ). Основной пик при 211 нм, в то время, как около 232 нм имеется наименьший пик, характеризующий присутствие небольшого количества окисленной линоленовой кислоты; на фиг.2 спектр МПФГ (концентрация 0,125 мМ), который имеет пики при 222, 327 и 387 нм; на фиг.3 спектр раствора линоленовой кислоты и МПФГ.
Этот спектр имеет пики при 211, 243 и 248 и 289 нм.Пик, полученный ранее (на фиг.1) при 232 нм, незначительно присутствует на фиг.3. Высота этого на фиг.3 показаны два новых пика при 248 и 289 нм.
Следующая схема отражает предполагаемый механизм процесса окисления насыщенной кислоты как описано.


Первоначальное воздействие на мостиковую группу СН2-оказывается Н-радикалом. Это вызывает перегруппировку с образованием сопряженных двойных связей. Результатом является образование радикала насыщенной кислоты, который образует в присутствии кислорода пероксидный радикал. В присутствии следующей молекулы насыщенной кислоты образуется гидропероксид насыщенной кислоты, а также радикал насыщенной кислоты, благодаря чему начинается цепная реакция.
Реакционная схема, показанная выше, может служить подтверждением (при 284 нм) диеновой реакции.
Из фиг. 1-3 может быть заключено, что пик для окисленной линоленовой кислоты исчезает при 232 нм (фиг.1) за счет прибавления МПФГ в концентрации 0,125 мМ (фиг.1), что вызывает прекращение цепной реакции, приведенной выше, и поэтому болезнь не прогрессирует.
Для разложения гидропероксида в присутствии вещества МПФГ, применяемого в соответствии с изобретением, предполагается следующий механизм с участием марганца как катализатора:
Предполагаемый механизм разложения гидропероксида МПФГ-Mn (катализатор)
Магний-пиридоксаль- Протеин амино-группы свободный бира-
5'-фосфат-глютаминат NH2- ->>NH= дикал (N-центры)
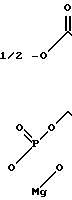
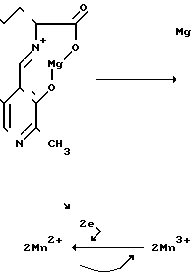
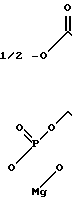
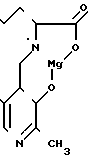
Доказательство протекания этой реакции разложения возможно с использованием индикатора аминоцикло- пропан-карбоновой кислоты (АЦК). АЦК основное вещество, из которого в организме образуется этилен. Выделяющийся этилен может быть определен количественно.
Разложение гидропероксида может быть подтверждено, например, с гидропероксидом кумола. АЦК служит индикатором. Предполагают, что реакция протекает через амин в пиридоксаль-фосфат, который вызывает образование радикала. Этот радикал инициирует разложение АЦК на С2Н4СО2и цианид.
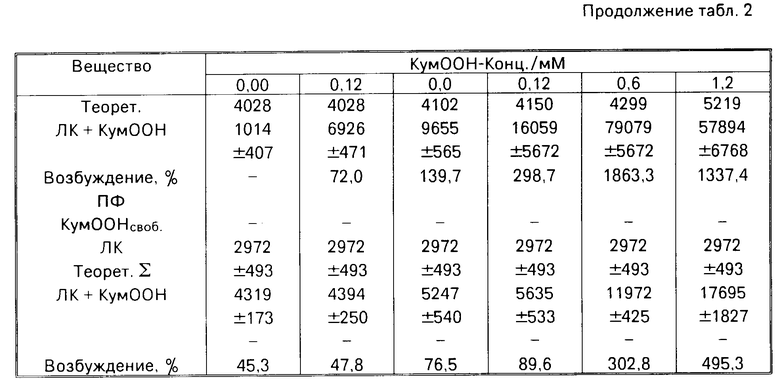
Следующие эксперименты показывают стимулирование диссоциации АЦК с ПМФГ в присутствии гидропероксида кумола в зависимости от концентрации гидропероксида кумола (КумООН). При одном и том же времени были выполнены сравнительные испытания c соответствующими количествами (молярные отношения пиридоксальфосфата (ПФ).
П р и м е р. Были приготовлены следующие растворы в буферном фосфате (0,1 М) рН 7,4 с различными концентрациями гидропероксида кумола. Загрузка: фосфат буфер 0,1 М и рН 7,4. АЦК: 1,0 мМ МПФГ 0,5 мМ Mn2+ 0,1 мМ ЛК 0,88 мМ КумООН 0,006-1,2 мМ
Дистиллированная вода 2 мл
На фиг. 4 показано возбуждение диссоциации АЦК с помощью МПФГ или ПФ в зависимости от концентрации КумООН.
При диссоциации АЦК с пиридоксальфосфатом наблюдалось умеренное выделение этилена в противоположность случаю с МПФГ, при более низкой концентрации кумолгидропероксида (0,00 мМ). При 0,12 мМ КумООН в присутствии МПФГ было обнаружено возбуждение диссоциации АЦК на 70% При концентрации 0,6-0,12 мМ отмечены несомненно более высокие возбуждающие эффекты в присутствии МПФГ в сравнении с ПФ.

Изобретение относится к медицине. Сущность изобретения: применение магний-пиридоксаль-5-фосфат глютамината, при необходимости содержащего марганцевую соль, для профилактики сосудистых заболеваний, обусловленных действием гликопротеинсвязанных пероксидов. 2 табл. 4 ил.
Применение магний-пиридоксаль-5-фосфат глютамината, при необходимости содержащего марганцевую соль, в качестве средства для профилактики сосудистых заболеваний, обусловленных действием гликопротеинсвязанных пероксидов.
| ОЁ ПОЛУЧЕНИЯ | 0 |
|
SU203649A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1995-08-20—Публикация
1991-05-24—Подача