Настоящее изобретение относится к фармацевтическим композициям, содержащим специфические антитела к пропротеину конвертазы субтилизина/кексина типа 9 (PCSK9) или их антигенсвязывающий фрагмент, предпочтительно, содержащим ингибитор 3-гидрокси-3-метил-глутарил-КоА-редуктазы (HMG-CoA-редуктазы). Настоящее изобретение также относится к инъекционным растворам, сухим составам и лекарственным формам, содержащим PCSK9-специфические антитела к или их антигенсвязывающие фрагменты, а также к их применению (предпочтительно, в комбинации с ингибитором HMG-CoA-редуктазы) для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9.
Настоящее изобретение также относится к изделиям, содержащим упаковку, PCSK9-специфические антитела или их антигенсвязывающие фрагменты, и этикетку или вкладыш в упаковку, в которой, например, указаны группы пациентов, которых можно лечить с помощью указанных антител или фрагментов, группы пациентов, которых нельзя лечить указанными антителами или фрагментами, и режим дозирования, который должен быть использован.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Пропротеин конвертазы субтилизина/кексина типа 9 (PCSK9) является пропротеином конвертазы подсемейства К-протеиназ семейства секретируемых субтилаз. Кодированный белок синтезируется в виде растворимого зимогена, который подвергается автокаталитическому внутримолекулярному процессингу в эндоплазматическом ретикулуме (ЕР). Имеющиеся данные свидетельствуют о том, что PCSK9 увеличивает уровни LDL холестерина (холестерина, относящегося к липопротеинам низкой плотности) в плазме, промотируя деградацию рецептора LDL, который опосредует эндоцитоз LDL в печени, являясь главным выведения LDL из циркуляции. Структура белка PCSK9 показывает, что он имеет сигнальную последовательность, затем продомен, каталитический домен, который содержит консервативную триаду остатков (D186, H226 и S386), и С-концевой домен. Он синтезируется в виде растворимого 74 кДа предшественника, который подвергается автокаталитическому расщеплению в ЕР, формируя 14 кДа продомен и 60 кДа каталитический фрагмент. Было показано, что его автокаталитическая активность требуется для секреции. После его расщепления, продомен остается жестко связанным с каталитическим доменом.
Антитела к PCSK9 описаны, например, в WO 2008/057457, WO 2008/057458, WO 2008/057459, WO 2008/063382, WO 2008/125623 и заявке США на патент № 2008/0008697. Антитела против PCSK9, которые, в частности, особенно хорошо подходит для целей настоящего изобретения, раскрыты в заявке на патент США № 2010/0166768 А1, содержание которой включено в настоящее описание в качестве ссылки в полном объеме.
ТЕХНИЧЕСКИЕ ПРОБЛЕМЫ, ЛЕЖАЩИЕ В ОСНОВЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Статины являются одними из наиболее широко используемых лекарственных средств в мире. Хотя статины обычно обладают высокой безопасностью, желательно дополнительно оптимизировать профиль безопасности за счет снижения и без того низкого уровня нежелательных побочных эффектов (например, миопатии).
Несмотря на широкую доступность гиполипидемических препаратов, таких как статины, в Соединенных Штатах в период между 1999 и 2006, приблизительно 30% всех взрослых пациентов, подвергавшихся лечению по поводу гиперхолестеринемии, не смогли достичь рекомендуемого для них уровня LDL-C. Причинами этого являются плохое соблюдение режима терапии, невосприимчивость/непереносимость лекарственных средств и наличие положительной связи между нежелательными явлениями и увеличением дозировки. Кроме того, поскольку наиболее эффективные гиполипидемические препараты могут уменьшить уровень LDL-C только на 55%, то достигаемые мишеневые уровни у пациентов, таких как с семейной гиперхолестеринемией, для которых требуется существенное снижение LDL-C, зачастую значительно ниже, чем ожидаемые. В этой связи для этих пациентов являются необходимыми более эффективные гиполипидемические средства и режимы лечения для достижения целевых уровней.
Авторы настоящего изобретения абсолютно неожиданно обнаружили, что введение антител против PCSK9 или их фрагментов увеличивает активности статинов по снижению LDL холестерина, при введении с конкретными режимами дозирования и/или при введении конкретным группам пациентов.
Таким образом, совместное введение антител против PCSK9 или их фрагментов повышает эффективность статинов и позволяет уменьшить дозы статинов, тем самым снижая нежелательные побочные эффекты.
Кроме того, авторы настоящего изобретения обнаружили, что конкретные режимы дозирования антител против PCSK9 и/или статинов, лучше подходят для снижения уровней LDL холестерина, чем другие. Авторы изобретения также обнаружили, что некоторые подгруппы пациентов получают большую выгоду, чем другие пациенты, в случае лечения их антителами против PCSK9 или их фрагментами и/или статинами. Авторы изобретения также обнаружили, что лечение антителами против PCSK9 или их фрагментами и/или статинами противопоказано для некоторых подгрупп пациентов.
Вышеприведенный обзор не может в полной мере описать все задачи, решаемые настоящим изобретением.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В первом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей антитело или его антигенсвязывающий фрагмент, специфически связывающий пропротеин конвертазы субтилизина/кексина типа 9 (PCSK9) вместе с фармацевтически приемлемым эксципиентом или носителем.
Во втором аспекте настоящее изобретение относится к инъекционному раствору, описанному в настоящем документе, содержащему антитело или его антигенсвязывающий фрагмент по изобретению, и, предпочтительно, содержащему в 1 мл объема от приблизительно 40 мг до приблизительно 200 мг или от приблизительно 50 мг до приблизительно 200 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг указанного антитела или его антигенсвязывающего фрагмента.
В третьем аспекте настоящее изобретение относится к сухому составу, описанному в настоящем описании, содержащему антитело или его антигенсвязывающий фрагмент по изобретению, и, предпочтительно, содержащему от приблизительно 40 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 400 мг, от приблизительно 50 мг до приблизительно 300 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг и, более предпочтительно, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг и, еще более предпочтительно, приблизительно 150 мг, приблизительно 200 мг или приблизительно 300 мг антитела или его антигенсвязывающего фрагмента на одну дозу.
В четвертом аспекте настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту, содержащемуся в одной из фармацевтических композиций согласно девятнадцатому аспекту настоящего изобретения.
В пятом аспекте настоящее изобретение относится к лекарственной форме, содержащей антитело, его антигенсвязывающий фрагмент или фармацевтическую композицию по настоящему изобретению.
В шестом аспекте настоящее изобретение относится к изделию, содержащему фармацевтическую композицию по изобретению, жидкий состав по изобретению или сухой состав по изобретению, антитело или его антигенсвязывающий фрагмент по изобретению, или одну или несколько лекарственных форм по изобретению, и контейнер или пакет.
В седьмом аспекте настоящее изобретение относится к фармацевтической композиции или антителу или его антигенсвязывающему фрагменту по изобретению для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9. Если в следующих вариантах осуществления изобретения по седьмому аспекту указано, например, "антитело для применения в» или «антитело или его антигенсвязывающий фрагмент для применения в ..." в определенном медицинском режиме, то это указание также применяется для соответствующего применения фармацевтической композиции по изобретению.
В восьмом аспекте настоящее изобретение относится к способу получения фармацевтической композиции по изобретению, например, согласно девятнадцатому аспекту, включающему смешивание антитела или его антигенсвязывающего фрагмента и, необязательно, ингибитора HMG-CoA-редуктазы с одним или несколькими фармацевтическими эксципиентами или носителями.
В девятом аспекте настоящее изобретение относится к способу получения лекарственной формы по изобретению, включающему отмеривание количества фармацевтической композиции, антитела или его антигенсвязывающего фрагмента, жидкого состава или сухого состава по изобретению, содержащего одну или несколько доз антитела или его антигенсвязывающего фрагмента и, необязательно, ингибитора HMG-CoA-редуктазы, и придания им формы в виде физически дискретных единиц, подходящих в качестве единичных доз для введения человеку и/или животному.
В десятом аспекте настоящее изобретение относится к способу получения или сборки изделия по изобретению, включающему упаковку фармацевтической композиции, антитела, жидкого состава или сухого состава по изобретению в контейнер, необязательно вместе с одним или несколькими из следующих компонентов: этикетка, инструкции по применению, устройство для применения.
В одиннадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, включающему:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В двенадцатом аспекте настоящее изобретение относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл; и
определение эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C по меньшей мере на 25%, по отношению к уровню перед введением дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
В тринадцатом аспекте настоящее изобретение относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
определение эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, где снижение уровня LDL-C, по меньшей мере на 25%, по сравнению с уровнем до введения дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
В четырнадцатом аспекте настоящее изобретение относится к упаковке, включающей антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9 (см. раздел "Предпочтительные антитела для осуществления настоящего изобретения"), и метку.
В пятнадцатом аспекте настоящее изобретение относится к способу регулирования уровня LDL в крови, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В шестнадцатом аспекте настоящее изобретение относится к способу предотвращения эффектов (постоянных) увеличенного уровня LDL в крови, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В семнадцатом аспекте настоящее изобретение относится к способу определения того, что используемое фармацевтическое соединение облегчает, улучшает, ингибирует или предотвращает заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает: (а) введение индивиду соединения, которое специфически связывается с PCSK9, предпочтительно, антитела или его антигенсвязывающего фрагмента, специфически связывающегося с PCSK9, и (b) определение, какая часть PCSK9 в крови связана с соединением, указанным в (а).
В восемнадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом,
где индивид, нуждающийся в этом, входит в одну или несколько из следующих групп индивидов: (i) индивиды, имеющие уровень LDL холестерина (LDL-C) в сыворотке по меньшей мере 100 мг/дл; (ii) индивиды, имеющие уровень HDL-C в сыворотке менее 40 мг/дл; (iii) индивиды, имеющие уровень холестерина в сыворотке по меньшей мере 200 мг/дл; (iv) индивиды, имеющие уровень триглицеридов сыворотки по меньшей мере 150 мг/дл, где указанный уровень триглицеридов определяется после голодания в течение по меньшей мере 8 часов; (v) индивиды в возрасте по меньшей мере 35 лет; (vi) индивиды в возрасте до 75 лет; (vii) индивиды, имеющие индекс массы тела (BMI) 25 или более; (viii) индивиды мужского пола; (ix) индивиды женского пола; (х) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 30 мг/дл, по сравнению с уровнем до введения дозы; или (xi) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 20% по сравнению с уровнем до введения дозы.
В девятнадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом,
при этом индивид, нуждающийся в этом, не входит в одну или несколько групп из числа следующих групп индивидов: (i) курильщики; (ii) лица в возрасте 70 лет или старше; (iii) лица, страдающие от гипертензии; (iv) беременные женщины; (v) женщины, пытающиеся забеременеть; (vi) женщины, которые кормят грудью; (vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень; (viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени; (ix) лица, которые употребляют чрезмерное количество алкоголя; (х) лица, имеющие проблемы с почками; (xi) лица, страдающие гипотиреозом; (xii) лица, страдающие мышечными расстройствами; (xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами; (xiv) лица, имеющие серьезные проблемы с дыханием; (xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой; (xvi) лица, выпивающие более 0,1 л сока грейпфрута в день; (xvii) лица, имеющие индекс массы тела (BMI) более 40; (xviii) лица, имеющие индекс массы тела (BMI) менее 18; (xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2; и (xx) лица, имеющие положительную реакцию на гепатит В или С; (xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
В двадцатом аспекте настоящее изобретение относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл; и
определение эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C, по меньшей мере на 25%, по отношению к уровню до введения дозы, по меньшей мере у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
при этом каждый пациент входит в одну или несколько групп индивидов, как указано в тринадцатом аспекте.
В двадцать первом аспекте настоящее изобретения относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
определение эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C, по меньшей мере на 25%, по отношению к уровню до введения дозы, по меньшей мере у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
где каждый пациент входит в одну или несколько групп индивидов, как изложено в тринадцатом аспекте.
В двадцать втором аспекте настоящее изобретение относится к способу испытания эффективности соединения для снижения уровней холестерина у индивида, где способ включает стадии: (а) предоставление животных грызунов, (b) введение антитела или его антигенсвязывающего фрагмента, который специфически связывает PCSK9 у грызунов, (c) введение испытуемого соединения указанным грызунам, (d) определение эффекта испытуемого соединения у грызунов, где снижение уровня холестерина у грызунов по сравнению с уровнем холестерина у контрольного животного означает, что испытуемое соединение эффективно для снижения уровней холестерина у индивида, при этом контрольное животное относится к тому же виду, как и указанные грызуны, и где испытуемое соединение не вводилось контрольному животному.
В двадцать третьем аспекте настоящее изобретение относится к способу повышения активности статинов по снижению уровней LDL-C у индивида, проходящему статиновую терапию, где способ включает введение индивиду антитела или его антигенсвязывающего фрагмента, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9), при этом антитело или его антигенсвязывающий фрагмент вводят в дозе количестве от приблизительно 5 мг до приблизительно 500 мг, повышая тем самым активность статинов в терапии по снижению уровней LCL-C у индивида.
В двадцать четвертом аспекте настоящее изобретение относится к набору для лечения повышенных уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), у индивида, где набор включает (а) фармацевтическую лекарственную форму, содержащую антитело или его антигенсвязывающий фрагмент, который специфически связывается с hPCSK9, и фармацевтически приемлемый носитель, при этом антитело или его антигенсвязывающий фрагмент присутствует в дозе количестве от приблизительно 5 мг до приблизительно 500 мг, и (b) этикетку или вкладыш в упаковку с инструкциями по применению.
В двадцать пятом аспекте настоящее изобретение относится к способу лечения индивида, страдающего заболеванием или расстройством, которое характеризуется повышенными уровнями холестерина, относящегося к липопротеинам низкой плотности (LDL-C), где способ включает:
(а) выбор индивида с уровнем LDL-C в крови выше 100 мг/дл, и
(b) введение указанному индивиду композиции, содержащей антитело или антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающегося в этом.
В двадцать шестом аспекте настоящее изобретение относится к способу снижения уровней холестерина у индивида, нуждающегося в этом, где способ включает:
(а) выбор индивида с уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), в крови более 100 мг/дл; и
(b) введение указанному индивиду композиции, содержащей антитело или антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающегося в этом.
Это краткое изложение сущности изобретения не обязательно описывает все признаки настоящего изобретения. Другие варианты осуществления изобретения будут очевидны из рассмотрения нижеприведенного подробного описания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На фиг.1 показано процентное снижение уровней LDL холестерина (LDL-C) по отношению к исходному уровню для трех групп пациентов при лечении антителами 316P, направленными против PCSK9. Эти группы пациентов представляют собой следующие группы: (1) пациенты с наследственной гиперхолестеринемией (HeFH), (2) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся на диете, и подвергающиеся постоянной терапии аторвастатином, и (3) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся только на диете. Дозу 50 мг антител против PCSK9 вводили подкожно в дни 1, 29 и 43. Результаты, полученные в отношении групп пациентов, получавших антитела (50 мг для не-FH, 50 мг для FH; 50 мг для комбинированной группы) показаны сплошными линиями, а результаты, полученные в случае пациентов, получавших плацебо (PBO - не-FH; PBO-FH; PBO-комбинированная), показаны пунктирными линиями.
На фиг.2 показано процентное снижение уровня LDL холестерина (LDL-C) по отношению к исходному уровню для трех групп пациентов при лечении антителами 316P, направленными против PCSK9. Эти группы пациентов представляют собой следующие группы: (1) пациенты с наследственной гиперхолестеринемией (HeFH), (2) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся на диете, и подвергающиеся постоянной терапии аторвастатином, и (3) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся только на диете. Дозу 100 мг антител против PCSK9 вводили подкожно в дни 1, 29 и 43. Результаты, полученные в отношении групп пациентов, получавших антитела (100 мг для не-FH, 100 мг для FH; 100 мг для комбинированной группы) показаны сплошными линиями, а результаты, полученные в случае пациентов, получавших плацебо (PBO - не-FH; PBO - FH; PBO - комбинированная), показаны пунктирными линиями.
На фиг.3 показано процентное снижение уровня LDL холестерина (LDL-C) по отношению к исходному уровню для трех групп пациентов при лечении антителами 316P, направленными против PCSK9. Эти группы пациентов представляют собой следующие группы: (1) пациенты с наследственной гиперхолестеринемией (HeFH), (2) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся на диете, и подвергающиеся постоянной терапии аторвастатином, и (3) пациенты с другими формами первичной гиперхолестеринемии (не-FH), находящиеся только на диете. Дозу 150 мг антител против PCSK9 вводили подкожно в дни 1, 29 и 43. Результаты, полученные в отношении групп пациентов, получавших антитела (150 мг для не-FH, 150 мг для FH; 150 мг для комбинированной группы) показаны сплошными линиями, а результаты, полученные в случае пациентов, получавших плацебо (PBO-не-FH; PBO-FH; PBO-комбинированная), показаны пунктирными линиями.
На фиг.4 показана схема исследования стадии 2 для группы пациентов, получавших гиполипидемическое лечение помимо аторвастатина или не получавших такое лечение, при постоянной дозе аторвастатина 10 мг в течение не менее 6 недель до скрининга, или для пациентов, не получавших никакого лечения.
На фиг.5 показана схема исследования 2 для группы пациентов, получавших постоянную дозу аторвастатина 10 мг по меньшей мере в течение 6 недель до скрининга.
На фиг.6 показано распределение средних значений LDL-C у пациентов стадии 1, получавших антитела 316Р при постоянном лечении аторвастатином в течение 12 недель и LOCF (перенос вперед данных последнего наблюдения). Исследование было разработано для оценки эффективности и безопасности применения антител 316P в отношении пациентов с гиперхолестеринемией с повышенным LDL-С (>100 мг/дл или >2,59 ммоль/л), получавшими постоянные дозы аторвастатина (10 мг, 20 мг или 40 мг). Во время вводного периода, состояние пациентов было стабилизировано приемом аторвастатина (10 мг, 20 мг или 40 мг), если он не принимался ранее. После одной дополнительной недели пациенты были рандомизированы по центру IVRS/IWRS в отношении 1:1:1:1:1:1 в одну из 6 групп (плацебо, 50 мг 316P E2W, 316P 100 мг E2W, 316P 150 мг E2W, 316P 200 мг E4W, 316P 300 мг E4W) и были подвергнуты лечению в двойной слепой выборке в течение приблизительно 12 недель. Рандомизация представляла собой группировку по дозам аторвастатина, полученных до рандомизации. В ходе двойного слепого лечения пациентов возвращали на место каждые 2 недели для приема исследуемого препарата (316Р или плацебо). Затем период двойного слепого лечения был заменен на базовый уровень с 8-недельным периодом наблюдения. Как следует из фиг.6, все группы пациентов, получавших лечение, за исключением группы пациентов, получавших плацебо, имели значительное и постоянное снижение уровней LDL-C в течение всего периода исследования.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
До подробного описания настоящего изобретения, приведенного ниже, следует понимать, что данное изобретение не ограничивается конкретной методологией, протоколами и реагентами, описанными в настоящем описании, поскольку они могут варьироваться. Кроме того, следует понимать, что используемая в настоящем описании терминология предназначена для целей описания конкретных вариантов осуществления изобретения и не предназначена для ограничения объема настоящего изобретения, который ограничивается только прилагаемой формулой изобретения. Если не определено иначе, все технические и научные термины, используемые в настоящем описании, имеют те же значения, которые обычно понятны обычному специалисту в области техники, к которой относится изобретение.
Предпочтительно, чтобы термины, используемые в настоящем описании, определены, как описано в "A multilingual glossary of biotechnological terms: (IUPAC Recommendations)", Leuenberger, H.G.W, Nagel, B. and Kölbl, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland).
В данном описании и формуле изобретения, если контекст не требует иного, слово "содержать" и его вариации, такие как "содержит" и "содержащий", подразумевает включение определенного целого или определенной стадии, или группы целых или группы стадий, но не исключает любое другое целое или стадию, или группы целых или стадий.
Несколько документов (например, патенты, заявки на патенты, научные публикации, инструкции производителя, инструкции, номера последовательностей, представленные GenBank, и т.д.) приведены по тексту настоящего описания. В настоящем описании ничего не должно быть истолковано как допущение того, что изобретение не может предполагать свое раскрытие на основании предшествующих изобретений. Некоторые документы, процитированные в настоящем описании, характеризуется как "включенные в качестве ссылки". В случае конфликта между определениями или раскрытиями, представленными в таких включенных ссылках, и определениями или раскрытиями, представленными в настоящем описании, текст настоящего описания имеет безусловный приоритет.
Последовательности: все последовательности, упомянутые в настоящем описании, раскрыты в прилагаемом списке последовательностей, полное содержание и раскрытие которого является частью настоящего описания.
Термин "приблизительно", используемый вместе с числовым значением, предназначен для охвата числового значения в пределах диапазона, имеющего нижний предел, равный на 5% меньше, чем указанное числовое значение, и имеющего верхний предел, равный на 5% больше, чем указанное числовое значение.
Термин "пропротеин конвертазы субтилизина/кексина типа 9 человека" или "hPCSK9", используемый в настоящем описании, относится к hPCSK9, имеющему аминокислотную последовательность SEQ ID NO:755, кодируемого последовательностью нуклеиновой кислоты SEQ ID NO:754, и или к его биологически активному фрагменту.
Термин "специфически связывает", "специфическое связывание" и т.п. означает, что антитело или его антигенсвязывающий фрагмент образует комплекс с антигеном, который в физиологических условиях является относительно стабильными. Специфическое связывание можно охарактеризовать константой равновесной диссоциации, равной по меньшей мере приблизительно 1×10-6 М или менее (например, меньшее значение KD обозначает сильное связывание). Методы определения того, являются ли две молекулы специфически связанными, хорошо известны специалистам в данной области, и включают, например, равновесный диализ, поверхностный плазмонный резонанс и т.п. Выделенное антитело, которое специфически связывается с hPCSK9, может, однако, обладать перекрестной реактивностью в отношении других антигенов, таких как молекулы PCSK9 из других видов. Кроме того, как используется в настоящем описании, мультиспецифические антитела (например, биспецифические), которые связываются с hPCSK9 и с одним или несколькими дополнительными антигенами, рассматриваются, тем не менее, как антитела, которые "специфически связываются" с hPCSK9.
Термин "KD", используемый в настоящем описании, предназначен для обозначения константы равновесной диссоциации конкретного взаимодействия антитело-антиген. Константа равновесной диссоциации обычно измеряется в единицах "моль/л" (используется сокращение "M").
Термин "низкая скорость диссоциации", "Koff" или "kd" связан с антителом, которое диссоциирует из комплекса с hPCSK9 с константой скорости 1×10-3 с-1 или менее, предпочтительно, от 1×10-4 с-1 или менее, как определяется с помощью поверхностного плазмонного резонанса, например, с помощью BIACORE™.
Термин "высокая аффинность" антитела относится к таким моноклональным антителам (mAb), которые имеют аффинность связывания hPCSK9 не менее 10-10 М, предпочтительно, 10-11 М, еще более предпочтительно, 10-12 М, измеряемую с помощью поверхностного плазмонного резонанса, например, с помощью BIACORE™ или анализом ELISA для определения аффинности в растворе.
Термин "поверхностный плазмонный резонанс", используемый в настоящем описании, относится к оптическому явлению, которое позволяет проводить анализ биоспецифических взаимодействий в режиме реального времени путем обнаружения изменений концентраций белка в биосенсорной матрице, например, с помощью системы BIACORE™ (Pharmacia Biosensor AB, Uppsala, Sweden and Piscataway, N.J.).
"Эпитоп", также известный как антигенная детерминанта, является областью антигена, который распознается иммунной системой, в частности, антителами, В-клетками или Т-клетками. Используемый в настоящем описании термин "эпитоп" является частью антигена, которая способна связываться с антителом или его антигенсвязывающим фрагментом, как описано в настоящем документе. В этом контексте термин "связывание" относится, предпочтительно, к "специфическому связыванию", как определено в настоящем описании. Эпитопы обычно состоят из химически активных поверхностных группировок молекул, таких как аминокислоты, боковые цепи сахаров, фосфорильные группы или сульфонильные группы, и могут иметь специфические трехмерные структурные характеристики и/или специфические характеристики заряда. Конформационные и не конформационные эпитопы можно отличить тем, что в присутствии денатурирующих растворителей связывание разрушается для первых, и не разрушается для вторых.
"Паратоп" является частью антитела, которое специфически связывается с эпитопом.
Термин "антитело", используемый в настоящем описании, предназначен для обозначения молекул иммуноглобулина, состоящего из четырех полипептидных цепей: двух тяжелых (Н) цепей и двух легких (L) цепей, соединенных между собой дисульфидными связями. Термин "антитело" также охватывает все рекомбинантные формы антител, в частности, антител, описанных в настоящем описании, например, антитела, экспрессируемые прокариотами, негликозилированные антитела и любые антигенсвязывающие фрагменты антитела и производные антител, как описано ниже. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи ("HCVR" или "VH"), и константную область тяжелой цепи (состоящую из доменов CH1, CH2 и CH3). Каждая легкая цепь состоит из вариабельной области легкой цепи ("LCVR" или "VL") и константной области легкой цепи (CL). Области VH и VL могут быть дополнительно разделены на гипервариабельные области, называемые областями, определяющими комплементарность (CDR), чередующиеся с более консервативными областями, которые называются каркасными областями (FR). Каждая VH и VL состоит из трех CDR, и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антитела могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплемента.
Также возможна замена одного или нескольких остатков в CDR или пропуск одного или нескольких CDR. В научной литературе были описаны антитела, в которых один или два CDR не являются необходимыми для связывания. В работе Padlan et al. (1995 FASEB J. 9:133-139), на основе опубликованных кристаллических структур, представлен анализ контактных областей между антителами и их антигенами, и авторы пришли к выводу, что только приблизительно от одной пятой до одной трети остатков в CDR фактически контактируют с антигеном. Padlan et al. также нашли многие антитела, где в одной или двух CDR не имелось аминокислот, находящихся в контакте с антигеном (Vajdos et al. 2002 J Mol Biol 320:415-428).
Остатки в CDR, которые не контактируют с антигеном, могут быть определены на основе предварительных исследований (например, остатки H60-H65 в CDRH2 часто не требуется), из областей CDR по Kabat, лежащих вне областей CDR по Chothia, молекулярным моделированием и/или эмпирически. Если CDR или остаток(ки) пропущены, то, как правило, имеет место замещение на аминокислоту, занимающую соответствующее положение в другой последовательности антитела человека или в консенсусе таких последовательностей. Позиции для замещения в CDR, аминокислоты для замены также могут быть выбраны эмпирически. Эмпирические замены могут быть консервативным или не консервативными заменами.
Термин "антигенсвязывающий фрагмент" антитела (или просто "связывающая часть"), как используется в настоящем описании, относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с hPCSK9. Было показано, что антигенсвязывающая функция антитела может быть реализована фрагментами полноразмерного антитела. Примеры связывающих фрагментов, охватываемых термином "антигенсвязывающий фрагмент" антитела включают (i) Fab-фрагменты, моновалентные фрагменты, состоящие из доменов VL, VH, CL и CH; (ii) F(ab′)2-фрагменты, бивалентные фрагменты, содержащие два Fab-фрагмента, связанные дисульфидным мостиком в шарнирной области; (iii) Fd-фрагменты, состоящие из VH и CH доменов; (iv) Fv-фрагменты, состоящие из VL и VH доменов одного плеча антитела, (v) dAb фрагменты (Ward et al., (1989) Nature 341: 544-546), которые состоят из домена VH; (vi) выделенных областей, определяющих комплементарность (CDR); и (vii) в комбинации из двух или нескольких выделенных CDR, которые необязательно могут быть соединены синтетическим линкером. Кроме того, хотя два домена фрагмента Fv, а именно, VL и VH, кодируются отдельными генами, они могут быть соединены с помощью синтетического линкера, с использованием рекомбинантных способов, что обеспечивает получение одноцепочечного белка, в котором VL и VH области связаны в пару, с образованием моновалентных молекул (известных как одноцепочечные Fv (ScFv), см., например, Bird et al. (1988) Science 242: 423-426; and Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85: 5879-5883). Такие одноцепочечные антитела также могут быть включены в определение термина "антигенсвязывающий фрагмент" антитела. Еще одним примером является слитый белок доменсвязывающего иммуноглобулина, содержащий (i) полипептид связывающего домена, который слит с полипептидом шарнирной области иммуноглобулина, (ii) константную область CH2 тяжелой цепи иммуноглобулина, слитой с шарнирной областью и (iii) константную область СН3 тяжелой цепи иммуноглобулина, слитую с константной областью CH2. Связывающий домен полипептида может быть вариабельной областью тяжелой цепи или вариабельной областью легкой цепи. Слитые белки доменсвязывающего иммуноглобулина дополнительно описаны в патенте США № 2003/0118592 и патенте США № 2003/0133939. Эти фрагменты антител получают с использованием обычных методов, известных специалистам в данной области техники, и фрагменты подвергают скринингу на полезность, аналогично как и в случае интактных антител. Другими примерами "антигенсвязывающих фрагментов" являются так называемые микроантитела, которые получены из одного CDR. Например, в работе (Heap CJ et al. (2005) J. Gen. Virol. 86:1791-1800) описаны микроантитела из 17 аминокислотных остатков, полученные из CDR3 тяжелой цепи антитела, которые направлены против оболочечного гликопротеина gp120 HIV-1. Другие примеры включают малые миметики антител, содержащие две или более областей CDR, предпочтительно, из родственных каркасных областей, которые слиты друг с другом. Такой малый миметик антитела, содержащий VH CDR1 и VL CDR3, которые связаны родственными VH FR2, был описан в работе (Qiu X-Q, et al. (2007) Nature biotechnology 25(8):921-929).
Таким образом, термин "антитело или его антигенсвязывающий фрагмент", используемый в настоящем описании, относится к молекулам иммуноглобулина и иммунологически активным частям молекул иммуноглобулина, т.е. к молекулам, которые содержат антигенсвязывающий сайт, который иммуноспецифически связывается с антигеном.
Антитела и их антигенсвязывающие фрагменты, используемые в изобретении, могут быть любого животного происхождения, включая птиц и млекопитающих. Предпочтительно, антитела или фрагменты являются происходящими от человека, шимпанзе, грызунов (например, от мыши, крысы, морской свинка или кролика), курицы, индейки, свиньи, овцы, козы, верблюда, коровы, лошади, осла, кошки или собаки. В частности, предпочтительно, когда антитела являются антителами человека или мыши. Антитела по изобретению также включают химерные молекулы, в которых константная область антитела получена от одного вида, предпочтительно, человека, объединена с антигенсвязывающим сайтом, полученным от других видов, например, мыши. Кроме того, антитела по изобретению включают гуманизированные молекулы, в которых антигенсвязывающие сайты антитела получены из видов, не относящихся к человеку (например, от мыши), и они объединены с константными и каркасными областями человека.
Как проиллюстрировано в настоящем описании, антитела по изобретению могут быть получены непосредственно из гибридов, которые экспрессируют антитела, или они могут быть клонированы и рекомбинантно экспрессироваться в клетке-хозяине (например, в клетке СНО или в лимфоцитарной клетке). Другими примерами клеток-хозяев являются микроорганизмы, такие как E.coli и грибы, такие как дрожжи. Альтернативно, они могут быть получены рекомбинантно в трансгенных животных, не относящихся к человеку, или растениях.
Термин "химерное антитело" относится к таким антителам, в которых одна часть каждой аминокислотной последовательности тяжелой цепи и легкой цепи является гомологичной соответствующим последовательностям в антителах, полученных от конкретного вида или принадлежащих к конкретному классу, а остальной сегмент цепи является гомологичным соответствующим последовательностям от другого вида или класса. Обычно вариабельная область легкой цепи и тяжелой цепи имитирует вариабельные области антител, полученных из одного вида млекопитающих, в то время как константные части являются гомологичными последовательностям антител, происходящих от другого вида. Одним из очевидных преимуществ таких химерных форм является то, что вариабельная область может быть легко получена из известных в настоящее время источников с использованием легкодоступных B-клеток или гибридом от организма-хозяина, не относящегося к человеку, и она может быть объединена с константными областями, полученными, например, из препаратов клеток человека. В то время как вариабельная область имеет преимущество в легкости ее получения, и ее специфичность не зависит от источника, константная область, происходящая от человека, с меньшей вероятность вызывает иммунный ответ индивида-человека, когда такие антитела вводят человеку, чем в случае, когда константная область имеет происхождение от источника, не являющегося человеком. Однако вышеуказанное определение не ограничено этим конкретным примером.
Термин «гуманизированное антитело» относится к молекуле, имеющей антигенсвязывающий сайт, который по существу получен из иммуноглобулина видов, не относящихся к человеку, при этом оставшиеся структуры иммуноглобулина молекулы основаны на структуре и/или последовательности иммуноглобулина человека. Антигенсвязывающий сайт может включать либо полные вариабельные домены, слитые с константными доменами, или только области, определяющие комплементарность (CDR), встроенные в соответствующие каркасные области вариабельных доменов. Антигенсвязывающие сайты могут быть дикого типа или могут быть модифицированы путем одной или нескольких аминокислотных замен, например, они могут быть модифицированы для более точного соответствия иммуноглобулинам человека. Некоторые формы гуманизированных антител сохраняют все последовательности CDR (например, гуманизированное мышиное антитело, которое содержит все шесть CDR из антител мыши). Другие формы имеют одну или несколько CDR, которые изменены по отношению к исходному антителу.
Специалистам известны различные способы гуманизации антител, как рассмотрено в работе (Almagro JC and Fransson J (2008) Frontiers in Bioscience 13:1619-1633), содержание которой включено в настоящее описание в качестве ссылки. Almagro and Fransson различают рациональные подходы и эмпирические подходы. Рациональные подходы характеризуются генерацией нескольких вариантов генно-инженерного антитела и оценкой их связывания или любого другого свойства, представляющего интерес. Если разработанные варианты не дают ожидаемых результатов, то инициируется новый цикл конструирования и оценки связывания. Рациональные подходы включают встраивание CDR, повторную укладку, супергуманизацию и оптимизацию содержимого цепи человека. В противоположность этому, эмпирические подходы основаны на генерации больших библиотек гуманизированных вариантов и отбор лучших клонов с использованием технологий обогащения или высокопроизводительного скрининга. Таким образом, эмпирические подходы зависят от надежности системы отбора и/или скрининга, что позволяет проводить поиск в большом объеме вариантов антител. Специалистам хорошо известны технологии дисплеев in vitro, такие как фаговый дисплей и рибосомный дисплей, которые отвечают этим требованиям. Эмпирические подходы включают использование библиотеки FR, направленный отбор, перетасовку каркасов и инженерию с использованием последовательностей человека.
Термин "антитело человека", используемый в настоящем описании, охватывает антитела, имеющие вариабельные и константные области, полученные из последовательностей иммуноглобулина зародышевой линии человека. Моноклональные антитела человека (mAb) по изобретению могут включать аминокислотные остатки, которые не кодируются последовательностями для иммуноглобулина зародышевой линии человека (например, мутации, введенные случайным или сайт-специфическим мутагенезом in vitro или соматическими мутациями in vivo), например, в CDR, и, в частности, в CDR3. Однако термин "антитело человека", используемый в настоящем описании, не предназначен для включения моноклональных антител, в которых последовательности CDR, полученные из зародышевой линии других видов млекопитающих (например, мышей), были встроены в последовательности FR человека. Антитела человека по изобретению включают антитела, выделенные из библиотек иммуноглобулинов человека или из животных, трансгенных по одному или нескольким иммуноглобулинам человека, и которые не экспрессируют эндогенные иммуноглобулины, как описано, например, в патенте США № 5939598, на имя Kucherlapati and Jakobovits.
Термин "моноклональное антитело", используемый в настоящем описании, относится к препарату молекул антител одного молекулярного состава. Моноклональное антитело проявляет одну специфичность связывания и аффинность к конкретному эпитопу. В одном из вариантов осуществления изобретения, моноклональные антитела продуцируются гибридомой, которая включает В-клетки, полученные из животных, не относящихся к человеку, например, из мыши, слитые с иммортализованной клеткой.
Термин "рекомбинантное антитело", используемый в настоящем описании, включает все антитела, полученные, экспрессированные, созданные или выделенные рекомбинантными способами, например, такие как (а) антитела, выделенные из животного (например, мыши), которое является трансгенным или трансхромосомным в отношении генов иммуноглобулина, или из гибридомы, полученной из них, (b) антитела, выделенные из клетки-хозяина, трансформированной для экспрессии антитела, например, из трансфектомы, (c) антитела, выделенные из рекомбинантной комбинаторной библиотеки антител, и (d) антитела, полученные, экспрессированные, созданные или выделенные любыми другими средствами, которые включают сплайсинг последовательностей гена иммуноглобулина с другими последовательностями ДНК.
Термин "трансфектома", используемый в настоящем описании, включает рекомбинантные, экспрессирующие антитела эукариотические клетки-хозяева, такие как клетки СНО, клетки NS/0, клетки НЕК293, клетки HEK293T, клетки растений или грибов, в том числе клетки дрожжей.
Используемый в настоящем описании термин "гетерологичное антитело" определяется в зависимости от трансгенного организма, продуцирующего такое антитело. Этот термин относится к антителу, имеющему аминокислотную последовательность, или кодируемого последовательностью нуклеиновой кислоты, которая соответствует антителу, которые имеются в организме, не являющимся трансгенным, и которое в целом получено из видов, отличных от трансгенных организмов.
Используемый в настоящем описании термин "гетерогибридное антитело" относится к антителу, имеющему легкую цепь и тяжелую цепь, происходящие из различных организмов. Например, антитело, имеющее тяжелую цепь человека, связанную с мышиной легкой цепью, представляет собой гетерогибридное антитело.
Таким образом, "антитела и их антигенсвязывающие фрагменты", пригодные для использования в настоящем изобретении, включают, но не ограничиваются перечисленными, поликлональные, моноклональные, моновалентные, биспецифические, гетероконъюгатные, мультиспецифические, рекомбинантные гетерологичные, гетерогибридные, химерные, гуманизированные (в частности, со встроенной CDR), деиммунизированные антитела или антитела человека, Fab-фрагменты, Fab′-фрагменты, F(ab′)2-фрагменты, фрагменты, продуцируемые библиотекой, экспрессирующей Fab, Fd, Fv, Fv с дисульфидными связями (dsFv), одноцепочечные антитела (например, scFv), диатела или тетратела (Holliger P. et al. (1993) Proc. Natl. Acad. Sci. U.S.A. 90(14), 6444-6448), нанотела (также известные как однодоменные антитела), антиидиотипические (анти-Id) антитела (включая, например, анти-Id антитела к антителам по изобретению) и эпитоп-связывающие фрагменты любых из вышеупомянутых антител.
Антитела, описанные в настоящем документе, предпочтительно, являются выделенными. "Выделенное антитело", как используется в настоящем документе, относится к антителам, которые по существу не содержат других моноклональных антител, имеющих иные антигенные специфичности (например, выделенное антитело, которое специфически связывает hPCSK9, по существу не содержит моноклональных антител, которые специфически связывают антигены, отличные от hPCSK9). Однако выделенное антитело, которое специфически связывает hPCSK9, может иметь перекрестную реактивность к другим антигенам, например, к молекулам PCSK9 других видов.
Используемый в настоящем описании термин "антагонист PCSK9" означает соединение, которое ингибирует по меньшей мере одну биологическую активность PCSK9, предпочтительно, протеиназную активность PCSK9. Предпочтительные антагонисты PCSK9 характеризуются тем, что они связывают от 10% до 100% (предпочтительно, 50%-100%) PCSK9, присутствующего в крови, при использовании в стехиометрических количествах. Предпочтительные антагонисты PCSK9 по настоящему изобретению представляют собой нейтрализующие антитела.
Термин "нейтрализующее антитело", используемый в настоящем документе (или "антитело, которое нейтрализует активность PCSK9»), предназначен для обозначения антител, которые за счет связывания hPCSK9 приводят к ингибированию по меньшей мере одной биологической активности PCSK9, предпочтительно, к ингибированию протеиназной активности PCSK9. Это ингибирование биологической активности PCSK9 может быть оценено путем измерения одного или нескольких показателей биологической активности PCSK9 одним или несколькими из различных стандартных анализов in vitro или in vivo, известных в данной области. Такие анализы описаны, например, в заявке на патент США № 2010/0166768 А1, содержание которой включено в настоящее описание в качестве ссылки в полном объеме.
Поскольку PCSK9 увеличивает уровень LDL холестерина в плазме за счет промотирования деградации рецептора LDL, активность PCSK9 оказывает влияние на несколько заболеваний, связанных с повышенным уровнем LDL холестерина в плазме. Соответственно, антагонисты PCSK9, такие как нейтрализующие антитела против hPCSK9 или их антигенсвязывающие фрагменты, которые полезны для снижения повышенного уровня общего холестерина, холестерина, не являющегося HDL холестерином, LDL холестерина и/или аполипопротеина B100 (Apo-B100). Следовательно, антагонисты PCSK9 полезны для ослабления, улучшения, ингибирования или предотвращения нескольких таких заболеваний, включая, но без ограничения, гиперхолестеринемию, гиперлипидемию, дислипидемию, атеросклероз и сердечно-сосудистые заболевания.
В конкретных вариантах осуществления изобретения, антитела против PCSK9 или их антигенсвязывающие фрагменты, описанные в настоящем описании, могут быть конъюгированы с терапевтической молекулой, такой как цитотоксин, химиотерапевтическое средство, иммунодепрессант или радиоизотоп ("иммуноконъюгат").
"Консервативная аминокислотная замена" представляет собой такую замену, где аминокислотный остаток заменен другим аминокислотным остатком, имеющим боковую цепь (R группу) со сходными химическими свойствами (например, заряд или гидрофобность). В общем, консервативная аминокислотная замена не будет существенно изменять функциональные свойства белка. В тех случаях, когда две или более аминокислотных последовательностей, отличаются друг от друга консервативными заменами, процент или уровень сходства может быть увеличен для коррекции консервативного характера замещения. Средства для такой коррекции хорошо известны специалистам в данной области техники. См., например, Pearson (1994) Methods MoI. Biol. 24: 307- 331. Примеры групп аминокислот, имеющих боковые цепи со сходными химическими свойствами, включают
1) аминокислоты с алифатическими боковыми цепями: глицин, аланин, валин, лейцин и изолейцин;
2) аминокислоты с алифатическими гидроксильными боковыми цепями: серин и треонин;
3) аминокислоты с амидсодержащими боковыми цепями: аспарагин и глутамин;
4) аминокислоты с ароматическими боковыми цепями: фенилаланин, тирозин и триптофан;
5) аминокислоты с основными боковыми цепями: лизин, аргинин и гистидин;
6) аминокислоты с кислыми боковыми цепями: аспартат и глутамат, и
7) аминокислоты с серосодержащими боковыми цепями: цистеин и метионин.
Предпочтительные консервативные аминокислотные замены группируются следующим образом: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. Альтернативно, консервативная замена, в любом случае, имеет положительное значение в матрице логарифмического правдоподобия РАМ250, как раскрыто в работе Gonnet et al. (1992) Science 256: 1443-45. "Умеренно консервативная" замена в любом случае имеет неотрицательное значение в матрице логарифмического правдоподобия РАМ250. С учетом известности генетического кода, методов рекомбинантных и синтетических ДНК, опытный специалист может легко сконструировать ДНК, кодирующие консервативные аминокислотные варианты.
Используемый в настоящем описании термин "неконсервативные замены" или "неконсервативные аминокислотные замены" определяется как замена одной аминокислоты другой аминокислотой, указанной в другой группе из семи стандартных аминокислотных группы 1)-7), как указано выше.
Термин "значительная идентичность" или "практически идентична", когда относится к нуклеиновой кислоте, или ее фрагменту, показывает, что при оптимальном выравнивании ее с соответствующей нуклеотидной инсерцией или делецией с другой нуклеиновой кислотой (или ее комплементарной цепью), то идентичность нуклеотидной последовательности по меньшей мере составляет приблизительно 90%, а более предпочтительно, по меньшей мере приблизительно 95%, 96%, 97%, 98% или 99% нуклеотидных оснований, как измерено с помощью любого хорошо известного алгоритма определения идентичности последовательностей, таких, как FASTA, BLAST или GAP, как описано ниже.
Применительно к полипептидам, термин "значительное сходство" или "по существу идентична" означает, что две пептидные последовательности при оптимальном выравнивании, например, с помощью программ GAP или BESTFIT, с использованием весов брешей по умолчанию, имеют по меньшей мере 90%-ую идентичность последовательности, еще более предпочтительно, по меньшей мере 95%, 98% или 99%-ую идентичность последовательности. Предпочтительно, когда положения остатков, которые не являются идентичными, отличаются консервативными аминокислотными заменами.
Сходство последовательностей полипептидов обычно измеряется с помощью программного обеспечения для анализа последовательности. Программное обеспечение для анализа белка сопоставляет сходные последовательности, используя меры сходства, назначенные для различных замен, делеций и других модификаций, в том числе для консервативных аминокислотных замен. Например, программное обеспечение GCG включает программы, такие как GAP и BESTFIT, которые могут быть использованы с параметрами по умолчанию для определения гомологии последовательности или идентичности последовательности между близкородственными полипептидами, такими как гомологичные полипептиды из различных видов организмов или между белком дикого типа и его мутеином. Смотрите, например, программу GCG версии 6.1. Полипептидные последовательности также могут быть сравнены с использованием программы FASTA с параметрами по умолчанию или с рекомендуемыми параметрами; эта программа входит в пакет GCG версии 6.1. Программа FASTA (например, FASTA2 и FASTA3) обеспечивает выравнивание и вычисляет процент идентичности последовательностей областей по лучшему совпадению между запросом и поиском последовательностей (Pearson (2000), смотрите выше). Другой предпочтительный алгоритм при сравнении последовательности настоящего изобретения с базой данных, содержащей большое количество последовательностей из различных организмов, реализован компьютерной программой BLAST, в особенности BLASTP или TBLASTN, с использованием параметров по умолчанию. См., например, Altschul et al., (1990) J. Mol. Biol. 215: 403 410 и (1997) Nucleic Acids Res. 25:3389 402, каждая из которых включена в настоящее описание в качестве ссылки.
Когда проценты идентичности последовательности, указываются в настоящей заявке, эти проценты рассчитаны по отношению к полной длине всей последовательности, если иначе не указано специально. Это вычисление по отношению к полной длине всей последовательности относится как к последовательностям нуклеиновых кислот, так и к полипептидным последовательностям.
Используемый в настоящем описании термин "лечить" или "лечение" заболевания или расстройства означает выполнение одного или нескольких из следующего: (а) снижение тяжести и/или длительности расстройства, (b) ограничения или профилактики развития симптомов, характерных для расстройства (расстройств), которое лечат, (c) ингибирование ухудшения симптомов, характерных для расстройства (расстройств), которые лечат, (d) ограничение масштабов или профилактики рецидивов расстройства (расстройств) у пациентов, у которых ранее имелось расстройство (расстройства), и (е) ограничение масштабов или предотвращение рецидива симптомов у пациентов, у которых ранее имелась симптоматика расстройства (расстройства).
Используемый в настоящем описании термин "предотвращение", "предотвращать", "предупреждение" или "профилактика" заболевания или расстройства означает предотвращение возникновения расстройства у индивида.
Как используется в настоящем описании, выражения "для введения" и "к введению" имеют такое же значение, как "готовый к введению". Другими словами, указание, что активное соединение предназначено "для введения" должно быть понято, что активное вещество было приготовлено в виде препарата и представлено в дозах, где указанное активное соединение находится в состоянии, способном проявлять свою терапевтическую активность.
Термины "терапевтически эффективное количество" или "терапевтическое количество" означают количество лекарственного средства или фармацевтического средства, вызывающего биологический или медицинский ответ ткани, системы, животного или человека, которого добивается исследователь, ветеринар, врач или иной клиницист. Термин "профилактически эффективное количество" означает количество фармацевтического препарата, позволяющее предотвратить или уменьшить риск возникновения биологического или медицинского события, которое желает предотвратить в ткани, системе, животном или человеке исследователь, ветеринар, врач или иной клиницист. В частности, доза, получаемая пациентом, может быть выбрана таким образом, чтобы достичь снижения количества LDL холестерина (холестерин, представляющий собой липопротеин низкой плотности) до желаемого; доза, получаемая пациентом, также может быть установленной в течение долгого периода времени для того, чтобы достичь целевого уровня LDL. Режим дозирования при использовании антитела или его антигенсвязывающего фрагмента, как описано в настоящем описании, выбирают в соответствии с различными факторами, включающими тип, вид, возраст, вес, индекс массы тела, пол и медицинское состояние пациента, тяжесть состояния, подлежащего лечению, эффективность соединения, выбранного для введения, путь введения, цель введения; а также почечную и печеночную функцию у пациента.
Используемый в настоящем описании термин "пациент" означает любого человека или животного, не являющегося человеком, такого как млекопитающее, рептилия и птица, которые могут извлечь пользу от лечения антителами и их антигенсвязывающими фрагментами, описанными в настоящем документе. Предпочтительно, "пациент" выбирается из группы, состоящей из лабораторных животных (например, мыши или крысы), домашних животных (включая, например, морскую свинку, кролика, курицу, индейку, свинью, овцу, козу, верблюда, корову, лошадь, осла, кошку или собаку), грызунов или приматов, включая шимпанзе, гориллу, бонобо, и человека. Особенно предпочтительно, когда "пациент" является человеком.
Термины "индивид" или "субъект" используются в настоящем описании взаимозаменяемо. Используемый в настоящем документе термин "индивид" относится к человеку или животному, не являющемуся человеком (например, к млекопитающему, птице, рептилии, рыбе, амфибии и беспозвоночному), предпочтительно, к индивидууму, который может либо получить положительный результат от одного из различных аспектов настоящего изобретения (например, от способа лечения или от лекарственного средства, определенных в способах по изобретению), или который может быть использован в качестве лабораторного животного для идентификации и характеризации лекарственного средства или метода лечения. Индивидуум может быть, например, человеком, диких животным, домашним животным или лабораторным животным; примеры включают: млекопитающего, например, человека, нечеловекообразных приматов (шимпанзе, бонобо, горилла), собаку, кошку, грызуна (например, мышь, морскую свинку, крысу, хомяка или кролика, лошадь, осла, корову, овцу, козу, свинью, верблюда, птицу, такую как утка, голубь, индейка, гусь или цыпленок; рептилия, такая как: сухопутная черепаха, пресноводная черепаха, змея, ящерица, амфибия, такая как лягушка (например, Xenopus Laevis), рыба, такая как кои или данио; беспозвоночное такое, как червь (например, с. elegans) или насекомое (например, муха, в частности, дрозофила). Термин индивидуум также охватывает представителей отдельных различных морфологических стадий развития птицы, рыбы, рептилии или насекомого, например, яйцо, куколка, личинка или имаго. Кроме того, предпочтительно, когда индивид представляет собой "пациента".
Используемый в настоящем описании термин "лекарственная форма" относится к физически дискретным единицам, подходящим в качестве разовых доз для человека и/или животного, причем каждая единица содержит заранее определенное количество активного материала (например, от приблизительно 50 мг до приблизительно 500 мг антитела против PCSK9 и/или например, от 0,05 мг до 100 мг ингибитора HMG-CoA-редуктазы), рассчитанное на получение желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим разбавителем, носителем или эксципиентом. Требования к новым лекарственным формам данного изобретения диктуются и непосредственно зависит от (а) уникальных характеристик активного материала и достигаемого определенного терапевтического эффекта, и (b) ограничения, присущего в данной области при получении препаратов из такого активного материала для терапевтического применения у животных или людей, как раскрыто в данном описании, и эти требования и характеристики являются признаками настоящего изобретения. Примерами подходящих лекарственных форм по настоящему изобретению являются флаконы, таблетки, капсулы, пастилки, суппозитории, пакетики с порошком, облатки, крахмальные капсулы, ампулы, разделенные на части множества любых вышеуказанных форм, а также другие формы, описанные в настоящем описании или общеизвестные в уровне техники. Одна или несколько таких лекарственных форм антитела могут быть включены в изделие по настоящему изобретению, необязательно дополнительно содержащему одну или несколько лекарственных форм ингибитора HMG-CoA-редуктазы (например, блистер таблеток, содержащих в качестве активного ингредиента ингибитор HMG-CoA-редуктазы).
Термин "активное вещество" относится к любому материалу, обладающему терапевтической активностью, например, к одному или нескольким активным ингредиентам. Активные ингредиенты, которые должны быть использованы в качестве терапевтических агентов, могут быть легко получены в такой лекарственной форме, с применением фармацевтических материалов, которые сами по себе являются доступными в данной области, или которые могут быть получены известными способами.
Следующие препараты являются иллюстративными препаратами в виде лекарственных форм по настоящему изобретению, и не являются его ограничениями. Некоторые лекарственные формы могут быть получены по соответствующие варианту осуществления настоящего изобретения. Например, единичная доза на один флакон может содержать 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл, 5 мл, 6 мл, 7 мл, 8 мл, 9 мл, 10 мл, 15 мл или 20 мл раствора антитела против PCSK9 или его фрагмента, с содержанием антитела против PCSK9 в диапзоне от приблизительно 40 мг до приблизительно 500 мг. Если необходимо, эти препараты могут быть скорректированы до требуемой концентрации путем добавления в каждый флакон стерильного разбавителя. В одном из вариантов осуществления изобретения, компоненты композиции по изобретению поставляются либо отдельно, либо в смеси друг с другом в виде лекарственной формы, например, в виде сухого лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, таком как флакон, ампула или саше, с указанием количества активного агента. Когда композиция предназначена для введения путем инфузии, она может быть включена во флакон для инфузии, содержащий стерильную воду или физиологический раствор фармацевтической чистоты. Когда композицию вводят путем инъекции, может быть предоставлена ампула со стерильной водой для инъекций или с физиологическим раствором для того, чтобы ингредиенты могли быть смешаны перед введением.
Композиции по изобретению включают композиции нерасфасованных лекарственных форм, которые используются при получении фармацевтических композиций (например, композиций, пригодных для введения индивиду или пациенту), которые, в свою очередь, могут быть использованы при получении дозированных форм. В предпочтительном варианте осуществления изобретения, композиция представляет собой фармацевтическую композицию. Такие композиции содержат профилактически или терапевтически эффективное количество одного или нескольких профилактических или терапевтических средств (например, антитела по изобретению или другого профилактического или терапевтического средства) и фармацевтически приемлемый носитель. Предпочтительно, фармацевтические композиции получают в форме, подходящей для соответствующего способа введения пациенту.
Активные вещества или ингредиенты (например, антитела или их фрагменты и ингибиторы HMG-CoA-редуктазы) могут быть получены в виде различных дозированных форм, в том числе в виде твердых дозированных форм для перорального введения, таких как капсулы, таблетки, пилюли, порошки и гранулы, в виде жидких дозированных форм для перорального применения, таких как фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры, в виде инъекционных препаратов, например, как стерильные инъецируемые водные или масляные суспензии, в виде композиций для ректального или вагинального введения, предпочтительно, в виде суппозиториев, и в виде дозированных форм для местного применения или трансдермального введения, таких как мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, ингаляторы или пластыри.
В конкретном варианте осуществления изобретения, термин "фармацевтически приемлемый" означает одобренный регулирующим ведомством США на федеральном уровне или на уровне штата, или одобренный EMA (Европейское агентство по лекарственным средствам), или указанный в Фармакопее США (United States Pharmacopeia-33/National Formulary-28 Reissue, published by the United States Pharmacopeial Convention, Inc., Rockville Md., publication date: April 2010) или в другой общепризнанной фармакопее для применения животным и, в частности, для людей. Термин "носитель" относится к разбавителю, вспомогательному веществу (например, к адъюванту Фрейнда (полному и неполному)), эксципиенту или носителю, с которым вводят лекарственное средство. Такими фармацевтическими носителями могут быть стерильные жидкости, такие как вода и масла, включая масла из нефти, масла животного, растительного или синтетического происхождения, например, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Вода является предпочтительным носителем для случая, когда фармацевтическую композицию вводят внутривенно. Солевые растворы и водные растворы декстрозы и глицерина также могут быть использованы в качестве жидких носителей, в частности, для инъекционных растворов. Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропиленгликоль, воду, этанол и т.п. Использование эксципиентов, и дополнительные эксципиенты описаны в работе “Handbook of Pharmaceutical Excipients”, fifth edition, R.C.Rowe, P.J. Seskey and S.C. Owen, Pharmaceutical Press, London, Chicago. Композиция, при желании, может также содержать небольшие количества смачивающих или эмульгирующих средств, или средств, буферирующих рН. Эти композиции могут быть представлены в виде растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, препаратов длительного высвобождения и т.п. Препарат для перорального применения может содержать стандартные носители, такие как маннит, лактозу, крахмал, стеарат магния, сахарин натрия, целлюлозу, карбонат магния и т.п. Примеры подходящих фармацевтических носителей описаны в "Remington′s Pharmaceutical Sciences" под ред. E.W. Martin. Такие композиции будут содержать профилактически или терапевтически эффективное количество антитела, предпочтительно, в очищенной форме, вместе с подходящим количеством носителя так, чтобы обеспечить форму, подходящую для введения пациенту. Препарат должен соответствовать способу введения.
Как правило, ингредиенты композиции по изобретению поставляются либо отдельно, либо в смеси друг с другом в виде лекарственной формы, например, в виде сухого состава для растворения, такого как лиофилизированного порошка, порошка, высушенного с замораживанием, или в виде безводного концентрата в герметично закрытом контейнере, таком как ампула или саше, с указанием количества активного агента. Ингредиенты композиции по изобретению также могут поставляться в виде смешанного жидкого состава (например, в виде раствора для инъекции или инфузии) в герметично закрытом контейнере, таком как ампула, саше, предварительно заполненный шприц или автоинъектор, или картридж для многоразового шприца или аппликатора (например, для ручки или автоинъектора). Когда композиция предназначена для введения путем инфузии, она может быть включена во флакон для инфузии, содержащий стерильную воду или физиологический раствор фармацевтической чистоты. Когда композицию вводят путем инъекции, может быть предоставлена ампула со стерильной водой для инъекций или с физиологическим раствором для того, чтобы ингредиенты могли быть смешаны перед введением.
Данное изобретение обеспечивает также композицию, упакованную в герметично закрытый контейнер, такой как ампула или саше, с указанием количества антитела. В одном из вариантов осуществления изобретения, состав по изобретению, содержащий антитело, поставляется в виде сухого состава, например, в виде стерилизованного лиофилизированного порошка, лиофилизированного порошка, порошка, высушенного распылением, или в виде безводного концентрата в герметично закрытом контейнере, и композиция может быть восстановлена, например, водой или физиологическим раствором, до соответствующей концентрации, требуемой для введения индивиду. В другом варианте осуществления антитело или его антигенсвязывающий фрагмент поставляется в виде жидкой композиции, такой как раствор для инъекции или инфузии. В одном из вариантов осуществления изобретения, состав по изобретению, содержащий антитело, поставляется в виде сухого состава или в виде жидкого состава в герметично закрытом контейнере, с содержанием единичной дозы антитела или антигенсвязывающего фрагмента равной, по меньшей мере 40 мг, по меньшей мере 50 мг, более предпочтительно, по меньшей мере 75 мг, по меньшей мере 100 мг, по меньшей мере 150 мг, по меньшей мере 200 мг, по меньшей мере 250 мг, по меньшей мере 300 мг, по меньшей мере 350 мг, по меньшей мере 400 мг, по меньшей мере 450 мг, по меньшей мере 500 мг. Лиофилизированный состав по изобретению, содержащий антитело, следует хранить при температуре от 2 до 8°C в оригинальной упаковке, и антитело должно быть введено индивиду в течение 12 ч, предпочтительно, в течение 6 часов, в течение 5 часов, в течение 3 часов или в течение 1 часа после того, как она была восстановлена. Состав по изобретению, содержащий антитела, может быть получен в нейтральной форме или в форме соли. Фармацевтически приемлемые соли включают соли, происходящие из хлористоводородной, фосфорной, уксусной, щавелевой, виннокаменной кислот и т.д., и соли, образованные с катионами, такие как соли, происходящие из гидроксидов натрия, калия, аммония, кальция, железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и т.д.
Взрослые индивиды характеризуются как имеющие "гипертензию" или высокое кровяное давление, когда они имеют систолическое артериальное давление более 140 мм рт.ст. и/или диастолическое артериальное давление более 90 мм рт.ст.
Конкретные популяции пациентов, которые можно лечить с помощью терапевтических методов по изобретению, включают пациентов с одним или несколькими состояниями из следующих групп: индивиды, которым назначен LDL аферез, индивиды с мутациями, активирующими PCSK9 (увеличенная функция мутации, "GOF"), индивиды с повышенными уровнями общего холестерина, индивиды с повышенным уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), индивиды с первичной гиперхолестеринемией, такие как индивиды с первичной семейной или не-семейной гиперхолестеринемией, индивиды с гетерозиготной семейной гиперхолестеринемией (heFH); индивиды с гиперхолестеринемией, особенно с первичной гиперхолестеринемией, у которых имеется непереносимость статинов или на которых не действуют статины, и индивиды, подверженные риску развития гиперхолестеринемии, которые могли получать ранее профилактическое лечение. Другие показания включают гиперлипидемию и дислипидемию, особенно когда они связаны с вторичными причинами заболевания, такими как сахарный диабет типа 2, холестатическое заболевание печени (первичный билиарный цирроз), нефротический синдром, гипотиреоз, ожирение, а также профилактику и лечение атеросклероза и сердечно-сосудистых заболеваний, например, такого как коронарная болезнь сердца (CHD). Состояния или расстройства, которые указаны выше для популяций или индивидов, представляют собой состояния или расстройства, для которых лечение антителом по изобретению является особенно подходящим.
Однако, в зависимости от тяжести вышеуказанных заболеваний и состояний, лечение пациентов антителами и их антигенсвязывающими фрагментами по изобретению может быть противопоказано при некоторых заболеваниях и состояниях.
Термин "неблагоприятное влияние" (или "побочный эффект") относится к вредному и нежелательному эффекту от действия лекарства. Неблагоприятный эффект может быть назван "побочным эффектом", если он оценивается как вторичный по отношению к основному или терапевтическому эффекту. Некоторые побочные эффекты возникают только при начале, усилении интенсивности лечения или при прекращении лечения. Побочные эффекты могут привести к медицинским осложнениям заболевания и негативно влиять на его прогноз. Примерами побочных эффектов являются аллергические реакции, рвота, головная боль или головокружение, или любой другой эффект, описанных в настоящем описании.
Используемый в настоящем описании термин "лечить" или "лечение" заболевания или расстройства означает выполнение одного или нескольких из следующего: (а) снижение тяжести и/или длительности расстройства, (b) ограничение или предотвращение развития симптомов, характерных для расстройства (расстройств), которое лечат, (c) ингибирование ухудшения симптомов, характерных для расстройства (расстройств), которые лечат, (d) ограничение или предотвращении рецидивов расстройства (расстройств) у пациентов, у которых ранее имелось расстройство (расстройства), и (е) ограничение или предотвращение рецидива симптомов у пациентов, у которых ранее имелась симптоматика расстройства (расстройства).
Используемый в настоящем описании термин "предотвращение", "предотвращать", "предупреждение" или "профилактика" заболевания или расстройства означает предотвращение возникновения расстройства у индивида.
Повышенные уровни общего холестерина понимаются в контексте настоящего изобретения как уровни, при которых уровень общего холестерина составляет 200 мг/дл или более, особенно 240 мг/дл или более. Международные руководства по лечению рекомендуют снижение уровня LDL-С до <2,0-2,6 ммоль/л (<77-100 мг/дл) у пациентов с диагностированными сердечно-сосудистыми заболеваниями (CVD) и <1,8-2,0 ммоль/л (<70-77 мг/дл) в группах высокого риска, таких как имеющих CVD и одновременно сахарный диабет, курящих, имеющих плохо контролируемую гипертензию, метаболический синдром, или перенесших инфаркт миокарда. Таким образом, в контексте настоящего изобретения, повышенные уровни LDL-C понимаются как уровни, когда уровень LDL-C составляет 77 мг/дл или более (особенно для пациентов с одним или несколькими показателями из следующего: диагностированные CVD и диабет, курение, плохо контролируемая гипертензия, метаболический синдром или перенесенный инфаркт миокарда) и 100 мг/дл или более (особенно для пациентов с диагностированным CVD), 130 мг/дл или более, или 160 мг/дл или более, или 190 мг/дл или более. Низкие уровни липопротеинов высокой плотности (HDL-уровни), в контексте настоящего изобретения, предпочтительно, понимаются как уровни, составляющие менее приблизительно 40 мг/дл.
Повышенные уровни общего холестерина понимаются в контексте настоящего изобретения, предпочтительно, как уровни, при которых уровень общего холестерина составляет 200 мг/дл или более, особенно 240 мг/дл или более. Международные руководства по лечению рекомендуют снижение уровня LDL-С до <2,0-2,6 ммоль/л (<77-100 мг/дл) у пациентов с диагностированными сердечно-сосудистыми заболеваниями (CVD) и <1,8-2,0 ммоль/л (<70-77 мг/дл) в группах высокого риска, таких как имеющих CVD и одновременно сахарный диабет, курящих, имеющих плохо контролируемую гипертензию, метаболический синдром, или перенесших инфаркт миокарда. Таким образом, в контексте настоящего изобретения, повышенные уровни LDL-C понимаются как уровни, когда уровень LDL-C составляет 77 мг/дл или более (особенно для пациентов с одним или несколькими показателями из следующего: диабет, курение, плохо контролируемая гипертензия, метаболический синдром или перенесенный инфаркт миокарда) и 100 мг/дл или более (особенно для пациентов с диагностированным CVD), 130 мг/дл или более, или 160 мг/дл или 190 мг/дл или более. Низкие уровни липопротеинов высокой плотности (HDL-уровни), в контексте настоящего изобретения, предпочтительно, понимаются как уровни, составляющие менее приблизительно 40 мг/дл.
Термины "статины не действуют" или "устойчивый к действию статинов", особенно в контексте гиперлипидемии, гиперхолестеринемии и т.п., используются как синонимы и относятся к состояниям, например, гиперлипидемии, когда лечение статинами (т.е. регулярный прием пациентом статинов, например, аторвастатина) не приводит к значительному снижению общего холестерина или LDL-C, или не является достаточным для достижения нормальных липидемических уровней у пациента, или не является достаточным для установления липидемического (например, общего холестерина и LDL-C) уровня, который уже не будет рассматриваться как существенный фактор риска для развития сердечно-сосудистых заболеваний. Это означает, например, что лечение статинами не является достаточным для установления уровней менее 130 мг/дл в целом, или менее 100 мг/дл (например, от приблизительно ≥77 мг/дл до приблизительно 100 мг/дл), особенно у пациентов с диагностированными сердечно-сосудистыми заболеваниями, или для установления уровней приблизительно менее 77 мг/дл (например, приблизительно >70-77 мг/дл), особенно в группах повышенного риска, т.е. в группах пациентов, имеющих диагностированные CVD и диабет, курящих, имеющих плохо контролируемую гипертензию, метаболический синдром или перенесших инфаркт миокарда. В контексте настоящего изобретения понятие "устойчивость к статинам", предпочтительно, относится к устойчивости к аторвастатину.
Варианты осуществления изобретения
Настоящее изобретение далее будет описано подробно. Различные аспекты настоящего изобретения далее будут раскрыты более детально. Каждый аспект, как он раскрыт, может быть объединен с любым другим аспектом или аспектами, если явно не указано иное. В частности, любой признак, указанный как предпочтительный или преимущественный, может быть объединен с любым другим признаком или признаками, указанными как предпочтительные или преимущественные, если явно не указано иное.
В первом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей от приблизительно 40 мг до приблизительно 500 мг антитела, специфически связывающегося с пропротеином конвертазы субтилизина/кексина типа 9 (PCSK9), вместе с фармацевтически приемлемым эксципиентом или носителем.
Подходящие антитела или их фрагменты, для целей осуществления изобретения по первому аспекту, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения". Предпочтительные варианты антител или их фрагментов являются такими, как, например, описано в четвертом, седьмом и одиннадцатом аспекте настоящего изобретения.
В соответствии с предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит от приблизительно 40 мг до приблизительно 500 мг или от приблизительно 50 мг до приблизительно 500 мг антитела или его антигенсвязывающего фрагмента на одну дозу.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 300 мг, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела, или его антигенсвязывающего фрагмента.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит приблизительно 150, 200 или 300 мг антитела или его антигенсвязывающего фрагмента.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит эффективную дозу антитела или его антигенсвязывающего фрагмента, которое специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), где такая доза достаточна для устойчивого снижения уровней липопротеинов низкой плотности (LDL-C) в течение по меньшей мере 14 дней, по меньшей мере 15 дней, по меньшей мере 16 дней, по меньшей мере 17 дней, по меньшей мере 18 дней, по меньшей мере 19 дней, по меньшей мере 20 дней, по меньшей мере 21 дня, по меньшей мере 22 дней, по меньшей мере 23 дней или по меньшей мере 28 дней после введения, вместе с фармацевтически приемлемым эксципиентом или носителем. В соответствии с другим предпочтительным вариантом осуществления изобретения, доза является достаточной для устойчивого снижения уровней LDL-C в течение по меньшей мере 14 дней, 28 дней или одного месяца.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит эффективное количество ингибитора HMG-CoA-редуктазы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция скомпонована вместе с эффективным количеством ингибитора HMG-CoA-редуктазы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитором HMG-CoA-редуктазы является статин, выбранный, предпочтительно, из группы, состоящей из: церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина, и, предпочтительно, статин представляет собой аторвастатин.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит от приблизительно 0,05 мг до приблизительно 100 мг, от приблизительно 0,5 мг до приблизительно 100 мг, от приблизительно 5 мг до приблизительно 90 мг, приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг ингибитора HMG-CoA-редуктазы, и, предпочтительно, композиция содержит приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг ингибитора HMG-CoA-редуктазы.
В более предпочтительных вариантах осуществления изобретения, статин в первом и других аспектах настоящего изобретения представляет собой:
- церивастатин, в количестве от 0,05 мг до 2 мг, предпочтительно, 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, в количестве от 2 мг до 100 мг, предпочтительно, 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, в количестве от 2 мг до 100 мг, 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, в количестве от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, в количестве от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, в количестве от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, в количестве от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, в количестве от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит эффективную дозу ингибитора HMG-CoA-редуктазы, достаточную для снижения уровней LDL-D при введении один раз в день.
В более предпочтительных вариантах осуществления изобретения по первому аспекту настоящего изобретения, статин представляет собой:
- церивастатин, в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В соответствии с предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент, при введении индивиду, например, человеку или млекопитающему, не относящемуся к человеку, характеризуется одним или несколькими признаками из следующих:
а. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 25%, и более предпочтительно, по меньшей мере 30%, по сравнению с уровнем до введения дозы, в частности, при введении в дозе от приблизительно 40 мг до приблизительно 60 мг, предпочтительно, от приблизительно 45 мг до приблизительно 55 мг, и, более предпочтительно, приблизительно 50 мг при режиме введения один раз в две недели (через одну неделю, E2W);
b. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 65%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40% и, более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 100 мг в режиме E2W;
с. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 60% до по меньшей мере приблизительно 75% (например, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70% или по меньшей мере приблизительно 75%), по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 55%, и более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
d. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 40% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 35%, и более предпочтительно, по меньшей мере 40%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 200 мг в режиме E4W;
е. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 300 мг в режиме E4W;
f. увеличение уровней сывороточного HDL холестерина по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5%, по сравнению с уровнем до введения дозы индивиду, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
g. наличие небольшого или нерегистрируемого эффекта на уровни тропонина, при введении индивиду;
h. увеличение одного или нескольких из следующего: уровней общего холестерина, уровней ApoB, уровней холестерина, не относящегося к HDL-С, соотношения ApoB/ApoA-1, при введении индивиду.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент способен устранить устойчивость к статинам при введении индивиду с гиперхолестеринемией, устойчивой к действию статинов.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO:90/92, или из пар по существу идентичных им последовательностей, имеющих по меньшей мере 98% или 99% идентичности с ними.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит пару аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO: 90/92, или пару по существу идентичных им последовательностей, имеющих по меньшей мере 98% или 99% идентичности с ними.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание с антителом против hPCSK9 или с его антигенсвязывающим фрагментом, содержащим пару аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий аминокислотный остаток 238 hPCSK9 (SEQ ID NO:755).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий один или несколько аминокислотных остатков в положениях 238, 153, 159 и 343 hPCSK9 (SEQ ID NO:755).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп, который не содержит аминокислотного остатка в положениях 192, 194, 197 и/или 237 hPCSK9 (SEQ ID NO: 755).
Фармацевтическая композиция может быть получена в любой фармацевтически приемлимой форме, как известно в данной области и, в частности, как описано в настоящем документе, например, в виде сухого состава для растворения или в виде жидкого состава. Подходящие формы составов антител известны в данной области и включают сухие составы (например, в лиофилизированной форме, в высушенной замораживанием или распылением форме, в виде безводного концентрата), а также жидкие составы (например, растворы). Подходящие составы статинов являются хорошо известными в данной области и включают сухие составы, а также жидкие составы, например, суспензии, дисперсии и растворы (для справки см., например, работу R. Tiwari, K. Pathak "Statins therapy: a review on conventional and novel formulation approaches", Journal of Pharmacy and Pharmacology, 2011, содержание которой включено в настоящее описание в качестве ссылки в полном объеме).
В соответствии с предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит антитело или его антигенсвязывающий фрагмент в виде сухого состава для растворения, такого как лиофилизированный порошок, порошок высушенный замораживанием или распылением, или в виде безводного концентрата.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит антитело или его антигенсвязывающий фрагмент в виде жидкого состава, например, раствора для инъекции или инфузии.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция содержит ингибитор HMG-CoA-редуктазы в форме состава для орального или перорального приема, например, в виде капсулы или таблетки, или в форме жидкого состава, например, в виде суспензии, дисперсии или раствора, например, для перорального введения, инъекции или инфузии.
В соответствии с другим предпочтительным вариантом осуществления изобретения, фармацевтическая композиция предназначена для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, или для снижения повышенного уровня общего холестерина или повышенного уровня LDL-C. Кроме того, предпочтительные применения, схемы дозировки, схемы введения антитела или его фрагмента или ингибитора HMG-CoA-редуктазы, или популяции, которые подвергаются лечению фармацевтической композицией, описаны в настоящей заявке, например, в седьмом аспекте, в аспектах с одиннадцатого по тринадцатый, или в восемнадцатом и девятнадцатом аспектах.
Во втором аспекте настоящее изобретение относится к инъекционному раствору, как описано в настоящем документе, где раствор содержит антитело или его антигенсвязывающий фрагмент по настоящему изобретению, и предпочтительно, содержит в 1 мл объема от приблизительно 40 мг до приблизительно 200 мг или от приблизительно 50 мг до приблизительно 200 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг антитела или его антигенсвязывающего фрагмента.
Препараты для инъекций могут включать дозированные формы для внутривенного, подкожного, внутрикожного и внутримышечного введения, для капельных вливаний и т.п. Эти препараты для инъекций могут быть получены общеизвестными способами. Например, препараты для инъекций могут быть получены, например, путем растворения, суспендирования или эмульгирования описанного выше антитела или его соли в стерильной водной среде или в масляной среде, которые обычно используют для инъекций. В качестве водной среды для инъекций, известны, например, физиологический раствор, изотонический раствор, содержащий глюкозу и другие вспомогательные средства, и т.п., которые могут быть использованы в сочетании с соответствующим солюбилизирующим средством, таким как спирт (например, этанол), многоатомный спирт (например, пропиленгликоль, полиэтиленгликоль), неионогенное поверхностно-активное вещество [например, полисорбат 80, НСО-50 (аддукт полиоксиэтилена (50 моль) и гидрированного касторового масла)] и т.п. В качестве масляной среды используют, например, кунжутное масло, соевое масло и т.п., которые могут быть использованы в сочетании с солюбилизирующим средством, таким как бензилбензоат, бензиловый спирт и т.п. Полученными таким образом растворами для инъекций, предпочтительно, заполняют соответствующие ампулы. Фармацевтическая композиция по настоящему изобретению может вводиться подкожно или внутривенно, с использованием стандартной иглы и шприца. Кроме того, в отношении подкожного введения, может быть применено готовое для применения устройство для введения типа ручки, снаряженное фармацевтической композицией по настоящему изобретению. Такое устройство для введения в виде ручки может быть многоразовым или одноразовым. В многоразовом устройстве для введения в виде ручки обычно используется сменный картридж, содержащий фармацевтическую композицию. После введения пациенту фармацевтической композиции картридж становится пустым, и пустой картридж можно легко снять и заменить новым картриджем, содержащим фармацевтическую композицию. Устройство для введения типа ручки может быть использовано повторно. В одноразовом устройстве для введения в виде ручки сменный картридж отсутствует. Как правило, одноразовые устройства для введения в виде ручки поставляются с резервуаром внутри устройства, уже заполненным фармацевтической композицией. Когда резервуар освобождается от фармацевтической композиции, все устройство выбрасывается.
В третьем аспекте настоящее изобретение относится к сухому составу, как в настоящем описании описано, содержащему антитело или его антигенсвязывающий фрагмент по настоящему изобретению, и предпочтительно, содержащему, из расчета на одну дозу, от приблизительно 40 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 400 мг, от приблизительно 50 мг до приблизительно 300 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг, и более предпочтительно, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, и еще более предпочтительно, приблизительно 150 мг, приблизительно 200 мг или приблизительно 300 мг антитела или его антигенсвязывающего фрагмента.
Подходящие составы антител известны в данной области и включают сухие составы (например, в лиофилизированной форме, в высушенной замораживанием или распылением форме, в виде безводного концентрата), а также жидкие составы (например, растворы). Подходящие составы статинов являются хорошо известными в данной области техники и включают сухие составы, а также жидкие составы, например, суспензии, дисперсии и растворы (для справки см., например, работу R. Tiwari, K. Pathak "Statins therapy: a review on conventional and novel formulation approaches", Journal of Pharmacy and Pharmacology, 2011, содержание которой включено в настоящее описание в качестве ссылки в полном объеме).
Композиции по настоящему изобретению могут содержать дополнительные активные ингредиенты, в частности, ингибиторы HMG-CoA-редуктазы, как описано в настоящем описании. Предпочтительные варианты осуществления составов по настоящему изобретению описаны в других разделах настоящей заявки, например, в других аспектах настоящего изобретения, таких как первый или четвертый аспект.
Согласно четвертому аспекту, настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), входящему в состав одной из фармацевтических композиций по изобретению.
В соответствии с предпочтительным вариантом осуществления изобретения, антитело, при введении индивиду, предпочтительно, человеку или млекопитающему, не относящемуся к человеку, характеризуется одним или несколькими признаками из следующих, обеспечивая:
1. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 25%, и более предпочтительно, по меньшей мере 30%, по сравнению с уровнем до введения дозы, в частности, при введении в дозе от приблизительно 40 мг до приблизительно 60 мг, предпочтительно, от приблизительно 45 мг до приблизительно 55 мг, и более предпочтительно, приблизительно 50 мг при режиме введения один раз в две недели (через одну неделю, E2W);
2. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 65%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 100 мг в режиме E2W;
3. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 60% до по меньшей мере приблизительно 75% (например, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70% или по меньшей мере приблизительно 75%), по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 55%, и более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
4. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 40% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 35%, и более предпочтительно, по меньшей мере 40%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 200 мг в режиме E4W;
5. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 300 мг в режиме E4W;
6. увеличение уровней сывороточного HDL холестерина по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
7. снижение уровня общего холестерина в сыворотке по меньшей мере от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 24 дней;
8. снижение уровня общего холестерина в сыворотке по меньшей мере от приблизительно 65% до приблизительно 80%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 24 дней;
9. снижение уровня триглицеридов в сыворотке по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы;
10. наличие небольшого или нерегистрируемого эффекта на функцию печени, по измерению ALT и AST;
11. наличие небольшого или нерегистрируемого эффекта на уровни тропонина;
12. увеличение одного или нескольких из следующего: уровней общего холестерина, уровней ApoB, уровней холестерина не относящегося к HDL-С, соотношения ApoB/ApoA-1.
Антитело по настоящему изобретению обладает вышеуказанными свойствами, когда его вводят, предпочтительно, в комбинации с применением ингибитора HMG-CoA-редуктазы. Предпочтительные варианты ингибиторов HMG-CoA-редуктазы, которые используются в сочетании с антителом по изобретению, режимы дозирования и введения можно найти в описании, в частности, как описано в аспектах, связанных с медицинскими применениями и способами лечения.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения, антитела и их антигенсвязывающие фрагменты представляют, в частности, антитело или его антигенсвязывающий фрагмент в соответствии с четвертым аспектом, при этом антитело или его антигенсвязывающий фрагмент имеет одну или несколько из следующих характеристик:
(i) антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO:90/92;
(ii) антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92;
(iii) антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения, антитела и их антигенсвязывающие фрагменты представляют, в частности, антитело или его антигенсвязывающий фрагмент в соответствии с четвертым аспектом, при этом антитело или его антигенсвязывающий фрагмент имеет одну или несколько из следующих характеристик:
(i) устраняет устойчивость к статинам у млекопитающих, особенно у грызунов, таких как хомяк;
(ii) увеличивает экспрессию LDLR у млекопитающих, особенно у грызунов, таких как хомяк;
(iii) снижает уровень сывороточного LDL-C у грызунов, таких как хомяк;
(iv) синергически снижает уровни LDL-С в сочетании с введением ингибитора HMG-CoA-редуктазы, в частности, у грызунов, таких как хомяк, где ингибитором HMG-CoA-редуктазы, предпочтительно, является аторвастатин.
Другие подходящие характеристики и структурные особенности антитела по настоящему изобретению и, в частности, антитела по четвертому варианту, а также антител и их антигенсвязывающих фрагментов, которые могут быть использованы для осуществления пятнадцатого и других аспектов настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
Антитело по настоящему изобретению, такое как антитело согласно четвертому аспекту, предпочтительно, готовят в виде фармацевтически приемлимого состава, как известно в данной области, и, в частности, как описано в настоящем документе, например, в виде сухого состава для растворения или в виде жидкого состава, например, как описано во втором или третьем аспекте изобретения.
В пятом аспекте настоящее изобретение направлено на лекарственную форму, содержащую антитело, антигенсвязывающий фрагмент или фармацевтическую композицию по настоящему изобретению. Подходящие варианты осуществления антитела, фармацевтической композиции или состава, который используется для осуществления пятого аспекта настоящего изобретения, могут быть получены, как указано в соответствующих разделах настоящей заявки, например, от первого до четвертого аспектов, или в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В соответствии с предпочтительным вариантом осуществления изобретения, лекарственная форма содержит приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела или его антигенсвязывающего фрагмента.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма содержит антитело или его фрагмент в виде сухого состава для растворения в герметично закрытом контейнере, таком как флакон, ампула или саше.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма содержит антитело или его фрагмент в виде жидкого состава в герметично закрытом контейнере, таком как флакон, саше, предварительно заполненный шприц, предварительно заполненный автоинъектор или картридж для многоразового шприца или аппликатора.
Согласно еще одному предпочтительному варианту осуществления изобретения, количество активного ингредиента указано на герметично закрытом контейнере.
Как использовано в различных аспектах и вариантах осуществления настоящего изобретения, и, в частности, в пятом аспекте, термин "лекарственная форма" относится к физически дискретным единицам, подходящим в качестве разовых доз для человека и животного, причем каждая единица содержит заранее определенное количество активного материала (например, приблизительно 40 мг или от приблизительно 50 мг до приблизительно 500 мг антитела против PCSK9 и/или, например, от 0,05 мг до 100 мг ингибитора HMG-CoA-редуктазы), рассчитанное на получение желаемого терапевтического эффекта, в сочетании с требуемым фармацевтическим разбавителем, носителем или эксципиентом. Требования к новым лекарственным формам данного изобретения диктуются и непосредственно зависят от (а) уникальных характеристик активного материала и достигаемого определенного терапевтического эффекта, и (b) ограничения, присущего в данной области при приготовлении составов из такого активного материала для терапевтического применения у животных или людей, как раскрыто в данном описании, и эти требования и характеристики являются признаками настоящего изобретения. Примерами подходящих лекарственных форм по настоящему изобретению являются флаконы, таблетки, капсулы, пастилки, суппозитории, пакетики с порошком, облатки, крахмальные капсулы, ампулы, разделенные на части множества любых вышеуказанных форм, а также другие формы, описанные в настоящем документе или общеизвестные в уровне техники.
Одна или несколько таких лекарственных форм антитела могут быть включены в изделие по настоящему изобретению, необязательно дополнительно содержащему одну или несколько лекарственных форм ингибитора HMG-CoA-редуктазы (например, блистер таблеток, содержащих в качестве активного ингредиента ингибитор HMG-CoA-редуктазы).
Термин "активное вещество" относится к любому веществу, обладающему терапевтической активностью, например, к одному или нескольким активным ингредиентам. Активные ингредиенты, которые должны быть использованы в качестве терапевтических средств, могут быть легко получены в такой лекарственной форме, с применением фармацевтических материалов, которые сами по себе являются доступными в данной области, или которые могут быть получены известными способами. Предпочтительные активные ингредиенты по настоящему изобретению представляют собой антитело или его фрагмент, или ингибитор HMG-CoA-редуктазы, такой как статин.
В предпочтительном варианте осуществления изобретения, лекарственная форма содержит от 40 мг до приблизительно 500 мг антитела или его антигенсвязывающего фрагмента по изобретению. В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма содержит приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг, и более предпочтительно, приблизительно 150 мг, приблизительно 200 мг или приблизительно 300 мг антитела или его антигенсвязывающего фрагмента. Кроме того, предпочтительные дозировки и режимы дозирования являются такими, как раскрыто по тексту описания, например, в первом и втором аспектах, или в аспектах с пятнадцатого по девятнадцатый.
Согласно другому предпочтительному аспекту, лекарственная форма содержит антитело, его антигенсвязывающий фрагмент или фармацевтическую композицию в виде сухого состава для растворения, такого как лиофилизированный порошок, порошок, высушенный замораживанием, или безводный концентрат. В соответствии с другим предпочтительным вариантом осуществления изобретения, сухой состав находится в герметично закрытом контейнере, таком как флакон, ампула или саше.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма содержит антитело, его антигенсвязывающий фрагмент или фармацевтическую композицию в виде жидкого состава, например, в виде раствора для инъекции или инфузии. В соответствии с другим предпочтительным вариантом осуществления изобретения, жидкий состав находится в герметично закрытом контейнере, таком как флакон, саше, предварительно заполненный шприц, предварительно заполненный автоинъектор или картридж для многоразового шприца или аппликатора.
Кроме того, предпочтительно, когда количество активного ингредиента (например, антитела) указано на герметичном контейнере для лекарственной формы.
Следующие перечисленные препараты являются иллюстративными для получения лекарственных форм по настоящему изобретению, при этом они не рассматриваются в качестве ограничения. Некоторые лекарственные формы могут быть получены по соответствующие варианту осуществления настоящего изобретения. Например, единичная доза из расчета на флакон может содержать 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл, 5 мл, 6 мл, 7 мл, 8 мл, 9 мл, 10 мл, 15 мл или 20 мл антитела против PCSK9 или его фрагмента, в количестве в пределах от приблизительно 40 мг до приблизительно 500 мг или от приблизительно 50 мг до приблизительно 500 мг антитела против PCSK9. Если необходимо, эти препараты могут быть скорректированы до требуемой концентрации путем добавления в каждый флакон стерильного разбавителя.
В одном из вариантов осуществления изобретения, компоненты композиции по изобретению поставляются отдельно или смешиваются вместе в виде лекарственной формы, например, в виде сухого состава для растворения или в виде жидкого состава. Получение фармацевтически приемлемых составов белковых молекул, таких как антитела или их антигенсвязывающих фрагментов, или низкомолекулярных соединений, таких как статины, в целом известны в данной области. Кроме того, смотрите раздел "Предпочтительные антитела для осуществления настоящего изобретения" или второй или третий аспект настоящего изобретения для некоторых подходящих составов антител, а для малых молекул ингибиторов HMG-CoA-редуктазы, таких как статины, см., например, "Statins therapy: a review on conventional and novel formulation approaches", R.Tiwari and K. Pathak, Journal of Pharmacy and Pharmacology 2011, p. 983-998. В соответствии с предпочтительным вариантом осуществления изобретения, активные ингредиенты, активное вещество или фармацевтическая композиция по настоящему изобретению представляет собой сухой состав для растворения в жидкости, например, такой, как лиофилизированный порошок, порошок, высушенный замораживанием или безводный концентрат, который, предпочтительно, находится в герметично закрытом контейнере, таком как флакон, ампула или саше, предпочтительно, с указанием количества активного агента. Когда композиция предназначена для введения путем инфузии, она может находиться во флаконе для инфузии, содержащем стерильную воду или физиологический раствор фармацевтической чистоты. Когда композицию вводят путем инъекции, может быть предоставлена ампула со стерильной водой для инъекций или физиологическим раствором, чтобы ингредиенты могли быть смешаны перед введением.
Составы по изобретению включают композиции нерасфасованных лекарственных форм, которые используются при изготовлении фармацевтических композиций (например, композиций, пригодных для введения индивиду или пациенту), которые, в свою очередь, могут быть использованы при изготовлении дозированных форм. В предпочтительном варианте осуществления изобретения, композиция представляет собой фармацевтическую композицию. Такие композиции содержат профилактически или терапевтически эффективное количество одного или нескольких профилактических или терапевтических средств (например, антитела по изобретению или другого профилактического или терапевтического средства) и фармацевтически приемлемый носитель. Предпочтительно, фармацевтические композиции готовят в форме, подходящей для соответствующего способа введения индивиду.
В конкретном варианте осуществления изобретения, термин "фармацевтически приемлемый" означает одобренный регулирующим ведомством США на федеральном уровне или на уровне штата, или одобренный EMA (Европейское агентство по лекарственным средствам), или указанный в Фармакопее США (United States Pharmacopeia-33/National Formulary-28 Reissue, published by the United States Pharmacopeial Convention, Inc., Rockville Md., publication date: April 2010) или в другой общепризнанной фармакопее для применения у животных и, в частности, для применения у людей.
Термин "носитель" относится к разбавителю, вспомогательному веществу (например, к адъюванту Фрейнда (полному и неполному)), эксципиенту или носителю, с которым вводят лекарственное средство. Такими фармацевтическими носителями могут быть стерильные жидкости, такие как вода и масла, включая масла из нефти, масла животного, растительного или синтетического происхождения, например, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Вода является предпочтительным носителем для случая, когда фармацевтическую композицию вводят внутривенно. Солевые растворы и водные растворы декстрозы и глицерина также могут быть использованы в качестве жидких носителей, в частности, для инъекционных растворов. Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропиленгликоль, воду, этанол и т.п. Композиция, при желании, может также содержать небольшие количества смачивающих или эмульгирующих агентов, или агентов, буферирующих рН. Эти композиции могут быть представлены в виде растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, составов длительного высвобождения и т.п. Состав для перорального применения может включать стандартные носители, такие как маннит, лактозу, крахмал, стеарат магния, сахарин натрия, целлюлозу, карбонат магния и т.п. Примеры подходящих фармацевтических носителей описаны в "Remington′s Pharmaceutical Sciences" под ред. E.W. Martin. Такие композиции будут содержать профилактически или терапевтически эффективное количество антитела, предпочтительно, в очищенной форме, вместе с подходящим количеством носителя так, чтобы обеспечить форму, подходящую для введения пациенту. Композиция может дополнительно содержать один или несколько других активных ингредиентов, таких как ингибитор HMG-CoA-редуктазы. Состав должен соответствовать способу введения.
Как правило, ингредиенты композиции по изобретению поставляются либо отдельно, либо в смеси друг с другом в виде лекарственной форме, например, в виде сухого состава для растворения, такого как лиофилизированного порошка, порошка, высушенного с замораживанием, или в виде безводного концентрата в герметично закрытом контейнере, таком как ампула или саше, с указанием количества активного агента. Ингредиенты композиции по изобретению также могут поставляться в виде смешанного жидкого состава (например, в виде раствора для инъекции или инфузии) в герметично закрытом контейнере, таком как ампула, саше, предварительно заполненный шприц или автоинъектор, или картридж для многоразового шприца или аппликатора (например, для ручки или автоинъектора). Когда композиция предназначена для введения путем инфузии, она может быть включена во флакон для инфузии, содержащий стерильную воду или физиологический раствор фармацевтической чистоты. Когда композицию вводят путем инъекции, может быть предоставлена ампула со стерильной водой для инъекций или с физиологическим раствором для того, чтобы ингредиенты могли быть смешаны перед введением. Композиция может также содержать два или более активных ингредиентов, каждый из которых приготовлен в виде состава другим или аналогичным образом, например, путем объединения антитела по настоящему изобретению вместе с ингибитором HMG-CoA-редуктазы.
Данное изобретение также относится к составу, упакованному в герметично закрытый контейнер, такой как ампула или саше, с указанием количества антитела. В одном из вариантов осуществления изобретения, состав по изобретению, содержащий антитело, поставляется в виде сухого состава, например, в виде стерилизованного лиофилизированного порошка, лиофилизированного порошка, порошка, высушенного распылением, или в виде безводного концентрата в герметично закрытом контейнере, и композиция может быть восстановлена, например, водой или физиологическим раствором, до соответствующей концентрации, требуемой для введения индивиду. В одном из вариантов осуществления изобретения, состав по изобретению, содержащий антитело, поставляется в виде сухого стерильного лиофилизированного порошка в герметично закрытом контейнере, с содержанием единичной дозы антитела или антигенсвязывающего фрагмента равной, по меньшей мере 40 мг, по меньшей мере 50 мг, более предпочтительно, по меньшей мере 75 мг, по меньшей мере 100 мг, по меньшей мере 150 мг, по меньшей мере 200 мг, по меньшей мере 250 мг, по меньшей мере 300 мг, по меньшей мере 350 мг, по меньшей мере 400 мг, по меньшей мере 450 мг, по меньшей мере 500 мг. Лиофилизированный состав по изобретению, содержащий антитело, следует хранить при температуре от 2 до 8°C в оригинальном контейнере, и антитело должно быть введено индивиду в течение 12 ч, предпочтительно, в течение 6 часов, в течение 5 часов, в течение 3 часов или в течение 1 часа после того, как он был восстановлен. Состав по изобретению, содержащий антитела, может быть получен в нейтральной форме или в форме соли. Фармацевтически приемлемые соли, такие как соли, происходящие из хлористоводородной, фосфорной, уксусной, щавелевой, виннокаменной кислот и т.д., и соли, образованные с катионами, такие как соли, происходящие из гидроксидов натрия, калия, аммония, кальция, железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и т.д.
В шестом аспекте настоящее изобретение относится к изделию, содержащему фармацевтическую композицию по изобретению, жидкий состав по изобретению или сухой состав по изобретению, антитело или его антигенсвязывающий фрагмент по изобретению, или одну или несколько лекарственных форм по изобретению, и контейнер или пакет.
В соответствии с предпочтительным вариантом осуществления изобретения, изделие содержит лекарственные формы антитела, в количестве, достаточном для введения в течение двух недель (14 дней), четырех недель (28 дней) или одного месяца, в режиме введения E2W, E4W или один раз в месяц.
Изделие может содержать одну или несколько лекарственных форм, которые содержат антитело и HMG-CoA-ингибитор, например, лекарственная форма может содержать жидкий состав для инъекции или инфузии, содержащий все активные ингредиенты. Изделие может также содержать антитело (или его антигенсвязывающий фрагмент) и ингибитор HMG-CoA-редуктазы в двух или нескольких отдельных лекарственных формах.
Согласно одному варианту осуществления изобретения, изделие содержит одну или несколько отдельных лекарственных форм ингибитора HMG-CoA-редуктазы по настоящему изобретению.
В соответствии с предпочтительным вариантом осуществления изобретения, каждая лекарственная форма ингибитора HMG-CoA-редуктазы содердит от приблизительно 0,05 мг до приблизительно 100 мг ингибитора HMG-CoA-редуктазы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы представляет собой статин, предпочтительно, выбранный из перечня, содержащего: церивастатин, аторвастатин, симвастатин, питавастатин, розувастатин, флувастатин, ловастатин, правастатин, или, предпочтительно, представляет собой аторвастатин.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы, например, статин, представлен в эффективной дозе из расчета введения один раз в день.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма ингибитора HMG-CoA-редуктазы содержит от приблизительно 0,5 до приблизительно 100 мг, от приблизительно от 5 до приблизительно 90 мг, или приблизительно 10 мг, 20 мг, 40 мг или 80 мг ингибитора HMG-CoA-редуктазы.
В соответствии с предпочтительным вариантом осуществления изобретения, изделие содержит лекарственные формы ингибитора HMG-CoA-редуктазы, в количестве, достаточном для ежедневного режима введения.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственная форма, содержащая антитело, представляет собой саше, предварительно заполненный шприц, предварительно заполненный автоинъектор или картридж для многоразового шприца или аппликатора, содержащих в частности, 1 мл или 2 мл раствора для инъекции.
Согласно другому варианту осуществления изобретения, изделие включает один или несколько следующих компонентов:
a. одну или несколько лекарственных форм, содержащих антитело по настоящему изобретению;
b. одну или несколько лекарственных форм, содержащих ингибитор HMG-CoA-редуктазы по настоящему изобретению;
c. инструкции по применению;
d. устройство для введения антитела, такое как шприц.
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие содержит лекарственные формы антитела и, предпочтительно, также ингибитор HMG-CoA-редуктазы в количестве, достаточном для:
(а) однократного введения антитела и ингибитора HMG-CoA-редуктазы; например, изделие содержит ампулу, саше, флакон, картридж или предварительно заполненный шприц, содержащий приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела, и предпочтительно, приблизительно 150 мг антитела, приблизительно 200 мг антитела или приблизительно 300 мг антитела, вместе с таблеткой или капсулой, например, для орального или перорального введения, содержащей HMG-СоА-ингибитор, например, содержащий приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг ингибитора HMG-CoA-редуктазы, такого как аторвастатин;
(b) введения в течение двух недель (т.е. 14 дней) антитела и ингибитора HMG-CoA-редуктазы; например, изделие содержит ампулу, саше, флакон, картридж или предварительно заполненный шприц, содержащий приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела, и предпочтительно, приблизительно 150 мг антитела, приблизительно 200 мг антитела или приблизительно 300 мг антитела, вместе с достаточным количеством дозированных единиц, содержащих ингибитор HMG-CoA-редуктазы (например, таблеток или капсул, например, для орального или перорального введения), обеспечивающим 14-дневное введение, например, 14 дозированных единиц ингибитора HMG-CoA-редуктазы для режима введения один раз в день, или 28 единиц для режима введения дважды в день и т.д., где лекарственная форма HMG-CoA-ингибитора из расчета приема на день, предпочтительно, содержит приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг HMG-CoA-ингибитора, такого как аторвастатин. В случае, когда антитело должно вводиться в дозе более 200 мг, может быть предпочтительным использование двух лекарственных форм антитела, которые вместе обеспечивают общую указанную дозу (например, два предварительно заполненных шприца, каждый из которых содержит приблизительно 150 мг антитела в 1 мл жидкого состава, обеспечивают (например, при подкожном введении) общее количество антитела, приблизительно равное 300 мг, за две инъекции, или может быть предпочтительным использование двух единиц, содержащих приблизительно 100 мг антитела для каждой, которые обеспечивают общую дозу антитела, приблизительно равную 200 мг, или двух единиц, содержащих приблизительно 175 мг антитела, которые обеспечивают общую дозу антитела, приблизительно равную 350 мг, и т.п.).
(с) введения в течение четырех недель (т.е. 28 дней) антитела и ингибитора HMG-CoA-редуктазы, например:
1. для введения антитела в количестве от приблизительно 50 мг до приблизительно 200 мг антитела на две недели по режиму E2W: изделие включает две лекарственные формы (например, как пояснено выше), каждая из которых содержит приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг антитела или его антигенсвязывающего фрагмента, вместе с 28 дозированными единицами ингибитора HMG-CoA-редуктазы (как пояснено выше), принимаемыми ежедневно по режиму один раз в день, или вместе с 56 дозированными единицами ингибитора HMG-CoA-редуктазы, принимаемыми ежедневно по режиму два раза в день, при этом, предпочтительно, наличие 28 дозированных единиц (например, капсул или таблеток), содержащих по приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг аторвастатина;
2. для введения антитела или его фрагмента в количестве приблизительно 200 мг на четыре недели (28 дней) по режиму E4W: изделие содержит одну лекарственную форму антитела, содержащую приблизительно 200 мг антитела (например, как пояснено выше), вместе с 28 или 56, предпочтительно, 28 дозированными единицами ингибитора HMG-CoA-редуктазы (как пояснено выше);
3. для введения антитела в количестве более 200 мг на четыре недели (28 дней) по режиму E4W: изделие содержит две лекарственные формы, которые вместе обеспечивают требуемую общую дозу антитела (например, два предварительно заполненных шприца, каждый из которых содержит 1 мл жидкого состава, содержащего 150 мг антитела), или изделие включает одну лекарственную форму, которая содержит требуемое общее количество антитела для введения (например, флакон, содержащий 300 мг антитела для растворения, или флакон, картридж или предварительно заполненный шприц, содержащие приблизительно 300 мг антитела в виде жидкого состава (т.е. приблизительно 2 мл жидкого состава, где 1 мл жидкого состава содержит приблизительно 150 мг антитела), вместе с 28 или 56, предпочтительно, 28 дозированными единицами ингибитора HMG-CoA-редуктазы (как пояснено выше);
(d) введения в течение одного месяца антитела и ингибитора HMG-CoA-редуктазы; изделие содержит такое же количество лекарственных форм антитела, как пояснено в пункте (с) для введения один или два раза в месяц, например, каждый первый день месяца или каждый первый понедельник месяца и т.п. при режиме введения один раз в месяц, или, например, каждый первый и 14-й или 15-й день месяца, при режиме введения два раза в месяц; кроме того, изделие содержит 31 дозированную единицу ингибитора HMG-CoA-редуктазы, предпочтительно, таблеток или капсул, размещенных в блистере, который содержит последовательную нумерацию от 1 до 31 дня месяца (при этом лишние таблетки или капсулы, соответствующие большему количеству дней, должны быть исключены из курса приема).
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие содержит: (а) упаковку, (b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и (c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие содержит: (а) упаковку, (b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и (c) этикетку или вкладыш в упаковку, где указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом осуществляется совместно с применением HMG-CoA-ингибитора, такого как статин.
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие включает: (а) упаковку, (b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и (c) этикетку или вкладыш в упаковку, где указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом вместе с HMG-CoA-ингибитором, таким как статин, противопоказано для пациентов, принадлежащих к одной или нескольким группам из числа следующих групп: (i) курильщики; (ii) лица в возрасте 70 лет и старше; (iii) лица, страдающие от гипертензии; (iv) беременные женщины; (v) женщины, пытающиеся забеременеть; (vi) женщины, которые кормят грудью; (vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень; (viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени; (ix) лица, которые употребляют чрезмерное количество алкоголя; (х) лица, имеющие проблемы с почками; (xi) лица, страдающие гипотиреозом; (xii) лица, страдающие мышечными расстройствами; (xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами; (xiv) лица, имеющие серьезные проблемы с дыханием; (xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой; (xvi) лица, выпивающие более 0,1 л сока грейпфрута в день или съедающие более половины грейпфрута в сутки; (xvii) лица, имеющие индекс массы тела (BMI) более 40; (xviii) лица, имеющие индекс массы тела (BMI) менее 18; (xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2; (xx) лица, имеющие положительную реакцию на гепатит В или С; (xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами; (xxii) лица, имеющие концентрацию нейтрофилов менее 1500/мм3; (xxiii) лица, имеющие концентрацию тромбоцитов менее 100000/мм3; (xxiv) мужчины, имеющие уровень креатинина в сыворотке более 1,5×ULN (верхняя граница нормы); (xxv) женщины, имеющие уровень креатинина в сыворотке более 1,4×ULN (верхняя граница нормы); (xxvi) индивиды, имеющие уровень аланинаминотрансферазы (ALT) или уровень аспартаттрансаминазы (AST) более чем 2×ULN, и (xxvii) индивиды, имеющие уровень СРК более 3×ULN.
В предпочтительных вариантах осуществления изобретения по шестому аспекту, антитело или его антигенсвязывающий фрагмент представляет собой антитело или его антигенсвязывающий фрагмент, описанный ниже в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
Этикетка или вкладыш, в соответствии с различными аспектами и вариантами осуществления изобретения, в частности, для различных изделий, получаемых согласно изобретению, может быть любым типом носителя данных, пригодным для компоновки с изделием (приложенным к изделию или прикрепленным к компоненту изделия, например, нанесенным на блистер или флакон, содержащий лекарственные формы антитела и/или ингибитора HMG-CoA-редуктазы), включенным в упаковку или контейнер, или находящимся на внешней стороне упаковки или контейнера. Предпочтительно, когда носитель данных (т.е. этикетка или чип, штрих-код или буклет, или этикетка, содержащая штрих-код и т.п.) содержит информацию, такую как:
(i) композиция, состав, концентрация и общее количество, тип активного ингредиента(ов), содержащегося в изделии, т.е. информацию в отношении антитела или его антигенсвязывающих фрагментов, ингибитора HMG-CoA-редуктазы, фармацевтической композиции, лекарственной формы или состава по настоящему изобретению;
(ii) количество и состав лекарственной формы, содержащейся в изделии;
(iii) показания, противопоказания для применения антитела или его антигенсвязывающих фрагментов, фармацевтической композиции, лекарственной формы или состава по настоящему изобретению;
(iv) индивиды/пациенты или популяции индивидов/пациентов, которым показано или противопоказано лечение с помощью антитела или его антигенсвязывающих фрагментов, фармацевтической композиции, лекарственной формы или состава по настоящему изобретению;
(v) инструкции по применению, режимы дозирования и/или режимы введения;
(vi) информации о качестве, такая как сведения о номере серии/партии антитела или его антигенсвязывающих фрагментов, фармацевтической композиции, лекарственной формы или препарата по настоящему изобретению, месте изготовления или комплектации, дата истечения срока действия или срок годности;
(vii) информация по правилам хранения и применения изделия, устройства для введения или антитела или его антигенсвязывающих фрагментов, фармацевтической композиции, лекарственной формы или препарата по настоящему изобретению;
(iv) информация о составе буфера(ов), разбавителя(ей), реагента(ов), эксципиентов, носителей, состава антитела или его антигенсвязывающих фрагментов, фармацевтической композиции, лекарственной формы или состава по настоящему изобретению;
(vi) предупреждение о возможных последствиях при применении неподходящих доз или схем введения и/или при использовании в случае противопоказаний для популяции пациентов.
В предпочтительных вариантах осуществления изобретения по шестому аспекту, этикетка или вкладыш в упаковку содержит указание на способ лечения или медицинского применения в соответствии с седьмым аспектом, аспектам с одиннадцатого по тринадцатый, с аспектом восемнадцатым или девятнадцатым, и на варианты осуществления изобретения по первому или второму аспекту, как описано в настоящем документе.
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие содержит: (а) упаковку, (b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и (c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, и дополнительно указано, что можно лечить индивидов, входящих в одну или несколько групп индивидов, перечисленных в восемнадцатом аспекте настоящего изобретения.
В соответствии с другим предпочтительным вариантом осуществления изобретения, изделие содержит: (а) упаковку, (b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и (c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, и дополнительно указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом противопоказано для пациентов, принадлежащих к одной или нескольким группам индивидов, указанных в девятнадцатом аспекте настоящего изобретения.
В предпочтительных вариантах осуществления изобретения по шестому аспекту, этикетка или вкладыш в упаковку содержит указание на способ лечения в соответствии с медицинскими применениями и способами лечения в соответствии, например, с седьмым аспектом, аспектам с одиннадцатого по тринадцатый, с аспектом восемнадцатым или девятнадцатым, как описано в настоящем документе.
Согласно седьмому аспекту, настоящее изобретение относится к фармацевтической композиции, антителу или его антигенсвязывающему фрагменту по изобретению для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9.
В соответствии с предпочтительным вариантом осуществления изобретения по седьмому аспекту, заболевание или состояние выбрано из группы, состоящей из: повышенных уровней общего холестерина, повышенных уровней липопротеинов низкой плотности (LDL-C), гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза, в частности, первичной гиперхолестеринемии, семейной гиперхолестеринемии или гиперхолестеринемии, которая не контролируется статинами.
В соответствии с другим предпочтительным вариантом осуществления изобретения, композицию, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W), каждую четвертую неделю (E4W) или один раз в месяц.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят совместно с фармацевтической композицией, антителом или его антигенсвязывающим фрагментом, при этом ингибитор HMG-CoA-редуктазы, предпочтительно, вводят в соответствии с одним из различных аспектов настоящего изобретения, например, в соответствии с первым или вторым аспектом.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят один раз в день, и предпочтительно, каждый день.
Во втором аспекте настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент пердназначен для введения в дозе в количестве от 5 мг до 500 мг,
где антитело или его антигенсвязывающий фрагмент дополнительно предназначен для введения в комбинации с ингибитором HMG-CoA-редуктазы в дозе в количестве от 0,05 мг до 100 мг.
В предпочтительных вариантах осуществления изобретения по седьмому и другим аспектам настоящего изобретения, заболевание или состояние, которые вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
В других предпочтительных вариантах осуществления настоящего изобретения по седьмому и другим аспектам, заболевание или состояние выбрано из группы, состоящей из: повышенных уровней общего холестерина, повышенных уровней липопротеинов низкой плотности (LDL-C), в частности, гиперхолестеринемии не контролируемой статинами, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, в частности, первичной гиперхолестеринемии, такой как первичная семейная гиперхолестеринемия или первичная несемейная гиперхолестеринемия.
В предпочтительных вариантах осуществления настоящего изобретения по седьмому и другим аспектам, антитело или его антигенсвязывающий фрагмент предназначен для введения индивиду, которому назначен LDL аферез, индивиду с мутациями, активирующими PCSK9, индивиду с гетерозиготной семейной гиперхолестеринемией, индивиду с первичной гиперхолестеринемией, индивиду с первичной гиперхолестеринемией, которая не контролируется статинами, индивиду с риском развития гиперхолестеринемии, индивиду с гиперхолестеринемией, индивиду с гиперлипидемией, индивиду с дислипидемией, индивиду с атеросклерозом или индивиду с сердечно-сосудистыми заболеваниями. Наиболее предпочтительно, когда индивидом является человек.
В некоторых вариантах осуществления настоящего изобретения по седьмому и другим аспектам, антитело или его антигенсвязывающий фрагмент предназначен для введения индивиду в комбинации с ингибитором HMG-CoA-редуктазы, который вводят три раза в день, два раза в день или один раз в день. В некоторых вариантах осуществления изобретения по второму и другим аспектам, ингибитор HMG-CoA-редуктазы вводится каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день или каждый шестой день. В некоторых вариантах осуществления изобретения по второму и другим аспектам, ингибитор HMG-CoA-редуктазы вводится каждую неделю, один раз в две недели, каждую третью неделю или один раз в четыре недели. В некоторых вариантах осуществления изобретения по второму и другим аспектам, ингибитор HMG-CoA-редуктазы вводится утром, в полдень или вечером. В предпочтительных вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводится один раз в день, предпочтительно, перорально и, предпочтительно, вечером.
В предпочтительных вариантах осуществления изобретения по седьмому и другим аспектам, ингибитор HMG-CoA-редуктазы представляет собой статин. Более предпочтительно, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В более предпочтительных вариантах осуществления изобретения по седьмому и другим аспектам настоящего изобретения, статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе, 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В других предпочтительных вариантах осуществления изобретения по седьмому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду каждую неделю, каждые четыре недели или один раз в месяц. Введение каждую четвертую неделю или введение один раз в месяц является предпочтительным с точки зрения пациента. Введение раз в две недели предпочтительнее при очень низких изменениях уровня холестерина в крови. Другие подходящие временные схемы введения антитела или его антигенсвязывающего фрагмента включают, но без ограничения, введение один раз в день, через день, каждый третий день, каждый четвертый день, каждый пятый день, каждый шестой день, каждую неделю, каждую третью неделю, каждую пятую неделю, каждую шестую неделю, каждую восьмую неделю, каждую десятую неделю и каждую двенадцатую неделю.
В другом предпочтительном варианте осуществления изобретения по седьмому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве от приблизительно 40 мг до приблизительно 500 мг, или от приблизительно 50 мг до приблизительно 500 мг, или от приблизительно 50 мг до приблизительно 400 мг, или от приблизительно от 50 мг до приблизительно 300 мг, или от приблизительно 100 мг до приблизительно 300 мг, или от приблизительно 100 мг до приблизительно 200 мг. В более предпочтительных вариантах осуществления изобретения антитело или его антигенсвязывающий фрагмент предназначен для введения в дозе в количестве приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 или приблизительно 400 мг.
В соответствии с другим предпочтительным вариантом осуществления седьмого аспекта изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W), каждую четвертую неделю (E4W) или один раз в месяц.
В предпочтительных вариантах осуществления изобретения по седьмому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 200 мг каждые две недели (т.е. режим дозирования E2W), предпочтительно, приблизительно 50 мг в режиме E2W, приблизительно 100 мг в режиме E2W, приблизительно 150 мг в режиме E2W, приблизительно 200 мг в режиме E2W, приблизительно 250 мг в режиме E2W или приблизительно 300 мг в режиме E2W, и более предпочтительно, приблизительно 50 мг в режиме E2W, приблизительно 100 мг в режиме E2W, приблизительно 150 мг в режиме E2W, приблизительно 200 мг в режиме E2W. В соответствии с особенно предпочтительным вариантом осуществления изобретения по второму и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент по изобретению вводят в режиме E2W в дозе от приблизительно 50 мг до приблизительно 200 мг, от приблизительно 100 мг до приблизительно 180 мг, от приблизительно 130 мг до приблизительно 170 мг, от приблизительно 140 мг до приблизительно 160 мг или в дозе, равной приблизительно 50 мг, приблизительно 100 мг, приблизительно 110 мг, приблизительно 120 мг, приблизительно 130 мг, приблизительно 140 мг, приблизительно 145 мг, приблизительно 150 мг, приблизительно 155 мг, приблизительно 160 мг, приблизительно 170 мг, приблизительно 180 мг, приблизительно 190 мг или приблизительно 200 мг в режиме E2W, причем доза, равная от приблизительно 145 мг до приблизительно 155 мг в режиме E2W, и доза, равная приблизительно 150 мг в режиме E2W, являюеся особенно предпочтительным вариантом осуществления изобретения.
В других предпочтительных вариантах осуществления по седьмому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 100 мг до приблизительно 400 мг каждую четвертую неделю (режим E4W), предпочтительно, приблизительно 100 мг в режиме E4W, приблизительно 150 мг в режиме E4W, приблизительно 200 мг в режиме E4W, приблизительно 250 мг в режиме E4W, приблизительно 300 мг в режиме E4W, приблизительно 350 мг в режиме E4W или приблизительно 400 мг в режиме E4W, при этом дозы от приблизительно 190 мг до приблизительно 310 мг в режиме E4W, от приблизительно 200 мг до приблизительно 300 мг в режиме E4W, от приблизительно 190 мг до приблизительно 210 мг в режиме E4W, от приблизительно 195 мг до приблизительно 205 в режиме E4W, от приблизительно 290 мг до приблизительно 310 мг в режиме E4W, от приблизительно 295 мг до приблизительно 305 мг в режиме E4W, приблизительно 200 мг в режиме E4W и приблизительно 300 мг в режиме E4W являются наиболее предпочтительными вариантами осуществления изобретения. Эти дозы, указанные для введения в режиме E4W, также являются подходящими для введения в режиме один раз в месяц.
Седьмой аспект осуществления изобретения также относится к антителу или его антигенсвязывающему фрагменту, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где антитело или его антигенсвязывающий фрагмент вводят в дозе, приблизительно равной от 50 мг до 500 мг.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления шестнадцатого аспекта настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения". Предпочтительные варианты осуществления настоящего изобретения по седьмому аспекту описаны в четвертом аспекте осуществления изобретения.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения по седьмому аспекту, антитело или его антигенсвязывающий фрагмент вводят в дозе, равной приблизительно 50 мг, 100 мг, 150 мг, 200 мг, 250 мг, 300 мг, 350 мг, 400 мг, 450 мг или 500 мг, и предпочтительно, в дозе, равной приблизительно 150 мг, 200 мг или 300 мг.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения по седьмому аспекту, заболевание или состояние выбрано из группы, состоящей из: повышенных уровней общего холестерина, повышенных уровней липопротеинов низкой плотности (LDL-C), гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза, в частности, первичной гиперхолестеринемии, семейной гиперхолестеринемии или гиперхолестеринемии, которая не контролируется статинами.
В соответствии с другим предпочтительным вариантом осуществления настоящего изобретения по седьмому аспекту, антитело или его антигенсвязывающий фрагмент имеет одну или несколько из следующих характеристик:
(i) предназначен для снижения уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 25%, и более предпочтительно, по меньшей мере 30%, по сравнению с уровнем до введения дозы, в частности, при предпочтительном введении антитела или его антигенсвязывающего фрагмента в дозе от приблизительно 40 мг до приблизительно 60 мг, от приблизительно 45 мг до приблизительно 55 мг или приблизительно 50 мг, при режиме введения E2W;
(ii) предназначен для снижения уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 65%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, при предпочтительном введении антитела или его антигенсвязывающего фрагмента в дозе приблизительно равной 100 мг в режиме E2W;
(iii) предназначен для снижения уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 60% до по меньшей мере приблизительно 75% (например, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70% или по меньшей мере приблизительно 75%), по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 55%, и более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы, при предпочтительном введении антитела или его фрагмента в дозе приблизительно равной 150 мг в режиме E2W;
(iv) предназначен для снижения уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 40% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 35%, и более предпочтительно, по меньшей мере 40%, по сравнению с уровнем до введения дозы, при предпочтительном введении антитела или его антигенсвязывающего фрагмента в дозе приблизительно равной 200 мг в режиме E4W;
(v) предназначен для снижения уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, при предпочтительном введении антитела или его антигенсвязывающего фрагмента в дозе приблизительно равной 300 мг в режиме E4W;
(vi) предназначен для увеличения уровней сывороточного HDL холестерина по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5%, по сравнению с уровнем до введения дозы;
(vii) предназначен для снижения уровня общего холестерина в сыворотке по меньшей мере от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 24 дней после введения;
(viii) предназначен для снижения уровня общего холестерина в сыворотке по меньшей мере от приблизительно 65% до приблизительно 80%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 24 дней после введения;
12. предназначен для снижения уровня триглицеридов в сыворотке по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы;
13. наличие небольшого или нерегистрируемого эффекта на функцию печени, по измерению ALT и AST, или на уровни тропонина;
14. увеличение одного или нескольких из следующего: уровней общего холестерина, уровней ApoB, уровней холестерина не относящегося к HDL-С, соотношения ApoB/ApoA-1.
В соответствии с другим предпочтительным вариантом осуществления изобретения по седьмому аспекту, антитело или его антигенсвязывающий фрагмент используется вместе с ингибитором HMG-CoA-редуктазы, где ингибитор HMG-CoA-редуктазы, предпочтительно, вводят в дозе от приблизительно 0,05 мг до приблизительно 100 мг, и ингибитор HMG-CoA-редуктазы, предпочтительно, представляет собой статин, где статин, предпочтительно, выбирают из группы, состоящей из: церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения по седьмому аспекту, статин вводят в соответствии с одним или несколькими из следующих режимов дозировки или введения:
(i) статин вводят один раз в день;
(ii) статин вводят в дозе от приблизительно 0,5 до приблизительно 100 мг, от приблизительно 5 мг до приблизительно 90 мг, приблизительно 10 мг, 20 мг, 40 мг или 80 мг, и статин, предпочтительно, является аторвастатином.
Другие режимы дозировки и введения антитела, его антигенсвязывающего фрагмента или ингибитора HMG-CoA-редуктазы описаны в других аспектах настоящего изобретения, и, предпочтительно, в одиннадцатом аспекте.
В другом предпочтительном варианте осуществления изобретения по седьмому аспекту, настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент вводят индивиду, нуждающемуся в этом, где индивид входит в одну или несколько групп из следующих индивидов: (i) индивиды, имеющие уровень LDL холестерина (LDL-C) в сыворотке по меньшей мере 100 мг/дл, предпочтительно, по меньшей мере 130 мг/дл, более предпочтительно, по меньшей мере 160 мг/дл, и еще более предпочтительно, по меньшей мере 200 мг/дл; (ii) индивиды, имеющие уровень HDL-C в сыворотке менее 40 мг/дл; (iii) индивиды, имеющие уровень холестерина в сыворотке по меньшей мере 200 мг/дл, предпочтительно, по меньшей мере 240 мг/дл; (iv) индивиды, имеющие уровень триглицеридов сыворотки по меньшей мере 150 мг/дл, например, по меньшей мере 200 мг/дл или менее 500 мг/дл, где указанный уровень триглицеридов определяется после голодания в течение по меньшей мере 8 часов; (v) индивиды в возрасте по меньшей мере 35 лет, например, по меньшей мере 40 лет, по меньшей мере 45 лет, по меньшей мере 50 лет, по меньшей мере 55 лет, по меньшей мере 60 лет, по меньшей мере 65 лет или по меньшей мере 75 лет; (vi) индивиды в возрасте до 75 лет, например, моложе 70 лет, моложе 65 лет, моложе 60 лет, моложе 55 лет, моложе 50 лет, моложе 45 лет или моложе 40 лет; (vii) индивиды, имеющие индекс массы тела (BMI) 25 или более (например, 26 или более, 27 или более, 28 или несколько, 29 или более, 30 или более, 31 или более, 32 или несколько, 33 или более, 34 или более, 35 или более, 36 или более, 37 или более, 38 или более, или 39 или более); (viii) индивиды мужского пола; (ix) индивиды женского пола; (х) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 30 мг/дл, предпочтительно, по меньшей мере 40 мг/дл, более предпочтительно, по меньшей мере 50 мг/дл, более предпочтительно, по меньшей мере 60 мг/дл, более предпочтительно, по меньшей мере 70 мг/дл, по сравнению с уровнем до введения дозы; или (xi) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 20%, предпочтительно, по меньшей мере 30%, более предпочтительно, по меньшей мере 40%, более предпочтительно, по меньшей мере 50%, более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы.
В другом предпочтительном варианте осуществления изобретения по седьмому аспекту, настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент вводят индивиду, который не входит в одну или несколько из следующих групп индивидов: (i) курильщики; (ii) лица в возрасте 70 лет и старше; (iii) лица, страдающие от гипертензии; (iv) беременные женщины; (v) женщины, пытающиеся забеременеть; (vi) женщины, которые кормят грудью; (vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень; (viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени; (ix) лица, которые употребляют чрезмерное количество алкоголя; (х) лица, имеющие проблемы с почками; (xi) лица, страдающие гипотиреозом; (xii) лица, страдающие мышечными расстройствами; (xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами; (xiv) лица, имеющие серьезные проблемы с дыханием; (xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой; (xvi) индивиды, выпивающие более 0,1 л сока грейпфрута в день или съедающие более половины грейпфрута в сутки; (xvii) лица, имеющие индекс массы тела (BMI) более 40; (xviii) лица, имеющие индекс массы тела (BMI) менее 18; (xix) индивиды, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2; и (xx) лица, имеющие положительную реакцию на гепатит В или С; (xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами; (xxii) лица, имеющие концентрацию нейтрофилов менее 1500/мм3; (xxiii) лица, имеющие концентрацию тромбоцитов менее 100000/мм3; (xxiv) мужчины, имеющие уровень креатинина в сыворотке более 1,5×ULN (верхняя граница нормы); (xxv) женщины, имеющие уровень креатинина в сыворотке более 1,4×ULN (верхняя граница нормы); (xxvi) индивиды, имеющие уровень аланинаминотрансферазы (ALT) или уровень аспартаттрансаминазы (AST) более чем 2×ULN, и (xxvii) лица, имеющие уровень СРК более 3×ULN.
В предпочтительном варианте осуществления изобретения по седьмому аспекту, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
В предпочтительном варианте осуществления изобретения по седьмому аспекту, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбрано из группы, состоящей из: повышенных уровней LDL-C, гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других заболеваний и состояний, описанных в первом или втором аспекте.
В предпочтительном варианте осуществления изобретения по седьмому аспекту, антитело или его антигенсвязывающий фрагмент вводят индивиду, которому назначен LDL аферез, индивиду с мутациями, активирующими PCSK9, индивиду с гетерозиготной семейной гиперхолестеринемией, индивиду с первичной гиперхолестеринемией, индивиду с первичной гиперхолестеринемией, которая неконтролируется статинами, индивиду с риском развития гиперхолестеринемии, индивиду с гиперхолестеринемией, индивиду с гиперлипидемией, индивиду с дислипидемией, индивиду с атеросклерозом, индивиду с сердечно-сосудистыми заболеваниями или индивиду с любыми другими заболеваниями и состояниями, описанными в первом или втором аспекте изобретения. Наиболее предпочтительно, когда индивидом является человек.
В предпочтительном варианте осуществления изобретения по седьмому аспекту, антитело или его антигенсвязывающий фрагмент вводят в комбинации с ингибитором HMG-CoA-редуктазы в дозе от 0,05 мг до 100 мг. В некоторых вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводят три раза в день, два раза в день или один раз в день. В некоторых вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводят каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день или каждый шестой день. В некоторых вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводят каждую неделю, один раз в две недели, каждую третью неделю или один раз в четыре недели. В некоторых вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводят утром, в полдень или вечером. В предпочтительных вариантах осуществления изобретения ингибитор HMG-CoA-редуктазы вводят один раз в день, предпочтительно, перорально, предпочтительно, вечером. Предпочтительным ингибитором HMG-CoA-редуктазы является статин. Более предпочтительно, когда статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина. В еще одном предпочтительном варианте осуществления изобретения по аспектам с шестнадцатого по восемнадцатый, антитело или его антигенсвязывающий фрагмент вводят в комбинации со статином, где статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В восьмом аспекте настоящее изобретение относится к способу получения фармацевтической композиции по изобретению, например, фармацевтической композиции по первому аспекту, где способ включает смешивание антитела или его антигенсвязывающего фрагмента и, необязательно, ингибитора HMG-CoA-редуктазы, с одним или несколькими фармацевтическими эксципиентами или носителями.
Специалистам в данной области известны способы получения композиций по изобретению. Кроме того, соответствующая ссылка приведена по тексту описания.
В девятом аспекте настоящее изобретение относится к способу получения лекарственной формы по изобретению (например, по пятому аспекту), где способ включает отмеривание необходимого количества фармацевтической композиции, антитела или его антигенсвязывающего фрагмента, жидкого состава или сухого состава по изобретению, содержащего одну или несколько доз антитела или его антигенсвязывающего фрагмента, и, необязательно, ингибитора HMG-CoA-редуктазы, и получение физически дискретных единиц, подходящих в качестве единичных доз для введения человеку и/или животному.
В десятом аспекте настоящее изобретение относится к способу получения или сборки изделия по изобретению, где способ включает упаковку фармацевтической композиции, антитела по настоящему изобретению, жидкого состава или сухого состава по изобретению в контейнер, необязательно вместе с одним или несколькими из следующих компонентов: этикетка, инструкции по применению, устройство для применения (например, шприц).
В одиннадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В контексте настоящего описания, термин "заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9" понимается как включающий любое заболевание или состояние, при котором применение PCSK-9 антитела вызывает положительный эффект.
В предпочтительных вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
В других предпочтительных вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, заболевание или состояние выбрано из группы, состоящей из: повышенных уровней общего холестерина, повышенных уровней липопротеинов низкой плотности (LDL-C), гиперхолестеринемии, в частности, гиперхолестеринемии, которая не контролируется статинами, гиперлипидемии, дислипидемии, атеросклероза, сердечно-сосудистых заболеваний, первичной гиперхолестеринемии, такой как первичная семейная гиперхолестеринемия или первичная несемейная гиперхолестеринемия, гиперхолестеринемии (особенно первичная гиперхолестеринемия), которая не контролируется статинами (в частности, не контролируемая аторвастатином).
В предпочтительных вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, индивид, нуждающийся в лечении, является индивидом, которому назначен LDL аферез, индивидом с мутациями, активирующими PCSK9, индивидом с гетерозиготной семейной гиперхолестеринемией, индивидом с первичной гиперхолестеринемией, индивидом с первичной гиперхолестеринемией, которая не контролируется статинами, индивидом с риском развития гиперхолестеринемии, индивидом с гиперхолестеринемией, индивидом с гиперлипидемией, индивидом с дислипидемией, индивидом с атеросклерозом или индивидом с сердечно-сосудистыми заболеваниями. Наиболее предпочтительно, когда индивидом является человек.
В некоторых вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, ингибитор HMG-CoA-редуктазы вводят три раза в день, два раза в день или один раз в день. В некоторых вариантах осуществления изобретения по первому и другим аспектам настоящего изобретения, ингибитор HMG-CoA-редуктазы вводят каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день, или каждый шестой день. В некоторых вариантах осуществления изобретения по первому и другим аспектам настоящего изобретения, ингибитор HMG-CoA-редуктазы вводят один раз в неделю, один раз в две недели, каждую третью неделю или один раз в четыре недели. В некоторых вариантах осуществления изобретения по первому и другим аспектам настоящего изобретения, ингибитор HMG-CoA-редуктазы вводят утром, в полдень или вечером. В предпочтительных вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят один раз в день, предпочтительно, перорально, предпочтительно, вечером.
Предпочтительно, когда ингибитором HMG-CoA-редуктазы является статин. Более предпочтительно, когда статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В более предпочтительных вариантах осуществления изобретения по первому и другим аспектам настоящего изобретения статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В предпочтительных вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели, каждую четвертую неделю или один раз в месяц. Введение каждую четвертую неделю или введение один раз в месяц (то есть один раз в календарный месяц, например, каждый первый, второй и т.п. день месяца или один раз в первый, второй, третий понедельник, вторник и т.п. каждого месяца, в отличие от введения каждую четвертую неделю) является предпочтительным с точки зрения пациента. Введение каждые две недели, предпочтительно, из-за очень низкого изменения уровня холестерина в крови. Другие подходящие временные схемы введения антитела или антигенсвязывающего фрагмента, включают, без ограничения, введение один раз в день, через день, каждый третий день, каждый четвертый день, каждый пятый день, каждый шестой день, каждую неделю, каждую третью неделю, каждую пятую неделю, каждую шестую неделю, каждую восьмую неделю, каждую десятую неделю и каждую двенадцатую неделю.
В предпочтительных вариантах осуществления изобретения по одиннадцатому и другим аспектам настоящего изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве, например, от приблизительно 40 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до 300 мг или от приблизительно 100 мг до 200 мг. В более предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг. Дозы, составляющие от приблизительно 50 мг до приблизительно 200 мг, например, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг, особенно подходят для режима дозирования каждые две недели (т.е. применение один раз в две недели), дозы, составляющие от приблизительно 150 мг до приблизительно 400 мг, например, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг или приблизительно 400 мг, особенно подходят для режимов введения с более длительными интервалами, например, для введения каждую третью или каждую четвертую неделю или один раз в месяц.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления первого и других аспектов настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения" или в четвертом аспекте и его вариантах осуществления.
В двенадцатом аспекте настоящее изобретение направлено на способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других состояний или заболеваний, в соответствии с первым или вторым аспектом настоящего изобретения, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровни LDL холестерина (LDL-C) более 100 мг/дл; и
определение эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C, по меньшей мере, на 25% по отношению к уровню перед введением дозы, по меньшей мере, у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
В тринадцатом аспекте настоящее изобретение направлено на способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний или любых других состояний или заболеваний, в соответствии с первым или вторым аспектом настоящего изобретения, где указанный способ включает:
определение эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, при определении уровней LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, где снижение уровня LDL-C, по меньшей мере на 25% по сравнению с уровнем до введения дозы, по меньшей мере у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
В предпочтительных вариантах осуществления изобретения по двенадцатому и тринадцатому аспектам, каждый пациент в указанной популяции ранее получал гиполипидемическое лечение путем введения HMG-CoA-ингибитора, такого как статин, в течение по меньшей мере 6 недель до применения указанного антитела или его антигенсвязывающего фрагмента.
В предпочтительных вариантах осуществления изобретения по двенадцатому и тринадцатому аспектам, антитело или его антигенсвязывающий фрагмент представляют собой антитело или его антигенсвязывающий фрагмент, описанный ниже в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В предпочтительных вариантах осуществления изобретения по двенадцатому и тринадцатому аспектам, выбранная популяция пациентов подвергается лечению в соответствии со способом лечения по первому аспекту и вариантам осуществления изобретения по первому или второму аспекту, как описано в настоящем документе.
В четырнадцатом аспекте настоящее изобретение относится к упаковке, содержащей антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, по изобретению и этикетку.
Согласно одному варианту осуществления изобретения, этикетка представляет собой носитель данных, содержащий одно или несколько из следующего: напечатанные указания, чип или штрих-код.
В соответствии с предпочтительным вариантом осуществления изобретения по четырнадцатому аспекту, этикетка содержит информацию или является носителем информации (например, напечатанные указания, чип или штрих-код), которая сообщает пациенту, что лечение антителом вместе с ингибитором HMG-CoA-редуктазы, таким как статин, показано при одном или нескольких состояниях, выбранных из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других состояний или заболеваний, в соответствии с первым или вторым аспектом настоящего изобретения. Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления восьмого аспекта настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В соответствии с другим предпочтительным вариантом осуществления изобретения, указанная этикетка содержит информацию или является носителем информации (например, напечатанные указания, чип или штрих-код), которая сообщает пациенту, что лечение антителом вместе со статином противопоказано для пациентов, принадлежащим к одной или нескольким из следующих групп пациентов: (i) курильщики; (ii) лица в возрасте 70 лет и старше; (iii) индивиды, страдающие от гипертензии; (iv) беременные женщины; (v) женщины, пытающиеся забеременеть; (vi) женщины, которые кормят грудью; (vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень; (viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени; (ix) лица, которые употребляют чрезмерное количество алкоголя; (х) лица, имеющие проблемы с почками; (xi) лица, страдающие гипотиреозом; (xii) лица, страдающие мышечными расстройствами; (xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами; (xiv) лица, имеющие серьезные проблемы с дыханием; (xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой; (xvi) лица, выпивающие более 0,1 л сока грейпфрута в день или съедающие более половины грейпфрута в сутки; (xvii) лица, имеющие индекс массы тела (BMI) более 40; (xviii) лица, имеющие индекс массы тела (BMI) менее 18; (xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2; (xx) лица, имеющие положительную реакцию на гепатит В или С; (xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами; (xxii) лица, имеющие концентрацию нейтрофилов менее 1500/мм3; (xxiii) лица, имеющие концентрацию тромбоцитов менее 100000/мм3; (xxiv) мужчины, имеющие уровень креатинина в сыворотке более 1,5×ULN (верхняя граница нормы); (xxv) женщины, имеющие уровень креатинина в сыворотке более 1,4×ULN (верхняя граница нормы); (xxvi) лица, имеющие уровень аланинаминотрансферазы (ALT) или уровень аспартаттрансаминазы (AST) более чем 2×ULN, и (xxvii) лица, имеющие уровень СРК более 3×ULN.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления четырнадцатого аспекта настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В пятнадцатом аспекте настоящее изобретение относится к способу регулирования уровня LDL в крови, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В шестнадцатом аспекте настоящее изобретение относится к способу предотвращения эффектов (постоянных) увеличенного уровня LDL в крови, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
В предпочтительных вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектам, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9. В других предпочтительных вариантах осуществления изобретения по десятому и одиннадцатому аспектам, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбрано из группы, состоящей из: повышенных уровней LDL-C, гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других состояний или заболеваний в соответствии с одиннадцатым, восемнадцатым или девятнадцатым аспектом настоящего изобретения.
В предпочтительных вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектам, индивидом является индивид, которому показан LDL аферез, индивид с мутациями, активирующими PCSK9, индивид с гетерозиготной семейной гиперхолестеринемией, индивид с первичной гиперхолестеринемией, которая не контролируется статинами, индивид с риском развития гиперхолестеринемии, индивид с гиперхолестеринемией, индивид с гиперлипидемией, индивид с дислипидемией, индивид с атеросклерозом или индивид с сердечно-сосудистыми заболеваниями, или любой индивид, как описано в одиннадцатом, восемнадцатом или девятнадцатом аспекте настоящего изобретения. Наиболее предпочтительно, когда индивидом является человек.
В некоторых вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектам, ингибитор HMG-CoA-редуктазы вводят три раза в день, два раза в день или один раз в день. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день, или каждый шестой день. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят один раз в неделю, один раз в две недели, каждую третью неделю, каждую четвертую неделю или один раз в месяц. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят утром, в полдень или вечером. В предпочтительных вариантах HMG-CoA-редуктазы вводят один раз в день, предпочтительно, перорально, предпочтительно, вечером. Другие подходящие режимы введения описаны в первом или втором аспекте осуществления изобретения.
В других предпочтительных вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектам, ингибитором HMG-CoA-редуктазы является статин. Более предпочтительно, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В наиболее предпочтительных вариантах осуществления изобретения по десятому и одиннадцатому аспектам, статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В дополнительных предпочтительных вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектах, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели, каждую четвертую неделю или один раз в месяц. Введение каждую четвертую неделю или введение один раз в месяц является предпочтительным с точки зрения пациента. Введение один раз в две недели предпочтительнее при очень низких изменениях уровня холестерина в крови. Другие подходящие временные схемы введения антитела или его антигенсвязывающего фрагмента включают, но без ограничения, введение один раз в день, через день, каждый третий день, каждый четвертый день, каждый пятый день, каждый шестой день, каждую неделю, каждую третью неделю, каждую пятую неделю, каждую шестую неделю, каждую восьмую неделю, каждую десятую неделю и каждую двенадцатую неделю.
В предпочтительных вариантах осуществления изобретения по пятнадцатому и шестнадцатому аспектам, антитело или его антигенсвязывающий фрагмент вводят в дозе от 50 мг до 300 мг, например, от 100 мг до 200 мг. В более предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе, равной приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг или приблизительно 300 мг. Другие подходящие и предпочтительные режимы дозирования раскрыты в настоящем описании, например, в одиннадцатом аспекте осуществления изобретения.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления изобретения по десятому и одиннадцатому аспектам настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В семнадцатом аспекте настоящее изобретение относится к способу определения того, что используемое фармацевтическое соединение облегчает, улучшает, ингибирует или предотвращает заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает: (а) введение индивиду соединения, которое специфически связывается с PCSK9, предпочтительно, антитела или его антигенсвязывающего фрагмента, специфически связывающегося с PCSK9, и (b) определение, какая часть PCSK9 в крови связана с соединением, указанным в (а).
Как правило, соединения, которые специфически связывают от 10% до 100% (предпочтительно, 20%-100%, более предпочтительно, 30%-100%, более предпочтительно, 40%-100%, более предпочтительно, 50%-100%) PCSK9, присутствующего в крови, при использовании в стехиометрических количествах, будут использоваться для облегчения, улучшения, ингибирования или предотвращения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9.
Предпочтительно, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбрано из группы, состоящей из повышенных уровней LDL-C, гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других заболеваний, описанных в настоящем документе, например, в одиннадцатом аспекте осуществления изобретения.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления настоящего изобретения по двенадцатому аспекту, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В восемнадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом,
где индивид, нуждающийся в этом, входит в одну или несколько из следующих групп индивидов: (i) индивиды, имеющие уровень LDL холестерина (LDL-C) в сыворотке по меньшей мере 100 мг/дл, предпочтительно, по меньшей мере 130 мг/дл, более предпочтительно, по меньшей мере 160 мг/дл, еще более предпочтительно, по меньшей мере 200 мг/дл; (ii) индивиды, имеющие уровень HDL-C в сыворотке менее 40 мг/дл; (iii) индивиды, имеющие уровень холестерина в сыворотке по меньшей мере 200 мг/дл; (iv) индивиды, имеющие уровень триглицеридов сыворотки по меньшей мере 150 мг/дл, например, по меньшей мере 200 мг/дл или менее 500 мг/дл, где указанный уровень триглицеридов определяется после голодания в течение по меньшей мере 8 часов; (v) индивиды в возрасте по меньшей мере 35 лет, например, по меньшей мере 40 лет, по меньшей мере 45 лет, по меньшей мере 50 лет, по меньшей мере 55 лет, по меньшей мере 60 лет, по меньшей мере 65 лет или по меньшей мере 75 лет; (vi) индивиды в возрасте до 75 лет, например, моложе 70 лет, моложе 65 лет, моложе 60 лет, моложе 55 лет, моложе 50 лет, моложе 45 лет или моложе 40 лет; (vii) индивиды, имеющие индекс массы тела (BMI) 25 или более (например, 26 или более, 27 или более, 28 или несколько, 29 или более, 30 или более, 31 или более, 32 или несколько, 33 или более, 34 или более, 35 или более, 36 или более, 37 или более, 38 или более, или 39 или более); (viii) индивиды мужского пола; (ix) индивиды женского пола; (х) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 30 мг/дл, предпочтительно, по меньшей мере 40 мг/дл, более предпочтительно, по меньшей мере 50 мг/дл, более предпочтительно, по меньшей мере 60 мг/дл, более предпочтительно, по меньшей мере 70 мг/дл, по сравнению с уровнем до введения дозы; или (xi) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 20%, предпочтительно, по меньшей мере 30%, более предпочтительно, по меньшей мере 40%, более предпочтительно, по меньшей мере 50%, более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы.
В девятнадцатом аспекте настоящее изобретение относится к способу лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом,
при этом индивид, нуждающийся в этом, не входит в одну или несколько из следующих групп индивидов: (i) курильщики; (ii) лица в возрасте 70 лет и старше; (iii) лица, страдающие от гипертензии; (iv) беременные женщины; (v) женщины, пытающиеся забеременеть; (vi) женщины, которые кормят грудью; (vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень; (viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени; (ix) лица, которые употребляют чрезмерное количество алкоголя; (х) лица, имеющие проблемы с почками; (xi) лица, страдающие гипотиреозом; (xii) лица, страдающие мышечными расстройствами; (xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами; (xiv) лица, имеющие серьезные проблемы с дыханием; (xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой; (xvi) лица, выпивающие более 0,1 л сока грейпфрута в день или съедающие более половины грейпфрута в сутки; (xvii) лица, имеющие индекс массы тела (BMI) более 40; (xviii) лица, имеющие индекс массы тела (BMI) менее 18; (xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2; (xx) лица, имеющие положительную реакцию на гепатит В или С; (xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами; (xxii) лица, имеющие концентрацию нейтрофилов менее 1500/мм3; (xxiii) лица, имеющие концентрацию тромбоцитов менее 100000/мм3; (xxiv) мужчины, имеющие уровень креатинина в сыворотке более 1,5×ULN (верхняя граница нормы); (xxv) женщины, имеющие уровень креатинина в сыворотке более 1,4×ULN (верхняя граница нормы); (xxvi) индивиды, имеющие уровень аланинаминотрансферазы (ALT) или уровень аспартаттрансаминазы (AST) более чем 2×ULN, и (xxvii) индивиды, имеющие уровень СРК более 3×ULN.
В предпочтительных вариантах осуществления изобретения по восемнадцатому и девятнадцатому аспектам, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
В предпочтительных вариантах осуществления изобретения по тринадцатому и четырнадцатому аспектам, заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбрано из группы, состоящей из: повышенных уровней LDL-C, гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, или любых других заболеваний или состояний, описанных в других аспектах настоящего изобретения, например, в одиннадцатом аспекте.
В предпочтительных вариантах осуществления изобретения по тринадцатому и четырнадцатому аспектам, индивидом является индивидом, которому назначен LDL аферез, индивидом с мутациями, активирующими PCSK9, индивидом с гетерозиготной семейной гиперхолестеринемией, индивидом с первичной гиперхолестеринемией, например, индивидом с первичной семейной или первичной несемейной гиперхолестеринемией, индивидом с гиперхолестеринемией, такой как первичная гиперхолестеринемия, которая не контролируется статинами, индивидом с риском развития гиперхолестеринемии, индивидом с гиперхолестеринемией, индивидом с гиперлипидемией, индивидом с дислипидемией, индивидом с атеросклерозом или индивидом с сердечно-сосудистыми заболеваниями, или любым другим индивидом, как описано в первом или втором аспекте изобретения. Наиболее предпочтительно, когда индивидом, нуждающимся в этом является человек. Дополнительные предпочтительные или подходящие индивиды описаны в других аспектах настоящего изобретения, таких как в восемнадцатом или девятнадцатом аспекте.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления тринадцатого и четырнадцатого аспекта, а также других аспектов настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения".
В предпочтительных вариантах осуществления изобретения по восемнадцатому и девятнадцатому аспектам, способ дополнительно включает введение терапевтического количества ингибитора HMG-CoA-редуктазы индивиду в дозе от 0,05 мг до 100 мг. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят три раза в день, два раза в день или один раз в день. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день, или каждый шестой день. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят один раз в неделю, один раз в две недели, каждую третью неделю или один раз в четыре недели. В некоторых вариантах осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят утром, в полдень или вечером. В предпочтительных вариантах HMG-CoA-редуктазы вводят один раз в день, предпочтительно, перорально, предпочтительно, вечером. Предпочтительно, ингибитором HMG-CoA-редуктазы является статин. Более предпочтительно, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина. В еще одном предпочтительном варианте осуществления изобретения по тринадцатому и четырнадцатому аспектам, способ включает введение терапевтического количества статина индивиду, где статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг, предпочтительно, в суточной дозе 0,2 мг, 0,4 мг или 0,8 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 10 мг, 20 мг, 40 мг или 80 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе 5 мг, 10 мг, 20 мг, 40 мг или 80 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг, предпочтительно, в суточной дозе, равной 1 мг, 2 мг, 5 мг, 10 мг или 20 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 5 мг, 10 мг, 20 мг или 40 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 20 мг, 40 мг или 80 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг, предпочтительно, в суточной дозе, равной 10 мг, 20 мг, 40 мг или 80 мг.
В дополнительном предпочтительном варианте осуществления, настоящее изобретения объединяет признаки восемнадцатого и девятнадцатого аспектов, как описано в настоящем документе.
В двадцатом аспекте настоящее изобретение относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл; и
определения эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C, по меньшей мере на 25%, по отношению к уровню до введения дозы, по меньшей мере у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
при этом каждый пациент входит в одну или несколько групп индивидов, как указано в тринадцатом аспекте изобретения.
В двадцать первом аспекте настоящее изобретения относится к способу испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из повышенных уровней LDL-C, гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний (или для любого другого способа, как описано в первом или втором аспекте), где указанный способ включает:
определение эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C, по меньшей мере на 25%, по отношению к уровню до введения дозы, по меньшей мере у 75% пациентов популяции показывает, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
где каждый пациент входит в одну или несколько групп индивидов, как указано в тринадцатом аспекте.
В предпочтительных вариантах осуществления изобретения по двадцатому и двадцать первому аспектам, каждый пациент в указанной популяции подвергался гиполипидемическому лечению путем введения ингибитора HMG-CoA-редуктазы, такой как статин, в течение по меньшей мере 6 недель до применения указанного антитела или его антигенсвязывающего фрагмента.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления изобретения по девятнадцатому и двадцатому аспектам настоящего изобретения, описаны в разделе "Предпочтительные антитела для осуществления настоящего изобретения" или в другой части настоящего описания, где раскрыты антитела по изобретению, например, такие, как описано в четвертом аспекте.
В предпочтительных вариантах осуществления изобретения по двадцатому и двадцать первому аспектам, популяция пациентов подвергается или была подвергнута лечению способом по одиннадцатому, восемнадцатому или девятнадцатому аспекту и вариантам их осуществления, как описано в настоящем документе.
В других предпочтительных вариантах осуществления изобретения по двадцатому и двадцать первому аспектам, указанное антитело или указанный его антигенсвязывающий фрагмент используется в подгруппах указанной выбранной популяции пациентов, где указанные подгруппы были сгруппированы на основе по меньшей мере одного фактора группировки, выбранного из группы, состоящей из: популяция с гетерозиготной семейной гиперхолестеринемией (heFH); наличие в анамнезе инфаркта миокарда (MI); наличие в анамнезе инсульта; получение высокоинтенсивной терапии статинами; и географического региона происхождения пациента (например, из Северной Америки, Западной Европы, Восточной Европы и остального мира).
Для хомяков и других грызунов статины не являются эффективными для клиренса LDL из крови. В частности, введение одних статинов (например, аторвастатина) хомякам или другим грызунам не оказывает никакого влияния на экспрессию рецептора LDL (LDLR), вероятно из-за активности эндогенных PCSK9. Эксперименты по ингибированию PCSK9 путем введения антител против PCSK9, представленные в настоящем описании (см. Пример 4) показывают, что грызуны (например, хомяки) становятся чувствительными к терапии статинами. Таким образом, настоящее изобретение предлагает новую животную модель для испытания эффективности статинов или других препаратов, которые снижают уровень холестерина.
Таким образом, в двадцать втором аспекте настоящее изобретение направлено на способ испытания эффективности соединения по снижению уровней холестерина у индивида, где способ включает следующие стадии:
(a) предоставление грызуна;
(b) введение грызуну антитела или его антигенсвязывающего фрагмента, который специфически связывает PCSK9;
(c) введение указанному грызуну испытуемого соединения;
(d) определение эффекта от испытуемого соединения у грызуна, где снижение уровня холестерина у грызуна, по сравнению с уровнем холестерина у контрольного животного, означает, что испытуемое соединение эффективно для снижения уровней холестерина у индивида, при этом контрольное животное принадлежит к тому же самому виду, как и указанный грызун, и контрольное животное не подвергалось воздействию испытуемого соединения.
В предпочтительных вариантах осуществления изобретения по двадцать второму аспекту, грызуна выбирают из группы, состоящей из хомяка, мыши, крысы, морской свинки и кролика.
Антитела и их антигенсвязывающие фрагменты, которые могут быть использованы для осуществления двадцать второго аспекта настоящего изобретения, также раскрыты в других разделах настоящего описания, например, в четвертом аспекте раздела "Предпочтительные антитела для осуществления настоящего изобретения". Предпочтительно, когда антитело или его антигенсвязывающий фрагмент вводят грызуну в концентрации 1 мг/кг массы тела, 3 мг/кг массы тела или 10 мг/кг массы тела.
В предпочтительных вариантах осуществления изобретения по двадцать второму аспекту, снижение уровня холестерина определяют путем измерения уровня общего холестерина в сыворотке крови. В более предпочтительных вариантах, снижение уровня холестерина определяют путем измерения уровня LDL холестерина (LDL-C) в сыворотке крови.
В предпочтительных вариантах осуществления изобретения по двадцать второму аспекту, контрольное животное принадлежит к той же самой линии, что и грызун. Предпочтительно, когда грызуну и контрольному животному вводят одно и то же антитело или его антигенсвязывающий фрагмент. Предпочтительно, когда антитело или его антигенсвязывающий фрагмент вводят грызуну и контрольному животному в одной и той же концентрации (измеряемой в мг/кг массы тела).
В одном из вариантов осуществления изобретения по двадцать второму аспекту, контрольное животное является другим животном, т.е. другим видом, чем грызуны. Также можно определять уровень холестерина в двух или нескольких контрольных животных, и вычислять среднее значение уровня холестерина в этих двух или нескольких контрольных животных. Кроме того, антитело или его антигенсвязывающий фрагмент можно вводить двум или нескольким грызунам для того, чтобы определить уровень холестерина в этих двух или нескольких грызунах, и вычислять среднее значения уровня холестерина в этих двух или нескольких грызунах.
В альтернативном варианте осуществления изобретения по двадцать второму аспекту, контрольное животное является тем же самым животным, что и грызун, но контрольное животное оценивается в другой момент времени. Более конкретно, уровень холестерина у грызуна после введения испытуемого соединения можно сравнивать с уровнем холестерина до введения дозы этому же самому животному. Предпочтительно, когда указанный уровень холестерина до введения дозы определяется между стадиями (b) и (c), указанными выше.
Настоящее изобретение, согласно двадцать третьему аспекту, относится к способу повышения активности статинов по снижению LDL-C у индивида, проходящему статиновую терапию, где способ включает введение индивиду антитела или его антигенсвязывающего фрагмента, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9), при этом антитело или его антигенсвязывающий фрагмент вводят в дозе количестве от приблизительно 5 мг до приблизительно 500 мг, повышая тем самым активность статинов по снижению LCL-C у индивида.
Согласно предпочтительному варианту осуществления изобретения по двадцать третьему аспекту, индивид до введения антитела является устойчивым к действию статинов.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние представляет собой первичную гиперхолестеринемию или семейную гиперхолестеринемию.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве приблизительно 150 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 65% до приблизительно 80%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лечение снижает уровни триглицеридов в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лечение снижает уровень HDL холестерина в сыворотке не более чем на 5%, по сравнению с уровнем до введения дозы.
Согласно еще одному предпочтительному варианту осуществления изобретения, лечение имеет незначительный или не регистрируемый эффект на функцию печени, по измерению ALT и AST.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, статин является аторвастатином, который вводят в дозе 10 мг, 20 мг, 40 мг или 80 мг.
В двадцать четвертом аспекте настоящее изобретение относится к набору для лечения повышенных уровней холестерина, который относится к липопротеином низкой плотности (LDL-C), у индивида, где набор содержит (а) фармацевтическую лекарственную форму, содержащую антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и фармацевтически приемлемый носитель, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 5 мг до приблизительно 500 мг, и (b) этикетку или вкладыш в упаковку с инструкцией по применению.
Согласно предпочтительному варианту осуществления изобретения по двадцать четвертому аспекту, этикетка содержит информацию для пациентов, получающим лечение указанным антителом или его антигенсвязывающим фрагментом, что лечение показано при заболевании или состоянии, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является первичной гиперхолестеринемией или семейной гиперхолестеринемией. В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 50 мг до приблизительно 300 мг. В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве приблизительно 150 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, этикетка или вкладыш в упаковке указывает, что антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, этикетка или вкладыш в упаковке указывает, что антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, набор дополнительно включает ингибитор HMG-CoA-редуктазы. В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор присутствует в дозе в количестве приблизительно от 0,05 мг до 100 мг. В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы является статином. В соответствии с другим предпочтительным вариантом осуществления изобретения, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, инструкции указывают, что статин является аторвастатином, который вводят в дозе 10 мг, 20 мг, 40 мг или 80 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, инструкции указывают, что лечение антителом или его антигенсвязывающим фрагментом противопоказано для пациентов, принадлежащих к одной или нескольким из следующих групп пациентов:
(i) курильщики;
(ii) лица в возрасте 70 лет и старше;
(iii) индивиды, страдающие от гипертензии;
(iv) беременные женщины;
(v) женщины, пытающиеся забеременеть;
(vi) женщины, которые кормят грудью;
(vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(ix) лица, которые употребляют чрезмерное количество алкоголя;
(х) лица, имеющие проблемы с почками;
(xi) лица, страдающие гипотиреозом;
(xii) лица, страдающие мышечными расстройствами;
(xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xiv) лица, имеющие серьезные проблемы с дыханием;
(xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики или противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xvi) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xvii) лица, имеющие индекс массы тела (BMI) более 40;
(xviii) лица, имеющие индекс массы тела (BMI) менее 18;
(xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xx) лица, имеющие положительную реакцию на гепатит В или С;
(xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
В двадцать пятом аспекте настоящее изобретение относится к способу лечения индивида, страдающего заболеванием или расстройством, которое характеризуется повышенными уровнями холестерина, относящегося к липопротеинам низкой плотности (LDL-C), где способ включает:
(а) выбор индивида с уровнем LDL-C в крови выше 100 мг/дл, и
(b) введение указанному индивиду композиции, содержащей антитело или антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающегося в этом.
В соответствии с предпочтительным вариантом осуществления изобретения, заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является первичной гиперхолестеринемией или семейной гиперхолестеринемией.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет индекс массы тела (BMI) менее 18 кг/м2 или более 40 кг/м2.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид ранее не получал указаний находиться на диете по снижению уровня холестерина.
Согласно другому предпочтительному варианту осуществления изобретения, индивид ранее не принимал лекарственных средств для снижения уровня холестерина, за исключением аторвастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, аторвастатин принимался индивидом в количестве приблизительно 10 мг в день.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственное средство для снижения уровня холестерина выбрано из группы, состоящей из фибратов, смол желчных кислот, ниацина, блокаторов кишечной абсорбции холестерина (ICA) и омега-3 жирных кислот. В соответствии с другим предпочтительным вариантом осуществления изобретения, ниацин принимается в дозе более 500 мг в день. В соответствии с другим предпочтительным вариантом осуществления изобретения омега-3 жирные кислоты принимаются в дозе более 1000 мг в день.
Согласно другому предпочтительному варианту осуществления изобретения, индивид не страдает от диабета. В соответствии с другим предпочтительным вариантом осуществления изобретения, диабет является диабетом типа 1. В соответствии с другим предпочтительным вариантом осуществления изобретения диабет является диабетом типа 2. В соответствии с другим предпочтительным вариантом осуществления изобретения, диабет типа 2 лечится инсулином.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель концентрации гликозилированного гемоглобина в крови, более или равный 8,5%.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид является отрицательным на поверхностный антиген гепатита В и гепатита С.
Согласно другому предпочтительному варианту осуществления изобретения, индивид имеет концентрацию триглицеридов в крови более чем 350 мг/дл.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию нейтрофилов менее 1500 на кубический мм крови.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию тромбоцитов менее 100000 на кубический мм крови.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивидом является женщина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивидом является не беременная женщина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию тиреотропного гормона в крови выше нижней границы нормы и ниже верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель креатина в сыворотке менее 1,4 от верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид является мужчиной.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель креатина в сыворотке менее 1,5 от верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель количества аспартаттрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель количества аланинтрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 5 мг до приблизительно 500 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело вводят в количестве от 200 мг до 300 мг каждые четыре недели.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе приблизительно 150 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело вводят подкожно.
В соответствии с другим предпочтительным вариантом осуществления изобретения антитело вводят в брюшную полость.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивиду вводят ингибитор HMG-CoA-редуктазы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы вводят в дозе приблизительно от 0,05 мг до 100 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитором HMG-CoA-редуктазы является статин.
В соответствии с другим предпочтительным вариантом осуществления изобретения, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, статин представляет собой аторвастатин, который вводят в дозе 10 мг или 80 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, аторвастатин вводят в количестве приблизительно 10 мг в день и 80 мг в день в течение 8 недель.
В двадцать шестом аспекте настоящее изобретение относится к способу снижения уровней холестерина у индивида, нуждающегося в этом, где способ включает:
(а) выбор индивида с уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), в крови более 100 мг/дл; и
(b) введение указанному индивиду композиции, содержащей антитело или антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающегося в этом.
Согласно предпочтительному варианту осуществления изобретения по двадцать шестому аспекту, заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является первичной гиперхолестеринемией или семейной гиперхолестеринемией.
В соответствии с другим предпочтительным вариантом осуществления изобретения, заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет индекс массы тела (BMI) менее 18 кг/м2 или более 40 кг/м2.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид ранее не получал указаний находиться на диете по снижению уровня холестерина.
Согласно другому предпочтительному варианту осуществления изобретения, индивид ранее не принимал лекарственных средств для снижения уровня холестерина, за исключением аторвастатина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, аторвастатин принимался индивидом в количестве приблизительно 10 мг в день.
В соответствии с другим предпочтительным вариантом осуществления изобретения, лекарственное средство для снижения уровня холестерина выбрано из группы, состоящей из фибратов, смол желчных кислот, ниацина, блокаторов кишечной абсорбции холестерина (ICA) и омега-3 жирных кислот.
В соответствии с другим предпочтительным вариантом осуществления изобретения, ниацин принимается в дозе более 500 мг в день.
В соответствии с другим предпочтительным вариантом осуществления изобретения, омега-3 жирные кислоты принимаются в дозе более 1000 мг в день.
Согласно другому предпочтительному варианту осуществления изобретения, индивид не страдает от диабета.
В соответствии с другим предпочтительным вариантом осуществления изобретения, диабет является диабетом типа 1.
В соответствии с другим предпочтительным вариантом осуществления изобретения, диабет является диабетом типа 2.
В соответствии с другим предпочтительным вариантом осуществления изобретения, диабет типа 2 лечится инсулином.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель концентрации гликозилированного гемоглобина в крови, более или равный 8,5%.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид является отрицательным на поверхностный антиген гепатита В и гепатита С.
Согласно другому предпочтительному варианту осуществления изобретения, индивид имеет концентрацию триглицеридов в крови более чем 350 мг/дл.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию нейтрофилов менее 1500 на кубический мм крови.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию тромбоцитов менее 100000 на кубический мм крови.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивидом является женщина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивидом является не беременная женщина.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет концентрацию тиреотропного гормона в крови выше нижней границы нормы и ниже верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель креатина в сыворотке менее 1,4 от верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид является мужчиной.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель креатина в сыворотке менее 1,5 от верхней границы нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель количества аспартаттрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, индивид имеет показатель количества аланинтрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 5 мг до приблизительно 500 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело вводят в количестве от 200 мг до 300 мг каждые четыре недели.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят в дозе приблизительно 150 мг.
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO:90/92. В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92. В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO:90/92. В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело вводят подкожно. В соответствии с другим предпочтительным вариантом осуществления изобретения, антитело вводят в брюшную полость.
В соответствии с другим предпочтительным вариантом осуществления изобретения, способ дополнительно включает введение индивиду ингибитора HMG-CoA-редуктазы. В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA редуктазы вводят в дозе от приблизительно 0,05 мг до 100 мг. В соответствии с другим предпочтительным вариантом осуществления изобретения, ингибитор HMG-CoA-редуктазы является статином. В соответствии с другим предпочтительным вариантом осуществления изобретения, статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина. В соответствии с другим предпочтительным вариантом осуществления изобретения, статин является аторвастатином, который вводят в дозе 10 мг, 20 мг, 40 мг или 80 мг. В соответствии с другим предпочтительным вариантом осуществления изобретения, аторвастатин вводят в количестве приблизительно 10 мг в день и 80 мг в день в течение 8 недель.
Некоторые аспекты изобретения могут быть объединены друг с другом. Например, способ лечения заболевания или состояния, в соответствии с одиннадцатым аспектом, и способ лечения заболевания или состояния, в соответствии с восемнадцатым аспектом, могут быть объединены. В результате этой комбинации, настоящее изобретение относится к способу лечения заболевания или состояния, которое имеет признаки, характерные для лечения некоторых групп индивидов при определенных режимах дозирования. Аналогичным образом, различные варианты осуществления изобретения по различным аспектам, описанным в настоящем документе, могут быть объединены друг с другом; например, антитело или его антигенсвязывающий фрагмент, используемый при лечении заболеваний или состояний при определенном режиме дозирования в соответствии с седьмым аспектом, может быть объединен с антителом или его антигенсвязывающим фрагментом, используемым при лечении заболеваний или состояний для некоторых групп пациентов в соответствии с седьмым аспектом. Как результат этой комбинации, настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту для использования при лечении некоторых групп индивидов при определенных режимах дозирования.
В соответствии с другим примером, способ лечения заболевания или состояния, в соответствии с одиннадцатым аспектом, и способ лечения заболевания или состояния, согласно девятнадцатому аспекту, могут быть объединены. В результате этой комбинации настоящее изобретение относится к способу лечения заболевания или состояния, который исключают некоторые группы индивидов из лечения при определенном режиме дозирования. Аналогичным образом, различные варианты осуществления изобретения по различным аспектам, описанным в настоящем документе, могут быть объединены друг с другом; например, антитело или его антигенсвязывающий фрагмент, используемый при лечении заболевания или состояния в соответствии с одним из вариантов осуществления изобретения по седьмому аспекту при определенном режиме дозирования, может быть объединен с антителом или его антигенсвязывающим фрагментом, используемым при лечении заболеваний или состояний согласно варианту осуществления изобретения по седьмому аспекту, связанного с исключением некоторых групп индивидов из лечения. Как результат этой комбинации, настоящее изобретение относится к антителу или его антигенсвязывающему фрагменту для использования при лечении с определенным режимом дозирования, где некоторые группы индивидов исключены из лечения.
Специалисту в данной области понятны другие предпочтительные варианты осуществления изобретения, которые следуют из подходящих комбинаций различных аспектов и вариантов осуществления настоящего изобретения.
Фармацевтические применения по настоящему изобретению, как описано в настоящем документе, также относятся к использованию данного антитела или его антигенсвязывающего фрагмента, данной фармацевтической композиции и т.п. для получения лекарственного средства для лечения одного или несколько заболеваний или состояний, как описано в настоящем документе.
ПРЕДПОЧТИТЕЛЬНЫЕ АНТИТЕЛА ДЛЯ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В следующем разделе описаны функциональные и структурные особенности антител и их антигенсвязывающих фрагментов, которые могут быть использованы для осуществления всех двадцати одного аспекта настоящего изобретения. Таким образом, выражения, такие как "в предпочтительных вариантах осуществления изобретения", "в некоторых вариантах осуществления изобретения", "в другом предпочтительном варианте осуществления изобретения" и аналогичные им выражения, следует понимать как относящиеся к вариантам осуществления изобретения по первому аспекту настоящего изобретения, по второму аспекту настоящего изобретения, по третьему аспекту настоящего изобретения, по четвертому аспекту настоящего изобретения, по пятому аспекту настоящего изобретения, по шестому аспекту настоящего изобретения, по седьмому аспекту настоящего изобретения, по восьмому аспекту настоящего изобретения, по девятому аспекту настоящего изобретения, по десятому аспекту настоящего изобретения, по одиннадцатому аспекту настоящего изобретения, по двенадцатому аспекту настоящего изобретения, по тринадцатому аспекту настоящего изобретения, по четырнадцатому аспекту настоящего изобретения, по пятнадцатому аспекту настоящего изобретения, по шестнадцатому аспекту настоящего изобретения, по семнадцатому аспекту настоящего изобретения, по восемнадцатому аспекту настоящего изобретения, по девятнадцатому аспекту настоящего изобретения, по двадцатому аспекту настоящего изобретения, по двадцать первому аспекту настоящего изобретения, по двадцать второму аспекту настоящего изобретения, по двадцать третьему аспекту настоящего изобретения, по двадцать четвертому аспекту настоящего изобретения, по двадцать пятому аспекту настоящего изобретения и двадцать шестому аспекту настоящего изобретения.
Все антитела или антигенсвязывающие фрагменты, подходящие для осуществления настоящего изобретения, специфически связывают hPCSK9. В предпочтительных вариантах осуществления любого аспекта настоящего изобретения, антитело или его антигенсвязывающий фрагмент является рекомбинантным человеческим антителом или его фрагментом. В более конкретных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент представляет собой полностью человеческое моноклональное антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9 и нейтрализует активность PCSK9.
Моноклональные антитела (mAb), используемые в настоящем изобретении, могут быть полноразмерными антителами (например, IgG1 или IgG4-антитело) или могут содержать только антиген-связывающую часть (например, Fab-, F(ab′)2- или scFv-фрагмент), и они могут быть модифицированы в части их функциональности, например, для устранения остаточных эффекторных функций (Reddy et al. (2000) J. Immunol. 164:1925-1933).
В предпочтительных вариантах осуществления изобретения, антитела, при введении индивиду, предпочтительно, человеку или млекопитающему, не относящемуся к человеку, а более предпочтительно, человеку, характеризуются одним или несколькими из следующих признаков:
- снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 25%, и более предпочтительно, по меньшей мере 30%, по сравнению с уровнем до введения дозы, в частности, при введении в дозе от приблизительно 40 мг до приблизительно 60 мг, предпочтительно, от приблизительно 45 мг до приблизительно 55 мг, и более предпочтительно, приблизительно 50 мг при режиме введения один раз в две недели (через одну неделю, E2W);
- снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 65%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 100 мг в режиме E2W;
- снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 60% до по меньшей мере приблизительно 75% (например, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70% или по меньшей мере приблизительно 75%), по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения, где устойчивое снижение, предпочтительно, составляет по меньшей мере 55%, и более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
- снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 40% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 35%, и более предпочтительно, по меньшей мере 40%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 200 мг в режиме E4W;
- снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 300 мг в режиме E4W;
- увеличение уровней сывороточного HDL холестерина по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5%, по сравнению с уровнем до введения дозы индивиду, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
- наличие небольшого или нерегистрируемого эффекта на уровни тропонина;
- увеличение одного или нескольких из следующего: уровней общего холестерина, уровней ApoB, уровней холестерина, не относящегося к HDL-С, соотношения ApoB/ApoA-1.
Антитела по изобретению обладают указанными выше свойствами, предпочтительно, когда их вводят в комбинации с ингибитором HMG-CoA-редуктазы. Предпочтительные варианты ингибиторов HMG-CoA-редуктазы, которые используются в сочетании с антителом по изобретению, дозировки и режимы их введения можно найти в описании, в частности, как описано в аспектах, связанных с медицинскими применениями и способами лечения.
В соответствии с другим предпочтительным вариантом осуществления антител и их антигенсвязывающих фрагментов по изобретению, антитело или его антигенсвязывающий фрагмент имеет одну или несколько из следующих характеристик:
- антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92;
- антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92;
- антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
В соответствии с другим предпочтительным вариантом осуществления антител и их антигенсвязывающих фрагментов по изобретению, антитело или его антигенсвязывающий фрагмент имеет одну или несколько из следующих характеристик:
- устраняет устойчивость к статинам у млекопитающих, особенно у грызунов, таких как хомяк;
- увеличивает экспрессию LDLR у млекопитающих, особенно у грызунов, таких как хомяк;
- снижает уровень сывороточного LDL-C у грызунов, таких как хомяк;
- синергически снижает уровни LDL-С в сочетании с введением ингибитора HMG-CoA-редуктазы, в частности, у грызунов, таких как хомяк, где ингибитором HMG-CoA-редуктазы, предпочтительно, является аторвастатин.
В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент характеризуется одним или несколькими признаками из следующего:
(i) способностью снижать уровень общего холестерина в сыворотке по меньшей мере на от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней, предпочтительно, снижать уровень общего холестерина в сыворотке по меньшей мере приблизительно на 30-40%;
(ii) способностью снижать уровень LDL холестерина в сыворотке по меньшей мере приблизительно на 65-80%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней;
(iii) способностью снижать уровень триглицеридов в сыворотке, по меньшей мере приблизительно на 25-40%, по сравнению с уровнем до введения дозы;
(iv) достигать одного или нескольких признаков (i)-(iii), не снижая уровня сывороточного HDL холестерина, или снижать уровень сывороточного HDL холестерина не более чем на 5%, по сравнению с уровнем до введения дозы;
(v) достигать одного или нескольких признаков (i)-(iii), при небольшом или нерегистрируемом эффекте на функцию печени, по измерению ALT и AST.
В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент характеризуется одним или несколькими признаками из следующего:
(i) способностью снижать уровень LDL холестерина в сыворотке по меньшей мере приблизительно на 40-70%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 60 или 90 дней;
(ii) способностью уменьшать уровень триглицеридов в сыворотке по меньшей мере приблизительно на 25-40%, по сравнению с уровнем до введения дозы;
(iii) не снижать уровень HDL холестерина в сыворотке или уменьшать уровень HDL холестерина не более чем на 5%, по сравнению с уровнем до введения дозы.
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент характеризуется как связывающий эпитоп, содержащий аминокислотный остаток 238 hPCSK9 (SEQ ID NO:755). В более конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий один или несколько аминокислотных остатков в положениях 238, 153, 159 и 343 hPCSK9 (SEQ ID NO:755). В более конкретном варианте осуществления изобретения антитело или его фрагмент характеризуется связыванием эпитопа, который не содержит аминокислотных остатков в положениях 192, 194, 197 и/или 237 из SEQ ID NO:755.
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент характеризуется как связывающий эпитоп, содержащий аминокислотный остаток 366 hPCSK9 (SEQ ID NO:755). В более конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий один или несколько аминокислотных остатков в положениях 147, 366 и 380 hPCSK9 (SEQ ID NO:755). В более конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент антитела характеризуется как связывающий эпитоп, который не содержит аминокислотного остатка в положении 215 или 238 SEQ ID NO:755.
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи (HCVR), выбранную из группы, состоящей из последовательностей SEQ ID NO: 2, 18, 22, 26, 42, 46, 50, 66, 70, 74, 90, 94, 98, 114, 118, 122, 138, 142, 146, 162, 166, 170, 186, 190, 194, 210, 214, 218, 234, 238, 242, 258, 262, 266, 282, 286, 290, 306, 310, 314, 330, 334, 338, 354, 358, 362, 378, 382, 386, 402, 406, 410, 426, 430, 434, 450, 454, 458, 474, 478, 482, 498, 502, 506, 522, 526, 530, 546, 550, 554, 570, 574, 578, 594, 598, 602, 618, 622, 626, 642, 646, 650, 666, 670, 674, 690, 694, 698, 714, 718, 722, 738 и 742, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения HCVR содержит аминокислотную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO: 50, 66, 70, 74, 90, 94, 122, 138, 142, 218, 234, 238, 242, 258, 262, 314, 330 и 334. В более конкретном варианте HCVR содержит последовательность SEQ ID NO: 90 или 218.
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент дополнительно содержит вариабельную область легкой цепи (LCVR), выбранную из группы, состоящей из последовательностей SEQ ID NO: 10, 20, 24, 34, 44, 48, 58, 68, 72, 82, 92, 96, 106, 116, 120, 130, 140, 144, 154, 164, 168, 178, 188, 192, 202, 212, 216, 226, 236, 240, 250, 260, 264, 274, 284, 288, 298, 308, 312, 322, 332, 336, 346, 356, 360, 370, 380, 384, 394, 404, 408, 418, 428, 432, 442, 452, 456, 466, 476, 480, 490, 500, 504, 514, 524, 528, 538, 548, 552, 562, 572, 576, 586, 596, 600, 610, 620, 624, 634, 644, 648, 658, 668, 672, 682, 692, 696, 706, 716, 720, 730, 740 и 744, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения LCVR содержит аминокислотную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO: 58, 68, 72, 82, 92, 96, 130, 140, 144, 226, 236, 240, 250, 260, 264, 322, 332 и 336. В более конкретном варианте осуществления LCVR содержит последовательность SEQ ID NO: 92 или 226.
В конкретных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит пару последовательностей HCVR и LCVR (HCVR/LCVR), выбранную из группы, состоящей из пар последовательностей SEQ ID NO: 2/10, 18/20, 22/24, 26/34, 42/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/466, 474/476, 478/480, 482/490, 498/500, 502/504, 506/514, 522/524, 526/528, 530/538, 546/548, 550/552, 554/562, 570/572, 574/576, 578/586, 594/596, 598/600, 602/610, 618/620, 622/624, 626/634, 642/644, 646/648, 650/658, 666/668, 670/672, 674/682, 690/692, 694/696, 698/706, 714/716, 718/720, 722/730, 738/740 и 742/744. В одном из вариантов осуществления изобретения, пара последовательностей HCVR и LCVR содержит одну из пар последовательностей SEQ ID NO:50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 314/322, 330/332 и 334/336. В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность HCVR, как показано в SEQ ID NO:90, и аминокислотную последовательность LCVR, как показано в SEQ ID NO:92. В другом предпочтительном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность HCVR, как показано в SEQ ID NO:218 и аминокислотную последовательность LCVR, как показано в SEQ ID NO:226.
В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домен CDR3 тяжелой цепи (HCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 8, 32, 56, 80, 104, 128, 152, 176, 200, 224, 248, 272, 296, 320, 344, 368, 392, 416, 440, 464, 488, 512, 536, 560, 584, 608, 632, 656, 680, 704 и 728, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%, и домен CDR3 легкой цепи (LCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 16, 40, 64, 88, 112, 136, 160, 184, 208, 232, 256, 280, 304, 328, 352, 376, 400, 424, 448, 472, 496, 520, 544, 568, 592, 616, 640, 664, 688, 712 и 736, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, пара последовательностей HCDR3/LCDR3 выбрана из группы, состоящей из пар последовательностей SEQ ID NO:56/64, 80/88, 128/136, 224/232, 248/256 и 320/328. В более предпочтительных вариантах осуществления изобретения, антитело или антигенсвязывающий фрагмент содержит домен HCDR3, как показано в SEQ ID NO: 80, и домен LCDR3, как показано в SEQ ID NO:88. В другом предпочтительном варианте осуществления изобретения, антитело или антигенсвязывающий фрагмент содержит домен HCDR3, как показано в SEQ ID NO:224, и домен LCDR3, как показано в SEQ ID NO:232.
В еще одном варианте осуществления изобретения, антитело или антигенсвязывающий фрагмент дополнительно содержит домен CDR1 тяжелой цепи (HCDR1), выбранный из группы, состоящей из последовательностей SEQ ID NO:4, 28, 52, 76, 100, 124, 148, 172, 196, 220, 244, 268, 292, 316, 340, 364, 388, 412, 436, 460, 484, 508, 532, 556, 580, 604, 628, 652, 676, 700 и 724, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%; домен CDR2 тяжелой цепи (HCDR2), выбранный из группы, состоящей из последовательностей SEQ ID NO: 6, 30, 54, 78, 102, 126, 150, 174, 198, 222, 246, 270, 294, 318, 342, 366, 390, 414, 438, 462, 486, 510, 534, 558, 582, 606, 630, 654, 678, 702 и 726, или по существу аналогичным им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%; домен CDR1 легкой цепи (LCDR1), выбранный из группы, состоящей из последовательностей SEQ ID NO: 12, 36, 60, 84, 108, 132, 156, 180, 204, 228, 252, 276, 300, 324, 348, 372, 396, 420, 444, 468, 492, 516, 540, 564, 588, 612, 636, 660, 684, 708 и 732, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%, и домен CDR2 легкой цепи (LCDR2), выбранный из группы, состоящей из последовательностей SEQ ID NO: 14, 38, 62, 86, 110, 134, 158, 182, 206, 230, 254, 278, 302, 326, 350, 374, 398, 422, 446, 470, 494, 518, 542, 566, 590, 614, 638, 662, 686, 710 и 734, или из по существу аналогичных им последовательностям, имеющим идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, последовательности CDR тяжелой цепи и CDR легкой цепи содержат последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO: 52, 54, 56, 60, 62, 64, 76, 78, 80, 84, 86, 88; 124, 126, 128, 132, 134, 136; 220, 222, 224, 228, 230, 232; 244, 246, 248, 252, 254, 256; и 316, 318, 320, 324, 326, 328. В более конкретных вариантах осуществления изобретения, последовательности CDR содержат последовательности SEQ ID NO: 76, 78, 80, 84, 86, 88; или 220, 222, 224, 228, 230, 232. В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент состоит из аминокислотной последовательности CDR тяжелой цепи и аминокислотной последовательности CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88. В другом предпочтительном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент состоит из аминокислотной последовательности CDR тяжелой цепи и аминокислотной последовательности CDR легкой цепи, как показано в SEQ ID NO: 220, 222, 224, 228, 230 и 232.
В родственном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домены CDR тяжелой цепи и CDR легкой цепи, находящиеся в паре последовательности тяжелой цепи и легкой цепи, выбранной из группы, состоящей из пар последовательностей SEQ ID NO: 2/10, 18/20, 22/24, 26/34, 42/44, 46/48, 50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 98/106, 114/116, 118/120, 122/130, 138/140, 142/144, 146/154, 162/164, 166/168, 170/178, 186/188, 190/192, 194/202, 210/212, 214/216, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 266/274, 282/284, 286/288, 290/298, 306/308, 310/312, 314/322, 330/332, 334/336, 338/346, 354/356, 358/360, 362/370, 378/380, 382/384, 386/394, 402/404, 406/408, 410/418, 426/428, 430/432, 434/442, 450/452, 454/456, 458/466, 474/476, 478/480, 482/490, 498/500, 502/504, 506/514, 522/524, 526/528, 530/538, 546/548, 550/552, 554/562, 570/572, 574/576, 578/586, 594/596, 598/600, 602/610, 618/620, 622/624, 626/634, 642/644, 646/648, 650/658, 666/668, 670/672, 674/682, 690/692, 694/696, 698/706, 714/716, 718/720, 722/730, 738/740 и 742/744. В одном из вариантов осуществления изобретения, последовательности CDR, содержащиеся в HCVR и LCVR, выбраны из пар аминокислотных последовательностей SEQ ID NO:50/58, 66/68, 70/72, 74/82, 90/92, 94/96, 122/130, 138/140, 142/144, 218/226, 234/236, 238/240, 242/250, 258/260, 262/264, 314/322, 330/332 и 334/336. В более конкретных вариантах осуществления изобретения, последовательности CDR, находящиеся в HCVR/LCVR, выбраны из пар аминокислотных последовательностей SEQ ID NO:90/92 или 218/226. В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи пары аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO:90/92. В другом предпочтительном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи пары аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO:218/226.
В одном конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи (HCVR) с аминокислотной последовательностью SEQ ID NO:90 или по существу с аналогичной ей последовательностью, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере, 95%, по меньшей мере 98% или по меньшей мере 99%.
В одном конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент дополнительно содержит вариабельную область легкой цепи (LCVR) с аминокислотной последовательностью SEQ ID NO:92 или по существу с аналогичной ей последовательностью, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или, по меньшей мере 99%.
В конкретных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит HCVR с аминокислотной последовательностью, как показано в SEQ ID NO:90 и LCVR с аминокислотной последовательностью, как показано в SEQ ID NO:92.
В конкретных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домен CDR3 тяжелой цепи (HCDR3) SEQ ID NO:80, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере, 98% или по меньшей мере 99%, и/или домен CDR3 легкой цепи (LCDR3) SEQ ID NO:88, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, пара последовательностей HCDR3/LCDR3 представляет собой пару последовательностей SEQ ID NO: 80/88. В более предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домен HCDR3, как показано в SEQ ID NO: 80, домен и LCDR3, как показано в SEQ ID NO: 88.
В другом конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент дополнительно содержит домен CDR1 тяжелой цепи (HCDR1) с аминокислотной последовательностью SEQ ID NO:76, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%, и/или домен CDR2 тяжелой цепи (HCDR2) с аминокислотной последовательностью SEQ ID NO: 78, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%, и/или домен CDR1 легкой цепи (LCDR1) с аминокислотной последовательностью SEQ ID NO:84, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%, и/или домен CDR2 легкой цепи (LCDR2) с аминокислотной последовательностью SEQ ID NO:86, или по существу с аналогичной ей последовательностью, имеющий идентичность последовательности, равную меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, последовательности CDR тяжелой цепи и CDR легкой цепи содержат последовательности, выбранные из группы, состоящей из последовательностей SEQ ID NO: 76, 78, 80, 84, 86, 88. В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88.
В другом конкретном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домены CDR тяжелой цепи и CDR легкой цепи, находящиеся в паре последовательностей тяжелой цепи и легкой цепи SEQ ID NO:90/92.
Особенно предпочтительный вариант осуществления изобретения, относится к антителу, содержащему HCVR/LCVR с последовательностями SEQ ID NO:90/92 и/или CDR с последовательностями SEQ ID NO:76, 78, 80 и/или CDR с последовательностями SEQ ID NO:84, 86, 88. Другой особенно предпочтительный вариант осуществления изобретения относится к антителу, содержащему HCVR/LCVR с последовательностями SEQ ID NO: 90/92, CDR с последовательностями SEQ ID NO:76, 78, 80 и CDR с последовательностями SEQ ID NO: 84, 86, 88 ("316P").
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит HCVR, кодируемую последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из последовательностей SEQ ID NO: 1, 17, 21, 25, 41, 45, 49, 65, 69, 73, 89, 93, 97, 113, 117, 121, 137, 141, 145, 161, 165, 169, 185, 189, 193, 209, 213, 217, 233, 237, 241, 257, 261, 265, 281, 285, 289, 305, 309, 313, 329, 333, 337, 353, 357, 361, 377, 381, 385, 401, 405, 409, 425, 429, 433, 449, 453, 457, 473, 477, 481, 497, 501, 505, 521, 525, 529, 545, 549, 553, 569, 573, 577, 593, 597, 601, 617, 621, 625, 641, 645, 649, 665, 669, 673, 689, 693, 697, 713, 717, 721, 737 и 741, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, HCVR кодируется последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из последовательностей SEQ ID NO: 49, 65, 69, 73, 89, 93, 121, 137, 141, 217, 233, 237, 241, 257, 261, 313, 329 и 333. В более конкретных вариантах осуществления изобретения, HCVR кодируется последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из SEQ ID NO: 89 и 217.
В одном из вариантов осуществления изобретения, антитело или его фрагмент дополнительно содержит LCVR, кодируемую последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из последовательностей SEQ ID NO: 9, 19, 23, 33, 43, 47, 57, 67, 71, 81, 91, 95, 105, 115, 119, 129, 139, 143, 153, 163, 167, 177, 187, 191, 201, 211, 215, 225, 235, 239, 249, 259, 263, 273, 283, 287, 297, 307, 311, 321, 331, 335, 345, 355, 359, 369, 379, 383, 393, 403, 407, 417, 427, 431, 441, 451, 455, 465, 475, 479, 489, 499, 503, 513, 523, 527, 537, 547, 551, 561, 571, 575, 585, 595, 599, 609, 619, 623, 633, 643, 647, 657, 667, 671, 681, 691 695, 705, 715, 719, 729, 739 и 743, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, LCVR кодируется последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из последовательностей SEQ ID NO: 57, 67, 71, 81, 91, 95, 129, 139, 143, 225, 235, 239, 249, 259, 263, 321, 331 и 335. В более конкретных вариантах осуществления изобретения, LCVR кодируется последовательностью нуклеиновой кислоты, выбранной из группы, состоящей из SEQ ID NO: 91 и 225.
В одном из вариантов осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит домен HCDR3, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO: 7, 31, 55, 79, 103, 127, 151, 175, 199, 223, 247, 271, 295, 319, 343, 367, 391, 415, 439, 463, 487, 511, 535, 559, 583, 607, 631, 655, 679, 703 и 727, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%, и домен LCDR3, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO: 15, 39, 63, 87, 111, 135, 159, 183, 207, 231, 255, 279, 303, 327, 351, 375, 399, 423, 447, 471, 495, 519, 543, 567, 591, 615, 639, 663, 687, 711 и 735, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, HCDR3 и LCDR3 содержат пару последовательностей, кодируемых последовательностями нуклеиновой кислоты SEQ ID NO: 55/63, 79/87, 127/135, 223/231, 247/255 и 319/327 соответственно. В более конкретных вариантах осуществления изобретения, HCDR3 и LCDR3 содержат пару последовательностей, кодируемых последовательностями нуклеиновой кислоты SEQ ID NO: 79/87 и 223/231.
В дополнительном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент дополнительно содержит: домен HCDR1, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO: 3, 27, 51, 75, 99, 123, 147, 171, 195, 219, 243, 267, 291, 315, 339, 363, 387, 411, 435, 459, 483, 507, 531, 555, 579, 603, 627, 651, 675, 699 и 723, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%; домен HCDR2, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO: 5, 29, 53, 77, 101, 125, 149, 173, 197, 221, 245, 269, 293, 317, 341, 365, 389, 413, 437, 461, 485, 509, 533, 557, 581, 605, 629, 653, 677, 701 и 725, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%; домен LCDR1, кодируемый нуклеотидной последовательностью, выбранной из группы, включающей последовательностей SEQ ID NO: 11, 35, 59, 83, 107, 131, 155, 179, 203, 227, 251, 275, 299, 323, 347, 371, 395, 419, 443, 467, 491, 515, 539, 563, 587, 611, 635, 659, 683, 707 и 731, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%; и домен LCDR2, кодируемый нуклеотидной последовательностью, выбранной из группы, состоящей из последовательностей SEQ ID NO: 13, 37, 61, 85, 109, 133, 157, 181, 205, 229, 253, 277, 301, 325, 349, 373, 397, 421, 445, 469, 493, 517, 541, 565, 589, 613, 637, 661, 685, 709 и 733, или по существу идентичной им последовательности, имеющей идентичность последовательности, равную по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99%. В одном из вариантов осуществления изобретения, последовательности CDR тяжелой цепи и CDR легкой цепи, кодируются последовательностями нуклеиновых кислот SEQ ID NO: 51, 53, 55, 59, 61, 63; 75, 77, 79, 83, 85, 87; 123, 125, 127, 131, 133, 135; 219, 221, 223, 227, 229, 231; 243, 245, 247, 251, 253, 255; и 315, 317, 319, 323, 325, 327. В более конкретных вариантах осуществления изобретения, последовательности CDR тяжелой цепи и CDR легкой цепи, кодируются последовательностями нуклеиновых кислот SEQ ID NO: 75, 77, 79, 83, 85, 87; и 219, 221, 223, 227, 229, 231.
В еще одном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент содержит HCDR3 и LCDR3, где HCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20 (SEQ ID NO:747), где X1 представляет собой Ala, X2 представляет собой Arg или Lys, X3 представляет собой Asp, Х4 представляет собой Ser или Ile, Х5 представляет собой Asn или Val, X6 представляет собой Leu или Trp, X7 представляет собой Gly или Met, X8 представляет собой Asn или Val, X9 представляет собой Phe или Tyr, X10 представляет собой Asp, X11 представляет собой Leu или Met, X12 представляет собой Asp или отсутствует, X13 представляет собой Tyr или отсутствует, X14 представляет собой Tyr или отсутствует, X15 представляет собой Tyr или отсутствует, X16 представляет собой Tyr или отсутствует, Х17 представляет собой Gly или отсутствует, X18 представляет собой Met или отсутствует, X19 представляет собой Asp или отсутствует, и X20 представляет собой Val или отсутствует; и LCDR3 содержит аминокислотную последовательность формулы X1-X2-X3-X4-X5-X6-X7-X8-X9 (SEQ ID NO:750), где X1 представляет собой Gln или Met, X2 представляет собой Gln, X3 представляет собой Tyr или Thr, Х4 представляет собой Tyr или Leu, X5 представляет собой Thr или Gln, X6 представляет собой Thr, X7 представляет собой Pro, X8 представляет собой Tyr или Leu, и X9 представляет собой Thr.
В еще одном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент дополнительно содержит последовательность HCDR1 формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID NO:745), где X1 представляет собой Gly, Х2 представляет собой Phe, X3 представляет собой Thr, Х4 представляет собой Phe, Х5 представляет собой Ser или Asn, X6 представляет собой Ser или Asn, X7 представляет собой Tyr или His, и X8 представляет собой Ala или Trp; последовательность HCDR2 формулы X1-X2-X3-X4-X5-X6-X7-X8 (SEQ ID NO:746), где X1 представляет собой Ile, X2 представляет собой Ser или Asn, X3 представляет собой Gly или Gln, Х4 представляет собой Asp или Ser, Х5 представляет собой Gly, Х6 представляет собой Ser или Gly, X7 представляет собой Thr или Glu, и X8 представляет собой Thr или Lys; последовательность LCDR1 формулы X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12 (SEQ ID NO:748), где X1 представляет собой Gln, Х2 представляет собой Ser, Х3 представляет собой Val или Leu, X4 представляет собой Leu, X5 представляет собой His или Tyr, X6 представляет собой Arg или Ser, X7 представляет собой Ser или Asn, X8 представляет собой Asn или Gly, X9 представляет собой Asn, X10 представляет собой Arg или Asn, X11 представляет собой Asn или Tyr, и X12 представляет собой Phe или отсутствует; последовательность LCDR2 формулы X1-X2-X3 (SEQ ID NO: 749), где X1 представляет собой Trp или Leu, X2 представляет собой Ala или Gly, и Х3 представляет собой Ser.
В еще одном варианте осуществления изобретения, антитело или его антигенсвязывающий фрагмент является анти-антителом человека против PCSK9 или его антигенсвязывающим фрагментом, содержащим вариабельную область тяжелой цепи (HCVR), кодируемую сегментами нуклеотидной последовательности, полученной из последовательностей VH, DH и JH зародышевой линии, и вариабельную область легкой цепи (LCVR), кодируемую сегментами нуклеотидной последовательности, полученной из последовательностей VK и JK зародышевой линии, при этом последовательности зародышевой линии представляют собой: (а) сегмент 3-23 гена VH, сегмент 7-27 гена DH, сегмент 2 гена JH, сегмент 4-1 гена VK и сегмент 2 гена JK, или (b) сегмент 3-7 гена VH, сегмент 2-8 гена DH, сегмент 6 гена JH, сегмент 2-28 гена VK и сегмент 4 гена JK.
В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывается с тем же эпитопом на hPCSK9, как и антитело, содержащее аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88, или как показано в SEQ ID NO: 220, 222, 224, 228, 230 и 232.
В предпочтительных вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом, содержащим аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88, или как показано в SEQ ID NO: 220, 222, 224, 228, 230 и 232.
Изобретение охватывает антитела против PCSK9 с модифицированным гликозилированием. В некоторых вариантах осуществления изобретения могут быть полезны модификации для удаления нежелательных сайтов гликозилирования, или, например, для удаления фукозного фрагмента, с целью увеличения зависимой от антител клеточной цитотоксичности (ADCC) (смотрите Shield et al. (2002) JBC 277:26733). В других вариантах осуществления изобретения, может быть выполнена модификация галактозилирования, для того, чтобы модифицировать комплемент-зависимую цитотоксичность (CDC).
Некоторые предпочтительные последовательности, относящиеся к предпочтительным вариантам антител для осуществления настоящего изобретения представлены ниже.
SEQ ID NO:76: Gly Phe Thr Phe Asn Asn Tyr Ala
SEQ ID NO:78: Ile Ser Gly Ser Gly Gly Thr Thr
SEQ ID NO:80: Ala Lys Asp Ser Asn Trp Gly Asn Phe Asp Leu
SEQ ID NO:84: Gln Ser Val Leu Tyr Arg Ser Asn Asn Arg Asn Phe
SEQ ID NO:86: Trp Ala Ser
SEQ ID NO:88: Gln Gln Tyr Tyr Thr Thr Pro Tyr Thr
SEQ ID NO:90:

SEQ ID NO:92:


SEQ ID NO:775 (hPCSK9):


ПОЛУЧЕНИЕ АНТИТЕЛ ЧЕЛОВЕКА
Способы получения антител человека в трансгенных мышах известны (см. например, патент США № 6596541, Regeneron Pharmaceuticals, VelocImmune™). Технология VelocImmune™ включает получение трансгенной мыши, имеющей геном, содержащий вариабельные области тяжелой и легкой цепей человека, функционально связанные с эндогенным локусом константной области мыши, таким образом, что мышь, в ответ на антигенную стимуляцию, продуцирует антитело, содержащее вариабельную область человека и константную область мыши. ДНК, кодирующую вариабельные области тяжелой и легкой цепей антитела, выделяют и функционально связывают с ДНК, кодирующей константные области тяжелой и легкой цепей человека. Затем ДНК экспрессируют в клетке, способной экспрессировать полностью человеческое антитело. В конкретном варианте осуществления изобретения, клетка представляет собой клетку СНО.
Антитела могут быть терапевтически полезными для блокировании взаимодействие лиганд-рецептор или для ингибирования взаимодействия компонентов рецептора, не приводя к киллингу клеток посредством связывания комплемента и участия в комплемент-зависимой цитотоксичности (CDC) или к киллингу клеток посредством зависимой от антител клеточной цитотоксичности (ADCC). При этом константная область антитела играет важную роль в способности антитела к связыванию комплемента и к опосредованию клеточной цитотоксичности. Таким образом, изотип антитела может быть выбран на основе того, желательна или нет опосредованная антителом цитотоксичность.
Антитела человека могут существовать в двух формах, которые связаны с шарниром гетерогенности. В одной форме, молекула антитела содержит стабильный четырехцепочечный конструкт, с приблизительной массой 150-160 кДа, где димеры связаны вместе посредством межцепочечных дисульфидных связей в тяжелых цепях. Во втором варианте, димеры не связаны посредством межцепочечных дисульфидных связей, и молекула, с приблизительной массой 75-80 кДа, состоит из ковалентно связанных легкой цепи и тяжелой цепи (полу-антитело). Эти формы чрезвычайно трудны для разделения, даже после аффинной очистки.
Частота присутствия второй формы в различных изотипах интактных IgG обусловлена, но без ограничения этим, структурными различиями, связанными с шарнирной областью изотипа антитела. Одна аминокислотная замена в шарнирной области IgG4 человека может значительно снизить присутствие второй формы (Angal et al. (1993) Molecular Immunology 30:105) до уровней, обычно наблюдаемых при использовании шарнира IgG1 человека. Настоящее изобретение охватывает антитела, имеющие одну или несколько мутаций в шарнирной области, СН2 или СН3, что может быть желательным, например, при получении антител, в частности, для повышения выхода формы целевого антитела.
Как правило, VelocImmune™ мышь иммунизируют представляющим интерес антигеном, и из мышей выделяют лимфатические клетки (например, B-клетки), которые экспрессируют антитела. Лимфатические клетки могут быть слиты с миеломной клеточной линией, с получением линии бессмертных гибридомных клеток, и такие линии гибридомых клеток подвергают скринингу и отбирают для линии гибридомных клеток, которые идентифицированы как продуцирующие антитела, специфичные к представляющему интерес антигену. ДНК, кодирующую вариабельные области тяжелой цепи и легкой цепи, могут быть выделены и связаны с константными областями тяжелой цепи и легкой цепи желательных изотипов. Такой антительный белок может быть получен в клетках, таких как клетки СНО. Альтернативно, ДНК, кодирующие антигенспецифические химерные антитела или вариабельные домены легкой и тяжелой цепей, могут быть непосредственно выделены из антигенспецифических лимфоцитов.
Первоначально были выделены высокоаффинные химерные антитела, имеющие вариабельную область человека и константную область мыши. Как описано ниже, антитела были охарактеризованы и отобраны по желательным характеристикам, включая аффинность, селективность, эпитоп и т.п. Константные области мышей были заменены на желаемую константную область человека, с получением полностью человеческого антитела по изобретению, например, в виде антитела дикого типа или модифицированного IgG1 или IgG4 (например, SEQ ID NO: 751, 752, 753). В то время, как выбранная константная область может варьироваться в зависимости от конкретного применения, вариабельная область является ответственной за характеристики в части высокой аффинности связывания антигена и целевой специфичности.
КАРТИРОВАНИЕ ЭПИТОПА И СВЯЗАННЫЕ С НИМ ТЕХНОЛОГИИ
Для скрининга антител, которые связываются с конкретным эпитопом (например, которые блокируют связывание IgE с его высокоаффинным рецептором), может быть выполнена процедура анализа кросс-блокировки, такого, как описано в Antibodies, Harlow and Lane (Cold Spring Harbor Press, Cold Spring Harb., NY). Другие методы включают аланин-сканирующий мутагенез, пептидный блоттинг (Reineke (2004) Methods Mol Biol 248:443-63; включено в виде ссылки в полном объеме), или анализ пептидного расщепления. Кроме того, могут быть использованы такие методы, как исключение эпитопа, экстракция эпитопа и химическая модификация антигенов (Tomer (2000) Protein Science 9: 487-496; включено в виде ссылки в полном объеме).
Термин «эпитоп» относится к сайту на антигене, с которым реагируют В- и/или Т-клетки. В-клеточные эпитопы могут быть сформированы как из смежных аминокислот, так и несмежных аминокислот, которые оказываются рядом друг с другом при третичной укладке белка. Эпитопы, которые формируются из смежных аминокислот, как правило, сохраняются под воздействием денатурирующих растворителей, тогда как эпитопы, образованные третичной укладкой, обычно теряются при обработке денатурирующими растворителями. Эпитоп обычно содержит по меньшей мере три, и, как правило, по меньшей мере 5 или 8-10 аминокислот в уникальной пространственной конформации.
Профилирование с помощью модификаций (MAP), также известное как профилирование антител на основе антигенной структуры (ASAP), является методом, которым классифицируют большое количество моноклональных антител (mAb), направленным против того же антигена в соответствии со сходством профиля связывания каждого антитела с поверхностями, химически или ферментативно модифицированными антигенами (заявка на патент США № 2004/0101920; включена в виде ссылки в полном объеме). Каждая группа может отражать уникальный эпитоп, или заметно отличаться от эпитопа другой категории, или частично перекрывается с ним. Эта технология позволяет выполнить быструю фильтрацию генетически идентичных моноклональных антител, так что характеризация может быть сосредоточена на генетически различных mAb. При применении гибридомного скрининга, MAP может способствовать обнаружению редких гибридомных клонов, которые продуцируют моноклональные антитела с нужными характеристиками. MAP может использоваться для сортировки mAb против PCSK9 по настоящему изобретению в группах mAb, связывающих различные эпитопы.
В различных вариантах осуществления изобретения, антитело против hPCSK9 или антигенсвязывающий фрагмент антитела связывает эпитоп в пределах каталитического домена, который находится в пределах аминокислотных положений приблизительно 153-425 в последовательности SEQ ID NO:755, в частности, эпитоп соответствует положениям от приблизительно 153 до приблизительно 250, или от приблизительно 250 до приблизительно 425, более конкретно, антитело или фрагмент антитела по изобретению связывает эпитоп в пределах фрагмента в аминокислотных положениях от приблизительно 153 до приблизительно 208, от приблизительно 200 до приблизительно 260, от приблизительно 250 до приблизительно 300, от приблизительно 275 до приблизительно 325, от приблизительно 300 до приблизительно 360, от приблизительно 350 до приблизительно 400 и/или от приблизительно 375 до приблизительно 425.
В различных вариантах осуществления изобретения, антитело против hPCSK9 или антигенсвязывающий фрагмент антитела связывают эпитоп в пределах пропептидного домена (остатки с 31 по 152 в последовательности SEQ ID NO: 755), в частности, эпитоп находится в пределах аминокислотных положений от приблизительно остатка 31 до приблизительно остатка 90 или от приблизительно остатка 90 до приблизительно остатка 152, в частности, антитело или фрагмент антитела по изобретению связывает эпитоп в пределах фрагмента, находящегося в пределах от приблизительно остатка 31 до приблизительно остатка 60, от приблизительно остатка 60 до приблизительно остатка 90, от приблизительно остатка 85 до приблизительно остатка 110, от приблизительно остатка 100 до приблизительно остатка 130, от приблизительно остатка 125 до приблизительно остатка 150, от приблизительно остатка 135 до приблизительно остатка 152, и/или от приблизительно остатка 140 до приблизительно остатка 152.
В некоторых вариантах осуществления изобретения, антитело против hPCSK9 или антигенсвязывающий фрагмент антитела связывают эпитоп в С-концевом домене (остатки 426-692 в последовательности SEQ ID NO:755), в частности, эпитоп находится в положении от приблизительно остатка 426 до приблизительно остатка 570 или от приблизительно остатка 570 до приблизительно остатка 692, в частности, антитело или фрагмент антитела по изобретению связывает эпитоп в пределах фрагмента, находящегося в положении от приблизительно остатка 450 до приблизительно остатка 500, от приблизительно остатка 500 до приблизительно остатка 550, от приблизительно остатка 550 до приблизительно остатка 600 и/или от приблизительно остатка 600 до приблизительно остатка 692.
В некоторых вариантах осуществления изобретения, антитело или фрагмент антитела связывают эпитоп, который включает более одного из перечисленных эпитопов в пределах каталитического домена, пропептидного домена или С-концевого домена, и/или находится в пределах двух или трех различных доменов (например, эпитопов в каталитическом домене и С-концевом домене, или в пределах пропептидного домена и каталитического домена, или в пределах пропептидного домена, каталитического домена и С-концевого домена).
В некоторых вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп на hPCSK9, содержащий аминокислотный остаток 238 из hPCSK9 (SEQ ID NO: 755). Экспериментальные результаты (смотрите заявку на патент США № 2010/0166768) показали, что при наличии мутации D238 значение KD для mAb 316P показало более чем 400-кратное снижение аффинности связывания (с приблизительно 1×10-9 М до приблизительно 410×10-9 M) и T1/2 уменьшилось более чем в 30 раз (с приблизительно 37 до приблизительно 1 мин). В конкретном варианте осуществления изобретения мутация D238R. В конкретных вариантах изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп на hPCSK9, содержащий два или более аминокислотных остатков в положениях 153, 159, 238 и 343.
Как было показано ранее (смотрите заявку на патент США № 2010/0166768), мутации аминокислотных остатков 153, 159 или 343 приводят к приблизительно 5-10-кратному уменьшению аффинности или аналогичному снижению значения T1/2. В конкретных вариантах осуществления изобретения мутация представляет собой S153R, E159R и/или D343R.
В некоторых вариантах осуществления изобретения, антитело или его антигенсвязывающий фрагмент связывает эпитоп на hPCSK9, содержащий аминокислотный остаток 366 в hPCSK9 (SEQ ID NO: 755). Экспериментальные результаты (смотрите заявку на патент США № 2010/0166768) показали, что при мутации E366, аффинность mAb 300N уменьшилась приблизительно в 50 раз (с приблизительно 0,7×10-9 М до приблизительно 36×10-9 М) и аналогичное уменьшение имело место в отношении T1/2 (с приблизительно 120 до приблизительно 2 мин). В конкретном варианте осуществления изобретения мутация представляет собой E366K.
Настоящее изобретение относится к антителам против PCSK9, которые связывают тот же самый эпитоп, что и любое из конкретных антител, описанных в настоящем документе в качестве примеров. Кроме того, настоящее изобретение также включает антитела против PCSK9, которые конкурируют за связывание с PCSK9 или с фрагментом PCSK9, с любым конкретными антителами, описанными в настоящем документе в качестве примера.
С помощью стандартных методов, известных в данной области техники, можно легко определить, связывает или нет антитело тот же самый эпитоп, как и референсное антитело против PCSK9, или конкурирует за связывание с ним. Например, чтобы определить, связывает или нет испытуемое антитело тот же самый эпитопом, как и референсное антитело против PCSK9 по изобретению, референсному антителу дают связаться с белком или пептидом PCSK9 при насыщающих условиях. Затем оценивают способность испытуемого антитела связывать молекулу PCSK9. Если испытуемое антитело способно связывать PCSK9 в условиях насыщения связывания с референсным антителом против PCSK9, то можно сделать вывод о том, что испытуемое антитело связывается с другим эпитопом, чем референсное антитело против PCSK9. С другой стороны, если испытуемое антитело не способно связывать молекулу PCSK9 после насыщения связывания при использовании референсного антитела против PCSK9, то испытуемое антитело способно связывать тот же самый эпитоп, с которым связывается антитело против PCSK9 по изобретения.
Для того чтобы определить конкурирует ли антитела за связывание с референсным антителом против PCSK9, вышеописанная методика связывания выполняется в двух вариантах: в первом варианте референсному антителу дают связаться с молекулой PCSK9 в условиях насыщения, с последующей оценкой связывания испытуемого антитела с молекулой PCSK9. Во втором варианте, испытуемому антителу дают связаться с молекулой PCSK9 в условиях насыщения с последующей оценкой связывания референсного антитела с молекулой PCSK9. Если в обоих вариантах только первое (насыщающее) антитело способно связываться с молекулой PCSK9, то можно сделать вывод о том, что испытуемое антитело и контрольное антитело конкурируют за связывание с PCSK9. Как понятно специалисту в данной области техники, антитело, которое конкурирует за связывание с референсным антителом, не обязательно связывается с идентичным эпитопом, с которым связывается референсное антитело, но такое антитело может стерически блокировать связывание референсного антитела путем связывания перекрывающегося эпитопа, или эпитопа, который прилегает к эпитопу, который связывает референсное антитело.
Два антитела связывают тот же самый эпитоп или перекрывающиеся эпитопы, если каждый из них конкурентно ингибирует (блокирует) связывание другого антитела с антигеном. То есть, 1-, 5-, 10-, 20- или 100-кратный избыток одного антитела ингибирует связывание другого антитела по меньшей мере на 50%, но предпочтительно, на 75%, 90% или даже на 99%, по измерению анализом конкурентного связывания (см., например, Junghans et al., Cancer Res. 1990 50:1495-1502). Альтернативно, два антитела имеют один и тот же эпитоп для связывания, если по существу все аминокислотные мутации в антигене, которые уменьшают или устраняют связывание одного антитела, снижают или устраняют связывание другого. Два антитела имеют перекрывающиеся эпитопы для связывания, если некоторые аминокислотные мутации, которые уменьшают или устраняют связывание одного антитела, снижают или устраняют связывание другого.
Для подтверждения того, на самом ли деле имеет место отсутствие связывания испытуемого антитела из-за связывания с тем же эпитопом референсного антитела, или же отсутствие связывания вызвано стерическим блокированием (или другим явлением), можно выполнить дополнительные обычные эксперименты (например, пептидные мутации и анализы связывания). Эксперименты такого типа могут быть выполнены с использованием ELISA, RIA, поверхностного плазмонного резонанса, проточной цитометрии или любого другого количественного или качественного анализа связывания антитела, известного в данной области техники.
В конкретном варианте осуществления, настоящее изобретение содержит антитело против PCSK9 или антигенсвязывающий фрагмент антитела, которое связывает белок PCSK9 с аминокислотной последовательностью SEQ ID NO: 755, где связывание антитела или его фрагмента с белком PCSK9 и вариантом белка PCSK9 составляет менее 50% от величины связывания антитела или его фрагмента с белком PCSK9, имеющим аминокислотную последовательность SEQ ID NO: 755. В одном конкретном варианте осуществления изобретения, вариант белка PCSK9 содержит по меньшей мере одну мутацию аминокислотного остатка в положении, выбранном из группы, состоящей из положений 153, 159, 238 и 343. В более конкретном варианте осуществления изобретения, по меньшей мере одна мутация представляет собой S153R, E159R, D238R и/или D343R. В другом конкретном варианте осуществления изобретения, вариант белка PCSK9 содержит по меньшей мере одну мутацию аминокислотного остатка в положении 366. В одном конкретном варианте осуществления изобретения, вариант белка PCSK9 содержит по меньшей мере одну мутацию аминокислотного остатка в положении, выбранном из группы, состоящей из положений 147, 366 и 380. В более конкретном варианте осуществления изобретения мутация представляет собой S147F, E366K и V380M.
ИММУНОКОНЪЮГАТЫ
Изобретение охватывает моноклональное человеческое антитело против PCSK9, конъюгированное с фрагментом, проявляющим терапевтическую активность ("иммуноконъюгат"), таким как цитотоксин, химиотерапевтическое средство, иммунодепрессант или радиоизотоп. Цитотоксические средства включают любое средство, которое является вредным для клеток. Примеры подходящих цитотоксических средств и химиотерапевтических средств, используемых для получения иммуноконъюгатов, известны в данной области, см., например, заявку WO 05/103081.
БИСПЕЧИФИЧНОСТЬ
Антитела по настоящему изобретению могут быть моноспецифическими, биспецифическими или мультиспецифическими. Мультиспецифические моноклональные антитела могут быть специфичными к различным эпитопам одного мишеневого полипептида или могут содержать антиген-связывающие домены, специфичные более чем к одному мишеневому полипептиду. См., например, Tutt et al. (1991) J. Immunol. 147:60-69. Человеческие моноклональные антитела против PCSK9 могут быть связаны или совместно экспрессироваться с другой функциональной молекулой, например, с другим пептидом или белком. Например, антитело или его фрагмент могут быть функционально связаны (например, путем химического связывания, генетического слияния, нековалентной связи или иным образом) с одним или несколькими другими молекулярными объектами, такими как другое антитело или фрагмент антитела, с получением биспецифических или мультиспецифических антител, имеющих вторую специфичность связывания.
Примеры биспецифических антител, которые могут быть использованы в контексте настоящего изобретения, включают использование первого домена СН3 иммуноглобулина (Ig), и второго домена СН3 Ig, где первый и второй СН3-домены Ig отличаются друг от друга по меньшей мере на одну аминокислоту, и где по меньшей мере одна отличающаяся аминокислота уменьшает связывание биспецифического антитела с белком А, по сравнению с биспецифическим антителом, в котором отсутствует аминокислотное различие. В одном из вариантов осуществления изобретения, первый СН3-домен Ig связывается с белком А, а второй СН3-домен Ig содержит мутацию, которая уменьшает или устраняет связывания с белком А, такую как модификацию H95R (нумерация экзонов по IMGT; или H435R по ЕС нумерации). Второй CH3 может дополнительно содержать модификацию Y96F (по IMGT; или Y436F по ЕС). Дополнительные модификации, которые могут быть представлены во втором CH3-домене, включают: D16E, L18M, N44S, K52N, V57M и V82I (по IMGT; или D356E, L358M, N384S, K392N, V397M и V422I по ЕС), в случае антител IgG1; N44S, K52N и V82I (IMGT; N384S, K392N и V422I по ЕС), в случае антител IgG2, и Q15R, N44S, K52N, V57M, R69K, E79Q и V82I (по IMGT; или Q355R, N384S, K392N, V397M, R409K, E419Q и V422I по ЕС) в случае антител IgG4. Вариации биспецифических антител, описанные выше, находятся в пределах объема притязаний настоящего изобретения.
БИОЭКВИВАЛЕНТЫ
Антитела против PCSK9 и фрагменты антител по настоящему изобретению содержат белки, имеющие аминокислотные последовательности, которые отличаются от последовательностей описанных моноклональных антител, но которые сохраняют способность связывать PCSK9 человека. Такие варианты моноклональных антител и фрагментов антител содержат одно или несколько добавлений, делеций или замен аминокислот, по сравнению с исходной последовательностью, но обладают биологической активностью, которая по существу эквивалентна описанным моноклональным антителам. Кроме того, последовательности ДНК, кодирующие антитела против PCSK9 настоящего изобретения, содержат последовательности, которые содержат одну или несколько добавлений, делеций или замен нуклеотидов, по сравнению с раскрытыми последовательности, но при этом кодирующие антитела против PCSK9 или фрагменты антитела, которые по существу биоэквивалентны антителам против PCSK9 или фрагментам антител по изобретению. Примеры таких аминокислотных вариантов и последовательностей ДНК описаны выше.
Два антигенсвязывающих белка или антитела считаются биоэквивалентными, если, например, они являются фармацевтически эквивалентными или фармацевтически альтернативными, когда их скорость и степень абсорбции не имеют существенных различий при введении их в схожих экспериментальных условиях в одной и той же молярной дозе, в виде одной или нескольких доз. Некоторые антитела считаются эквивалентами или фармацевтическими альтернативами, если они эквивалентны по степени их абсорбции, но не по их скорости абсорбции; при этом их можно считать биоэквивалентными, несмотря на то, что такие различия в скорости абсорбции являются преднамеренными и отражены в их описанной характеристике, но не являются значимыми для достижения эффективной концентрации препарата в организме, например, при постоянном применении, и не считаются значимыми с медицинской точки зрения, для конкретного изучаемого лекарственного препарата. В одном из вариантов осуществления изобретения, два антигенсвязывающих белка рассматриваются как биоэквивалентные, если нет никаких клинически значимых различий в их безопасности, чистоте и эффективности воздействия.
В одном из вариантов осуществления изобретения, два антигенсвязывающих белка считаются биоэквивалентными, если пациент может один или несколько раз переключаться с приема референсного продукта на прием другого биологического продукта, без ожидаемого увеличения риска развития побочных эффектов, включая клинически значимые изменения в иммуногенности или уменьшение эффективности лечения, по сравнению со случаем лечения без такого переключения.
В одном из вариантов осуществления изобретения, два антигенсвязывающих белка считаются биоэквивалентными, если они оба действуют по общим механизмам, или общие механизмы воздействия на состояние или условия использования являются известными.
Биоэквивалентность может быть продемонстрирована методами оценки in vivo и in vitro. Оценки биоэквивалентности включают, например, (а) испытания in vivo на людях или на других млекопитающих, где измеряется концентрация антитела или его метаболитов в крови, плазме, сыворотке или других биологических жидкостях организма, как функции времени; (b) испытания in vitro, где получают коррелируемые и прогностические данные по биодоступности у человека в условиях in vivo; (с) испытания in vivo на людях или на других млекопитающих, где измеряется соответствующий острый фармакологический эффект от действия антитела (или состояние его мишени) в зависимости от времени; и (d) полностью контролируемое клиническое испытание, где устанавливается безопасность, эффективность, биодоступность или биоэквивалентность антитела.
Биоэквивалентные варианты антител против PCSK9 по изобретению могут быть получены, например, в результате различных замен остатков или последовательностей, или удаления концевых или внутренних остатков или последовательностей, которые не влияют на биологическую активность. Например, остатки цистеина не является существенными для биологической активности, и они могут быть удалены или заменены другими аминокислотами, чтобы предотвратить формирование ненужных или неправильных внутримолекулярных дисульфидных мостиков при денатурации.
ЛЕЧЕНИЕ ПОПУЛЯЦИЙ
Изобретение относится к терапевтическим способам лечения пациентов, которые являются людьми, нуждающимся в получении композиции по изобретению. В то время как изменение образа жизни и традиционное медикаментозное лечение являются часто успешными при снижении уровня холестерина, не все пациенты способны достичь рекомендуемых целевых уровней холестерина при таких подходах. Различные патологические состояния, например, семейная гиперхолестеринемия (FH), по-видимому, устойчивы к снижению уровней LDL-C, несмотря на активное использование обычной терапии. Гомозиготная и гетерозиготная семейные гиперхолестеринемии (hoFH, heFH) представляют собой патологические состояния, связанные с преждевременным атеросклеротическим сосудистым заболеванием. Тем не менее, пациенты с диагнозом hoFH в значительной степени не реагируют на обычное медикаментозное лечение и получают ограниченные варианты лечения. В частности, лечение статинами, которые снижают уровни LDL-C путем ингибирования синтеза холестерина и положительной регуляции рецепторов LDL, может оказать незначительное влияние на пациентов, у которых рецепторы LDL являются слабоактивными или дефективными. Среднее снижение уровней LDL-C составляет величину только менее приблизительно 20%, как было недавно сообщено в отношении пациентов с подтвержденным генотипом hoFH, которым вводили максимальные дозы статинов. Добавление эзетимиба в количестве 10 мг/день к этому режиму лечения, привело к снижению уровней общего LDL-C на 27%, что далеко от оптимального уровня. Кроме того, многие пациенты не отвечают на лечение статинами, имеют заболевания, которые контролируются терапией статинами, или не могут переносить лечение статинами; в общем, в отношении таких пациентов нет возможности контроля уровней холестерина, используя альтернативные способы лечения. Таким образом, существует большая неудовлетворенная медицинская потребность в новых способах лечения, которые могут устранить недостатки имеющихся вариантов способов лечения.
Конкретные популяции пациентов, которые можно лечить с помощью терапевтических способов по изобретению, включают индивидов, которым назначен LDL аферез, индивидов с мутациями, активирующими PCSK9 (увеличенная функция мутации, "GOF"), индивидов с первичной гиперхолестеринемией, у которых имеется непереносимость статинов или на которых не действуют статины; и индивидов, подверженных риску развития гиперхолестеринемии, которые могли получать ранее профилактическое лечение. Другие показания включают гиперлипидемию и дислипидемию, особенно когда они связаны со вторичными причинами заболевания, такими как сахарный диабет типа 2, холестатическое заболевание печени (первичный билиарный цирроз), нефротический синдром, гипотиреоз, ожирение, а также профилактику и лечение атеросклероза и сердечно-сосудистых заболеваний. Однако, в зависимости от тяжести вышеупомянутых заболеваний и состояний, лечение пациентов антителами и антигенсвязывающими фрагментами по изобретению может быть противопоказано для некоторых заболеваний и состояний.
ТЕРАПЕВТИЧЕСКИЕ СОСТАВЫ И ИХ ВВЕДЕНИЕ
Настоящее изобретение относится к терапевтическим композициям, содержащим антитела против PCSK9 или их антигенсвязывающие фрагменты по настоящему изобретению. Терапевтические композиции в соответствии с изобретением могут быть введены с подходящими носителями, эксципиентами и другими средствами, которые включаются в составы для обеспечения улучшенного перевода, доставки, переносимости и т.п. Множество подходящих составов можно найти в фармацевтическом справочнике, известном всем фармацевтам: Remington′s Pharmaceutical Sciences, Mack Publishing Company, Easton, PA. Такие композиции включают, например, порошки, пасты, мази, гели, воски, масла, жиры, липидсодержащие везикулы (катионные или анионные, например, LIPOFECTIN™), ДНК-конъюгаты, безводные поглощающие пасты, эмульсии масло-в-воде и вода-в-масле, эмульсии на основе карбовакса (полиэтиленгликоли различной молекулярной массы), полутвердые гели и полутвердые смеси, содержащие карбовакс. Смотрите также Powell et al. "Compendium of excipients for parenteral formulations" PDA (1998) J Pharm Sci Technol 52:238-311.
Доза может варьироваться в зависимости от возраста и размеров индивида, который будет подвергаться лечению, от вида заболевания, подлежащего лечению, от состояния индивида, от пути введения и т.п. Когда антитело по настоящему изобретению используют для лечения различных состояний и заболеваний, связанных с PCSK9, в том числе для лечения гиперхолестеринемии, расстройств, связанных с LDL и аполипопротеином В, нарушения липидного метаболизма и т.п., у взрослого пациента, предпочтительно, когда антитело по настоящему изобретению вводят внутривенно в разовой дозе обычно от приблизительно 0,01 мг/кг до приблизительно 20 мг/кг массы тела, более предпочтительно, от приблизительно 0,02 мг/кг до приблизительно 7 мг/кг, от приблизительно 0,03 мг/кг до приблизительно 5 мг/кг, или от приблизительно 0,05 мг/кг до приблизительно 3 мг/кг массы тела. В зависимости от тяжести состояния, частота и длительность лечения могут быть скорректированы.
Известны и могут быть использованы для введения фармацевтической композиции по изобретению различные системы доставки, например, инкапсулирование в липосомы, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать мутантные вирусы, рецептор-опосредованный эндоцитоз (смотрите, например, Wu et al. (1987) J. Biol. Chem. 262:4429-4432). Способы введения включают, но без ограничения перечисленным, внутрикожное введение, внутримышечное введение, внутрибрюшинное введение, внутривенное введение, подкожное введение, интраназальное введение, эпидуральное введение, а также оральный или пероральный пути введения. Если антитело по изобретению вводят путем инъекции, то предпочтительным является подкожное введение. Для ингибитора HMG-CoA, например, статина, предпочтительным является оральное введение или пероральное введение. Композицию можно вводить любым удобным способом, например, путем инфузии или болюсной инъекции, путем абсорбции через эпителиальный или кожно-слизистый слой (например, через слизистую оболочку полости рта, ректальную слизистую оболочку и слизистую оболочку кишечника, и т.д.), и могут быть введены вместе с другими биологически активными агентами. Введение может быть системным или местным.
Фармацевтическая композиция может доставляться в везикуле, в частности, в липосоме (смотрите Langer (1990) Science 249:1527-1533; Treat et al. (1989) in Liposomes in the Therapy of Infectious Disease and Cancer, Lopez Berestein and Fidler (eds.), Liss, New York, pp. 353-365; Lopez-Berestein, pp. 317-327, там же; а также смотрите весь документ).
Фармацевтическая композиция, в определенных ситуациях, может быть доставлена с помощью системы с контролируемым высвобождением. В одном из вариантов можно использовать насос (Langer, смотрите выше;. Sefton (1987) CRC Crit. Ref. Biomed. Eng. 14:201). В другом варианте осуществления изобретения, могут быть использованы полимерные материалы, смотрите Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Florida (1974). В еще одном варианте осуществления изобретения, система с контролируемым высвобождением может быть размещена в непосредственной близости у цели, в отношении которой применяется композиция, и, таким образом, в этом случае, требуется только часть системной дозы (например, Goodson, Medical Applications of Controlled Release, vol. 2, pp. 115-138, 1984, см. выше).
Составы для инъекций могут включать дозированные формы для внутривенного, подкожного, внутрикожного и внутримышечных инъекций, капельных вливаний и т.д. Эти препараты для инъекций могут быть получены общеизвестными способами. В частности, препараты для инъекций могут быть получены, например, путем растворения, суспендирования или эмульгирования антитела или его соли, как описано выше, в стерильной водной среде или в масляной среде, которые обычно используют для инъекций. В качестве водной среды для инъекций применяют, например, физиологический раствор, изотонический раствор, содержащий глюкозу и другие вспомогательные средства, и т.п., которые могут быть использованы в сочетании с соответствующим солюбилизирующим средством, таким как спирт (например, этанол), многоатомный спирт (например, пропиленгликоль, полиэтиленгликоль), неионогенное поверхностно-активное вещество [например, полисорбат 80, НСО-50 (аддукт полиоксиэтилена (50 моль) и гидрированного касторового масла)], и т.п. В качестве масляной среды используют, например, кунжутное масло, соевое масло и т.п., которые могут быть использованы в сочетании с солюбилизирующим средством, таким как бензилбензоат, бензиловый спирт и т.п. Препараты для инъекции, полученные таким образом, предпочтительно, расфасовывают в соответствующие ампулы. Фармацевтическая композиция по настоящему изобретению может быть введена подкожно или внутривенно с использованием стандартной иглы и шприца. Кроме того, для подкожного введения фармацевтической композиции по настоящему изобретению, может быть использовано готовое для применения устройство типа ручки. Такое устройство для доставки типа ручки может быть многоразовым или одноразовым. В многоразовом устройстве для доставки типа ручки обычно используется сменный картридж, содержащий фармацевтическую композицию. После того как вся фармацевтическая композиция в картридже для введения израсходована и картридж становится пустым, пустой картридж можно легко снять и заменить новым картриджем, который содержит фармацевтическую композицию. Устройство для доставки типа ручки может использоваться повторно. В одноразовом устройстве для доставки типа ручки нет сменного картриджа. Как правило, одноразовое устройство для доставки типа ручка поставляется заполненным фармацевтической композицией, находящейся в резервуаре внутри устройства. Когда резервуар освобождается от фармацевтической композиции, все устройство выбрасывают.
Различные устройства типа ручки многоразового использования и автоинъекторные устройства могут быть применены для подкожной доставки фармацевтической композиции по настоящему изобретению. Примеры включают, но конкретно не ограничиваются перечисленным, AUTOPEN™ (Owen Mumford, Inc., Woodstock, UK), DISETRONIC™ Pen (Disetronic Medical Systems, Burghdorf, Switzerland), HUMALOG MIX 75/25™ Pen, HUMALOG™ Pen, HUMALIN 70/30™ Pen (Eli Lilly and Co., Indianapolis, IN), NOVOPEN™ I, II and III (Novo Nordisk, Copenhagen, Denmark), NOVOPEN JUNIOR™ (Novo Nordisk, Copenhagen, Denmark), BD™ Pen (Becton Dickinson, Franklin Lakes, NJ), OPTIPEN™, OPTIPEN PRO™, OPTIPEN STARLET™ и OPTICLIK™ (Sanofi-Aventis, Frankfurt, Germany), которые являются только некоторыми из них. Примеры одноразовых устройств для доставки типа ручки, которые могут быть применены для подкожной доставки фармацевтической композиции по настоящему изобретению, включают, но конкретно не ограничиваются перечисленным, SOLOSTAR™ Pen (Sanofi-Aventis), FLEXPEN™ (Novo Nordisk) и KWIKPEN™ (Eli Lilly).
Предпочтительно, когда фармацевтические композиции для перорального или парентерального применения, как описано выше, получают как лекарственные средства в виде лекарственной формы, соответствующей дозе активных ингредиентов. Такие лекарственные средства в виде лекарственной формы включают, например, таблетки, пилюли, капсулы, растворы для инъекций (ампулы), суппозитории и т.п. Количество вышеуказанного антитела обычно составляет от приблизительно 4 мг до приблизительно 500 мг или от приблизительно 5 мг до приблизительно 500 мг на одну единичную дозу лекарственного средства, особенно в случае раствора для инъекций; предпочтительно, когда вышеуказанные антитела содержатся в количестве от приблизительно 5 мг до приблизительно 100 мг или от приблизительно 5 мг до 400 мг (например, от приблизительно 50 мг до приблизительно 200 мг на 1 мл раствора для инъекций) и от приблизительно 10 мг до приблизительно 250 мг или приблизительно 500 мг для других дозированных форм.
Настоящее изобретение относится к терапевтическим способам, где антитело или фрагмент антитела по изобретению является полезным для лечения гиперхолестеринемии, связанной с различными состояниями, в которые вовлечен hPCSK9. Антитела против PCSK9 или фрагменты антител по изобретению являются особенно полезными для лечения гиперхолестеринемии и т.п. Комбинированная терапия может включать антитела против PCSK9 по изобретению и, например, один или несколько из числа любых агентов, которые (1) индуцируют клеточное истощение синтеза холестерина путем ингибирования редуктазы 3-гидрокси-3-метилглутарил-кофермента А (HMG-CoA), и представляют собой, например, церивастатин, аторвастатин, симвастатин, питавастатин, розувастатин, флувастатин, ловастатин и правастатин; (2) ингибируют поглощение холестерина и/или ингибируют повторное поглощение желчных кислот; (3) увеличивают катаболизм липопротеинов (например, ниацин) и активируют фактор транскрипции LXR, который играет важную роль в элиминации холестерина, такого как 22-гидроксихолестерина, или представляют собой фиксированную комбинацию, например, комбинацию эзетимиба и симвастатина; комбинацию статина с желчными смолами (например, холестирамин, колестипол, колесевелам), фиксированную комбинацию ниацина и статина (например, комбинацию ниацина с ловастатином), или с другими гиполипидемическими средствами, например, таким, как этиловые эфиры омега-3-жирных кислот (например, омакор).
ПРЕДПОЧТИТЕЛЬНЫЕ АСПЕКТЫ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Далее будут указаны некоторые предпочтительные аспекты и варианты осуществления настоящего изобретения
А - АСПЕКТЫ, СВЯЗАННЫЕ С ПОПУЛЯЦИЯМИ ПАЦИЕНТОВ
1. Способ лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, включающий
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом,
где индивид, нуждающийся в этом, входит в одну или несколько из следующих групп индивидов:
(i) индивиды, имеющие уровень LDL холестерина (LDL-C) в сыворотке не менее 100 мг/дл, [по меньшей мере 130 мг/дл, по меньшей мере 160 мг/дл, по меньшей мере 200 мг/дл];
(ii) индивиды, имеющие, имеющие уровни HDL-C в сыворотке менее 40 мг/дл;
(iii) индивиды, имеющие уровень холестерина в сыворотке по меньшей мере 200 мг/дл [240 мг/дл];
(iv) индивиды, имеющие уровень триглицеридов в сыворотке по меньшей мере 150 мг/дл [по меньшей мере 200 мг/дл, по меньшей мере, 500 мг/дл], где указанный уровень триглицеридов определяется после голодания в течение по меньшей мере 8 часов;
(v) индивиды в возрасте по меньшей мере 35 лет [в возрасте по меньшей мере 40/50/55/60/65/70 лет];
(vi) индивиды в возрасте до 75 лет [65/60/55/50/45/40 лет];
(vii) индивиды, имеющих BMI от 25 [26/27/28/29/30/31/32/33/34/35/36/37/38/39] или более;
(viii) индивиды мужского пола;
(ix) индивиды женского пола;
(х) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 30 мг/дл, [40 ммоль/л, 50 мг/л, 60 мг/дл, 70 мг/дл] по сравнению с уровнем до введения дозы; или
(xi) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 20% [30%, 40%, 50%, 60%] по сравнению с уровнем до введения дозы.
2. Способ лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, включающий
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом,
где индивид, нуждающийся в этом, не входит в одну или несколько из следующих групп индивидов:
(i) курильщики;
(ii) лица в возрасте 70 лет и старше;
(iii) индивиды, страдающие от гипертензии;
(iv) беременные женщины;
(v) женщины, пытающиеся забеременеть;
(vi) женщины, которые кормят грудью;
(vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(ix) лица, которые употребляют чрезмерное количество алкоголя;
(х) лица, имеющие проблемы с почками;
(xi) лица, страдающие гипотиреозом;
(xii) лица, страдающие мышечными расстройствами;
(xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xiv) лица, имеющие серьезные проблемы с дыханием;
(xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xvi) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xvii) лица, имеющие индекс массы тела (BMI) более 40;
(xviii) лица, имеющие индекс массы тела (BMI) менее 18;
(xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xx) лица, имеющие положительную реакцию на гепатит В или С;
(xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
3. Антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент предназначен для введения индивиду, который входит по меньшей мере в одну из следующих групп индивидов:
(i) индивиды, имеющие уровень LDL холестерина (LDL-C) в сыворотке не менее 100 мг/дл, [по меньшей мере 130 мг/дл, по меньшей мере 160 мг/дл, по меньшей мере 200 мг/дл];
(ii) индивиды, имеющие уровни HDL-C в сыворотке менее 40 мг/дл;
(iii) индивиды, имеющие уровень холестерина в сыворотке по меньшей мере 200 мг/дл [240 мг/дл];
(iv) индивиды, имеющие уровень триглицеридов в сыворотке по меньшей мере 150 мг/дл [по меньшей мере 200 мг/дл, по меньшей мере, 500 мг/дл], где указанный уровень триглицеридов определяется после голодания в течение по меньшей мере 8 часов;
(v) индивиды в возрасте по меньшей мере 35 лет [в возрасте по меньшей мере 40/50/55/60/65/70 лет];
(vi) индивиды в возрасте до 75 лет [65/60/55/50/45/40 лет];
(vii) индивиды, имеющих BMI от 25 [26/27/28/29/30/31/32/33/34/35/36/37/38/39] или более;
(viii) индивиды мужского пола;
(ix) индивиды женского пола;
(х) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 20 мг/дл [30 мг/дл, 40 мг/дл, 50 мг/дл, 60 мг/дл, 70 мг/дл]; или
(xi) индивиды, у которых введение указанного антитела или его антигенсвязывающего фрагмента приводит к снижению уровня LDL-С в сыворотке по меньшей мере на 10% [20%, 30%, 40%, 50%, 60%].
4. Антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент предназначен для введения индивиду, который не входит в одну или несколько из следующих групп индивидов:
(i) курильщики;
(ii) лица в возрасте 70 лет и старше;
(iii) индивиды, страдающие от гипертензии;
(iv) беременные женщины;
(v) женщины, пытающиеся забеременеть;
(vi) женщины, которые кормят грудью;
(vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(ix) лица, которые употребляют чрезмерное количество алкоголя;
(х) лица, имеющие проблемы с почками;
(xi) лица, страдающие гипотиреозом;
(xii) лица, страдающие мышечными расстройствами;
(xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xiv) лица, имеющие серьезные проблемы с дыханием;
(xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xvi) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xvii) лица, имеющие индекс массы тела (BMI) более 40;
(xviii) лица, имеющие индекс массы тела (BMI) менее 18;
(xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xx) лица, имеющие положительную реакцию на гепатит В или С;
(xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
5. Способ по аспекту 1 или 2, или антитело по аспекту 2 или 3, где заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
6. Способ или антитело по любому из аспектов 1-5, где заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбирают из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
7. Способ или антитело по любому из аспектов 1-6, где индивид, нуждающийся в таком лечении, является индивидом, которому назначен LDL аферез, индивидом с мутациями, активирующими PCSK9, индивидом с гетерозиготной семейной гиперхолестеринемией, индивидом с первичной гиперхолестеринемией, которая не контролируется статинами, индивидом с риском развития гиперхолестеринемии, индивидом с гиперхолестеринемией, индивидом с гиперлипидемией, индивидом с дислипидемией, индивидом с атеросклерозом или индивидом с сердечно-сосудистыми заболеваниями.
8. Способ или антитело по любому из аспектов 1-7, где антитело или его антигенсвязывающий фрагмент представляет собой рекомбинантное человеческое антитело или его фрагмент.
9. Способ или антитело по любому из аспектов 1-8, где антитело или его антигенсвязывающий фрагмент характеризуется одним или несколькими признаками из следующего:
(i) способностью снижать уровень общего холестерина в сыворотке по меньшей мере на от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней;
(ii) способностью снижать уровень LDL холестерина в сыворотке по меньшей мере приблизительно на 65-80%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней;
(iii) способностью снижать уровень триглицеридов в сыворотке, по меньшей мере приблизительно на 25-40%, по сравнению с уровнем до введения дозы;
(iv) достигать одного или нескольких признаков (i)-(iii), не снижая уровня сывороточного HDL холестерина, или снижать уровень сывороточного HDL холестерина не более чем на 5%, по сравнению с уровнем до введения дозы;
(v) достигать одного или нескольких признаков (i)-(iii), при небольшом или нерегистрируемом эффекте на функцию печени, по измерению ALT и AST.
10. Способ или антитело по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент содержит:
- домен CDR3 тяжелой цепи (HCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 8, 32, 56, 80, 104, 128, 152, 176, 200, 224, 248, 272, 296, 320, 344, 368, 392, 416, 440, 464, 488, 512, 536, 560, 584, 608, 632, 656, 680, 704 и 728, и
- домен CDR3 легкой цепи (LCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 16, 40, 64, 88, 112, 136, 160, 184, 208, 232, 256, 280, 304, 328, 352, 376, 400, 424, 448, 472, 496, 520, 544, 568, 592, 616, 639, 664, 688, 712 и 736.
11. Способ или антитело по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из пары аминокислотной последовательности HCVR/LCVR, как показано в SEQ ID NO: 90/92.
12. Способ или антитело по аспекту 11, где антитело или его антигенсвязывающий фрагмент содердит CDR тяжелой цепи и CDR легкой цепи, как показано в последовательностях SEQ ID NO: 76, 78, 80, 84, 86 и 88.
13. Способ или антитело по аспекту 12, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность HCVR, как показано в последовательности SEQ ID NO:90, и аминокислотную последовательность LCVR, как показано в последовательности SEQ ID NO:92.
14. Способ или антитело по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент связывает тот же самый эпитоп на hPCSK9 как и антитело, содержащее аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88.
15. Способ или антитело по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом, содержащим аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88.
16. Способ или антитело по любому из аспектов 1-15, дополнительно включающие:
введение терапевтического количества ингибитора HMG-CoA-редуктазы индивиду в дозе от 0,05 мг до 100 мг.
17. Способ или антитело по аспекту 16, где ингибитор HMG-CoA редуктазы представляет собой статин.
18. Способ или антитело по аспекту 17, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
19. Способ или антитело по аспекту 18, где статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг.
20. Изделие, содержащее:
(а) упаковку;
(b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9; и
(c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, и дополнительно указано, что можно лечить индивидов, входящих в одну или несколько групп индивидов, указанных в аспекте 1.
21. Изделие, содержащее:
(а) упаковку;
(b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9; и
(c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, и дополнительно указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом противопоказано для пациентов, принадлежащих к одной или нескольким группам индивидов, указанных в аспекте 2.
22. Изделие по аспекту 20 или 21, где антитело или его антигенсвязывающий фрагмент представляет собой антитело или его антигенсвязывающий фрагмент, как указано в любом из аспектов 3-19.
23. Изделие по любому из аспектов 20-22, где этикетка или вкладыш в упаковку содержит указание о способе лечения по любому из аспектов 1, 2 или 5-19.
24. Способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл; и
определение эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C по меньшей мере на 25%, по отношению к уровню перед введением дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
где каждый пациент входит в одну или несколько групп индивидов, указанных в аспекте 1.
25. Способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
определение эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, где снижение уровня LDL-C, по меньшей мере на 25%, по сравнению с уровнем до введения дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов;
где каждый пациент входит в одну или несколько групп индивидов, указанных в аспекте 1.
26. Способ по аспекту 25, где каждый пациент в указанной популяции получал гиполипидемическое лечение путем введения статина в течение по меньшей мере 6 недель перед лечением указанным антителом или его антигенсвязывающим фрагментом.
27. Способ по любому из аспектов 24-26, где антитело или его антигенсвязывающий фрагмент представляют собой антитело или его антигенсвязывающий фрагмент, как определено в любом из аспектов 3-19.
28. Способ по любому из аспектов 24-27, где выбранная популяция пациентов подвергается лечению или была подвергнута лечению в соответствии со способом лечения по любому из аспектов 1, 2 или 5-19.
29. Способ испытания эффективности соединения по снижению уровней холестерина у индивида, где способ включает следующие стадии:
(a) предоставление грызуна;
(b) введение грызуну антитела или его антигенсвязывающего фрагмента, который специфически связывает PCSK9;
(c) введение указанному грызуну испытуемого соединения;
(d) определение эффекта испытуемого соединения у грызуна, где снижение уровня холестерина у грызуна, по сравнению с уровнем холестерина у контрольного животного, означает, что испытуемое соединение эффективно для снижения уровней холестерина у индивида, при этом контрольное животное принадлежит к тому же самому виду, как и указанный грызун, и контрольное животное не подвергалось воздействию испытуемого соединения.
В - АСПЕКТЫ, СВЯЗАННЫЕ С ПОПУЛЯЦИЯМИ ПАЦИЕНТОВ
1. Способ лечения индивида, страдающего заболеванием или расстройством, которое характеризуется повышенными уровнями холестерина, относящегося к липопротеинам низкой плотности (LDL-C), где способ включает:
(а) выбор индивида с уровнем LDL-C в крови выше 100 мг/дл, и
(b) введение указанному индивиду композиции, содержащей антитело или его антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающемуся в этом.
2. Способ по аспекту 1, где заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
3. Способ по аспекту 1, где заболевание или состояние представляет собой первичную гиперхолестеринемию или семейную гиперхолестеринемию.
4. Способ по аспекту 1, где заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
5. Способ по аспекту 1, где индивид имеет индекс массы тела (BMI) менее 18 кг/м2 или более 40 кг/м2.
6. Способ по аспекту 1, где индивид ранее не получал указаний находиться на диете по снижению уровня холестерина.
7. Способ по аспекту 1, где индивид ранее не принимал лекарственных средств для снижения уровня холестерина, за исключением аторвастатина.
8. Способ по аспекту 7, где аторвастатин принимался индивидом в количестве приблизительно 10 мг в день.
9. Способ по аспекту 7, где лекарственное средство для снижения уровня холестерина выбрано из группы, состоящей из фибратов, смол желчных кислот, ниацина, блокаторов кишечной абсорбции холестерина (ICA) и омега-3 жирных кислот.
10. Способ по аспекту 9, где ниацин принимается в дозе более 500 мг в день.
11. Способ по аспекту 9, где омега-3 жирные кислоты принимаются в дозе более 1000 мг в день.
12. Способ по аспекту 1, где индивид не страдает от диабета.
13. Способ по аспекту 12, где диабет является диабетом типа 1.
14. Способ по аспекту 12, где диабет является диабетом типа 2.
15. Способ по аспекту 12, где диабет типа 2 лечится инсулином.
16. Способ по аспекту 12, где индивид имеет показатель концентрации гликозилированного гемоглобина в крови, более или равный 8,5%.
17. Способ по аспекту 1, где индивид является отрицательным на поверхностный антиген гепатита В и гепатита С.
18. Способ по аспекту 1, где индивид имеет концентрацию триглицеридов в крови более чем 350 мг/дл.
19. Способ по аспекту 1, где индивид имеет концентрацию нейтрофилов менее 1500 на кубический мм крови.
20. Способ по аспекту 1, где индивид имеет концентрацию тромбоцитов менее 100000 на кубический мм крови.
21. Способ по аспекту 1, где индивидом является женщина.
22. Способ по аспекту 21, где индивидом является не беременная женщина.
23. Способ по аспекту 1, где индивид имеет концентрацию тиреотропного гормона в крови выше нижней границы нормы и ниже верхней границы нормы.
24. Способ по аспекту 23, где индивид имеет показатель креатина в сыворотке менее 1,4 от верхней границы нормы.
25. Способ по аспекту 1, где индивид является мужчиной.
26. Способ по аспекту 25, где индивид имеет показатель креатина в сыворотке менее 1,5 от верхней границы нормы.
27. Способ по аспекту 1, где индивид имеет показатель количества аспартаттрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
28. Способ по аспекту 1, где индивид имеет показатель количества аланинтрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
29. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 5 мг до приблизительно 500 мг.
30. Способ по аспекту 29, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
31. Способ по аспекту 29, где антитело вводят в количестве от 200 мг до 300 мг каждые четыре недели.
32. Способ по аспекту 29, где антитело или его антигенсвязывающий фрагмент вводят в дозе приблизительно 150 мг.
33. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
34. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
35. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
36. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
37. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
38. Способ по аспекту 1, где антитело вводят подкожно.
39. Способ по аспекту 38, где антитело вводят в брюшную полость.
40. Способ по аспекту 1, дополнительно включающий введение индивиду ингибитора HMG-CoA-редуктазы.
41. Способ по аспекту 40, где ингибитор HMG-CoA-редуктазы вводят в дозе приблизительно от 0,05 мг до 100 мг.
42. Способ по аспекту 41, где ингибитором HMG-CoA-редуктазы является статин.
43. Способ по аспекту 42, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
44. Способ по аспекту 42, где статин представляет собой аторвастатин, который вводят в дозе 10 мг или 80 мг.
45. Способ по аспекту 44, где аторвастатин вводят в количестве приблизительно 10 мг в день и 80 мг в день в течение 8 недель.
46. Способ снижения уровней холестерина у индивида, нуждающегося в этом, где способ включает:
(а) выбор индивида с уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), в крови более 100 мг/дл; и
(b) введение указанному индивиду композиции, содержащей антитело или его антигенсвязывающий фрагмент, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9); снижая, тем самым, уровни холестерина у индивида, нуждающегося в этом.
47. Способ по аспекту 46, где заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
48. Способ по аспекту 46, где заболевание или состояние является первичной гиперхолестеринемией или семейной гиперхолестеринемией.
49. Способ по аспекту 46, где заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
50. Способ по аспекту 46, где индивид имеет индекс массы тела (BMI) менее 18 кг/м2 или более 40 кг/м2.
51. Способ по аспекту 46, где индивид ранее не получал указаний находиться на диете по снижению уровня холестерина.
52. Способ по аспекту 46, где индивид ранее не принимал лекарственных средств для снижения уровня холестерина, за исключением аторвастатина.
53. Способ по аспекту 52, где аторвастатин принимался индивидом в количестве приблизительно 10 мг в день.
54. Способ по аспекту 52, где лекарственное средство для снижения уровня холестерина выбрано из группы, состоящей из фибратов, смол желчных кислот, ниацина, блокаторов кишечной абсорбции холестерина (ICA) и омега-3 жирных кислот.
55. Способ по аспекту 54, где ниацин принимается в дозе более 500 мг в день.
56. Способ по аспекту 54, где омега-3 жирные кислоты принимаются в дозе более 1000 мг в день.
57. Способ по аспекту 46, где индивид не страдает от диабета.
58. Способ по аспекту 57, где диабет является диабетом типа 1.
59. Способ по аспекту 57, где диабет является диабетом типа 2.
60. Способ по аспекту 57, где диабет типа 2 лечится инсулином.
61. Способ по аспекту 57, где индивид имеет показатель концентрации гликозилированного гемоглобина в крови, более или равный 8,5%.
62. Способ по аспекту 46, где индивид является отрицательным на поверхностный антиген гепатита В и гепатита С.
63. Способ по аспекту 46, где индивид имеет концентрацию триглицеридов в крови более чем 350 мг/дл.
64. Способ по аспекту 46, где индивид имеет концентрацию нейтрофилов менее 1500 на кубический мм крови.
65. Способ по аспекту 46, где индивид имеет концентрацию тромбоцитов менее 100000 на кубический мм крови.
66. Способ по аспекту 46, где индивидом является женщина.
67. Способ по аспекту 66, где индивидом является не беременная женщина.
68. Способ по аспекту 46, где индивид имеет концентрацию тиреотропного гормона в крови выше нижней границы нормы и ниже верхней границы нормы.
69. Способ по аспекту 68, где индивид имеет показатель креатина в сыворотке менее 1,4 от верхней границы нормы.
70. Способ по аспекту 46, где индивид является мужчиной.
71. Способ по аспекту 70, где индивид имеет показатель креатина в сыворотке менее 1,5 от верхней границы нормы.
72. Способ по аспекту 46, где индивид имеет показатель количества аспартаттрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
73. Способ по аспекту 46, индивид имеет показатель количества аланинтрансаминазы, который не превышает двукратного показателя, соответствующего верхней границе нормы.
74. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 5 мг до приблизительно 500 мг.
75. Способ по аспекту 74, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
76. Способ по аспекту 74, где антитело вводят в количестве от 200 мг до 300 мг каждые четыре недели.
77. Способ по аспекту 74, где антитело или его антигенсвязывающий фрагмент вводят в дозе приблизительно 150 мг.
78. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
79. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
80. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
81. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
82. Способ по аспекту 46, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
83. Способ по аспекту 46, где антитело вводят подкожно.
84. Способ по аспекту 38, где антитело вводят в брюшную полость.
85. Способ по аспекту 46, дополнительно включающий введение индивиду ингибитора HMG-CoA-редуктазы.
86. Способ по аспекту 85, где ингибитор HMG-CoA редуктазы вводят в дозе от приблизительно 0,05 мг до 100 мг.
87. Способ по аспекту 86, где ингибитор HMG-CoA-редуктазы представляет собой статин.
88. Способ по аспекту 87, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
89. Способ по аспекту 88, где статин является аторвастатином, который вводят в дозе 10 мг или 80 мг.
90. Способ по аспекту 89, где аторвастатин вводят в количестве приблизительно 10 мг в день и 80 мг в день в течение 8 недель.
А - АСПЕКТЫ, СВЯЗАННЫЕ С РЕЖИМАМИ ДОЗИРОВАНИЯ
1. Способ лечения заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
2. Антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) для применения при лечении заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9,
где антитело или его антигенсвязывающий фрагмент предназначен для введения в дозе в количестве от 5 мг до 500 мг,
где антитело или его антигенсвязывающий фрагмент дополнительно предназначен для введения в комбинации с ингибитором HMG-CoA-редуктазы в дозе в количестве от 0,05 мг до 100 мг.
3. Способ по аспекту 1 или антитело по аспекту 2, где заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, облегчается, улучшается, ингибируется или предотвращается за счет воздействия антагониста PCSK9.
4. Способ или антитело по любому из аспектов 1-3, где заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, выбирают из группы, состоящей из:
гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
5. Способ или антитело по любому из аспектов 1-4, где индивид, нуждающийся в таком лечении, является индивидом, которому назначен LDL аферез, индивидом с мутациями, активирующими PCSK9, индивидом с гетерозиготной семейной гиперхолестеринемией, индивидом с первичной гиперхолестеринемией, которая не контролируется статинами, индивидом с риском развития гиперхолестеринемии, индивидом с гиперхолестеринемией, индивидом с гиперлипидемией, индивидом с дислипидемией, индивидом с атеросклерозом или индивидом с сердечно-сосудистыми заболеваниями.
6. Способ или антитело по любому из аспектов 1-5, где ингибитор HMG-CoA-редуктазы вводят три раза в день, два раза в день или один раз в день.
7. Способ или антитело по любому из аспектов 1-6, где ингибитор HMG-CoA-редуктазы вводится каждый день, через день, каждый третий день, каждый четвертый день, каждый пятый день или каждый шестой день.
8. Способ или антитело по любому из аспектов 1-6, где ингибитор HMG-CoA-редуктазы вводят один раз в неделю, один раз в две недели, каждую третью неделю или один раз в четыре недели.
9. Способ или антитело по любому из аспектов 1-8, где ингибитор HMG-CoA-редуктазы вводят утром, в полдень или вечером.
10. Способ или антитело по любому из аспектов 1-9, где ингибитор HMG-CoA редуктазы представляет собой статин.
11. Способ или антитело по аспекту 10, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
12. Способ или антитело по аспекту 11, где статин представляет собой:
- церивастатин, который вводят в суточной дозе от 0,05 мг до 2 мг;
- аторвастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- симвастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- питавастатин, который вводят в суточной дозе от 0,2 мг до 100 мг;
- розувастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- флувастатин, который вводят в суточной дозе от 2 мг до 100 мг;
- ловастатин, который вводят в суточной дозе от 2 мг до 100 мг; или
- правастатин, который вводят в суточной дозе от 2 мг до 100 мг.
13. Способ или антитело по любому из аспектов 1-12, где антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели.
14. Способ или антитело по любому из аспектов 1-13, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 50 мг до 300 мг.
15. Способ или антитело по любому из аспектов 1-14, где антитело или его антигенсвязывающий фрагмент представляет собой рекомбинантное человеческое антитело или его фрагмент.
16. Способ или антитело по любому из аспектов 1-15, где антитело или его антигенсвязывающий фрагмент характеризуется одним или несколькими признаками из следующего:
(i) способностью снижать уровень общего холестерина в сыворотке по меньшей мере на от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней;
(ii) способностью снижать уровень LDL холестерина в сыворотке по меньшей мере приблизительно на 65-80%, по сравнению с уровнем до введения дозы, и поддерживать это снижение по меньшей мере в течение 24 дней;
(iii) способностью снижать уровень триглицеридов, по меньшей мере приблизительно на 25-40%, по сравнению с уровнем до введения дозы;
(iv) достигать одного или нескольких признаков (i)-(iii), не снижая уровня сывороточного HDL холестерина, или снижать уровень сывороточного HDL холестерина не более чем на 5%, по сравнению с уровнем до введения дозы;
(v) достигать одного или нескольких признаков (i)-(iii), при небольшом или нерегистрируемом эффекте на функцию печени, по измерению ALT и AST.
17. Способ или антитело по любому из аспектов 1-16, где антитело или антигенсвязывающий фрагмент содержит:
- домен CDR3 тяжелой цепи (HCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 8, 32, 56, 80, 104, 128, 152, 176, 200, 224, 248, 272, 296, 320, 344, 368, 392, 416, 440, 464, 488, 512, 536, 560, 584, 608, 632, 656, 680, 704 и 728, и
- домен CDR3 легкой цепи (LCDR3), выбранный из группы, состоящей из последовательностей SEQ ID NO: 16, 40, 64, 88, 112, 136, 160, 184, 208, 232, 256, 280, 304, 328, 352, 376, 400, 424, 448, 472, 496, 520, 544, 568, 592, 616, 639, 664, 688, 712 и 736.
18. Способ или антитело по любому из аспектов 1-16, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из пары аминокислотной последовательности HCVR/LCVR, как показано в SEQ ID NO: 90/92.
19. Способ или антитело по аспекту 18, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи, как показано в последовательностях SEQ ID NO: 76, 78, 80, 84, 86 и 88.
20. Способ или антитело по аспекту 19, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность HCVR, как показано в последовательности SEQ ID NO: 90, и аминокислотную последовательность LCVR, как показано в последовательности SEQ ID NO: 92.
21. Способ или антитело по любому из аспектов 1-16, где антитело или его антигенсвязывающий фрагмент связывает тот же самый эпитоп на hPCSK9 как и антитело, содержащее аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88.
22. Способ или антитело по любому из аспектов 1-16, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом, содержащим аминокислотные последовательности CDR тяжелой цепи и CDR легкой цепи, как показано в SEQ ID NO: 76, 78, 80, 84, 86 и 88.
23. Изделие, содержащее:
(а) упаковку;
(b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9; и
(c) этикетку или вкладыш в упаковку, где указано, что пациенты, получающие лечение указанным антителом или его антигенсвязывающим фрагментом, будут лечить заболевание или состояние, выбранное из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
24. Изделие, содержащее:
(а) упаковку;
(b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9; и
(c) этикетку или вкладыш в упаковку, где указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом осуществляется совместно с применением статина.
25. Изделие, содержащее:
(а) упаковку;
(b) антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9; и
(c) этикетку или вкладыш в упаковку, где указано, что лечение пациентов указанным антителом или его антигенсвязывающим фрагментом вместе со статином противопоказано для пациентов, принадлежащих к одной или нескольким следующим группам:
(i) курильщики;
(ii) лица в возрасте 70 лет и старше;
(iii) лица, страдающие от гипертензии;
(iv) беременные женщины;
(v) женщины, пытающиеся забеременеть;
(vi) женщины, которые кормят грудью;
(vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(ix) лица, которые употребляют чрезмерное количество алкоголя;
(х) лица, имеющие проблемы с почками;
(xi) лица, страдающие гипотиреозом;
(xii) лица, страдающие мышечными расстройствами;
(xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xiv) лица, имеющие серьезные проблемы с дыханием;
(xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xvi) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xvii) лица, имеющие индекс массы тела (BMI) более 40;
(xviii) лица, имеющие индекс массы тела (BMI) менее 18;
(xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xx) лица, имеющие положительную реакцию на гепатит В или С;
(xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
26. Изделие по любому из аспектов 23-25, где антитело или антигенсвязывающий фрагмент представляет собой антитело или его антигенсвязывающий фрагмент, как определено в любом из аспектов 2-22.
27. Изделие по любому из аспектов 23-26, где этикетка или вкладыш в упаковку содержит указание о способе лечения по любому из аспектов 1 или 3-22.
28. Способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
лечение выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл; и
определение эффективности указанного антитела или его антигенсвязывающего фрагмента, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, при этом снижение уровня LDL-C по меньшей мере на 25%, по отношению к уровню перед введением дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
29. Способ испытания эффективности антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9, для лечения заболевания или состояния, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний, где указанный способ включает:
определения эффективности антитела или его антигенсвязывающего фрагмента, который был использован для лечения выбранной популяции пациентов указанным антителом или его антигенсвязывающим фрагментом, где каждый пациент в указанной популяции имеет уровень LDL холестерина (LDL-C) более 100 мг/дл, путем определения уровня LDL-C в популяции пациентов до и после введения указанного антитела или его антигенсвязывающего фрагмента, где снижение уровня LDL-C, по меньшей мере на 25%, по сравнению с уровнем до введения дозы, по меньшей мере у 75% пациентов популяции свидетельствует о том, что указанное антитело или его антигенсвязывающий фрагмент является эффективным для лечения указанного заболевания или состояния в указанной популяции пациентов.
30. Способ по аспекту 28 или 29, где каждый пациент в указанной популяции получал гиполипидемическое лечение путем введения статина в течение по меньшей мере 6 недель перед лечением указанным антителом или его антигенсвязывающим фрагментом.
31. Способ по любому из аспектов 28-30, где антитело или его антигенсвязывающий фрагмент представляют собой антитело или его антигенсвязывающий фрагмент, как определено в любом из аспектов 2-22.
32. Способ по любому из аспектов 28-31, где выбранная популяция пациентов подвергается лечению в соответствии со способом лечения по любому из аспектов 1 или 3-22.
33. Упаковка, содержащая антитело или его антигенсвязывающий фрагмент по любому одному или нескольким аспектам 2-22, и этикетку, где указанная этикетка содержит напечатанные указания, сообщающие пациенту, что лечение антителом вместе со статином показано при одном или нескольким состояниях по аспекту 4.
34. Упаковка, содержащая антитело или его антигенсвязывающий фрагмент по любому одному или нескольким аспектам 2-22, и этикетку, где указанная этикетка содержит напечатанные указания, сообщающие пациенту, что лечение антителом вместе со статином противопоказано для пациентов, принадлежащих к одной или нескольким следующим группам:
(i) курильщики;
(ii) лица в возрасте 70 лет и старше;
(iii) лица, страдающие от гипертензии;
(iv) беременные женщины;
(v) женщины, пытающиеся забеременеть;
(vi) женщины, которые кормят грудью;
(vii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(viii) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(ix) лица, которые употребляют чрезмерное количество алкоголя;
(х) лица, имеющие проблемы с почками;
(xi) лица, страдающие гипотиреозом;
(xii) лица, страдающие мышечными расстройствами;
(xiii) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xiv) лица, имеющие серьезные проблемы с дыханием;
(xv) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xvi) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xvii) лица, имеющие индекс массы тела (BMI) более 40;
(xviii) лица, имеющие индекс массы тела (BMI) менее 18;
(xix) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xx) лица, имеющие положительную реакцию на гепатит В или С;
(xxi) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
35. Способ регулирования уровня LDL в крови, где способ включает:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека) индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
36. Способ предотвращения эффектов (постоянных) увеличенного уровня LDL в крови, включающий:
введение терапевтического количества антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), индивиду, нуждающемуся в этом, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от 5 мг до 500 мг, и
введение терапевтического количества ингибитора HMG-CoA-редуктазы указанному индивиду, где ингибитор HMG-CoA-редуктазы вводят в дозе в диапазоне от 0,05 мг до 100 мг.
37. Способ определения того, что фармацевтическое соединение облегчает, улучшает, ингибирует или предотвращает заболевание или состояние, которое вызывается воздействием экспрессии или активности PCSK9, где способ включает:
(а) введение индивиду соединения, которое специфически связывается с PCSK9, предпочтительно, антитела или его антигенсвязывающего фрагмента, специфически связывающегося с PCSK9, и
(b) определение, какая часть PCSK9 в крови связана с соединением, указанным в (а).
В - АСПЕКТЫ, СВЯЗАННЫЕ С РЕЖИМАМИ ДОЗИРОВАНИЯ
1. Способ лечения индивида, страдающего заболеванием или расстройством, которое характеризуется повышенными уровнями холестерина, относящегося к липопротеинам низкой плотности (LDL-C), где способ включает введение индивиду: (1) антитела или его антигенсвязывающего фрагмента, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9) и (2) ингибитора HMG-CoA редуктазы, где антитело или его антигенсвязывающий фрагмент вводят в дозе в диапазоне от приблизительно 5 мг до приблизительно 500 мг, осуществляя, тем самым, лечение индивида.
2. Способ по аспекту 1, где заболевание или состояние выбрано из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
3. Способ по аспекту 1, где заболевание или состояние представляет собой первичную гиперхолестеринемию или семейную гиперхолестеринемию.
4. Способ по аспекту 1, где заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
5. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
6. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят в дозе приблизительно 150 мг.
7. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
8. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
9. Способ по аспекту 1, где лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
10. Способ по аспекту 1, где лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 65% до приблизительно 80%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
11. Способ по аспекту 1, где лечение снижает уровни триглицеридов в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы.
12. Способ по аспекту 1, где лечение снижает уровень HDL холестерина в сыворотке не более чем на 5%, по сравнению с уровнем до введения дозы.
13. Способ по аспекту 1, где лечение имеет незначительный или не регистрируемый эффект на функцию печени, по измерению ALT и AST.
14. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
15. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
16. Способ по аспекту 1, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
17. Способ по аспекту 1, где ингибитор HMG-CoA редуктазы вводят в дозе в количестве приблизительно от 0,05 мг до 100 мг.
18. Способ по аспекту 1, где ингибитор HMG-CoA редуктазы представляет собой статин.
19. Способ по аспекту 1, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
20. Способ по аспекту 1, где статин представляет собой аторвастатин, который вводят в дозе 10 мг или 80 мг.
21. Способ повышения активности статинов по снижению уровней LDL-C у индивида, проходящему статиновую терапию, где способ включает введение индивиду антитела или его антигенсвязывающего фрагмента, который специфически связывает пропротеин конвертазы субтилизина/кексина типа 9 человека (hPCSK9), при этом антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве от приблизительно 5 мг до приблизительно 500 мг, повышая тем самым активность статинов в терапии по снижению LCL-C у индивида.
22. Способ по аспекту 21, где индивид до введения антитела является устойчивым к действию статинов.
23. Способ по аспекту 21, где индивид страдает заболеванием или состоянием, выбранным из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза.
24. Способ по аспекту 21, где заболевание или состояние представляет собой первичную гиперхолестеринемию или семейную гиперхолестеринемию.
25. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент вводят в дозе от приблизительно 50 мг до приблизительно 300 мг.
26. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент вводят в дозе в количестве приблизительно 150 мг.
27. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
28. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
29. Способ по аспекту 21, где лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 35%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
30. Способ по аспекту 21, где лечение снижает уровень общего холестерина в сыворотке по меньшей мере на величину от приблизительно 65% до приблизительно 80%, по сравнению с уровнем до введения дозы, и поддерживает снижение в течение по меньшей мере 24 дней.
31. Способ по аспекту 21, где лечение снижает уровни триглицеридов в сыворотке по меньшей мере на величину от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы.
32. Способ по аспекту 21, где лечение снижает уровень HDL холестерина в сыворотке не более чем на 5%, по сравнению с уровнем до введения дозы.
33. Способ по аспекту 21, где лечение имеет незначительный или не регистрируемый эффект на функцию печени, по измерению ALT и AST.
34. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
35. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
36. Способ по аспекту 21, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
37. Способ по аспекту 21, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
38. Способ по аспекту 21, где статин представляет собой аторвастатин, который вводят в дозе 10 мг или 80 мг.
39. Фармацевтическая лекарственная форма, содержащая антитело или его антигенсвязывающий фрагмент, который специфически связывает hPCSK9, и фармацевтически приемлемый носитель, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 5 мг до приблизительно 500 мг.
40. Лекарственная форма по аспекту 39, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 50 мг до приблизительно 300 мг.
41. Лекарственная форма по аспекту 39, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве 150 мг.
42. Лекарственная форма по аспекту 39, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
43. Лекарственная форма по аспекту 39, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
44. Лекарственная форма по аспекту 39, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
45. Лекарственная форма по аспекту 39, дополнительно содержащая ингибитор HMG-CoA-редуктазы.
46. Лекарственная форма по аспекту 39, где ингибитор HMG-CoA-редуктазы присутствует в дозе в количестве от приблизительно 0,05 мг до 100 мг.
47. Лекарственная форма по аспекту 39, где ингибитор HMG-CoA редуктазы представляет собой статин.
48. Лекарственная форма по аспекту 39, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
49. Лекарственная форма по аспекту 39, где статин представляет собой аторвастатин, присутствующий в дозе в количестве 10 мг или 80 мг.
50. Набор для лечения повышенных уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), у индивида, где набор содержит (а) фармацевтическую лекарственную форму, содержащую антитело или его антигенсвязывающий фрагмент, который специфически связывается с hPCSK9, и фармацевтически приемлемый носитель, при этом антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 5 мг до приблизительно 500 мг, и (b) этикетку или вкладыш в упаковку с инструкцией по применению.
51. Набор по аспекту 50, где этикетка указывает пациентам, получающим лечение указанным антителом или его антигенсвязывающим фрагментом, что лечение показано при заболевании или состоянии, выбранного из группы, состоящей из гиперхолестеринемии, гиперлипидемии, дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
52. Набор по аспекту 51, где заболевание или состояние является первичной гиперхолестеринемией или семейной гиперхолестеринемией.
53. Набор по аспекту 51, где заболевание или состояние является гиперхолестеринемией, которая не контролируется статинами.
54. Набор по аспекту 50, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве от приблизительно 50 мг до приблизительно 300 мг.
55. Набор по аспекту 50, где антитело или его антигенсвязывающий фрагмент присутствует в дозе в количестве 150 мг.
56. Набор по аспекту 50, где этикетка или вкладыш в упаковке указывает, что антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W).
57. Набор по аспекту 50, где этикетка или вкладыш в упаковке указывает, что антитело или его антигенсвязывающий фрагмент вводят индивиду каждую четвертую неделю (E4W).
58. Набор по аспекту 50, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи из аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
59. Набор по аспекту 50, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
60. Набор по аспекту 50, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание hPCSK9 с антителом или его антигенсвязывающим фрагментом, содержащим аминокислотную последовательность пары HCVR/LCVR, как показано в SEQ ID NO: 90/92.
61. Набор по аспекту 50, дополнительно содержащий ингибитор HMG-CoA-редуктазы.
62. Набор по аспекту 61, где ингибитор HMG-CoA-редуктазы присутствует в дозе в количестве от приблизительно 0,05 мг до 100 мг.
63. Набор по аспекту 50, где ингибитор HMG-CoA редуктазы представляет собой статин.
64. Набор по аспекту 50, где статин выбирают из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина.
65. Набор по аспекту 50, где инструкции указывают, что статин представляет собой аторвастатин, который принимают в дозе 10 мг или 80 мг.
66. Набор по аспекту 50, где инструкции указывают, что лечение пациентов антителом или его антигенсвязывающим фрагментом противопоказано для пациентов, принадлежащих к одной или нескольким следующим группам:
(xxii) курильщики;
(xxiii) лица в возрасте 70 лет и старше;
(xxiv) лица, страдающие от гипертензии;
(xxv) беременные женщины;
(xxvi) женщины, пытающиеся забеременеть;
(xxvii) женщины, которые кормят грудью;
(xxviii) лица, которые имеют или когда-либо имели заболевание, поражающее печень;
(xxix) лица, которые имели любые необъяснимые аномальные анализы крови в отношении функции печени;
(xxx) лица, которые употребляют чрезмерное количество алкоголя;
(xxxi) лица, имеющие проблемы с почками;
(xxxii) лица, страдающие гипотиреозом;
(xxxiii) лица, страдающие мышечными расстройствами;
(xxxiv) лица, ранее сталкивавшиеся с мышечной проблемой во время лечения гиполипидемическими лекарственными средствами;
(xxxv) лица, имеющие серьезные проблемы с дыханием;
(xxxvi) лица, которые принимают один или несколько из следующих препаратов: лекарственные средства, изменяющие работу иммунной системы, (например, циклоспорин или антигистаминные препараты), антибиотики и противогрибковые препараты (например, эритромицин, кларитромицин, кетоконазол, итраконазол, рифампицин и фузидиевая кислота), лекарственные препараты, регулирующие уровни липидов, (например, гемфиброзил, колестипол), блокаторы кальциевых каналов (например, верапамил, дилтиазем), лекарственные препараты, регулирующие сердечный ритм (дигоксин, амиодарон), ингибиторы протеазы, используемые при лечении ВИЧ (например, нелфинавир), варфарин, пероральные контрацептивы, антациды или зверобой;
(xxxvii) лица, выпивающие более 0,1 л сока грейпфрута в день;
(xxxviii) лица, имеющие индекс массы тела (BMI) более 40;
(xxxix) лица, имеющие индекс массы тела (BMI) менее 18;
(xl) лица, страдающие сахарным диабетом типа 1 или сахарным диабетом типа 2;
(xli) лица, имеющие положительную реакцию на гепатит В или С;
(xlii) лица, имеющие зарегистрированную чувствительность к терапии моноклональными антителами.
АСПЕКТЫ, СВЯЗАННЫЕ С КОМПОЗИЦИЯМИ
1. Фармацевтическая композиция, содержащая от приблизительно 40 мг до приблизительно 500 мг антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), из расчета на одну дозу, вместе с фармацевтически приемлемым эксципиентом или носителем.
2. Фармацевтическая композиция по аспекту 1, содержащая от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 300 мг, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела или его антигенсвязывающего фрагмента.
3. Фармацевтическая композиция по аспекту 1 или 2, содержащая приблизительно 150 мг, 200 мг или 300 мг антитела или его антигенсвязывающего фрагмента.
4. Фармацевтическая композиция по любому из аспектов 1-3, содержащая эффективную дозу антитела или его антигенсвязывающего фрагмента, который специфически связывает hPCSK9 (пропротеин конвертазы субтилизина/кексина типа 9 человека), где доза достаточна для устойчивого снижения уровней липопротеинов низкой плотности (LDL-C) в течение по меньшей мере 14 дней, по меньшей мере 15 дней, по меньшей мере 16 дней, по меньшей мере 17 дней, по меньшей мере 18 дней, по меньшей мере 19 дней, по меньшей мере 20 дней, по меньшей мере 21 дня, по меньшей мере 22 дней, по меньшей мере 23 дней или по меньшей мере 28 дней после введения, вместе с фармацевтически приемлемым эксципиентом или носителем.
5. Фармацевтическая композиция по любому из аспектов 1-4, где доза является достаточной для устойчивого снижения уровней LDL-C в течение по меньшей мере 14 дней, 28 дней или одного месяца.
6. Фармацевтическая композиция по любому из аспектов 1-5, дополнительно содержащая эффективное количество ингибитора HMG-CoA-редуктазы.
7. Фармацевтическая композиция по аспекту 6, где ингибитор HMG-CoA редуктазы представляет собой статин, предпочтительно, выбранный из группы, состоящей из церивастатина, аторвастатина, симвастатина, питавастатина, розувастатина, флувастатина, ловастатина и правастатина и, предпочтительно, представляет собой аторвастатин.
8. Фармацевтическая композиция по аспекту 6 или 7, содержащая от приблизительно 0,05 мг до приблизительно 100 мг, от приблизительно 0,5 мг до приблизительно 100 мг, от приблизительно 5 мг до приблизительно 90 мг, приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг ингибитора HMG-CoA-редуктазы, и, предпочтительно, приблизительно 10 мг, приблизительно 20 мг, приблизительно 40 мг или приблизительно 80 мг.
9. Фармацевтическая композиция по любому из аспектов 6-8, содержащая эффективную дозу ингибитора HMG-CoA-редуктазы, достаточную для снижения уровней LDL-D при введении один раз в день.
10. Фармацевтическая композиция по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент характеризуется одним или несколькими признаками из следующих:
а. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 25% до приблизительно 40%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 25%, и более предпочтительно, по меньшей мере 30%, по сравнению с уровнем до введения дозы, в частности, при введении в дозе от приблизительно 40 мг до приблизительно 60 мг, предпочтительно, от приблизительно 45 мг до приблизительно 55 мг, и более предпочтительно, приблизительно 50 мг при режиме введения один раз в две недели (через одну неделю, E2W);
b. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 65%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 100 мг в режиме E2W;
с. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 60% до по меньшей мере приблизительно 75% (например, по меньшей мере приблизительно 60%, по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70% или по меньшей мере приблизительно 75%), по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 14 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 55%, и более предпочтительно, по меньшей мере 60%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
d. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 40% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней, где устойчивое снижение, предпочтительно, составляет по меньшей мере 35%, и более предпочтительно, по меньшей мере 40%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 200 мг в режиме E4W;
е. снижение уровней холестерина, относящегося к липопротеинам низкой плотности (LDL-C), на величину по меньшей мере от приблизительно 50% до приблизительно 75%, по сравнению с уровнем до введения дозы, при устойчивом снижении в течение периода по меньшей мере 28 дней после введения индивиду, где устойчивое снижение, предпочтительно, составляет по меньшей мере 40%, и более предпочтительно, по меньшей мере 45%, по сравнению с уровнем до введения дозы, в частности, при введении дозы приблизительно равной 300 мг в режиме E4W;
f. увеличение уровней сывороточного HDL холестерина по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5%, по сравнению с уровнем до введения дозы индивиду, в частности, при введении дозы приблизительно равной 150 мг в режиме E2W;
g. наличие небольшого или нерегистрируемого эффекта на уровни тропонина, при введении индивиду;
h. увеличение одного или нескольких из следующего: уровней общего холестерина, уровней ApoB, уровней холестерина, не относящегося к HDL-С, соотношения ApoB/ApoA-1.
11. Фармацевтическая композиция по любому из аспектов 1-9, где антитело или его антигенсвязывающий фрагмент способен устранить устойчивость к статинам при введении индивиду с гиперхолестеринемией, устойчивой к действию статинов.
12. Фармацевтическая композиция по любому из аспектов 1-10, где антитело или его антигенсвязывающий фрагмент содержит CDR тяжелой цепи и CDR легкой цепи аминокислотной последовательности пары HCVR/LCVR, как показано в SEQ ID NO: 90/92, или из пар по существу идентичных им последовательностей, имеющих по меньшей мере 98% или 99% идентичности с ними.
13. Фармацевтическая композиция по любому из аспектов 1-11, где антитело или его антигенсвязывающий фрагмент содержит пару аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO:90/92, или пару по существу идентичных им последовательностей, имеющих по меньшей мере 98% или 99% идентичности с ними.
14. Фармацевтическая композиция по любому из аспектов 1-10, где антитело или его антигенсвязывающий фрагмент конкурирует за связывание с антителом против hPCSK9 или с его антигенсвязывающим фрагментом, содержащим пару аминокислотных последовательностей HCVR/LCVR, как показано в SEQ ID NO:90/92.
15. Фармацевтическая композиция по любому из аспектов 1-13, где антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий аминокислотный остаток 238 hPCSK9 (SEQ ID NO:755).
16. Фармацевтическая композиция по любому из аспектов 1-14, где антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий один или несколько аминокислотных остатков в положениях 238, 153, 159 и 343 hPCSK9 (SEQ ID NO:755).
17. Фармацевтическая композиция по любому из аспектов 1-15, где антитело или его антигенсвязывающий фрагмент связывает эпитоп, который не содержит аминокислотного остатка в положениях 192, 194, 197 и/или 237 hPCSK9 (SEQ ID NO: 755).
18. Фармацевтическая композиция по любому из аспектов 1-16, содержащая антитело или его антигенсвязывающий фрагмент в виде сухого состава для растворения, такого как лиофилизированный порошок, порошок высушенный замораживанием и распылением, или в виде безводного концентрата.
19. Фармацевтическая композиция по любому из аспектов 1-17, содержащая антитело или его антигенсвязывающий фрагмент в виде жидкого состава, например, раствора для инъекции или инфузии.
20. Фармацевтическая композиция по любому из аспектов 4-18, содержащая ингибитор HMG-CoA-редуктазы в форме состава для перорального приема, например, в виде капсулы или таблетки, или в форме жидкого состава, например, в виде суспензии, дисперсии или раствора, например, для перорального введения, инъекции или инфузии.
21. Раствор для инъекций по аспекту 19, предпочтительно, содержащий от приблизительно 40 мг до приблизительно 200 мг или от приблизительно 40 мг до приблизительно 200 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг или приблизительно 200 мг антитела или его антигенсвязывающего фрагмента в 1 мл объема раствора.
22. Сухой состав по аспекту 17, предпочтительно, содержащий от приблизительно 40 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 500 мг, от приблизительно 50 мг до приблизительно 400 мг, от приблизительно 50 мг до приблизительно 300 мг, например, приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг, и более предпочтительно, приблизительно 50 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, и еще более предпочтительно, приблизительно 150 мг, приблизительно 200 мг или приблизительно 300 мг антитела или его антигенсвязывающего фрагмента из расчета на одну дозу.
23. Антитело или его антигенсвязывающий фрагмент, входящий в состав одной из фармацевтических композиций по любому из аспектов 1-17.
24. Лекарственная форма, содержащая фармацевтическую композицию по любому из аспектов 1-20, раствор для инъекций по аспекту 21, сухой состав по аспекту 22 или антитело по аспекту 23.
25. Лекарственная форма по аспекту 24, содержащая приблизительно 40 мг, приблизительно 50 мг, приблизительно 75 мг, приблизительно 100 мг, приблизительно 150 мг, приблизительно 200 мг, приблизительно 250 мг, приблизительно 300 мг, приблизительно 350 мг, приблизительно 400 мг, приблизительно 450 мг или приблизительно 500 мг антитела или его антигенсвязывающего фрагмента.
26. Лекарственная форма по аспекту 24 или 25, содержащая антитело или его фрагмент, в виде сухого состава для растворения, в герметично закрытом контейнере, таком как флакон, ампула или саше.
27. Лекарственная форма по аспекту 24 или 25, содержащая антитело или его фрагмент, в виде жидкого состава, в герметично закрытом контейнере, таком как флакон, саше, предварительно заполненный шприц, предварительно заполненный автоинъектор или картридж для многоразового шприца или аппликатора.
28. Лекарственная форма по аспекту 26 или 27, где количество активного ингредиента указано на герметично закрытом контейнере.
29. Изделие, содержащее фармацевтическую композицию по любому из аспектов 1-20, жидкий состав по аспекту 21 или сухой состав по аспекту 22, антитело или его антигенсвязывающий фрагмент по аспекту 23, или одну или несколько лекарственных форм по любому из аспектов 24-28, и контейнер.
30. Изделие по аспекту 29, содержащее отдельные лекарственные формы антител по аспекту 23 и ингибитор HMG-CoA-редуктазы по любому из аспектов 5-9 или по аспекту 20.
31. Изделие по аспекту 30, содержащее один или несколько из следующих компонентов:
a. одну или несколько лекарственных форм, содержащих антитело по аспекту 23;
b. одну или несколько лекарственных форм, содержащих ингибитор HMG-CoA-редуктазы по по любому из аспектов 6-9 или по аспекту 20;
c. инструкции по применению;
d. устройство для введения антитела, такое как шприц.
32. Изделие по аспекту 31, содержащее лекарственные формы антитела, а также, предпочтительно, ингибитора HMG-CoA-редуктазы, в количестве, достаточном для одного однократного введения антитела и ингибитора HMG-CoA-редуктазы, для курса лечения антителом и ингибитором HMG-CoA-редуктазы в течение двух недель (например, для 14-дневного курса), для курса лечения антителом и ингибитором HMG-CoA-редуктазы в течение четырех недель (т.е. для 28-дневного курса) или для курса лечения антителом и ингибитором HMG-CoA-редуктазы в течение одного месяца.
33. Изделие по аспекту 32, содержащее лекарственные формы антитела, в количестве, достаточном для курса лечения в режиме введения один раз в две недели, в режиме введения один раз в четыре недели или в режиме введения один раз в месяц.
34. Изделие по аспекту 32 или 33, содержащее лекарственные формы ингибитора HMG-CoA-редуктазы в количестве, достаточном для ежедневного приема.
35. Фармацевтическая композиция по любому из аспектов 1-20, или антитело или его антигенсвязывающий фрагмент по аспекту 21 для применения при лечении заболевания или состояния, которое вызывается воздействием экспрессии или активности PCSK9, предпочтительно, для применения при снижении повышенных уровней LDL-С (липопротеина низкой плотности С).
36. Фармацевтическая композиция, или антитело или его антигенсвязывающий фрагмент по аспекту 35, где заболевание или состояние выбрано из группы, состоящей из: повышенных уровней общего холестерина, повышенных уровней липопротеинов низкой плотности (LDL-C), гиперхолестеринемии, гиперлипидемии, дислипидемии и атеросклероза, в частности, первичной гиперхолестеринемии, семейной гиперхолестеринемии или гиперхолестеринемии, которая не контролируется статинами.
37. Фармацевтическая композиция, или антитело или его антигенсвязывающий фрагмент по аспекту 35 или 36, где композицию, антитело или его антигенсвязывающий фрагмент вводят индивиду один раз в две недели (E2W), каждую четвертую неделю (E4W) или один раз месяц.
38. Фармацевтическая композиция, или антитело или его антигенсвязывающий фрагмент по любому из аспектов 35-37, включающий совместное введение HMG-CoA-редуктазы, предпочтительно, ингибитора HMG-CoA-редуктазы по любому из аспектов 7-9 или по аспекту 20.
39. Фармацевтическая композиция, или антитело по аспекту 38, где ингибитор HMG-CoA-редуктазы вводят один раз в день, и предпочтительно, каждый день.
40. Способ получения фармацевтической композиции по любому из аспектов 1-20, включающий смешивание антитела или его антигенсвязывающего фрагмента, и, необязательно, ингибитора HMG-CoA-редуктазы, с одним или несколькими фармацевтическими эксципиентами или носителями.
41. Способ получения лекарственной формы по любому из аспектов 24-28, включающий отмеривание необходимого количества фармацевтической композиции по любому из аспектов 1-20, антитела по аспекту 21, жидкого состава по аспекту 22 или сухого состава по аспекту 23, содержащего одну или несколько доз антитела, и, необязательно, ингибитора HMG-CoA-редуктазы, и получение физически дискретных единиц, подходящих в качестве единичных доз для введения человеку и/или животному.
42. Способ получения изделия по любому из аспектов 29-34, включающий упаковку фармацевтической композиции по любому из аспектов 1-20, антитела по аспекту 21, жидкого состава по аспекту 22, сухого состава по аспекту 23, или одной или нескольких лекарственных форм по любому из аспектов 24-28, в контейнер.
ПРИМЕРЫ
Далее представлены следующие примеры, предназначенные для предоставления специалистам в данной области техники полного раскрытия и описания того, как выполнять и использовать способы и композиции по изобретению, при этом эти примеры не предназначены для ограничения объема изобретения, предоставленного авторами изобретения. Авторами изобретения были предприняты усилия, чтобы обеспечить точность в отношении используемых численных значений, однако некоторые экспериментальные ошибки и отклонения должны быть приняты во внимание. Если не указано иное, молекулярная масса представляет собой среднюю молекулярную массу, температура выражена в градусах Цельсия, а давление было равно или являлось близким к атмосферному.
Исследование 1
Исследование 1 представляло собой многоцентровое, рандомизированное, двойное слепое, выполняемое в параллельных группах, плацебо-контролируемое 12-недельное исследование, выполненное с целью оценки эффективности и безопасности антител 316P для пациентов с повышенным уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), (≥100 мг/дл или 2,59 ммоль/л), при лечении аторвастатином (10 мг, 20 мг или 40 мг) при постоянной дозе в течение времени не менее 6 недель. Рандомизация была выполнена по сгруппированным дозам аторвастатина, которые получали до рандомизации. После двойного слепого периода, пациенты наблюдались в течение последующего 8-недельного периода. Основной целью исследования являлась оценка влияния антител 316P на уровни LDL-C после 12 недель лечения, по сравнению с плацебо, у пациентов с LDL-C (≥100 мг/дл или 2,59 ммоль/л), проходящим курс лечения постоянными дозами аторвастатина.
Были оценены следующие дозы и режимы дозирования составов: 50 мг, 100 мг и 150 мг каждые 2 недели (E2W), 200 мг и 300 мг каждые 4 недели (E4W), в сравнении с плацебо.
В настоящее исследование было включено в общей сложности 122 пациента (20 в группе плацебо, 19 в группе 50 мг E2W, 20 в группе 100 мг E2W, 20 в группе 150 мг E2W, 22 в группе 200 мг E4W и 21 в группе 300 мг E4W). Их распределили случайным образом в совокупные группы, принимающие аторвастатин: сорок шесть (37,7%) пациентов, принимающих 10 мг аторвастатина; 43 пациента (35,2%), принимающих 20 мг аторвастатина; и 33 пациента (27,0%), принимающих 40 мг аторвастатина.
Отбор пациентов
Критерии включения:
- пациенты (пациенты, получающие гиполипидемическое лечение с приемом иных препаратов, чем аторвастатин, или не получавших постоянной дозы аторвастатина 10 мг, 20 мг или 40 мг в течение периода не менее 6 недель до периода скрининга, или пациенты, не получавшие никакого лечения) с первичной гиперхолестеринемией, имеющие уровень холестерина, относящегося к липопротеинам низкой плотности (LDL-C) ≥100 мг/дл (≥2,59 ммоль/л) в конце вводного периода в курс лечения с использованием аторвастатина (неделя-1);
или
- пациенты с первичной гиперхолестеринемией, получавшие аторвастатин в постоянной дозе 10 мг, 20 мг или 40 мг в течение периода, равного не менее 6 неделям до скринингового периода, и которые имеют уровень LDL-С ≥100 мг/дл (≥2,59 ммоль/л) при посещении для скрининга на неделе-1.
Критерии исключения:
- Уровень LDL-С <100 мг/дл (<2,59 ммоль/л) в неделю-1 (V1):
○ после вводного периода в курс лечения с использованием аторвастатина (10 мг, 20 мг или 40 мг) у пациентов, получавших гиполипидемическое лечение с приемом иных препаратов, чем аторвастатин, или не получавших постоянной дозы аторвастатина 10 мг, 20 мг или 40 мг в течение периода не менее 6 недель до периода скрининга, или у пациентов, не получавших никакого лечения;
или
○ при первом посещении у пациентов, которые проходят лечение с использованием постоянной дозы аторвастатина (10 мг, 20 мг или 40 мг) в течение периода не менее 6 недель до посещения для скрининга на неделе-1.
- Использование статинов, кроме аторвастатина, в дозе 10 мг, 20 мг или 40 мг, или использование других гиполипидемических лекарственных средств, включая, но не ограничиваясь перечисленными, фибраты, смолы желчных кислот, ниацин >500 мг, блокаторы кишечной абсорбции холестерина (ICA) или омега-3 жирные кислоты в дозах >1000 мг в течение периода скрининга.
- Индекс массы тела (BMI) <18 или >40 кг/м2 на неделе-7 или на неделе-1.
- Пациенты, ранее не получавшие указаний по приему диеты для снижения уровня холестерина.
- Пациенты с сахарным диабетом типа 1.
- Пациенты с сахарным диабетом типа 2, который лечится инсулином.
- Пациенты с сахарным диабетом типа 2 и с HbA1c ≥8,5% на неделе-7 или на неделе-1 (пациенты считаются плохо контролируемыми).
- Пациенты с результатами лабораторных исследований до рандомизации:
○ Положительный тест на поверхностный антиген гепатита В и/или антитела гепатита С.
○ Уровень триглицеридов (TG) >350 мг/дл (>3,95 ммоль/л) на неделе-7 или неделе-1.
○ Уровень нейтрофилов <1500/мм3 и/или тромбоцитов <100000/мм3.
○ Положительной тест сыворотки или мочи на беременность у женщин детородного возраста.
○ Аномальный чувствительный уровень TSH (>ULN или <LLN) по сравнению с нормальными значениями, определенными Центральной лабораторией.
○ Заключение о почечной недостаточности по результатам анализа:
- Мужчины: сывороточный креатинин >1,5×ULN.
- Женщины: сывороточный креатинин >1,4×ULN.
○ ALT или AST >2×ULN.
○ CPK>3×ULN (допустим 1 лабораторный повтор).
- Наличие любых противопоказаний к протоколу фонового лечения (т.е. к терапии аторвастатином) или к предупреждениям/предосторожностям (когда применимо), указанным на маркировке продукции, предписываемой соответствующим национальным органом по контролю за лекарствами, при использовании препаратов, конкретизирующие эти критерии исключения.
- Зарегистрированная чувствительность к лечению моноклональными антителами.
- Беременность или кормление грудью для женщин.
- Женщины детородного возраста, применяющие неэффективный метод контрацепции.
Популяция пациентов:
Демографические и исходные характеристики были в целом аналогичны для всех групп лечения. Возраст пациентов составлял 24-75 лет, средний возраст пациентов - 58,0 лет (28,7% пациентов имели возраст ≥65 лет). Средний диапазон значений базовых уровней LDL-C и общего холестерина во всех группах был одинаковым и составлял от 3,214 ммоль/л до 3,500 ммоль/л для LDL-C, и от 5,284 ммоль/л до 5,521 ммоль/л для общего холестерина. BMI (кг/м2) составлял 19,7-40,5, при среднем значении 29,04 и медианном значении 28,4 (63,6% пациентов имели BMI <30 и 36,4% пациентов имели индекс массы тела >30). 80 пациентов (65,6%) из 122 имели гиперлипопротеинемию типа IIa (семейную гиперхолестеринемию) в соответствии с классификацией по Фредриксону, 41 пациентов (33,6%) имели гиперлипопротеинемию типа IIb (комбинированную гиперлипидемию) и 1 пациент (0,8%) имел гиперлипопротеинемию типа IV (эндогенную гиперлипидемию). 82% пациентов ранее получали лечение с применением гиполипидемических средств, в то время как 22% пациентов не получали такого лечения.
Продолжительность периода исследования для индивидов:
Продолжительность участия в исследовании зависело от состояния пациента при скрининге:
- Для пациентов, получавших аторвастатин в постоянной дозе 10 мг, 20 мг или 40 мг в течение периода не менее 6 недель до скрининга, продолжительность участия в исследовании составляло приблизительно 21 неделю, включая период скрининга на неделе-1, двойного слепого лечения в течение 12 недель и последующего периода, продолжительностью 8 недель.
- Для пациентов, получавших гиполипидемическое лечение иными препаратами, кроме аторвастатина, или не получавших постоянной дозы аторвастатина 10 мг, 20 мг или 40 мг в течение периода не менее 6 недель до периода скрининга, или для пациентов, не получавшие никакого лечения, продолжительность участия в исследовании составляло приблизительно 27 недель, включая период скрининга в течение 7 недель (в том числе вводного периода в течение 6 недель), двойного слепого лечения в течение 12 недель и последующего периода, продолжительностью 8 недель.
Активные вещества:
Антитело 316P:
Антитело 316P представляет собой полностью человеческое антитело, содержащее HCVR, как показано в SEQ ID NO: 90, и LCVR, как показано в SEQ ID NO: 92 в списке последовательностей. Последовательности CDR показаны в SEQ ID NO: 76, 78 и 80 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO: 84, 86 и 88 (CDR1, CDR2, CDR3 легкой цепи).
Антитело 300N:
Антитело 300N представляет собой полностью человеческое антитело, содержащее HCVR, как показано в SEQ ID NO: 218, и LCVR, как показано в SEQ ID NO: 226 в списке последовательностей. Последовательности CDR показаны в SEQ ID NO: 220, 222 и 224 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO: 228, 230 и 232 (CDR1, CDR2, CDR3 легкой цепи).
Группы исследования:
Группа 1: Первая группа пациентов получала две инъекции антитела 316P, по 1 мл каждая, которые вводили подкожно в область живота, дозами по 50 мг, каждые две недели, в течение 12-недельного периода лечения;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Группа 2: Вторая группа пациентов получала две инъекции антитела 316P, по 1 мл каждая, которые вводили подкожно в область живота, дозами по 100 мг, каждые две недели, в течение 12-недельного периода лечения;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Группа 3: Третья группа пациентов получала две инъекции антитела 316P, по 1 мл каждая, которые вводили подкожно в область живота, дозами по 150 мг, каждые две недели, в течение 12-недельного периода лечения;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Группа 4: Четвертая группа пациентов получала две инъекции раствора плацебо, по 1 мл каждая, которые вводили подкожно в области живота каждые две недели, в течение 12 недель;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Группа 5: Пятая группа пациентов получала две инъекции антитела 316P, по 1 мл каждая, которые вводили подкожно в область живота, дозами по 200 мг, каждые четыре недели, в течение 12-недельного периода лечения;
Раствор плацебо вводили переменного с введением антитела 316P, так что пациент имел такую же схему инъекций, как и пациенты в группах 1-4, т.е. пациент получал две инъекции раствора плацебо по 1 мл в недели 2, 6, 10, и две инъекции антитела 316P по 1 мл в недели 0, 4, 8 и 12.
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Группа 6: Шестая группа пациентов получала две инъекции антитела 316P, по 1 мл каждая, которые вводили подкожно в область живота, дозами по 300 мг, каждые четыре недели, в течение 12-недельного периода лечения;
Раствор плацебо вводили переменного с введением антитела 316P, так что пациент имел такую же схему инъекций, как и пациенты в группах 1-4, т.е. пациент получал две инъекции раствора плацебо по 1 мл в недели 2, 6, 10, и две инъекции антитела 316P по 1 мл в недели 0, 4, 8 и 12;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг, 20 мг или 40 мг, в качестве фоновой терапии.
Первичные и основные вторичные конечные точки:
Основным показателем эффективности является процентное изменение уровней LDL-С, рассчитываемое на 12-й неделе по сравнению с исходным уровнем, который определяется следующим образом:
100×[(рассчитанное значение LDL-C на 12-й неделе)-(рассчитанное значение LDL-C в начале исследования)]/(рассчитанное значение LDL-C в начале исследования).
В случае недоступности рассчитанного значения LDL-C на 12 неделе, как определено выше, то расчеты выполняют по последнему значению LDL-C, измеренному во время эффективного периода до 12-ой недели временного окна. Это значение (для последнего наблюдения в ходе процедуры [LOCF]) будет использоваться как отсутствующее значение LDL-C для 12-ой недели.
Вторичными показателями эффективности являются следующие:
Абсолютное изменение (выраженное в ммоль/л и мг/дл), по сравнению с исходным, для рассчитанного значения LDL-C на 12-ой неделе, которое определяется следующим образом:
(рассчитанное значение LDL-C на 12-ой неделе) - (рассчитанное исходное значение LDL-C),
используя те же определения и правила для численных значений, как и для первичной конечной точки.
Процент пациентов с рассчитанным значением LDL-С <70 мг/дл (1,81 ммоль/л) и <100 мг/дл (2,59 ммоль/л) на 12-й неделе.
Процентное изменение в ApoB от исходного уровня до 12-ой недели: используются те же определения и правила, как и для LDL-C, за исключением исходной величины, которая является величиной ApoB, измеренной во время посещения при рандомизации (посещение 2) и перед первой IP-инъекцией, или, при их отсутствии, используют последние незапланированное значение, полученное в период времени от посещения 1 (неделя-1) до первой IP-инъекции.
Изменения значений уровней липопротеинов, не относящихся к HDL-C, выраженные в процентах и по абсолютной величине (выраженной в ммоль/л и мг/дл), до 12-й недели, по сравнению с исходными уровнями: используются те же самые определения и правила, как и для LDL-С.
Изменения значений уровней триглицеридов, выраженные в процентах и по абсолютной величине (выраженной в ммоль/л и мг/дл), до 12-ой недели, по сравнению с исходными уровнями: используются те же самые определения и правила, как и для LDL-С, за исключением измерений у пациентов, которые приняли пищу, или за исключением измерений у пациентов, которые не соблюдают режим голодания.
Процентное изменение в ApoA-1 от исходного уровня до 12-й недели: используются те же самые определения и правила, как и для AboB.
Абсолютное изменение соотношения AboB/ApoA-1 от исходного уровня до 12-й недели: используются те же самые определения и правила, как и для AboB.
Процентное изменение в Lp(а) от исходного уровня до 12-й недели: используются те же самые определения и правила, как и для AboB. В случае, когда значения Lp(а) находятся ниже предела обнаружения, для расчета используют значение, равное половине интервала между нулем и пределом обнаружения.
Результаты:
Влияние лечения антителом 316P на снижение уровней LDL-С
Уровни LDL-C в ммоль/л (мг/дл) на 12-й неделе
Во всех группах, по сравнению с группой плацебо, наблюдались статистически значимое снижение LDL-С на 12 неделе (изменение в процентах от исходного уровня). Наибольшее снижение наблюдалось в группе 100 мг E2W (-63,90%) и в группе 150 мг E2W (-72,68%), по сравнению с незначительным снижением в группе плацебо (-6,08%), при этом средняя разность по методу наименьших квадратов, по сравнению с группой плацебо, составила -58,36% и -68,78%, соответственно, причем эти снижения наблюдались после первой инъекции и сохранялись в течение всего исследования, и, в частности, в течение периода времени между инъекциями. Значительное снижение LDL-С на 12 неделе от исходного уровня наблюдались и в группах 200 мг E4W и 300 мг E4W (-47,23% и 48,29%, соответственно, и средняя разность по методу наименьших квадратов, по сравнению с группой плацебо, составила -42,53% и -42,26%, соответственно), при этом снижение составляло по меньшей мере приблизительно 40% в течение всего интервала времени. У 17 пациентов из 18, входящих в группу 150 мг E2W, наблюдалось снижение LDL-C на 12 неделе по сравнению с исходным уровнем более чем на 50%.
Воздействие лечения антителом 316P на другие основные конечные точки эффективности
Надежные результаты в части уменьшения были отмечены для общего холестерина, ApoB и для холестерина, не относящегося к HDL. Для HDL-C наблюдалась тенденция увеличения во всех группах; аналогичная картина была отмечена для ApoA-1. Антитело 316P хорошо переносится при всех испытанных дозах и режимах дозирования в течение 12-недельного лечения. Важно отметить, что во всех группах, подвергавшихся лечению, не было отмечено никаких изменений в уровне тропонина.
Выводы:
Результаты этого исследования показали, что режимы дозирования по схемам E2W или E4W и различные дозы антитела 316P против PCSK9, которые были использованы в данном исследовании, оказались эффективной и безопасной терапией для снижения уровней LDL-C у пациентов с гиперлипопротеинемией и/или гиперлипидемией, и, таким образом, они применимы для лечения гиперлипопротеинемии и/или гиперлипидемии. Лучшие общие результаты достигаются при использовании дозы 150 мг по режима E2W. Однако, принимая во внимание удобства для пациента, следует признать, что режим введения антитела только один раз в месяц, также как и режим E4W, предоставляет очень хорошие результаты в данном исследовании.
Исследование 2
Исследование 2 представляло собой рандомизированное, двойное слепое, выполняемое в 3 параллельных группах, плацебо-контролируемое исследование с фиксированной дозой и режимом дозирования, многоцентровое, 8-недельное исследовании пациентов с первичной гиперхолестеринемией в возрасте 18-75 лет. Одна из целей этого исследования состояла в оценке эффективности и безопасности применения антитела 316P в отношении пациентов с повышенным уровнем LDL-C (≥100 мг/дл или ≥2,59 ммоль/л), которые получают аторвастатин в постоянной дозе, равной 10 мг.
Во время периода скрининга пациенты должны были быть стабилизированы в приеме аторвастатина с постоянной дозой, равной 10 мг, в течение периода не менее 6 недель, если они этого не сделали ранее. Затем, после дополнительного скрининга на первой неделе, пациенты были рандомизированы по центру IVRS/IWRS в соотношении 1:1:1 в одну из 3 групп, подвергаемых лечению (обработке): группа плацебо для 316P+80 мг аторвастатина, группа 150 мг 316P E2W+80 мг аторвастатина, группа 150 мг 316P E2W+10 мг аторвастатина; и их подвергали лечению двойным слепым методом в течение 8 недель. Антитело 316P вводили каждые 2 недели путем подкожных инъекций, а аторвастатин пациенты принимали перорально один раз в день вечером в домашних условиях. После периода двойного слепого лечения следовал 8-недельный периода наблюдения.
Были отобраны и рандомизированы около 90 пациентов (по 30 пациентов в каждой группе) приблизительно из 20 мест проживания.
ЦЕЛИ
Первичная цель
Оценить влияние антитела 316P на уровни холестерина, относящегося к липопротеинам низкой плотности (LDL-C) по сравнению с плацебо, при совместном введении с аторвастатином в дозе 80 мг, после 8 недель лечения пациентов с уровнем LDL-С ≥100 мг/дл (≥2,59 ммоль/L) аторвастатином в дозе 10 мг.
Вторичная цель
Основными вторичными целями этого эксперимента, как источника информации и данных, являются:
- оценка влияния антитела 316P на уровни других липидов, по сравнению с плацебо, при совместном введении с 80 мг аторвастатина после 8 недель лечения;
- оценка эффективности антитела 316P при совместном введении с аторвастатином в высокой дозе (80 мг), по сравнению с аторвастатином в дозе 10 мг;
- оценка безопасности и переносимости антитела 316P при совместном введении с 2 разными дозами аторвастатина;
- оценка влияния антитела 316P на другие экстраполируемые конечные точки: уровни глюкозы в плазме натощак, гликозилированного гемоглобина A1c (HbA1c), высокочувствительного С-реактивного белка (hs-CRP).
Отбор пациентов:
Критерии включения:
- пациенты (пациенты, получающие гиполипидемическое лечение с приемом иных препаратов, чем аторвастатин, или не получавших постоянной дозы аторвастатина 10 мг в течение периода не менее 6 недель до периода скрининга, или пациенты, не получавшие никакого лечения) с первичной гиперхолестеринемией, имеющие уровень холестерина, относящегося к липопротеинам низкой плотности (LDL-C) ≥100 мг/дл (≥2,59 ммоль/л) в конце вводного периода в курс лечения с использованием аторвастатина (неделя-1);
или
- пациенты с первичной гиперхолестеринемией, получавшие аторвастатин в постоянной дозе 10 мг в течение периода не менее 6 недель до скринингового периода, и которые имеют уровень LDL-С ≥100 мг/дл (≥2,59 ммоль/л) при посещении для скрининга на неделе-1.
Критерии исключения:
- Уровень LDL-С <100 мг/дл (<2,59 ммоль/л) в неделю-1 (V1):
○ после вводного периода в курс лечения с использованием аторвастатина в дозе 10 мг у пациентов, получавших гиполипидемическое лечение с приемом иных препаратов, чем аторвастатин, или не получавших постоянной дозы аторвастатина 10 мг в течение периода, равного не менее 6 неделям до периода скрининга, или у пациентов, не получавших никакого лечения;
или
○ при первом посещении у пациентов, которые проходят лечение с использованием аторвастатина в постоянной дозе 10 мг в течение периода не менее 6 недель до посещения для скрининга на неделе-1.
- Индекс массы тела (BMI) <18 или >40 кг/м² на неделе-7 или на неделе-1.
- Пациенты, ранее не получавшие указаний по приему диеты для снижения уровня холестерина.
- Использование статинов, иных чем аторвастатин в дозе 10 мг, или использование других гиполипидемических лекарственных средств, включая, но не ограничиваясь перечисленными, фибраты, смолы желчных кислот, ниацин >500 мг, блокаторы кишечной абсорбции холестерина (ICA) или омега-3 жирные кислоты в дозах >1000 мг в течение периода скрининга.
- Пациенты с сахарным диабетом типа 1.
- Пациенты с сахарным диабетом типа 2, который лечится инсулином.
- Пациенты с сахарным диабетом типа 2 и с HbA1c ≥8,5% на неделе-7 или на неделе-1 (пациенты считаются плохо контролируемыми).
- Пациенты с результатами лабораторных исследований до рандомизации:
○ Положительный тест на поверхностный антиген гепатита В и/или антитела гепатита С.
○ Уровень триглицеридов (TG) >350 мг/дл (>3,95 ммоль/л) на неделе-7 или неделе-1.
○ Уровень нейтрофилов <1500/мм3 и/или тромбоцитов <100000/мм3.
○ Положительной тест сыворотки или мочи на беременность у женщин детородного возраста.
○ Аномальный чувствительный уровень TSH (>ULN или <LLN) по сравнению с нормальными значениями, определенными Центральной лабораторией.
○ Заключение о почечной недостаточности по результатам анализа:
● Мужчины: сывороточный креатинин >1,5×ULN.
● Женщины: сывороточный креатинин >1,4×ULN.
○ ALT или AST >2×ULN (допустим 1 лабораторный повтор).
○ CPK>3×ULN (допустим 1 лабораторный повтор).
- Наличие любых противопоказаний к протоколу фонового лечения (т.е. к терапии аторвастатином) или к предупреждениям/предосторожностям (когда применимо), указанным на маркировке продукции, предписываемой соответствующим национальным органом по контролю за лекарствами, при использовании препаратов, конкретизирующие эти критерии исключения.
- Зарегистрированная чувствительность к лечению моноклональными антителами.
- Беременность или кормление грудью для женщин.
- Женщины детородного возраста, применяющие неэффективный метод контрацепции.
Продолжительность периода исследования для индивидов:
Продолжительность участия в исследовании зависела от состояния пациента при скрининге:
- Для пациентов, получавших аторвастатин в постоянной дозе 10 мг в течение периода не менее 6 недель до скрининга, продолжительность участия в исследовании составляло приблизительно 17 неделю, включая период скрининга на неделе-1, двойного слепого лечения в течение 8 недель и последующего периода, продолжительностью 8 недель (см. фиг.5).
- Для пациентов, получавших гиполипидемическое лечение иными препаратами, кроме аторвастатина, или не получавших постоянной дозы аторвастатина 10 мг в течение периода не менее 6 недель до периода скрининга, или для пациентов, не получавших никакого лечения, продолжительность участия в исследовании составляла приблизительно 23 недели, включая период скрининга в течение 7 недель (в том числе вводного периода в течение 6 недель), двойного слепого лечения в течение 8 недель и последующего периода, продолжительностью 8 недель (см. фиг.4).
Активные вещества:
Антитело 316P:
Антитело 316P представляет собой полностью человеческое антитело, содержащее HCVR, как показано в SEQ ID NO: 90, и LCVR, как показано в SEQ ID NO: 92 в списке последовательностей. Последовательности CDR показаны в SEQ ID NO:76, 78 и 80 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO:84, 86 и 88 (CDR1, CDR2, CDR3 легкой цепи).
Антитело 300N:
Антитело 300N представляет собой полностью человеческое антитело, содержащее HCVR, как показано в SEQ ID NO: 218, и LCVR, как показано в SEQ ID NO: 226 в списке последовательностей. Последовательности CDR показаны в SEQ ID NO: 220, 222 и 224 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO: 228, 230 и 232 (CDR1, CDR2, CDR3 легкой цепи).
Группы исследования:
Группа 1: Первая группа пациентов получала одну подкожную инъекцию антитела 316P объемом 1 мл, которую вводили в брюшную полость через каждые две недели, дозой по 150 мг, для двойного слепого лечения в течение 8 недель;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг в качестве фоновой терапии.
Аторвастатин вводили в дозе 80 мг один раз в течение 8 недель двойной слепой терапии.
Группа 2: Вторая группа пациентов получала одну подкожную инъекцию раствора плацебо объемом 1 мл, которую вводили в брюшную полость через каждые две недели, дозой по 150 мг, для двойного слепого лечения в течение 8 недель;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг в качестве фоновой терапии.
Аторвастатин вводили в дозе 80 мг (по 2 таблетки с двойной оболочкой инкапсулированного аторвастатина по 40 мг) один раз в течение 8 недель двойной слепой терапии.
Группа 3: Третья группа пациентов получала одну подкожную инъекцию антитела 316P объемом 1 мл, которую вводили в брюшную полость через каждые две недели, дозой по 150 мг, для двойного слепого лечения в течение 8 недель;
Аторвастатин вводили один раз в день, при постоянной дозе 10 мг в качестве фоновой терапии.
Аторвастатин вводили в дозе 10 мг (1 таблетка с двойной оболочкой инкапсулированного аторвастатина по 10 мг и 1 таблетка аналогичного вида с плацебо) один раз в течение 8 недель двойной слепой терапии.
Первичные и основные вторичные конечные точки
Первичные конечные точки
Основным показателем эффективности является процентное изменение уровней LDL-С, рассчитываемое на 8-ой неделе по сравнению с исходным уровнем, который определяется следующим образом:
100×[(рассчитанное значение LDL-C на 8-ой неделе)-(рассчитанное значение LDL-C в начале исследования)]/(рассчитанное значение LDL-C в начале исследования).
В случае недоступности рассчитанного значения LDL-C на 8 неделе, как определено выше, то расчеты выполняют по последнему значению LDL-C, измеренному во время эффективного периода до 8-ой недели временного окна, это значение (для последнего наблюдения в ходе процедуры [LOCF]) будет использоваться как отсутствующее значение LDL-C для 8-ой недели
Вторичные основные конечные точки
Вторичными показателями эффективности являются следующие:
- Абсолютное изменение (выраженное в ммоль/л и мг/дл), по сравнению с исходным, для рассчитанного значения LDL-C на 8-ой неделе, которое определяется следующим образом:
(рассчитанное значение LDL-C на 8-ой неделе) - (рассчитанное исходное значение LDL-C).
- Процент пациентов с рассчитанным значением LDL-С <70 мг/дл (1,81 ммоль/л) и <100 мг/дл (2,59 ммоль/л) на 8-ой неделе.
- Процентное изменение в ApoB от исходного уровня до 8-ой недели.
- Изменения значений уровней липопротеинов, не относящихся к HDL-C, выраженные в процентах и по абсолютной величине (выраженной в ммоль/л и мг/дл), до 8-ой недели, по сравнению с исходными уровнями.
- Изменения значений уровней триглицеридов, выраженные в процентах и по абсолютной величине (выраженной в ммоль/л и мг/дл), до 8-ой недели, по сравнению с исходными уровнями.
- Процентное изменение в АроА-1 от исходного уровня до 8-й недели.
- Абсолютное изменение соотношения ApoB/ApoA-1 от исходного уровня до 8-й недели.
- Процентное изменение в Lp(а) от исходного уровня до 8-й недели.
Расчет ожидаемых результатов по примеру
Как и ожидалось, в исследовании приняло участие приблизительно 90 пациентов.
Для обнаружения разницы в 20% при изменении уровней LDL-С от исходного до 8-недельного уровня между группой, получавшей 316P 150 мг + аторвастатин 80 мг, и группой плацебо для группы 316P + аторвастатин 80 мг, с ожидаемым не поддающимся оценке 5%-ым уровнем для первичной конечной точки, были оценены результаты для 30 пациентов группы, что приводит к 95%-ой мощности оценки, при стандартном отклонении в 20%, а также использовался двусторонний Т-тест с уровнем значимости 0,05.
Расчеты проводили с использованием программы nQuery Advisor 6.01.
Статистические методы
Оцениваемые популяции
Популяция для оценки эффективности
Первичная популяция для анализа эффективности представляла собой модифицированную популяцию с намерением к лечению (mITT).
Модифицированная популяция с намерением к лечению
Модифицированная ITT (mITT) популяция: рандомизированная популяция с оцениваемой первичной конечной точкой.
Первичная конечная точка была определена при соблюдении двух следующих условий:
- наличие по меньшей мере одного расчетного значение LDL-C с момента посещения 1 (в неделю-1) и до первой IP инъекции.
- наличие по меньшей мере одного расчетного значение LDL-C в течение эффективного периода и в течение 8-недельного окна или до него.
Пациенты в популяции mITT были проанализированы аналогично, как и пациенты в группе, подвергаемой лечению, с выделением рандомизацией.
Популяция для предварительного протокола
Популяция для предварительного протокола (РР) представляла собой подгруппу в популяции mITT, за исключением пациентов:
- со значимыми для протокола отклонениями, влияющими на оценку исходного LDL-C или LDL-C на 8-ой неделе,
- получающих запрещенную терапию, которая может повлиять на уровни липидов в течение периода до лечения или в течение эффективного периода до установления первичной конечной точки,
- с плохой переносимостью антитела 316P при IP введении,
- с плохой переносимостью аторвастатина (без IP) в течение периода до лечения или с непереносимостью аторвастатина при IP в течение 3 дней до установления первичной конечной точки.
Популяция для оценки безопасности
Популяция для оценки безопасности была определена как рандомизированная популяция индивидов, которые фактически IP получали хотя бы одну дозу или частичную дозу антитела 316P, и которые оценивались в соответствии с фактически полученным лечением. Пациенты, которые получили лечение, но не были рандомизированы, не рассматриваются как рандомизированные и не включаются в какую-либо популяцию. Результаты по безопасности в отношении пациентов, получавших лечение, и которые не были рандомизированы, представляются отдельно.
Первичный анализ эффективности
Изменения на 8 неделе/LOCF, выраженные в процентах, по сравнению с исходным уровнем LDL-C, рассчитанное как определено выше, оценивали в популяции mITT с использованием модели ковариационного анализа (ANCOVA) для группы, подвергнутой лечению с фиксируемым эффектом, и исходным уровнем LDL-C, используемым в качестве независимой переменной. Фактор для группы, подвергнутой лечению, имел три уровня: плацебо + аторвастатин 80 мг, антитело 316P 150 мг (E2W) + аторвастатин 10 мг и антитело 316P 150 мг (E2W) + аторвастатин 80 мг.
В рамках модели ANCOVA, группу, получавшую антитело 316P 150 мг (E2W) + аторвастатин 80 мг, сравнивали с группой, получавшей плацебо + аторвастатин 80 мг, используя соответствующие сопоставления и 95%-ый доверительный интервал (CI) для различий.
Не проводилось никаких формальных сравнений для группы, получавшей антитело 316P 150 мг (E2W) + аторвастатин 10 мг: была определена только величина 95%-ого доверительного интервала (95% CI) для различия при сравнении с другими группами.
Анализ эффективности для вторичных основных точек
Было проанализировано непрерывное изменение показателей вторичной эффективности в популяции mITT с использованием модели ANCOVA, как и для первичной конечной точки. Для триглицеридов и липопротеина (Lp(a)), которые, как известно, не имеют распределение Гаусса, использовался ранговый метод ANCOVA.
Бинарные показатели вторичной эффективности были проанализированы в популяции mITT с использованием точной условной модели логистической регрессии для группы, подвергаемой лечению (эффекты), и исходного уровня LDL-C.
Анализ безопасности
Анализ безопасности был основан на регистрации нежелательных явлений (AE), при их наличии, и другой информации, касающейся безопасности, такой как клинические лабораторные данные, основные показатели состояния организма и результаты ЭКГ.
Период TEAE (период лечения тяжелых нежелательных явлений) был определен как время от первой IP-инъекции до последней IP-инъекции + 70 дней (10 недель).
В число нежелательных явлений (AE), представляющих интерес, были включены следующие условия:
- возможные реакции на месте инъекции (HLT "реакции на месте инъекции");
- возможные аллергические реакции (HLGT "аллергические состояния")
- наличие пациентов с LDL-C <25 мг/дл (если таковые имеются) или LDL <15 мг/дл (если таковые имеются).
Другой анализ оценок
Другие оценки конечных точек, определенные ниже, являются исследовательскими переменными. Они включали метаболические и воспалительные параметры:
- абсолютное изменение HbA1c (в %) от исходного уровня до 8 недель;
- абсолютное изменение глюкозы в плазме натощак (ммоль/л) от исходного уровня до 8 недель;
- изменение hs-CRP (высокочувствительный С-реактивный белок) в процентах от исходного уровня до 8 недель.
Конечные точки были обобщены временными точками в группе mITT с использованием описательной статистики. Был построен временной профиль (включая значения LOCF) для каждого параметра по группам лечения с соответствующими стандартными ошибками.
Критерий PCSA (потенциально клинически значимой аномалии) для hs-CRP также был обобщен по группам лечения с использованием описательной статистики.
Результаты
Исследование 2 представляло собой многоцентровое, рандомизированное, двойное слепое, выполняемое в параллельных группах, плацебо-контролируемое 8-недельное исследование, выполненное в США для оценки эффективности и безопасности антител 316P для пациентов с повышенным уровнем холестерина, относящегося к липопротеинам низкой плотности (LDL-C), (≥100 мг/дл или ≥2,59 ммоль/л), при лечении аторвастатином при постоянной дозе 10 мг в течение времени не менее 6 недель. После 8-недельного двойного слепого периода лечения пациенты наблюдались в течение 8-недельного периода наблюдения.
Основная цель исследования заключалась в оценке влияния антитела 316P на уровни LDL-C по сравнению с плацебо при совместном введении с аторвастатином в дозе 80 мг после 8 недель лечения пациентов, с уровнями LDL-С ≥100 мг/дл (≥2,59 ммоль/L), которые ранее получали лечение аторвастатином в дозе 10 мг. Оценка эффективности совместного введения антитела 316P с высокой дозой аторвастатина (80 мг) по сравнению с совместным введением антитела 316P с аторвастатином в дозе 10 мг была одной из вторичных целей. Был оценен режим дозирования антитела 150 мг каждые 2 недели (E2W) по сравнению с плацебо.
Анализ эффективности проводили на 88 пациентах (29 пациентов в группе плацебо + аторвастатин 80 мг, 29 в пациентов в группе антитело 316P 150 мг + аторвастатин 10 мг, и 30 в пациентов в группе антитело 316P 150 мг + аторвастатин 80 мг).
Демографические и исходные характеристики пациентов были схожими для всех групп. Средний возраст пациентов составил 58,0 лет (25,0% пациентов были в возрасте ≥65 лет). Средние исходные уровни LDL-C и общего холестерина составляли соответственно от 3,101 ммоль/л до 3,288 ммоль/л, и от 5,447 ммоль/л до 5,200 ммоль/л.
Эффективность:
Статистически значимое изменение снижения уровня LDL-С, выраженного в процентах, от исходного до 8-недельного, наблюдалась в группе, получавшей антитело 316P 150 мг + аторвастатин 80 мг по сравнению с группой плацебо + аторвастатин 80 мг (средняя разность по методу наименьших квадратов составила -55,8%, р<0,0001). Из-за отсутствия гауссовского распределения и из-за неоднородности дисперсии для первичной конечной точки эффективности, анализ чувствительности был проведен с использованием рангового ковариационного анализа, который показал аналогичные результаты: величина эффекта при оценке группы, получавшей антитело 316P 150 мг + аторвастатин 80 мг, по сравнению с группой плацебо + аторвастатин 80 мг, составила -54,5%, р<0,0001. Значительное снижение по сравнению с исходными значениями были отмечены в обеих группах, где проводили лечение антителом 316P в дозе 150 мг, которое вводили вместе с аторвастатином, при средним снижении, равном -70,4% для группы антитело 316P 150 мг + аторвастатин 10 мг, и - 70,6% для группы антитело 316P 150 мг + аторвастатин 80 мг, по сравнению со средним снижением, равным -26,9%, в группе плацебо + аторвастатин 80 мг.
Соответствующие результаты наблюдали для общего холестерина, ApoB, холестерина, не относящегося к липопротеинам высокой плотности, и для соотношения ApoB/ApoA-1. Для холестерина, не относящегося к липопротеинам высокой плотности, наблюдали увеличение изменения, выраженного в процентах, по сравнению с исходным уровням в обеих группах, где антитело 316P в дозе 150 мг вводили вместе с аторвастатином в дозе 10 мг или 80 мг (средняя разность по методу наименьших квадратов составила +2,6% и +5,8%, соответственно), по сравнению со снижением в группе плацебо + аторвастатин 80 мг (средняя разность по методу наименьших квадратов составила -3,6%).
Безопасность:
Антитело 316P хорошо переносилось в течение 8-недельного лечения во всех группах, получавших лечение. Важно отметить, что во всех группах, получавших лечение, не было отмечено никаких изменений в уровнях тропонина.
Выводы:
Было зарегистрировано статистически значимое изменение снижения, выраженного в процентах, уровня LDL-С от исходного до 8-недельного в группе, получавшей антитело 316P в дозе 150 мг + аторвастатин в дозе 80 мг, по сравнению с группой плацебо + аторвастатин 80 мг (средняя разность по методу наименьших квадратов составила -55,8%, р<0,0001). Аналогичная величина наблюдаемого эффекта для антитела 316P была отмечена независимо от дозы аторвастатина (10 мг или 80 мг) при существенном снижением уровня LDL-С при совместном введении с аторвастатином в указанных двух дозах.
Соответствующие результаты наблюдали для общего холестерина, ApoB, холестерина, не относящегося к липопротеинам высокой плотности, и для соотношения ApoB/ApoA-1. Для холестерина, не относящегося к липопротеинам высокой плотности, наблюдали тенденцию к увеличению в обеих группах, где антитело 316P в дозе 150 мг вводили вместе с аторвастатином в дозе 10 мг или 80 мг.
Введение антитела 316P в дозе 150 мг по режиму E2W хорошо переносилось в течение 8 недель лечения во всех группах пациентов, подвергавшихся лечения. Не было отмечено никаких конкретных сигналов в отношении безопасности лечения.
В данном исследовании была подтверждена эффективность антитела 316P в дозе 150 мг по режиму введения E2W, а также хороший профиль безопасности, независимо от дозы вводимого аторвастатина (10 мг или 80 мг).
Исследование 3
Исследование 3 представляло собой рандомизированное, двойное слепое, плацебо-контролируемое с множеством возрастающих доз, многоцентровое клиническое испытание на пациентах с первичной гиперхолестеринемией.
Цель этого исследования состояла в определении того, является ли полностью человеческое моноклональное антитело против PCSK9 (антитело 316P) эффективным и безопасным при использовании его в качестве первичного или вспомогательного средства для снижения уровней LDL-C у пациентов с гетерозиготной семейной гиперхолестеринемией (HeFH) или с другими формами первичной гиперхолестеринемии, не относящимися к семейной гиперхолестеринемии (не-FH). В этом клиническом испытании участвовал 61 взрослый пациент с документально подтвержденным наличием HeFH (N = 21) или не-FH (N = 30), при этом пациенты находились на диете и принимали постоянную терапию аторвастатином (atorvaRx), или пациенты с не-FH (n=10), которые находились только на диете. Пациенты, принимающие постоянную терапию аторвастатином, имели уровни LDL-С ≥2,6 ммоль/л, а пациенты, которые находились только на диете, имели уровни LDL-С ≥3,4 ммоль/л. Антитело 316P в дозах 50, 100 и 150 мг вводили подкожно (sc) в течение 1, 29 и 43 дней. Первичной конечной точкой была частота и тяжесть лечения нежелательных явлений (TEAE). Первичной конечной точкой эффективности являлась величина изменения уровня LDL-С в сыворотке, выраженная в процентах и абсолютном значении, от исходного уровня до значения при каждом посещении. Дополнительные конечные точки включали уровни аполипопротеина В (Аро-В), общего холестерина, холестерина высокой плотности, холестерина, относящегося к липопротеинам очень низкой плотности (VLDL-C), а также соотношение Аро-В/Apo-A1. Было обследовано 109 пациентов, и 61 пациент был рандомизированы в группы для участия в испытании (14 пациентов в группе, получающих плацебо, 47 пациентов в группе, получающих антитело 316P) со 100%-ым завершением лечения в течение 148 +/- 7 дней, с последующим контролем. По сравнению с группой пациентов с не-FH, группа с FH была моложе по возрасту (средний возраст составлял 40 лет, против 52 лет), в ней было больше мужчин (81% против 57%) и она получала более высокие дозы аторвастатина (52% для дозы 40 мг, против 3%). Базовые уровни LDL-C составляли 3,45, 2,88 и 4,46 ммоль/л в группах FH, не-FH + atorvaRx и не-FH + только диета, соответственно. Лечение антителом 316P вместе со статинами привело к среднему значению снижения уровней LDL-C, выраженному в процентах, на 57-й день равному 35,6%, 50,2% и 57,5%, при дозах 50, 100 и 150 мг, соответственно, в комбинированных группах FH и не-FH. Хотя не проводили никакого статистического анализа, не наблюдали явного различия в ответах между группами FH и не-FH, или в группах, получавших и не получавших статины. Ответы на лечение антителом 316P показаны на фиг.1, фиг.2 и фиг.3. Благоприятные изменения наблюдали в отношении уровней HDL-C и apoA1. Не было замечено никаких серьезных побочных эффектов, и отмечено, что лечение хорошо переносилось в целом. Не было замечено никаких побочных эффектов, связанных с приемом лекарственных препаратов, со стороны печени, на основании тестирования ее функций или других лабораторных показателей.
Это первое мультидозовое испытание, подтверждающее концепцию применения ингибитора PCSK9, для групп пациентов с FH и не-FH при постоянной терапии статинами, показывает, что лечение антителом против PCSK9, в частности, антителом 316P, является перспективным методом лечения для пациентов с повышенным уровнем холестерина, имеющим или не имеющим HeFH, при терапии статинами.
Исследование 4
Это исследование по влиянию антитела 316P, полностью человеческого моноклонального антитела, блокирующего PCSK9, на снижение уровня холестерина у животных, в частности, у самцов сирийских хомячков.
Введение
Печеночный рецептор LDL (LDLR) является основным компонентом для гомеостаза холестерина. PCSK9 регулирует уровень печеночных LDLR за счет увеличения их деградации. Транскрипция LDLR и PCSK9 является повышающе-регулируемой за счет воздействия статинов через SREBP-2, ограничивая тем самым ее величину так, что статины могут снизить уровни LDL холестерина (LDL-C) у человека и, даже в большей степени, у грызунов, где статины не являются эффективными для снижения LDL-C.
Цель
Целью данного исследования было изучение влияния антитела 316P, человеческого моноклонального антитела против PCSK9 человека, как отдельно, так и в комбинации со статинами, на экспрессию печеночного LDLR, и, в итоге, на уровни LDL-C в сыворотке крови.
Результаты
Одна подкожная инъекция антитела 316P (1/3/10 мг/кг) хомячку, приводила к дозозависимому снижению LDL-С в течение более 2 недель. Максимальный эффект на уровни LDL-C (-17/-27/-60%) наблюдался в течение 7 дней. Фармакокинетические данные при введении антитела 316P находятся в соответствии с его дозозависимым влиянием на уровни LDL-C. Лечение аторвастатином, вплоть до максимально переносимой дозы, не влияет на экспрессию печеночных LDLR и не уменьшает уровни LDL-C. Применение антитела 316P совместно с аторвастатином смогло устранить устойчивость экспрессии LDLR к статинам, и сократить уровень LDL-C в сыворотке. Комбинированное лечение оказалось более эффективным, чем лечение одним антителом 316P, при этом было установлено, что применение аторвастатина в отдельности не имеет никакого эффекта.
Выводы
Ингибирование PCSK9 привело к дозозависимому снижению уровней LDL-C у хомяков. Тем не менее, при введении комбинации с обычно неэффективной дозой аторвастатина, потенцированного снижения уровней LDL-C не наблюдалось. Эти данные позволяют предположить, что нейтрализация PCSK9 является эффективным для устранения устойчивости к статинам, которая наблюдается в животной модели на хомячках. Эти данные находятся в соответствии с результатами первой фазы исследований на человеке, где значение снижения уровней LDL-C превысило величину 60% и продолжалось в течение 30 дней после однократного IV введения. Это подтверждает, что хомячок является удобной моделью для исследования препаратов, для которых PCSK9 является мишенью.
Исследование 5
Это рандомизированное, двойное слепое, плацебо-контролируемое, несимметричное (2:1, для 316P:плацебо), исследование с параллельными группами, с открытым (без плацебо) продолжением.
Цель (цели)
Основная цель данного исследования заключается в оценке долгосрочной безопасности и переносимости антитела 316P после основного периода лечения пациентов с гиперхолестеринемией, имеющих риск сердечно-сосудистых заболеваний, которые должным образом не контролировались в ходе гиполипидемического лечения.
Вторичные цели
- оценка долгосрочной безопасности и переносимости антитела 316P после полного периода исследования;
- оценка влияния антитела 316P на уровни LDL-C после 12 недель лечения по сравнению с плацебо;
- оценка долгосрочной эффективности антитела 316P на уровни LDL-C;
- оценка влияния антитела 316P на общий холестерин (ТС), на холестерин, не относящийся к липопротеинам высокой плотности (non-HDL-C), на аполипопротеин В (ApoB), на HDL-C, на триглицериды (TG), на аполипопротеин А-1 (АроА-1), на соотношение ApoB/ApoA-1, и на липопротеин а (Lp (а)) после 12 недель лечения, по сравнению с плацебо, и после длительного лечения;
- оценка образования антител против антитела 316P.
- оценка фармакокинетики (РК) антитела 316P.
- изучение влияние антитела 316P на зарегистрированные сердечно-сосудистые проявления в течение основного периода лечения, по сравнению с плацебо, и после полного периода исследования.
Структура исследования
Пациенты будут стратифицированы в популяцию с гетерозиготной семейной гиперхолестеринемией (heFH), где пациенты ранее имели случаи инфаркта миокарда (MI) или инсульта, по уровню интенсивности терапии статинами (например, аторвастатин в дозе от 40 мг до 80 мг в день или розувастатин в дозе от 20 мг до 40 мг в день) и по географическим регионам. Пациенты, рандомизированные в группу 316P, будет получать подкожных инъекции (sc) антитела 316P дозой 150 мг каждые 2 недели. Эти доза и режимы дозирования, оцениваемые на первой фазе программы, также относятся к оцениваемым показателям на второй фазе программы. В настоящем исследовании была выбрана доза и режим дозирования, состоящий в подкожном введение 150 мг антитела 316P каждые 2 недели, как обеспечивающие наибольшее системное воздействие 316P в диапазоне доз и режимов введения, которые, вероятно, будут эффективными. При необходимости эти дозы и режимы могут быть скорректированы в ходе исследования на другие дозы и периодичности введения, путем поправки к протоколу, когда станет доступным полный набор данных о предполагаемых дозах и режимах введения.
Исследование состоит из следующих стадий:
● скрининговый период продолжительностью до 2 недель, включающий промежуточные посещения, в ходе которых пациент или другое назначенное лицо (например, супруг, родственник и т.п.) будет обучен самостоятельно выполнять инъекции с помощью плацебо;
● период двойного слепого исследования в течение 18 месяцев лечения антителом 316P или с применением плацебо, для всех пациентов;
- основной период лечения определяется целью первичного анализа, и этот период, который заканчивается через 12 месяцев после завершения лечения последнего пациента (LPI), является рандомизированным по охвату пациентов с различной длительностью двойного слепого лечения, и составляет от 12 до 18 месяцев;
- открытый (т.е. без использования плацебо) период (OLP), который состоит из исследования по лечения пациентов с помощью антитела 316P, которые завершили 18-месячный периода двойного слепого лечения. Продолжительность OLP будет различной, и этот период заканчивается для всех пациентов через 24 месяцев после LPI или через 39 месяцев после FPI (завершение лечения первого пациента), в зависимости от того, что наступит раньше;
- период продолжения (без лечения) в течение 8 недель после окончания открытого периода.
Пациенты будут проинструктированы о приеме постоянной диеты (диеты NCEP-ATPIII TLC или ее эквивалента) в течение всего времени исследования, начиная с момента скрининга. Дозы статинов, а также дозы других принимаемых гиполипидемических средств (если применимо) должны быть постоянными в течение всего периода исследования. Во время периода двойного слепого лечения разрешается модификация режима при определенных условиях. Во время открытого периода модификации режима базируются на мнении исследователя. Во время исследования исключается прием фибратов (за исключением фенофибрата). Во время периода двойного слепого лечения данные об уровнях липидов будут скрыты от исследователя.
ИССЛЕДОВАНИЕ ПОПУЛЯЦИИ ПАЦИЕНТОВ
Критерии включения
Пациенты, относящиеся к категории А или В, как указано ниже, и состояние которых не контролируется должным образом при постоянном применении максимально переносимой дозы статинов в течение по меньшей мере за 6 недель до скринингового визита (в неделю-2), с применением или без применения другой гиполипидемической терапии (LLT).
А) пациенты с гетерозиготной семейной гиперхолестеринемией (heFH);
или
B) пациенты с несемейной гиперхолестеринемией (не-FH), имеющие диагностированную ишемическую болезнь сердца (CHD) или эквивалентный риск развития CHD.
Примечания
- Все применяемые до лечения LLT, включающие любые иные терапии, кроме применения статаинов, должны выполняться с применением постоянной дозы в течение не менее 6 недель до скринингового визита (неделя -2).
- При проведения исследования допустимыми статинами являются симвастатин, аторвастатин и розувастатин, принимаемые ежедневно.
- Пациенты имеют право принимать участие в исследовании, если они имеют максимальную переносимость статинов, даже если принимаемый статин не относится к числу высокоэффективных статинов. Максимальная переносимость статинов определяется как любая максимальная переносимая суточная доза симвастатина, аторвастатина и розувастатина. Высокоэффективный статин определяется как аторвастатин в дозе от 40 мг до 80 мг в день или розувастатин в дозе от 20 мг до 40 мг в день.
- Если пациент не принимает высокоэффективные статины в период скрининга, то причина этого должна быть задокументирована (т.е. наличие миалгии, нарушения печеночных ферментов и т.п.).
- Если в период скрининга (посещение на неделе-2) уровни LDL-C составляют ≥160 мг/дл (4,14 ммоль/л), пациенту должны были быть предложена другая LLT до проведения исследования, в дополнение к максимально переносимому статину. Кроме того, если пациенты получают только терапию максимально переносимым статином, то причина этого должна быть задокументирована, при этом эти пациенты сохраняют право участия в исследовании, и не исключаются из него.
- Для включения в исследование не допускаются пациенты, принимающие симвастатин в суточной дозе более 80 мг, аторвастатин в суточной дозе более 80 мг или розувастатин в суточной дозе более 40 мг.
- Прием симвастатина в дозе 80 мг допускается только для пациентов, которые принимали эту дозу в течение 12 месяцев и более без признаков повреждения мышц (миопатии), и не должно применяться в отношении пациентов, включая пациентов, которые уже принимают низкие дозы препарата.
- Предписания при других LLT должны осуществляться в соответствии с этикеткой (инструкцией) на продукте, утвержденной соответствующим национальным органом по контролю за лекарствами.
Основные критерии исключения
- уровни LDL-С <70 мг/дл (<1,8 ммоль/л) при скрининговом визите (неделя-2);
- уровни TG >350 мг/дл (>3,95 ммоль/л) при скрининговом визите (неделя-2);
- использование иных фибратов, кроме фенофибрата, в течение 6 недель до скринингового визита (неделя-2) или планирование его приема.
Ожидаемое общее количество пациентов
Примерно 2100 рандомизированных пациентов (1400:700, для групп 316P:плацебо)
Исследование лечения
Исследуемый лекарственные продукт(ы): антитело 316P и плацебо в течение курса применения антитела 316P.
Антитело 316P представляет собой полностью человеческое антитело, содержащее HCVR, как показано в последовательности SEQ ID NO: 90 и LCVR, как показано в последовательности SEQ ID NO: 92 списка последовательностей. Последовательности CDR показаны в SEQ ID NO: 76, 78 и 80 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO: 84, 86 и 88 (CDR1, CDR2, CDR3 легкой цепи).
Альтернативно, исследование может быть выполнено с использованием антитела 300N (т.е. резервного соединения) вместо антитела 316P. Антитело 300N является полностью человеческим антителом, содержащим HCVR, как показано последовательности в SEQ ID NO: 218 и LCVR, как показано в последовательности SEQ ID NO: 226 списка последовательностей. Последовательности CDR показаны в SEQ ID NO: 220, 222 и 224 (CDR1, CDR2, CDR3 тяжелой цепи), а также в SEQ ID NO: 228, 230 и 232 (CDR1, CDR2, CDR3 легкой цепи).
Составы
Предварительно заполненные шприцы: антитело 316P, 150 мг/мл, или плацебо для антитела 316P.
Пути введения:
- подкожный (sc);
- вводимый объем: 1 мл для общей дозы 150 мг;
- одна подкожная инъекция объемом 1 мл в области живота, бедра или на внешней области плеча (т.е. в области дельтовидной мышцы).
Режим дозирования: доза 150 мг каждые 2 недели
Первичная и вторичная конечная точка(и)
Первичная конечная точка
Параметры безопасности (побочные эффекты [включая зарегистрированные случаи сердечно-сосудистых патологий], лабораторные данные, основные показатели состояния организма и ЭКГ), оцениваемые в течение основного периода лечения.
Главные вторичные конечные точки:
- параметры безопасности (побочные эффекты [включая зарегистрированные случаи сердечно-сосудистых патологий], лабораторные данные, основные показатели состояния организма и ЭКГ), оцениваемые в течение основного периода лечения;
- изменение уровня LDL-С в процентах от исходного уровня до 12-й недели (главная временная точка);
- наличие антител против 316P
- концентрации антитела 316P в сыворотке.
Схема проведения оценки
Оценки пациентов в период скрининга:
- На месте посещения: неделя-2 (поседение для скрининга), неделя-1 (посещение для обучения введения инъекций).
Оценки пациентов в период двойного слепого исследования:
- На месте посещения: неделя 0 (рандомизации посещений = исходный уровень), 4-я неделя, 8-я неделя, 12-я неделя, 16-я неделя, 24-я неделя, 36-я неделя, 52-я неделя/12-й месяц, 64-я неделя/15-й месяц, 78-ая неделя/18-ый месяц (конец периода двойного слепого исследования).
- Телефонные звонки: 2-я неделя*, 20-я неделя, 28-я неделя, 32-я неделя, 40-я неделя, 44-я неделя, 48-я неделя, 56-я неделя, 60-я неделя, 68-я неделя, 72-я неделя и 76-я неделя.
* Примечание: 2-я неделя может стать посещением на месте для дополнительного обучения пациентов по введению инъекций по схеме введения инъекций, как запланировано в двойном слепом исследовании лечения, с помощью комплекта средств, распределенных по IVRS, если это необходимо.
Оценки пациентов в открытом периоде:
- На месте посещения: каждые 12 недель после окончания посещений в период двойного слепого исследования и до конца посещений в период открытого исследования.
- Телефонные звонки: каждые 4 недели между посещениями на месте.
Примечание: В ходе исследования, в рамках проводимой оценки безопасности, комиссия по мониторингу данных (DMC) будет оценивать адекватность частоты посещений и соответствующих процедур, выполняемых в открытом периоде, и выдавать необходимые рекомендации.
Оценки пациентов в последующем периоде
На месте посещения: посещение на 8-й неделя после окончания открытого периода.
Статистический анализ
Для оценки безопасности, объем выборки из 2100 пациентов (соотношение при рандомизации 2:1, т.е. 316P: 1400, плацебо: 700) позволит иметь данные о долгосрочной безопасности в объеме широкой базы данных. При этом выборки из 1050 и 364 пациентов, как ожидается, будут подвергаться лечению с помощью 316P в течение как минимум 12 месяцев и 18 месяцев, соответственно, и оцениваться во время первичного анализа (12 месяцев после последнего пациента). Кроме того, участие 1400 пациентов, которые будут получать антитело 316P, обеспечит уровень нежелательных проявлений ≥0,002, который будет определяться с 95% вероятностью.
Факторы распределения по группам включают: популяцию с heFH, предшествующий инфаркт миокарда (MI) или инсульт, применение высокоэффективных статинов и область проживания (Северная Америка, Западная Европа, Восточная Европа, остальные страны).
Обобщение переменных показателей, характеризующих безопасность, будут выполняться на основе оценок для популяции по изучению безопасности. Популяция по изучению безопасности состоит из рандомизированной популяции индивидов, которые фактически получали хотя бы одну дозу или частичную дозу исследуемого лекарственного средства (IMP), и которые оценивались в соответствии с фактически полученным лечением.
Для подготовки обобщения переменных показателей этого исследования будет использоваться описательная статистика. Для неблагоприятных событий, в дополнение к обобщающим таблицам, где представляются необработанные показатели, будет использоваться таблица всех TEAE (лечения случаев нежелательных явлений), где представлены уточненные показатели, которые получают в течение года от пациента. Если обнаруживают какой-либо клинически значимый сигнал, и необходимо дальнейшее исследования неблагоприятного события или потенциально клинически значимой аномалии (PCSA), которая представляет интерес, анализ времени наступления события будет проведен методом Каплана-Мейера. Кроме того, должны быть предоставлены данные по частоте неблагоприятных событий или PCSA во времени. Первичный анализ безопасности будет сделан на основе безопасности событий, которые можно отнести к случаю лечения при двойном слепом исследовании в основном периоде. Вторичный анализ безопасности будет проводиться на основе безопасности событий, наблюдаемых во время двойного слепого исследования и в течение открытого периода.
Популяция для анализа эффективности будет представлять собой модифицированную популяцию с намерением к лечению (mITT), определяемую как популяция ITT (т.е. рандомизированная популяция) с оцениваемой конечной точкой по уровню LDL-C. Эта конечная точка будет считаться как оцениваемая, при соблюдении двух следующих условий:
- доступно значение LDL-C на исходном уровне;
- по меньшей мере одно значение уровня LDL-С получено в основном периоде оценки эффективности.
Основной период оценки эффективности будет определяться следующим образом:
- время от первой инъекции IMP (за исключением периода обучения по введению инъекций) до последней инъекции IMP плюс 21 день для пациентов, которые окончательно прекратят инъекции IMP до 12 недели.
- время от первой инъекции IMP (за исключением периода обучения по введению инъекций) до 12-ой недели для пациентов, которых получали лечение по меньшей мере в течение 12 недель.
Пациенты в популяции MITT будут проанализированы в соответствии группой лечения, с распределением путем рандомизации.
Изменение уровня LDL-С, выраженное в процентах, от исходного уровня до 12-ой недели (основная вторичная конечная точка) и для других временных точек в ходе всего исследования (другие вторичные конечные точки), будут проанализированы с помощью модели ковариационного анализа (ANCOVA) для группы лечения, и каждый фактор распределения (популяция с HeFH, предшествующий инфаркт миокарда (MI) или инсульт, применение высокоэффективных статинов и область проживания) будет рассматриваться как фиксированный эффект, а исходный уровень LDL-C будет рассматриваться как независимая переменная. Фактор для группы лечения будет иметь 2 уровня: плацебо и антитело 316P. В рамках всей модели ANCOVA, группа, получающая антитело 316P будет сравниваться с группой, получающей плацебо, с использованием соответствующих различий, так чтобы получить 95%-ый доверительный интервал (CI) для различий.
В случае отсутствия показателя для уровня LDL-С на 12-ой неделе в период лечения, будет использоваться принцип переноса последнего зарегистрированного значения наблюдения (LOCF).
Продолжительность периода исследования (для одного пациента)
Продолжительность исследования для каждого пациента является переменной. Максимальная продолжительность исследования включает: до 2 недель периода скрининга, 18 месяцев лечения в период двойного слепого исследования, до 21 месяцев лечение антителом 316P в открытый период (в зависимости от того, когда пациент был рандомизирован в исследование, и от продолжительности набора) и 8 недель последующего периода. Таким образом, максимальная продолжительность исследования составляет до приблизительно 42 месяцев для первого пациента, рандомизированного в исследование, и до приблизительно 27 месяцев для последнего пациента, рандомизированного в исследование.
Исследование 6
Рандомизированное, двойное слепое, мультидозовое, плацебо-контролируемое исследование с привлечением 75 пациентов из числа пациентов с гетерозиготной семейной гиперхолестеринемией (heFH). В этом исследовании пациенты должны соответствовать критериям Всемирной Организации Здравоохранения для heFH, постоянно ежедневно принимать статины в течение по меньшей мере 6 недель до начала исследования, и иметь уровень LDL-С сыворотке крови ≥100 мг/дл. Пациентам было разрешено принимать эзетимиб в дополнение к ежедневному приему статина. Первичной конечной точкой исследования является изменение уровня LDL-С от исходного значения, в сравнении с плацебо, в течение 12-недельного периода исследования.
Промежуточный анализ, выполненный в рамках исследования 6 для группы пациентов с гетерозиготной семейной гиперхолестеринемией и с повышенным уровнем холестерина (LDL-C ≥100 мг/дл), принимающим постоянные дозы статинов с эзетимибом или без него, показал, что у пациентов, получавших антитело 316P каждые две или четыре недели, достигнуты значительно большие средние значения снижения уровней LDL-C на 12-й неделе, по сравнению с пациентами, получавшими плацебо. У пациентов, получавших различные дозы антитела 316P, на 12-й неделе, которая была первичной конечной точкой исследования, достигнуты средние значения снижения уровней LDL-C на величину, равную от приблизительно 30% до более чем 60%, по сравнению с исходным уровнем, при 10%-ным снижением в группе плацебо (р<0,01). Промежуточный анализ был выполнен, когда все пациенты достигли первичной конечной точки на 12-й неделе.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ЧЕЛОВЕКА К PCSK9 ДЛЯ ПРИМЕНЕНИЯ В СПОСОБАХ ЛЕЧЕНИЯ КОНКРЕТНЫХ ГРУПП ИНДИВИДУУМОВ | 2012 |
|
RU2603481C2 |
| АНТИТЕЛА ЧЕЛОВЕКА К PCSK9 ДЛЯ ПРИМЕНЕНИЯ В СПОСОБАХ ЛЕЧЕНИЯ КОНКРЕТНЫХ ГРУПП ИНДИВИДУУМОВ | 2012 |
|
RU2721279C2 |
| ВЫСОКОАФФИННЫЕ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К PCSK9 | 2009 |
|
RU2552169C2 |
| ВЫСОКОАФФИННЫЕ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К PCSK9 | 2009 |
|
RU2697773C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ХОЛЕСТЕРИНОМ | 2021 |
|
RU2832333C1 |
| СПОСОБЫ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ГЕТЕРОЗИГОТНОЙ СЕМЕЙНОЙ ГИПЕРХОЛЕСТЕРИНЕМИЕЙ (HEFH) | 2015 |
|
RU2735521C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ВЫСОКИМ РИСКОМ ВОЗНИКНОВЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ, ИМЕЮЩИХ ГИПЕРХОЛЕСТЕРИНЕМИЮ | 2015 |
|
RU2723018C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ГИПЕРЛИПИДЕМИИ У ПАЦИЕНТОВ С ДИАБЕТОМ ПОСРЕДСТВОМ ВВЕДЕНИЯ ИНГИБИТОРА PCSK9 | 2018 |
|
RU2772712C2 |
| ЛЕЧЕНИЕ АНТИТЕЛАМИ ПРОТИВ PCSK9 | 2012 |
|
RU2576034C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРА PCSK9 ДЛЯ СНИЖЕНИЯ СЕРДЕЧНО-СОСУДИСТОГО РИСКА | 2019 |
|
RU2837845C2 |













































































































































































































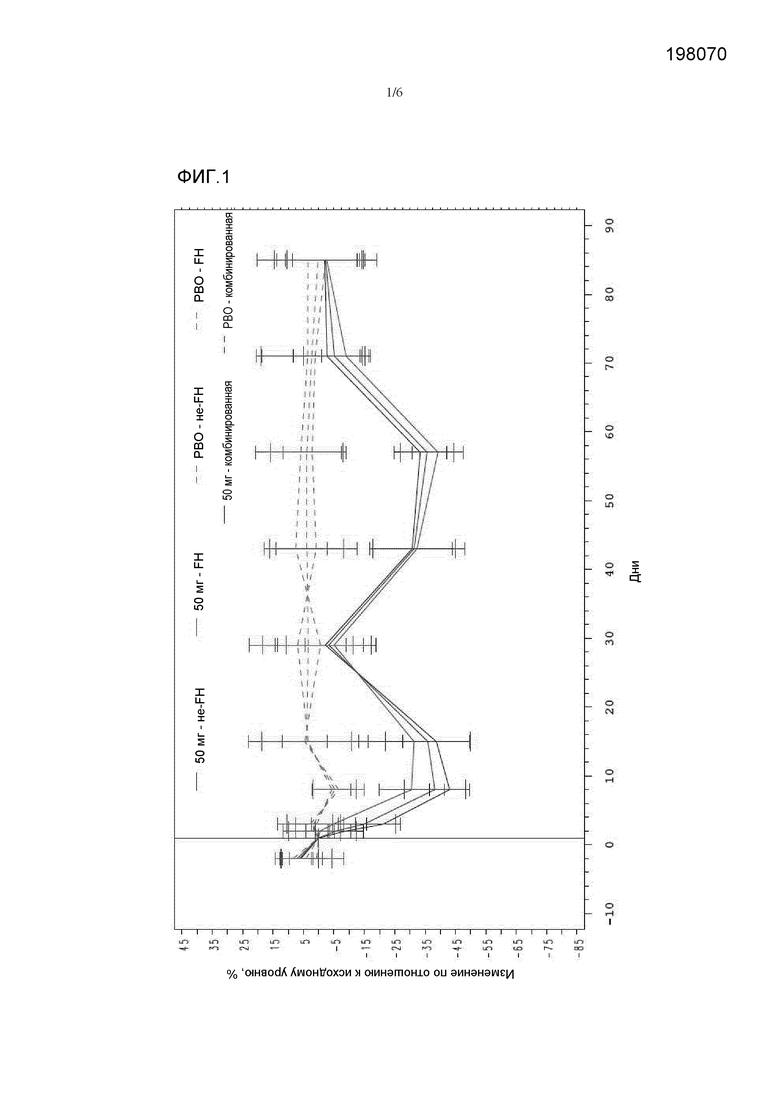
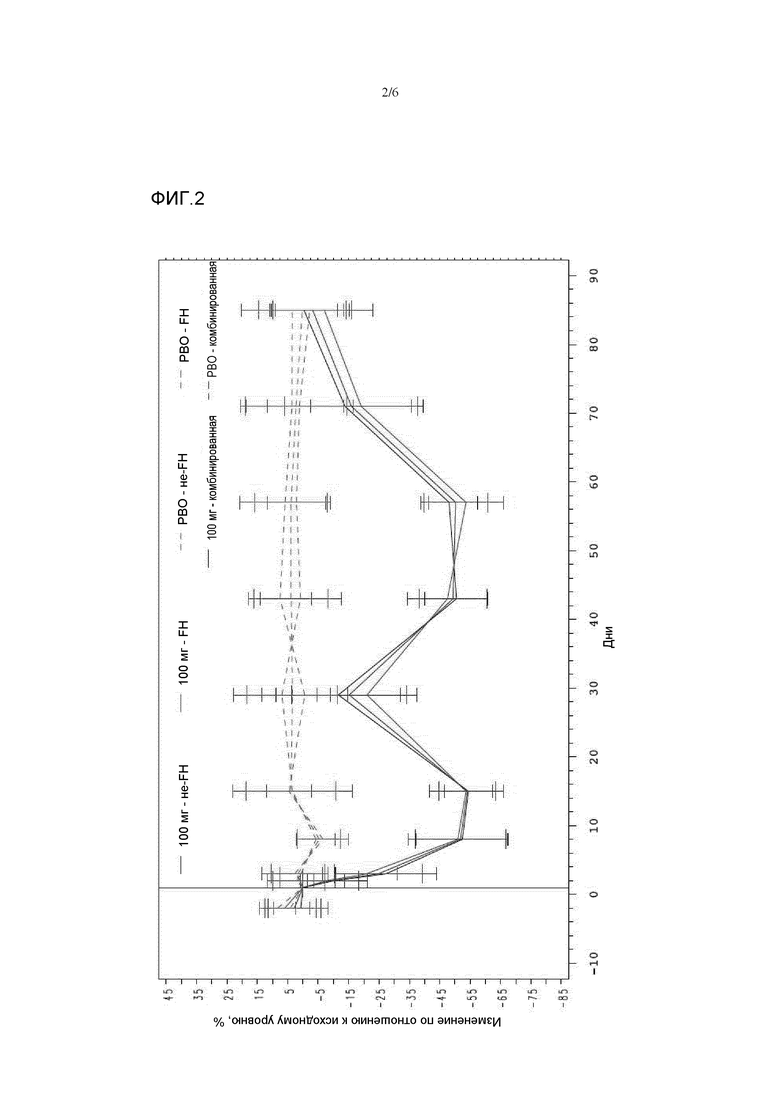
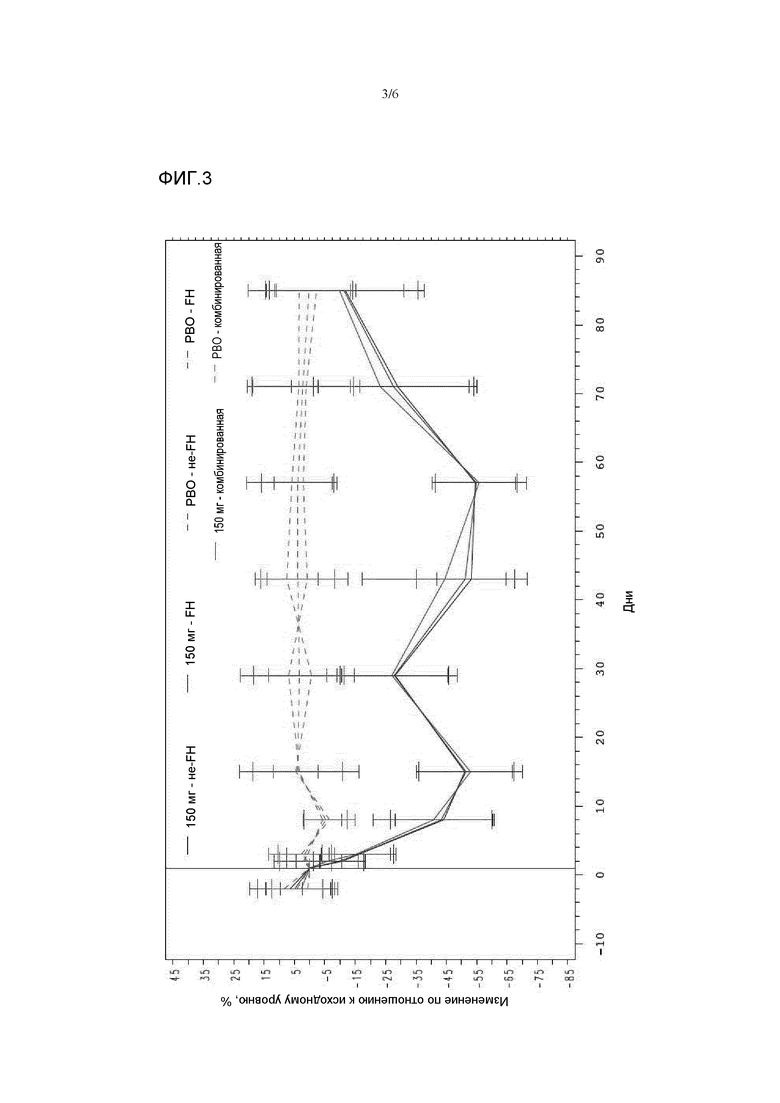
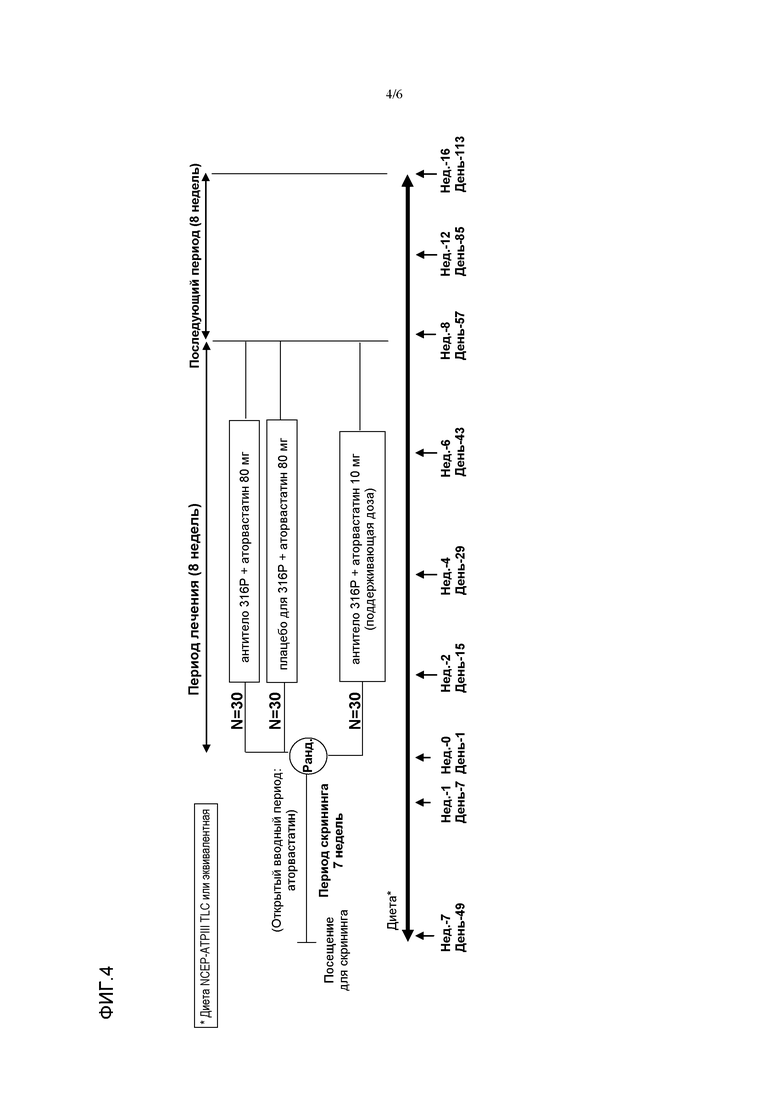
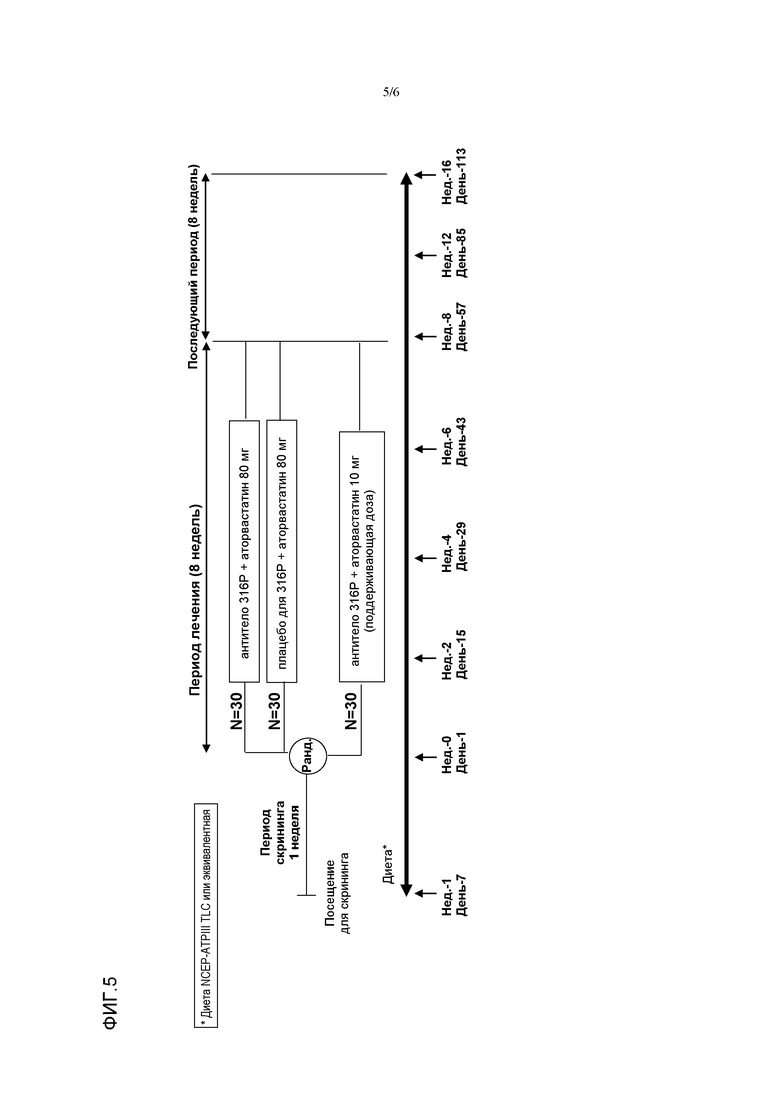
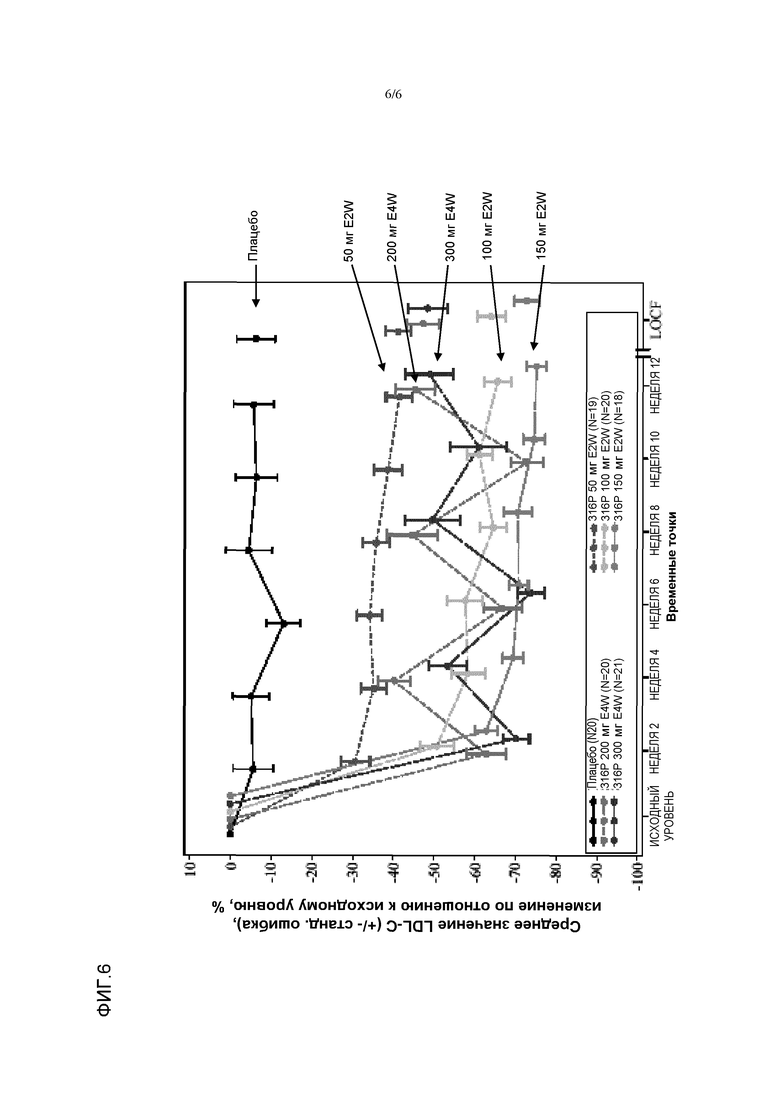
Группа изобретений раскрывает фармацевтические композиции для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9, содержащие антитело, которое специфически связывается с человеческим пропротеином конвертазы субтилизина/кексина типа 9 (PCSK9). Применение композиций согласно группе изобретений обеспечивает эффективное снижение уровня LDL-C, увеличение уровня холестерина HDL в сыворотке, снижение одного или нескольких из: уровней общего холестерина, уровней АроВ, уровней холестерина, не относящегося к HDL-C, соотношения Аро-В/АроА-1. 4 н. и 15 з.п. ф-лы, 6 ил., 1 табл., 6 пр.
1. Фармацевтическая композиция для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9, содержащая фиксированную дозу 75, 150 или 300 мг антитела или его антиген-связывающего фрагмента, которое специфически связывается с пропротеином конвертазы субтилизина/кексина типа 9 человека (hPCSK9), и фармацевтически приемлемый эксципиент или носитель, где антитело или его антигенсвязывающий фрагмент
(a) содержит три CDR тяжелой цепи, определенные в SEQ ID NO: 76, 78 и 80, и три CDR легкой цепи, определенные в SEQ ID NO: 84, 86 и 88; или
(b) конкурирует за связывание с hPCSK9 с антителом или его антиген-связывающим фрагментом, содержащим три CDR тяжелой цепи, определенные в SEQ ID NO: 76, 78 и 80, и три CDR легкой цепи, определенные в SEQ ID NO: 84, 86 и 88.
2. Фармацевтическая композиция по п. 1, где антитело или его антигенсвязывающий фрагмент
(a) содержит аминокислотную последовательность вариабельной области тяжелой цепи (HCVR) и аминокислотную последовательность вариабельной области легкой цепи (LCVR), определенные в SEQ ID NO: 90 и 92, соответственно; или
(b) конкурирует за связывание с hPCSK9 с антителом или его антиген-связывающим фрагментом, которое содержит аминокислотную последовательность вариабельной области тяжелой цепи (HCVR) и аминокислотную последовательность вариабельной области легкой цепи (LCVR), определенные в SEQ ID NO: 90 и 92, соответственно.
3. Фармацевтическая композиция по п. 1, содержащая фиксированную дозу 75 мг антитела или его антиген-связывающего фрагмента.
4. Фармацевтическая композиция по п. 1, содержащая фиксированную дозу 150 мг антитела или его антиген-связывающего фрагмента.
5. Фармацевтическая композиция по п. 1, содержащая фиксированную дозу 300 мг антитела или его антиген-связывающего фрагмента.
6. Фармацевтическая композиция по п. 1, где 1 мл раствора для инъекции содержит фиксированную дозу 75 мг, 150 мг, или 300 мг антитела или его антигенсвязывающего фрагмента.
7. Фармацевтическая композиция по п. 6, где раствор для инъекции содержит фиксированную дозу 75 мг антитела или его антигенсвязывающего фрагмента.
8. Фармацевтическая композиция по п. 6, где раствор для инъекции содержит фиксированную дозу 150 мг антитела или его антигенсвязывающего фрагмента.
9. Фармацевтическая композиция по п. 6, где раствор для инъекции содержит фиксированную дозу 300 мг антитела или его антигенсвязывающего фрагмента.
10. Фармацевтическая композиция по п. 1, представленная в виде лекарственной формы, где лекарственная форма содержит фиксированную дозу 75 мг, 150 мг или 300 мг антитела или его антиген-связывающего фрагмента.
11. Фармацевтическая композиция по п. 10, где лекарственная форма содержит фиксированную дозу 75 мг антитела или его антиген-связывающего фрагмента.
12. Фармацевтическая композиция по п. 10, где лекарственная форма содержит фиксированную дозу 150 мг антитела или его антиген-связывающего фрагмента.
13. Фармацевтическая композиция по п. 10, где лекарственная форма содержит фиксированную дозу 300 мг антитела или его антиген-связывающего фрагмента.
14. Фармацевтическая композиция по п. 1, где фармацевтическая композиция находится в герметически закрытом контейнере, выбранном из группы, состоящей из флакона, саше, предварительно заполненного шприца или автоинъектора, картриджа для многоразового шприца и аппликатора.
15. Фармацевтическая композиция по п. 1, где антитело или его антигенсвязывающий фрагмент связывает эпитоп, содержащий один или несколько аминокислотных остатков в положениях 153, 159, 238 и 343 hPCSK9 (SEQ ID NO: 755).
16. Фармацевтическая композиция по п. 1, где антитело или его антигенсвязывающий фрагмент при введении субъекту обеспечивает одно или несколько из следующего:
(a) снижение LDL-C от по меньшей мере 60% до по меньшей мере 75% относительно уровня до введения дозы с устойчивым снижением на протяжении периода по меньшей мере на 14 дней после введения субъекту дозы в 150 мг каждые две недели;
(b) снижение LDL-C от по меньшей мере 50% до по меньшей мере 75% относительно уровня до введения дозы с устойчивым снижением на протяжении периода по меньшей мере на 28 дней после введения субъекту дозы в 300 мг каждые четыре недели;
(c) увеличение уровня холестерина HDL в сыворотке по меньшей мере на 2%, по меньшей мере на 2,5%, по меньшей мере на 3%, по меньшей мере на 3,5%, по меньшей мере на 4%, по меньшей мере на 4,5%, по меньшей мере на 5% или по меньшей мере на 5,5% относительно уровня до введения дозы в 150 мг каждые две недели; и
(d) снижение одного или нескольких из: уровней общего холестерина, уровней АроВ, уровней холестерина, не относящегося к HDL-C, соотношения Аро-В/АроА-1.
17. Фармацевтическая композиция для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9, содержащая фиксированную дозу 75 мг антитела или его антиген-связывающего фрагмента, которое специфически связывается с hPCSK9, где антитело или его антиген-связывающий фрагмент содержит аминокислотную последовательность вариабельной области тяжелой цепи (HCVR) и аминокислотную последовательность вариабельной области легкой цепи (LCVR), определенные в SEQ ID NO: 90 и 92, соответственно, и где антитело или его антигенсвязывающий фрагмент находятся в 1 мл раствора для инъекции.
18. Фармацевтическая композиция для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9, содержащая фиксированную дозу 150 мг антитела или его антиген-связывающего фрагмента, которое специфически связывается с hPCSK9, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность вариабельной области тяжелой цепи (HCVR) и аминокислотную последовательность вариабельной области легкой цепи (LCVR), определенные в SEQ ID NO: 90 и 92, соответственно, и где антитело или его антигенсвязывающий фрагмент находится в 1 мл раствора для инъекции.
19. Фармацевтическая композиция для лечения заболеваний или состояний, которые вызываются воздействием экспрессии или активности PCSK9, содержащая фиксированную дозу 300 мг антитела или его антиген-связывающего фрагмента, которое специфически связывается с hPCSK9, где антитело или его антигенсвязывающий фрагмент содержит аминокислотную последовательность вариабельной области тяжелой цепи (HCVR) и аминокислотную последовательность вариабельной области легкой цепи (LCVR), определенные в SEQ ID NO: 90 и 92, соответственно, и где антитело или его антигенсвязывающий фрагмент находится в 1 мл раствора для инъекции.
| WO2008057458 A2, 15.05.2008 | |||
| WO2008063382 A2, 29.05.2008 | |||
| US2008008697 A1, 10.01.2008 | |||
| C | |||
| J | |||
| DUFF et al | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Biochem J | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ ПУСКА В ХОД АВИАЦИОННЫХ МОТОРОВ | 1924 |
|
SU577A1 |
Авторы
Даты
2016-12-10—Публикация
2012-01-27—Подача