Предметом изобретения являются новые соединения с фенильной и амидными группами (или их гомологи), способ их получения, использование новых соединений в качестве агента для защиты растений от грибковых болезней, промежуточные продукты для их получения и способы получения промежуточных продуктов.
В настоящем описании все приведенные формулы приведены в конце текста описания. Термин низший, примененный к радикалам, имеющим углеродную цепь, означает, что в этой углеродной цепи имеется от одного до четырех атомов углерода (или от 2 до 4 атомов углерода в ненасыщенных углеродных цепях).
Новые продукты в соответствии с изобретением имеют формулу (I), в которой:
знак цикл, окруженный полукругом, представляет, вместе с двумя атомами углерода, к которым этот полукруг присоединен, углеродный или гетероциклический цикл, имеющий от 4 до 7 звеньев (предпочтительно 5 или 6), имеющий, по крайней мере, одну ненасыщенную связь этиленового или ароматического характера, между двумя атомами углерода, носителями группы -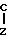 =Y и фенильной группой, указанный цикл может быть замещен органическими радикалами, которые имеют не более 30 атомов углерода,
=Y и фенильной группой, указанный цикл может быть замещен органическими радикалами, которые имеют не более 30 атомов углерода,
Y атом кислорода или серы,
Z атом хлора, группа OW', NHR1 или NR1R2 (соединения, в формуле которых Z представляет собой NR1R2, являются предпочтительными для борьбы с болезнями растений, и соединения, в которых Z является атомом хлора, группой или группой NHR' в основном полезны как промежуточные химические вещества),
W' атом водорода или низший алкильный радикал, или щелочной, или щелочноземельный металл,
R1R2 идентичные или различные представляют собой:
низший алкильный радикал или низший алкокси радикал (по крайней мере, один из радикалов R1 и R2 является отличным от алкокси), или циклоаксильный, имеющий от 3 до 7 атомов углерода, в случае необходимости эти радикалы замещаются, по крайней мере, одним атомом галогена и/или низшей группой гидрокси, или низшим алкокси, или алкокси (низшей) алкил (низшей), или ацилокси (низшей) группой или фенильной, или гетероциклической группы с 4-6 звеньями, включающими 1 или 2 гетероатома (O, N, S) или группой амино, моно- или дизамещенной низшими алкилами;
алкенильный или алкинильный радикал, имеющий от 3 до 7 атомов углерода,
или же R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетероцикл, насыщенный или ненасыщенный, содержащий от 4 до 7 звеньев (предпочтительно 5 или 6) и 1,2 или 3 гетероатома (0, N или S), причем этот гетероцикл может быть замещен группами низший алкил или низший алкокси или гидрокси, или радикалом оксо, или одним или несколькими атомами галогена, или группой алкил (низший) алкокси (низшая)
R3, R4, R5 идентичные или различные, представляют собой:
атом водорода или галогена, по крайней мере, один из этих радикалов R3, R4, R5 иной, чем атом водорода или галогена;
группа амино, в случае необходимости замещенная одной или двумя низшими алкильными группами;
группа низшего алкила или низшего алкокси, или алкил (низший) алкокси (низший), или низший алкилтиорадикал, в случае необходимости гидроксисодержащий или галогенсодержащий,
R3 и R4 (в положении мета и пара) могут образовывать вместе единый двухвалентный радикал с 3 или 4 звеньями, включающий 1 или 2 невицинальных атома кислорода.
Изобретение особенно относится к соединениям, полезным при борьбе с грибковыми поражениями растений. Это соединения формулы I, в которых Z означает NR1R2 и в которых различные радикалы и заместители выбирают по типу и положению, таким образом, чтобы десятичный логарифм (log P) их коэффициента разделения октанол/вода (Р) был бы равен от 2 до 5, предпочтительно от 2,5 до 4,5.
Коэффициент разделения октанол/вода Р химического продукта определяется известными методами.
Экспериментально этот коэффициент является отношением концентраций равновесия вещества, растворенного в двухфазной системе, образованной двумя несмешиваемыми растворителями, октанол и вода, т.е.
Р С октанол/С вода.
Измерение проводится при 20оС при трех различных концентрациях и трех различных соотношениях фаз, причем считается, что для этих трех концентраций и для этих трех соотношений фаз должна быт получена одна и та же величина Р. Если имеется продукт, более растворимый в воде, то готовят три водных раствора этого продукта с концентрациями 0,25; 0,5 и 1 г/л, и каждый из этих растворов смешивают с октанолом в таком количестве, чтобы объемное отношение водного раствора продукта к октанолу было соответственно 80/20, 90/10 и 95/5. Затем эти смеси перемешивают, декантируют и измеряют в каждой из них количество растворенного продукта методом высококачественной жидкостной хроматографии, и коэффициент разделения определяют в соответствии с приведенной выше формулой.
Наоборот, если продукт больше растворяется в октаноле, то готовят три октаноловых раствора этого продукта при концентрациях 0,25; 0,5 и 1 г/л, и каждый из этих растворов смешивают с водой в таком количестве, чтобы объемное отношение октанолового раствора продукта к воде было равно соответственно 80/10, 90/10 и 95/5.
Если продукты очень мало растворимы как в воде, так и в октаноле, так что ни для одного из них нельзя достигнуть концентрации 0,25; 0,5 и 1 г/л, то работают с более низкими концентрациями, например 0,05; 0,1 и 0,2 г/л, или с еще более низкими.
Таким образом, в этих условиях получают три величины Р, которые должны быть идентичными (если они разные, то берут более низкие концентрации, которые позволяют получить три одинаковые величины), и этой единой величине, общей для трех измерений, соответствует коэффициент разделения Р (или его логарифм log P), который характеризует продукт.
Однако на практике стало общим правилом заменять это измерение коэффициента разделения на величину, полученную расчетом на основе структуры молекулы. Указания о методах расчета приведены Ханшем и Лео в книге "Константы замещения для корреляционного анализа в химии и биологии" (C.Hanseh, A.Leo. "Substituent Constants for Correlation Analysis in Chemistry and Biology, 1979, стр.18-43). Этот метод немного развился за последние годы, не только в направлении уточнения, т.е. большего приближения к реальной величине, получаемой прямым измерением. Так, метод расчета коэффициента разделения был усовершенствован, чтобы учитывать корректирующие факторы взаимодействий (A. Leo, I.Chem. Pernin Trans. II рр.825-838, 1983). Для облегчения расчетов были подготовлены в продажу программы для вычислительных машин, которые непосредственно сами осуществляют расчет коэффициента разделения (log P). В настоящей работе использованы величины, полученные при помощи программы "Medchem" описанной в "Medchem Software Manual, release 3.52" nov. 1987 ed. Pomona College a claremont. Galifornia). Даже если в будущем эта программа для ЭВМ будет развиваться, то ее развитие будет идти в направлении большего приближения к экспериментальной величине log.P. Принцип замены измеренной величины, рассчитанной величиной log P, стал настолько общим, что этот метод принят Агентством по охране окружающей среды США. В настоящем тексте используются величины log P, рассчитанные, как описано выше.
В дальнейшем тексте, если указывается значение многократных радикалов, например (Rn), т. е. радикал R, взятый n раз, то подразумевают, в общем случае, что разные радикалы R могут быть одинаковыми или разными, это же относится ко всем типам радикалов и заместителей.
Среди большой группы соединений формулы I особенно предпочтительны различные подгруппы. Так, предпочтительны соединения, имеющие одну или другую, или несколько следующих характеристик:
R1 и R2 представляют:
низший алкильный радикал, циклоалкильный радикал, имеющий от 3 до 7 атомов углерода, алкенильный или алкинильный радикал, имеющий от 3 до 7 атомов углерода, алкоксиалкильный радикал, имеющий от 3 до 8 атомов углерода;
или R1 и R2 могут образовывать вместе с атомом азота, с которым они связаны, насыщенный или ненасыщенный гетероцикл, имеющий от 4 до 7 звенев и 1 или 2 гетероатома (O, N, S), причем этот гетероцикл может быт замещен алкильными радикалами, имеющими от 1 до 3 атомов углерода, или алкоксиалкильными группами с 2-4 атомами углерода;
R3, R4, R5 находятся соответственно в положениях, мета, пара и мета в фенильной группе, замещающей цикл (эти положения обозначаются по отношению к валентной связи, соединяющей указанную фенильную группу с указанным циклом),
R3, R4, R5 представляют собой атом водорода или галогена (по крайней мере, один из этих трех радикалов иной, чем атом водорода или галогена), или низший алкильный радикал, или низший алкокси радикал, или алкоксиалкил, имеющий от 2 до 4 атомов углерода, или низший алкилтио, или гидрокси, или группа амино, монозамещенная или дизамещенная низшим алкильным радикалом, или
R3, R4 (в положениях мета и пара) могут вместе образовывать один двухвалентный радикал с 3 или 4 звеньями, включающий 1 или 2 невидинальных атома кислорода,
знак цикл, окруженный полукругом, представляет двухвалентный радикал -К6-К7-К8-К9- или -К6-К7-К10-, так чтобы образовывать вместе с двумя атомами углерода, с которыми он связан, цикл с 5 или 6 звеньями (как графически показано в формулах (Ia) и (Ib), при этом группы К6, К7, К8, К9 и К10 такие, что:
К6 представляет -N= или -C(R6)
К7 представляет -N= или -C(R7)-
К8 представляет -N= или -C(R8)-
К9 представляет -N= или -C(R9)-
К10 представляет -N= или -C(R10)- и, кроме того, в случае, когда знак цикл окружен полукругом и представляет К6, К7, К10 эти радикалы К6, К7, К10 могут быть такими, что:
К6 представляет -N(R6)- или -C(R6)2- или -0- или -S(0)n
К7 представляет -N(R7)- или -C(R7)2- или -0- или -S(0)n
К10 представляет -N(R10)- или -C(R10)2- или -0- или -S(0)n или -СО-, где n целое число, равное 0,1,2, подразумевается, что в обоих случаях, когда знак цикл обозначает -К6-К7-К8-К9 и -К6-К7-К10-, по крайней мере, одна группа К6 и К7 представляет -С(R6)= или -C(R6)2- или -C(R7)= или -C(R7)2- и что, кроме того, эти двухвалентные радикалы -К6-К7-К8-К9- и -К6-К7-К10 cодержат в их основной цепи только 0, 1 или 2 гетероатома (N, O, S) и не содержат никакого ряда -0-0- или -S-S- (следует заметить, что -К6-К7-К8-К9 на практике образует цикл с ароматическим свойством).
-R6, R7, R8,R9,R10 каждый являются идентичными или отличающимися от других, oни представляют собой:
атом водорода или галогена, по крайней мере, один из радикалов R6или R7 иной, чем атом водорода,
группа циано, нитро, тиоцианато, гидрокси или карбокси,
алкил, циклоалкил, алкенил, алкинил, алкил- S(0)n (где n 0, 1 или 2), алкокси, циклоалкокси, содержащая от 3 до 8 атомов углерода, алкенилокси, алкинилокси, причем эти радикалы имеют преимущественно от 1 до 8 атомов углерода и могут быть замещены одним или несколькими атомами галогена,
радикал фенил, нафтил, фенил -S(0)n, (где n 0, 1 или 2) фенокси, фенилалкил (низший алкил), фенилалкил (низший алкил, n 0, 1 или 2), фенилалкокси (низший алкокси) или остаток гетероцикла, который может быть замещен, насыщенный или ненасыщенный, имеющий в цикле 5 или 6 звеньев с 1-3 гетероатомами, которые выбираются из группы кислород, сера, азот, причем фенильное или гетероциклическое ядро каждого из этих радикалов может быть замещено, по крайней мере, одним заместителем, выбираемым из группы, куда входят:
атом галогена,
группа нитро, циано, карбокси, гидрокси, меркапто, тиоцианато, алкокси (низший)-карбонил, -CO-NR'R'', NR'R'', -N(R')-CO-R'', -O-CO-R'. -O-CO-NR'R'' или
радикал низший алкильный, низший алкокси, алкил (низший) -S(O)n(где n 0, 1 или 2), циклоалкильный (с 3-7 атомами углерода), фенил, фенокси, фенил- S(O)n (где n 0, 1 или 2), фенилакил, фенилалкокси, фенилалкил- S(O)n (где n 0, 1 или 2), эти радикалы могут содержать галогены и имеют от 1 до 4 атомов углерода в алкильной части,
группа алкокси(низший) -карбонил, СО-NR'R'', NR'R'', N(R')-CO-R'', O-CO-R', O-CO-NR'R'',
R' и R'' идентичные или различные, представляют собой каждый атом водорода, низший алкильный радикал, циклоалкил с 3-7 атомами углерода, фенил, возможно галогенсодержащий, фенилалкил (низший алкил, возможно галогенсодержащий алкенил или алкинил с 3-7 атомами углерода, алкоксиалкил с 3-8 атомами углерода.
Когда К6 и К7 представляют -C(R6)= или -C(R6)2- или -C(R7)= или -C(R7)2-, тогда R6 c R7 или один из радикалов R6 с одним из радикалов R7могут образовывать, вместе с двумя атомами углерода, несущими R6 и R7цикл, углеродный или гетероциклический, насыщенный или ненасыщенный, имеющий 5 или 6 звеньев и 0, 1 или 2 невицикальных гетероатома (O, N или S).
Когда К6 или К7 или К8, К9 или К10 имеют одно из значений -N(R6)-, -N(R7)-, -N(R8)-, -N(R9)-, -N(R10)- тогда соответствующий радикал R6, R7, R8, R9, R10 имеет указанные ниже значения (причем, по крайней мере, один из радикалов R6 или R7 должен быть иным, чем атом водорода):
атом водорода, алкильный радикал с 1-6 атомами углерода, фенильный или фенилалкильный (низший алкил) радикал, иногда замещенный одним или несколькими атомами галогена или группой циано, или нитро, или низшим алкильным радикалом, или низшим алкокси радикалом.
В соответствии с изложенным, соединения формул (Ia) и (Ib) образуют особые группы согласно данному изобретению.
Среди соединений формул (I), (Ia), (Ib) особый интерес представляют те, которые более доступны для получения и которые имеют наиболее интересные свойства. Эти соединения более точно определены ниже, в частности отвечают формулам (II), (III), (IV), (V), (VI), (VII).
Для борьбы против грибковых заболеваний растений предпочтительно использовать соединения, которые имеют указанную величину.
Первая подгруппа соединений в соответствии с изобретением образована соединениями формулы (II), в которой:
К110 атом кислорода, группа S(O)n1, в которой n1 целое число, равное 0, 1 или 2, или группа NR110 или C(R110)2, или группа оксо
Z1 атом галогена или группа OW1 (в которой W1 имеет одно из значений, данных для W'), или группа NHR11, или NR11 R12, в которой R11и R12 идентичные или различные, имеют значения, которые даны для R1 и R2,
R13, R14 и R15 идентичные или различные, имеют одно из значений, которые даны для R3, R4, R5,
R13 и R14 могут вместе образовывать группу метилендиокси или этилендиокси, причем углероды в них могут быть замещены низшим алкильным радикалом или атомами галогена.
R16, R17, R18, R19 идентичные или различные, такие имеют одно из значений, которые даны для R6, R7, R8, R9,
если К 110 представляет собой -C(R110)- или -C(R110)2-, тогда R110представляет атом водорода или низший алкильный радикал, или радикал бензил, или гидрокси, или низший алканоилокси (например, ацетилокси), или низший алкокси,
если К110 является -N(R110)-, тогда R110 представляет собой атом водорода или низший алкильный радикал, или бензильный радикал.
Когда Z1 представляет собой группу NR11 R12, то производные имеют формулу (II'), а когда Z1 представляет собой группу OW1, то производные имеют формулы (II'').
Из производных с формулой (II) предпочтение отдается таким, у которых в формуле:
К110 является атомом кислорода, серы или представляет собой -N(R110)- или -C(R110)2-,
Z1 является радикалом OW1 таким, как он определен выше, группой NHR11 или NR11 R12, где R11 и R12 являются низшими алкилами такими, что R11 и R12 содержат в сумме не более шести атомов углерода или же они образуют вместе группу морфолино или тиоморфолино.
R13, R14, R15 имеют то же значение, что и R3, R4, R5
Являются особенно предпочтительными производные формулы (II), в которой:
Z1 является группой OW1, определенной выше, или группой NR11 R12, которая является группой морфолино, тиоморфолино, N-метилэтиламино или N-диэтиламино,
R13, R14, R15 идентичные или различные, являются атомом водорода или галогена, низшим алкилом, низшим алкокси, низшим алкилтио,
R16, R18, R19 являются атомом водорода или фтора,
R17 атом водорода или галогена, радикал низший алкил, низший алкокси, низший алкилтио, низший галогеналкил, низший галогеналкокси, низший галогеналкилтио, группа нитро, циано: радикал низший алкенильный, низший алкинильный или алкокси (низший) карбонил.
Для применений в качестве пестицидов особенно предпочтительными являются перечисленные выше продукты, у которых величина log P в пределах от 2,5 до 4.
Среди различных соединений формулы (I), составляющих часть изобретения, особый интерес представляет вторая подгруппа фениламидов с формулой (III), в которой Z2 представляет:
атом галогена или
группу OW2 (в которой W2 имеет одно из значений, которые даны для W'), или группа NHR21, или группу NR21 R22, в которой R21 и R22идентичные или различные, имеют одно из значений, которые даны для R1 и R2,
R23, R24, R25 идентичные или различные, имеют одно из значений, которые даны соответственно для R3, R4, R5,
R23 и R24 могут также образовывать вместе группу метилендиокси или этилендиокси, причем углероды в них могут быть замещены низшим алкильным радикалом или атомами галогена,
R26 и R27 идентичные или различные, имеют одно из значений, которые даны соответственно для R6, R7 при условии, что R26 и R27 не являются одновременно атомами водорода.
R28 и R29 идентичные или различные, могут быть атомом водорода или галогена, группой гидрокси, низшим алкильным радикалом, низшим алкокси, алкокси (низший)- алкил (низший), алкокси (низший) -карбонил.
Из производных формулы (III) предпочтительными являются те, у которых в формуле:
Z2 является радикалом OW2 (в котором W2 имеет одно из значений, данных для W'), группой NHR21 или группой NR21 R22, где R21 и R22представляют собой низшие алкилы такие, что R21 и R22 имеют в сумме не более шести углеродов, или же они вместе образуют группу морфолино или тиоморфолино.
R23, R24, R25 идентичные или различные, имеют такое же значение, что и R3, R4, R5.
R28 и R29 идентичные или различные, могут быт атомом водорода или галогена, или гидроксильной группой.
Особенно предпочтительными являются производные с формулой (III), в которой:
Z2 является группой OW2, определенной выше, или группой NR21 R22, которая является группой морфолино, тиоморфолино, N-метилэтиламино или N-диэтиламино.
R23, R24, R25 идентичные или различные, являются атомами водорода или галогена, низшим алкилом, низшим алкокси, низшим алкилтио.
R26, R27 идентичные или различные, являются атомами водорода или галогена, низшим алкилом, низшим алкенилом, низшим алкокси, низшим алкилтио, низшей галогеналкокси, низшим галогеналкилом или низшим галогеналкилтио.
R28 и R29 идентичные или различные, являются атомом водорода или фтора.
Для применения в качестве пестицидов предпочтительными являются перечисленные выше продукты, у которых величина в пределах от 2,5 до 4.
Среди соединений формулы (I), составляющих часть изобретения, особый интерес представляет третья подгруппа, она представляет собой никотиновые производные формулы (IV), в которой
Z3 представляет:
атом галогена, или
группу OW3 (в которой W3 имеет одно из значений, указанных для W') или группу NHR31 или
группу NR31 R32, в которой R31 и R32 идентичные или различные, имеют одно из значений, указанных соответственно для R1 и R2.
R33, R34, R35 идентичные или различные, имеют одно из значений, которые даны соответственно для
R33 и R34 могут также образовывать вместе метилендиоксигруппу/или этилендиокси группу, углероды этих групп могут быть замещены низшими алкилами или атомами галогена.
R37 имеет одно из значений, которые даны для R7 при условии, что R7не является атомом водорода.
R38 и R39 идентичные или различные, могут быть атомом водорода или галогена, низшим алкилом, низшим алкокси, алкокси (низшим)- алкил (низшим), или низшим алкоксикарбонилом, или группой циано. Кроме того, когда R37 является фенильной группой, то R38 может образовывать с атомом углерода R37 и орто, связанным с пиридиновым ядром, цепь Y3-(CH2)n3, в которой Y3 атом кислорода или серы, или метиленовая группа и n3 число, равное 0, 1 или 2.
Среди соединений формулы (IV) предпочитают такие, у которых R33, R34, R35 идентичные или различные, являются атомом водорода или галогена (по крайней мере один из этих трех радикалов иной, чем атом водорода или галогена), или низший алкил, или низший алкокси, или низший алкилтио.
Среди соединений формулы (I) особый интерес представляет четвертая подгруппа, которая образована производными формулы (V), в которой
Z4 представляет:
атом галогена или
группу OW4 (в которой W4 имеет одно из значений, которые даны для W'), группу NHR41 или группу NR41 R42, в которой R41 и R42 идентичные или различные, имеют одно из значений, которые даны для R1 и R2,
R43, R44, R45 идентичные или различные, имеют одно из значений, которые данные соответственно для R3, R4, R5,
R47 имеет значение, которое дано для R7 но иное, чем атом водорода,
R49 может быть атомом водорода или низшим алкильным радикалом.
Среди производных формулы (V) предпочтение отдается тем, в формуле которых:
Z4 является радикалом OW4 (в котором W4 имеет одно из значений, которые даны для W'), группой NHR41 или группой NR41 R42, в которых R41и R42 являются низшими алкилами такими, что R41 и R42 содержат в сумме не более шести углеродов, или же образуют вместе группу морфолино или тиоморфолино.
R43, R44, R45 идентичные или различные, являются атомом водорода или галогена, низшим алкилом, низшим алкокси, низшим алкилтио,
R49 атом водорода.
Пятая подгруппа соединений в соответствии с формулой (I) образована соединениями формулы (VI), в которой:
Z5 представляет атом галогена или группу OW5 (в которой W5 имеет одно из значений, которые даны для W'), или группу NHR51 или группу NR51R52, в которых R51 и R52 идентичные или различные, имеют одно из значений, которые даны для R1 и R2 соответственно R53, R54, R55, идентичные или различные, имеют одно из значений, которые даны соответственно для R3, R4, R5.
R53 и R54 могут также образовывать высотe группу метилендиокси или этилендиокси, причем углероды в этих группах могут быть замещены на низший алкил или на атомы галогена.
R56 и R57 имеют одно из значений, которые даны для R6 и R7, при условии, что R6 и R7 одновременно не являются атомом водорода.
R59 может быть атомом водорода или галогена, низшим алкильным радикалом, радикалом гидрокси, низшим алкокси или низшим алкоксиалкилом, причем эти радикалы могут быть галоидсодержащими.
Среди соединений формулы (VI) предпочтение отдается таким, в формуле которых R53, R54, R55 идентичные или различные, являются атомом водорода или галогена, или низшим алкилом, или низшим алкокси, или низшим алкилтио.
R59 атом водорода или низший алкил.
Шестая подгруппа соединений в соответствии с общей формулой (I) образована продуктами формулы (VII), в которой Z6 представляет:
атом галогена,
группу OW6 (в которой W6 имеет одно из значений, которые даны для W'), группу NHR61 или группу NR61 R62, в которой R61 и R62, идентичные или различные, имеют одно из значений, которые даны соответственно для R1 и R2.
К66 атом азота замещенный -N(R66)- или -N= или атом серы или кислорода или атом углерода, замещенныйC(R66)-
К67 атом серы или кислорода, или атом азота, замещенный -N(R67)- или -N= атом углерода, замещенный C(R67)-, предполагается, что К66 и К67 не могут быть одновременно -N(R66)- и -N(R67).
К610 атом азота, замещенный -N(R610)-, или -N= или атом серы или кислорода, или атом углерода, замещенныйC(R610)-, предполагается, что К610 и К67 не могут быть одновременно один -N(R610)-, а другой N(R67)-,
R63, R64, R65 идентичные или различные, имеют одно из значений, которые даны соответственно для R3, R4, R5,
R66, R67, R610, идентичные или различные, имеют значения, которые даны для R6, R7, R10.
Среди производных формулы (VII) предпочтение отдается тем, в формуле которых:
Z6 является радикалом OW6 (в котором W6 имеет одно из значений, которые даны для W'), группой NHR61 или группой NR61 R62, в которых R61и R62 содержат не более шести атомов углерода в сумме, или же они образуют вместе группу морфолино или тиоморфолино.
К66 атом азота, замещенный -N(R66)-,
К67 атом азота -N= или атом углерода, замещенныйC(R67)-,
К610 атом углеродаСН-,
R63, R64, R65 идентичные или различные, являются атомом водорода или галогена, или низшим алкилом, или низшим алкокси, низшим алкилтио,
R66 и R67 атом водорода, группа алкил, фенил, фенилакил, замещенная галогенами или галогеноалкильными группировками, предполагается, что R66 и R67 не могут быть одновременно атомом водорода.
Производные в соответствии с изобретением особенно интересны в качестве промежуточных продуктов, а вследствие их замечательных фунгицидных свойств в качестве фунгицидов для сельского хозяйства, а также в качестве промежуточных для синтеза производных, в частности, других производных формулы (I).
Описанные выше различные формулы соединений в соответствии с изобретением являются новыми соединениями. Однако, что касается Федеративной Республики Германии, следующие соединения исключаются из формулы изобретения:
соединения формулы (Ia), в которой Y-атом кислорода, и одновременно К8 и К9 являются или -СН= или же один -N= а другой -CH= и одновременно К6 и К7 образуют вместе ненасыщенный углеродный цикл, присоединенный к циклу с 5 звеньями, включающему К10;
соединения формулы (Ib), в которой Y атом кислорода и одновременно К10 это 0, S или SO, или SO2, или NR10 (где R10 имеет приведенное выше значение), или СН2, или СО и одновременно К6 и К7образуют вместе ненасыщенный углеродный цикл, соединенный с циклом с 5 звеньями, включающими К10.
Производные в соответствии с изобретением могут быть приготовлены многими способами.
Ниже описывается получение соединений формулы (II).
В соответствии с первым способом (способ А), который особенно подходит для соединений формулы (II), в которых К110 является -O-, -S- или NHR110, исходят из бензофенона формулы (XII''), в которой с R13 по R19 имеют значения, указанные выше (включая предпочтительные значения) и А1 замещаемый атом галогена (бром или предпочтительно хлор или фтор) или группа нитро и ведут реакцию с производным формулы:
H K110 -CH2-CO-Z1, в которой К110 и Z1 имеют указанные значения, с последующим замещением А1 и циклизацией и получают продукт формулы II.
Эту реакцию осуществляют предпочтительно в спиртовом растворителе (например, низший алканоил) в присутствии соовтетствующего алканолята (напрмер, СH3ONa, C2H5ONa, C3H7ONa) или в присутствии органического основания такого как амин, предпочтительно третичный (триэтиламин), или неорганическое основание, например гидроксиды, карбонаты или дикарбонаты, причем это основание является производным щелочных или щелочноземельных металлов таких, как натрий, калий и кальций.
Реакцию може можно проводить в присутствии тех же самых оснований в дипольном апротонном растворителе таком, как диметилсульфоксид, диметилформамид, N, N-диметилацетамид, N-метилпирролидон или гексаметилфосфаортриамид.
В случае производных формулы (II''), они могут быть переведены (способ G) в производные формулы (II') путем нагрева при темепратуре от 100оС до 200оС, в случае необходимости под давлением, с избытком амина NHR11R12, в соответствии со схемой:
(II″)+NHR″R12__→ (II′)+W′OH
Когда в формуле (II') W1 является атомом водорода, эти производные сначала активируют по кислотной функции при помощи такго агента, как тионилхлорид (SOCl2), фосфорилхлорид (POCl3), трихлорид или пентилхлорид фосфора, (PCl3, PCl5), дициклогексилкарбодиимид, диимидазолкарбонил, этилхлорформиат или трифторуксусный ангидрид, перед обработкой амином NHR11 R12 при температуре от 0 до 50оС в растворителе таком, как ТГФ (тетрагидрофуран или в хлорном растворителе в частности, алифатический или ароматический углеводород, предпочтительно при избытке амина) или в присутствии неорганического или органического основания такого, как триэтиламина.
Исходя из производных формулы (II'), можно получить и другие производные формулы (II') классическим методом получения функциональных групп.
Например, если в случае, когда получают нитросоединение (формулы II, в которой R16, или R17, или R18, или R19 является NH2) оно может быть восстановлено (способ В) в аминовое производное при помощи восстановителя такого, как металл (железо, олово) или соли этих металлов (хлорид олова) в среде неорганической (HCl, H2SO4) или органической (этиловый спирт) или карбоксиловая кислота, в частности, уксусная кислота. В качестве восстановителя можно использовать водород (в случае необходимости под давлением) или его предшественники (боргидрид натрия, производные муравьиной кислоты, циклогексен), в присутствии переходного металла такого, как палладий. В этом случае используют в качестве растворителя этилацетат, уксусную кислоту и спирт, например этиловый.
Полученное аминопроизводное (формула (II), в которой R16, или R17, или R18, или R19 является NH2) может само подвергаться реакциям ацилирования (способ С) или диазотирования. Реакцию ацилирования проводят с помощью производных карбоксильной кислоты (хлорид или ангидрид кислоты), в присутствии органического основания (триэтиламин, пиридин) или неорганического основания (гидроксид, карбонат или водородкарбонат щелочных металлов) в апротонном растворителе, таком, как хлорные растворители (хлорметилен, хлороформ) или ароматические (бензол, толуол), или алифатический эфир (диэтилоксид, тетрагидрофуран, 1,2-диметоксиэтан). Диазотирование (способ D) реализуется путем обработки раствора аминопроизводного (формула (II), в которой R16, или R17, или R18, или R19 являются NH2) в сильной неорганической кислоте (соляная, бромистоводородная или серная) щелочным натрием (нитрат натрия), при температуре от -10 до +15оС. Полученная таким образом соль диазония разлагается при температурах от 5 до 100оС, в присутствии различных реагентов таких, как хлорид меди, бромид меди, иодид калия, окись меди или этилтиоксантат калия, чтобы создать соответственно производные, в которых группа амино замещена атомом хлора, атомом брома, атомом иода, группой гидроксильной или группой меркапто.
В случае, если введен атом брома, можно провести реакцию арилового сочетания (способ Е) с бороновой кислотой R17B(OH)2, в которой R17 может быть гетероцикл, фенил, или виниловая группа (эти группы могут быть замещены, как указано в определении R7), чтобы получить другие производные в соответствии с изобретением.
(II′′′) 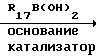 (II″″)
(II″″)
Реакцию проводят как с Z1 OW1(W2 H, или алкил, или щелочной металл), или с Z1 NR11R12.
В качестве катализатора можно использовать комплексы палладия Pd[P(C6H5)3] 4, тетракистрифонилфосфин палладия, или получаемые ин ситу из соли палладия, например ацетата палладия и фосфина например трифенилфосфин или три-о-толилфосфин. В качестве основания можно использовать неорганическое основание, например карбонаты и кислые карбонаты щелочных металлов (Na2CO3, NaHCO3), или органическое основание, например амин (триэтиламин). Реакцию с неорганическим основанием проводят в гетерогенной среде, включающей органическую фазу, которой может быть углеводородный растворитель, например бензол или толуол, или эфир, с высокой точкой кипения, как глим или его высшие производные, как диглим, триглим, и водную щелочную фазу. Реакцию можно также проводить с органическим основанием в гомогенной среде, в присутствии растворителя, например диметилформамида или N-метилпирролидом. Используемые бороновые кислоты могут являться торговыми продуктами или приготавливаться путем взаимодействия металлорганического производного R17M1, где R17 имеет указанное значение (M1 Li или MgX, где Х Cl, Br), с алкилборатом B(OR)3 (где R'=CH3, C3H7, C2H5, i-C3H7, C4H9), вслед зачем проводят кислый гидролиз в соовтетствии с процедурой, описанной в работах Organic Synt. coll. vol. 4p. 68 или Journal of organie chemistry 49, p.5237-5243 (1984).
Реактивы используются в следующих пропорциях:
бороновая кислота R17B(OH)2 от 1,05 до 1,50 эквивалентов
основание от 4,00 до 6,00 эквивалентов
катализатор от 0,005 до 0,03 эквивалентов
субстрат формулы II''' 1,00 эквивалентов
Реакцию проводят при температуре от 50 до 150оС с обратным холодильником в течение времени от 2 до 48 ч. Производное формулы (II''') выделяют обычными методами, экстракцией или осаждением, при добавлении воды к реакционной смеси, и может быть очищено перекристаллизацией или хроматографически в соовтетствующем растворителе.
В другом способе (способ F), который является вариантом способа D, проводят реакцию при температуре от 40оС до температуры кипения растворителя путем взаимодействия соединения формулы (II), в которой один из заместителей с R16 по R19 представляет собой незамещеную аминогруппу и Z1 и R13, R14, R15 имеют указанное значение, с нитридом низшего алкила, например с нитритом трет-бутила, в растворителе, например тетрагидрофуран или диметилформамиде, чтобы получить производное формулы (II), в которой группа амино замещена атомом водорода и где Z1 и R13 по R19 имеют указанное значение.
Производное формулы (XII') могут быть получены при помощи реакции Фриделя-Крафта в соответствии со схемой:
(XII′′′)+(XII″) __→ (XII′) в которой А1 и R13 по R19 имет указанное значение, причем сами соединения (XII''') и (XII'') известны.
Эту реакцию проводят в присутствии кислот Льюиса в каталитическом или стехиометрическом количестве (FeCl3, AlCl3, ZnCl2, SnCl4) в присутствии или при отсутствии растворителя (нитробензол, алифатические хлорированные растворители, дисульфид углерода). Реакция проводится при темепратуре от -10 до 200оС, в зависимости от применяемых экспериметальных условий.
По другому способу (способ G), который особенно подходит для соединений формулы (II), в которой К110 является группой C(R110)2 и в которой R13 по R19 имеют указанное значение, (включая предпочтительные значения), проводят реакцию бензофенона формулы (XXII'), в которой Z11 OH R13 по R19 имеют указанные значения (включая предпочтительные значения), с тионилхлоридом (SoCl2) фосфорилхлоридом (PoCl3), трихлорфосфором или пентахлорфосфором (PCl3 или PCl5), и получают бензофенон формулы (XXII'), в которой Z1=Cl и R13 по R19 имеют указанные значения.
Как правило, полученное таким образом соединение можно не выделять, а подвергать его взаимодействию с малонатом низшего алкила, в присутствии основания, которым предпочтительно может быть алконат магния, например этилат магния. Полученное таким образом соединение формулы (XXII'), в которой W1 низший алкил, затем обрабатывают основанием, например, алконоатом щелочного или щелочно-земельного металла или неорганическим основанием, например гидроксидом или карбонатом щелочных металлов, в водной или спиртовой среде или в дипольном апротонном растворителе, например в диметилсульфоксиде, диметилформамиде, N-метилпирролидоне, и получают соединение формулы (II), в которой К110 группа оксо, R13 по R19 имеют указанное значение, и Z1 группа OW1, где W1 низший алкил.
Из этого соединения, обработанного при температуре от 100 до 200оС, в случае необходимости при высоком давлении, при избытке амина NHR11R12, в присутствии растворителя или без растворителя, получают соединение формулы (II), в которой К110 группа оксо и где R13 по R19 имеют указанное значение, и Z1 группа NR11R12 как она определена. Это последнее соединение может быть восстановлено соответствующим восстановителем, например боргидрид натрия, в присутствии трихлорида церия, в алканоле, например этаноле, и получается соединение формулы (II), в которой К110 группа CH(OH) и Z1 группа NR11R12 как она определена выше.
С этими двумя последними продуктами можно проводить классические в органической химии реакции (добавление металлорганического соединения для первого, ацилирование или алкилирование для второго), и получить другие производные формулы (II).
В соответствии с другим способом (способ Н), который особенно подходит для соединений формулы (II), в которой К110 является группой С(R110)2 и где R13 по R19 имеют указанные значения, (включая предпочтительные значения), проводят реакцию производного формулы (XXXII'), в которой группа OW1 или NR1R2 с галогенидом бензила формулы (XXXII'), где R16 по R110 имеют указанное значение, и где Hal обозначает атом галогена, например хлор или бром. Реакцию проводят в присутствии основания, предпочтительно алканоата щелочного или щелочно-земельного металла, или в присутствии неорганического основания, например гидроксида щелочных металов, в среде алканола или в апротонном дипольном растворителе, например в диметилсульфоксиде диметилформамиде или N-метилпирролидоне, и получают соединение формулы (XXXII''') в которой R13 по R19 и Z1 имеют предыдущие значения. При обработке этого соединения органической или неорганической кислотой, предпочтительно полифосфорной кислотой, в присутствии или в остутствии растворителя (толуол, ксилол), при температуре от 0 до 150оС, получают производное формулы (II), в которой К110 группа C(R110)2 и R13 по R19 имеют предыдущее значение. Если получается соединение Z1 OW1, где W1 низший алкил или атом водорода, то его можно трансформировать в производное, в котором Z1 NR1R2 классическими методами органическй химии, которые указаны в первом способе.
В соответствии с другим способом (способ I), который особенно подходит для соединений формулы (II), в которой К110 группа с (R110)2 и где R13 по R19 имеют указанное значения, (включая предпочтительные значения), проводят реакцию производного формулы (XXXII') в которой Z1 группа OW1 или NR11 R12, с бензальдегидом, замещенным радикалами R16, R17, R18 или R19. Реакцию проводят в растворителе, например ароматический углеводород или карбоксиловая кислота, в присутствии катализатора, которым предпочтительно является двузамещенный амин, например пиперидин, таким образом получают соединение формулы (XXXXII'), в которой группы Z1 и R13 по R19 имеют указанное значение. Затем это соединение восстанавливают соответствующим восстановителем, например боргидридом натрия, в присутствии хлорида церия, как описано выше во втором способе. Получаемый аллиловый спирт циклизуют путем обработки органической или неорганической кислотой, в количестве каталитическом или превышающем стехиометрию, в присутствии или отсутствии растворителя (толуол, ксилол), при температуре от 0 до 150оС, и получают производное формулы (II), в которой К110 группа СН2 и R13 по R19 имеют предыдущее значение. Если получают соединение Z1=OW1, где W1 низший алкил или атом водорода, то его можно трансформировать в Z1 NR1R2 при помощи классических реакций органической химии, которые указаны для первого способа.
Ниже описывается получение соединений формулы (III).
Соединения формулы (III) получаются по способу, который является частью изобретения, при помощи реакции арилового сочетания бороновой кислоты R27B(OH)2, в которой R27 может быть гетероциклом, фенилом или виниловой группой (эти группы могут быть замещены, как это указано в определении R7) с бромистым производным формулы (XIII'), подразумевается, что ни один из других заместителей не может быть одновременно атомом брома или иода. Реакционная схема такого арилового сочетания следующая:
(XIII′)+R27B(OH)2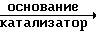 (III)
(III)
Реакция проводится также с Z2 OW2 (W2 H или алкил, или щелочной металл) и с Z2 NR21R22.
В качестве катализатора можно использовать коммерческие комплексы палладия Pd[P(C6H5)3]4, тетракистрифенилфосфин палладия, или получаемым ин ситу из соли палладия, например ацетата палладия, и фосфина, например, трифенилфосфина или три-о-толиолфосфина. В качестве основания можно использовать неорганическое основание, например карбонаты или бикарбонаты щелочных металлов (Na2CO3, NaHCO3), или органические основания, например амин (триэтиламин). Реакцию проводят с неорганическим основанием в гетерогенной среде, куда входят органическая фаза, это может быть углеводородный растворитель, например бензол или толуол, или эфир с повышенной точкой кипения, как глим или его высшие производные диглим, триглим, и водная щелочная фаза. Реакция также может проводиться с органическим основанием в гомогенной среде в присутствии растворителя, например диметилформамида или N-метилпирролидона. Применяемые бороновые кислоты могут быть коммерческими или они могут быть получены путем взаимодействия металлорганического производного R27М2, где R27 имеет указанное значение, (M2 Li или MgX, где X Cl, Br) с алкилборатом B(OR)3, (где R' CH3; C2H5, C3H7) i C3H7, C4H9), после чего проводится
кислотный гидролиз по методике, описанной в Organic Systhesis coll. vol.4, p. 68 или Journal organ. Chemistry, 49, p 5237 (1984). Реагенты используются в следующих пропорциях:
бороновая кислота R27B(OH)2 от 1,05 до 1,50 эквивалентов
основание от 4,00 до 6,00 эквивалентов
катализатор от 0,005 до 0,03 эквивалентов
субстрат формулы XIII' 1,00 эквивалент
Реакция проводится при температуре от 50 до 150оС, предпочтительно с обратным холодильником, в течение периода от 2 до 48 ч. Производное формулы (III) выделяют обычными методами экстракции или осаждения при добавлении воды к реакционной смеси, и оно очищается путем рекристаллизации или хроматографически в соответствующем растворителе.
Производное брома формулы (XIII') может быть получено путем диазотирования амина формулы (XIII'')
(XIII″)  (XIII′)
(XIII′)
Реакцию осуществляют как с производными, в формуле которых Z2 OW2(W2 H или алкил), так и с производными, в формуле которых Z2 NR21R22. Реакция осуществляется путем обработки раствора аминопроизводного (XIII') в сильной неорганической кислоте (серная или бромистоводородная), которая, в случае необходимости содержит органическую кислоту (уксусная кислота), щелочным нитритом (нитритом натрия), при температуре от -10 до +10оС. Полученная таким способом соль диазония затем разлагается при температурах от 5 до 90оС, в присутствии бромистоводородной кислоты и бромида меди.
Продукт формулы (XIII') выделяется обычными методами, экстрагирования или осаждения добавлением воды к реакционной смеси, и может быть очищен рекристаллизацией или хроматографически в соответствующем растворителе.
Амин (XIII'') получается реакцией арилового сочетания фенилбороновой кислоты формулы (A2), соответственно замещенной R23, R24, R25 с галогенпроизводным (бром или иод) формулы (XIII'''), в соответствии со схемой
(XIII′′′)+(A2) 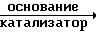 (XIII″) в которых формулы радикалов Z2, R26, R28, R29, при условии, что R26, R28и R29 не являются одновременно атомом брома или иода, имеют указанное значение Hal обозначает атом галогена, в частности бром или йод.
(XIII″) в которых формулы радикалов Z2, R26, R28, R29, при условии, что R26, R28и R29 не являются одновременно атомом брома или иода, имеют указанное значение Hal обозначает атом галогена, в частности бром или йод.
Реакцию осуществляют как с Z2 OW2 (W2 H или алкил/ или щелочной металл), так и с Z2 NR21R22. Условия реакции идентичны описанным ранее для перехода от (XIII') и (III).
Амин (XIII''') может быть получен путем восстановления нитратного производного (XIII''').
Реакция осуществляется как с производными, в формуле которых Z2 OW2 (W2 H или алкоил), так и с производными в формуле которых Z2 NR21 R22. В качестве восстановителя можно использовать металл (например, железо, олово), или соли этих металлов (например, хлорид олова), в среде неорганической кислоты (HCl, H2SO4) или органической кислоты (уксусная кислота). Можно также использовать в качестве восстановителя водород (в случае необходимости под давлением) или его предшественники (боргидрид натрия, производные муравьиной кислоты, циклогексен), в присутствии переходных металлов, таких как палладий или платина. В этом случае в качестве растворителя предпочтительно используется этилацетат, кусусная кислота или спирт, как, например, этиловый спирт. Продукт с формулой (XIII''') выделяется обычными методами: экстрагирование или осаждение при добавлении воды к реакционной смеси, и он может быть очищен путем рекристаллизации или хроматографически в соовтетствующем растворителе.
Производные типа (XIII'''') являются известными соединениями.
Соединения формулы (III'') и (XIII'), в формуле которых Z2 OW2, можно перевести в производные, в формуле которых Z2NR21 R22классическими методами органической химии. Так, если Z2 OW2, где W2алкил, то его можно перевести в Z2 NR21R22 путем нагрева при температуре от 100 до 200оС, в случае необходимости под давлением, при избытке амина NHR21R22 в соответствии со следующей схемой:
соединение (III′)(соединение (III) c группой CO-OW2)+  H
H [соединение (III)
[соединение (III)
На основе соединений, в формулах (III'', XIII' или XIII'''') которых Z2 OW2, где W2 алкил, можно получить соединения, в формуле которых Z2 OM2, где М2 щелочной металл, при помощи реакции омыления с неорганическим основанием, например спиртовым раствором щелочи калия или щелочи натрия при обработке этих соединений неорганической кислотой, например соляной или серной, получают соответственно производные (III), (XIII') или (XIII'''') с Z2 ОН.
Из производного формулы [(III), (XIII') или (XIII'''')] в которой Z2 OH, можно также получить соединение, в формуле которого Z2 NR21R22 после активирования функции карбоновой кислоты таким реагентом, как тионилхлорид (SOCl2), фосфорилхлорид (POCl3), трихлорид или пентахлорид фосфора (PCl3, PCl5), дициклогексилкарбодинимид, карбонилдимидазол, хлороформиата алкенила или трихлоруксусный ангидрид, и реакцией с амином NHR21R22 в присутствии органического или неорганического основания, в органическом растворителе, например хлорированном или ароматическом растворителе, или в эфире, например в тетраметилформамиде.
Далее описывается получение соединения формулы (IV).
Получить соединение формулы (IV) можно, например, путем циклизации производного формулы (XIV')
R37-CO-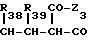 -Ar 3 (XIV′) в которой Ar3 группа формулы (XIV''), т. е. фенил, замещенный радикалами R33, R34, R35 a Z3, R33 по R39 имеют указанное значение, при нагревании, в присутствии донора аммиака, в кислой среде.
-Ar 3 (XIV′) в которой Ar3 группа формулы (XIV''), т. е. фенил, замещенный радикалами R33, R34, R35 a Z3, R33 по R39 имеют указанное значение, при нагревании, в присутствии донора аммиака, в кислой среде.
Промежуточные производные формулы (XIV') являются новыми соединениями, которые являются частью изобретения. Они могут быть получены в соответствии со способом, отличающимся тем, что проводят реакицю 3-пропиокетона с бензоилацетатом или ацетамидом, соответствующим образом замещенным по схеме:
R37-CO-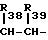 T3+Z3-CO-CH2-CO-Ar3__→ (XIV′) в которой формулы Z3 и R33 по R39 имеют такие же значения, как и для формулы (XIV'), Т3 обозначает удаляемую группу такую, как атом галогена или четвертичный аммоний, в присутствии сильной неорганической кислоты и растворителя.
T3+Z3-CO-CH2-CO-Ar3__→ (XIV′) в которой формулы Z3 и R33 по R39 имеют такие же значения, как и для формулы (XIV'), Т3 обозначает удаляемую группу такую, как атом галогена или четвертичный аммоний, в присутствии сильной неорганической кислоты и растворителя.
В случае, если группа Т3 является четвертичным аммонием, то проводят реакцию производного основания Манниха, т.е. производного формулы
R37-CO-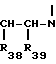 + I- с производным формулы: Ar3-CO-CH2-CO-Z3 в щелочной среде, в присутствии растворителя типа спиртового. Эти последние производные известны.
+ I- с производным формулы: Ar3-CO-CH2-CO-Z3 в щелочной среде, в присутствии растворителя типа спиртового. Эти последние производные известны.
Производные формулы (IV), в которой Z3 группа ОН, т.е. производные формулы (IV'') с W3=Н могут быть также получены способом, отличающимся тем, что производят омыление эфира формулы (IV''), в которой W3 низший алкильный радикал, затем производят подкисление.
Можно перейти от производных формулы (IV'') c W3 низший алкил, к производным формулы (IV'), в которой Z3 группа NR31R32, путем омыления, как указано в предыдущем абзаце с последующим галогенированием полученных кислот до галогенидов кислот и реакцией с амином формулы NHR31R32, в которой R31 и R32 имеют указанное значение.
Далее описывается получение продуктов формулы (V).
В соответствии с первым способом проводят реакцию онона формулы (XV'):
O 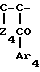 =
=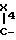 R49 (XV′) в которой
R49 (XV′) в которой
Ar4 имеет формулу (XV'')
R43, R44, R45, R49 и Z4 имеют такое же значение, как и в формуле (V), и
Х4 группа диалкил (низший)-амино или алкокси (низший), с амидином формулы:
R47- NH или с одной из его солей формулы:
NH или с одной из его солей формулы:
R47- N+H2 анион- в которых R47 имеет указанное значение в присутствии растворителя, в щелочной среде.
N+H2 анион- в которых R47 имеет указанное значение в присутствии растворителя, в щелочной среде.
Эта реакция проводится предпочтительно в органическом растворителе, в частности, спиртовом, например метанол, этанол, пропанол, в присутствии соответствующего алкоголята или органического основания, такого как амин, предпочтительно четвертичный, или неорганического основания такого как, например гидроксид, карбонат или бикарбонат щелочного или щелочно-земельного металла, например натрия, калия или кальция.
Реакция может также проводиться в воде, в присутствии неорганических оснований, которые перечислены выше.
В случае производных формулы (V'), т.е. производных формулы (V), в которой Z4 группа NR41 R42 как определено выше, проводят реакцию производного формулы (V''), т.е. производного формулы (V), в которой Z4- группа OW4, как определено выше, с амином формулы NHR41R42, и затем удаляют W4OH. Если в формуле (V'') W4 являются атомом водорода, то у этих производных сначала активируют кислотную функцию таким агентом, как дициклогексилкарбодиимид, карбонидиимидазол, этил хлорформиат или трифторуксусный ангидрид, тионилхлорид (SOCl2), фосфорилхлорид (POCl3), трихлорид или пентахлорид фосфора (РCl3, PCl5) перед обработкой амином NHR41R42 в присутствии органического основания, в органическом растворителе, например хлорированный растворитель или ароматический растворитель (в частности, углеводород или эфир, например, ТГФ).
Из этих производных формулы (V') можно получить другие производные формулы (V') классическими методами органической химии.
Производные формулы (XV') могут быть получены способом, в котором проводят взаимодействие производного формулы (XV''')
Ar4- CH 2 (XV′′′) в которой Ar4, R43, R44, R45, Z4 имеют указанное значение, с производным формулы (XV'''')
CH 2 (XV′′′) в которой Ar4, R43, R44, R45, Z4 имеют указанное значение, с производным формулы (XV'''')
R49-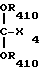 (XV′′′) в которой R49 и Х4 имеют указанное значение, R410 является низшим алкильным радикалом.
(XV′′′) в которой R49 и Х4 имеют указанное значение, R410 является низшим алкильным радикалом.
В соответствии с вторым способом получения производных формулы (V), в случае, если R47 не радикал алкил- или бензил-сульфинил или сульфонил, проводят реакцию производного формулы (XXV'), в которой R43 по R45, R49и Z4 имеют указанное значение, и А4 группа алкил (низший) сульфонил или бензилсульфонил, с производным формулы R47 H, в которой R47 радикал, имеющий то же значение, что и R7, при условии, что валентная связь, которая связывает его с атомом водорода, связана также в R47 с гетероатомом, например, O, S или N R47.
Эта реакция проводится в среде растворителя и щелочной среде предпочтительно протонного или апротонного растворителя, в присутствии органического или неорганического основания, такого как гидроксиды, карбонаты или бикарбонаты щелочных или щелочно-земельных металлов таких, как натрий, калий или кальций.
Производные формулы (XXV') могут быть получены путем окисления производного формулы (V), в которой R47 группа низший алкилтио или бензилтио, при помощи окислителя, например перекиси водорода или перкислоты, например перуксусной кислоты, метахлорпербензойной кислоты или перфталата магния.
Далее описывается получение соединений формулы (VI).
В соответствии с этим способом проводят реакцию (реакция Михеля) 2-этиленфенилкетона формулы (XVI') со сложным эфиром или β-кетоамидом формулы R59 -CO-CH2-COZ5, в которых R53 по R59, Z5 имеют указанное значение, в присутствии органического или неорганического основания, например частично дегидратированного барита, в низшем алканоле, например в этиловом спирте, и при температуре от 0оС до температуры кипения применяемого растворителя. Полученное соединение формулы (XVI''), в формуле которого R53 по R59, и Z5 имеют указанное значение, может быть циклизовано простым нагревом при 40оС с обратным холодильником в среде карбоновой кислоты, предпочтительно в среде уксусной кислоты, в присутствии донора азота, например аммиака или органической соли аммония или неорганической соли аммония. Таким образом получают соединение формулы (VI'') или (VI'), в которой R53 по R59 имеют указанное значение, и соответственно Z5 OW5 и Z5 NR51R52.
Если получено соединение формулы (VI''), то его можно перевести в производное формулы (VI') классическими методами органической химии, которые упомянуты в предыдущих способах.
Далее описывается получение соединений формулы (VII).
Соединения формулы (VII), в которой К66 означает кислород и К67означает -C(R67)= и K610 означает -C(R610)= получаются из сложных эфиров или гамма-дикетоамидов формулы (XVII') путем циклизации в спирте или в карбоновой кислоте, например в уксусной кислоте, простым нагревом реактива в присутствии каталитического количества (от 0,1 до 5%) сильной кислоты (неорганической или органической, например соляной или серной), при температуре от 40 до 120оС, в соответствии с общей методикой, описанной Краффом и Даалем
Kraff, Daal. Chem. Ber. 21, р. 3053(1888) и воспроизведенной авторами Требо и Тест,
Bull. Soch. Chrin. Fr. p 5272 (1970).
Соединения формулы (VII), в которой К66 эот NR66, К67 это -C(R67)= K610 это -C(R610)= получают из сложных эфиров или β, гамма-дикетоамидов формулы (XVII'), путем циклизации в кислой среде при нагревании, в присутствии амина формулы NHR66, в которой R66 имеет указанное значение. В качестве растворителя можно использовать карбоновую кислоту, например уксусную кислоту, которая также играет роль катализатора. Можно также добавлять каталитические количества сильной неорганической кислоты, например соляной или серной. Реакция проводится при температуре от 40оС до температуры кипения используемого растворителя.
В случае, если реакцию проводят с гидролитом окиси аммония, то полученный продукт имеет формулу (VII), в которой К66 это NH1K67 это -С(R67)= K610 это -С(R610)= Это соединение может быть обработано галогеновым производным R66 Hal, где Hal-галоген (может быть атом хлора, брома или иода), в присутствии неорганической или органической кислоты, в среде растворителя, например диметилсульфоксида, диметилфор- мамида или N-метилпирролидона, и получают производное формулы (VII), в которой К66 это NR66, K67 это -С(R67)= и К610 это -С(R610)=
Сложные эфиры и диметоновые амиды формулы (XVII') могут быть получены по способу, отличающемуся тем, что проводят реакцию галогенкетона (возможно, замещенного радикалами и R610 формулы (XVII'') с бензоилацетатом или ацетамидом, соответственно замещенным, по схеме: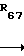 -
- Z
Z -COAr6__→ в которой Ar6 группа формулы (XVII'''), т. е. фенил, замещенный радикалами R63, R64 и R65, в которых формулы Z6 и R63 по R69 имеют указанное значение Hal обозначает удаляемую группу, такую как атом галогена.
-COAr6__→ в которой Ar6 группа формулы (XVII'''), т. е. фенил, замещенный радикалами R63, R64 и R65, в которых формулы Z6 и R63 по R69 имеют указанное значение Hal обозначает удаляемую группу, такую как атом галогена.
Соединения формулы (VII), в которой К66 это -N- или -N(R66)- и К67это -N= или -N(R67)-, при условии, что К66 и К67 не будут одновременно -N(R66)- и -N(R67)- получают путем взаимодействия eнона формулы (XXVII'):
O 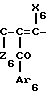 R610 (XXVII′) в которой Ar6 группа формулы (XVII'''), т.е. фенил, замещенный R63, R64и R65; Z6 и R610 имеют такое же значение, как и выше, и Х6 группа диалкил (низший) амино или алкокси, с гидразином, в случае необходимости замещения не более одним радикалом R66. Реакция проводится в алканоле, например в этиловом спирте, в присутствии неорганического или органического основания, например триэтиламина.
R610 (XXVII′) в которой Ar6 группа формулы (XVII'''), т.е. фенил, замещенный R63, R64и R65; Z6 и R610 имеют такое же значение, как и выше, и Х6 группа диалкил (низший) амино или алкокси, с гидразином, в случае необходимости замещения не более одним радикалом R66. Реакция проводится в алканоле, например в этиловом спирте, в присутствии неорганического или органического основания, например триэтиламина.
В случае, если R66 группа низший алкил или низший аралкил, то можно получить два изомера положения формулы (VII') и (VII''), в которых соответственно:
К66 это N= и K67 это N(R67)- или
К66 это -N(R66)- и K67 это -N= последний является преобладающим.
Используемый в качестве исходного вещества енон получается как указано в способе приготовления соединений формулы (V).
Соединения формулы (VII), если получено производное, в формуле которого Z6 OW6, можно перевести в производное, в формуле которого Z6= NR61, R62, при помощи классических методов органической химии. Если Z6это OW6, где W6 низший алкил, его можно трансформировать в Z6 NR61R62, путем нагревания при температуре от 100 до 200о, в случае необходимости под давлением, при избытке амина NHR61R62.
Из соединений, в формуле (VII) которых Z6 это 0-алкил, можно также получить соединения, в формуле которых Z6 это ОМ6, где М6 щелочной металл, при помощи реакции омыления с неорганическим основанием, например, со спиртовым раствором щелочи калия или щелочи натрия. Это соединение, образованное неорганической кислотой, например соляной или серной, дает производное (VII) с Z6 OH.
Из производного, в формуле (VII) которого Z6 это ОН, можно также получить соединение, в формуле которого Z6 NR61R62, после активирования функции карбоновой кислоты таким реагентом как тионилхлорид (SOCl2), фосфорилхлорид (POCl3), трихлорид или пентахлорид фосфора (PCl3, PCl5), дициклогексилкарбодиимид, карбонилдиимидазол, алкоилхлорформиат или трифторуксусный ангидрид, затем проводят реакцию с амином NHR61R62 в присутствии неорганического или органического основания, в среде органического растворителя, такого, как, например, хлорированный или ароматический растворитель (в частности, углеводород) или эфир, например ТГФ.
Следующие примеры, приводимые в качестве неограничивающих, иллюстрируют изобретение и показывают как его можно реализовать.
Структура в этих различных примерах была подтверждена методом ядерного магнитного резонанса.
В этих примерах были использованы следующие сокращения: PF точка плавления, выражена в оС (градусы Цельсия). Когда log P для продукта не приводится, это означает, что продукт является промежуточным химическим продуктом, а не продуктом, который можно использовать для лечения грибковых заболеваний растений.
Примеры с 101 по 170 относятся к продуктам подгруппы формулы (II).
П р и м е р 101. 2-(4-Морфолинокарбонил)-5-иодо-3-(3,4-диметоксифенил) бензотиофен (способ D, соединение 101).
В колбу 100 мл помещают 1,47 г (0,0037 моль) 2-(4-морфолинокарбонил)-5-амино-3-(3,4-диметоксифенил) бензоотиофена, 10 мл дистиллированной воды и 1,0 мл серной кислоты с концентрацией 98% В то время, как поддерживают температуру смеси меньше или равную 50оС, вливают постепенно раствор, содержащий 0,27 г (0,0039 моль) нитрита натрия в 5 мл воды. Перемешивают в течение 1 ч, затем реакционную смесь вливают и раствор, содержащий 10 мл воды и 0,65 г (0,0039 моль) иодида калия. Полученную смесь постепенно нагревают до 60оС и выдерживают при этой температуре в течение 1 ч. После охлаждения реакционную смесь экстрагируют 3 раза, каждый раз 50 мл метиленхлорида, органическую фазу промывают водой, высушивают над сульфатом магния и выпаривают. Очистку проводят хроматографическим путем на окиси алюминия, и получают 0,9 г 2-(4-морфолинокарбонил)-5-иодо-3-(3,4-диметоксифенил) бензотиофена, который плавится при 214оС (выход 48% соединение 101).
П р и м е р 102. 2-(4-Морфолинокарбонил)-5-(4-хлорбензоиламино)-3-(3,4-диметоксифенил)бензоти офен(способ С, соединение 102).
В колбу 100 мл последовательно помещают 2,0 г (0,005 моль) 2-(4-морфолинокарбонил)-5-амино-3-(3,4-диметоксифенил) бензотифен, 50 мл дихлорметана, 0,74 мл (0,0052 моль) триэтиламина и 0,70 мл (0,0052 моль) 4-хлоробензоилхлорида. После перемешивания при 20оС в течение 1 ч испаряют растворитель, промывают водой, сушат на воздухе, затем прополаскивают полученное твердое вещество 20 мл дихлорметана. Получают таким образом 1,0 г (37%) 2-(4-морфолинокарбонил)-5-(4-хлоробензоиламино)-3-(3,4-диметоксифенил)бензот иофекоторый плавится при 247оС (соединение 102).
П р и м е р 103. 2-(4-Морфолинокарбонил)-5-амино-3-(3,4-диметоксифенил)бензотиофен (способ В, соединение 103).
В колбу 250 мл последовательно помещают 10,7 г (0,025 моль) 2-(4-морфолинокарбонил)-5-нитро-3-(3,4-диметоксифенил) бензотиофена, 100 мл абсолютного этанола, 3 мл концентрированной соляной кислоты и 4,2 г (0,075 моль) порошка железа. В течение 2 ч реакционную смесь выдерживают с обратным холодильником, затем, после охлаждения, выливают в 200 мл насыщенного раствора бикарбоната натрия. После 6 экстрагирований при помощи 100 мл этилацетата органическую фазу высушивают над сульфатом магния, отфильтровывают и затем выпаривают, получают 9,2 г (выход 92%) 2-(4-морфолинокарбонил)-5-амино-3-(3,4-диаметокси-3,4-фенил) бензотиофена, который плавится при 213оС (соединение 103).
П р и м е р 104. 2-(4-Морфолинокарбонил)-5-нитро-3-(3,4-диметоксифенил)-бензотиофен (способ А, соединение 104).
В колбу последовательно помещают 9,0 г (0,0056 моль) альфа-меркаптоацетоморфолида, 13,8 г (0,1 моль) карбоната калия, 14,8 г (0,046 моль) 2-хлор-3', 4'-диметокси-5-нитробензофенона и 200 мл этанола. Смесь при помешивании нагревают с обратным холодильником в течение 2 ч, затем охлаждают до комнатной температуры и выливают в 1 л воды, образовавшийся желтый осадок отфильтровывают, промывают водой, просушивают током воздуха. Получают 18,1 г (92% ) 2-(4-морфолинокарбонил)-5-нитро-3-(3,4-диметоксифенил)-бензотиофена, который плавится при 144,5оС (соединение 104).
П р и м е р 105. 2-(4-Морфолинокарбонил)-5-(пропен-2-ил)-3-(3,4-диметоксифенил) бензотиофен (способ Е, соединение 105).
В колбу с инертной атмосферой последовательно помещают 2,0 г (0,005 моль) 2-(4-морфолинокарбонил)-5-бромо-3- (3,4-диметиоксифенил) бензотиофена, полученного по способу 1,50 мл 1,2-диметоксиэтана, 0,2 г тетракистрифенилфосфин палладия, 0,5 г (0,006 моль) 2-пропен-ил бороновой кислоты и 20 см3 2М-водного карбоната натрия. Смесь выдерживают с обратным холодильником в течение 8 ч, затем выливают в смесь воды и льда. Полученный продукт бежевого цвета отделяют фильтрованием, промывают в воде, затем высушивают на воздухе. При помощи хроматографии на окиси кремния получают 1,5 г (выход 81,5%) соединения 105, температура плавления 135оС.
П р и м е р 106. 2-(4-Морфолинокарбонил)-3-(4-метоксифенил)бензотиофен (способ F, соединение 106).
В колбу в инертной атмосфере помещают 1,0 г (0,0027 моль) 5-амино-2-(4-морфолинокарбонил)-3-(4-метоксифенил) бензо- тиофена и 50 мл тетрагидрофурана дистиллированного (ТГФ). Смесь доводят до рефлюкса, затем каплями приливают 0,7 мл (0,0054 моль) нитрита трет-бутила, растворенного в 20 мл ТГФ. Через 3 ч реакционную смесь обрабатывают водой, экстрагируют СН2Сl, промывают водой и высушивают над сульфатом магния. После выпаривания и хроматографии выделяют 0,5 г (выход 53%) соединения 106, которое плавится при 131оС.
П р и м е р 107. 2-(N,N-диэтилкарбоксамид)-3-(3,4-диметоксифенил)бензотиофен (способ G, соединение 107).
В колбу помещают 25 г (0,08 моль) 3-(3,4-диметоксифенил)бензотиофен-3-карбоновой кислоты, полученной по способу D, 300 мл 1,2-дихлорэтана, 12 мл (0,16 моль) тионилхлорида и 1 мл ДМФ. Смесь постепенно нагревают с обратным холодильником, твердое вещество понемногу растворяется и дает желтый прозрачный раствор. Через 4 ч растворители выпаривают, и получают 24,7 г (выход 96%) 2-(хлорокарбонил)-3-(3,4-диметоксифенил)бензотиофена. 2,5 г этого продукта сразу же вводят в реакцию с 4 см3 (0,0375 моль) N,N-диэтиламина в 100 мл ТГФ, после обработки водой и экстрагирования этилацетатом получают 2,5 г (выход 90% ) 2-(N,N-диэтилкарбоксамид)-3-(3,4-диметоксифенил)бензотиофена, который кристаллизуют при растирании в пентане. Температура плавления 113оС (соединение 107).
П р и м е р 108. 3-(3,4-Диметоксифенил)-2-этоксикарбонилинденон (способ G).
а) К 15 г 2-(3,4-диметоксибензоил)бензойной кислоты добавляют 25 г тионилхлорида и нагревают при 50оС до прекращения газовыделения. В конце реакции добавляют толуол и выпаривают, чтобы удалить избыточный SOCl2. Полученный хлорид кислоты представляет собой твердое оранжевое вещество.
b). Проводят реакцию хлорида кислоты с небольшим избытком этилмалонатонолята магния в толуоле (получается из этиламалоната и этилата магния). Реакционную смесь выливают в разбавленную серную кислоту и экстрагируют этилацетатом. После промывания водой и просушивания выпаривают растворитель, и получают красное масло, которое используется на следующем этапе.
с). Полученное масло нагревают с обратным холодильником с 300 мл 5%-ного раствора карбоната натрия в течение 35 мин. Образуется красное твердое вещество. Охлаждают, удаляют воду декантированием и снова добавляют 300 мл воды, снова нагревают с обратным холодильником в течение 35 мин. Охлаждают, фильтруют, промывают водой и высушивают. Получают инденон в форме оранжевого твердого вещества, температура плавления 130оС, выход 49% (соединение 108).
П р и м е р 109. 3-(3,4-Диметоксифенил)-2-морфолинокарбонилиденон.
Нагревают 0,9 г иденона, полученного в примере 108, вместе с 10 мл морфолина в течение 1 ч. Реакционную смесь выливают в разбавленный раствор соляной кислоты и экстрагируют этилацетатом, промывают водой и концентрируют. Получают продукт с выходом 98% (температура плавления 71,5оС, соединение 109).
П р и м е р 110. 1-(3,4-Диметоксифенил)-2-морфолинокарбонил-3-гидроксиинден.
0,5 г инденона из примера 109 восстанавливают 0,05 г NaBH4 и 0,5 г хлорида церия в 20 мл метанола. Реакция заканчивается через 10 мин, и реакционную смесь выливают в воду. При помощи разбавленной соляной кислоты доводят рН до 5 н. экстрагируют этилацетатом. Промывают водой и выпаривают растворитель. Получают 0,49 г инденола, температура плавления 134оС (выход 99% соединение 110).
П р и м е р 111. 2-Морфолинокарбонил-3-(3,4-диметоксифенил)-6-метоксиинден (способ Н).
а). В реакторе проводят реакцию 0,8 г натрия и 100 г абсолютного этанола. Затем добавляют 10 г 3,4-метоксибензоилацетоморфолида и перемешивают 15 мин. Затем добавляют 5,3 г хлорида 3-метилбензила. Нагревают с обратным холодильником в течение 1 ч 30 мин и концентрируют реакционную смесь при пониженном давлении. Промывают водой и разбавленной соляной кислотой и экстрагируют этилацетатом. Получают оранжевое масло.
b). К 5,1 г полученного масла добавляют 53 г полифосфорной кислоты и нагревают при 70оС в течение 6 ч. В реакионную смесь наливают воду и размешивают до растворения, затем экстрагируют этилацетатом. Проводят хроматографическую очистку (элюант этилацетат). Выход 25% Температура плавления 115оС (соединение III).
П р и м е р 112. 2-Морфолинокабонил-3-(3,4-диметоксифенил)-5,6-метоксиниден (способ I).
а). Конденсируют 3,4-(диметоксибензоил)ацетоморфолид с вератральдегидом в уксусной кислоте, в присутствии пиперидина и уксусного ангидрида. Нагревают до 100оС выливают в воду, экстрагируют этилацетатом и промывают органическую фазу концентрированным К2СО3. Проводят очистку на окиси алюминия, элюант-смесь гептан/этилацетат 10/90. Получают красное твердое вещество с температурой плавления 150оС.
b). Затем этиленкетон восстанавливают NaBH4 в присутствии хлорида церия в метаноле. Таким образом получают аллиловый спирт с выходом 83% (т-ра плавления 110оС).
с). В 80 мл толуола добавляют 2,2 г полученного ранее аллилового спирта и в каталитическом количестве паратолуолсульфоновую кислоту. Держат с обратным холодильником в течение 5 ч, удаляя воду, которая образуется в рeакции. Выливают в воду и декантируют, промывают в разбавленном бикарбонате натрия, затем опять промывают водой. Получают 1,9 порошка светло-каштанового цвета (соединение 112).
Следующие соединения были получены, используя один из описанных способов. Их структура, физико-химические характеристики и способ получения указаны в табл.1.
Эти соединения имеют формулу (II), в которой R15 означает Н и NR11R12 обозначает радикал 4-морфолино.
Структуры даются в табл.1 при помощи радикалов К110, R13, R14, R16, R17, R18, R19 формулы (II).
В табл.2 сведены данные по структуре и физико-химическим свойствам соединений формулы (II), в которых К110 атом серы, R13 и R14 метокси радикалы, R15, R16, R18, R19 атом водорода, R17 и NR11R12 указаны в табл.2. Соединения были получены по способу G.
П р и м е р ы 171-184. 2-Хлор-3'4'-диметокси-5-нитробензофенон (промежуточный продукт для приготовления продуктов формулы (II), в которой К110 O, S или N (R110).
В колбу помещают последовательно 11 г (0,05 моль) хлорида 2-хлор-5-нитробензоила, 20 мл (0,15 моль) 1,2-диметоксибензол и 0,5 г безводного хлорного железа. Затем смесь постепенно нагревают до 150оС и выдерживают при этой температуре в течение 1 ч. После охлаждения реакционную смесь выливают в 200 мл 1 н. HCl, затем три раза экстрагируют с помощью 200 мл дихлорметана каждый раз. После промывания раствором бикарбоната натрия органическую фазу высушивают над MgSO4, затем концентрируют при пониженном давлении, и получают коричневое масло. При растирании в 300 мл пентана выделяют 12,5 г (выход 79% ) 2-хлор-3',4'-диметокси-5-нитробензофенона в виде твердого продукта бежевого цвета, температура плавления 138оС (соединение 171).
Приведенные ниже соединения были получены в одинаковых условиях, их структура и физико-химические характеристики указаны в табл.3. Эти соединения являются продуктами формулы (XII'), в которой R15 означает H, R14 -радикал метокси и А1, R13, R16, R17, R18 и R19 имеют значения, указанные в табл.3.
Примеры с 201 по 253 относятся к соединениям, относящимся к подгруппе (II) формулы (III).
П р и м е р 201. 2-(3,4-Диметоксифенил)-4-(4-фторфенил)-1-морфолинокарбонилбен- зол.
В колбу 100 мл помещают 1,6 г (0,00454 моль) 2-(3,4-диметоксифенил)-4-(4-фторo-фенилбензойной кислоты (соединение 204), 50 мл тетрагидрофурана и 0,92 г (0,0057 моль) диимидазолкарбонила. Перемешивают при 20оС в течение 2 ч. Затем добавляют 1 мл (0,0113 моль) морфолина и выдерживают при помешивании в течение 6 ч. Реакционную смесь выливают в 150 мл дистиллированой воды, осадок отфильтровывают, промывают 100 мл воды, затем сушат на воздухе. Получают 1,3 г (выход 68%) 2-(3,4-диметоксифенил)-4-(4-фторфенил)-1-морфолинокарбонилбензол в виде белого твердого вещества, температура плавления 153оС (соединение 201).
Аналогичным образом получают соединения с 201 по 231. Эти соединения имеют формулу (III), в которой R23 и R24 являются группами метокси, R25, R28, R29 атом водорода и R26, R27, Z2 имеют приведенное в табл.4 значение.
Другая подгруппа соединений имеют формулу (III), в которой R23 и R24 вместе образуют двухвалентный радикал метилендиокси, R25, R26, R28, R29 атом водорода и R27 и Z2 имеет значение, данное в табл.5.
П р и м е р 232. 2-(3,4-Диметоксифенил)-4-(4-фторфенил)бензойная кислота (соединение 232).
В колбу 100 мл помещают 2,8 г (0,074 моль) 2-(3,4-диметоксифенил)-4-(4-фторфенил) этилбензоата, 50 мл абсолютного этанола и 2 мл 10 н. щелочи натрия. Смесь выдерживают при рефлюксе в течение 2 ч, затем выливают в 150 мл 1н. соляной кислоты. Осадок отфильтровывают на отожженном стекле, промывают водой и сушат на воздухе. Получают 2,1 г (выход 81%) соединения 232 (т-ра пл. 210оС).
П р и м е р 233. 2(3,4-Диметоксифенил)-4-(4-фторфенил)бензоатэтил (соединение 233).
В трехгорлую колбу 250 мл помещают 30 мл 1,2-диметоксиэтана, дегазированного аргоном, затем добавляют 3,65 г (0,010 моль) 4-бром-2-(3,4-диметоксифенил)бензоатэтила (соединение 209), 0,1 г тетракис(трифенил)фосфина палладия, 1,7 г (0,012 моль) 4-фторфенилбороновой кислоты и 20 мл карбоната натрия 2М. После выдержки при рефлюксе в течение 8 ч реакционную смесь выливают в 100 мл дистиллированной воды. Затем проводят экстрагирование 2 раза, каждый раз с 100 мл дихлорметана, затем промывают 100 мл воды, сушат над сульфатом магния и пропускают через слой окиси кремния, затем выпаривают. Получают 3,4 г (выход 89,5%) 2-(3,4-диметоксифенил)-4-(4-фторфенил)бензоатэтила, температура плавления 127оС (соединение 233). Аналогичным образом получают соединения формулы (III), в которой R23 и R24 группы метокси, R25, R26, R28, R29 атом водорода, R27 и Z2 имеют значения, которые приведены в табл.6.
Получены также соединения формулы (III), в которой R23 и R24образуют вместе двухвалентный радикал метилендиоксо, R25, R26, R27, R29- атом водорода и R27 и Z2 имеют значение, приведенное в табл.7.
П р и м е р 250. 4-Бром-2-(3,4-диметоксифенил)-6-бензоатэтила (соединение 250).
В трехгорлую колбу 1000 мл помещают 20,0 г (0,066 моль) 4-амино 2-(3,4-диметоксифенил)бензоатэтила (соед. 252) и 200 мл уксусной кислоты. После растворения добавляют 60 мл бромистоводородной кислоты, 47% охлаждают до 0оС, затем добавляют 150 мл дистиллированной воды. Вливают 4,6 г (0,066 моль) нитрита натрия, растворенного в 30 мл воды. Перемешивают при температуре от 0 до 5оС в течение 1 ч, затем смесь выливают в раствор бромида меди (0,066 моль, 0,5 г) в 100 мл 47%-ной бромистоводородной кислоты. Смесь нагревают при 65оС в течение часа, затем выливают в воду. Образующийся осадок отфильтровывают, промывают водой, затем сушат в воздухе. Получают 18,4 г (выход 76,3%) 4-бромо-2-(3,4-диметоксифенил)бензоатэтила, температура плавления 53оС (соединение 250).
Аналогичным образом получают соединения формулы (III), в которой R23, R24 группы метокси, R25, R26, R28, R29 атом водорода, Z2 имеет значение, приведенное в табл.8 и R2 атом брома.
П р и м е р 252. 4-Амино-2-(3,4-диметоксифенил)бензоатэтила (соединение 252).
В колбу 500 мл помещают 200 мл 1,2-диметоксиэтана, затем 17 г (0,07 моль) 4-амино-2-бромбензоатэтила (соединение 218), 0,3 г тетракис(трифенил)фосфина и 100 мл карбоната натрия 2М. Через 8 ч кипячения с обратным холодильником реакционную смесь выливают в 600 мл воды. Фильтруют, промывают водой и сушат на воздухе полученное твердое вещество. Промывают 50 мл пентана. Получают 20,0 г (выход 95%) 4-амин-2-(3,4-диметоксифенил)бензоатэтила, температура плавления 127оС (соединение 252).
Аналогично получают соединения формулы (III), в которой R23, R24группы метокси, R25, R28, R29 атомы водорода, а Z2, R27, R26 имеют приведенное в табл.9 значение.
П р и м е р 254. 4-Амин-2-бромбензоатэтила (соединение 254).
В колбу 1 л помещают последовательно 46 г (0,17 моль) 2-бромо-4-нитробензоатэтила, 250 мл этанола, 28 г (0,5 моль) порошка железа и 20 мл концентрированной соляной кислоты. Смесь нагревают с обратным холодильником в течение 4 ч. После охлаждения реакционную смесь обрабатывают 500 мл насыщенного раствора бикарбоната натрия и экстрагируют 5 раз, каждый раз с 300 мл этилацетата. После высушивания на сульфате магния, фильтрования и выпаривания выделяют 35,2 г (выход 86%) 4-амин-2-бромбензоатэтила, который плавится при 93оС (соединение 254).
Примеры с 301 по 390 и с 3100 по 3119 иллюстрируют получение соединений формулы (IV).
П р и м е р 301. N-(2-(3,4-диметоксифенил)-6-фенилникотиноил) морфолин (соединение 301) (способ b).
К раствору 1,9 г (0,005 моль) хлорида 2-3,4-диметоксифенил-6-фенил)никотиноила (соединение 2) в 60 мл тетрагидрофурана приливают по каплям при 25-30оС 1,8 г (0,002 моль) морфолина. Хлоргидрат выпадает в осадок с начала приливания. По окончании добавления оставляют на 10 мин, разбавляют 100 мл воды. Раствор высушивают над безводным сульфатом магния, затем концентрируют при пониженном давлении. Получают масло, которое кристаллизуется в эфире. После фильтрования и просушивания получают 1,9 г порошка бежевого цвета (выход 95%), температура плавления 185,5оС.
Примеры с 304 по 309: хлорид 2-(3,4-диметоксифенил)-6-фенилникотиноила (соединение 302).
Смесь 1,8 г (0,0054 моль) 2-(3,4-диметоксифенил)-6-фенилникотиновой кислоты (соединение 303) и 20 мл тионилхлорида нагревают в течение 1 ч при кипении с обратным холодильником. Среду концентрируют при пониженном давлении. Получают 1,9 г (выход 100%) желтого меда.
Проводя те же операции, получают хлориды никотиноила формулы (IV'''), в которой Z3 атом хлора и R371 имеет приведенные в табл.10 значения.
П р и м е р ы 303, 310-313. 2-(3,7-Диметоксифенил)-6-фенилникотиновая кислота (соединение 303).
К раствору 3,6 г (0,01 моль) 2-(3,4-диметоксифенил)-6-фенилникотинатэтила (соединение 309) в 100 мл 95%-ного спирта добавляют 2 мл 30%-ной щелочи натрия. Нагревают при 60-70оС 2 ч. Среду концентрируют при пониженном давлении и остаток растворяют в 100 мл воды. Среду подкисляют 2 мл концентрированной соляной кислоты. С выпадением смолообразного продукта. Экстрагируют 100 мл этилацетата. Раствор промывают 2 раза 100 мл воды, сушат над безводным сульфатом магния, затем концентрируют при пониженном давлении. Получают вещество в виде воздушной массы, которое кристаллизуют при растирании в 50 мл эфира. После фильтрования и сушки получают 2,5 г (выход 75%) порошка бежевого цвета, который плавится при 178оС. Точно таким же способом получают соединения формулы (IV'''), в которой Z3группа гидрокси, а R361 имеет приведенные в табл.11 значения.
П р и м е р ы 309, 315-317. 2-(3,4-Диметоксифенил)-6-фенилникотинатэтила (соединение 309) (способ а').
В течение 4 ч нагревают с обратным холодильником смесь 7,7 г (0,02 моль) 2-(3,4-диметоксибензоил)-5-окси-5-фенилвалератэтила (соединение 314), 3,1 г (0,04 моль) ацетата аммония и 30 мл уксусной кислоты. Реакционную смесь выливают в 300 мл воды с образованием масла. Масло экстрагируют 200 мл этилацетата. органический раствор промывают 5 раз 100 мл воды, затем сушат над безводным сульфатом магния и концентрируют при пониженном давлении. Получают 4,5 г светло-коричневого масла (выход 62%), которое соответствует 2-(3,4-диметоксифенил)-6-фенилникотинат этила.
Точно таким же способом получают соединения формулы (IV'''), в которой Z2 этокси, а R371 имеет значения, приведенные в табл.12.
П р и м е р ы 318-320. Проводя операции по способу а' с помощью соответствующих промежуточных соединений, соответственно замещенных, получают соединения формулы (IV''') с Z3-этокси, приведенные в табл.13.
П р и м е р ы 321-344. 2-(3,4-Диметоксибензоил)-5-оксо-5-фенилвалерат этила (соединение 314).
К спиртовому раствору 13,7 г (0,05 моль) натриевой соли (3,4-диметоксибензоил)ацетат этила добавляют 8,4 г (0,05 моль) 3-хлоропропиофенона: реакция экзотермическая и температура постепенно повышается от 24 до 35оС. Проводят реакцию при помешивании в течение 3/4 ч (возвращается к комнатной температуре). Выливают реакционную смесь в 400 мл воды: продукт выделяется в виде смолы. Его экстрагируют 300 мл хлороформа. Хлороформовый раствор промывают 5 раз 200 мл воды, сушат над безводным сульфатом магния и концентрируют при пониженном давлении. Получают 19,5 г продукта в виде коричневого меда. Продукт кристаллизуют после растворения в 100 мл эфира. После фильтрования осадка и сушки получают 15 г (выход 77%) порошка бежевого цвета, температура плавления 70оС соответствует 2-(3,4-диметоксибензоил)-5-оксо-6-фенилвалерат этила.
Точно таким же способом получают соединения, которые приведены в табл. 14, формулы
(3/4-диметоксифенил)-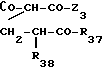
П р и м е р 345. Получение N-[5-(4-хлорфенил)-2-(3,4-диметоксибензол)-5-никотиноил]морфолина (соединение 345) (способ а).
Растворяют 46 г (0,1 моль) N-[5-(4-хлорфенил)-2-(3,4-диметоксибензоил)-5-оксова- лерил] морфолино (соединение 346) и 15,4 г (0,2 моль) ацетата аммония в 150 мл уксусной кислоты. Нагревают в течение 4 ч до кипения с обратным холодильником, пропуская через среду воздух. Охлаждают до комнатной температуры, выливают в 0,5 л воды, образуется смолообразный продукт. Смолу экстрагируют 200 мл хлорметилена. Хлорметиленовый раствор промывают водой, затем раствор обрабатывают активированным углем. Раствор концентрруют. Получают продукт в виде желтоватого меда, который кристаллизуют при растирании в 200 мл эфира. Кристаллический продукт отфильтровывают, промывают в эфире и затем сушат при пониженном давлении. Получают 21,2 г порошка бежевого цвета, который плавится при температуре 152оС (выход 48%).
П р и м е р ы 345-394. Работают, как указано в примерах 345 (способ а) и 301 (способ b), но исходят из промежуточных продуктов, соответственно замещенных. Получают производное формулы (IV''') у которого заместители, применяемый метод и физические характеристики указаны в табл.15.
Замещенные радикалы морфолино пронумерованы по атому кислорода, при этом свободная валентность относится к атому азота. Звездочка означает, что соединение является промежуточным при синтезе.
П р и м е р ы 3110-3119. Проводят операции, как это описано в примере 345 (способ а), но исходят из соответственно замещенных промежуточных соединений, и получают производные формулы (IV'), в которой NR31R32 радикал морфолино и R37 имеет значения, которые перечислены в табл.16-17, приводятся также физические характеристики продуктов.
В примерах с 401 по 458 описывается приготовление производных соединений формулы (V).
П р и м е р 401. 3-(3,4-Диметоксифенил)-3-оксо-2-(диметиламинометилен)пропионат этила (соединение 401).
В реактор помещают 20 г 3,4-диметоксибензоилацетат этила, 80 мл толуола и 20 г диметилформамиддиметилацеталя. Нагревают с обратным холодильником в течение 2 ч и оставляют на ночь при комнатной температуре. Выпаривают растворитель и избыток реактива. Продукт очищают пропусканием через окись алюминия (элюант: этилацетат). Получают продукт в виде желтого меда с выходом 94%
П р и м е р 402. 1-(3,4-Диметоксифенил)-3-диметиламино-2-морфолинокарбонил- пропенон (соединение 402).
В реактор помещают 20 г 3,4-диметоксибензоилацетоморфолида, 28 г диметилформамид диметилацеталя и 20 мл диметилформамида. В течение 7 ч нагревают при 60оС и оставляют на ночь при комнатной температуре. Выливают в воду и профильтровывают полученный осадок. Получают желтое твердое вещество с температурой плавления 156,8оС, выход 84%
П р и м е р 403. Проводя операции, как в примерах 401 и 402, но используя соответственно замещенные промежуточные соединения, получают производные формулы (XV'), в которой Ar4 имеет указанное значение и в которой R43 и R44 группы метокси, R45 и R49 атом водорода.
X4 и Z4 имеют значение, указанное в табл.18.
П р и м е р 405. 5-Карбетокси-2(4-хлорфенил)-4-(3,4-диметоксифенил)пиримидин (соединение 405).
В реактор помещают 20 мл абсолютного этанола и 0,3 г натрия. После растворения добавляют 3,7 г гидроиодида 4-хлоробензамидина. Нагревают с обратным холодильником в течение часа и добавляют 4,06 г енаминона, синтезированного в примере 401. Нагревают с обратным холодильником в течение 2,5 ч, выпаривают растворитель, промывают полученный осадок водой и сушат. Получают 4,2 г белого твердого вещества, которое плавится при 115,4оС.
П р и м е р 406. 5-Карбокси-2-(4-хлорфенил)-2-(3,4-диметоксифенил) пиримидин (соединение 406).
Полученный в примере 404 продукт (3,3 г) растворяют в 100 мл этанола и обрабатывают 2 мл 10 н. щелочи натрия. Смесь нагревают в течение часа при 80оС и выпаривают. Промывают остаток в воде и подкисляют соляной кислотой. Получают желтый осадок, который фильтруют и промывают водой.
Выход 95% температура плавления 258,1оС.
П р и м е р 407. 2-(4-Хлорфенил)-4-(3,4-диметоксифенил)-5-морфолинокарбонилпи- римидин (соединение 407).
Нагревают 1,5 г кислоты, полученной в примере 406, с 35 мл тионилхлорида в течение 1,5 ч при 75оС. Концентрируют и добавляют дихлорметан, снова выпаривают, чтобы полностью удалить избыточный реактив. Получают твердое вещество оранжевого цвета. Полученный хлорид кислоты растворяют в 100 мл этилового эфира и охлаждают до 0оС. Добавляют по капле раствор 0,7 г морфолина и 0,4 г пиридина в 40 мл эфира. После добавления перемешивают в течение 1,5 ч при комнатной температуре. Выливают в воду и экстрагируют эфиром, сушат над сульфатом магния и концентрируют. После рекристаллизации в эфире получают 1 г твердого вещества, которое плавится при 168оС (выход 48%).
П р и м е р 408. 2-(3,4-Дихлорфенил)-4-(3,4-диметоксифенил)-5-морфолинокарбо-нилпиримидин (соединение 408).
В реактор помещают 10 мл абсолютного этанола и 0,1 г натрия. Перемешивают до растворения и добавляют 1,35 г 3,4-дихлорбензамидин-бензолсульфоната. Нагревают при 60оС в течение 30 мин и добавляют енаминон, полученный в примере 402, и 15 мл абсолютного этанола. Нагревают с обратным холодильником в течение 5 ч, фильтруют и промывают осадок в холодном этаноле и в гептане. Сушат и получают твердое вещество, которое плавится при 181оС (выход 83%).
Проводят операции, как и в примерах с 405 по 408, но используя промежуточные продукты, соответственно замещенные, получают производные формулы (V), в которой R43 и R44 группа метокси, R45 и R49 атома водорода, Z4 и R47 имеют приведенные в табл.19 значения.
П р и м е р 423. 4-(3,4-Диметоксифенил)-2-метилтио-5-морфолинокарбонилпирими- дин (соединение 423).
В реакторе растворяют 6,6 г КОН в 60 мл воды, затем добавляют 16,3 г сульфата S-метилизотиомочевины и сразу же 13,6 г енаминона, синтезированного в примере 402. После нагревания с обратным холодильником в течение 1,5 ч образуется осадок, который фильтруют, промывают водой и высушивают. Получают твердое вещество, выход 58% температура плавления 151оС.
П р и м е р 432. 4-(3,4-Диметоксифенил)-2-метилсульфонил-5-морфолинокарбонил- пиримидин (соединение 432).
В 10 мл дихлорметана растворяют 9,5 г пиримидина, полученного в примере 423, и при температуре 0оС добавляют частями 11 г метахлорпероксибензойной кислоты. Перемешивают при комнатной темепратуре в течение 2,5 ч. Избыток перкислоты разрушают бисульфатом натрия и затем промывают раствор бикарбонатом. Промывают и сушат над сульфатом магния. После выпаривания растворителя получают 9,9 г твердого белого вещества, температура плавления которого равна 77оС.
П р и м е р 433. 4-(3,4-Диметоксифенил)-2-(4-метил-фенокси)-5-морфолинокарбонилпиримидин (соединение 433).
В реактор помещают 10 мл ацетонитрила, 0,6 г карбоната натрия, 2,7 г паракрезола и 1 г пиримидина, полученного в примере 432, а также три капли [трис(3,6-диокса-гептил)амина] в качестве катализатора. Нагревают при 65оС в течение часа и выпаривают растворитель. Обрабатывают водой и экстрагируют эфиром, сушат над MgSO4 и выпаривают. Получают твердое белое вещество выход 75% температура плавления 152оС.
Проводя операции, как и в примерах 423, 432, 433, но, используя соответственно замещенные промежуточные вещества, получают производные формулы (V), в которой R43 и R44 группы метокси, R45 и R49 атомы водорода, Z4 и R47 имеют значения, указанные в табл.20.
П р и м е р 501. 2-Ацетил-3-(3,4-диметоксифенил)-5-фенил-5-оксивалерат этила (соединение 501).
Растворяют 26,8 г (0,1 моль) 3,5-диметоксихалкон (m, p-(CH3O)2C6H3CH= CH-CO C6H5) и 13 г (0,1 моль) этилацетоацетата в 300 мл этанола. Добавляют 1 г активированного барита и перемешивают 20 ч при 20оС. Осадок оксовалерата фильтруют, промывают этанолом и сушат. Получают 27 г (выход 68%) соединения 501, которое плавится при 135оС.
П р и м е р 502. 4-(3,4-Диметоксифенил)-2-метил-6-фенилникотинат этила (соединение 502).
В течение 5 ч кипятят с обратным холодильником смесь 20 г (0,05 моль) соединения 501, 7,7 г (0,1 моль) ацетата аммония и 80 мл уксусной кислоты. Выпаривают, растворяютв 200 мл метиленхлорида, промывают в водном растворе бикарбоната натрия, затем в воде. Концентрируют и очищают хроматографически на окиси алюминия. Получают 8,5 г твердого вещества бежевого цвета, которое плaвится при 82оС (выход 45% соединение 502).
П р и м е р 503. 4-(3,4-Диметоксифенол)-2-метил-6-фенилникотиновая кислота (соединение 503).
В течение 30 ч кипятят с обратным холодильником, смесь 10 мл водного 10 н. раствора щелочи натрия с раствором 8,4 г (0,022 моль) соединения 502 в 100 мл этанола. Концентрируют, растворяют в воде, подкисляют, экстрагируют этилацетатом, сушат, концентрируют. Получают 4,7 г (выход 61%) соединения 503, которое плавится при 208оС.
П р и м е р 504. Хлорид 4-(3,4-диметоксифенил)-2-метил-6-фенилникотиноила (соединение 504).
В течение 1 ч кипятят с обратным холодильником смесь 3,5 г (0,01 моль) соединения 503 с 20 мл тинилхлорида. Концентрируют. Получают целевой продукт красно-оранжевого цвета, кристаллический. Выход 100% Температура плавления 140оС.
П р и м е р 505. N-[4-(3,4-Диметоксифенил)-2-метил-6-фенилникотиноил] морфо- лин (соединение 505).
Этот продукт имеет формулу (VI), где R59 метил, Z5=морфолино, R53=R54= метокси, R55 R56 H, R57 C6Н5. К раствору 1,2 г (0,033 моль) соединения 503 в 50 мл хлороформа добавляют 2 мл морфолина. Реакция идет при 20оС в течение 3 ч, затем промывают водой, концентрируют, кристаллизуют в эфире, фильтруют, сушат. Получают 0,9 г соединения 505 (белый порошок, выход 65%), температура плавления 176оС log P 3,8.
П р и м е р ы 506, 507. Соединения 506, 507 получают точно так же, как и в примере 505, заменяя морфолин соответственно на CH3-NH-C2H5 и на CH3-NH-CH2-CH2-O-CH3. Соединение 506 плавится при 76оС (log P4,2). Соединение 507 представляет собой мед (log P 4,0).
П р и м е р 601. 2-(3,4-Диметоксифенил)-6-фенил-3-фуран карбоксилат этила.
В течение 12 ч нагревают с обратным холодильником смесь 10 г (0,027 моль) 2-(3,4-диметоксибензоил-4-фенил)-4-оксобутира- та этила, 2,75 г (0,027 моль) уксусного ангидрида, 2 кпли концентрированной серной кислоты и 50 мл уксусной кислоты. Реакционную смесь выливают в 500 мл воды. Продукт экстрагируют в 300 мл этилацетата, промывают органический раствор водой с бикарбонатом, затем чистой водой. Раствор сушат над безводным сульфатом магния, концентрируют при пониженном давлении, получают смолу, которая кристаллизуется при растирании в 50 мл гептана. После фильтрования и высушивания получают 6,5 г (выход 68%) продукта в виде порошка бежевого цвета, который плавится при 68оС (соединение 601).
П р и м е р 602. 2-(3,4-Диметоксифенил)-6-фенил-3-фуроиновая кислота.
В течение часа нагревают с обратным холодильником смесь, которая содержит 5 г (0,0142 моль) соединения, полученного в примере 601, 6 мл 10 н. щелочи натрия и 100 мл этилового спирта. Концентрируют при пониженном давлении, растворяют остаток в 100 мл воды и подкисляют до рН 4 водный раствор концентрированной соляной кислотой: выпадает белое твердое вещество. Осадок фильтруют, промывают водой, высушивают продукт при пониженном давлении в присутствии Р2О5. Получают 4,3 г (выход 93%) продукта в виде порошка белого цвета, который плавится при 177оС (соединение 602).
П р и м е р 603. Хлорангидрид 2(3,4-диметоксифенил)-6-фенил-3-фуроиновой кислоты.
В течение 45 мин нагревают с обратным холодильником смесь 2,8 г продукта из примера 602 и 20 мл тионилхлорида. Концентрируют при пониженном давлении, при этом кристаллизуется зеленое твердое вещество. Получают 3 г (количественный выход) продукта, который плавится при 114оС (соединение 603).
П р и м е р 604. 2-(3,4-Диметоксифенил)-5-фенил-N-этил-N-этил-3-фуранкарбокса- мид.
Растворяют 1,51 г (4,4 ммоль) хлорида из примера 603 в 20 мл ТГФ. При помешивании добавляют 0,59 г (10 ммоль) метилетиламина: сразу же выпадает в осадок хлоргидрат амина. Перемешивают в течение 1/4 ч при обычной температуре, хлоргидрат фильтруют и фильтрат концентрируют. Обрабатывают остаточный мед в 100 мл хлороформа. Хлороформовый раствор промывают водой, раствор концентрируют, кристаллизуют продукт в смеси диизопропилового эфира и гептана. После фильтрования и просушивания получают 0,6 г (выход 37%) соединения в виде порошка бежевого цвета, которой плавится при 74оС (соединение 604).
П р и м е р 605. N-[2-(3,4-Диметоксифенил)-6-(4-фторфенил)-3-фуроил]морфолин.
В течение 30 ч нагревают с обратным холодильником смесь, которая содержит 1 г (2,3 ммоль) N-[2-(3,4-диметоксибензоил)-4-(4-фторфенил)-4-оксобутироил] -морфолина, 20 мл этанола и 1 мл концентрированной соляной кислоты. Реакционную смесь выливают в 200 мл воды, продукт экстрагируют 150 мл хлороформа. Хлороформовый раствор промывают водой, хлороформовый раствор концентрируют, кристаллизуют при растирании в 20 мл эфира. После фильтрования и сушки получают 0,8 г (выход 83%) продукта в виде белого порошка, который плавится при 168оС (соединение 605).
П р и м е р 606. 2-(3,4-Диметоксифенил)-5-(4-фторфенил)-3-(морфолинокарбонил) пиррол.
В течение 12 ч с обратным холодильником нагревают смесь: 5 г (11,6 ммоль) N-[2-(3,4-диметокси-бензоил)-4-(4-фторфенил-4-оксобутирил)]морфолина, 1,8 г (23,2 ммоль) ацетата аммония, 30 мл уксусной кислоты.
Реакционную смесь выливают в 30 мл воды, экстрагируют продукт 200 мл этилацетата, органический раство промывают бикарбонатовой водой, затем чистой водой, раствор сушат над безводным сульфатом магния. Раствор концентрируют, продукт кристаллизуют в 300 мл толуола. Получают 1,4 г (выход 28%) продукта в виде желтого порошка, который плавится при 190оС (соединение 606).
П р и м е р 607. 5-(4-Фторфенил-2-(3,4-диметоксифенил)-4-метил-3-(морфолино- карбонил)пиррол.
В 30 мл уксусной кислоты растворяют 0,72 г (0,023 моль) монометиламина, 5 г (0,00115 моль) N-[2-(3,4-диметоксибензоил)-4-(4-фенил)-4-оксо-бутироил] морфолина. В течение 10 ч реакционную смесь нагревают с обратным холодильником. Затем реакционную смесь выливают в 300 мл воды. Продукт экстрагируют 200 мл этилацетата. Раствор промывают бикарбонатовой водой, затем чистой водой. Затем раствор над сульфатом магния и концентрируют. Получают твердое вещество каштанового цвета, которое рекристаллизуется в эфире. Получают 1,3 г продукта (выход 26%), температура плавления 148оС (соединение 607).
П р и м е р 608. 2-(4-Хлорфенил)-3-(диметокси-3,4-фенил)-4-(морфолинокарбонил) пиразол.
В реактор помещают 2,5 г 1-(3,4-диметоксифенил)-3-(диметиламино)-2-морфоли- нокарбонил пропенона (пример 402), 2,1 г хлоргидрата 4-хлорфенилгидразина, 1,2 г хлоргидрата 4-хлорфенилгидразина, 1,2 г триэтиламина и 100 мл этанола. Нагревают с обратным холодильником в течение 8 ч 30 мин. Растворитель выпаривают, выливают в воду, над сульфатом натрия и концентрируют. После фильтрования через окись алюминия (элюент этилацетат/гептан 90/10) получают 2,1 г желтого твердого вещества, которое плавится при 125оС (выход 60%) (соединение 608).
П р и м е р 609. 4-Карбэтокси-2-(4-хлорфенил)-3-(3,4-диметоксифенил)пиразол.
В реактор помещают 2,5 г 3-(3,4-диметоксифенил)-3-оксо-2-(диметиламиномети- лен) пропионат этила (пример 401), 1,49 г хлоргидрата 4-хлорфенилгидразина, 0,82 г триэтиламина и 100 мл этанола. Нагревают с обратным холодильником в течение 8 ч. Выпаривают растворитель, выливают в воду и обрабатывают этилацетатом. После сушки над сульфатом, натрия и выпаривания растворителя получают 3 г твердого вещества каштанового цвета (выход 95%), которое используется без очистки (соединение 609).
П р и м е р 610. 4-Карбокси-2-(4-хлорофенил)-3-(3,4-диметоксифенил)пиразол.
Полученный в примере 609 эфир (3 г) помещают в реактор, который содержит 150 мл этанола, и обрабатывают 1,01 г растертой 86%-ной гидроокиси калия. Нагревают с обратным холодильником в течение 4 ч. Выпаривают растворитель, выливают в воду и подкисляют 1 н. раствором соляной кислоты до рН 1. Полученный осадок отфильтровывают, промывают водой, затем гептаном, и получают 2,6 г порошка каштанового цвета (93,3%), который применяют без очистки (соединение 610).
П р и м е р 611. 4-(N-Метил-N-этиламинокарбонил)-2-(4-хлорфенил)-3-(3,4-димето- ксифенил) пиразол.
Нагревают 2,6 г кислоты, полученной в примере 610, с 50 мл тионилхлорида (75% ) в течение 8 ч. Обрабатывают продукт в дихлорметане и концентрируют. Полученное масло растворяют в 30 мл хлорметилена и охлаждают до 3оС. Добавляют раствор 0,54 г N-метил-N-этиламина и 0,3 г пиримидина, 30 мл хлорметилена, поддерживая температуру ниже 5оС. Перемешивают в течение 6 ч 20 мин при комнатной температуре. Выливают в воду и экстрагируют хлорметиленом. Сушат над сульфатом натрия и концентрируют. Получают 1,2 г оранжевого осадка, который плавится при 110оС (соединение 611).
П р и м е р 612. 4-(N,N-Диэтиламинокарбонил)-2-(4-хлорфенил)-3-(3,4-диметоксифе- нил)-пиразол.
Проводят операции, что и в примере 611, используя диэтиламин. Выход 80% це- левого продукта в виде оранжевого меда (соединение 612).
П р и м е р 613. 1-Бензил-3-(3,4-диметоксифенил)-4-(морфолинокарбонил)пиразол.
Проводят операции, что и в примере 608, используя хлоргидрат бензилгидразина. Получают 22,8% целевого продукта в виде желтого масла вместе с ожидаемым в данных условиях изомером (45,7%) (соединение 613).
П р и м е р 614. 1-(4-Бромбензил)-3-(3,4-диметоксифенил)-4-(морфолинокарбонил)пиразол.
В реактор помещают 0,7 г 3-(3,4-диметоксифенил)-4-(морфолинокарбонил)пира-зола (получен при проведении тех же операций, что и в примере 608, с гидратом гидразина), 0,7 г 4-бромбензила, 0,4 карбоната калия к 70 мл ДМФ (диметилформамид), нагревают при 75оС в течение 5 ч 30 мин. Выливают в воду, экстрагируют этилацетатом, высушивают и концентрируют. После фильтрования через окись алюминия получают 0,6 г (выход 43,5%) твердого продукта, который имеет температуру плавления 122оС (соединение 614).
Проводя те же операции, что и в примерах с 601 по 614, но используя соответственно замещенные промежуточные соединения, получают соединения формулы (VII), в которой R610 означает -СН-, R63 и R64 группы метокси, R65 атом водорода, NR61 R62, К66, К67 имеют значения, которые указаны в табл.21.
Биологические испытания.
Приведенные ниже испытания показывают фунгицидные свойства соединений в соответствии с изобретением.
П р и м е р В1. Лечение милдью томатов (Phytophtore infestans).
Томатные растения (Lycopesicon esculentum) сорта Марманд выращивают в стаканчиках. Когда возраст растений достиг одного месяца (стадия 5-6 листьев, высота 12-15 см), их обрабатывают разбрызгиванием суспензии водного раствора исследуемого веществ при требуемой концентрации и с добавлением поверхностно активного вещества, которое представляет собой соконденсат моноолеата сорбитана с 20 молекулами этиленоксида. Концентрация поверхностно-активного вещества составляет половину концентрации активного вещества. На каждое томатное растение попадает около 5 мл суспензии или дисперсии. Для каждой концентрации исследуемого активного вещества проводят обработку двух растений. Растения, используемые в качестве контрольных образцов, обрабатывают раствором, который не содержит активное вещество, но в нем такая же концентрация поверхностно-активного вещества. После высушивания в течение 24 ч каждое растение заражают путем пульверизации водной суспензии спор Phуtophtora infestans, которые вызывают милдью, из расчета 5 мл/растение (т.е. около 50 000 спор на растение). После этого заражения томатные растения инкубируют в течение дня, в насыщенной влажностью атмосфере при 15оС, затем пять дней при 17оС при относительной влажности 70-90%
Через неделю после заражения сравнивают результаты, полученные для растений, обработанных активным веществам, и для контрольных растений.
В этих условиях было установлено, что доза 1000 ppm (1 г/л) соединений 104, 110, 111, 112, 113, 117, 118, 129, 133, 148, 149, 150, 164, 166, 167, 169, 201-203, 205, 206, 208, 209, 211, 212, 214, 222, 223, 235, 236, 237, 238, 301, 345, 347, 349, 350, 353, 356, 359, 369, 370, 379, 381, 382, 384-386, 388, 391, 393, 396, 3113, 3118, 3119, 407, 414-416, 433, 434, 435, 440, 445, 458, 505-507, 607, 619, 621, 608, 6084 вызывают задержку не менее чем на 80% развития грибка.
П р и м е р В2. Обработка милдью виноградников (Plasmopara viticola).
Черенки винограда (Vitis vinifera) сорта Шардоне выращивают в горшочках. Когда их возраст достигает 2 месяца (стадия 8-10 листочков, высота 20-30 см), их обрабатывают точно так же, как и в примере В1. После сушки в течение 24 ч каждое растение заражали распылением водной суспензии спор Plasmopora viticola, которые вызывают милдью винограда, из расчета 5 мл растение (около 100 000 спор на растение). После заражения растения инкубируют в течение двух дней при 18оС в атмосфере при насыщенной влажности, затем в течение 5 дней при 20-22оС при относительной влажности 90-100%
Через неделю после заражения сравнивают результаты для растений, обработанных активным веществом, и для контрольных растений.
Для этих условий было установлено, что при дозе 330 ppm (0,33 г/л) соединения 101, 104, 105, 107, 110-118, 121-125, 127-134, 136, 137, 141, 148-150, 152-160, 162-164, 166-170, 201-203, 204, 205, 206, 208, 209, 210, 211, 212, 213, 214, 215, 217, 222, 223, 229, 234-239, 301, 345, 347, 349-351, 353-356, 358, 359, 361-370, 373-380, 382-391, 393, 394, 396, 397, 399, 3100, 3110, 3112-3119, 407, 414-416, 420, 421, 433-442, 445, 450, 458, 505-507, 616, 607, 608, 612, 613, 619, 621, 623, 626 задерживают не менее чем на 80% развитие грибка.
П р и м е р В3. Действие на фитопатогенные грибки почвы.
Соединениями в соответствии с изобретением обрабатывают следующие грибки.
Phytophtora citophtora паразит корней цитрусовых растений, проявляется микозамин и деформациями воздушных частей корней. При каждом испытании действуют следующим образом: питательную среду на основе картофельного экстракта, отвержденного агар-агаром, вносят в переохлажденном состоянии в серию чашек Петри (20 мл в чашке) после стерилизации в автоклаве при 20оС. В ходе заполнения чашек в переохлажденную среду впрыскивают ацетоновый раствор активного вещества, чтобы получить требуемую концентрацию. В качестве контрольных берут чашки Петри, аналогичные предыдущим, в которые наливают такие же количества питательной среды, не содержащей активного вещества. После отверждения каждую чашку засевают фрагментом мицелия с предыдущей культуры того же грибка. Чашки хранят в течение 5 дней при 22оС, затем сравнивают рост грибка в чашках с активным веществом и в контрольных чашках. В этих условиях, при дозе 30 ppm (частей на миллион) следующие соединения вызвали не менее 80% задержки развития грибков: 101, 102, 104, 105, 107, 110-118, 121-129, 131-137, 141, 149, 150, 153-158, 162-164, 166, 167, 169, 201-203, 204, 205, 206, 208, 209, 210, 211, 212, 213, 214, 215, 216, 217, 222, 223, 224, 228, 229, 230, 231, 234-239, 301, 345, 347, 349, 350, 350, 353, 353, 354, 355, 356, 358-360, 363-370, 373, 376-386, 388-397, 3110-3119, 407, 414-416, 420, 425-430, 433-442, 445, 447, 449, 450, 458, 505, 507, 607, 608, 619-621.
Использование соединений по изобретению.
Соединения в соответствии с изобретением могут использоваться как активные фунгицидные вещества, в частности, для борьбы с грибковыми заболеваниями растений, в частности, вызванными патогенными грибками, в частности, семейства комицетов типа Phytophtora sp. например, Phytophtora indestans (милдью картофеля или томатов) Phytophtora citrophtora, Phytophtora capsici. Phytophtora cactorum, Phytophtora palmivora, Phytophtora cinnamoni, Phytophtora megasperma, Phytophtora parasitica, Peronospora sp. (в частности, милдью табака, Plasmopora sp. в частности, Plasmopara vitecola (милдью виноградника) и Plasmopora nalstedei (милдью подсолнечника), Pseudoperonospora sp. (в частности, милдью тыквенных и хмеля), Bremia lactucae (Бремия салата), а также почвенные грибки.
Они применяются преимущественно в дозах от 0,01 до 5 кг/га и, более специфично, в дозах от 0,02 до 1,5 кг/га. На практике они редко применяются одни. Чаще всего они являются частью композиций. Композиции, которые используются для защиты растений от грибковых заболеваний, или в композициях-регуляторах роста растений, они содержат, по крайней мере, одно соединение в соответствии с изобретением, как они описаны раньше, в сочетании с твердыми или жидкими инертными основами, которые применимы в сельском хозяйстве, и/или поверхностно-активными веществами, совместимыми с активным веществом, которые также допустимы в сельском хозяйстве. В частности, применяются обычные инертные основы и обычные поверхностно-активные вещества.
Термином "основа" в настоящем описании обозначают органическое или минеральное вещество, пригодное или синтетическое, с которым сочетается активное вещество, чтобы облегчить его попадание на растение, на зерна или на почву. Обычно эта основа инертная, и она должна быть приемлемой для сельского хозяйства, в частности, для растений. Основа может быть твердой (природные или искусственные глины, силикаты, окись кремния, смолы, воски, твердые удобрения.) или жидкой (вода, спирты, кетоны, нефтяные фракции, ароматические или парафинированные углеводороды, хлорированные углеводороды) или газообразной.
Композиции в соответствии с изобретением (которые предназначаются для продажи в концентрированном виде или же для применения в разбавленном виде) обычно содержат от 0,0001 до 0,95% активного вещества, предпочтительно от 0,0005 до 90% а также от 0 до 20% поверхностно-активного вещества, предпочтительно от 0,5 до 15% Концентрированные композиции, предназначенные для торговли, обычно содержат от 0,1 до 95% активного вещества, предпочтительно от 0,5 до 90%
Поверхностно-активное вещество может быть эмульгатором, диспергатором или смачивающим веществом ионного или неионного типа. В качестве примера можно указать соли полиакриловых кислот, соли лигносульфониевых кислот, соли фенолсульфониевых или нафталенсульфониевых кислот, поликонденсаты этиленоксида с жирными спиртами или с жирными кислотами, или с жирными аминами, замещенные фенолы (в частности, алкилфенолы или арилфенолы), соли эфиров сульфоянтарных кислот, производные торина (в частности, алкилтораты), фосфорные эфиры спиртов или полиоксиэтиловых фенолов. Присутствие, по крайней мере, одного поверхностно-активного вещества является необходимым, когда активное вещество и/или инертная основа нерастворимы в воде и если агентом применения является вода.
Композиции, которые используются в изобретении, могут быть в формах достаточно разнообразных: жидкие или твердые.
В качестве жидких текучих форм композиций можно перечислить эмульгируемые концентраты, эмульсии, концентрированные водные суспензии, пасты, растворы, а частично водорастворимые концентраты, концентрированные растворы в органической среде (растворы ULV-ультранизкого объема) и аэрозоли.
Растворимые или эмульгируемые концентраты чаще всего содержат от 10 до 80% активного вещества, причем эмульсии или растворы, готовые к употреблению, содержат от 0,001 до 20% активного вещества. Кроме активного вещества и растворителя эмульгируемые концентраты могут, в случае необходимости, содержат соответствующий растворитель и от 2 до 20% соответствующих добавок в качестве стабилизаторов, агентов проникновения, ингибиторов коррозии, красителей, адгезирующих веществ. Путем растворения в воде из этих концентратов можно получить эмульсии любой концентрации, которые подходят, в частности, для нанесения на культуры. В качестве примера приводятся составы нескольких эмульгируемых концентратов.
П р и м е р СЕ1. Состав, г/л: активное вещество (соединение 102, 202 или 301) 250; растительное эпоксидированное масло 25; смесь алкиларилсульфоната с простым эфиром полигликоля и жирных спиртов 100; диметилформамид 50; ксилол 575.
П р и м е р СЕ2. Состав, г/л: активное вещество (соединение105, или 206, или 345) 400; додецилбензолсульфонат щелочной 24; оксиэтилированный нонилфенол с 10 молекулами этиленоксида 16; циклогексанон 200 и ароматический растворитель до 1 л.
Из этих концентратов разбавлением водой можно получить эмульсии любой желаемой концентрации, которые особенно подходят для нанесения на листья. Концентрированные суспензии, также применимые для пульверизации, приготовляются так, чтобы получить стабильный текучий продукт, который не расслаивается, и они содержат обычно от 10 до 75% активного вещества, от 0,5 до 15% поверхностно-активного вещества, от 0,1 до 10% тиксотропного вещества, от 0,1 до 10% тиксотропного вещества, от 0,1 до 10% тиксотропного вещества, от 0 до 10% соответствующих добавок, как антивспениватели, ингибиторы коррозии, стабилизаторы, агенты для ненетрации и адгезивы, в качестве основы вода или органическая жидкость, в которой активное вещество малорастворимо или нерастворимо; некоторые твердые органические вещества или минеральные соли могут растворяться в основе, чтобы помогать или препятствовать седиментации или в качестве антигелей для воды.
Приводятся составы нескольких концентрированных водных суспензий в соответствии с изобретением.
П р и м е р SAC1, Состав, г/л: активное вещество (соединения 106, 206 или 350) 100; смачивающий агент (полиэтоксилированный алкилфенол) 10; антигель 100; загуститель (полисахарид) 3; биоцид (формальдегид) 1 и вода до 1 л.
П р и м е р SAC2. Состав, г/л: активное вещество (соединение 108, 208 или 301) 250; смачивающее вещество (полиэтоксилированный С13синтетический спирт) 10; диспергант (лигносульфонат натрия) 15; антигель (мочевина) 50; загуститель (полисахарид) 2,5; биоцид (формальдегид) 1 и вода до 1 л.
П р и м е р SAС3. Приготовляют водную суспензию, которая содержит, г/л: активное вещество (соединение 107, 209 или 345) 500; смачивающий агент (полиэтоксилированный С13 синтетический спирт) 10; диспергатор (этоксилированный полиарилфосфат фенол, солеобразующий) 50; антигель (пропиленгликоль) 100 г/л; загуститель (полисахарид) 1,6; биоцид (4-метилгидроксибензоат натрия) 3,3 и вода до 1 л.
В качестве твердых композиций можно перечислить порошки для распыления (содержание активного вещества может доходить до 100%) и гранулы, в частности гранулы, полученные экструзией, прессованием, пропитыванием гранулированной основы из порошка (содержание вещества формулы (1) в этих гранулах может быть от 0,5 до 80% для последних случаев).
Смачиваемые порошки (или порошки для пульверизации) обычно приготовляются таким образом, что они содержат от 10 до 95% активного вещества, и они обычно содержат, кроме твердой основы, от 0 до 5% смачивающего агента, от 3 до 10% дисперганта и, в случае необходимости, от 0 до 10% одного или нескольких стабилизаторов и/или другие добавки, как вещества для проникновения, адгезивы, или вещества против окомкования, красители и т.д.
В качестве примере приводятся составы нескольких смачиваемых порошков.
П р и м е р РМ1. Состав, активное вещество (соединение 111, 211 или 350) 10; синтетический оксоспирт типа разветвленного с С13этоксилированный 8-10 этиленоксидом (смачивающий агент) 0,75; нейтральный лигносульфонат (диспергатор) 12; карбонат кальция (инертный наполнитель) 100.
П р и м е р РМ2. Состав, активное вещество (соединение 102, 202 или 301) 50; этоксилированный жирный спирт (смачиватель) 2,5; этоксилированный стирилфенол (диспергатор) 5; мел (инертный наполнитель) 42,5.
П р и м е р РМ3. Содержит те же ингредиенты, что и в предыдущем примере, но в следующих пропорциях, активное вещество (соединение 105, 206 или 345) 75; смачивающий агент 1,5; диспергатор 8; карбонат кальция (инертный наполнитель) до 100.
П р и м е р РМ4. Состав, активное вещество (соединение 106, 206 или 350) 90; этоксилированный жирный спирт (смачивающее) 4; этоксилированный стирилфенол (диспергант) 6.
Для получения этих порошков для пульверизации или смачиваемых порошков тщательно перемешивают активное вещество в соответствующих смесителях с добавками и измельчают в мельницах или других измельчителях. Получают порошки для пульверизации, которые хорошо смачиваются и переводятся в суспензию, их можно перевести в суспензию с водой при любой требуемой концентрации, и эта суспензия используется для нанесения на листья растений.
Соединения формулы (I) могут использоваться в виде порошков для распыления можно также использовать состав, который содержит 50 г активного вещества и 950 г талька, можно также применять состав, который содержит 20 г активного вещества, 10 г мелкодисперсной окиси кремния и 970 г талька, эти компоненты перемешивают и измельчают, затем смесь наносят распылением. Гранулы для распыления имеют размеры от 0,1 до 2 мм и могут приготовляться путем агломерации или пропитывания. В общем случае гранулы содержат от 0,5 до 25% стабилизаторов, модифицирующих агентов с медленным выделением, связующих и растворителей.
Приводим два примера состава гранул.
П р и м е р G1 и G2. Состав соответственно, г: активное вещество (соединение 108, 208 или 301) 50 и 200; пропиленгликоль 50 и 50; цетиловый или полигликолевый эфир 2,5 и 2,5; полиэтиленгликоль 35 и 35; каолин (гранулометрия от 0,3 до 0,8 мм) 910 и 760.
Соединения в соответствии с изобретением могут быть в форме гранул, которые диспергируются в воде, и тоже включаются в рамки изобретения. Эти диспергируемые гранулы, кажущейся плотности от 0,3 до 0,6, имеют размеры части, в общем случае от 150 до 2000 мкм, и предпочтительно от 300 до 1500 мкм. Содержание активного вещества в гранулах может быть в общем случае от 1 до 90% и предпочтительно от 25 до 90%
Остаток гранулы состоит в основном из твердого наполнителя и, в случае необходимости, поверхностно-активных добавок, которые придают гранулам свойство диспергируемости в воде. Эти гранулы могут быть в основном двух типов, в зависимости от того, растворим или не растворим наполнитель. В случае водорастворимого наполнителя он может быть минеральным или предпочтительно органическим. Отличные результаты были получены с мочевиной. В случае нерастворимого наполнителя предпочтителен минеральный, например каолин или бентонит. Вместе с наполнителем вводят поверхностно-активные вещества ( и из расчета от 2 до 20% по массе гранулы), не менее половины поверхностно-активных веществ составляют диспергенты, в основном анионные, например поли(нафтален сульфонат, щелочной или щелочно-земельный) или лигносульфонат, щелочной или щелочно-земельный, а остаток состоит из неионных или анионных смачивателей, например алкоил-нафтален сульфонат, щелочной или щелочно-земельный. Хотя это и не необходимо, можно добавлять другие агенты, например антивспениватели.
Гранулы в соответствии с изобретением, могут быть приготовлены путем смешивания необходимых ингредиентов, затем производится грануляция при помощи известной техники (дражирователь, псевдоожиженный слой, экструзия и т. д.). Заканчивается операция измельчением и просеиванием для получения выбранного размера частиц в указанных пределах.
Предпочтительно гранулы в соответствии с изобретением получают экструзией. Проводя операции, как указано в приведенных ниже примерах, получают следующие композиции диспергируемых гранул.
П р и м е р GD1. В смесителе перемешивают 90 мас. активного вещества (соединение 111 или 211) и 10% мочевины в крошках. Затем смесь перемалывается в молотковой дробилке. Получают влажную смесь, которую экструдируют в экструдере с перфорированным роликом. Получают гранулят, который сушат, затем дробят и просеивают так, чтобы остались только гранулы размерами от 150 до 2000 мкм.
П р и м е р GD2. В смесителе перемешивают следующие компоненты, активное вещество (соединение 105, 202 или 345) 75; смачивающее вещество (алкилиафталенсульфонат натрия) 2; диспергатор (полинафталенсульфонат натрия) 8% инертный наполнитель, нерастворимый в воде (каолин) 15.
П р и м е р GD3. Состав, активное вещество (соединение 105, 206 или 350) 20; алкилнафталенсульфонат натрия 2; метиленбионафталенсульфонат натрия 8; каолин 70.
Эту смесь гранулируют в жидком слое, в присутствии воды, затем сушат, измельчают и просеивают, чтобы получить гранулы размером от 0,16 до 0,40 мм. Эти гранулы могут использоваться сами по себе, в виде раствора или дисперсии в воде, чтобы получить требуемую дозу. Они могут использоваться для получения смесей с другими активными веществами, в частности фунгицидами, последние могут быть в виде смачиваемых порошков или гранул, или водных суспензий.
Соединения в соответствии с изобретением могут быть в виде органических растворов в капсулах, в частности, за счет полимеризации на поверхности раздела, в капсулах с полимерными стенками, например, на основе полиамидов полимочевин или полиамидмочевины. Эти капсулы находятся в состоянии концентрированной водной дисперсии, которую можно разбавить, чтобы получить распыляемый туман. Как уже было сказано, водные эмульсии или дисперсии, например, композиции, получаемые разбавлением водой смачиваемого порошка или эмульгируемого концентрата в соответствии с изобретением, включены в общие рамки композиций, используемых изобретении. Эмульсии могут быть типа вода в масле или масло в воде, и они могут иметь густую консистенцию, как "майонез".
Кроме того, изобретение касается способа лечения растений от заболеваний, вызванных фитопатогенными грибками, в частности, семейства сомицетов типа Phytophtora sp. например Phytophtora infestans (милдью картофеля или томатов) Phytophtora cytrophtora, Phytophtora capsici, Phytophtora cactorum, Phytophtora palmivora, Phytophtora cinnamoni, Phytophtora megasporma, Phytophtora parasitica, Peronospora sp. (в частности, милдью табака), Plasmopara sp. Plasmopara viticola (милдью винограда) и Plasmopara halstedei (милдью подсолнечника), Pseudoperonospora sp. (милдью тыквенных и хмеля), Bremia lactucae (Бремия салата), а также почвенными грибками.
Этот способ отличается тем, что он состоит в нанесении на эти растения эффективного количества композиции, которая содержит в качестве активного вещества соединение формулы (I). Под термином "эффективное количество" подразумевают количество, достаточное, чтобы контролировать разрушение грибков, имеющихся на растениях, однако дозы применения могут меняться в широких пределах, в зависимости от грибка, типа культуры, климатических условий и в зависимости от используемого соединения. На практике дозы меняются от 1 г/л до 500 г/л, которые точно соответствуют дозам активного вещества на гектар от 10 до 5000 г/га, такие дозы дают обычно хорошие результаты.
В качестве примера обработки можно перечислить распыление на листья или на почву, смачивание, внесение в почву гранул, порошков или растворов, полив, инжектирование в деревья, обмазывание и обработка посевов. Формулы, на которые ссылаются в тексте описания.
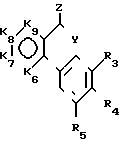 формула Iа
формула Iа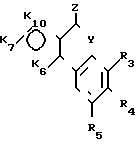 формула Ib
формула Ib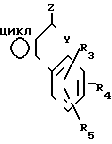 формула I
формула I формула II
формула II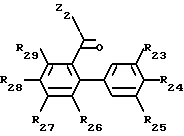 формула III
формула III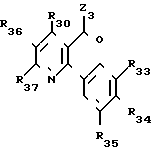 формула IV
формула IV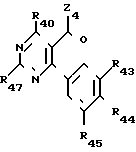 формула V
формула V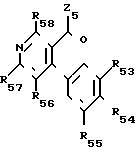 формула VI
формула VI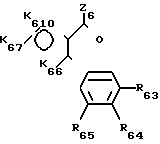 формула VII
формула VII формула II'
формула II'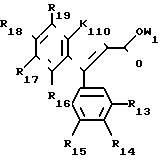 формула II''
формула II''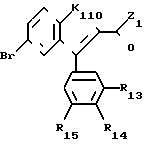 формула II'''
формула II'''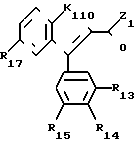 формула II''''
формула II''''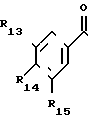
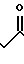 Z1 формула XXXII'
Z1 формула XXXII'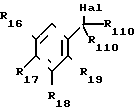 формула XXXII''
формула XXXII'' формула XXXII'''
формула XXXII'''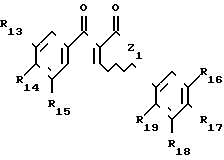 формула XXXXII'
формула XXXXII'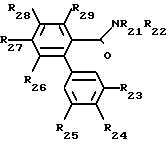 формула III'
формула III' формула III''
формула III'' формула XIII'
формула XIII'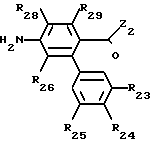 формула XIII''
формула XIII''
H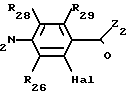 формула XIII'''
формула XIII'''
O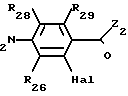 формула XIII''''
формула XIII''''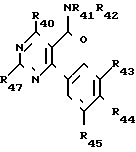 формула V'
формула V'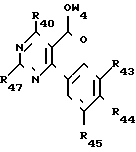 формула V''
формула V'' формула XV''
формула XV''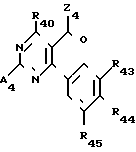 формула XXV'
формула XXV'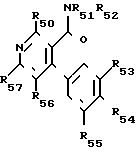 формула VI'
формула VI' формула VI''
формула VI''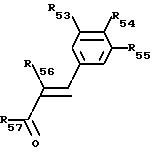 формула XVI'
формула XVI'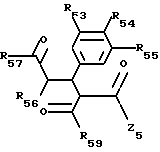 формула XVI''
формула XVI''
R N
N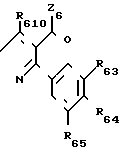 формула VII'
формула VII'
N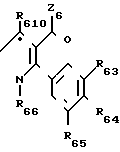 формула VII''
формула VII''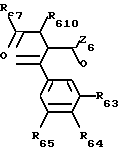 формула XVII'
формула XVII'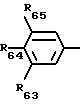 формула XVII''
формула XVII''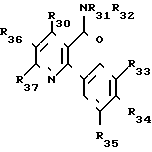 формула IV'
формула IV'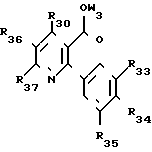 формула IV''
формула IV''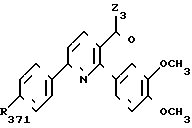 формула IV'''
формула IV'''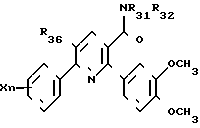 формула IV''''
формула IV''''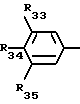 формула XIV'
формула XIV'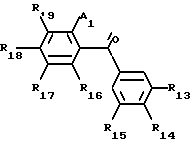 формула XII'
формула XII'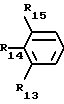 формула XII''
формула XII'' формула XII'''
формула XII'''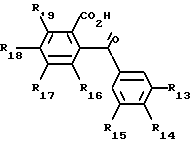 формула XXII'
формула XXII'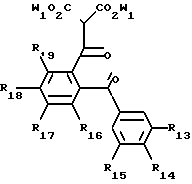 формула XXII''
формула XXII''
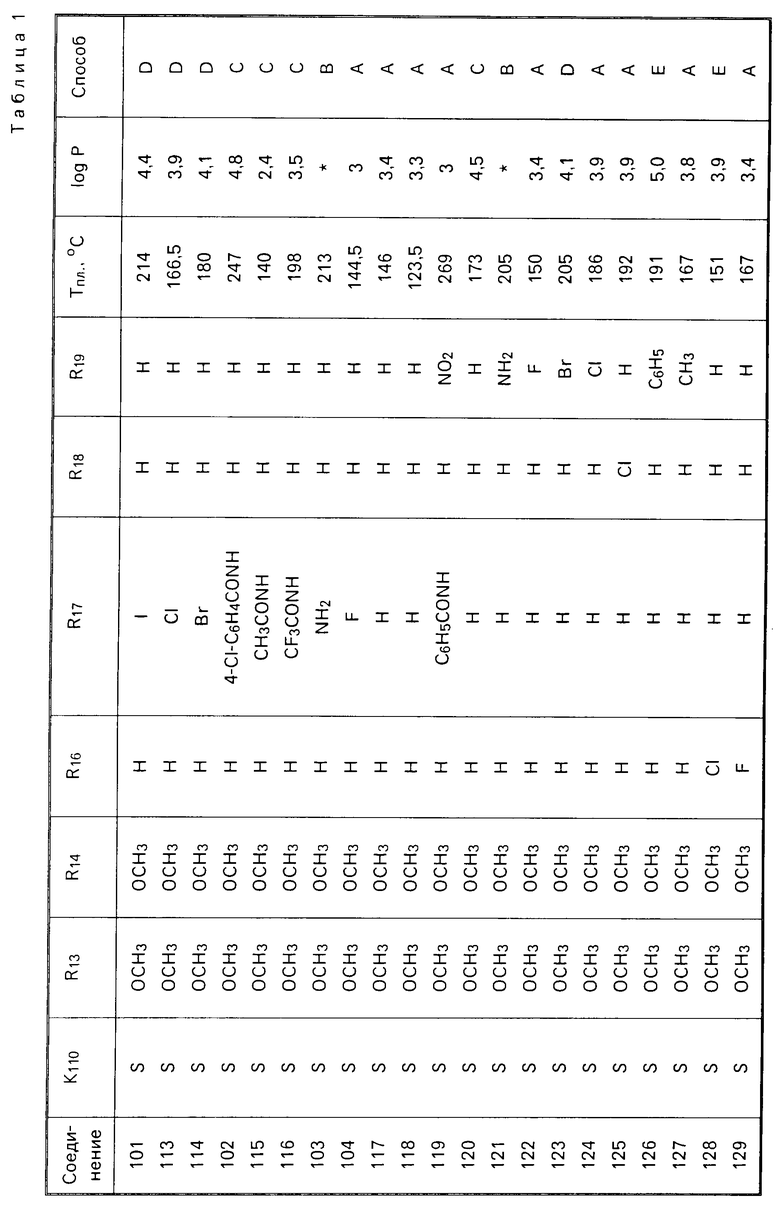
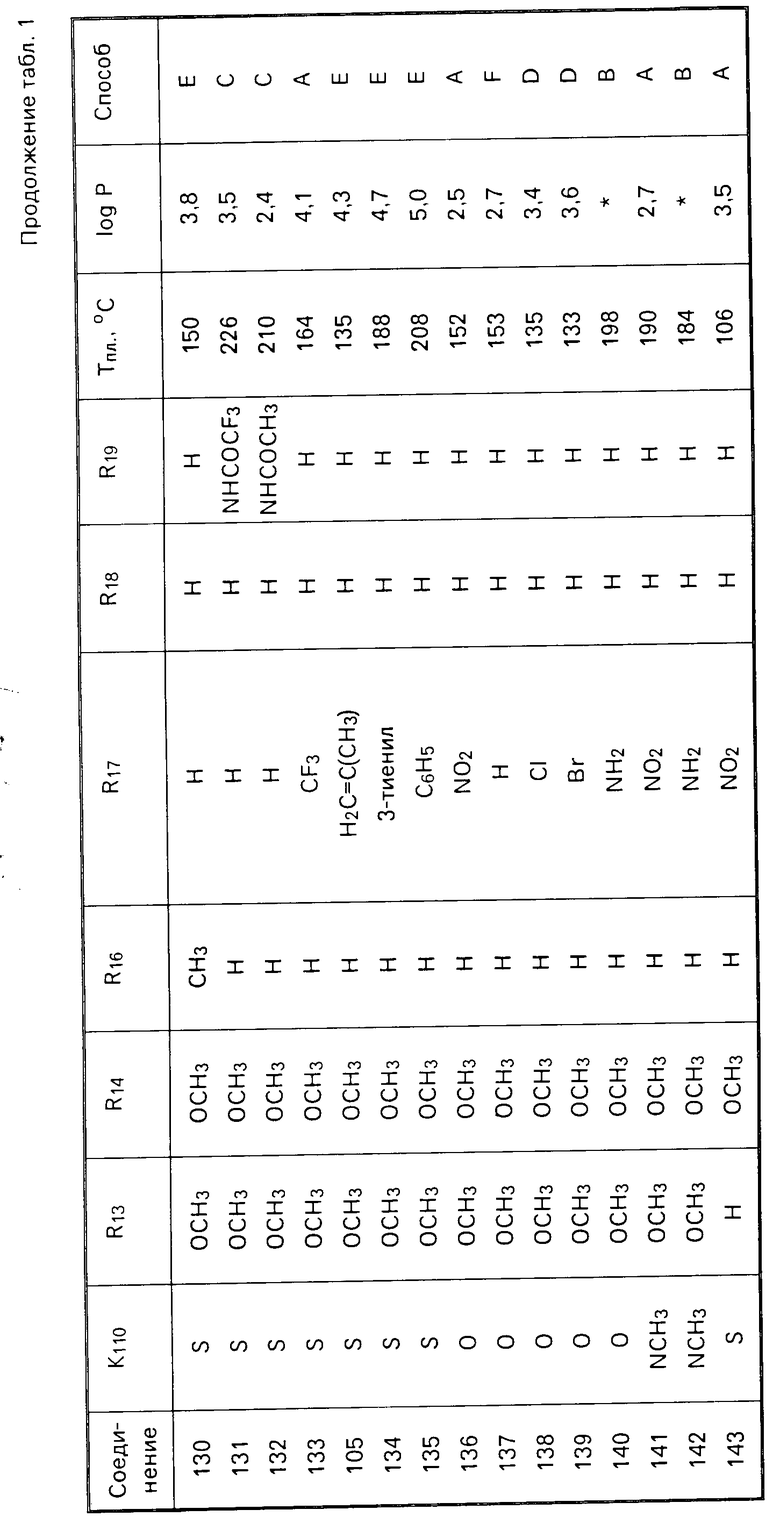
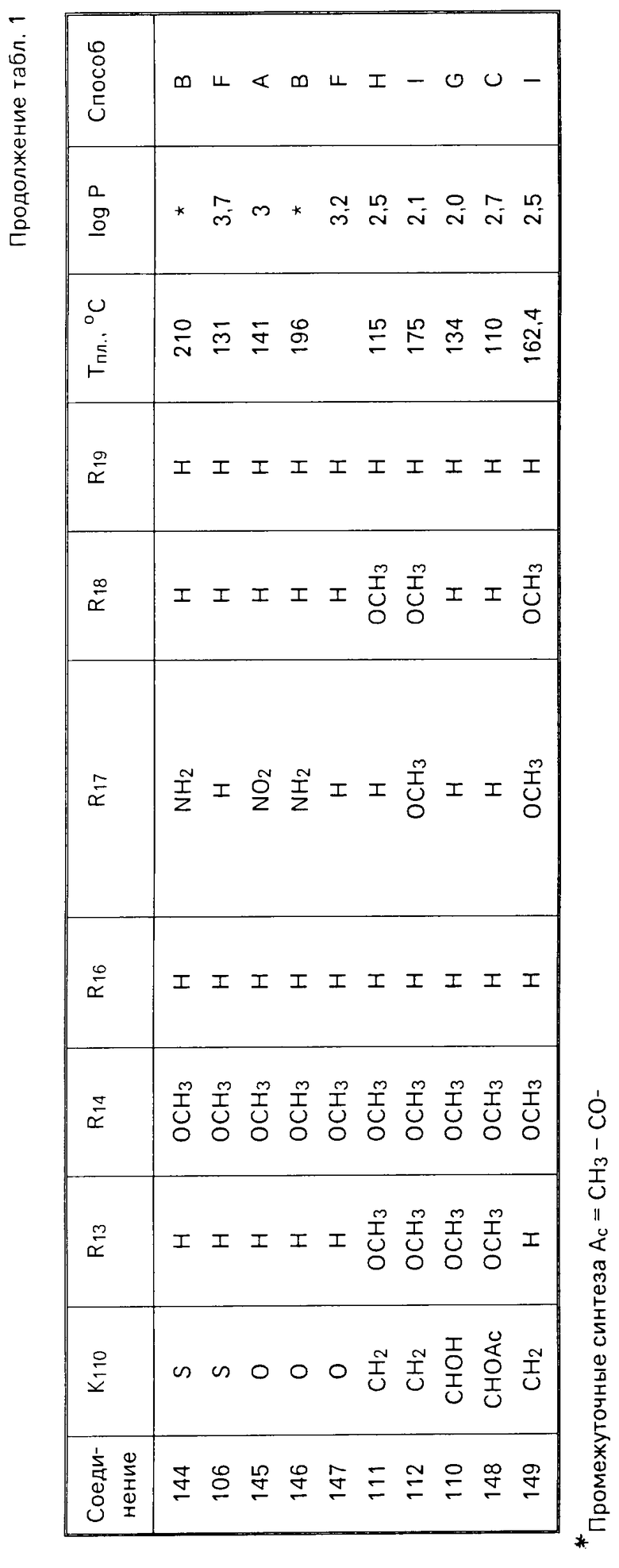

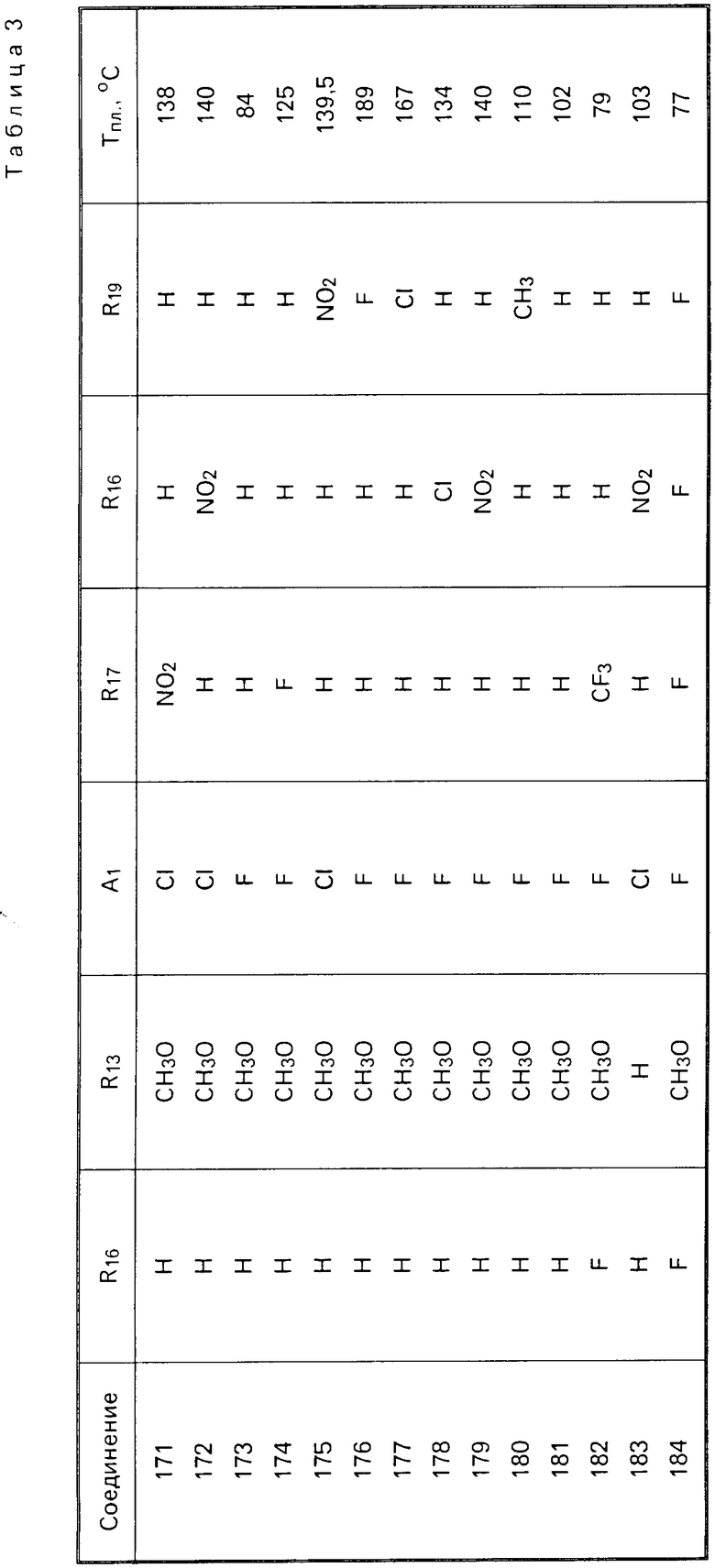
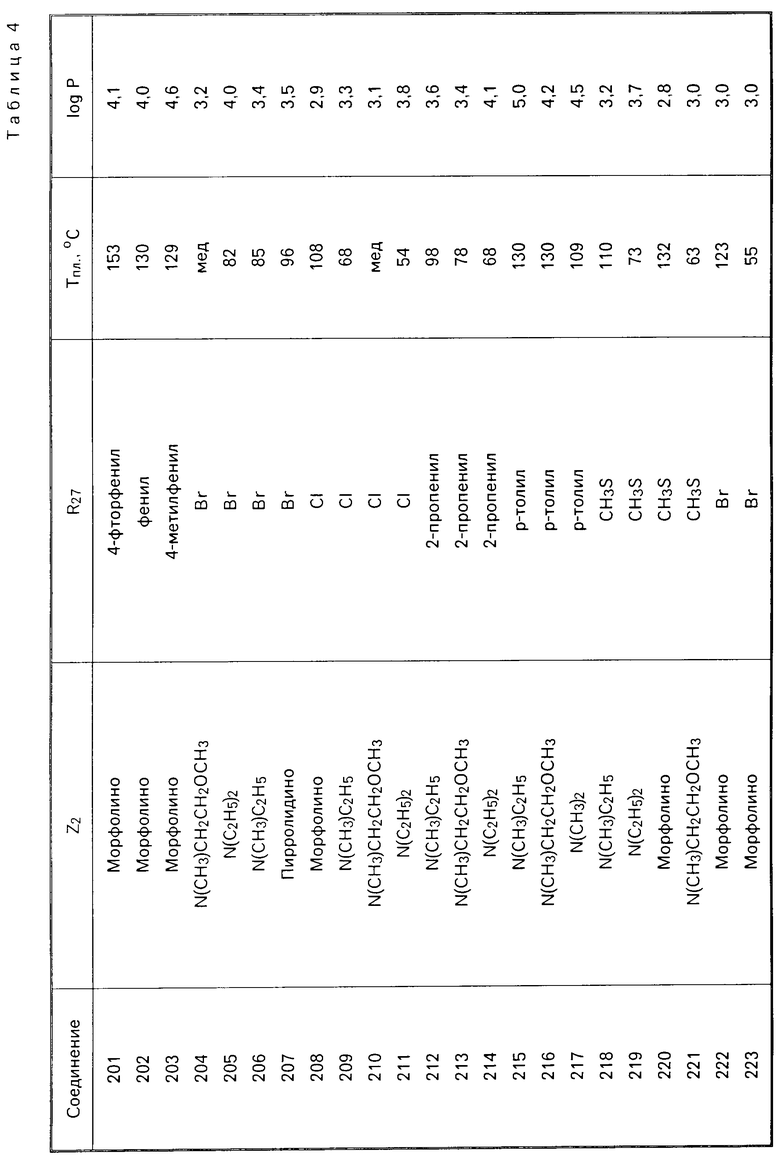
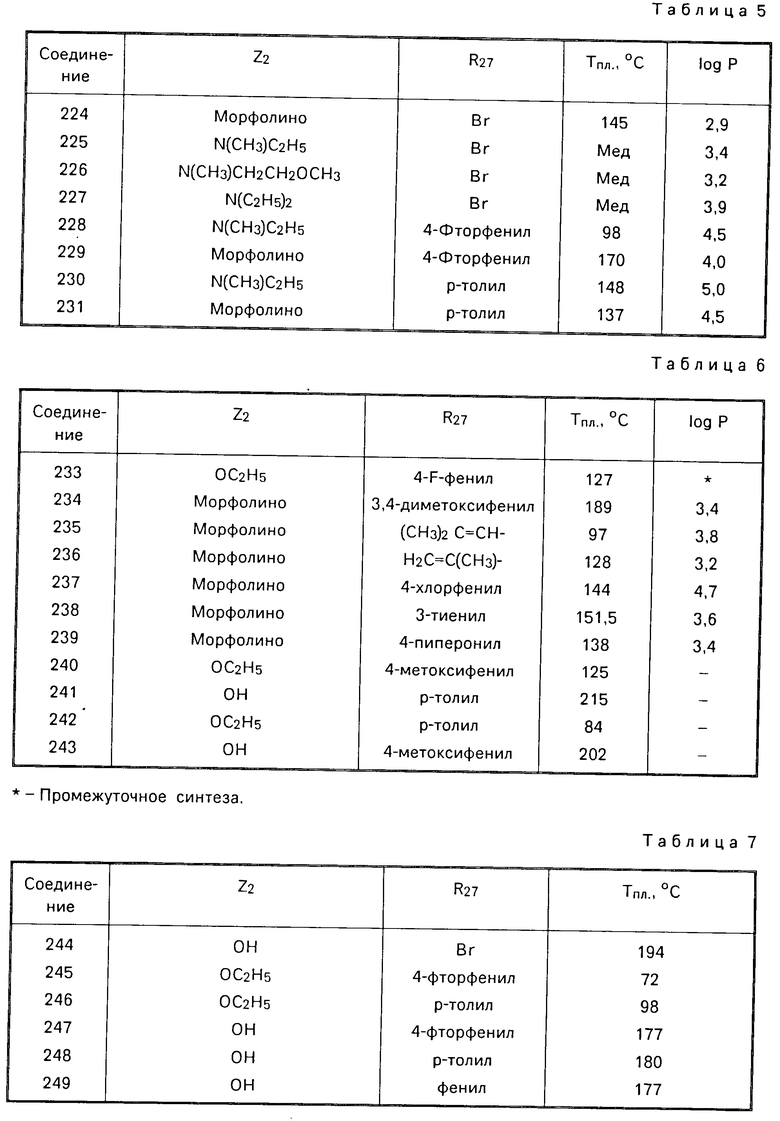
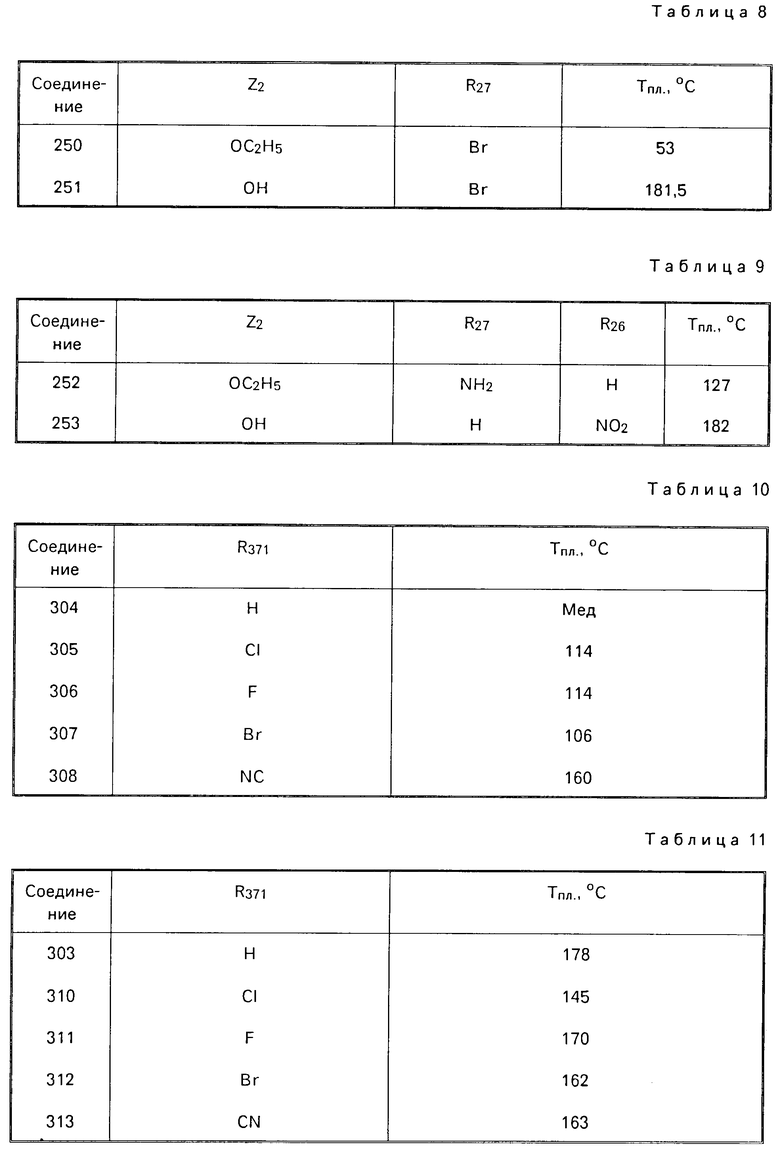
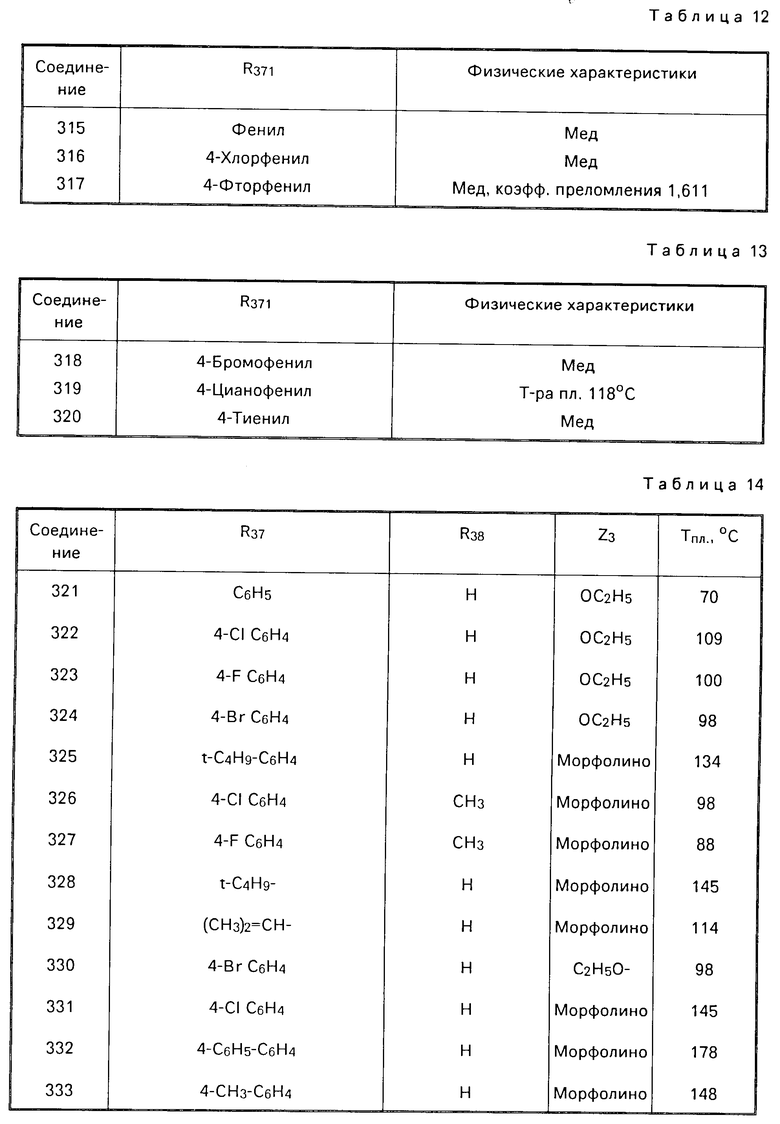
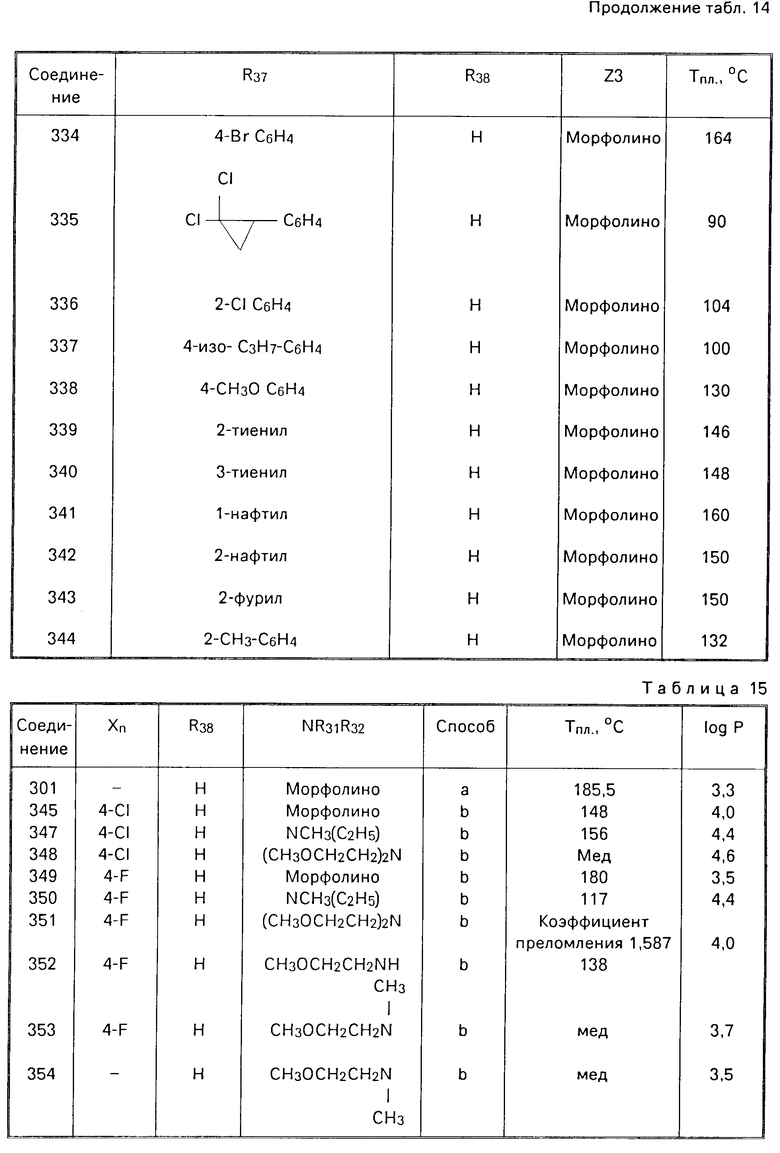
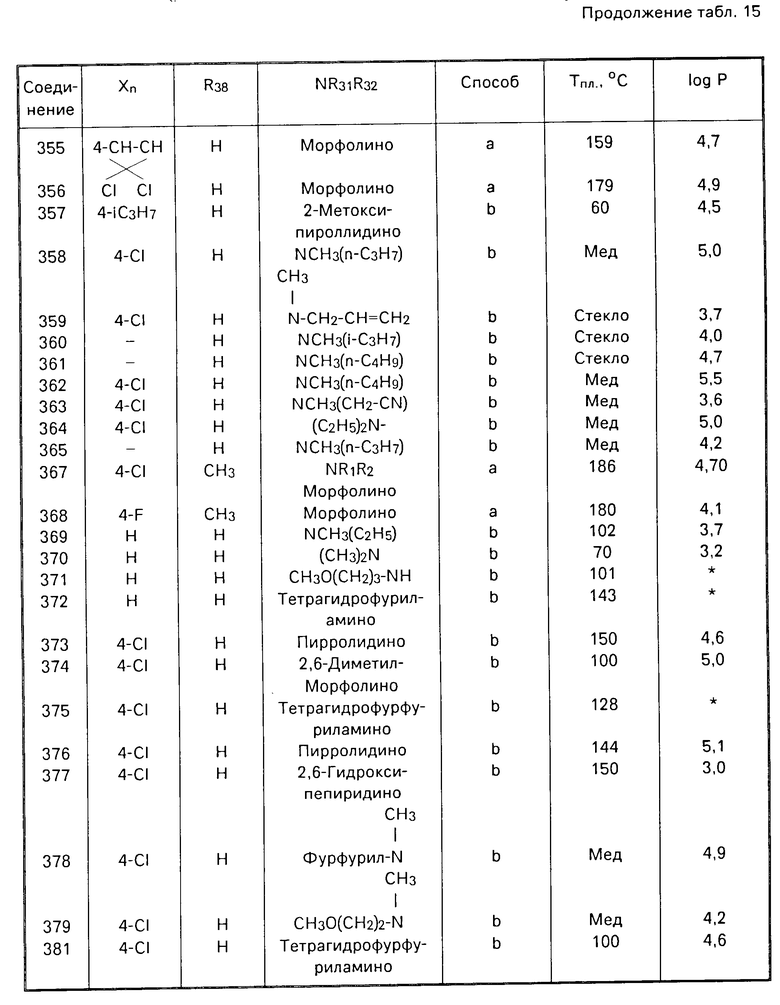
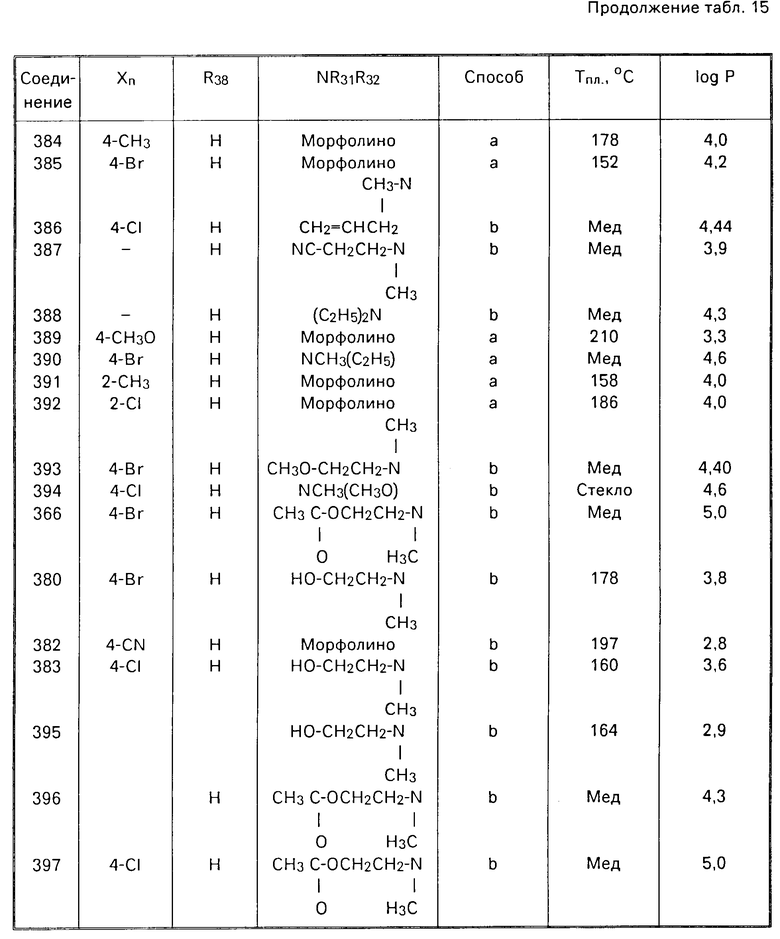
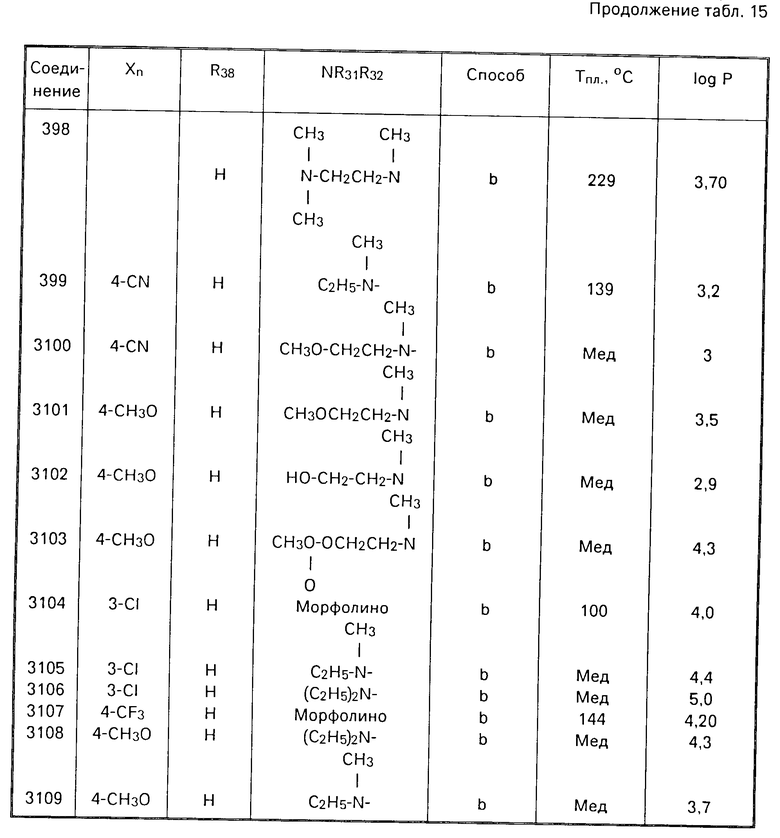
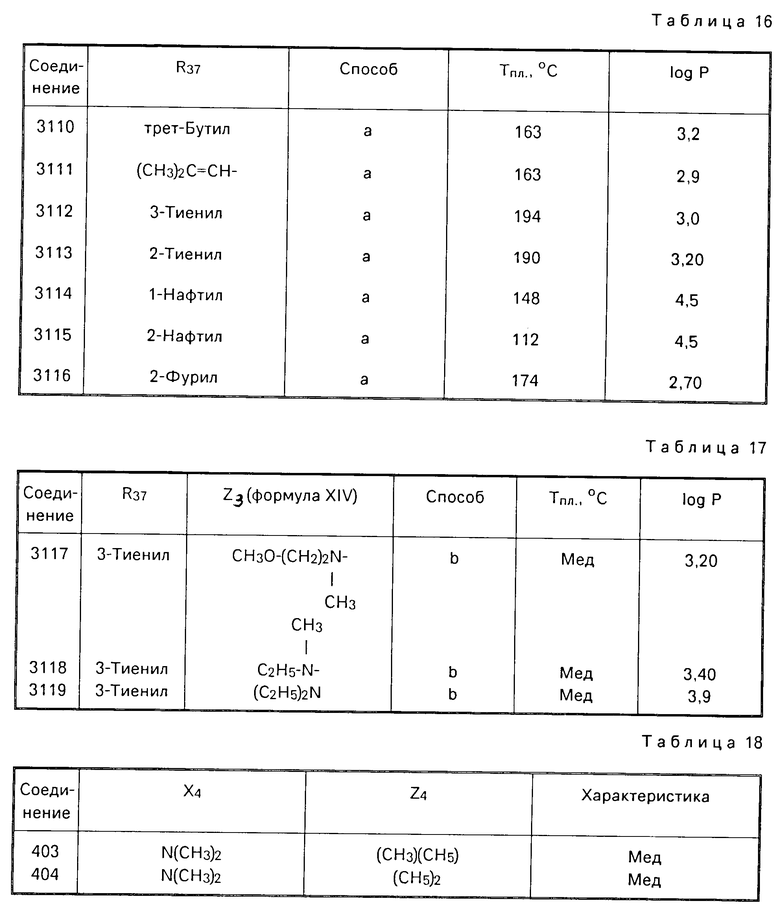

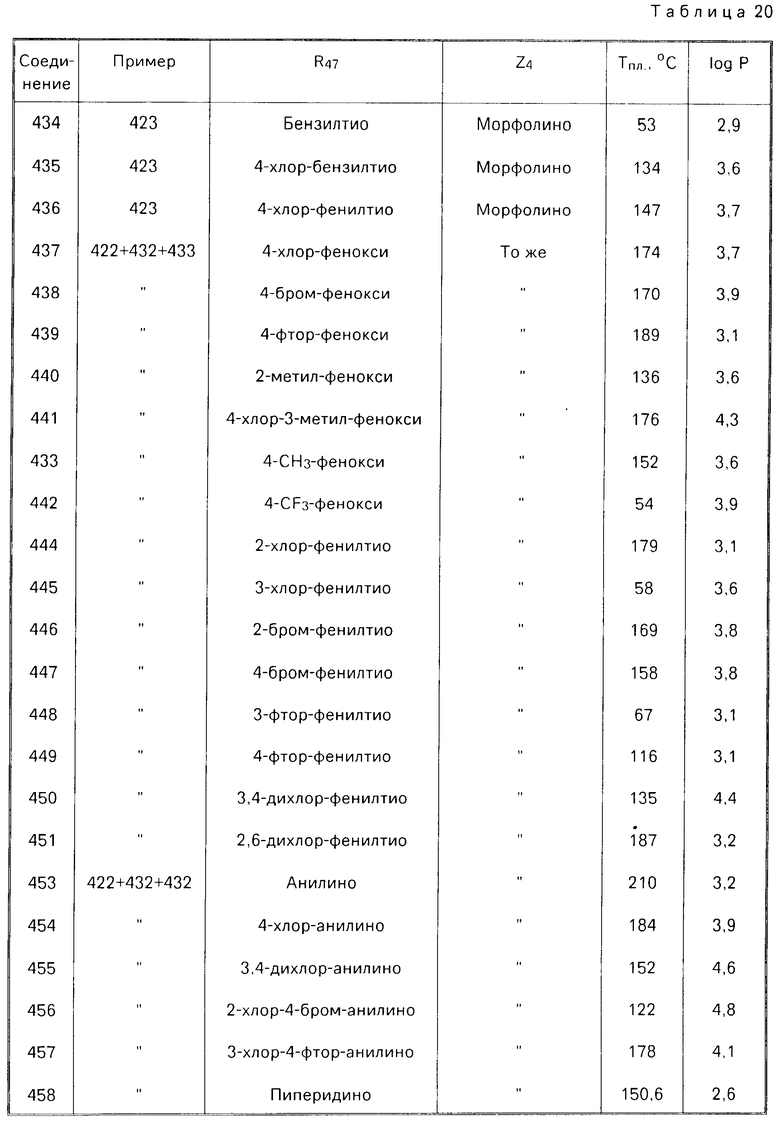
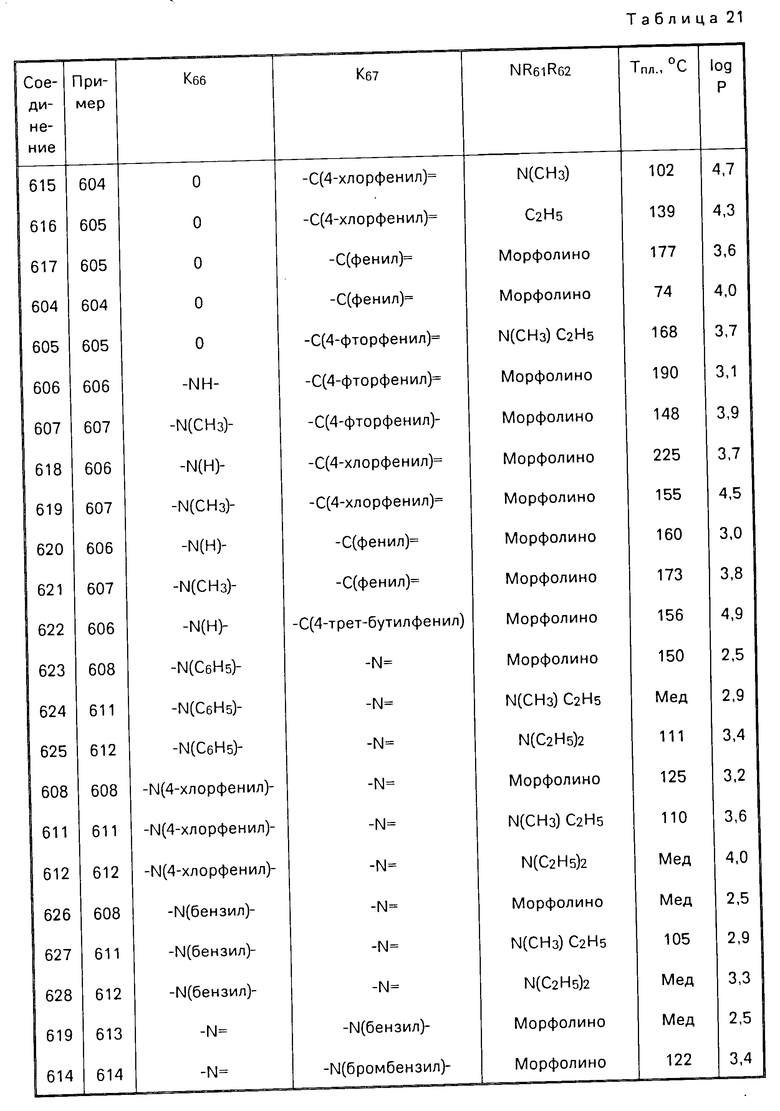
Использование: сельское хозяйство, для обработки пораженных грибками растений. Сущность изобретения: фенил- и амидосодержащие соединения ф-лы I при определенных значениях радикалов (см.рис.) 3 с. и 16 з.п. ф-лы, 21 табл.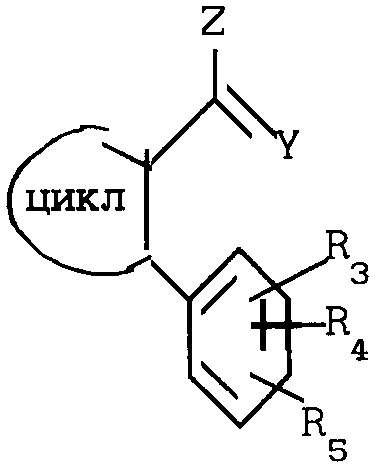

в которой знак цикл, окруженный полукругом, обозначает вместе с двумя атомами углерода, к которым этот полукруг присоединен, углеродный или гетероциклический цикл, имеющий от 4 до 7 звеньев, имеющий по крайней мере одну ненасыщенную связь этиленового или ароматического типа между двумя атомами углерода, носителями группы
и фенильной группой, указанный цикл, в случае необходимости, замещен органическими радикалами, которые имеют не более 30 атомов углерода;
Y атом кислорода или серы;
Z группа NR1R2;
R1 и R2, идентичные или различные, представляют низший алкильный или низший алкокси радикал (по крайней мере один из радикалов R1 и R2 иной, чем алкокси), или циклоалкильный радикал, имеющий от 3 до 7 атомов углерода, эти радикалы, в случае необходимости, замещены по крайней мере одним атомом галогена и/или группой гидрокси или низший алкокси, или алкокси (низший)-алкил (низший), или ацилокси (низший), или фенильной, или гетероциклической группой, из 4 6 звеньев цепи, включающей 1 или 2 гетероатома (0, N или S), или группой амино-, моно- или дизамещенной низшими алкилами, радикал алкенильный или алкинильный, имеющий от 3 до 7 атомов углерода, или R1 и R2 образуют вместе в атомом азота, к которому они присоединены, гетероцикл, насыщенный или ненасыщенный, имеющий от 4 до 7 звеньев (предпочтительно 5 или 6) и 1,2 или 3 гетероатома (0, N или S), причем этот гетероцикл может быть замещен группами низший алкил, или низший алкокси или гидрокси, или радикалом оксо-, или одним или несколькими атомами галогена, или группой алкил(низший)-алкокси(низший), R3, R4 и R5, идентичные или различные, водород или галоген, причем по крайней мере один из этих радикалов R3, R4, R5 иной, чем атом водорода или галогена, группа амино, в случае необходимости, замещенная одной или двумя группами низших алкилов, группа низший алкил или низший алкокси, или алкил (низший)-алкокси(низший), или низший алкилтио, в случае необходимости, гидроксил-или галогенсодержащий;
R3 и R4 (в положении мета и пара) могут вместе образовывать один двухвалентный радикал с 3 или 4 звеньями, включающими 1 или 2 невицинальных атома кислорода для обработки пораженных грибками растений.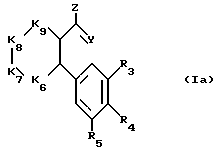
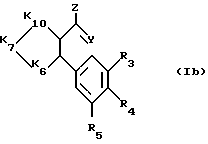
где R1 и R2 низший алкильный радикал, циклоалкильный радикал, имеющий от 3 до 7 атомов углерода, радикал алкенильный или алкинильный, имеющий от 3 до 7 атомов углерода, причем алкоксиалкильный радикал имеет от 3 до 8 атомов углерода, или R1 и R2 могут образовывать вместе с атомом азота, к которому они присоединены, насыщенный или ненасыщенный гетероцикл, имеющий от 4 до 7 звеньев и 1 или 2 гетероатома (0, N, S), причем этот гетероцикл может быть замещен алкильными радикалами с 1 3 атомами углерода или алкоксиалкильными группами с 2 4 атомами углерода;
R3, R4, R5 находится в положении соответственно мета, пара и мета на фенильной группе, замещающей цикл (эти положения обозначаются по отношению к валентной связи, соединяющей указанную фенильную группу с указанным циклом), и R3, R4, R5 представляют атом водорода или галогена (по крайней мере один их этих радикалов иной, чем атом водорода или галогена), или радикал низший алкильный или низший алкокси, или алкоксиалкильный, имеющий от 2 до 4 атомов углерода, или низший алкилтио, или гидрокси, или группа амино, в случае необходимости монозамещенная или дизамещенная низшим алкильным радикалом, или R3 и R4 (в положении мета и пара) могут образовывать вместе один двухвалентный радикал с 3 или 4 звеньями, включающими 1 или 2 невицинальных атомов кислорода;
знак цикл, окруженный полукругом, представляет двухвалентный радикал - K6 K7 K8 H9 или -K6 K7 - K10- так, чтобы образовывать с двумя атомами углерода, к которым они присоединены, цикл с 5 или 6 звеньями (как представлено графически в формулах (1а) и (1b)), причем группы K6, K7, K8, K9, K10 такие, что
K6 представляет -N= или -C(R6)-;
K7 -N= или -C(R7)-;
K8 -N= или -C(R8)-;
K9 -N= или -C(R9)-;
K10 -N= или -C(R10)-.
Кроме того, в случае, если знак цикл, окруженный полукругом, представляет собой K6, K7, K10, эти радикалы K6 K7 K10 могут быть такими, что:
K6 представляет -N(R5)- или -C(R6)2- или -О- или -S(O)n;
K7 представляет -N(R7)- или -C(R7)2- или -О- или -S(O)n;
K10 представляет -N(R10)- или -C(R10)2- или -О- или -S(О)n или -CO-,
где n целое число 0, 1 или 2,
предполагается, что в обоих случаях, когда знак цикл представляет собой -K6 K7 K8 K9 и -K6 K7 - K10-, по крайней мере одна из групп K6 и K7 представляет -C(R6)= или -C(R6)2-, или -C(R7)= или -C(R7)2 и что, кроме того, эти двухвалентные радикалы K6 - K7 K8 K9 и -K6 K7 K10 - содержат в своей основной цепи 0, 1 или 2 гетероатома (N, O, S) и не содержат никакого из рядов -О-О- или -S-S-, -R6, R7, R8, R9, R10 каждый, идентичный или отличающийся от других, представляют
атом водорода или галогена, причем по крайней мере один из радикалов R6 или R7 иной, чем атом водорода;
группа циано, нитро, тиоцианато, гидрокси или карбокси, алкил, циклоалкил, алкенил, алкинил, алкил- S(O)n (где n 0, 1 или 2), алкокси, циклоалкокси с 3 8 атомами углерода, алкенилокси, алкинилокси, эти радикалы имеют предпочтительно от 1 до 8 атомов углерода и могут быть, в случае необходимости, замещены одним или несколькими атомами галогена;
радикал фенильный, нафтильный, фенил S(O)n (где n 0, 1 или 2), фенокси, фенилалкильный (низший алкил), фенилалкил -S(O)n (низший алкил), (n 0, 1 или 2), фенилалкокси (низший алкокси) или же остаток гетероцикла, в случае необходимости, замещенного, насыщенного или ненасыщенного, имеющего в цикле 5 или 6 звеньев с 1 3 гетероатомами из группы, включающей кислород, серу, азот, причем фенильное или гетероциклическое ядро каждого из этих радикалов может быть замещено по крайней мере одним заместителем из группы: галогена, группа нитро, циано, карбокси, гидрокси, меркапто, тиоцианато, алкокси (низший) карбонил, -CO-NR′-R″, NR′-R″ , -N(R′)-CO-R″, -O-CO-R′, -O-CO-NR′-R″ или радикал низший алкильный, низший алкокси, алкил(низший) -S(O)n (где n 0, 1 или 2), циклоалкильный (с 3 7 атомами углерода), фенильный, фенокси, фенил- S(O)n (где n 0, 1 или 2), фенилалкильный фенилалкокси, фенилалкил- S(O)n (где n 0, 1 или 2), эти радикалы могут содержать галоген и имеют от 1 до 4 атомов углерода в алкильной части, группа алкокси (низший)/карбонил, CO-NR′R″, NR′R″, N(R′)-CO-R″ , O-CO-R′, O-CO-NR′R″, R′ и R″, идентичные или различающиеся, каждый представляет атом водорода, радикал низший алкильный, циклоалкил с 3 7 атомами углерода фенил, возможно содержащий галоген, фенилалкил (низший алкил, возможно содержащий галоген, алкенил или алкинил с 3 7 атомами углерода, алкоксиалкил с 3 8 атомами углерода;
когда K6 и K7 представляет -C(R6)= или -C(R6)2, или -C(R7)= или -C(R7)2-, тогда R6 вместе с R7 или один из радикалов R6 вместе с одним из радикалов R7 могут образовывать с двумя атомами углерода, несущими R6- и R7-углеродный или гетероциклический цикл, насыщенный или ненасыщенный, который содержит 5 или 6 звеньев и 0, 1 или 2 невицинальных гетероатома (О, N или S):
когда K6, или K7, или K8, K9 или K10 имеют одно из значений -N(R6)-, -N(R7)-, -N(R8)-, -N(R9)-, -N(R10)-, тогда соответствующий радикал R6, R7, R8, R9, R10 имеет одно из следующих значений (если только по крайней мере один из радикалов R6 или R7 иной, чем атом водорода): атом водорода, алкильный радикал с 1 6 атомами углерода, радикал фенильный или фенилалкильный (низший алкил), возможно замещенный одним или несколькими атомами галогена или группой циано или нитро, или радикалом и низшим алкильным или низшим алкокси.
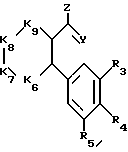

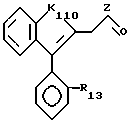
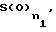 где n1 целое число, равное нулю, 1 или 2, или группа NR110 или -CR110)2, или группа оксо;
где n1 целое число, равное нулю, 1 или 2, или группа NR110 или -CR110)2, или группа оксо;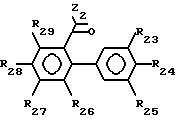
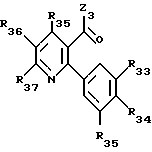
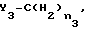 в которой Y3 атом кислорода или серы, или группа метилен,
в которой Y3 атом кислорода или серы, или группа метилен,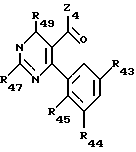

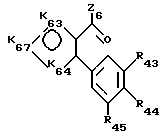
| Способ лечения верхней микрогнатии | 1976 |
|
SU609535A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
1995-08-20—Публикация
1989-08-31—Подача