Изобретение относится к новым окисленным производным глутатиона, в частности к окисленным глутатионалкиловым эфирам и к способу их получения.
Известно, что глутатионалкиловые эфиры (восстановленные) превосходят глутатион в отношении способности перемещаться в живых организмах, например в отношении попадания их в печень и почки, и что после такого переноса они подвергаются гидролизу с образованием глутатиона.
Авторы изобретения провели работу по поиску производных глутатиона, которые удовлетворительно абсорбировались бы тканями, а также обладали бы достаточной стабильностью. В результате этой работы ими было установлено, что путем окисления моноалкиловых эфиров глутатиона, осуществляемого простым способом, а именно с помощью воздуха, перекиси водорода или иода, могут быть получены окисленные глутатионалкиловые эфиры, обладающие высокой стабильностью и высокой фармацевтической активностью. Эти исследования далее были сконцентрированы и в конечном счете привели к созданию изобретения.
Изобретение, таким образом, относится к окисленным глутатионалкиловым эфирам формулы I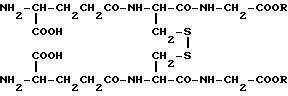
(I) в которой R означает низший алкил, к способу их получения.
В изобретении низший алкил предпочтительно означает алкил с 1-10 атомами углерода. Это может быть любой прямой, разветвленный или циклический алкил, выбранный из указанной предпочтительной группы, а также алкил, представляющий собой комбинацию указанных алкилов.
Примерами предпочтительных низших алкилов являются метил, этил, н-пропил, изопропил, циклопропил, н-бутил, втор-бутил, трет-бутил, н-пентил, 1-этилпропил, изопентил, бензил и т.п.
Способ получения заявляемых соединений заключается в следующем.
Вначале глутатион в спиртовой среде и в присутствии кислоты переводят в кислую соль моноэфира глутатиона формулы II
NH2-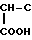 H2CH2CO-NH-
H2CH2CO-NH-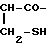 NH-CH2-COOR
NH-CH2-COOR
(II) Эту соль нейтрализуют затем щелочью и в полученный нейтральный водный раствор для окисления моноэфира глутатиона вводят воздух или добавляют к нему при интенсивном перемешивании по каплям перекись водорода или спиртовой раствор иода. Указанной кислой солью моноэфира глутатиона может быть, например, гидрохлорид, сульфат или п-толуолсульфонат, хотя изобретение и не ограничивается только этими солями. Указанные реакции легко могут быть осуществлены простыми способами и полученный в результате реакционный раствор может быть подвергнут хроматографии для очистки или перекристаллизации для получения целевого соединения.
Соединения в соответствии с изобретением способны подавлять повышение уровня аспартат-аминотрансферазы, аламин-аминотрансферазы и т.д. Они эффективно предотвращают начало острых и хронических заболеваний печени. Благодаря этому они могут использоваться для профилактики и лечения острых и хронических гепатитов. Кроме того, они в успехом могут использоваться и для лечения других заболеваний печени, вызываемых лекарствами, например, ацетаминофеном. И, наконец, весьма вероятно, что их можно использовать для предотвращения прогресса и лечения катаракты.
Соединения в соответствии с изобретением могут вводиться в организм как орально, так и парентерально. Фармацевтические композиции на их основе могут быть приготовлены, например, в виде таблеток, гранул, порошков или капсул, жидких препаратов, например глазных капель, или в любой другой форме известными способами, в зависимости от природы заболевания и подлежащего лечению органа. Такие препараты могут содержать обычно используемые в таких случаях компоненты, такие как связующие, диспергаторы, загустители, дезинтеграторы, агенты, способствующие резоpбции, вкусовые добавки, буферирующие агенты, поверхностно-активные вещества, солюбилизаторы, консерванты, эмульгаторы, изотонирующие добавки и добавки для установления нужного рН. Доза активного компонента обычно может находиться в пределах, например, примерно 1-1000 мг/день для взрослых для инъекций и примерно 10-2000 мг/дозу (при приеме несколько раз в день) для взрослых в случае орального приема, хотя она может и меняться в зависимости от природы и тяжести заболевания, возраста и веса пациента, формы препарата и т.п.
Фармацевтические композиции для лечения заболеваний печени, содержащие в качестве активного компонента соединение в соответствии с изобретением, могут содержать одно, два или более заявляемых соединений в соответствующей комбинации. Кроме того, они могут содержать и другие компоненты, обладающие такой же или отличной терапевтической активностью, причем выбор этих компонентов обусловлен тем, чтобы они не подавляли активности заявляемых соединений.
П р и м е р 1. Дисульфид σ L-глутамил-L-цистеинилглицинизопропилового эфира (окисленный глутаионизопропиловый эфир).
Способ А.
10 г. сульфата σ-L-глутамил-L-цистеинилглицинизопропилового эфира (сульфат GSH-изопропилового эфира) суспендируют в 200 мл воды. Полученную суспензию нейтрализуют путем постепенного добавления к ней 3,0 г карбоната кальция. В результате GSH-изопропиловый эфир выделяется в свободном виде и растворяется, а сульфат кальция выпадает в осадок. Смесь затем фильтруют и к фильтрату при охлаждении добавляют по каплям 14 мл 5%-ной перекиси водорода. После перемешивания в течение 3 ч, реакционную смесь концентрируют в вакууме при температуре не выше 40оС. К концентрату добавляют ацетонитрил и выпадающие кристаллы отфильтровывают, получая в результате 6 г сырых кристаллов.
Эти сырые кристаллы подвергают очистке с помощью колоночной хроматографии (колонка: УМС ODS 120A S-50; элюент: смесь ацетонитрила и воды в соотношении 1: 4) и растворитель отгоняют в вакууме. Остаток кристаллизуют из ацетонитрила и затем перекристаллизовывают из водно-ацетонитрильной смеси, получая в результате 2,5 г бесцветной аморфной кристаллической массы.
Тонкослойная хроматография (силикагель): Rf 0,26 (н-бутанол/уксусная кислота/вода 4/1/1). [α]D20 -82,7о (с 1, Н2О).
Результаты элементного анализа из расчета на формулу С26Н44О12N6S2. 2H2O
Рассчитано, C 42,61; H 6,60; N 11,47.
Найдено, C 42,84; H 6,50; N 11,52
Cпособ В.
Раствор GSH-изопропилового эфира получают таким же образом, как и в случае способа А, используя в качестве исходного материала 10 г сульфата GSH-изопропилового эфира. К этому раствору добавляют по каплям двухпроцентный раствор иода в метаноле при комнатной температуре, до тех пор, пока цвет раствора не становится светло-желтым. Смесь перемешивают в течение еще 2 ч при 40оС и затем нейтрализуют карбонатом кальция. Выпадающие в осадок неорганические кристаллы отфильтровывают и фильтрат концентрируют в вакууме. К концентрату добавляют ацетонитрил и выпадающие кристаллы отфильтровывают, получая в результате 5 г сырого продукта. Сырые кристаллы подвергают очистке с помощью колоночной хроматографии таким же образом, как и в случае способа А, получая в результате 1,9 г очищенного продукта.
Способ С.
Раствор GSH-изопропилового эфира получают таким же образом, как и в случае способа А, используя в качестве исходного материала 10 г сульфата GSН-изопропилового эфира. Через полученный раствор при комнатной температуре и интенсивном перемешивании в течение 24 ч пропускают воздух. Смесь затем обрабатывают таким же образом, как и в случае способа А, получая в результате 2,3 г очищенного продукта.
П р и м е р 2. Дисульфид σ-L-глутамил-L-цистеинилглицинэтилового эфира (окисленный глутатионэтиловый эфир).
Процесс проводят таким же образом, как и в случае способа А в примере 1, используя в качестве исходных материалов 10 г гидрохлорида σ -L-глутамил-L-цистеинилглицинэтилового эфира и 3,0 г карбоната кальция. Окисление осуществляют с помощью 5%-ной перекиси водорода. Для очистки используют аналогичные колонку (УМС DDS 120А S-50) и элюент (ацетонитрил/вода 7/43). Полученные кристаллы перекристаллизовывают из водно-ацетонитрильной смеси, получая в результате 1,5 г бесцветной аморфной кристаллической массы.
Тонкослойная хроматография (силикагель): Rf 0,16 (н-бутанол/уксусная кислота/вода 4/1/1); [ α]D20 -89,7о (с 1, Н2О).
Результаты элементного анализа из расчета на формулу С24Н40О12N6S2. 2H2O
Рассчитано, C 40,90; H 6,29; N 11,92
Найдено, С 40,62; Н 6,41; N 11,61
Фармакологические испытания.
Методика.
Самцов крыс породы Wistar массой примерно 180 г не кормили в течение 24 ч, после чего вводили им орально через канюлю соответственно 87-349 мг окисленного глутатионизопропилового эфира (в дальнейшем называемого также "GSSG-изопропил"), представляющего собой одно из соединений в соответствии с изобретением, 102 мг восстановленного глутатионизопропилового эфира х 1/2 Н2SO4 x 1/2 H2O (87 мг восстановленного глутатионизопропилового эфира, называемого далее также "GSH-изопропил") или 5%-ный раствор гумиарабика (для сравнения). Через час животным вводили внутрибрюшинно 400 мг/кг ацетаминофена, соединения, вызывающего заболевания печени. Еще через 24 ч крыс анестезировали пентобарбиталом, собирали кровь из брюшной аорты и определяли содержание в ней S-аспартатаминотрансферазы и S-аламинаминотрансферазы для сравнения подавляющего действия на заболевание печени GSSG-изопропила и GSH- изопропила.
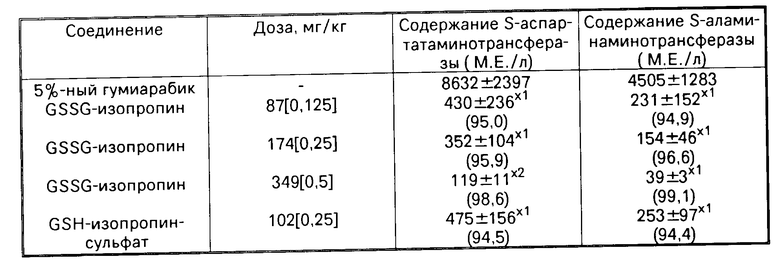
В результате было показано (см.таблицу), что увеличение содержания в крови S-аспартатаминотрансферазы и S-аламинаминотрансферазы существенно подавляется (в зависимости от величины дозы) при введении животным 87-349 мг/кг GSSG-изопропила. Показано также, что введение 102 мг/кг GSH-изопропилсульфата существенно тормозит увеличение содержания в крови S-аспартатаминотрансферазы и S-аламинаминотрансферазы и что введение 87 мг/кг GSSG-изопропила в этом плане практически эквивалентно 102 мг/кг GSH-изопропилсульфата.
Влияние GSSG-изопропила и GSH-изопропила на вызываемое ацетаминофеном заболевание печени у крыс показано в таблице.
В приведенной таблице все приведенные значения представляют собой средние значения ± стандартное отклонение (n 4-8). Цифры в квадратных скобках представляют собой молярную дозу (ммоль/кг) испытуемых соединений. Цифры в круглых скобках представляют собой процент торможения. Существенное различие по сравнению с 5%-ным раствором гумиарабика: x1: p < 0,05; x2: p < 0,01.
Примеры композиции
П р и м е р 1. Таблетки для орального введения, мг:
Окисленный глутатионизо- пропиловый эфир 100 Лактоза 80 Крахмал 17 Стеарат магния 3
Из указанных компонентов получают таблетки обычным способом. Такие таблетки могут также содержать сахар.
П р и м е р 2. Препарат для
инъекций, г:
Окисленный глутатионизо- пропиловый эфир 1,0 Хлорид натрия 0,7
Дистиллированная вода для инъекций 100 мл.
Перечисленные компоненты смешивают и стерилизуют путем фильтрации. По 2 мл фильтрата заливают в асептических условиях в стеклянные пузырьки, которые затем герметизируют термическим способом, получая в результате препарат для инъекций.
П р и м е р 3. Глазные капли, г: Окисленный глутатионизо- пропиловый эфир 1,0 Борная кислота 0,7 Метил-п-оксибензоат 0,02 Хлорбутанол 0,3
10%-ный водный раствор В нужном
гидроксида натрия количестве
до рН 6,0
Стерильная очищенная
вода До 100 мл
Перечисленные компоненты перемешивают до образования раствора обычным образом. Полученный раствор стерилизуют путем фильтрации и разливают в стерильные пузырьки.
Использование: в медицине как вещества, обладающие гепатопротекторной активностью. Сущность изобретения: дисульфиды L-глутамил L - цистеинилглициналкиловые (низшие) эфиры получают путем окисления воздухом, перекисью водорода, йодом в водной среде солей-2-глутамил- L цистеинилглициналкиловых (низших) эфиров. 2 с.п.ф-лы.
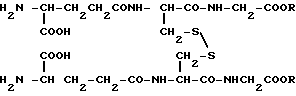
где R низший алкил.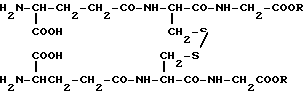
где R низший алкил,
отличающийся тем, что глутатионмоноалкиловый эфир формулы II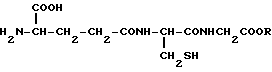
где R низший алкил,
окисляют воздухом, перекисью водорода или йода в воде или в водном растворе.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Rajinder N | |||
| Puri, Alton Meisfer "Transfort of glutathione, as $$$ glutamylcysteinylglycyl ester, into liver and Kiducy" Por | |||
| Natl | |||
| Acad | |||
| Sci | |||
| USA, 80, стр.5258-5260, 1983. | |||
Авторы
Даты
1995-09-20—Публикация
1991-12-27—Подача