Изобретение относится к биофизическим способам анализа, предназначено для определения концентраций CN--ионов в растворе и может быть использовано для контроля за содержанием циан-ионов в технологическом цикле золотоизвлекающих фабрик и других предприятий, а также в их сточных водах.
Известен спектрофотометрический способ определения концентрации CN--ионов в растворах с помощью пиридин-бензидинового метода. Сущность этого способа состоит в проведении с анализируемой пробой ряда химических реакций (с участием брома, гидразина, смеси пиридина и бензидина) и последующем спектрофотометрированием образца при λ= 520 нм. По величине оптической плотности и калибровочному графику, полученному с использованием стандартных циансодержащих растворов, определяют концентрацию CN--ионов в исследуемой пробе.
Недостатками этого способа являются низкая оперативность определения концентраций CN--ионов в производственных условиях (время анализа около 2 ч), а также необходимость использования в лабораторном анализе вредных для здоровья людей химических веществ (бензидин).
Техническим результатом изобретения является интенсификация процесса и улучшения условий труда.
Это достигается тем, что в качестве аналитического индикатора используют микроводоросль хлореллу, которую в присутствии циан-ионов первоначально облучают видимым светом с интенсивностью 30-50 Вт/м2 ФАР в течение 50-70 с, затем после 8-10-секундного перерыва облучают возбуждающим светом с интенсивностью 5-8 Вт/м2 ФАР, регистрируя при этом кинетику замедленной флуоресценции водоросли, а количество циан-ионов рассчитывают по величине Kц , где Н и К максимальная интенсивность быстрой и медленной фазы замедленной флуоресценции (ЗФ) соответственно.
, где Н и К максимальная интенсивность быстрой и медленной фазы замедленной флуоресценции (ЗФ) соответственно.
Сущность способа заключается в определении эффекта, который оказывают CN--ионы на величину медленной фазы индукции ЗФ водоросли.
П р и м е р 1. В семь кварцевых кювет наливают по 2 мл активно растущей хлореллы (Chlorella vulgaris), взятой из культиватора. Добавляют в них по 2 мл стандартных растворов цианида натрия по спадающей концентрации (25; 12,5; 6,25 мг/л и т.д.), а в остальные вносят такое же количество исследуемых растворов. При этом рН стандартных и исследуемых растворов должны быть одинаковыми.
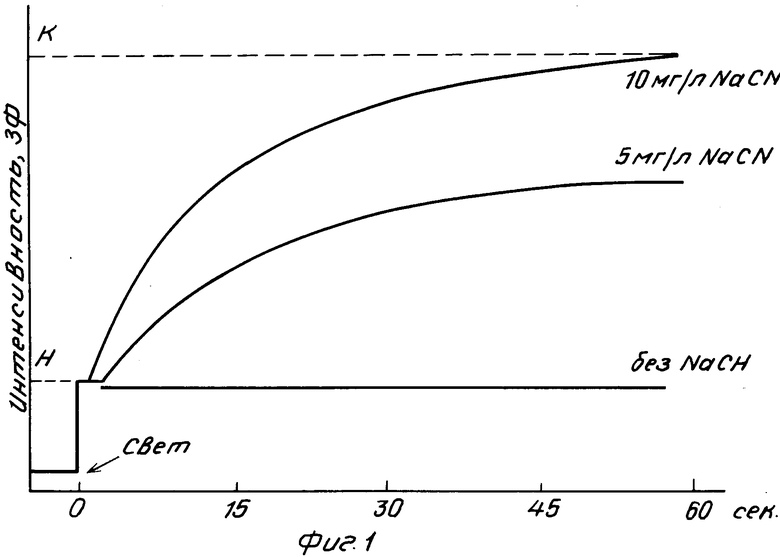
После 50 с облучения видимым светом интенсивностью 30 Вт/м2 ФАР и последующей восьмисекундной темновой паузы быстро включают возбуждающий свет интенсивностью 5 Вт/м2 ФАР и регистрируют кинетику индукционных измерений ЗФ. Как показано на фиг. 1, интенсивность ЗФ водоросли в циансодержащей среде в первый момент освещения быстро увеличивается до начального пика (быстрая фаза), а затем значительно более медленно возрастает до своей максимальной величины (медленная фаза).
С уменьшением концентрации CN--ионов в пробе медленная фаза индукции становится меньше, практически исчезая в образцах, не содержащих циан-ионы, тогда как быстрая фаза изменяется очень мало.
Если выразить долю медленной фазы в виде коэффициента Кц, то его величина в широком интервале концентраций линейно связана с содержанием CN--ионов в исследуемых растворах (фиг. 2):
Kц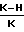 (1) где Н и К значения интенсивности ЗФ в начале и конце ее индукции.
(1) где Н и К значения интенсивности ЗФ в начале и конце ее индукции.
Используя данную концентрационную зависимость как калибровочный график, можно определить содержание циан-ионов в исследуемых растворах. Для этого нужно отложить на оси ординат графика значение Кц для исследуемой пробы и провести линию, параллельную оси абсцисс, и вычислить величину концентрации циан-ионов в образце (фиг. 2).
Поскольку ось абсцисс представлена здесь в логарифмическом масштабе, концентрацию цианида натрия в пробе (Спр) рассчитывают по формуле
Cпр.=Cб·10
 (2) где Сб ближайшая по величине концентрация цианида натрия на калибровочной кривой большая, чем Спр; lпр длина от Сб до пересечения перпендикуляра с осью абсцисс, мм; lo длина спадающего концентрационного шага на оси абсцисс, мм.
(2) где Сб ближайшая по величине концентрация цианида натрия на калибровочной кривой большая, чем Спр; lпр длина от Сб до пересечения перпендикуляра с осью абсцисс, мм; lo длина спадающего концентрационного шага на оси абсцисс, мм.
Для фиг. 2 lпр составляет 8,5 мм, что при lo 20 мм соответствует концентрация цианида натрия в пробе
Спр 4,65 мг/л. Время анализа составляет 5 мин.
П р и м е р 2. Кюветы (взятые по примеру 1) со стандартными растворами NaCN и исследуемым раствором облучают видимым светом интенсивностью 50 Вт/м2 ФАР в течение 70 с. После десятисекундной темновой паузы включают возбуждающий свет интенсивностью 8 Вт/м2 ФАР и регистрируют кинетику индукционных изменений ЗФ. Калибровочная кривая для данного опыта приведена на фиг. 3. Величина lпр для исследуемой пробы составляет 8,6 мм, и соответственно концентрация цианида натрия в ней
Спр 4,64 мг/л. Время анализа пробы 6 мин.
Расчет содержания цианида натрия в пробе может быть произведен не только графическим, но и аналитическим способом. Для этого используется следующая формула:
Cпр.= C2·10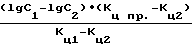 (3) где Спр, С1 и С2 концентрации цианида в пробе и в двух стандартных растворах соответственно; Кц.пр. и Кц1, Кц2 коэффициенты Кц этих растворов.
(3) где Спр, С1 и С2 концентрации цианида в пробе и в двух стандартных растворах соответственно; Кц.пр. и Кц1, Кц2 коэффициенты Кц этих растворов.
Для получения максимальной точности определения цианида натрия необходимо строго сохранять выбранный режим измерения в течение всего сеанса регистрации индукционных кривых ЗФ стандартных и исследуемых образцов. С этой же целью все образцы для каждого сеанса должны быть приготовлены из одной общей культуры водоросли.
П р и м е р 3. Интенсивность возбуждающего света 8 Вт/м2 ФАР. Для концентраций 6,25 мг/л NaCN (С1) и 3,12 мг/л NaCN (С2) в суспензии хлореллы получены величины Кц, равные соответственно 0,6 и 0,52. Кцпробы определяемой концентрации составила 0,57.
Подставляя указанные выше данные в формулу (3), имеют
Cпр 4,66 мг/л NaCN.
Умножением данной величины на коэффициент 0,53 получают искомую величину концентрации СN--ионов в исследуемой пробе.
Проведенные с помощью биофизического метода анализы проб показали хорошую сходимость результатов определения концентрации циан-ионов и используемым пиридин-бензидиновым методом. Так, анализ трех проб растворов, приведенный предлагаемым способом, указал на наличие в них циан-ионов в следующих концентрациях: 1,9; 5,1 и 6,5 мг/л. Анализ этих же проб в химической лаборатории пиридин-бензидиновым методом дал следующие результаты: 2; 5; 6,7 мг/л соответственно.
Преимущество заявляемого способа по сравнению с пиридин-бензидиновым методом заключено в значительно меньшей длительности анализа (5 мин вместо 120), простоте и экономичности анализа из-за использования в качестве индикатора одного биологического объекта вместо набора дорогостоящих химических реактивов, безопасных условиях работы для персонала, поскольку в предлагаемом способе не используются вредные для здоровья реактивы (бензидин).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ФИТОТОКСИЧЕСКИХ ВЕЩЕСТВ | 1992 |
|
RU2069851C1 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ПРИРОДНЫХ, СТОЧНЫХ ВОД И ВОДНЫХ РАСТВОРОВ | 2001 |
|
RU2222003C2 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ТОКСИЧНОСТИ ВОД И ВОДНЫХ РАСТВОРОВ | 2011 |
|
RU2482474C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ПОЧВ | 2007 |
|
RU2375714C2 |
| УСТРОЙСТВО ДЛЯ ВЫРАЩИВАНИЯ МИКРОВОДОРОСЛЕЙ | 1999 |
|
RU2165973C2 |
| Устройство фотоэлектрохимическое для оценки токсичности жидкости | 1980 |
|
SU957104A1 |
| Фотореактор для культивирования микроводорослей | 1977 |
|
SU686686A1 |
| Способ управления культивированием микроорганизмов в группе реакторов | 1980 |
|
SU977489A1 |
| Термофильный штамм водоросли Chlorella vulgaris Beijer для оперативного биотестирования токсичности водных сред | 2023 |
|
RU2819768C1 |
| СПОСОБ КУЧНОГО ВЫЩЕЛАЧИВАНИЯ ЗОЛОТА ИЗ МИНЕРАЛЬНОГО СЫРЬЯ | 2015 |
|
RU2608481C2 |


Способ может быть использован для контроля содержания циан-ионов технологическом цикле золотоизвлекающих фабрик и других предприятий, а также в их сточных водах. Сущность изобретения: в качестве аналитического индикатора используют микроводоросль хлореллу, которую первоначально облучают видимым светом с интенсивностью 30-50 Вт/м2 ФАР в течение 50-70 с. После 8-10-секундного темнового периода включают свет с интенсивностью 5-8 Вт/м2 и регистрируют индукцию замедленной флуоресценции водоросли, выделяя из нее медленную фазу, величина которой является показателем содержания циан-ионов в среде. 3 ил.
СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ЦИАН-ИОНОВ В РАСТВОРЕ, включающий взаимодействие циан-ионов с аналитическим индикатором и регистрацию его свечения, отличающийся тем, что в качестве аналитического индикатора используют микроводоросль хлореллу, которую в присутствии циан-ионов первоначально облучают видимым светом с интенсивностью 30 50 Вт/м2 в течение 50 70 с, затем после 8 10 секундного перерыва облучают возбуждающим светом с интенсивностью 5 8 Вт/м2, регистрируя при этом кинетику замедленной флуоресценции водоросли, а концентрацию Kц циан-ионов рассчитывают по величине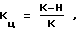
где H и K максимальная интенсивность быстрой и медленной фазы замедленной флуоресценции соответственно.
| Лурье Ю.Ю | |||
| Унифицированные методы анализа воды | |||
| М.: Химия, 1973, с.215 - 222. |
Авторы
Даты
1995-10-20—Публикация
1992-01-27—Подача