Изобретение относится к области средств защиты сельскохозяйственных культур от грибковых заболеваний.
В частности изобретение относится к новым производным β-феноксинитрилов и к способу борьбы с грибковыми заболеваниями культур.
Известны многочисленные соединения с пиридиловыми группами, имеющими фунгицидные свойства. В частности, из заявки на патент ЕР-А-145260 известны фунгициды, производные 2-/3-пиридил/2-фениламиноуксусной кислоты. Из заявки на патент ЕР-А-214793 известны фунгициды, производные 2-арил/3-пиридилпропионитрилов.
Задача изобретения разработка фунгицидных соединений с более широким спектром активности, чем известные.
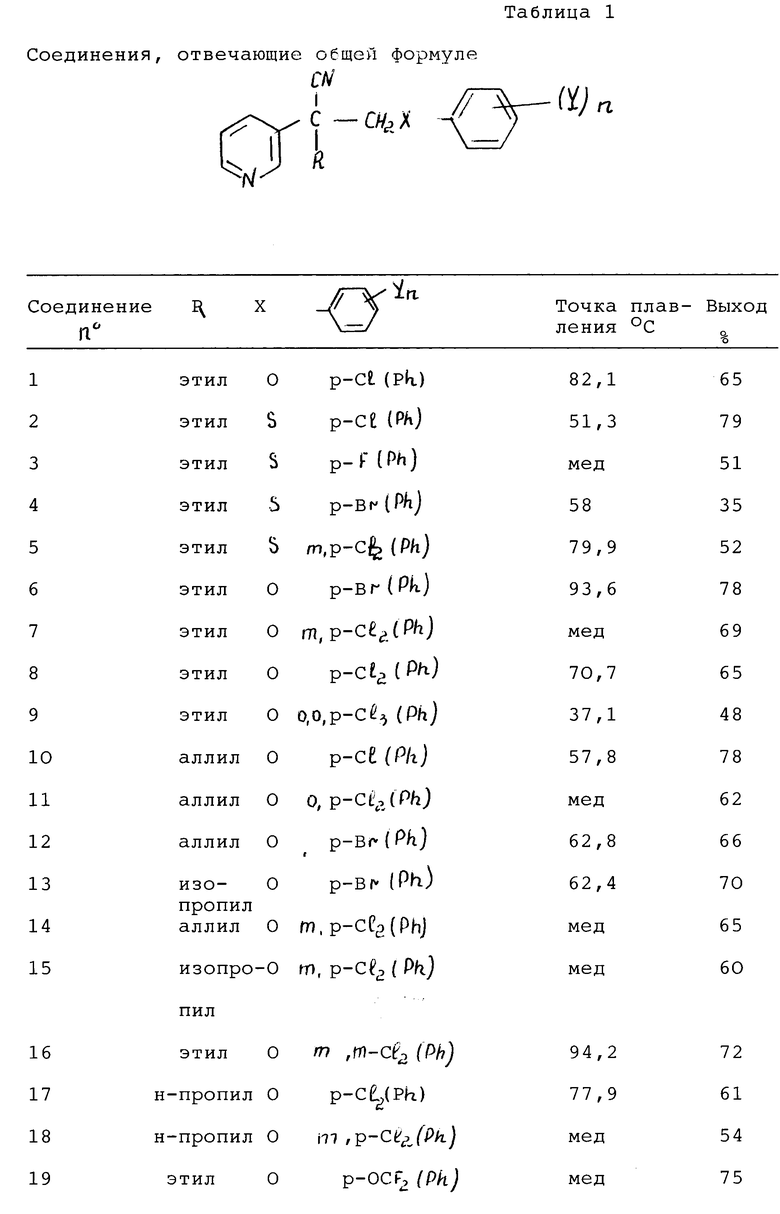
Эта задача решается с помощью производных b-феноксинитрилов общей формулы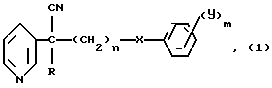
в которой
R водород, метил, этил, изопропил, н-пропил, аллил,
n 1 или 2,
x атом кислорода или серы,
y хлор, бром, фтор,
m 1, 2, 3, проявляющим фунгицидную активность.
Новые соединения могут быть полезны при борьбе с такими заболеваниями стеблей, как гниль корневой шейки, или с заболеваниями листьев такими, как оидиум, септориоз, пирикулариоз, фузариозы, ринхоспориоз, с болезнями, вызванными патогенными грибками, такими, как Botrytis, Phoma, Aschochyta, Alternaria у таких различных культур, как, например, зерновые культуры, виноградник, рис, кукуруза, соя.
Способ получения соединений формулы (1), где n 1, заключается в реакции, на первом этапе, соединения формулы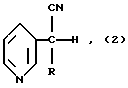 в которой R имеет указанное выше значение, с дигалогенметиленом формулы (3):
в которой R имеет указанное выше значение, с дигалогенметиленом формулы (3):
(Гал)2CH2, (3)
где Гал означает галогенатом, предпочтительно хлор или бром, в среде основного характера при молярном соотношении III:II предпочтительно составляющем 0,8-1,2, в известных случаях, в присутствии инертного растворителя, с получением соединения формулы
и на втором этапе, полученное соединение подвергают взаимодействию с соединением формулы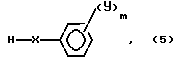
в которой X, Y и m имеют указанное выше значение в присутствии сильного основания типа гидридов щелочного металла или алкоголятов щелочного металла в присутствии в известных случаях соответствующего апротонного полярного растворителя такого, как, например, диметилформамид, диметилацетамид, диметилсульфоксид, ацетонитрил, N-метилпирролидон при молярном соотношении IV: V, предпочтительно составляющем 0,8 1,2 и предпочтительно при температуре 20-100oC или при рефлюксе растворителя, если он присутствует.
На первом этапе используют минеральные основания, например, едкий натр или едкое кали, карбонаты щелочных или щелочноземельных металлов или органические основания такие, как алкоголяты щелочных металлов типа этилата натрия. Предпочтительно используются 0,5 3,0 молярных эквивалентов основания.
В качестве инертного растворителя можно назвать апротонные полярные растворители такие, как, например, дибутилэфир, диизопропилэфир, ТГФ, диизоамилэфир или дигалогенометилен формулы (3). При желании, эта реакция может осуществляться в присутствии соответствующего катализатора. В качестве возможного катализатора можно назвать катализаторы переноса фаз такие, как, например, четвертичные производные аммония типа хлорида тетрабутиламмония или хлорида метилтриалкил (C8-C10) аммония.
Предпочтительно первый этап осуществляется при температуре 20 100oC или при температуре рефлюкса растворителя, если он присутствует.
В случае получения соединений формулы (1), где n 2, способ заключается на первом этапе в реакции соединения формулы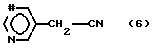
с соединением формулы
где Х, У и m имеют указанное выше значение;
Гал атом галогена,
в присутствии сильного основания в молярном соотношении 7:6, предпочтительно составляющем 0,8-1,2, в известных случаях в присутствии полярного апротонного растворителя, что приводит к соединению формулы
затем на втором этапе полученное соединение подвергают взаимодействию с соединением формулы Гал-R, причем Гал является галогенатомом, а R имеет значение, указанное выше, за исключением H, в среде основного характера, в молярном отношении предпочтительно составляющем 0,8-1,2, в известных случаях в присутствии полярного апротонного растворителя, как указывается на этапе 2, и при температуре, составляющей 20-100oC, или при рефлюксе растворителя, если он присутствует.
В конце реакции независимо от используемого способа целевое соединение выделяется из реакционной среды обычными методами такими, как отгонка растворителя или кристаллизация продукта из реакционной среды, или фильтрация, затем, если необходимо, целевой продукт очищают, например посредством рекристаллизации в соответствующем растворителе или посредством хроматографии.
Изобретение относится также к использованию соединений формулы (1) в качестве фунгицидов.
Соединения согласно изобретению могут использоваться для превентивной обработки незараженных культур или для обработки культур, зараженных грибками, в частности грибками типа базидиомицетов, аскомицетов, аделомицетов или фунги-имперфекти, в частности ржавчина, оидиум, грибковая болезнь злаков, фузариозы, гельминтоспориозы, септориозы, ризоктонии растений и, в частности зерновых культур таких, как пшеница, ячмень, рожь, овес и их гибриды, а также рис и кукуруза. Соединения, согласно изобретению, являются активными, в частности по отношению к грибкам типа базидиомицеты, аскомицеты, аделомицеты или фунги-имперфекти типа Botrytis cinerea, Erysiphe graminis, Puccinia recondita, Piricularia oryzae, Cercospora beticola, Puccinia striiformis, Erysiphe cicho racearum, Fusarium oxysporum (melonis), Pyrenophora avenae, Septoria tritici, Venturia inaegualis, Whetzelinia sclerotiorum, Monilia laxa, Mycosphaerella bijiensis, Marssonina panettoniana, Alternaria solani, Aspergillus niger, Cercospora arachidicola, Cladosporium herbarum, Helminthosporium oruzae, Penicillium expansum, Pestalozzia sp, Phialophora cinerescens, Phoma betae, Phoma boveata, Phoma lingam, Ustilago maydis, Verticillium dahliae, Ascochyta pisi, Jyighardia bidwellii, Corticium rolfsii, Phomopsis viticola, Sclerotinia sclerotiorum, Sclerotinia minor, Coryneum cardinale, Phizoctonia solani, Uncinula necator, Podosphaera leucotricha, Fusicladium sp.
Они также активны по отношению к следующим грибкам: Acrostalagmus koningi, Alternari, Colletotrichum, Corticium rolfsii, Diplodia natalensis, Jaeumannomyces graminis, Jibberella fojikuroi, Hormodedron cladosporioides, Lentinus degener или tigrinus, Lenzites quercina, Nemnoniella echinata, Myrothecium verrucaria, Paecylomyces varioti, Pellicularia sasakii, Phellinus megaloporus, Polystictus sanguineus, Poria vaporaria, Sclerotium rolfsii, Stachybotris atra, Stereum, Stilbum sp, Trametes trabea, Trichodermapseu dokoningi, Trichothecium roseum.
Соединения изобретения особенно интересны своим широким спектром действия против болезней злаковых культур (оидиум, ржавчина, офиоболез при полегании гельминтоспориозы, септориозы и фузариозы). Они представляют также большой интерес в связи с активностью на серой гнили (Botrytis) и пирикулариозах, поэтому они могут применяться на таких разнообразных культурах, как виноградник, овощные культуры и разведение деревьев, а также на тропических культурах таких, как арахис, банан, кофейное дерево, орех, рис и другие.
Вследствие отсутствия фитотоксичности соединения могут использоваться для защиты средств размножения растений от грибковых болезней.
Термином "средство размножения" обозначаются все воспроизводящие части растений, которые можно использовать для его размножения. Можно назвать, например, семена, корни, плоды, клубни, луковицы, корневища, части стебля, саженцы (ростки) и другие части растений. Можно назвать также проросшие растения и саженцы, которые должны пересаживаться после прорастания или после выхода из земли. Эти молодые саженцы могут защищаться перед трансплантацией путем полной или частичной обработки посредством погружения.
Так, эти соединения могут использоваться для обработки семян (например, злаковых культур, хлопчатника, свеклы, рапса, фуражного зерна, овощей) в форме гранул или нанесенной пленки.
Кроме уже описанных областей применения продукты согласно изобретению обладают, и отличной биоцидной активностью по отношению ко многим другим разновидностям микроорганизмов, среди которых можно назвать в качестве неограниченного примера, грибки:
Pullularia рода P. pullulans;
Chaetomium рода C. globosum;
Aspergillus рода Aspergillus niger;
Coniophora рода C. puteana.
Ввиду их биоцидной активности продукты изобретения позволяют эффективно бороться с микроорганизмами, размножение которых создает много проблем в сельском хозяйстве и в промышленности. Для этой цели они особенно пригодны для защиты растений или промышленных изделий таких, как древесина, кожа, краски, бумага, снасти, пластмассы, промышленные водостоки.
Особенно они пригодны для защиты древесно-целлюлозных изделий и, в частности меблировки, строительного леса или древесины, подвергающейся воздействию климатических условий, таких, как деревянная изгородь, виноградные колья, железнодорожные шпалы.
Для обработки древесины соединения согласно изобретению обычно применяются вместе с органическими растворителями и могут в известных случаях соединяться с одним или с несколькими известными биоцидными продуктами такими, как пентахлорфенол, металлические соли, в частности медь, марганец, кобальт, хром, цинк, производные минеральных или карбоновых кислот (гептановые, октановые, гексагидробензойные кислоты); органические комплексные соединения олова, меркаптобензотиазол, инсектициды такие, как пиретроиды или органохлорированные соединения.
Наконец, соединения обладают отличной селективностью по отношению к культурам.
Преимущественно, они применяются в дозах от 0,005 5,0 кг/га и особенно 0,03 1,0 кг/га.
При практическом применении соединения согласно изобретению редко используются в отдельности. Чаще всего они входят в композиции. Эти композиции, которые могут использоваться для защиты растений от грибковых болезней, содержат в качестве активного вещества одно из вышеописанных соединений согласно изобретению в сочетании с твердыми или жидкими подложками, приемлемыми в сельском хозяйстве, и/или с поверхностно-активными веществами, приемлемыми в сельском хозяйстве.
Эти композиции обычно содержат 0,5 95,0 соединения согласно изобретению.
Композиции на основе соединения формулы (1) могут быть твердыми или жидкими.
В качестве твердых композиций можно назвать порошки для опудривания или диспергирования (с содержанием соединения формулы (1), которое может доходить до 100%) и гранулы, в частности полученные путем экструзии, прессования, пропитки гранулированной подложки, гранулирования порошка (с содержанием соединения формулы (1) в этих гранулах 1-80).
В качестве форм жидких композиций можно назвать растворы, в частности растворимые в воде концентраты, эмульгирующиеся концентраты, эмульсии, концентрированные суспензии, аэрозоли, смачивающиеся порошки (или порошок для распыления), пасты.
Эмульгирующиеся или растворимые концентраты содержат чаще всего 10-80% активного вещества, а готовые к применению эмульсии или растворы содержат 0,01 20,0% активного вещества.
При использовании соединений формулы (1) в качестве фунгицидов дозы нанесения могут изменяться в широких пределах, в частности в зависимости от вирулентности грибков и климатических условий.
Нижеприведенные примеры иллюстрируют получение соединений согласно изобретению, а также их использование для борьбы с фитопатогенными грибками. Структуры соединений, описанных в этих примерах, были подтверждены спектрометрией ядерного магнитного резонанса (ЯМР) и/или инфракрасной спектрометрией.
Пример 1. Этап 1. Получение 2-/3-пиридинил/2-этил-3-бромпропаннитрила. Используют трехгорлую колбу, снабженную мешалкой, термометром, охладителем и капельной воронкой.
В колбу последовательно загружают 14,6 г 2-/3-пиридинил/бутаннитрила, 30 мл метиленбромида и 3 г хлорида метилтриалкил /C8-C10/аммония /Адоген 464/, смесь выдерживают при перемешивании.
Затем добавляют 12 г едкого натра, растворенного в 12 мл воды.
Смесь доводят до 90oC в течение 3 ч. После охлаждения добавляют 20 мл воды в коричневатый раствор, который экстрагируют метиленхлоридом.
Собранные органические фазы промывают водой, высушивают на сульфате магния, затем концентрируют.
Полученное сырое масло хроматографируют на колонне двуокиси кремния (элюент: диизопропиловый эфир).
Получают 19,6 г 2-/3-пиридинил/-2-этил-3-бромпропаннитрила в виде светло-желтого вязкого масла. Выход: 82%
Ниже приводятся характеристики промежуточных соединений формулы V, полученных таким же образом.
Этап 2. Получение 2-/3-пиридинил/-2-этил-3-/4-хлорфенокси/пропаннитрила. Используют устройство, описанное в предыдущем примере. В колбу вводят 100 мл диметилформамида, затем 3,75 г (0,126 г-атом) гидрида натрия (80 в масле). На суспензию, охлажденную до 100oC, выливают 15,4 г (0,12 моль) 4-хлорфенола, растворенного в 30 мл диметилформамида. Смесь выдерживают 30 мин при температуре окружающей среды.
Затем добавляют 23,9 г (0,1 моль) 2-/3-пиридинил/-2-этил-3-бромпропаннитрила, растворенные в 20 мл диметилформамида. Раствор доводят до 100oC в течение 6 ч. После охлаждения до 10oC добавляют 300 мл ледяной воды в раствор, затем экстрагируют этилацетатом (3•60 мл). Собранные органические фазы последовательно промывают посредством 100 мл 10% -ного водного раствора KHCO3, затем 200 мл воды и высушивают на сульфате магния, затем концентрируют.
Полученный вязкий осадок хроматографируют на колонне двуокиси кремния (элюент: диизопропиловый эфир). Получают бежевое твердое вещество, которое рекристаллизируют из 40 мл смеси диизопропиловый эфир/гептан, 50/50 и получают 18,6 г (0,065 моль) 2-/3-пиридинил/2-этил-3-/4-хлорфенокси/пропаннитрила в виде белого твердого вещества, плавящегося при 82,1oC.
Выход (рассчитанный исходя из 2-/3-пиридинил/-2-этил-3-бромпропаннитрила): 65%
Таким же образом получают соединения по примерам 2-25, которые приводятся в табл.1 и номенклатура которых указывается после примеров.
Пример 26. Этап 1: Получение 2-/3-пиpидинил/-4-/4-xлopфeнокcи/бутaннитрила. Используют трехгорлую колбу, снабженную мешалкой, термометром, охладителем и капельной воронкой.
В колбу вводят 250 мл безводного диметилформамида, затем 3,15 г (0,105 моль) гидрида натрия (80 в масле).
В этом случае добавляют по каплям 11,8 г (0,1 моль) 2-/3-пиридинил/ацетонитрила, растворенного в 30 мл диметилформамида.
На образовавшуюся соль добавляют затем по каплям 23,5 г (0,1 моль) 1-бром-2-/4-хлорфенокси/этана, растворенного в 30 мл диметилформамида.
Раствор выдерживают 2 ч с перемешиванием при 25oC. В этом случае смесь выливают на 500 мл ледяной воды, затем экстрагируют этилацетатом (3•150 мл). Собранные органические фазы промывают посредством 300 мл воды, высушивают на сульфате магния, затем концентрируют.
Полученное сырое масло восстанавливают посредством 100 мл этилового эфира.
Быстро появляющийся белый осадок фильтруют, собранная масса в 3,5 г плавится при 141oC.
Концентрированный фильтрат хроматографируют на колонне двуокиси кремния. Получают 16,8 г 2-/3-пиридинил/-4-/4-хлор-фенокси/бутаннитрила в виде светло-желтого масла. Выход 62%
Этап 2: Получение 2-/3-пиридинил/2-метил-4-4-/4-хлорфенокси/ бутаннитрила. Используют то же самое устройство, описанное на этапе 1. В колбу вводят 100 мл безводного диметилформамида, затем 1,57 г /5,25 10-2 г-атом/гидрида натрия.
В этом случае добавляют по каплям 13,6 г (0,05 моль) 2-/3-пиридинил/-4-/4-хлорфенокси/бутаннитрила, растворенного в 20 мл диметилформамида. Затем наливают 3,2 мл (0,05 моль) метилиодида, растворенного в 20 мл диметилформамида.
Раствор выдерживают 3 ч с перемешиванием при 25oC.
В этом случае смесь выливают на 300 мл ледяной воды, затем экстрагируют этилацетатом (3•60 мл). Собранные органические фазы промывают посредством 150 мл воды, высушивают на сульфате магния, затем концентрируют.
Полученное сырое масло хроматографируют на колонне двуокиси кремния (элюент: диизопропиловый эфир) и получают 7,7 г 2-/3-пиридинил/2-метил-4-/4-хлорфенокси/бутаннитрила в виде желтого масла. Выход 54
Номенклатура
Пример 2:
2-/3-пиридинил-/2-этил-3-/4-хлортиофенокси/пропаннитрил.
Пример 3:
2-/3-пиридинил/2-этил-3-/4-фтортиофенокси/пропаннитрил.
Пример 4:
2-/3-пиридинил/-2-этил-3-/4-бромтиофенокси/пропаннитрил.
Пример 5:
2-/3-пиридинил/2-этил-3-3,4-дихлортиофенокси/пропаннитрил.
Пример 6:
2-/3-пиридинил-/2-этил-3-/4-бромфенокси/пропаннитрил.
Пример 7:
2-/3-пиридинил/2-этил-3-/3,4-дихлорфенокси/пропаннитрил.
Пример 8:
2-/3-пиридинил/2-этил-3-/2,4-дихлорфенокси/пропаннитрил.
Пример 9:
2-/3-пиридинил/2-этил-3-/2,4,6-трихлорфенокси/пропаннитрил.
Пример 10:
2-/3-пиридинил/2-аллил-3-/4-хлорфенокси/пропаннитрил.
Пример 11:
2-/3-пиридинил/2-аллил-3-/2,4-дихлорфенокси/пропаннитрил.
Пример 12:
2-/3-пиридинил-/2-аллил-3-/4-бромфенокси/пропаннитрил.
Пример 13:
2-/3-пиридинил/2-метилэтил-3-/4-бромфенокси/пропаннитрил.
Пример 14:
2-/3-пиридинил/2-аллил-3-/3,4-дихлорфенокси/пропаннитрил.
Пример 15:
2-/3-пиридинил/2-метилэтил-3-/3,4-хлорфенокси/пропаннитрил.
Пример 16:
2-/3-пиридинил/2-этил-3/3,5-дихлорфенокси/пропаннитрил.
Пример 17:
2-/3-пиридинил/2-пропил-3-/4-хлорфенокси/пропаннитрил.
Пример 18:
2-/3-пиридинил/2-пропил-3/3,4-дихлорфенокси/пропаннитрил.
Пример 19:
2-/3-пиридинил/2-этил-3-/4-трифторметоксифенокси/пропаннитрил.
Пример 20:
2-/3-пиридинил/2-этил-3-/4-фторфенокси/пропаннитрил.
Пример 21:
2-/3-пиридинил/2-этил-3-/3-фторфенокси/пропаннитрил.
Пример 22:
2-/3-пиридинил/2-этил-3-/3,4,5-трихлорфенокси/пропаннитрил.
Пример 23:
2-/3-пиридинил/2-этил-3-/2,4-дибромфенокси/пропаннитрил.
Пример 24:
2-/3-пиридинил/-4-/4-хлорфенокси/бутаннитрил.
Пример 25:
2-/3-пиридинил/2-метил-4-/4-хлорфенокси/бутаннитрил.
Пример 26:
2-/3-пиридинил/2-этил-4-/4-хлорфенокси/бутаннитрил.
Пример 27:
2-/3-пиридинил/2-4-/4-хлорфенокси/бутаннитрил.
Пример 28:
2-/3-пиридинил/2-аллил-4/4-хлорфенокси/бутаннитрил.
Пример 29:
2-/3-пиридинил/2-этил-4-/3,4-дихлорфенокси/бутаннитрил.
Пример 30:
2-/3-пиридинил/2-пропил-4-/3,4-дихлорфенокси/бутаннитрил.
Пример 31:
2-/3-пиридинил/-4-/4-хлортиофенокси/бутаннитрил.
Пример 32:
2-/3-пиридинил-/2-метил-4-/4-хлортиофенокси/бутаннитрил.
Пример 33:
2-/3-пиридинил/2-этил-4-/4-хлортиофенокси/бутаннитрил.
Пример 34:
2-/3-пиридинил/2-пропил-4-/4-хлортиофенокси/бутаннитрил.
Пример 35:
2-/3-пиридинил/-4-/4-бромтиофенокси/бутаннитрил.
Пример 36:
2-/3-пиридинил/2-метил-4-/4-бромтиофенокси/бутаннитрил.
Пример 37:
2-/3-пиридинил/2-этил-4-/4-бромтиофенокси/бутаннитрил.
Пример 38:
2-/3-пиридинил/2-пропил-4-/4-бромтиофенокси/бутаннитрил.
Пример Тест in vitro на грибках семян и на грибках почвы. Изучается воздействие соединений согласно изобретению на следующие грибки, ответственные за болезни зерновых культур и других растений:
11) Pyrenophorae avenae;
6) Septoria nodorum;
12) Helminthosporium teres;
9) Fusarium roseum;
8) Fusarium nivale;
7) Fusarium culmorum;
13) Rhizoctonia ceredlis;
14) Septoria tritici;
1) Botrytis cinerea, чувствительный к карбендазиму и циклическим имидам;
2) Botrytis cinerea, стойкий к карбендазиму и циклическим имидам;
5) Pseudocercosporella herpotrichoides;
3) Fusarium oxysporum F. sp melonis;
4) Rhizoctonia solani;
10) Helmithosporium gramineum.
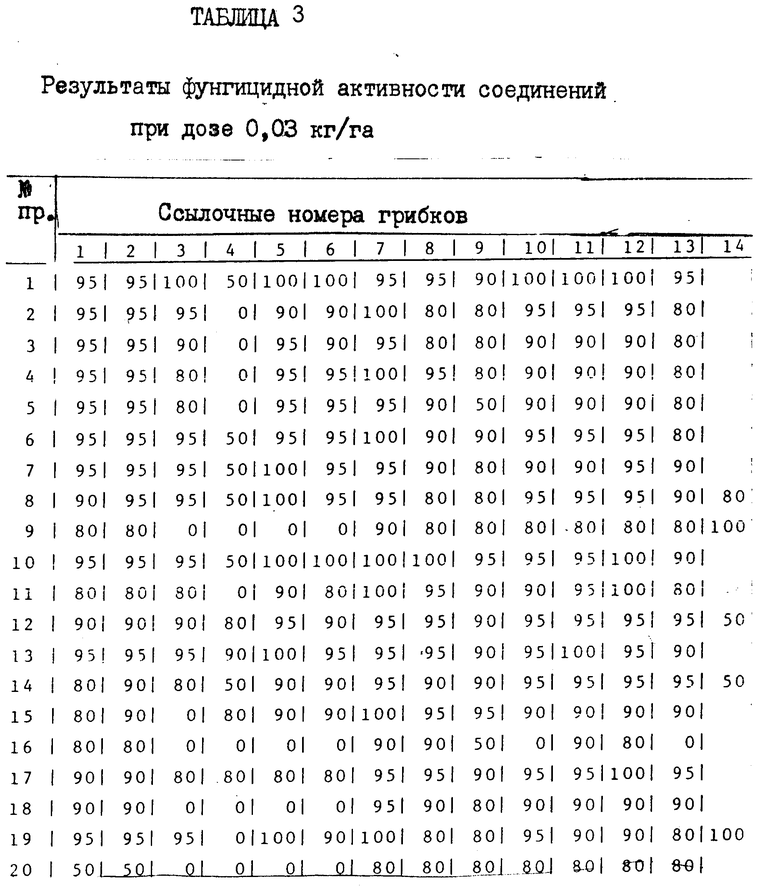
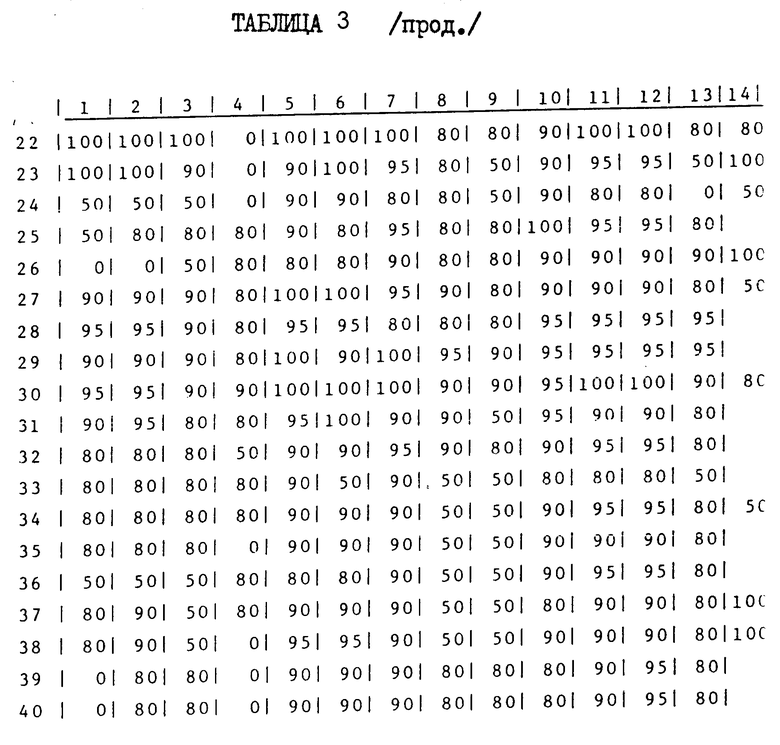
Цифры, стоящие перед названиями, будут использованы для ссылки на эти грибки в табл. 3.
В каждом опыте действуют следующим образом: питательная среда, состоящая из картофеля, глюкозы и агара (среда РДА) вводится в режиме переохлаждения в серию чашек Петри (20 мл на чашку) после стерилизации в автоклаве при 120oC.
В ходе заполнения чашек в переохлажденную среду впрыскивают ацетонный раствор активного вещества для получения заданной конечной концентрации.
В качестве контрольных, принимают чашки Петри, аналогичные предыдущим чашкам, в которые помещают одинаковые количества питательной среды, не содержащей активного вещества.
После 24 или 48 ч каждая чашка засевается путем внесения фрагмента мицелия из предыдущей культуры того же грибка.
Чашки хранят в течение 2 10 дней (в зависимости от используемого грибка) при 22oC и сравнивают в этом случае рост грибка в чашках, содержащих исследуемое активное вещество, с ростом того же грибка в чашке, использованной в качестве контрольной.
Таким образом, определяют для каждого исследуемого соединения степень задержки роста рассматриваемого грибка при дозе 30 ppm. Результаты указаны в табл. 3.
Пример: тест in vivo на Botrytis Cinerea томата. Путем тонкого измельчения получают водную суспензию тестируемого активного вещества, имеющую следующий состав, мг:
Активное вещество 40,0
Твин 80 (поверхностно-активное вещество, состоящее из монолаурата поликсиэтиленированного производного сорбитана) 0,4
Вода 40,0 мл
Эта водная суспензия затем разбавляется водой для получения заданной концентрации.
Томаты, выращенные в теплице (сорт Марманд), возраст 60-75 дней, обрабатывают путем пульверизации водных суспензий описанного состава при концентрации активного вещества 1 г/л (1000 ppm). Испытание повторяют два раза.
После 24 ч срезают листья и помещают их в две чашки Петри (диаметр 11 см), дно которых предварительно снабжено диском из влажной фильтровальной бумаги (5 листочков на чашку).
Затем с помощью шприца вносят прививку путем нанесения капелек (три капельки на листочек) суспензии спор. Эту суспензию Botrytis cinerea получают из 15-дневной культуры, с последующим суспензированием в питательном растворе (80000 ед. /см3). Контроль осуществляют примерно через 4-6 дней после заражения путем сравнения с необработанным контрольным образцом. Таким образом оценивают процент защиты по сравнению с необработанным контрольным образцом.
В условиях, отмечают, что при концентрации 1 000 мг/л процент защиты составляет по меньшей мере 75% для следующих соединений: 1, 4, 5, 6, 7, 10, 12, 13, 15, 17, 18, 22, 23, 27, 28, 30, 35.
Пример: тест in vivo на оидиуме ржи с превентивной обработкой. Путем тонкого измельчения получают водную суспензию тестируемого активного вещества, имеющую следующую композицию, мл:
Тестируемое активное вещество 60,0 мг
Твин 80 (поверхностно-активное вещество, состоящее из монолаурата полиоксиэтиленированного производного (сорбитана)), разбавленного в пропорции 1/10 0,3
Вода 60,0
Эту водную суспензию затем разбавляют водой для получения заданной концентрации.
Саженцы ржи (Hordeum vulgare), сорт Берак, выращивают в горшках. Через 5-6 дней после посева их листву обрабатывают путем пульверизации на каждый саженец 8 мл суспензии активного вещества в дистиллированной воде, содержащей Твин 80 заданной концентрации.
Наносят активное вещество три раза. Контрольные саженцы обрабатывают таким же образом, но без активного вещества.
После высушивания на следующий день после обработки саженцы заражают спорами сидиума ржи (Erysiphe graminis) посредством опудривания, затем выдерживают в теплице при 22oC ± 2oC при относительной влажности 60 80%
Через 14 дней после обработки суспензией активного вещества определяют процент задержки развития грибка путем сравнения с необработанным контрольным образцом.
В этих условиях отмечают, что при концентрации 1 000 мг/л процент задержки развития грибка составляет по меньшей мере 75% для соединений: 5, 7, 9, 18, 22, 23.
Пример: тест in vivo на Puccina recondita, ответственном за ржавчину пшеницы. Пшеницу в горшках, засеянную в перегнойную почву, обрабатывают на стадии 10 см высоты путем пульверизации водными эмульсиями (названными пульпой) того же состава, что описан в предыдущем примере, с различными концентрациями исследуемого соединения. Испытание повторяют два раза с каждой концентрацией.
По истечении 24 ч водную суспензию спор (50000 спор на см3) распыляют на пшеницу: эту суспензию получают из зараженных саженцев. Затем помещают пшеницу на 48 ч в инкубационную камеру при примерно 18oC и с относительной влажностью 100%
По истечении этих двух дней относительную влажность доводят до 60% Проверку состояния саженцев осуществляют между 11 и 15 днем после заражения путем сравнения с необработанным образцом.
При дозе 1 г/л наблюдают защиту по меньшей мере на 75% при использовании соединений 1, 4, 6, 7, 10, 13, 19, 20, 28, 29.
Пример: тест in vivo на Piricularia oryzae, ответственном за пирикулариоз риса (Rice Blast). Рис в горшках, засеянный в смеси 50/50 обогащенного торфа и пуццолана, обрабатывают на стадии 10 см высоты путем распыливания вышеопределенной водной эмульсии (названной пульпой) с указанной концентрацией. Испытание повторяют два раза. По истечении 24 ч обрабатывают суспензией спор, полученных на чистой культуре, путем нанесения на листву.
В этом случае обработанные и зараженные таким образом растения помещают в инкубационную камеру при 25 28oC с насыщенной влажностью на 24 ч, затем во влажную камеру в теплице при 25 28oC.
Проверку осуществляют через 8 дней после заражения. В этих условиях, отмечают следующие результаты: при дозе 1 г/л защита по меньшей мере на 75% с использованием соединений 1, 2, 4, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 22, 23, 24, 29, 30, 32, 37, 38.


Использование: сельское хозяйство, в качестве вещества, обладающего фунгицидной активностью. Сущность изобретения: продукт формулы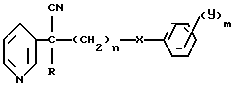 ,
,
где R - водород, метил, этил, изопропил, н-пропил, аллил; n = 1 или 2; x - атом кислорода или серы; y - хлор, бром, фтор; m = 1, 2, 3.
Реагент I:  .
.
Реагент II: (Hal)2CH2.
Реагент III: 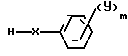 . Способ борьбы с грибковыми заболеваниями культур обработки листвы продуктом в количестве 0,03 - 1,0 кг/га. 2 с.п. ф-лы, 4 табл.
. Способ борьбы с грибковыми заболеваниями культур обработки листвы продуктом в количестве 0,03 - 1,0 кг/га. 2 с.п. ф-лы, 4 табл.

где R водород, метил, этил, изопропил, н-пропил, аллил;
n 1 или 2;
Х кислород или сера;
Y хлор, бром, фтор;
m 1, 2, 3,
проявляющие фунгицидную активность.
| ЕP, заявка, 0145260, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕP, заявка, 0214793, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ЕP, заявка, 0145620, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1997-10-27—Публикация
1989-03-28—Подача