Изобретение относится к катализатору на носителе для конверсии метана в этилен, к его приготовлению и к способу получения этилена с использованием указанного катализатора. Более конкретно изобретение относится к новому катализатору, который отвечает общей формуле (1), для реакции конверсии, к его приготовлению и к способу получения этилена прямой конверсией метана или метансодержащего газа в присутствии указанного катализатора.
Ma•Pc•D/S..........(1),
где
M обозначает металлический кластер или комплексное соединение металла, выбранного из групп VIII, VII и VI;
S обозначает неорганический носитель, такой, как SiO2;
P обозначает фосфорсодержащий промотор (соединение трехвалентного фосфора);
D обозначает соединение кобальта, такое, как CoCl2;
a обозначает количество массовых процентов металлического кластера или комплексного соединения металла в катализаторе, составляющее 0,01-10;
c- обозначает количество массовых процентов промотора в катализаторе, находящееся в интервале 1,0-35,0.
Обычно этилен широко используют в качестве одного из основных химикатов-реагентов в области нефтехимической промышленности и в тонкой химической технологии. Хорошо известно, что синтез этилена из метана дегидрогенизацией проводят при относительно высокой температуре, приблизительно 1500-1550oC, в процессах термического или электрического крекинга.
Однако осуществление такого метода сопряжено с некоторыми проблемами, такими, как потеря чрезмерных количеств тепловой энергии и потребность в высокотемпературном оборудовании, а также особенно сильная коррозия реакторная из-за высокой температуры.
В качестве примеров ранее описанного синтеза углеводородов реакцией окислительного сочетания и дегидрогенизацией с получением таких низших углеводородов, как этилен, содержащих двойную связь, прямой конверсией метана следует упомянуть патенты США 5066629, 5068486, 5118654, Канады 2016675 и Японии 04352730, 04368342.
Указанные способы в большей или меньшей степени обладают некоторыми недостатками, поскольку в них предусмотрено проведение реакции при относительно низкой температуре - примерно 700-800oC. Однако поскольку такую реакцию проводят в присутствии кислорода, гелия, азота и N2O в качестве газообразного окислителя или разбавителя, следствием является множество реагентов и большое количество таких побочных продуктов, как CO2. Более того, выделение или очистка реагентов сопряжена со многими затруднениями технологического порядка, не говоря о невозможности проведения непрерывного процесса и возникновения проблемы, связанной с загрязнением окружающей среды.
Между тем помимо метана в качестве основного компонента, природный газ содержит такие примеси, как двуокись углерода, H2S и влага. А эти примеси могут влиять на каталитическую активность и поэтому, если их не удалить, реакция не может протекать соответствующим образом.
С целью устранения указанных недостатков, связанных с упомянутыми способами, целью изобретения является, следовательно, разработка способа получения этилена с высоким выходом при проведении непрерывного процесса при относительно пониженной температуре в присутствии катализатора, без образования таких побочных продуктов, как двуокись углерода. Другой целью изобретения являет разработка способа прямой и непрерывной конверсии метана, содержащего некоторые примеси, в частности природного газа, в этилен. Еще одной целью изобретения является создание нового катализатора, используемого при осуществлении указанного способа, и способа его приготовления.
Для достижения упомянутой цели были проведены обширные исследования и было установлено, что катализатор конверсии может быть приготовлен следующим способом.
С помощью процесса прямой конверсии метана или метансодержащего газа в присутствии катализатора, отвечающего приведенной общей формуле (1), при 350-1050oC этилен с высоким выходом может быть получен без таких побочных продуктов, как двуокись углерода. Кроме того, упомянутый катализатор может быть приготовлен за счет проведения процесса путем добавления растворителя к компонентам по упомянутой общей формуле (1), суспендирования, перемешивания при приблизительно 20-200oC с обратным холодильником, выпаривания остатков перегонкой под пониженным давлением и сушкой в вакуумной сушилке.
Другими словами, катализатор для конверсии по изобретению используют при конверсии метана или метансодержащего газа в этилен, и он характеризуется тем, что отвечает общей формуле (1). Способ приготовления катализатора конверсии по изобретению характеризуется проведением следующего процесса, в котором к компонентам по общей формуле (1) добавляют растворитель, их суспендируют, перемешивают при приблизительно 20- 200oC с обратным холодильником, выпаривают остатки перегонкой под пониженным давлением и сушат в вакуумной сушилке. Способ получения этилена по данному изобретению характеризуется прямой конверсией метана или метансодержащего газа в этилен при 350-1050oC и под давлением 1-10 атм в присутствии упомянутого катализатора.
Катализатор по изобретению отвечает общей формуле (1). В указанной формуле (1) M обозначает металлический кластер или комплексное соединение такого металла, как Fe, Ru, Os, Co, Rh, Ir, Ni, Pd, Pt группы VIII, Mn, Re группы VII и Mo, W группы VI.
Так, например, класс таких соединений металла включает в себя RuCl2(PPh3)3, RuCl2(CO)2(PPH3)2, Ru3(CO)12, RhCl(CO)(PPh3)2, IrCl(CO)(PPh3)2, Pd(PPh3)4, Pt(PPh3)4, RuCl3•xH2O, RhCl3•H2O, IrCl3•xH2O, H2PtCl6•xH2O и PdCl2•xH2O. Среди них наиболее предпочтительными являются соединения металлов рядов Ru и Rh.
S обозначает неорганический носитель, в частности, α-Al2O3, γ-Al2O3, SiO2, SiO2-Al2O3, Y-цеолит, ZSM-5, цеолит, MgO и TiO2. Среди них наиболее предпочтительными соединениями являются α -Al2O3 и MgO. P служит промотором соединений трехвалентного фосфора, в частности, PPh3, P(OCH3)3, P(OC2H5)3 и P(O)(OC2H5)3. D обозначает такое соединение кобальта, как CoCl2•xH2O, Co(NO3)2•xH2O и Co(CH3COO)2•xH2O.
В том случае, когда метан содержит некоторые примеси, соединение кобальта используют для предотвращения снижения каталитической активности, а также предотвращения снижения выхода даже при отсутствии газообразного разбавителя, в частности, N2. В предпочтительном варианте его лучше всего использовать в интервале менее 0,3 мас.%. При превышении предела этого интервала происходит взаимное влияние с образованием химических связей между катализаторами, что может привести к снижению каталитической активности.
И a обозначает массовое процентное содержание металлического кластера или комплексного соединения металла в катализаторе, причем его величина равна 0,01-10, c обозначает массовое процентное содержание промотора в катализаторе, находящееся в пределах 1,0-35,0. Если величина a превышает указанный предел, это может вызвать уменьшение выхода, а если c превышает указанный предел, может произойти закупорка загрузочного или разгрузочного отверстия реактора.
Катализатор для конверсии по изобретению готовят с проведением следующих стадий:
(I) добавление указанных M, P, D и S в растворитель, такой, как дихлорметан или ацетон, при 20-200oC;
(II) смешение и суспендирование кипячением с обратным холодильником;
(III) сушка перегонкой под пониженным давлением.
Прямую конверсию метана или метансодержащего газа в этилен в присутствии упомянутого катализатора по изобретению проводят при нижеследующих реакционных условиях:
реакционная температура составляет 350- 1050oC, предпочтительно 650-950oC,
реакционное давление составляет 1-10 атм, предпочтительно 1-5 атм, и более предпочтительно давление равно нормальному,
концентрация катализатора равна менее 5,0 мас.%, предпочтительно 1,0-3,0 мас.%.
объемный расход исходного газа составляет 150-12000 см3/ч, предпочтительно 600-4800 см3/ч.
При выполнении способа по изобретению конверсия метана в этилен составляет приблизительно 15-20%, что меньше, чем при осуществлении упомянутых способов получения этилена, основанных на реакциях окислительного сочетания и дегидрогенизации, где она составляет 50-60%.
Однако по изобретению производительность дополнительно повышают благодаря возможности эффективного проведения непрерывной реакции конверсии без образования таких побочных продуктов, как двуокись углерода.
Даже в том случае, когда предназначенный для конверсии метан содержит некоторое количество примесей, по изобретению они могут не влиять на каталитическую активность. Таким образом, существенным преимуществом изобретения является возможность прямой конверсии природного газа в этилен без очистки.
Обычно массовое процентное содержание двуокиси углерода в природном газе в среднем равно 0-5%. При использовании катализатора конверсии по изобретению при содержании двуокиси углерода 0,2-1,0% стабильно достигаемая конверсия метана составляет 8,2-10,1%. А обычно массовое процентное содержание H2S в природном газе равно менее 1%. В случае применения катализатора по изобретению даже при содержании H2S в 1% стабильно достигается приблизительно 14%-ная конверсия метана.
Кроме того, природный газ может содержать небольшое количество влаги. В случае использования катализатора по изобретению даже в присутствии этой влаги стабильно достигаемая конверсия может составлять 8-12%. Другими словами, несмотря на присутствие любых примесей применение катализатора по изобретению позволяет достичь более, чем 10%-ной конверсии. Более того, без очистки в реакции конверсии может быть использован тот метан, который не подвергся конверсии при прохождении через реактор.
Ниже приведены примеры выполнения изобретения и даны определения указанных величин конверсии, выхода и селективности.
Величина конверсии (мол.%)=(число молей прореагировавшего метана/число молей введенного метана)•100
Выход (мол.%)=(число молей полученного низшего углеводорода/число молей введенного метана)•100
Селективность (мол. %)= (число молей полученного низшего углеводорода/число молей прореагировавшего метана)•100
Пример приготовления 1. Приготовление катализатора ряда Ru.
5,16 г α-Al2O3, 1,00 г (1,04 ммоля) RuCl2(PPh3)3, 1,09 г (4,16 ммоля) PPh3 и 0,01 г CoCl2•xH2O добавляли в смешанный растворитель из 20 мл дихлорметана и 10 мл ацетона и перемешивали в течение приблизительно 30 мин при примерно 40-60oC.
Эту суспензию, приготовленную по описанной процедуре, выпаривали перегонкой под пониженным давлением, а затем сушили в вакуумной сушилке в течение примерно 20 ч с получением катализатора RuCl2(PPh3)3•PPh3/α-Al2O3 (2 мас.% Ru).
Пример приготовления 2. Приготовление влагосодержащего катализатора ряда Ru.
1,0 г катализатора RuCl2(PPh3)3•PPh3/α-Al2O3 (2 мас.% Ru), приготовленного по примеру приготовления 1, погружали в 2 мл дистиллированной воды на несколько минут, а затем сушили 20 ч в вакуумной сушилке с получением влагосодержащего катализатора RuCl2(PPh3)3•PPh3•H2O/α-Al2O3 (2 мас.% Ru).
Пример приготовления 3. Приготовление катализатора ряда Ir.
Этот катализатор готовили аналогично изложенному в примере приготовления 1, за исключением того, что вместо 1,00 г RuCl2(PPh3)3 использовали 0,78 г IrCl(CO)(PPh3)2.
Пример приготовления 4. Приготовление катализатора ряда Rh.
Этот катализатор готовили аналогично изложенному в примере приготовления 1, за исключением того, что вместо 1,00 г RuCl2(PPh3)3 использовали 0,69 г RhCl(CO)(PPh3)2.
Пример приготовления 5. Приготовление катализатора ряда Pd.
Этот катализатор готовили аналогично изложенному в примере приготовления 1, за исключением того, что вместо 1,00 г RuCl2(PPh3)3 использовали 1,16 г Pd(PPh3)4.
Пример приготовления 6. Приготовление катализатора ряда Pt.
Этот катализатор готовили аналогично изложенному в примере приготовления 1, за исключением того, что вместо 1,00 г RuCl2(PPh3)3 использовали 1,24 г Pt(PPh3)4.
Пример 1. Метан без газообразного разбавителя вводили с расходом 600-2400 см3/ч в проточный реактор непрерывного действия с неподвижной фазой (внутренний диаметр 0,70 см, длина 40 см, материал - нержавеющая сталь марки 316) в присутствии катализатора, полученного по примеру приготовления 1.
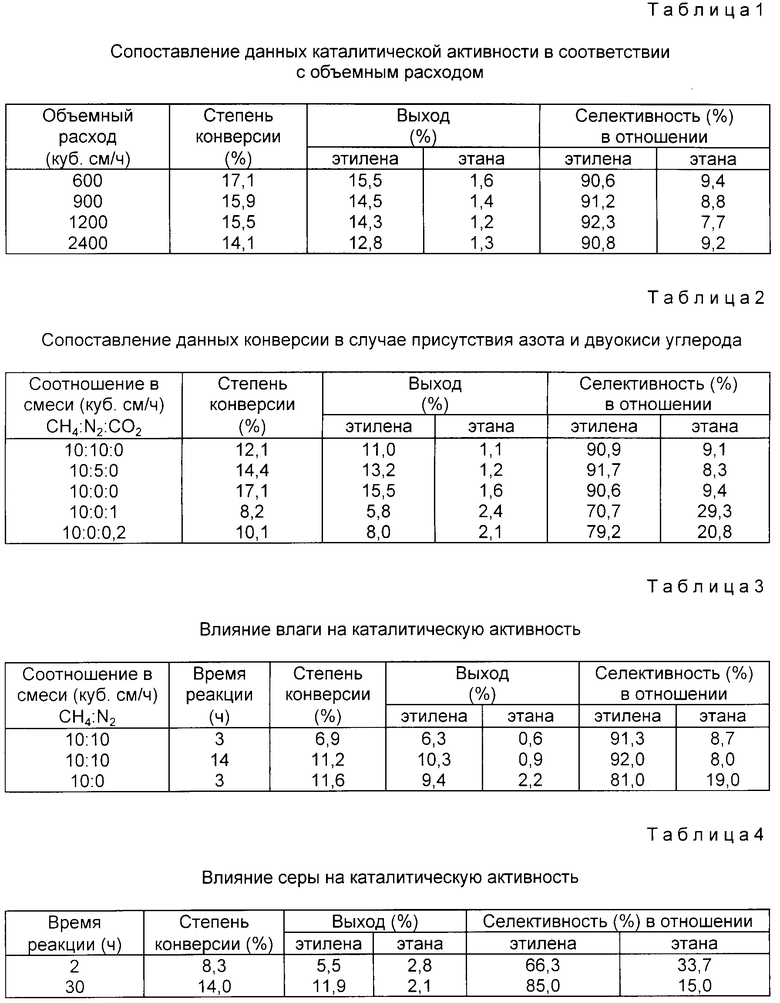
Продукты, полученные в ходе непрерывной реакции под давлением 1 атм и при температуре 810oC, анализировали газовой хроматографией; каталитическая активность представлена в табл. 1.
Пример 2. Для проверки различия результатов, достигаемых с использованием газообразного разбавителя и без использования газообразного разбавителя, и влияния двуокиси углерода, содержащейся в качестве примеси в природном газе, на каталитическую активность реакцию проводили аналогично изложенному в примере 1 путем подачи исходного газа при смешении метана, азота и двуокиси углерода в присутствии катализатора, полученного по примеру приготовления 1. Полученные результаты приведены в табл. 2.
Пример 3. Влияние влаги, содержащейся в природном газе, на каталитическую активность определяли согласно табл. 3 по результатам реакции, проведенной аналогично примеру 1, в присутствии катализатора, полученного по примеру приготовления 2.
Пример 4. Для проверки влияния соединения серы, содержащегося в природном газе, на каталитическую активность, реакцию проводили аналогично примеру 1 в присутствии катализатора, полученного по примеру приготовления 1. Результаты приведены в табл. 4.
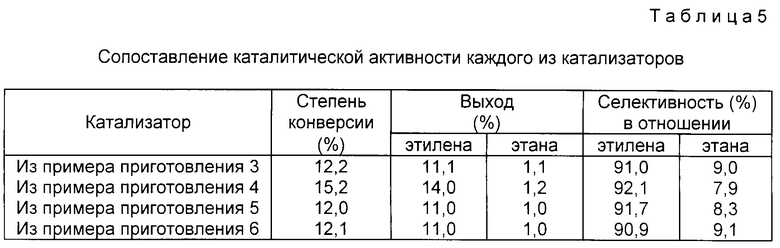
Пример 5. Влияние на каталитическую активность каждого из катализаторов, полученных по примерам приготовления 3-7, определяли согласно табл. 5, где представлены результаты реакции, проведенной по примеру 1, при объемном расходе 1200 см3/ч.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОРЫ НА НОСИТЕЛЯХ ДЛЯ КОНВЕРСИИ МЕТАНА ИЛИ ОЧИЩЕННОГО ПРИРОДНОГО ГАЗА, ИХ ПОЛУЧЕНИЕ И СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА С ИСПОЛЬЗОВАНИЕМ ЭТИХ КАТАЛИЗАТОРОВ | 1994 |
|
RU2106909C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ ЭТИЛЕНА, СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 1994 |
|
RU2113279C1 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ ИЗ МЕТАНА | 2007 |
|
RU2462444C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ МЕТАНА | 2007 |
|
RU2448079C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ И СИНТЕЗ-ГАЗА ИЗ МЕТАНА | 2007 |
|
RU2458899C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ МЕТАНА | 2007 |
|
RU2454389C2 |
| КАТАЛИЗАТОРЫ НА ОСНОВЕ БЛАГОРОДНЫХ МЕТАЛЛОВ И СПОСОБЫ РИФОРМИНГА МЕТАНА И ДРУГИХ УГЛЕВОДОРОДОВ | 2017 |
|
RU2777599C2 |
| ПОЛУЧЕНИЕ АЛКИЛИРОВАННЫХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2417974C2 |
| ПОЛУЧЕНИЕ ЖИДКИХ УГЛЕВОДОРОДОВ ИЗ МЕТАНА | 2005 |
|
RU2405764C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ ИЗ МЕТАНА | 2008 |
|
RU2491120C2 |
Изобретение относится к новому катализатору конверсии метана в этилен, его приготовлению и способу получения этилена с использованием указанного катализатора. Катализатор реакции конверсии при выполнении изобретения применяют для прямой конверсии метана или метансодержащего газа в присутствии указанного катализатора общей формулы (1):
Ma•Pc•D/S.......(1),
где M - металлический кластер или комплексное соединение металла, выбранного из групп VIII, VII и VI; S - неорганический носитель; P - промотор соединения трехвалентного фосфора; D - соединение кобальта и a - количество массовых процентов металлического кластера или комплексного соединения металла в катализаторе, составляющее 0,01-10; c - количество массовых процентов промотора в катализаторе, находящееся в интервале 1,0-35,0. 3 с. и 5 з.п. ф-лы, 5 табл.
Ma • Pc • D/S,
где M металлический кластер или комплексное соединение металла VIII группы Периодической системы;
P соединение трехвалентного фосфора;
D соединение кобальта в количестве менее 0,3 мас.
а количество металлического кластера или комплексного соединения металла VIII группы в катализаторе, составляющее 0,01 10,0 мас.
c количество соединения трехвалентного фосфора в катализаторе, составляющее 1 35 мас.
S неорганический носитель в количестве до 100 мас.
| EP, патент, 0205117, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1998-02-10—Публикация
1994-12-30—Подача