Предлагаемое изобретение относится к области органической химии, в частности к способу получения монохлорзамещенных производных адамантана и его гомологов (1-хлорадамантана, 1- и 4-хлордиамантанов).
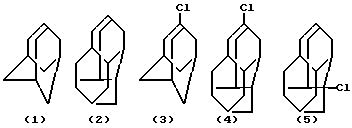
(1) - адамантан
(2) - диамантан
(3) - 1-хлорадамантан
(4) - 4-хлордиамантан
(5) - 1-хлордиамантан
Монохлорпроизводные адамантаноидов находят широкое применение в производстве термо- и хемостойких полимеров, служат исходным сырьем при получении лекарственных препаратов (Е.И.Багрий, Адамантаны. М.: Наука, 1989. С. 264. /1/; R.C.Fort, Adamantane: The Chemistry of Diamond Molecules. N.Y.: Dekker, 1976, 385 p. /2/) и используются в синтезе других производных адамантаноидов (амины, спирты, кислоты и т.д.).
Самым известным методом получения 1-хлорадамантана (3) является хлорирование адамантана с помощью свободного хлора путем инициирования реакции УФ-облучением (C.Walling, M.Magahi, J.Amer.Chem.Soc. 81, 1485 (1959) /3/; C. W.Smith, H.O.Williams, J.Org.Chem., 26, 2207 (1961) /4/; В.А.Некрасова, Н.И. Шуйкин. Изв.АН СССР, сер.хим., N 3, 714 (1969) /5/; H.Stetter, M.Krause, W. D.Last. Chem. Ber., 102, 3357-3363 (1969) /6/).
Селективность реакции по 1-хлорадамантану (3) при фотохимическом хлорировании при оптимальных условиях (в среде CCl4 или сероуглерода при комнатной температуре и продолжительности реакции 3 ч) составляет ~ 100% при общем выходе (3) 83% /5/.
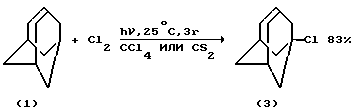
Способ получения хлорадамантанов фотохимическим методом хлора и адамантана имеет следующие недостатки:
1. Ввиду токсичности, летучести и высокой реакционной способности хлора метод является нетоксичным и экологически опасным.
2. Фотохимические реакции проходят исключительно в прозрачном стеклянном или кварцевом оборудовании. Объем этого оборудования обычно небольшой и строго лимитирован, следовательно, метод характеризуется низкой производительностью. 1-Хлорадамантан селективно можно получить хлорированием адамантана хлорсульфоновой кислотой (Б.И.Лерман, З.Я.Арефьева, А.Р.Кузыев, Г.А.Толстиков. Изв. АН СССР, сер.хим., N 4, 894 (1971) /7/). Реакция протекает при пониженных температурах (-5oC) с большим избытком хлорирующего реагента: мольное соотношение [AdH]:[ClSO2OH] = 1:8 - 1:10.
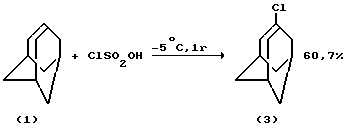
Данный метод имеет следующие недостатки:
1. Умеренный выход 1-хлорадамантана (3) - 60,7%.
2. Необходимость использования низких температур (-5oC).
3. Большой расход хлорирующего агента (8-10 кратный избыток).
4. Агрессивность и высокая коррозионная активность хлорсульфоновой кислоты и продуктов ее гидролиза (HCl, H2SO4).
5. Выделение целевого продукта из-за использования избытка (мольное соотношение /кислота/:/адамантан/ = 8:1) хлорсульфоновой кислоты представляет большие сложности. Метод препаративно неудобен, т.к. избыток кислоты необходимо разложить и нейтрализовать (водой, NaHCO3, Na2CO3) при низкой температуре. Перегонка с использованием нагрева неприменима из-за возможности дальнейшего хлорирования адамантана.
Что касается известных в литературе методов получения монохлорпроизводных гомологов адамантана (диамантана, триамантана), то синтез 1- и 40-хлордиамантанов (4,5) (в виде смеси изомеров в соотношении 1:1) был осуществлен путем взаимодействия полициклического углеводорода тетрагидробинора-S (6) (имеет такой же углеводородный состав, что и диамантан) с хлористым ацетилом в растворе дихлорметана в присутствии эквимолярного количества AlCl3 при 0oC в течение 12-22 ч. (D.Faulkner, R.A.Glendinning, D.E.Johnston, M. A. McKervey. Tetrahedron Letters., N 20, 1671 (1971) /8/; T.Courthey, D.E. Johnston, M. A. McKervey, J.J.Rooney, J.C.S.Perkin 2691 (1972) /9/). (Такой метод известен и для адамантана (I.Tabysi, J.Hamuro, R.Oda. J.Chem.Soc.Japan. Pure. Chem. Soc. 1968, 89, N 8, 794-797, A 46.. РЖХим. 1969, 9ж 175. /10/). Общий выход (4,5) при этом составил 80% /8, 9/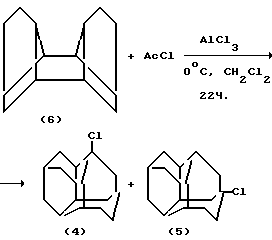
Данный метод, несмотря на высокий выход целевых продуктов, имеет ряд существенных недостатков:
1. Необходимость использования пониженных температур, что осложняет технологическое оформление процесса.
2. Применение в качестве флорирующего агента дефицитного хлористого ацетила является неоправданным, т.к. его необходимо получить путем хлорирования уксусной кислоты с помощью PCl3, PCl5 или хлористым тионилом (Г.Либ, В.Шенигер "Синтез органических препаратов из малых количеств веществ ". Госхимиздат, 1957, Л. , с. 53). PCl5, PCl3, SOCl2, сами являются хлорирующими реагентами (они используются для хлорирования адамантана (H.Stetter, M. Krause, W. -D. Last, Angew.Chem., 80, N 22, 970-971 (1968) /11/; G.Ola, P. Schilling, R.Renner, J.Kerekes, J.Org.Chem. 1974, 39, 3472-3476 /12/), следовательно их использование для введения хлора в адамантан по существу является лишней стадией и нецелесообразно.
3. Значительная продолжительность реакции (22 ч).
4. Большой расход катализатора AlCl3 и связанные с этим проблемы образования значительного количества трудноутилизируемых отходов (AlCl3•6H2O, Al(OH)3, HCl).
Для получения 1- и 4-хлордиамантанов можно использовать хлорсульфоновую кислоту /9/
Несмотря на высокий выход (4,5) это метод практически неприемлем для препаративных целей, т.к. требует чрезвычайно большого расхода агрессивного хлорирующего агента - хлорсульфоновой кислоты (мольное соотношение /диамантан/: /хлорсульфоновая кислота/ = 1:58) и низких температур. Применение большого избытка ClSO2OH создает большие трудности при выделении целевых продуктов. В соответствии с указанной методикой перед выделением 1- и 4-хлордиамантов реакционная масса выливается на лед. При этом хлорсульфоновая кислота гидролизуется с образованием HCl и H2SO4, водный раствор которых является отходом производства, а целевые 1- и 4-хлордиамантаны (4,5) экстрагируют эфиром из высококонцентрированного водного раствора серной и соляной кислот. Эта операция является опасной, ее следует проводить в стеклянном оборудовании или в аппаратуре из специальных сортов сталей.
Известен метод получения индивидуальных 1- и 4-хлордиамантонов (4, 5) соответственно из 1-диамантанола (7) и 4-диамантанола (8) путем их хлорирования с помощью хлористого тионила /12/.
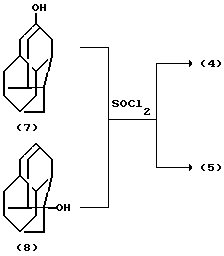
Однако данный метод весьма сложно использовать для синтеза значительных количеств (4,5), т.к. исходные спирты сами были получены из хлоридов (4,5) и разделены с помощью высокоэффективной жидкостной хроматографии /9/.
Немецкими учеными разработан метод получения хлорпроизводных адамантана (в том числе и 1-хлорадамантана (3) путем хлорирования адамантана с помощью четыреххлористого углерода, который выполняет две функции, одновременно являясь хлорирующим агентом и средой /6, 11/. Реакция хлорирования адамантана с помощью CCl4 является каталитической и осуществляется в присутствии кислот Льюиса, предпочтительно AlCl3 /11/. Данная реакция протекает неселективно с образованием смеси 1-хлор- и 1,3-дихлорадамантанов (3), (9) с преобладанием последнего. Процесс проходит в мягких условиях (20o, 4 ч), но с большим избытком катализатора AlCl3, который берут в эквимолярном количестве по отношению к адамантану.
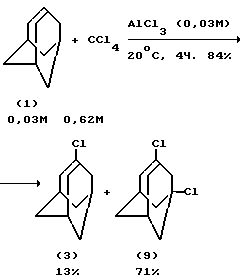
Выход целевого 1-хлорадамантана (3) составляет 13%. При замене AlCl3 на другой катализатор FeCl3/K10 (хлорное железо, нанесенное на катионит) селективность реакции по 1-хлорадамантану снижается до 2% (P.Kovacic, J.-H. Chen Chang. J.Org.Chem., 36, 3138 (1971) /13/).
На основании общности трех признаков (одинаковые реагенты: адамантан и сходный по свойствам с CCl4 хлороформ, использование катализатора, образование в результате реакции 1-хлорадамантана) за прототип взят метод хлорирования адаманатана с помощью CCl4 под действием AlCl3 /11/.
Прототип имеет следующие недостатки:
1. Низкий выход 1-хлорадамантана (13%).
2. Большой расход катализатора (AlCl3 используется в эквимолярном количестве по онтошению к адамантану).
3. Большой расход AlCl3 создает целый ряд проблем. Так, сильно усложняется процедура выделения и очистки целевого продукта. Для выделения 1-хлорадамантана после окончания процесса в реактор добавляется вода (или раствор HCl). Оба этих реагента очень энергично реагируют с безводным AlCl3, (образование кристаллогидрата AlCl3•6H2O сопровождается выделением большого количества тепла). При гидролизе выделяется свободная HCl, которая способствует коррозии аппаратуры.
4. Образуется значительное количество неорганических отходов (AlCl3•6H2O, Al(OH), HCl) и сточных вод, которые необходимо переработать (нейтрализовать), что требует больших трудо- и энергозатрат.
5. Процесс в целом является нетехнологичным и дорогим, большой расход катализатора, образование отходов, наличие дополнительной технологической стадии по разложению реакционной массы, невозможность повторного использования AlCl3 и CCl4, которые либо гидролизуются, либо загрязняются водой.
Авторами предлагается способ хлорирования адамантаноидов, свободный от указанных недостатков.
Сущность способа заключается в хлорировании адамантаноидов с помощью хлороформа под действием катализаторов: солей и комплексов металлов, таких как FeBr2, Fe(acac)3, NiBr2, Ni(acac)2, CrCl3, Cr(acac)3, CoCl2, CoBr2, Co(acac)2, Co(acac)3, предварительно активированных при 200oC 3, ч, в инертной атмосфере, в среде CHCl3, в герметичном автоклаве.
В оптимальных условиях (200oC, 6 ч, при мольном соотношении [AdH]:[K]: [CHCl3] = 1:0,01:3 - 17) выход 1-хлорадамантана (3) достигает 77%, 1- и 4-хлордиамантанов (4,5) - 75%.
Процесс отличается высокой селективностью по монохлорадамантаноидам, замещенным в узловых положениях (отсутствуют примеси дихлорзамещенных и замещенных в мостиковых положениях атомов углерода адамантаноидных структур).

Существенные отличия предлагаемого способа от прототипа.
1. Хлорирующим агентом служит хлороформ. Это тем более примечательно, т. к. из литературы известно, что взаимодействие адамантана с хлороформом сопровождается образованием не 1-хлорадамантана (3), а 1-дихлорметиладамантана (10) (J. Tabushi, L.-i.Voshida, N.Takahashi. J.Amer.Chem.Soc., 92, 6670 (1970) /14/).
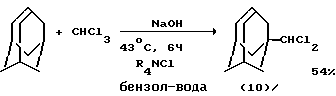
При использовании в качестве катализаторов комплексов Fe, Ni и Co направление реакции между адамантаном и хлороформом изменяется самым радикальным образом и проходит с образованием 1-хлорадамантана (3) с высоким выходом.
2. Для получения хлорадамантноидов хлорированием с помощью хлороформа используются новые дешевые и доступные катализаторы на основе соединений железа, никеля, кобальта и хрома.
3. Если в известном методе хлорирования катализатор используется в эквимолярном количестве, то в предлагаемом - только 0,01 молей по отношению к адамантану (или диамантану).
Преимущества предлагаемого метода.
1. Высокий выход целевого продукта и высокая селективность процесса по монохлорзамещенным производным адамантана и даиамантана.
2. Небольшой расход катализатора.
3. Упрощение технологии выделения целевого продукта из-за отсутствия стадии разложения катализатора разбавлением реакционной массы большим количеством H2O.
4. Доступность и дешевизна используемых катализаторов.
5. Уменьшение количества отходов из-за небольшого расхода катализаторов.
6. Уменьшение трудо- и энергозатрат, экологическая безопасность процесса.
Способ поясняется примерами:
Пример 1. Реакции проводили в стеклянной ампуле (V= 0,015 л) или в стальном микроавтоклаве (V = 0,017 л) (результаты параллельных опытов практически не отличается).
В стеклянную ампулу помещали 0,02 ммолей катализатора FeBr2, 0,27 г (2 ммолей) адамантана, 0,5-3 мл CHCl3. Ампулу запаивали и нагревали на масляной бане в течение 6 часов, 200oC.
После окончания реакции ампулу охлаждали до комнатной температуры, вскрывали, реакционную массу фильтровали через слой Al2O3 (2 г). Непрореагировавший CHCl3 отгоняли, остаток перегоняли в вакууме с воздушным холодильником (78-85oC/1 мм) - при этом происходит возгонка 1-хлорадамантана. Выделенный 1-хлорадамантан, перекристатллизованный из метанола, имел to пл. 164-165oC (лит.данные 163-164oC) /3-8/.
Получено 0,208, выход 77%.
Пример 2. В стеклянную ампулу V=0,015 л помещали 0,02 ммолей катализатора Ni(acac)2, 2 ммолей диамантана, от 0,5 до 3 мл CHCl3. Ампулу запаивали и нагревали на масляной бане в течение 6 ч, 200oC. После окончания реакции ампулу охлаждали до комнатной температуры, вскрывали, реакционную массу фильтровали через Al2O3 (2 г) непрореагировавший CHCl3 отгоняли, остаток перекристаллизовывали в ацетоне для удаления непрореагировавшего диаманатана. Выход хлордиамантанов составлял 75%. Разделение изомеров проводилось методов жидкостной хроматографии. Соотношение 1- и 4-хлордиамантанов примерно 45 - 55.
1-хлордиамантан: to пл. = 250-252oC, νmax = 1068, 972, 881, 808, 719 см-1, спектр ЯМР13C в CDCl3: 24,86 д; 30,47 д; 33,11 т; 36,89 д; 37,24 д; 37,89 т; 40,56 д; 44,66 д; 49,17 т; 76,26 с.
4-хлордиамантан: to пл = 75-76oC, νmax = 1078, 1069, 1049, 1044, 983, 969, 850, 829, 797, 708, 529 см-1. Спектр ЯМР 13C 25,02 д; 35,11 д; 40,22 д; 36,66т; 47,78 т; 67,16 с.
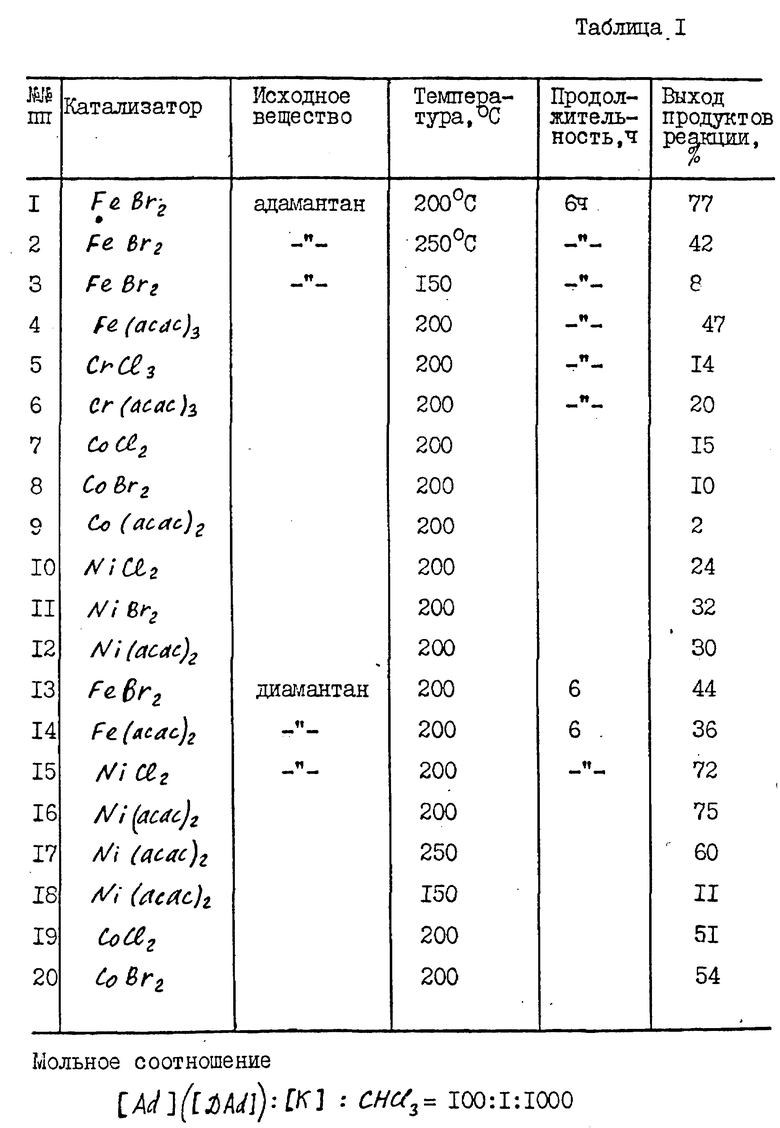
По этой же методике были проведены все остальные опыты, в том числе с использованием других катализаторов. Результаты этих опытов приведены в табл. 1.
Оптимальной является температура 200oC, при более низкой to значительно снижается конверсия исходного вещества, при более высокой возрастает образование смолистых продуктов реакции. При 200oC оптимальным является время реакции 6 ч. Для большинства катализаторов в таблице приведены результаты реакции только в оптимальных условиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ 1-ХЛОР- И 1,3-ДИХЛОРАДАМАНТАНОВ | 1996 |
|
RU2125551C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА, 1- И 4-ХЛОРДИАМАНТАНОВ | 2000 |
|
RU2185364C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА | 1996 |
|
RU2126784C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИХЛОРАДАМАНТАНА | 2000 |
|
RU2178401C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1- И 2-ХЛОРАДАМАНТАНОВ ИЗ 1- И 2-АДАМАНТАНОЛОВ | 2000 |
|
RU2178400C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА | 2011 |
|
RU2486169C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИХЛОРАДАМАНТАНА | 2011 |
|
RU2459797C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИРОВАННЫХ ПРОИЗВОДНЫХ ПОЛИБУТАДИЕНОВОГО И ПОЛИИЗОПРЕНОВОГО КАУЧУКОВ | 1997 |
|
RU2142962C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРПРОИЗВОДНЫХ ФУЛЛЕРЕНА C | 1998 |
|
RU2160226C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИ-1-АДАМАНТИЛОВОГО ЭФИРА | 1998 |
|
RU2147571C1 |
Изобретение относится к способам хлорирования органических соединений, в частности к получению монохлорзамещенных производных адамантана или диамантана каталитическим хлорированием соответствующих исходных соединений при температуре 150-250oC. Хлорирование ведут с помощью хлороформа в присутствии катализатора, выбранного из группы FeBr2, CoBr2, Co(асас)2CoCl2, NiCl2, NiBr2, Ni(acac)2, CrCl3, Cr(acac)3, в течение 6 ч при мольном соотношении адамантан (диамантан): катализатор : хлороформ = 100 : 1 : 1000. В результате снижается расход катализатора, уменьшается количество побочных продуктов и упрощается технология процесса. 1 табл.
Способ получения монохлорзамещенных произвольных адамантана и диамантана каталитическим хлорированием при повышенной температуре, отличающийся тем, что хлорирование ведут с помощью хлороформа в присутствии катализатора, выбранного из группы FeBr2, Fe(acac)3, CoBr2, Co(acac)2, CoCl2, NiCl2, NiBr2, Ni(acac)2, CrCl3, Cr(acac)3 при температуре 150 - 250oC в течение 6 ч при мольном соотношении адамантан (диамантан) : катализатор : хлороформ = 10 : 1 : 1000.0
| H.Stetter, M.Krause, W.D.Last, Angew | |||
| Chem., 1968, v.80, N 22, p.970-971 | |||
| CS 208270 A, 1981 | |||
| GB 1213761 A, 1970 | |||
| В.А.Некрасова, Н.И.Шуйкин | |||
| Изв | |||
| АН СССР | |||
| Серия "Химия" | |||
| Приспособление к индикатору для определения момента вспышки в двигателях | 1925 |
|
SU1969A1 |
Авторы
Даты
1999-01-27—Публикация
1996-12-05—Подача