Изобретение относится к области медицины, а именно к диагностическим способам, и может быть использовано для скрининговой диагностики онкологических заболеваний.
Известен способ диагностики онкологических заболеваний, основанный на селективном накоплении в опухолях флюорохрома и регистрации его спектра флюоресценции ("Верификация опухолей с помощью лазерной флюоресцентной спектроскопии", А.И.Гордиенко и др., Материалы VIII съезда онкологов УССР, Донецк, 1990 г., с. 183-184).
Известен способ лазерной спектроскопии в диагностике хронических, предопухолевых и опухолевых патологий, при котором спектроскопии подвергают срез ткани (Актуальные проблемы современной онкологии, Томск, 1994 г., с. 37-38).
По совокупности существенных признаков наиболее близким к изобретению аналогом является способ диагностики онкологических заболеваний, включающий исследования плазмы крови методом лазерной корреляционной спектроскопии (ЛКС) (К. И. Мерлич и др., "Субфракционный состав плазмы крови при доброкачественных опухолях и раке молочной железы по данным лазерной корреляционной спектроскопии", Бюллетень экспериментальной биологии и медицины, 1993 г., N 8, с. 193-195).
В данной работе экспериментально показана принципиальная возможность диагностики онкологических заболеваний (на примере рака молочной железы) методом динамического рассеяния света раствором исследуемой плазмы крови. При этом отмечается, что у онкологических больных по сравнению с другими пациентами в распределениях частиц по размерам наблюдается сдвиг распределения в область более мелких частиц с размерами порядка 10-12 нм.
Физическая сущность данного известного способа заключается в следующем (Лебедев А.Д. и др. Лазерная корреляционная спектроскопия в биологии. Киев, 1987 г.).
В простейшем случае раствора малых по сравнению с длиной волны падающего света оптически изотропных тождественных частиц автокорреляционная функция и спектральная плотность сигнала динамического рассеяния света имеют вид
G(τ) = Ae-Г(τ) (1)
S(ω) = [AГ2/π]/[(ω0-qV)2-Г2], (2)
где Г = Dtq2 - диффузионное уширение;
Dt - коэффициент трансляционной диффузии;
τ - радиус корреляции;
q = 4π(n0/λ)sin(θ/2) - волновой вектор;
n0 - показатель преломления растворителя;
λ - длина волны падающего света, а ωo - - соответствующая ей частота;
θ/2 - угол наблюдения рассеянного света (=90o);
qV - доплеровское смещение длины волны падающего света на частицах, перемещающихся в процессе трансляционной диффузии;
A - амплитуда (интенсивность) флуктуаций светорассеяния, соответствующая диффузионному уширению Г.
Коэффициент трансляционной диффузии Dt связан с гидродинамическим радиусом Rh рассеивающих частиц соотношением Стокса-Энштейна:
Г = [KT]/[6πξRh], (3)
где K - постоянная Больцмана;
T - абсолютная температура;
ξ - вязкость раствора.
Исходя из этого, оценка распределения макромолекул по размерам в исследуемой плазме крови производится в соответствии с соотношением
N(R) = [AГ(Rh)]/[R
где N(Rh) - количество молекул с гидродинамическим радиусом Rh;
AГ(Rh) - амплитуда (интенсивность) флуктуаций динамического рассеяния света, соответствующая диффузионному уширению Г(Rh);
m - параметр, учитывающий форм-фактор рассеивающих молекул раствора: m=3 - для "глобулярных частиц", m=2 - для "сфер и гауссова клубка".
Существенным недостатком данного подхода является то обстоятельство, что он корректен только для броуновской модели диффузионных процессов, когда коэффициент трансляционной диффузии определяется тепловой энергией KT - без учета достаточно сильного электростатического взаимодействия поверхностно заряженных макромолекул белков, энергия которого может многократно превышать тепловую энергию KT. Электростатическое взаимодействие между макромолекулами влияет на динамику их броуновского движения в растворе, что порождает сдвиг в оценке диффузионного уширения Г, что, в свою очередь, приводит к погрешности в оценке Rh (см. выражение (3)).
Другим недостатком известных методов (в том числе и ближайшего аналога-прототипа) является низкая точность вследствие того, что перед исследованиями образцы исходного биоматериала подвергают специальной обработке, так, например, в прототипе плазму крови замораживают и проводят двойное центрифугирование (при 1500q), что приводит к изменению физических параметров белков плазмы крови. Другим существенным недостатком известных методов является то, что диагностика проводится всего лишь по одному диагностическому признаку.
Известно устройство для реализации способа-прототипа, содержащее последовательно установленные нефелометр и корреляционный спектральный анализатор. Ему присущи все недостатки, которые присущи описываемым ранее способам.
Технический результат, достигаемый изобретением, заключается в определении параметров межмолекулярного взаимодействия белков нативной плазмы крови.
Сущность изобретения заключается в достижении упомянутого технического результата в способе диагностики онкологических заболеваний, включающем исследование плазмы крови методом лазерной корреляционной спектроскопии (ЛКС), в котором для исследования берут слабый раствор нативной плазмы крови, определяют спектральную плотность флуктуаций интенсивности светорассеяния в полосе частот 1-1000 Гц, выявляют спектральное ядро и диагностику проводят по частоте максимума огибающей спектрального ядра и отношению его интенсивности к его полуширине и при значении диагностических параметров ниже соответствующих норм диагностируют онкологическое заболевание, при этом в устройстве для диагностики онкологических заболеваний, содержащем последовательно установленные нефелометр и корреляционный спектральный анализатор, в нефелометр дополнительно введены второй приемник рассеянного света, расположенный симметрично относительно первого, перемножитель сигналов, входами подключенный к выходам первого и второго приемников рассеянного света, фильтр нижних частот, входом подключенный к выходу перемножителя сигналов, а выходом - к коррелятору спектрального анализатора, при этом в качестве измерительной кюветы нефелометра используется стандартная ампула для растворителя.
В настоящем изобретении для определения характеристических молекулярных параметров плазмы крови используется метод динамического рассеяния света разбавленными растворами нативной плазмы крови, приготовленного по стандартной технологии - как для биохимического анализа крови.
Теоретические и экспериментальные исследования данного метода показали, что усредненная спектральная плотность флуктуаций интенсивности светорассеяния тестируемым раствором позволяет выделить характеристическое спектральное ядро, специфика которого может быть представлена частотой максимума огибающей, интенсивностью центра тяжести и полушириной спектрального ядра. При этом у онкологических больных значения частоты максимума и интенсивности меньше, а полуширина больше по сравнению с значениями соответствующих параметров, характерными для неонкологических больных и практически здоровых лиц.
Это обусловлено следующими факторами.
В формировании клеточного состава крови участвуют самые различные органы и системы человеческого организма: печень, костный мозг, лимфатические узлы, селезенка и др. Как известно, кровь состоит из плазмы - 55 вес.% и взвешенных в ней форменных элементов - 45 вес.%: эритроцитов, лейкоцитов, кровяных пластинок. Плазма крови содержит макромолекулы альбумина и глобулинов, фибриногена.
В здоровом организме клеточный состав крови и кроветворные органы образуют сбалансированную биосистему, в которой происходит непрерывный авторегулируемый процесс замены состарившихся клеток крови на новые.
Любые изменения в организме вызывают нарушение этого равновесия, что сразу же отражается на состоянии крови. Различные заболевания, яды, канцерогенные вещества, ионизирующая радиация, воспалительные процессы и т.п. вызывают нарушения процесса кроветворения и приводят к синтезу структурно измененных, незрелых форменных элементов. В результате изменяется состав крови и молекулярные параметры входящих в нее белков, что, в принципе, может быть использовано для диагностических целей. Поэтому основной проблемой при разработке методов диагностики различных заболеваний является определение таких параметров крови, которые с наибольшей вероятностью позволяют различить здорового и больного данным заболеванием пациента. В этой связи представляют интерес специфические изменения непосредственно в макромолекулах плазмы крови при возникновении онкологических заболеваний.
При развитии канцерогенеза в плазме (сыворотке) крови происходят как количественные, так и качественные изменения, практически не зависящие от вида заболевания.
Во-первых, изменяются абсолютные и относительные значения концентраций молекул альбумина и глобулинов. Если у здорового человека концентрация молекул альбумина в три-четыре раза превышает концентрацию глобулинов, то при канцерогенезе отношение концентраций уменьшается и затем меняется на обратное: концентрация макромолекул глобулинов у онкологических больных становится много больше концентрации молекул глобулинов. Следует также иметь в виду, что на развитых стадиях канцерогенеза в плазме крови происходит уменьшение абсолютного значения концентраций макромолекул альбумина и глобулина.
Во-вторых, у молекул альбумина происходят качественные изменения в величине и распределении поверхностного заряда. Молекулы альбумина имеют веретенообразную структуру длиной (80-100)A и около (15-20)A в диаметре центральной части, обладают значительным электрическим дипольным моментом, который может достигать сотен дебай, имеют отрицательный заряд, расположенный в ее поверхностном слое. Причинами возникновения поверхностного заряда являются незаполненные химические связи и сильное сродство к электрону у поверхностных атомных комплексов.
При канцерогенезе происходит уменьшение заряда, что является следствием, с одной стороны, синтеза (по-видимому печенью) и появлением в крови положительно заряженных специфических ингибиторов, присоединяющихся к молекуле альбумина, и, с другой стороны, изменением химического состава поверхностных атомных комплексов.
Изменения в распределении поверхностного заряда у макромолекул альбумина существенным образом меняет характер их взаимодействия в растворе плазмы (сыворотке) крови. При этом преобладающие силы отталкивания (что характерно для состояния плазмы крови пациентов, не имеющих онкологических заболеваний) постепенно трансформируются в силы притяжения (что характерно для состояния плазмы крови онкологических больных пациентов). В результате этого происходит коагуляция молекул альбумина с образованием различных пространственных конфигураций, со значительно большим молекулярным весом.
В-третьих, при канцерогенезе происходит окисление многих клеточных мембран, что, в свою очередь, ведет к изменению физических свойств липопротеинов, а также снижению защитной реакции иммунной системы.
В-четвертых, при канцерогенезе в плазме крови появляются парапротеины и различные фракции альбумина с отличными молекулярными весами и зарядовыми характеристиками, а также происходит разрушение дисульфидных связей цистина в молекулах иммуноглобулина, тем самым разрушаются внутрицепочные связи и третичная структура денатуризируется, превращаясь в первичную. Наличие фрагментов молекул Ig является строгим маркером злокачественного процесса.
В-пятых, развитие канцерогенеза часто сопровождается нарушением водно-электролитного обмена, связанного с распадом опухолевой массы и выходом внутриклеточных элементов (калий, магний, фосфор, сера) во внеклеточное пространство и с потерей их с мочой, а также может сопровождаться сдвигами в кислотно-щелочном состоянии.
При неонкологических заболеваниях изменения в плазме крови происходят только в определенных пределах. Действительно, при развитии неонкологических заболеваний возникают нарушения в работе кроветворных органов, меняется состав плазмы крови, но одновременно с этим вступают в действие механизмы иммунной защиты (интенсивно синтезируются антитела, активизируются ферментные системы, усиливается репродукция ингибиторов вирусов и т.п.), которые подавляют дальнейшее развитие заболевания и ограничивают изменения параметров крови. При этом возникающие по разным причинам раковые клетки эффективно уничтожаются иммунными системами организма.
При онкологических заболеваниях раковые клетки синтезируют антигены с крайне низкой иммуногенностью. Поэтому раковые антигены не вызывают столь необходимую иммунную защитную реакцию. В этой связи неограниченное увеличение числа раковых клеток вызывает непрерывный рост концентрации токсинов в организме, в результате чего, рассмотренные выше, изменения в крови непрерывно возрастают и могут во много раз превышать предельные значения этих изменений при неонкологических заболеваниях. Возникновение онкологических заболеваний с наибольшей вероятностью возможно на этапе значительного и достаточно длительного отклонения иммунных систем и других органов человека от нормального функционирования, т.е. когда изменения параметров плазмы крови достигает определенного критического уровня.
Отсюда следует возможность разделения параметров плазмы крови на три смежные области, характеризующие практически здоровых, больных неонкологическими заболеваниями и онкологических больных пациентов. Когда изменения параметров плазмы крови приближаются к предельным значениям, разделяющим больных обычными заболеваниями и онкологических больных (зоны риска), у исследуемого пациента возникает угроза развития онкологического заболевания. В этом случае необходимо определить динамику этих изменений во времени - смещаются ли параметры плазмы крови в сторону онкологических больных или, наоборот, происходит их нормализация, что указывает на неонкологическую природу заболевания.
Рассмотренные выше изменения молекулярных параметров плазмы крови существенным образом влияют на характер броуновской динамики диффузионных процессов, наблюдаемых в исследуемых растворах плазмы крови, где диссипация энергии в диффузионных процессах определяется диполь-дипольными и диполь-зарядовыми межмолекулярными взаимодействиями, энергия которых может многократно превышать тепловую энергию KT. При этом реализуется так называемый механизм диэлектрического трения.
В этой связи в качестве диагностических признаков используются частота максимума (maxF) и отношение интенсивности (I) к полуширине (dF) огибающей спектрального ядра сигнала светорассеяния раствором тестируемой плазмы крови.
Предлагаемый способ диагностики реализуется следующим образом.
Кровь для получения плазмы крови берется у обследуемых пациентов из вены утром после сна натощак.
Приготавливается образец слабого раствора плазмы крови.
Используя последовательно включенные лазерный нефелометр и корреляционно-спектральный анализатор, получают сигнал флуктуаций интенсивности светорассеяния, который подвергают узкополосной спектральной обработке в диапазоне частот (1-1000) Гц.
Выделяют спектральное ядро и производят оценку численных значений: частотного положения его максимума - maxF, а также отношения интенсивности к его полушарию - I/dF.
При значениях диагностических показателей ниже соответствующих норм диагностируют онкологическое заболевание.
Устройство для реализации данного метода представляет собой последовательно включенные лазерный нефелометр, включающий в себя лазерный источник света, измерительную кювету для размещения тестируемого раствора биологической жидкости, первый первичный измерительный преобразователь рассеянного света в аналоговый сигнал - первый приемник света, расположенный под углом 90o к лазерному лучу, и корреляционно-спектральный анализатор наблюдаемого сигнала светорассеяния, содержащий последовательно включенные стандартные автокоррелятор и фурье-преобразователь с встроенным микропроцессором вторичной обработки спектрограмм, где, с целью улучшения отношения сигнал/шум на входе корреляционно-спектрального анализатора, в нефелометр дополнительно введены второй первичный измерительный преобразователь рассеянного света в аналоговый сигнал - второй приемник света, размещенный по другую сторону под углом 90o к лазерному лучу, а также перемножитель сигналов с выходов первого и второго первичных измерительных преобразователей, своим выходом подключенный к входу фильтра нижних частот, выход которого подключен к входу коррелятора.
Функциональная схема устройства, реализующая данный способ диагностики, представлена на чертеже, где обозначено:
1 - лазерный нефелометр;
2 - корреляционно-спектральный анализатор;
3 - лазерный источник света;
4 - измерительная кювета;
5 - первый первичный измерительный преобразователь рассеянного света в аналоговый сигнал - первый приемник света;
6 - коррелятор;
7 - фурье-преобразователь;
8 - микропроцессор;
9 - дополнительно введенный второй первичный измерительный преобразователь рассеянного света в аналоговый сигнал - второй приемник света;
10 - дополнительно введенный перемножитель сигналов;
11 - дополнительно введенный фильтр нижних частот.
Устройство работает следующим образом.
Рассеянный раствором тестируемой биологической жидкостью свет одновременно попадает на входы первого 5 и второго 9 приемников света, где преобразуются в аналоговые сигналы, которые поступают на первый и второй входы перемножителя сигналов 10. Перемножитель сигналов 10 с последовательно присоединенным фильтром нижних частот 11 образуют двухканальный корреляционный детектор. Наличие двух высокочастотных каналов с одним и тем же полезным сигналом и некоррелированнными внутренними шумами каналов позволяет получить выигрыш в отношении сигнал/шум при детектировании не менее чем в 1,4 раза по сравнению с квадратичным детектором (Поиск, обнаружение и измерение параметров сигналов в навигационных системах. Москва, "Советское радио", 1975 г., стр. 40-41). После детектирования сигнал с улучшенным отношением сигнал/шум поступает на вход коррелятора 6, где вычисляется автокорреляционная функция флуктуаций интенсивности светорассеяния, обусловленных изменением во времени оптической плотности в рассеивающем объеме, задающем лучем лазерного источника света 3 в измерительной кювете 4. Автокорреляционная функция, отражающая во временной области характер динамики молекул в тестируемом растворе, с выхода коррелятора 6 поступает в фурье-преобразователь 7, обеспечивающий получение спектральной плотности динамики светорассеяния. С выхода фурье-преобразователя 7 спектральная плотность поступать в микропроцессор 8, где осуществляется выделение спектрального ядра и определение его характеристических параметров: частотного положения максимума, интенсивности и полуширины, а также определение диагностических параметров, которые затем сравниваются с соответствующими нормами. При значениях диагностических показателей ниже соответствующих норм: (NORMA1/maxF > 1 и (NORMA2/(I/dF) > 1), диагностируют онкологическое заболевание. В отличие от известных схем построения нефелометров данное устройство содержит 2 (вместо одного) приемника света, симметрично расположенных относительно первичного лазерного луча, что обеспечивает существенное улучшение отношения сигнал/шум, что, в свою очередь, повышает точность оценок диагностических показателей.
Предлагаемый метод и устройство для его реализации характеризуются высокой автоматизацией процесса диагностики, экспрессностью, использует тот же исходный биоматериал, что и для биохимического анализа крови, не требует применения дорогостоящих оборудования и препаративного обеспечения, может обслуживаться одним оператором средней квалификации.
Процесс тестирования полностью исключает контакт с исследуемым пациентом и является совершенно безопасным для его здоровья.
Метод позволяет осуществлять текущий контроль эффективности проводимого лечения, а также проводить первичную скрининговую диагностику для формирования групп онкологического риска, в том числе для лиц, находящихся в зонах Чернобыльской катастрофы, а также в других экологически неблагоприятных регионах.
Предлагаемый метод и устройство для его реализации могут быть использованы также для тестирования различных биологических жидкостей (сыворотки крови, лимфы, спинно-мозговой жидкости, мочи и т.п.) с целью выявления нарушений гомеостаза исследуемых пациентов.
Метод и устройство могут быть использованы в диагностических центрах, в клинических и научно-исследовательских лабораториях как самостоятельно, так и в составе проблемно-ориентированных диагностических комплексов, в том числе онкологического профиля.
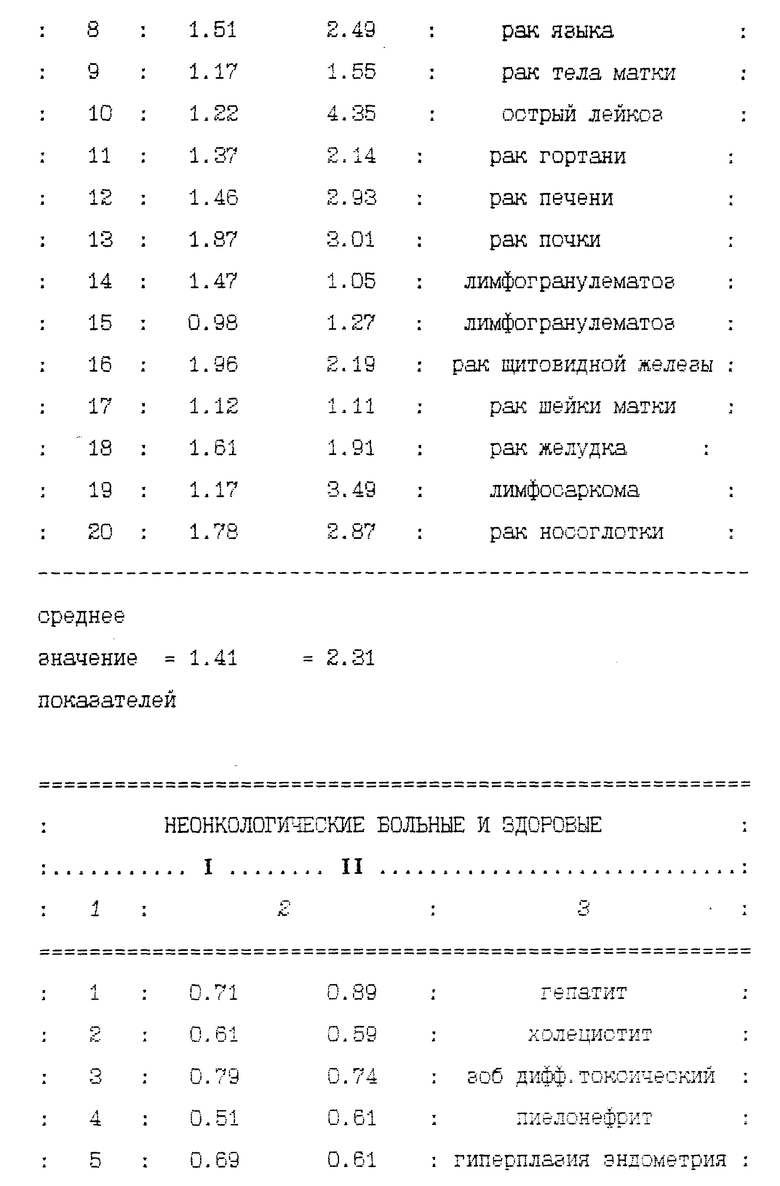
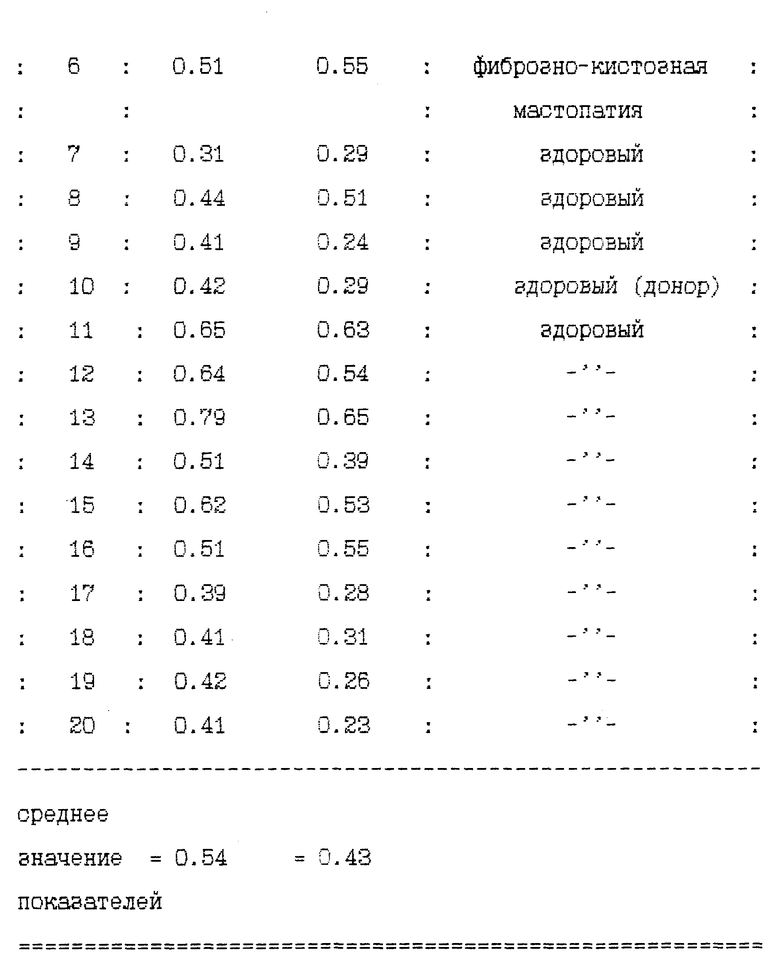
Пример 1 (неонкологический больной). Больная К., 69 лет, поступила с предварительным диагнозом - рак шейки матки. Рентгенография органов грудной клетки в пределах возрастной нормы. Ренография с гипураном без патологии. Биохимический анализ крови, клинические анализы крови и мочи без патологии. Произведено раздельное выскабливание матки. Цитологически - полип шейки матки, гиперплазия эндометрия. Выписана с диагнозом - гиперплазия эндометрия. При биофизическом исследовании способом согласно изобретению значения первого и второго показателей составили 0.69 и 0.61 соответственно.
Пример 2 (неонкологический больной). Больная Ш., 48 лет, поступила с диагнозом - рак правой молочной железы. Рентгенография органов грудной клетки без патологии. Маммаграфия - киста правой молочной железы. Клинические анализы крови и мочи без патологии. Цитограммы без атипии. Проведена операция - секторальная резекция правой молочной железы. Гистология - фиброзно-кистозная мастопатия. При биофизическом исследовании способом согласно изобретению значения первого и второго показателей составили 0.51 и 0.55 соответственно.
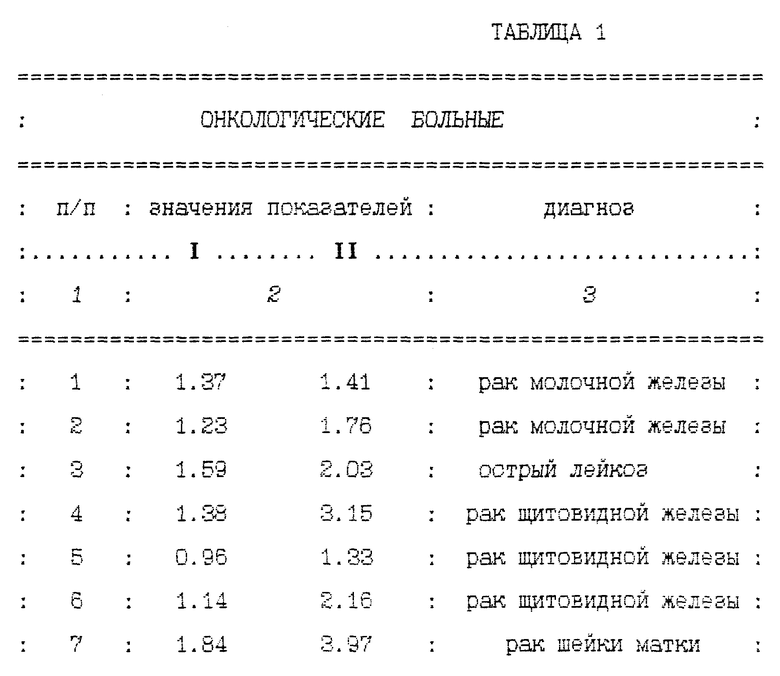
Пример 3 (онкологический больной). Больной К., 56 лет, поступил с диагнозом - рак языка 3 ст. Патологически - плоскоклеточный рак. Рентгенография органов грудной клетки, клинические анализы крови и мочи, биохимический анализ крови без особенностей. Гепатосцинтиграфия - диффузно-очагового поражения печени не выявлено. При УЗИ шеи метастазов в лимфатических узлах не выявлено, обнаружен узел в нижнем полюсе правой доли щитовидной железы. При сканировании щитовидной железы гиперфиксации и холодной зоны нее выявлено. Проведена сочетанная лучевая терапия на первичный очаг. Непосредственное излечение. В настоящее время заканчивается ДЛТ на зоны регионального лимфооттока. До начала лечения проведено биофизическое исследование согласно изобретению. Диагностические показатели составили 1.51 и 2.49 соответственно. В таблице приведен ряд значений первого (maxF) и второго (I/dF) показателей, полученные в процессе проведения предварительных клинических испытаний предлагаемого диагностического метода: для онкологических больных, а также для практически здоровых и неонкологических больных из числа обследованных пациентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ И УСТРОЙСТВО ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2219549C1 |
| СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 1995 |
|
RU2085946C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2005 |
|
RU2276786C1 |
| СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 1995 |
|
RU2085945C1 |
| УСТРОЙСТВО ДЛЯ ДИАГНОСТИКИ | 2005 |
|
RU2408280C2 |
| СПОСОБ ЭКСПРЕСС КОНТРОЛЯ КАЧЕСТВА СПИРТОВОДОЧНЫХ ИЗДЕЛИЙ ДЛЯ ИХ ИДЕНТИФИКАЦИИ | 1999 |
|
RU2142630C1 |
| НЕИНВАЗИВНЫЙ СПОСОБ ЛАЗЕРНОЙ НАНОДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2542427C2 |
| СПОСОБ ДИАГНОСТИКИ РАКА | 2006 |
|
RU2306868C1 |
| Способ ранней диагностики заболеваний путем оптического измерения физических характеристик нативной биологической жидкости | 2015 |
|
RU2622761C2 |
| СПОСОБЫ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИКИ ИЗОТИПИЧЕСКОГО СОСТАВА ИММУННЫХ КОМПЛЕКСОВ И ИХ ПРИМЕНЕНИЕ ПРИ ТЕРАПИИ И ДИАГНОСТИКЕ | 2015 |
|
RU2634861C9 |
Изобретение относится к медицине, онкологии. Исследованию подвергают слабый раствор нативной плазмы крови. Определяют спектральную плотность флуктуаций интенсивности светорассеяния в диапазоне 1-1000 Гц. Выявляют спектральное ядро. Диагностику производят по частоте максимума огибающей спектрального ядра и по отношению интенсивности к полуширине его центра тяжести. Устройство содержит нефелометр с лазерным источником света, измерительную кювету, измерительный преобразователь рассеянного света в аналоговый сигнал. Первый приемник света расположен под углом 90° к лазерному лучу. Корреляционно-спектральный анализатор сигнала светорассеяния содержит автокоррелятор и Фурье-преобразователь. На входе корреляционно-спектрального анализатора введены второй измерительный преобразователь, второй приемник счета, перемножитель сигналов. Способ и устройство позволяют производить простую экспресс-диагностику онкологических заболеваний, используя тот же биоматериал, что и при обычном анализе крови. 2 с.п.ф-лы, 1 ил., 1 табл.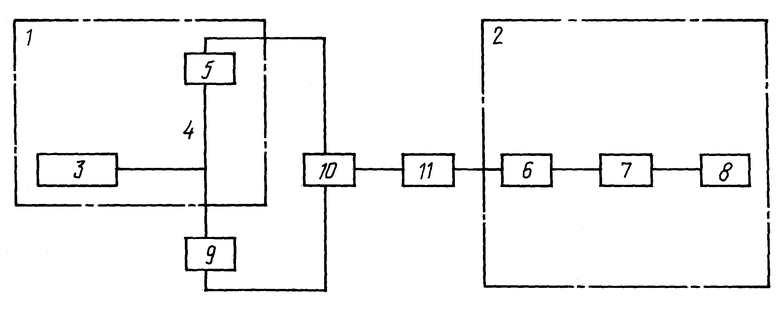
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Мерлич К.И | |||
| и др | |||
| Субфракционный состав плазмы крови при доброкачественных опухолях и раке молочной железы по данным лазерной корреляционной спектроскопии | |||
| Бюллетень экспериментальной биологии и медицины, 1993, N 8, с.193-195 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Гордиенко А.И | |||
| и др | |||
| Верификация опухолей с помощью лазерной флюоресцентной спектроскопии | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Донецк, 1990, с | |||
| Переносная мусоросжигательная печь-снеготаялка | 1920 |
|
SU183A1 |
Авторы
Даты
1999-07-10—Публикация
1996-09-30—Подача