Изобретение относится к медицине, а именно к области диагностики онкологических заболеваний, в частности, путем использования методов молекулярной физики и промышленно применимо в приборах, предназначенных для использования как при обследовании (скрининг) и наблюдении за ходом лечения (мониторинг), так и при подборе in vitro необходимых для лечения препаратов и их доз.
Известно устройство диагностики, в котором осуществляется приготовление раствора биологической жидкости, воздействие лазерным излучением на раствор и регистрацию физических параметров излучения, исходящего из раствора биологической жидкости, по которым судят о состоянии пациента, причем при регистрации физических параметров излучения, исходящего из раствора биологической жидкости, производят аналогово-цифровое преобразование сигнала и его компьютерную обработку [патент РФ №2219549, МПК G01N 33/52]. В этом устройстве измеряют физические параметры слабого водного раствора нативной сыворотки крови пациента методом лазерной корреляционной спектроскопии. Для этого готовят два раствора, в один из упомянутых растворов добавляют щелочь, а в другой - кислоту. Для каждого упомянутого раствора определяют вероятностную плотность распределения амплитуды флуктуации интенсивности светорассеяния.
Недостатком этого аналога является недостаточно большое число контролируемых параметров, по которым ведется диагностика.
Наиболее близким к заявляемому является устройство, содержащее лазерный модуль, который содержит источник лазерного излучения, оптический блок, который содержит кюветный узел, по меньшей мере, один модуль фотоприемного устройства, который содержит фотоприемное устройство, и аналогово-цифровой преобразователь, причем кюветный узел оптически связан с блоком фотоприемного устройства, а аналогово-цифровой преобразователь электрически связан с фотоприемным устройством и компьютером [патент РФ №2219549, МПК G01N 33/52]. С помощью этого устройства измеряют физические параметры слабого водного раствора нативной сыворотки крови пациента методом лазерной корреляционной спектроскопии. Для этого готовят два раствора, в один из упомянутых растворов добавляют щелочь, а в другой - кислоту. Для каждого упомянутого раствора определяют вероятностную плотность распределения амплитуды флуктуации интенсивности светорассеяния.
Недостатком этого ближайшего аналога является недостаточно большое число контролируемых параметров, по которым ведется диагностика.
С помощью заявляемого изобретения решается техническая задача обеспечения многопараметрической диагностики.
Поставленная цель достигается тем, что в известном устройстве для диагностики, содержащем лазерный модуль, который содержит источник лазерного излучения, оптический блок, который содержит кюветный узел, по меньшей мере, один модуль фотоприемного устройства, содержащий малошумящий усилитель и нормирующий усилитель, электрически связанный с малошумящим усилителем, а также аналогово-цифровой преобразователь, причем кюветный узел оптически связан с модулем фотоприемного устройства, а аналогово-цифровой преобразователь электрически связан с фотоприемным устройством и компьютером, оптический блок дополнительно содержит светоделительный шеврон, оптически связанный с источником лазерного излучения и кюветным узлом, а лазерный модуль и модуль фотоприемного устройства жестко закреплены на оптическом блоке.
В частности, светоделительный шеврон жестко может быть закреплен в оптическом блоке.
В частности, устройство может дополнительно содержать плату управления, электрически связанную с лазерным модулем и выполненную с возможностью задания циклограммы включения и выключения лазерного модуля.
В частности, оптический блок может дополнительно содержать узел формирования оптического тракта, оптически связанный с кюветным узлом и жестко закрепленный в оптическом блоке.
В частности, модуль фотоприемного устройства может дополнительно содержать блок формирующей входной оптики, оптически связанный с фотоприемным устройством и жестко закрепленный в этом модуле.
В частности, аналогово-цифровой преобразователь может дополнительно содержать фильтр, задающий таймер, буферную память, выполненные на одной плате.
В частности, устройство может регистрировать спектр биений между рэлеевским рассеянным излучением раствора биологической жидкости и опорным детерминированным лазерным излучением.
При этом лазерное излучение и опорное детерминированное лазерное излучение можно получать от одного и того же источника.
При этом при воздействии на раствор биологической жидкости лазерное излучение и опорное детерминированное лазерное излучение можно направлять под углом 90° друг к другу,
При этом рэлеевское рассеянное излучение можно регистрировать в направлении распространения опорного детерминированного лазерного излучения.
При этом рэлеевское рассеянное излучение можно регистрировать в двух направлениях, ориентированных под углом 180° друг к другу.
При использовании заявляемого изобретения для анализа достаточно 1 мл сыворотки или плазмы крови, остающейся невостребованной при проведении стандартного биохимического поликлинического анализа крови. Среднее время анализа составляет от 3 до 15 минут в зависимости от быстродействия компьютера. Изобретение позволяет производить массовую экспресс-диагностику, при этом онкологические больные могут быть выявлены на ранних стадиях заболевания, когда традиционные методы диагностики оказываются малоэффективными. При этом пациенты группы риска могут быть выявлены заранее, когда в организме только еще появляется предрасположенность к возникновению новообразований. Заявляемое изобретение может быть использовано для контроля эффективности лечения с применением всех современных методов лечения опухолей и последующего диспансерного мониторинга. Оно позволяет производить надежный контроль индивидуального лечения пациента.
Развитие патологических процессов в организме сопровождается изменениями ряда молекулярных параметров в клетках и тканях, а также в сыворотке крови. В сыворотку крови входят белки с различной массой и в различных пропорциях. К основным белкам сыворотки относятся альбумин, масса ~70000 (55%), α1-глобулины, средняя масса ~40000 (6%), α2-глобулины, средняя масса ~50000 (11%), β-глобулины, средняя масса ~70000 (7%), γ-глобулины ~150000 (16%). Оценки дают для средневесовой молекулярной массы частиц сыворотки величину ~100000.
Молекулы протеинов несут на своей поверхности электрический заряд, что обусловливает также наличие большого дипольного момента белка порядка нескольких сот единиц D (дебай). Поверхностный заряд белковой молекулы в растворах можно изменять в широких пределах, варьируя концентрацию свободных протонов (значение рН). Благодаря этим особенностям существует сильное электростатическое взаимодействие между зарядами белковых молекул, а также между молекулами полярного растворителя и заряженными поверхностными группами белка, что, в свою очередь, влияет на характер броуновского движения молекул.
Особенности рассеяния света в растворах сыворотки крови и лимфы определяются физическими параметрами растворенных молекул. В качестве моделей биологических жидкостей, таких как кровь или лимфа могут быть использованы водные растворы белков.
Наиболее прямым и эффективным методом исследования межмолекулярного взаимодействия, подвижности и поляризационных свойств растворов макромолекул, включая водные растворы протеинов, является метод рэлеевского рассеяния света. Метод дает возможность прямого определения молекулярной массы М, для чего необходимо измерить рэлеевский коэффициент или мутность R90 при нескольких концентрациях раствора С и экстраполировать полученную зависимость к С=0, откладывая величину CH/R90 как функцию С. Наклон этой прямой, равный 2 В, позволяет вычислить второй вириальный коэффициент В, который характеризует степень отклонения поведения раствора от идеального и служит мерой межмолекулярного взаимодействия в растворе. Для растворов заряженных молекул белков очень существенным оказывается влияние заряда на поверхности молекулы на ее поведение в растворе, в частности, на параметр межмолекулярного взаимодействия. Появление онкологического заболевания или предрасположенности к нему является результатом изменения поверхностного заряда на молекулах белков. С уменьшением заряда кулоновские силы отталкивания между молекулами протеинов ослабевают, и силы притяжения между ними начинают превалировать. Это приводит к изменению величины и знака коэффициента В и к образованию комплексов молекул, обладающих большей массой, чем отдельные протеины.
Динамические параметры рэлеевского рассеяния света определяют методом корреляции фотонов с Фурье-анализом спектрального состава рассеянного света. В этом методе исследуется корреляционная функция флуктуации интенсивности рассеянного света, обусловленных броуновским движением частиц раствора. При этом могут быть определены коэффициенты трансляционной диффузии частиц и их гидродинамические радиусы. Концентрационные зависимости коэффициента трансляционной диффузии и параметра рассеяния определяются одним и тем же вириальным коэффициентом. Динамические параметры заряженных молекул в растворах также существенно зависят от поверхностного заряда молекулы белков. Наличие онкологического заболевания приводит к изменению поверхностного электрического заряда молекул белков крови, что приводит к изменению интенсивности спектральных компонент рассеянного света и их полуширин.
Развитие онкологических заболеваний имеет начальную автокаталитическую стадию, которая связана с образованием свободно радикальных состояний в липидной фазе клеток и тканей. Эти процессы могут быть надежно обнаружены с помощью флуоресцентного анализа с использованием соответствующих зондов. Начальная стадия агрегации белков сыворотки крови может также быть обнаружена с помощью исследования поляризации флуоресценции различных зондов, соединенных с белками сыворотки крови, в том числе с хелатами.
При облучении флуоресцирующего объема, содержащего раствор молекул белков, монохроматическим линейно поляризованным светом имеет место анизотропия флуоресценции частиц раствора. Вращательная диффузия, которая происходит за время жизни возбужденного состояния и изменяет направление испускающего диполя флуорофора, может уменьшать измеряемую величину анизотропии до значений ниже максимального.
Флуоресценция белков определяется аминокислотным составом и наблюдается в ультрафиолетовой области. В связи с этим при исследовании белков в водных растворах специально подбирают соединения, которые при адсорбции на поверхности молекул белка флуоресцируют в видимой части спектра. В качестве таких соединений используют флуоресцентные зонды или красители. Обладая большим квантовым выходом, зонды интенсивно флуоресцируют в видимой части спектра, причем из параметров этой флуоресценции извлекают информацию о молекулярной подвижности белка. С помощью зондов можно изучать поверхностный заряд молекулы белка.
В дальнейшем изобретение поясняется чертежами, описанием конкретных вариантов его выполнения со ссылками на сопутствующие чертежи, на которых:
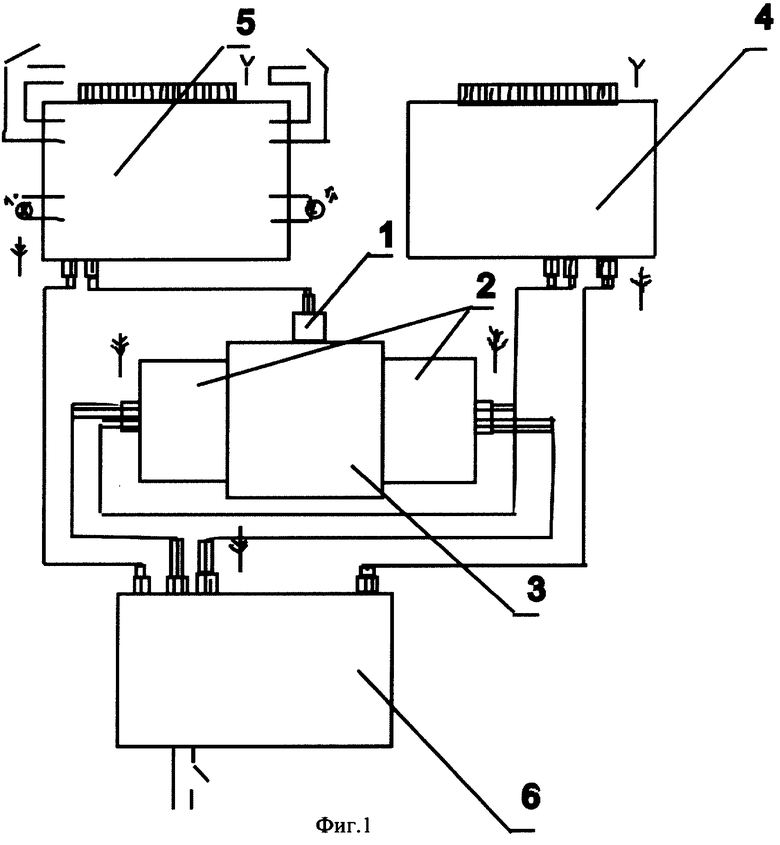
фиг.1 изображает схему заявляемого устройства;
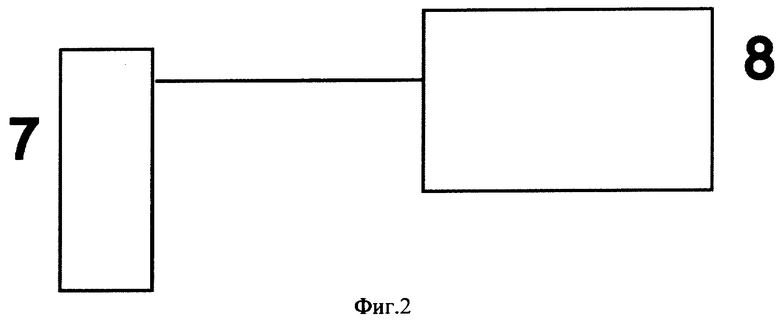
фиг.2 изображает схему лазерного модуля;
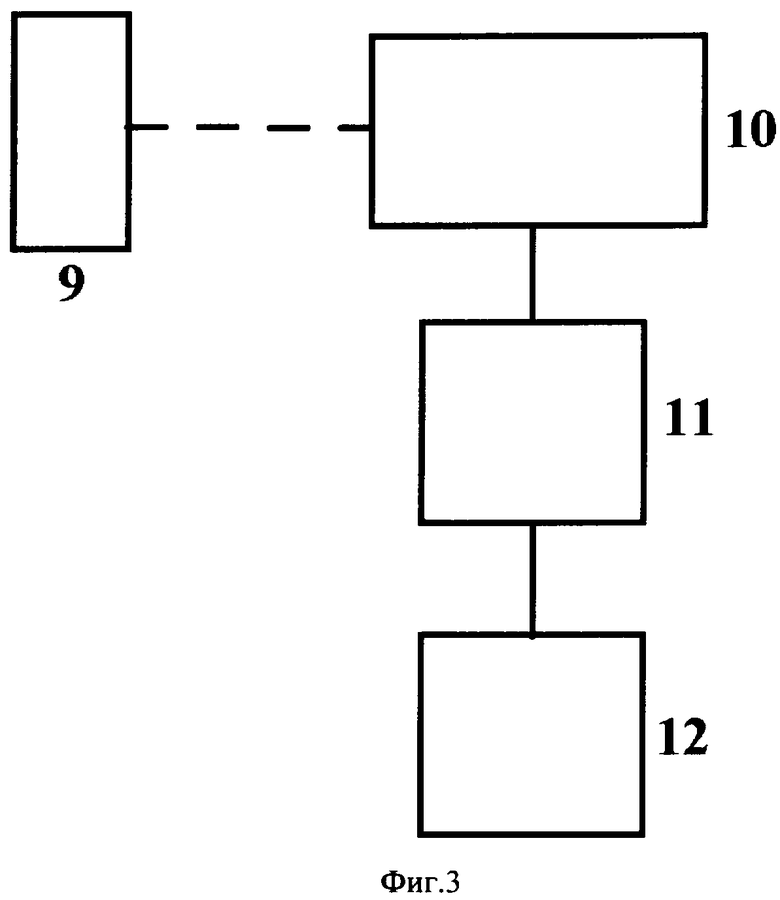
фиг.3 изображает схему оптического блока;
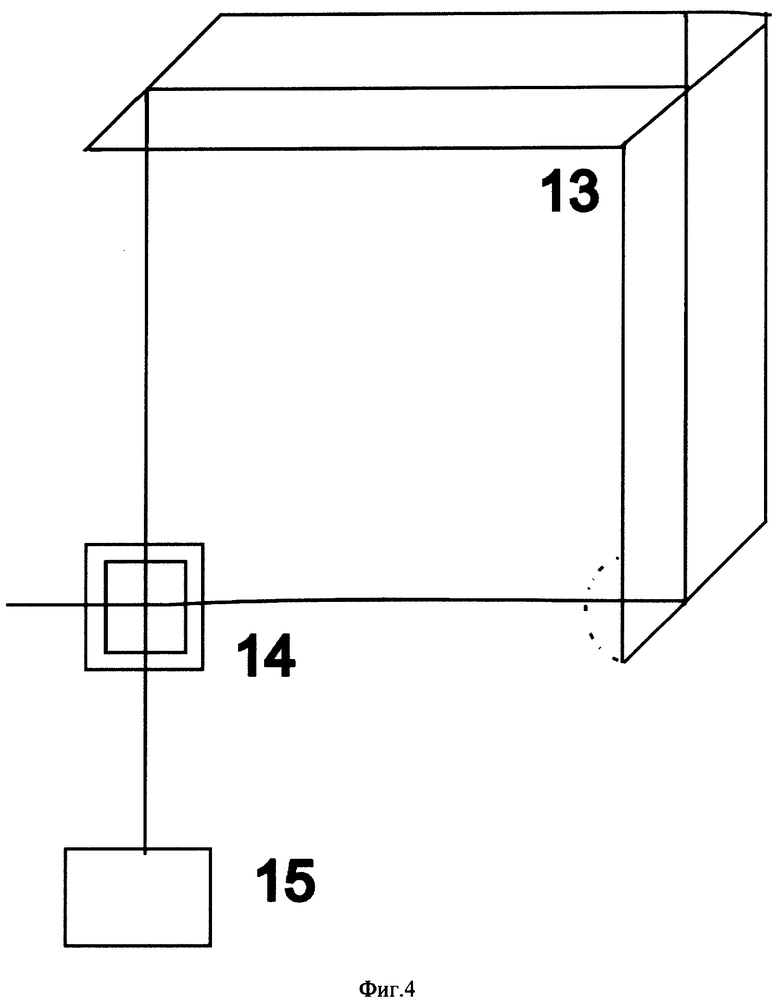
фиг.4 изображает схему модуля фотоприемного устройства;
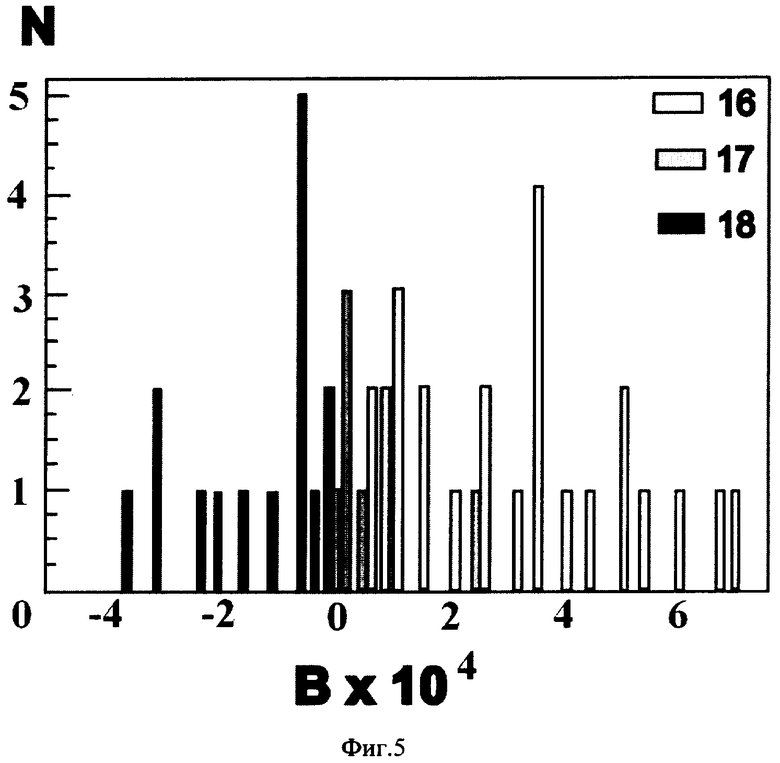
фиг.5 изображает однопараметрическую гистограмму коэффициента межмолекулярного взаимодействия для трех групп пациентов (здоровые пациенты, группа риска и онкологические больные);
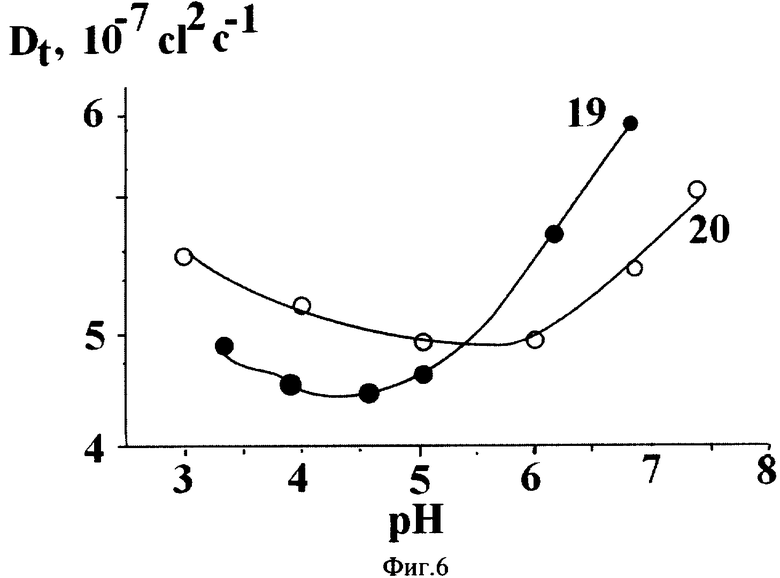
фиг.6 изображает зависимость коэффициента трансляционной диффузии от величины рН для водных растворов BSA и γ-глобулина;
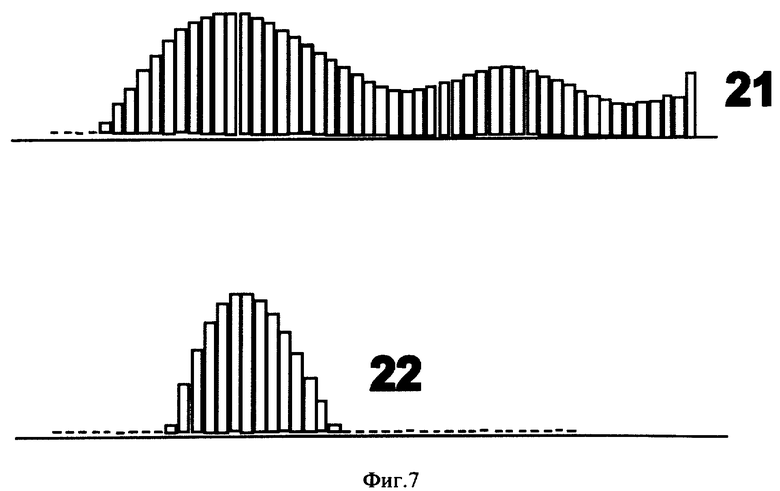
фиг.7 отображает результаты клинического обследования здоровых и больных пациентов по двум параметрам.
Устройство для диагностики (фиг.1) содержит лазерный модуль 1 и два модуля фотоприемных устройств 2, жестко закрепленные на оптическом блоке 3. Сигналы с фотоприемных устройств 2 поступают на плату аналогово-цифрового преобразователя 4, которая одновременно служит и платой обеспечения связи с компьютером через плату согласования, устанавливаемую на материнской плате компьютера. Функции контроля и управления функционированием устройства осуществляются платой управления 5, а его питание осуществляется от встроенного источника питания 6.
Лазерный модуль 1 (фиг.2) состоит из лазерного диода 7 и схемы его питания и управления 8, которая обеспечивает поддержание стабильности выходного излучения лазерного диода 7 и управление его работой по сигналам с платы управления 5.
Модуль фотоприемного устройства 2 (фиг.3) предназначен для обнаружения сигнала рэлеевского рассеяния и приведения его к уровню, необходимому для подачи на аналогово-цифровой преобразователь 4. Он содержит блок формирующей входной оптики 9, фотоприемное устройство 10, малошумящий усилитель 11 и нормирующий усилитель 12. Блок входной формирующей оптики 9 обеспечивает формирование волнового фронта рассеянного излучения, дающего максимально полезный сигнал на фотоприемном устройстве 10. Малошумящий усилитель 11 обеспечивает усиление принятого сигнала с минимально возможным ухудшением его шумовых характеристик. Нормирующий усилитель 12 предназначен для приведения сигнала к значению, обеспечивающему оптимальное использование динамического диапазона аналогово-цифрового преобразователя 4.
Оптический блок 1 (фиг.4) состоит из светоделительного шеврона 13, кюветного узла 14 и узла формирования оптического тракта 15. Кюветный узел 14 обеспечивает фиксацию кюветы с исследуемым раствором с необходимой точностью относительно луча лазерного диода 7 и входных апертур фотоприемного устройства 10. Узел формирования оптического 15 тракта обеспечивает настройку и фиксацию положения лазерного диода 7, фотоприемных устройств 10 и элементов формирующей оптики в процессе проведения измерений. Узел формирования оптического тракта 15 состоит из жесткой направляющей конструкции, на которой смонтированы диафрагмы, котировочные узлы и элементы креплений.
Аналогово-цифровой преобразователь 4 предназначен для ограничения полосы частот (фильтрации) анализируемого сигнала, преобразования фильтрованного анализируемого сигнала из аналоговой формы в цифровую, сохранения результатов в своей буферной памяти до записи их в оперативное запоминающее устройство, управления цифровым накоплением анализируемого сигнала, обеспечения протокола передачи сигнала в компьютер через посредство платы согласования, устанавливаемой в слот ISA материнской платы. Плата аналогово-цифрового преобразователя 4 выполнена в виде печатной платы и снабжена разъемом для стыковки с компьютером и содержит два входа аналогового сигнала и позволяет одновременно хранить 1048 выборок. Число разрядов аналогово-цифрового преобразователя - 12. Плата аналогово-цифрового преобразователя 4 может работать в режиме накопления и режиме передачи данных. Она содержит задающий таймер, буферную память, схему преобразования сигнала в цифровую форму, буферные регистры хранения старшего и младшего байтов числа для обеспечения протокола передачи его в компьютер.
Плата управления 5 предназначена для обеспечения функционирования устройства в штатном и аварийном режимах работы. Она задает циклограмму включения и выключения устройства, индикацию состояния готовности или неготовности устройства к работе, контроль работоспособности функциональных блоков устройства, контроль доступа и архивирования информации о состоянии устройства, выполнение служебных функций, для чего имеется связь устройства с внешним компьютером, осуществляемая через последовательный порт.
Блок питания 6 предназначен для преобразования входного напряжения 220 В частотой 50 Гц в постоянное напряжение с параметрами, обеспечивающими оптимальное функционирование устройства.
Принцип работы устройства (фиг.1) базируется на методе лазерной корреляционной спектроскопии, заключающийся в измерении спектров мощности квазиупругорассеянного света. Известно, что рассеяние света на частицах, совершающих броуновское движение, сопровождается увеличением ширины спектра исходного излучения - диффузионным уширением. Так как собственная ширина спектра лазерного излучения очень мала, ширина спектра рассеянного света пропорциональна коэффициенту трансляционной диффузии, связанному аналитически с размером рассеивающих частиц по известной формуле Стокса-Эйнштейна,
В случае полидисперсной системы, когда вклад в рассеяние дают частицы с разными коэффициентами диффузии, задача определения функции распределения рассеивающих частиц по размерам сводится к сложной математической обработке экспериментальных спектров, в процессе которой приходится решать плохо обусловленную обратную спектральную задачу. Устойчивость решения этой задачи достигается с помощью математического метода регуляризации. Полученные после процедуры регуляризации функции распределения рассеивающих частиц заносятся в компьютерную базу данных для проведения дальнейшего статистического многопараметрового анализа.
Заявляемое устройство, в котором используется когерентное возбуждающее излучение и анализируются рассеянное излучение в водном растворе сыворотки крови методами корреляционной спектроскопии, в том числе методами анализа интегрального и динамического рассеяния света, обеспечивает многопараметрическую диагностику распространенных заболеваний, главным образом, онкологических путем определения статических и динамических молекулярных параметров (масса, форма, коэффициенты межмолекулярного взаимодействия, коэффициенты деполяризации, коэффициенты трансляционной и вращательной диффузии, характеристическая вязкость и гидродинамические радиусы). В отличие от ближайшего аналога заявляемое изобретение позволяет производить одновременное измерение статических и динамических параметров частиц (белков или их агрегатов) водного раствора сыворотки крови, при этом может производиться как обследование (скрининг), и наблюдение за ходом лечения (мониторинг), так и подбор in vitro необходимых для лечения препаратов и их доз.
Метод рэлеевского рассеяния света был использован для диагностики рака. Измеряли относительную интенсивность интегрального рэлеевского рассеяния R (под углом 90° к падающему лучу), массу рассеивающих частиц М и коэффициент межмолекулярного взаимодействия В. Оказалось, что все три указанные параметра для растворов сыворотки крови здоровых людей и онкологических больных существенно различаются (см. таблицу).
Для здоровых пациентов и онкологических больных наиболее сильно различаются значения В (см. таблицу). Для онкологических больных В становится отрицательным, а масса рассеивающих молекул возрастает. Для больных с неонкологическими заболеваниями значения В и М мало отличаются от соответствующих параметров для здоровых пациентов. На фиг.5 показаны гистограммы коэффициента межмолекулярного взаимодействия В для здоровых пациентов 16, группы риска 17 и онкологических больных 18. Гистограммы для здоровых пациентов 16 и онкологических больных 18 практически не перекрываются (фиг.5).
Коэффициент трансляционной диффузии Dt, полученный методом динамического рассеяния света с помощью коррелометра фирмы Malvern для белка 19 и γ-глобулина 20, зависит от поверхностного заряда молекулы нелинейным образом с минимумом в изоэлектрической точке (фиг.6).
Результаты клинического обследования групп здоровых 21, из группы риска 22 и больных 23 пациентов по двум параметрам, характеризующим отношение концентраций Р альбумина и глобулина, а также ширину спектра альбумина W различаются (фиг.7).
При использовании метода флуоресцентного анализа в качестве зонда использовали флуорофор из ряда нафтиламинсульфоновых кислот. Этот зонд нековалентно связывается с белком, он почти не флуоресцирует в воде, но интенсивно флуоресцирует, когда он связан с молекулой белка. Низкий квантовый выход в водной фазе позволяет не учитывать эту часть излучения флуорофора. Анизотропия или степень поляризации флуоресценции также является диагностическим параметром и служит увеличению надежности диагностики.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ АНАЛИЗА БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 2012 |
|
RU2500999C2 |
| СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1996 |
|
RU2132635C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2005 |
|
RU2276786C1 |
| СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ У КОШЕК И СОБАК | 2010 |
|
RU2480748C2 |
| Способ ранней диагностики заболеваний путем оптического измерения физических характеристик нативной биологической жидкости | 2015 |
|
RU2622761C2 |
| СИСТЕМА КОЛИЧЕСТВЕННОГО ФОРМИРОВАНИЯ ИЗОБРАЖЕНИЙ И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2787527C2 |
| ЛАЗЕРНЫЙ ДОПЛЕРОВСКИЙ АНАЛИЗАТОР | 2008 |
|
RU2416803C2 |
| СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 1994 |
|
RU2108577C1 |
| ВОЛОКОННО-ОПТИЧЕСКОЕ УСТРОЙСТВО ДЛЯ ИЗМЕРЕНИЯ ТЕМПЕРАТУРНОГО РАСПРЕДЕЛЕНИЯ (ВАРИАНТЫ) | 2009 |
|
RU2413188C2 |
| УСТРОЙСТВО ДЛЯ ИССЛЕДОВАНИЯ МИКРОЦИРКУЛЯЦИИ КРОВИ | 2002 |
|
RU2243567C2 |
Изобретение относится к медицине. Устройство для исследования биологической жидкости содержит лазерный модуль, содержащий источник лазерного излучения, оптический блок, содержащий кюветный узел, модуль фотоприемного устройства и аналогово-цифровой преобразователь. Причем кюветный узел оптически связан с модулем фотоприемного устройства, а аналогово-цифровой преобразователь электрически связан с фотоприемным устройством и компьютером. Дополнительно модуль фотоприемного устройства содержит малошумящий усилитель и нормирующий усилитель, электрически связанный с малошумящим усилителем. Оптический блок содержит узел формирования оптического тракта и светоделительный шеврон, оптически связанные с источником лазерного излучения и кюветным узлом, а лазерный модуль и модуль фотоприемного устройства жестко закреплены на оптическом блоке. Применение данного устройства позволяет проводить многопараметрическую диагностику заболеваний. 10 з.п. ф-лы, 7 ил., 1 табл.
1. Устройство для исследования биологической жидкости, содержащее лазерный модуль, содержащий источник лазерного излучения, оптический блок, содержащий кюветный узел, по меньшей мере, один модуль фотоприемного устройства и аналогово-цифровой преобразователь, причем кюветный узел оптически связан с модулем фотоприемного устройства, а аналогово-цифровой преобразователь электрически связан с фотоприемным устройством и компьютером, отличающееся тем, что дополнительно модуль фотоприемного устройства содержит малошумящий усилитель и нормирующий усилитель, электрически связанный с малошумящим усилителем, оптический блок содержит узел формирования оптического тракта и светоделительный шеврон, оптически связанные с источником лазерного излучения и кюветным узлом, а лазерный модуль и модуль фотоприемного устройства жестко закреплены на оптическом блоке.
2. Устройство по п.1, отличающееся тем, что светоделительный шеврон жестко закреплен в оптическом блоке.
3. Устройство по п.1, отличающееся тем, что оно дополнительно содержит плату управления, электрически связанную с лазерным модулем и выполненную с возможностью задания циклограммы включения и выключения лазерного модуля.
4. Устройство по п.1, отличающееся тем, что узел формирования оптического тракта жестко закреплен в оптическом блоке.
5. Устройство по п.1, отличающееся тем, что модуль фотоприемного устройства дополнительно содержит блок формирующей входной оптики, оптически связанный с фотоприемным устройством и жестко закрепленный в этом модуле.
6. Устройство по п.1, отличающееся тем, что аналогово-цифровой преобразователь дополнительно содержит фильтр, задающий таймер, буферную память, выполненные на одной плате.
7. Устройство по п.1, отличающееся тем, что выполнено с возможностью регистрации спектра биений между рэлеевским рассеянным излучением раствора биологической жидкости и опорным детерминированным лазерным излучением.
8. Устройство по п.7, отличающееся тем, что лазерное излучение и опорное детерминированное лазерное излучение получают от одного и того же источника.
9. Устройство по п.7, отличающееся тем, что узел формирования оптического тракта выполнен с возможностью направления лазерного излучения и опорного детерминированного лазерного излучения под углом 90° друг к другу.
10. Устройство по п.7, отличающееся тем, что модуль фотоприемного устройства выполнен с возможностью регистрации рэлеевского рассеянного излучения в направлении распространения опорного детерминированного лазерного излучения.
11. Устройство по п.7, отличающееся тем, что модуль фотоприемного устройства выполнен с возможностью регистрации рэлеевского рассеянного излучения в двух направлениях, ориентированных под углом 180° друг к другу.
| СПОСОБ И УСТРОЙСТВО ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2219549C1 |
| Полевой передвижной опылитель | 1936 |
|
SU49620A1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2000 |
|
RU2196623C2 |
| US 6618144 B1, 09.09.2003 | |||
| Петрова Г.П | |||
| и др | |||
| Методы рэлеевского рассеяния света и электронного парамагнитного резонанса в экологическом контроле и медицинской диагностике | |||
| Ж.Биомедицинская радиоэлектроника, №5, 2000, с.4-10. | |||
Авторы
Даты
2011-01-10—Публикация
2005-12-15—Подача