Данное изобретение относится к способам и устройствам ускоренного изменения формы роговой оболочки глаза, включающим введение энзима(-мов) или других агентов, способствующих изменению формы роговицы с целью уменьшения или устранения дефектов преломления глаза.
Приблизительно 80% преломляющей способности глаза принадлежит роговице. Когда форма роговицы изменена или длина глаза по оси слишком велика или слишком мала, или линза глаза функционирует ненормально, могут возникать дефекты преломления, сказывающиеся в проявлении миопии, астигматизма или гиперопии. Очки исправляют дефекты преломления за счет преломления света линзой прежде, чем свет достигнет роговицы, путем изменения угла, под которым свет попадает на роговицу. Контактные линзы корректируют дефекты глаза путем замены роговицы с дефектной формой передним изгибом контактной линзы, который рассчитан таким образом, чтобы сделать глаз эмметропным (состояние, при котором не требуется коррекции зрения). Однако, когда линзу снимают, изменение формы роговицы все еще остается и дефекты преломления также имеют место.
Роговица сама состоит из пяти слоев. Внешний слой является эпителием с толщиной 4-5 клеток. Под эпителием расположена бесклеточная мембрана Боумана (Bowman). Средний слой представляет собой строму, которая состоит из роговичных фибробластов (кератоцитов), рассеянных среди пластинок коллагена, протеогликанов и гликопротеинов. Под стромой находится другой бесклеточный слой, называемый мембраной Десцемета (Descemet). Внутренний слой роговицы, представляющий собой монослой плоских клеток, называется эндотелием.
Структурными компонентами роговицы человека в основном являются протеогликаны и коллагены. Протеогликаны состоят из гиалуронатного ядра, белкового ядра и гликозаминогликанов, которые представляют собой мономеры протеогликана с повторяющимися дисахаридными звеньями. Приблизительно 60% гликозаминогликанов роговицы состоят из сульфата кератана, в то время как остальные 40% в основном состоят из сульфата хондроитина. Другой основной структурный компонент роговицы, коллаген, обнаружен в роговице человека в семи различных формах. Эти структурные компоненты роговицы являются довольно гибкими и позволяют роговице менять свою форму путем последовательной смены серии контактных линз с целью коррекции дефектов преломления.
Эта процедура известна как ортокератология. Методы ортокератологии, не использующие энзимы или другие агенты, возникли в 1962 г. как расширение области использования обычных контактных линз. Ортокератологией обычно называют терапевтическое использование контактных линз с целью изменения формы изгиба роговицы для исправления дефектов преломления глаза.
Д-р Charles May и д-р Stuart Grant считаются пионерами в этой области. Университетские исследования и клиническое изучение в течение следующих 20 лет подтвердили безопасность, эффективность и воспроизводимость этого метода. В настоящее время ортокератология является областью, использующей контактные линзы, для ограниченного числа частных врачей, в основном, в США.
Традиционная ортокератология использует последовательную смену серии контактных линз для изменения формы роговицы с целью придания роговой оболочке более сферической формы. Это приводит к уменьшению или исчезновению миопии и астигматизма и улучшает природное зрение. Как только желаемый изгиб (кривизна) роговицы достигается, для стабилизации результатов следует носить фиксирующие контактные линзы. Контактные линзы изготавливают из жесткого газопроницаемого материала и не содержат энзимов или других агентов.
Период лечения меняется от шести до восемнадцати месяцев при последовательной смене контактных линз и проверке зрения каждые 2-6 недель.
Обычно в ортокератологии для расчета используют следующую формулу:
Кривизна основания линзы в диоптриях=изгибу самого плоского участка роговицы в диоптриях.
Диаметр линзы = кривизна основания в мм+1,5 мм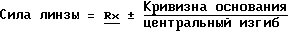
Толщина = 0,18 мм для 0 силы минус 0,01 мм на каждую одну диоптрию с минусом; плюс 0,02 мм на каждую одну диоптрию с плюсом.
Промежуточная кривизна = кривизна основания в мм + 1,5 мм, ширина = 0,35-0,5 мм.
Периферическая кривизна = кривизна основания в мм + 3,0 мм, ширина = 0,35 - 0,5 мм.
При лечении миопии методом ортокератологии вставляются новые контактные линзы с более плоской поверхностью кривизны, меньшей коррекцией, большими диаметрами и большей толщиной.
Кривизна центральной части роговицы пациента продолжает уменьшаться (становится более плоской и более сферической), миопия и астигматизм уменьшаются, и острота природного зрения значительно улучшается. При достижении максимально желаемого результата или прекращении улучшения зрения, для закрепления результатов следует носить все время или частично фиксирующие контактные линзы.
В традиционной ортокератологии университетские и клинические исследования показали следующие пределы изменений: 4 диоптрии при миопии и 2,5 диоптрии при астигматизме, отсутствие изменений при гиперопии, изменение центральной части роговицы 2 диоптрии и изменение остроты природного зрения, равное 9 строкам на диаграмме Snellen. Если не носить фиксирующие линзы, через несколько часов или дней, может возникнуть ухудшение.
Несмотря на вышесказанное, остается необходимость в создании усовершенствованного метода коррекции дефектов преломления глаза нехирургическим путем, который может исправлять большие дефекты преломления и позволяет получить устойчивые результаты за более короткий промежуток времени.
Первый аспект настоящего изобретения заключается в создании контактной линзы для подачи различных агентов в глаз. Линза включает жесткий передний слой и жесткий задний слой. Выпуклая сторона заднего слоя имеет более плоский изгиб, чем вогнутая сторона переднего слоя над центральной частью заднего слоя. Линза также включает канал в центре заднего слоя. Канал проходит из выпуклой части заднего слоя к вогнутой стороне заднего слоя. Вогнутая сторона переднего слоя и выпуклая сторона заднего слоя соединены, образуя центральную камеру между слоями, связанную с вогнутой частью заднего слоя при помощи канала. В предпочтительном варианте данного изобретения вогнутая сторона заднего слоя имеет кривизну, достаточную для придания эмметропии глазу.
Другой аспект настоящего изобретения относится также к контактной линзе для подачи различных агентов в глаз. Согласно этому варианту контактная линза также включает жесткий передний слой и жесткий задний слой. Промежуточная часть задней поверхности переднего слоя имеет более крутой радиус кривизны, чем передняя поверхность промежуточной части заднего слоя. По этому варианту линза имеет канал в промежуточной части заднего слоя. Канал проходит из выпуклой стороны заднего слоя к вогнутой стороне заднего слоя. Вогнутая сторона заднего слоя и выпуклая сторона заднего слоя соединяются, образуя периферическую камеру между слоями в промежуточных частях. Канал сообщается как с периферической камерой, так и с задней поверхностью заднего слоя контактной линзы. В предпочтительном варианте выполнения этой линзы вогнутая сторона заднего слоя характеризуется центральным радиусом кривизны, достаточным для придания эмметропии глазу. Еще одним аспектом настоящего изобретения является создание агента, смягчающего роговицу глаза млекопитающего, для коррекции дефектов преломления глаза. Агент должен быть в комбинации с жесткой контактной линзой. Контактная линза в такой комбинации, предпочтительно, имеет вогнутую поверхность для получения желаемой конфигурации.
Еще одним аспектом настоящего изобретения является способ изменения формы роговицы от первой конфигурации до второй желаемой конфигурации с целью коррекции дефектов преломления глаза млекопитающего. Согласно этому способу создается мягкая контактная линза, в которую загружается некоторое количество агента, смягчающего роговую оболочку, достаточное для смягчения роговицы глаза. Затем мягкая контактная линза вставляется в глаз (на роговицу) и смягчающий агент в мягкой контактной линзе вызывает размягчение роговицы и делает ее более гибкой. Это сопровождается удалением мягкой контактной линзы и надеванием по меньшей мере, одной жесткой контактной линзы на роговицу, когда последняя находится в смягченном состоянии, для того, чтобы изменить форму роговицы, придав ей конфигурацию вогнутой поверхности жесткой контактной линзы.
По предпочтительному варианту этого способа мягкая контактная линза выполняется из гидрофильного материала, например, коллагена. Мягкую контактную линзу можно наполнить смягчающим роговую оболочку агентом путем погружения линзы в раствор этого агента. Согласно одному предпочтительному варианту этого способа сверху мягкой контактной линзы надевают жесткую контактную линзу-сборник, в то время как мягкая контактная линза находится на роговице, чтобы удерживать ее форму в течение процесса смягчения. Согласно этому варианту, предпочтительно, чтобы мягкая контактная линза была соединена с жесткой контактной линзой. Согласно другому предпочтительному варианту, способ заключается во введении в глаз некоторого количества ингибитора агента с целью замедления или прекращения смягчающего действия этого агента.
Так, ингибитор добавляется после того, как роговица размягчится и примет желаемую конфигурацию. Ингибитор может быть ингибитором металлопротеиназы, например, ЭДТА (этилендиаминтетрауксусная кислота), N-этилмальимин, циклогексимид, 1,10-фенантролин, фенилметансульфонилфторид, TIMP, (тимидинфосфат), TIMP-2 или IMP (инозинмонофосфат). Ингибитор также может быть ингибитором коллагеназы, например, соединениями, содержащими ионы железа (Fe2+) или соединениями, содержащими ионы меди (Cu2+). Можно в качестве ингибитора применять цистеин.
Согласно еще одному аспекту изобретения предложен способ коррекции дефектов преломления глаза млекопитающего, заключающийся в стадии первого введения субъекту некоторого количества агента, смягчающего роговую оболочку глаза субъекта, для того, чтобы роговица изменила форму и приобрела вторую желаемую конфигурацию. После того, как роговица смягчилась, на нее надевается жесткая контактная линза, имеющая вогнутую поверхность желаемой конфигурации. Под воздействием линзы роговица принимает эту желаемую конфигурацию. Когда роговица удерживает нужную желаемую форму без поддержки линзы, последнюю снимают. Смягчающий роговую оболочку агент может быть выбран из любых энзимов, активаторов энзимов и других агентов, воздействующих на структурные компоненты роговицы. Например, смягчающим агентом может быть энзим, который разрушает протеогликаны в роговице, например, хондроитиназа AC, хондроитиназа ABC, кератаназа, гиалуронидаза, матрикс металлопротеиназы-3. Таким агентом может быть также энзим, который разрушает коллаген в оболочке, например, матрикс металлопротеиназы-1 или матрикс металлопротеиназы-2. Согласно другому варианту агентом является активатор эндогенного энзима, который разрушает структурные компоненты роговицы. Такой агент может быть, например, активатором энзима эндогенной металлопротеиназы, например, интерлейкином-1, интерлейкином -1α, фактором некроза опухоли, моногидратом мононатрийурата, аминофенилуксуснокислой ртутью, амилоидом A человеческой сыворотки, микроглобином B2 человека и хлоридом меди. Согласно еще одному варианту изобретения смягчающий роговицу агент, используемый в энзимортокератологии, может быть инактиватором, который инактивирует ингибитор эндогенного энзима. Таким инактиватором может быть, например, иодацетамид. Согласно предпочтительному варианту, вышеуказанные смягчающие агенты можно применять в комбинации с анастезирующими веществами, например, гидрохлоридом пропаракаина для того, чтобы свести к минимуму любое неприятное ощущение, связанное с применением таких агентов. Агент можно использовать в виде глазных капель. Глазные капли могут содержать липосомы, включающие агент. Агент также можно вводить в роговицу методом ионтофореза. Предпочтительно, чтобы жесткая контактная линза содержала агент в количестве, достаточном для смягчения роговицы, и указанный агент вводился в глаз посредством жесткой контактной линзы. По предпочтительному варианту этого способа жесткая контактная линза содержит камеру между передней и задней поверхностями и имеет отверстия, расположенные на задней поверхности.
Согласно этому предпочтительному варианту агент выходит из камеры и через отверстия и на роговицу могут успешно надевать серию жестких контактных линз, камера которых заполнена смягчающим агентом, причем радиус вогнутого участка задней поверхности каждой последующей линзы является последовательно более совпадающим с радиусом желаемой конфигурации роговой оболочки. Согласно другому предпочтительному варианту контактная линза может состоять из двух слоев, соединенных друг с другом. По этому варианту камера для жидкости формируется между двумя слоями, когда контактирующие поверхности двух слоев соединяются вместе. Задний слой контактной линзы имеет, по меньшей мере одно отверстие для подачи жидкости из камеры в глаз. Радиус центрального вогнутого участка контактной линзы может быть равен радиусу выпуклой части, который должен быть у роговицы для того, чтобы глаз стал эмметропным. Агент можно также применять путем инъекции его непосредственно в строму роговой оболочки сбоку или путем инъекции агента спереди через эпителий глаза. Способ может также включать надевание мягкой линзы, которая выполнена из вещества, например, коллагена, которое пропитано агентом до надевания жесткой контактной линзы. Это способ можно осуществлять с ингибиторами, которые замедляют или останавливают смягчающую активность агентов, используемых для смягчения роговицы по данному изобретению. Такие вещества помогают в отвердевании роговицы после того, как она смягчилась, и помогают удержать желаемую конфигурацию, приданную роговице. Ускорение указанного затвердевания роговицы предусматривает введение в глаз субъекта, в котором роговица была смягчена, определенного количества ингибитора, которое достаточно для замедления или прекращения действия смягчающего агента. Такой ингибитор добавляется после смягчения роговицы и придания ей желаемой конфигурации. Ингибитором может быть, например, ингибитор металлопротеиназы, например, ЭДТА, N-этилмальимин, циклогексилимид, 1,10-фенантролин, фенилметансульфонилфторид, TIMP, TIMP-2 или IMP. Такой ингибитор может также быть ингибитором коллагеназы, например, соединением, содержащим ион железа (Fe2+), или соединением, содержащим ион меди (Cu2+). Если в качестве смягчающего агента используют гиалуронидазу, ингибитором может быть ингибитор последней, например, цистеин и ЭДТК. Другим аспектом настоящего изобретения является метод коррекции дефектов преломления глаза млекопитающего.
Метод включает создание сложной контактной линзы, имеющей жесткий центр и мягкую полость (кромку), выходящую за внешний периметр жесткого центра.
Жесткий центр имеет парацентрическую кривизну, достаточную для того, чтобы сделать глаз млекопитающего эмметропным. Другой стадией этого метода является заполнение полости агентом, смягчающим роговицу, в количестве, достаточном для смягчения роговицы, подачу смягчающего агента на роговицу глаза, что приводит к смягчению роговицы и делает ее более гибкой. Затем, роговице придают форму задней кривой поверхности жесткого центра сложной линзы, и глаз становится эмметропным.
Изобретение имеет также еще один аспект, представляющий способ коррекции дефектов преломления глаза млекопитающего. Этот способ включает стадию создания контактной линзы, как при описании первого аспекта данного изобретения. Центральная камера контактной линзы заполняется определенным количеством смягчающего агента, достаточным для смягчения роговицы глаза. Этот агент попадает на роговицу из центральной камеры, тем самым смягчая роговицу и делая ее более гибкой, затем роговице, придается форма внутренней центральной кривой заднего слоя контактной линзы.
Еще одним аспектом изобретения также является способ коррекции дефектов преломления глаза млекопитающего. Согласно этому способу, берут контактную линзу по второму аспекту данного изобретения. Способ состоит из стадии заполнения периферийной камеры контактной линзы определенным количеством смягчающего роговицу агента, достаточным для смягчения роговицы. Смягчающий агент попадает на роговицу из центральной камеры, смягчает роговицу и делает ее более гибкой, и затем роговица приобретает форму внутренней центральной кривой заднего слоя линзы.
Изобретение также включает еще один аспект, по которому предусмотрен способ реабилитации искривлений роговицы и коррекции дефектов преломления глаза млекопитающего с искривленной роговицей. Этот способ включает стадию идентификации субъекта с искривленной формой роговицы.
Применяют смягчающий агент в количестве, достаточном для смягчения роговицы глаза субъекта, для того чтобы форму роговицы можно было изменить, придав ей желаемую вторую конфигурацию. Затем на роговицу надевают контактную линзу, у которой вогнутая часть имеет желаемую конфигурацию и роговица меняет свою форму, приобретая желаемую вторую конфигурацию под действием линзы. Линзу удаляют из глаза, когда роговица станет способна удерживать желаемую форму без поддержки линзы. Субъект может быть идентифицирован методом диагностики, предусматривающей наличие одного из условий: кератоконуса, искривления роговицы, вызванного контактной линзой, искривленной формы роговицы или неисправленного дефекта преломления вследствие хирургической операции роговицы.
Согласно еще одному аспекту, предусмотрен способ усовершенствования клинической хирургии глаза, включающий манипулирование с роговицей млекопитающего. Этот способ включает идентификацию субъекта, у которого с роговицей проводили какие-то манипуляции, и применение смягчающего роговицу глаза агента, который смягчает уже подвергшуюся изменениям роговицу субъекта для того, чтобы роговица изменила форму и приобрела желаемую вторую конфигурацию. Затем на роговицу надевают контактную линзу, имеющую вогнутую поверхность желаемой конфигурации, и под влиянием этой линзы роговица приобретает желаемую конфигурацию. Когда это достигнуто и роговица способна сохранять приобретенную форму, линзу удаляют из глаза. Манипуляции с роговицей могут быть любого вида, включая радиальную кератотомию, пересадку роговицы, операцию катаракты и изменение формы роговицы лазером.
Изобретение также включает способ замедления или прекращения смягчения роговицы и ускорения ее отвердевания. Этот способ включает применение определенного количества ингибитора энзима или агента, который способствует смягчению роговицы. Можно использовать различные ингибиторы, включая ЭДТК, N-этилмальимин, циклогексимид, 1,10-фенантролин, фенилметансульфонилфторид, TIMP, TIMP-2, IMP, цистеин, ион железа и ион меди.
В дальнейшем изобретение поясняется примерами выполнения со ссылками на прилагаемые чертежи, на которых:
фиг. 1 изображает горизонтальную проекцию жесткой газопроницаемой контактной линзы для лечения миопии в энзимортокератологии;
фиг. 2 - поперечный разрез по линиям 2-2 на фиг. 1;
фиг. 3A - схематическое изображение сплошными линиями поперечной конфигурации роговицы глаза при миопии в сравнении с идеальной формой, показанной штрихами, по методу, описанному в данном изобретении;
фиг. 3B - схематическое изображение конвергенции света на сетчатке глаза с нормальным зрением;
фиг. 3C - схематическое изображение конвергенции света впереди сетчатки глаза, страдающего близорукостью (миопией);
фиг. 4A - схематическая иллюстрация конвергенции света внутри глаза более, чем в одной точке, возникающей при астигматизме;
фиг. 4B - изображает кривизну центральной части роговицы глаза с астигматизмом, иллюстрирующую меньший радиус кривизны на первом плане и сравнительно больший радиус кривизны на втором плане, перпендикулярном первому плану;
фиг. 4C - горизонтальная проекция тороидальной контактной линзы для астигматизма, используемой в энзим-ортокератологии;
фиг. 5A изображает конвергенцию света за сетчаткой глаза при дальнозоркости (гиперопии);
фиг. 5B изображает сплошными линиями сравнительно плоскую роговицу перед энзим-ортокератологией по изобретению и штрихами показана форма роговицы по методу данного изобретения;
фиг. 5C изображает горизонтальную проекцию контактной линзы для дальнозоркости (гиперопии) по методу энзим-ортокератологии;
фиг. 5D - поперечное сечение вдоль линий 5D-5D на фиг. 5C;
фиг. 6 изображает горизонтальную проекцию мягкой коллагеновой контактной линзы, выделяющей энзим;
фиг. 7 изображает горизонтальную проекцию линзы "sarurntype" (типа "сатурн"), выделяющей энзим;
фиг. 8A изображает горизонтальную проекцию ортокератологической линзы, выделяющей энзим спины поросенка (piooy back");
фиг. 8B - поперечное сечение вдоль линий 8b-8b на фиг. 8A;
фиг. 9 изображает микрофотографию поперечного сечения роговицы человека;
фиг. 10 - увеличенная микрофотография стромы человека (коллагеновые фибриллы и мукополисахаридные слои);
фиг. 10A - схематическая диаграмма, показывающая поперечное сечение роговицы человека;
фиг. 10B - увеличенный схематический вид компонентов стромы роговой оболочки, заключенной в окружность 10b на фиг. 10a;
фиг. 11 изображает горизонтальную проекцию нижней стороны контактной линзы по изобретению;
фиг. 12 - поперечное сечение контактной линзы, изображенное на фиг. 11, по линии 12-12;
фиг. 13 изображает горизонтальную проекцию нижней части другого вида контактной линзы по изобретению;
фиг. 14 изображает поперечное сечение контактной линзы, показанной на фиг. 13 вдоль линии 14-14.
В соответствии с данным изобретением предложен усовершенствованный метод ортокератологии, называемый изобретателем Энзим-Ортокератологией. Энзим ортокератология включает использование одного или более энзимов и/или использование других агентов в серии контактных линз. По программе традиционной ортокератологии роговицу просто изгибают или сжимают, в то время как нижерасположенные структурные компоненты остаются неизменившимися.
С другой стороны, по методу Энзим-Ортокератологии роговицу смягчают, то есть структурные компоненты роговицы частично разлагаются и/или модифицируются таким образом, что они могут быть изменены. Таким образом, роговица может принимать и удерживать новую форму, предпочтительно без необходимости продолжительного использования или поддержки контактных линз. Хотя некоторые структурные компоненты роговицы расположены в эпителии 70 (фиг. 10a), мембране Bowman'a 72, мембране Descemet'a 74 и в эндотелии 76, основные структурные компоненты роговицы находятся в строме 78. Как показано схематически на фиг. 10B, структурные компоненты стромы включают коллагеновые фибриллы 82 и протеогликаны 84. Согласно методам Энзим-Ортокератологии энзимы и/или другие агенты, расщепляющие такие структурные компоненты, вводят в роговицу для того, чтобы смягчить ее и сделать более гибкой. Термин "смягчить" используется в данном контексте для обозначения модификации или деструкции одного или более структурных компонентов роговицы, что приводит к тому, что роговица становится мягче и гибче. Затем форма роговицы может быть изменена при помощи контактных линз или других средств.
I. Энзимы и другие агенты, используемые в Энзим-Ортокератологии.
Для смягчения роговой оболочки в энзим-ортокератологии можно использовать ряд энзимов. Однако энзим-ортокератология не ограничивается использованием энзимов. Используется также ряд других агентов, включая лекарства и химические вещества, которые можно применять для смягчения роговицы в добавление к энзимам или взамен энзимов.
Особенный интерес представляют агенты, активирующие или ингибирующие энзимы. Агенты, отличающиеся от энзимов, можно также использовать для выполнения других функций в энзим-ортокератологии помимо смягчения роговицы.
A. Экзогенные энзимы, используемые в энзим-ортокератологии.
Энзимы состоят из молекул белков и ускоряют химические реакции. Для того, чтобы ускорить реакцию, энзим соединяется с одной или более молекул субстрата с образованием сложной молекулярной структуры, которая катализирует химическую реакцию субстрата или субстратов. Энзим, который не подвергается при этой реакции изменению, затем отделяется от продукта или продуктов реакции.
Согласно одному аспекту данного изобретения экзогенные энзимы вводят субъекту для смягчения роговицы глаза.
Экзогенные энзимы - это те энзимы, которые происходят из источников, находящихся вне глаза субъекта, например, энзимы, очищенные из животных, растительных или микробных источников. Такие энзимы нужно применять таким образом, чтобы ввести их в роговицу глаза субъекта.
По предпочтительному варианту настоящего изобретения основным энзимом, используемым для смягчения роговицы, является гиалуронидаза. Это энзим, расщепляющий мукополисахариды. В частности, он катализирует гидролиз от одной до четырех связей гиалуроновой кислоты, сульфатов A и C хондроитина и хондроитина-4. Таким образом, он способен разрывать цепи мукополисахаридов. Мукополисахарид является одним из внутриклеточных основных веществ (цемент или животный клей) стромы, ткани соединительного типа среднего слоя роговицы.
Форма роговицы в значительной степени зависит от расположения коллагеновых фибрилл в слое стромы роговицы и от расположения мукополисахаридных слоев между этими фибриллами. Гиалуронидаза, которая специфична только к мукополисахаридному слою, разрывает мукополисахаридные цепи, будучи в роговице. Строма тогда временно смягчается и роговица становится более гибкой.
Гиалуронидазу можно получить из многих источников, включая бычьи тесты, овечьи тесты и streptomyces (бактерии). Энзим гиалуронидазу предпочтительно применять в виде лиофилизированного порошка (высушенного замораживанием). Одна форма гиалуронидазы доступна под товарным знаком Wydase® (Wyeth Laboratories Inc, Philadelphia, Pennsylvania. Wydase® - препарат высокочистой гиалуронидазы из бычьего семени, доступна в двух формах. Лиофилизированная форма доступна в виде стерильного белого бесцветного аморфного твердого порошка и может быть приготовлена перед употреблением инъекцией хлорида натрия, обычно в пропорциях от ~1 мл на 150 USP ед. гиалуронидазы. Раствор гиалуронидазы также доступен, содержит 150 USP ед.гиалуронидазы на мл, с 8,5 мг хлорида натрия, 1 мг динатрий ЭДТА, 0,4 мг хлорида кальция, буфера - монофосфата натрия и не более, чем ~0,1 мг тимерозаля. По предпочтительному варианту, лиофилизированную форму гиалуронидазы помещают в раствор, содержащий фосфат натрия - буфер для поддержания нужного pH, хлорид натрия, дистиллированную воду для растворения энзима; бычью или человеческую сыворотку для сохранения эффективности и активности энзима, и другие агенты, такие как HCl и гидроокись натрия для повышения или снижения pH. Можно включать в состав раствора лекарства, например, гидрохлорид пропаракаина для анестезирования роговицы.
Оптимальная концентрация гиалуронидазы очень зависит от времени лечения, природы средства для доставки лекарства, числа применений и, возможно, степени изменения формы роговицы для данного пациента. В общем используются концентрации в интервале от 50 ед/10 мкл до ~3000 ед/10 мкл, предпочтительно, в интервале от 500 ед/10 мкл до ~1000 ед/10 мкл и, наиболее предпочтительно, около 1500±10% ед/10 мкл.
Рецептура образца энзима с концентрацией 1000 ед/10 мкл следующая:
100000 ед бычьей гиалуронидазы (в виде лиофилизированного порошка) соединяют с 1 мл дистилированной воды и достаточным количеством NaCl, двухосновного NaPO2 и сыворотки бычьего альбумина с получением изотонического раствора. Измеряют pH и поддерживают его равным 5-7 (около биологического pH). HCl (0,5 моль) по каплям можно добавить для снижения pH, а для повышения pH добавляют NaOH.
Было установлено, что подходящая доза гиалуронидазы для смягчения роговицы глаза млекопитающего находится в интервале ~50-5000 ед энзима на мг субстрата-мукополисахарида роговицы.
В частности было найдено, что безопасными и эффективными являются дозы 100-1500 ед/мг субстрата. При низких дозах можно практиковать множественное применение, в то время как единичное применение эффективно при более высокой дозе энзима.
В соответствии с настоящим изобретением для смягчения роговицы могут быть использованы другие энзимы, которые действуют на протеогликановые структурные компоненты роговицы. Например, вместо гиалуронидазы или в добавление к ней могут быть использованы такие энзимы, как хондроитиназа ABC, хондроитиназа AC, кератаназа и стромелизин.
Эти энзимы действуют на различные протеогликановые компоненты роговицы, как показано в нижеследующей таблицу 1. Предпочтительно для смягчения роговицы пациента использовать комбинацию энзимов. Полагают, что разрыв различных структурных компонентов роговицы в одно и то же время вызывает более быстрое смягчение роговицы. Примером препарата для деструкции протеогликанов является Dispase TM, производимая Boehringer Mannheimm Biochemicals (Indianapolis, Indiana), которая состоит из неспецифической нейтральной протеазы из Bacillius polymyxa.
Энзимы, разрушающие коллагеновые компоненты роговицы, можно также использовать в методах смягчения роговицы по данному изобретению. Как показано в таблице 2, матрикс металлпротеиназы 1 и матрикс металлпротеиназы 2 разрушают различные типы коллагена. Такие энзимы можно использовать индивидуально или в смеси с энзимами, расщепляющими протеогликановые компоненты роговицы. Конечно, другие смягчающие роговицу агенты также можно использовать в сочетании с энзимами, действующими на протеогликановые или коллагеновые компоненты роговицы. Другие энзимы или рецептуры могут также обеспечить приемлемые результаты, что хорошо известно специалисту в данной области.
B. Эндогеннные энзимы, используемые в энзим-ортокератологии cогласно другому варианту изобретения для смягчения роговицы применяют вместо экзогенных энзимов эндогенные, то есть энзимы, которые уже присутствуют в глазах субъекта. Эндогенные энзимы, способные разрушать структурные компоненты роговицы, обычно находятся в глазах млекопитающих в пассивном состоянии. Для того, чтобы использовать такие энзимы, их, следовательно, прежде всего, нужно активировать. Механизм активации эндогенного энзима, конечно, будет меняться от энзима к энзиму. Эндогенные энзимы, являющиеся металлопротеиназами, например, могут быть активированы применением активатора, такого как интерлейкин-1. Другие известные активаторы металлопротеиназ, считающиеся эффективными, включают фактор некроза опухоли, моногидрат мононатрийурата, 4-аминофенилуксусную ртуть, амилоид A человеческой сыворотки, B2 - микроглобин человека и хлорид меди. Подобным образом полагают, что эндогенные энзимы, которые разрушают протеогликановые компоненты роговицы, могут быть активированы при помощи активаторов этих энзимов.
Иначе эндогенные энзимы могут быть активированы путем инактивации ингибиторов этих энзимов. Например, иодацетамид, выпускаемый Sigma Chemicel (St. Louis, Missouri) может быть введен в роговицу для того, чтобы инактивировать ингибиторы эндогенных энзимов металлопротеиназы. Как только ингибитор эндогенного энзима инактивируется, эндогенный энзим становится активным.
C. Ингибиторы энзимов, используемые в энзим-ортокератологии.
Согласно следующему аспекту настоящего изобретения, раскрываются ингибиторы энзимов и агентов, которые разрушают структурные компоненты роговицы.
Такие ингибиторы используются для замедления или остановки реакций, смягчающих роговицу, при этом контролируется скорость смягчения и/или степень смягчения роговицы, производимые за счет введения энзима или агента в глаз. Полагают, что путем замедления или прекращения процесса смягчения роговицы, ингибитор позволяет начать действовать природным механизмам субъекта по восстановлению или замене поврежденных или модифицированных структурных компонентов роговицы и процессу перестройки роговицы и возвращения ее в первоначальное структурное целое. Этот процесс можно назвать "отверждением" оболочки. Следовательно, ингибиторы могут быть использованы для более тщательного контроля степени смягчения, которое возникает в результате применения энзима или агента, вызывающего смягчение роговицы.
Среди ингибиторов, используемые по данному изобретению, находятся ингибиторы специфических энзимов, используемых для смягчения роговицы. Эти ингибиторы останавливают процесс смягчения путем ингибирования энзимов, которые разрушают коллаген, протеогликан и другие структурные компоненты роговицы.
Альтернативно, ингибиторы могут действовать путем изолирования активатора энзима, который разрушает структурные компоненты роговицы, или может действовать иначе, предотвращая активацию таких энзимов активатором. Если используют неэнзимные средства смягчения роговицы, например, химические средства, можно применять такой ингибитор, который изолирует или дезактивирует такое средство смягчения в роговице.
Ингибиторы по данному изобретению, которые ингибируют энзимы, могут быть ингибиторами как экзогенных, так и эндогенных энзимов. Например, если для смягчения роговицы применяют экзогенный металлопротеиназный энзим, для желаемого замедления или прекращения смягчающей активности металлопротеиназного энзима можно использовать ингибитор металлопротеиназы. Среди таких ингибиторов находятся ЭДТА (этилендиаминтетрауксусная кислота), N-этиламин, циклогексимид, 1,10-фенантролин и фенилметансульфонилфторид. Если желательно ингибировать энзим коллагеназы, можно использовать ЭДТА или цистеин. И если энзим разрушает мукополисахариды, например, гиалуронидазу, можно использовать ионы железа (Fe2+) или меди (Cu2+) в концентрации ~10-5 M.
Специалисту в данной области хорошо известны ингибиторы других эндогенных и экзогенных энзимов.
D. Подбор энзимов и ингибиторов и их доз.
Специалисты в данной области обычным экспериментированием могут подобрать энзимы, ингибиторы и другие агенты, используемые по данному изобретению, а также подходящие дозы таких агентов. Такие опыты могут заключаться в определении дозы энзима, ингибитора или другого агента для глазных яблок донора (глаз), укрепленных в пластиковых модельных гнездах или определении такой дозы на лабораторных животных. Короче говоря, для определения соответствующего количества известного смягчающего агента или агента, испытываемого на его способность смягчать роговицу, в роговую оболочку глаза донора или подопытного животного вводится определенная доза энзима или агента и затем определяется смягчающее действие агента.
Для того, чтобы определить, эффективен ли энзим в процессе смягчения роговицы или, если энзим является известным смягчающим агентом и нужно определить его дозу, энзим вначале смешивают с носителем, приемлемым для млекопитающего фармакологически. Предпочтительно энзим брать в виде лиофилизорованного (сухого) порошка и растворять в физиологическом растворе. Однако, специалисту ясно, что можно использовать множество фармакологически приемлемых носителей, которые не влияют на действие энзима. Испытуемая доза энзима в растворе затем вводится в испытуемую роговицу для того, чтобы определить смягчающее действие на роговицу. По одной методике испытуемый энзим вначале вводится в глазные яблоки (глаза донора), укрепленные в пластиковых гнездах. Эта процедура особенно предпочтительна для определения действия энзима на роговицу человека, так как таким образом роговица человека может быть исследована без проведения эксперимента на живом человеке. Донорское глазное яблоко используемое по этой методике, подготавливают для эксперимента путем инъекции в него количества физиологического раствора, достаточного для поддержания внутриглазного давления в глазном яблоке, приблизительно равного 20 мм Hg. Испытуемая доза энзима затем вводится в роговицу донора. Это можно осуществить, например, инъекцией энзима в роговицу. Обычно хрусталик становится после этого непрозрачным вследствие введения воды в глаз и изменения показателя преломления глаза. По окончании промежутка времени, нужного для эксперимента, глазное яблоко затем изучается на предмет смягчения роговицы, и, если таковое произошло, то какова степень этого смягчения.
Изучение роговицы можно осуществить например, при помощи щелевой лампы, которая может определить наличие и прозрачность роговицы. Если роговица исчезает после обработки, тогда использованная доза была завышена. Если роговица не разрушалась, следует провести ряд опытов для определения степени смягчения роговицы, что хорошо известно специалисту в данной области. Например, обработанную роговицу затем можно (подвергнуть: 1) пахиметрии для определения толщины роговицы; 2) компьютерной топографии для оценки топографических изменений роговицы; 3) измерению предела прочности роговицы при растяжении; 4) измерению растяжимости роговицы в ответ на увеличенное внутриглазное давление; 5) кератометрии для измерения кривизны центрального участка роговицы и 6) ретиноскопии для измерения дефектов преломления роговицы. Величины измерений можно сравнить с величинами, полученными до введения энзима.
Кроме того, обработанная роговица в донорском глазном яблоке может быть подвергнута ряду других испытаний для определения прочности и жизнеспособности роговицы после обработки. Например, световая, сканирующая и электронная микроскопия может быть использована для изучения морфологии роговицы; может быть приготовлена тканевая культура для определения жизнеспособности клеток роговицы после обработки; можно провести биохимическое изучение коллагенов и других структурных единиц после обработки, включая использование оптического многоканального анализатора, который позволяет осуществить спектроскопию ткани роговицы, а также иммунофлуоресцентное изучение с помощью антител, специфических к структурным компонентам стромы и испытуемым энзимам.
Иммунофлуоресцентный анализ, в частности, можно использовать для оценки соединяющих участков (сайтов) испытуемого энзима в роговице.
Вышеописанные опыты с глазными яблоками донора и роговицами можно использовать для проверки того факта, что использование конкретного энзима не подвергает риску прозрачность роговицы, не уменьшает жизнеспособность клеток и не повреждает структурную целостность роговицы. Исследование применения энзима для роговицы подопытного животного, однако, также желательно, чтобы убедиться, что энзим не оказывает нежелательного действия на живых млекопитающих, что не было установлено при исследованиях глаз донора. Для того, чтобы изучить эффект действия конкретного испытуемого энзима, исследуемая доза энзима на фармакологически приемлемом носителе (в растворе) используется для подопытного животного, в данном случае, для млекопитающего, для того, чтобы ввести этот энзим в роговицу животного. После введения энзима в роговицу животного, роговицу подвергают следующим исследованиям: пахиметрии для измерения толщины роговицы, компьютерной топографии для оценки топографических изменений поверхности роговицы; исследованию при помощи щелевой лампы для определения чистоты оболочки, передней камеры и зрачка; тонометрии для измерения внутриглазного давления; фондескопическому изучению оптического нерва и сетчатки глаза; кератотомии для измерения кривизны центрального участка роговицы; ретиноскопии для измерения дефектов преломления; и окрашиванию флуоресцеином или Бенгальским Розовым для выявления повреждения эпителия роговицы. Данные измерений можно сравнить с аналогичными данными, полученными до применения энзима, а также с данными, полученными для неподвергнутого лечению глаза животного. Вид активаторов эндогенных энзимов и других смягчающих роговиц агентов, не описанных здесь, а также соответствующие дозы этих известных и неизвестных агентов можно определить, как описано выше, в отношении определения вида и дозы энзимов.
Для того, чтобы определить, действует ли какой-то агент как ингибитор смягчения роговицы или эффективна ли определенная доза ингибитора, определенное количество экзогенного энзима для смягчения роговицы, активатора эндогенного энзима или другого смягчающего роговицу агента вначале вводится в целый ряд глазных яблок доноров или в роговицы подопытного животного, как описано выше. При использовании подопытных животных, как только роговицы начинают смягчаться, одна роговицы подопытного животного обрабатывается затем испытуемой дозой ингибитора или агента, который должен быть исследован на ингибирующее действие, для того, чтобы определить, действительно ли эта доза ингибитора или испытуемого агента может прекратить процесс смягчения. Другая роговица остается как контрольная при использовании глазных яблок донора, может быть исследовано большое количество роговиц, но одна остается контрольной. Обработанные роговицы могут быть исследованы с применением определенной дозы ингибитора или испытуемого агента. Контрольная роговица и испытуемые роговицы должны обрабатываться приблизительно в течение одного и того же промежутка времени, чтобы провести корректное сравнение эффективности ингибиторов и испытуемых агентов на исследуемой роговице.
После проведения испытания, мягкость или степень деструкции структурных компонентов каждой роговицы сравниваются с использованием методик, описанных выше по отношению к определению степени смягчения роговицы в случае изучения энзимов в качестве смягчающих агентов. Если обработанная ингибитором роговица является менее мягкой, чем необработанная, это свидетельствует о том, что испытанная доза ингибитора приемлема для ингибирования процесса смягчения.
II. Способы применения энзимов/агентов
Вышеуказанные энзимы и агенты для смягчения роговицы могут быть применены любым известным способом. Например, энзим или агент может вводиться путем непосредственной инъекции в глаз в месте, близком к роговице. В этом случае энзим или агент следует перемешать в среде фармакологически приемлемого для субъекта носителя, который не изменяет эффективность энзима или агента. Применение инъекции как метода введения особенно предпочтительно, когда агент или энзим состоят из больших молекул. Термин "большая молекула" означает молекулу, которая слишком велика или имеет слишком высокий молекулярный вес, чтобы диффундировать в роговицу с наружной поверхности глаза, или же диффундирует слишком медленно, чтобы оказывать ощутимый эффект смягчения и поэтому должна быть введена в роговицу другими методами, кроме диффузии. Этот термин также означает любую молекулу, которая не может диффундировать вглубь роговицы по какой-либо другой причине.
Инъекция, однако, является таким методом введения, который неприятен для субъекта, и поэтому не является предпочтительным, когда возможны другие методы введения энзима или агента. Более предпочтительны методы, ускоряющие диффузию через глаз в роговицу. Такие методы включают, например, применение липосом для введения энзима или агента. Энзим или агент "упаковывают" в липосомы, которые могут проходить через липидную растворимую мембрану эпителия роговицы в строму роговицы. Другие методы диффузии включают применение электрического тока для того, чтобы сделать внешнюю мембрану глаза более проницаемой для прохождения энзимов и агентов, известное как ионтофорез.
Согласно предпочтительному варианту, энзимы и агенты для смягчения роговицы субъекта вводят в виде глазных капель. Этот метод особенно предпочтителен, когда вводимые агент или энзим не являются большими молекулами. Например, иодацетамид вводят в виде глазных капель. Раствор 0,05-0,25% (г/100 мл объема) иодацетамида готовят растворением 0,05-0,25 г иодацетамида в 100 мл физиологического раствора. Затем одну или две капли раствора вводят субъекту каждый час в течение 4-х часов. Еще более предпочтительный метод применения агентов и энзимов заключается во введении агентов и энзимов непосредственно из контактной линзы. Как будет подробно обсуждено ниже, методы согласно данному изобретению включают надевание жесткой контактной линзы на смягчившуюся роговицу для того, чтобы изменить форму этой роговицы, придав ей желаемую конфигурацию. Согласно этому варианту настоящего изобретения, надевание контактной линзы и введение энзима и/или агента происходят одновременно. Этот вариант наиболее предпочтителен, когда энзим и/или агент не являются большой молекулой и поэтому способны диффундировать от внешней поверхности глаза в роговицу.
В качестве примера осуществления этого варианта данного изобретения приводится следующий. Необходимое для смягчения роговицы количество гиалуронидазного энзима с рецептурой, описанной выше, загружают в камеру внутри жесткой контактной линзы, предпочтительно газопроницаемой. Такая линза может быть одной из линз, показанных на фиг. 2, 4D, 5D, 12 и 14, которые имеют камеру для хранения раствора энзима или агента. Альтернативно, энзим или агент могут быть загружены в (или ими можно пропитать) мягкую линзу, способную захватить энзим или агент при погружении в раствор, содержащий энзим или агент. Энзим или агент могут быть введены в комбинацию мягкой и жесткой линз, как показано на фиг. 8B.
Во всех вышеуказанных вариантах контактной линзы для введения энзима или агента, энзим или агент вводятся по мере диффузии (выхода из) из камеры в линзе или из материала линзы (если энзим или агент пропитали мягкую линзу). Если используемый энзим является гиалуронидазой, дозы обычно находятся в интервале от двух до шести капель и, предпочтительно от трех до пяти капель с концентрацией 500 ед/мкл рецептуры, описанной выше. Дозы для различных условий и видов контактных линз могут оптимизироваться специалистом в данной области простым экспериментированием. В соответствии с одним методом введения при помощи контактных линз по данному изобретению, энзимы и агенты могут быть введены в глаз с помощью жесткой контактной линзы 10, как показано на фиг. 1-2. Эти линзы могут быть изготовлены из известного кремнийсодержащего фторакрилатного полимера, который является газопроницаемым. Линза снабжена внутренней камерой 11 для хранения смягчающего роговицу агента. Камера 11, предпочтительно, представляет собой радиально симметричное пространство, окружающее всю линзу 10 между передней поверхностью 12 и задней поверхностью 13 линзы 10.
Жесткие линзы для данной цели могут быть легко изготовлены токарной обработкой, формованием или фрезерованием задней части и передней части, которые во время изготовления могут быть скреплены вместе с образованием линзы склеиванием известными клеями по известной технологии. Камера 11 может быть образована токарной обработкой - созданием кольцевой полости на выпуклой поверхности задней части линзы перед окончательным изготовлением линзы. Хотя, согласно данному изобретению, можно использовать различные размеры, предпочтительно, чтобы линза 10 была снабжена кольцевой камерой 11, имеющей ширину около 1,0-1,5 мм и глубину около 0,05-0,1 мм.
В задней части линзы 10 изготавливают множество микроскопических отверстий 16 для того, чтобы обеспечить переход жидкости из камеры 11 в глаз, тем самым ускоряется введение энзима/агентов в роговицу. Эти отверстия 16 могут быть изготовлены механическим или лазерным сверлением или путем формования до сборки частей линзы. Предпочтительно просверливать отверстия 16 при помощи механической дрели с угольным сверлом. Накачивающее действие век в соединении с естественным выделением слез помогает прохождению энзима или агента сквозь крошечные отверстия 16. Предпочтительно, отверстия изготавливают механической дрелью с микроскопическим угольным сверлом и они имеют диаметр ~0,002-0,01 мм, предпочтительно, ~0,005 мм. Число и диаметр отверстий 16 может меняться, влияя на время прохождения жидкости, как это очевидно специалисту. В общем, однако, для интервала диаметров, указанного выше, следует изготавливать от 3 до 10 отверстий. В предпочтительном варианте изготовления линзы 10 на фиг. 1 и 2, задняя часть линзы имеет толщину в центре ~ 0,12 мм и кольцевая полость вытачивается на глубину ~0,075 мм. Ряд отверстий 16, каждое диаметром ~0,005 мм, высверливаются на дне камеры 11, причем располагаются на равных расстояниях друг от друга по периферии камеры 11 для обеспечения сообщения с задней поверхностью 13 линзы. Хотя на фиг. 1 показано пять отверстий, число их будет меняться в зависимости от желаемой скорости введения энзима или агента из камеры 11. Передняя часть линзы, имеющая в центральной части толщину около 0,12 мм, затем крепится к задней части, охватывая кольцевую полость и образуя камеру 11, таким образом получается линза, имеющая в центре толщину ~0,24 мм. Соединение может быть выполнено нанесением небольшого количества клея, например, ConciseTM, продаваемого 3M (St. Paul, Minnesota). Другие средства для соединения задней и передней частей контактной линзы очевидны для специалиста в данной области.
Радиусы кривизны задней части (основная кривая 14, промежуточная кривая 15 и периферическая кривая 17) линзы 10 выбраны таким образом, чтобы изменить форму изгиба передней части роговицы, придав глазу эмметропность (не требуется коррекции зрения). Задняя и передняя конфигурации контактной линзы в соответствии с данным изобретением похожа на конфигурации, используемые в обычных методиках ортокератологии. В общем выпуклая передняя поверхность линзы 12 приближается к однородному радиусу кривизны вдоль всех плоскостей и может изменяться от несферической до сферической или любой другой конфигурации, необходимой пациенту. Вогнутая задняя поверхность 13 линзы 10 разделена на несколько дискретных зон, каждая из которых имеет единственную в своем роде кривизну. Например, ссылаясь на фиг. 2, центральная основная кривая 14 расположена радиально симметрично около центральной части линзы 10. Промежуточный задний изгиб 15 расположен кольцеобразно около радиальной внешней периферии задней центральной основной кривой 14. К внешней стороне промежуточный задней кривой 15 примыкает третья периферическая задняя кривая 17. Таким образом, можно считать, что линза 10 состоит из трех различных зон, показанных на фиг. 1, центральной оптической зоны 18, промежуточной зоны 19 и периферической зоны 20.
Предпочтительно, в соответствии с настоящим изобретением, кольцевая камера 11 расположена внутри промежуточной зоны 19.
В соответствии с другим аспектом настоящего изобретения, создана контактная линза, которая состоит из двух слоев, которые соединены вместе, как показано на фиг. 12 и 14. В этом образце может находиться большая камера для хранения энзима или агента.
В этой контактной линзе, передняя часть 110 контактной линзы 100 изготавливается с передней поверхностью 112 и задней поверхностью 114. Задняя часть 113 контактной линзы 100 также изготавливается с передней поверхностью 115 и задней поверхностью 117. Внешний периметр 120 задней поверхности 114 передней части 110 имеет тот же самый радиус кривизны, что и внешний периметр 124 (лучше показан на фиг. 11) передней поверхности 115 задней части 113. Таким образом, когда задняя поверхность 114 передней части 110 и передняя поверхность 115 задней части 113 соединяются вместе, между внешними периметрами 120, 124 передней и задней частей образуется изолирующий слой.
Однако в центральной части 126 передней части 110, задняя поверхность 114 имеет более крутой радиус кривизны, чем передняя поверхность 115 центральной части 128 задней части 113.
Благодаря этому более крутому радиусу кривизны, когда передняя часть 110 и задняя часть 113 соединяются вместе, между центральной частью 126 передней части 110 и центральной частью 128 задней части 113 контактной линзы 100 образуется камера 130. Объем камеры 130 может быть регулируемым путем изменения радиусов кривизны задней поверхности 114 центральной части 126 и передней поверхности 113 центральной части 128, что будет очевидно специалисту в данной области. До изготовления линзы, одно или более отверстий 116 изготавливают в центральной части 128 задней половины 113 контактной линзы этой конструкции. Предпочтительно отверстия 116 изготавливать механическим сверлением при помощи микроскопического угольного сверла или при помощи лазера, например, аргонового, диаметр отверстий равен ~0,002-0,01 мм, предпочтительно ~ 0,005 мм. Число и диаметр отверстий 116 может меняться для регулирования времени введения агента, как это очевидно специалисту. Таким образом, скорость, при которой доза энзима или агента проходит из камеры 130 в значительной степени контролируется размером и числом отверстий, имеющихся в центральной части 128 задней части 113 линзы 100. В общем, однако для величины диаметров, указанной выше, достаточно от 3 до 10 отверстий. Предпочтительно, эти отверстия 116 располагать вокруг центральной части 128 задней половины 113 контактной линзы 100 для обеспечения сообщения между камерой 130 и поверхностью глаза субъекта, который носит линзу 100.
В предпочтительном варианте выполнения линзы 100 (фиг. 12), задняя половина 113 линзы 100 имеет толщину в центральной части ~0,125 мм. У передней половины 110 линзы 100 толщина в центре, предпочтительно, равна ~0,125 мм. Когда передняя половина 100 и задняя 113 соединяются, образуется линза, у которой толщина в центральной точке равна ~0,24 мм. Если желательно менять форму роговицы быстрее, можно использовать линзу большей толщины, которая оказывает большее давление на роговицу для придания желаемой конфигурации. Соединение частей линзы можно осуществлять с применением достаточного количества клея, например. ConciseTM, продаваемого фирмой 3M (St. Paul, Minnesota). Специалисту в данной области очевидны другие способы соединения. Как и в случае других вариантов настоящего изобретения, радиусы кривизны вогнутой части задней поверхности 117 задней части 113 линзы 100 выбираются таким образом, чтобы можно было изменить изгиб передней части роговицы, придав ей желаемую форму и уменьшив дефекты преломления. Таким образом, задняя и передняя конфигурации контактной линзы согласно данному варианту настоящего изобретения подобны тем, которые используются в обычной ортокератологии и очевидны специалисту в данной области. Линза по данному варианту, предпочтительно, изготавливается из известного кремнийсодержащего полифторакрилата. Такие жесткие линзы изготавливают токарной обработкой, формованием или фрезерованием задней и передней половин. После изготовления этих половин, они могут быть прикреплены друг к другу с образованием целостной линзы с использованием клеев, обычной технологии соединения известных специалисту.
Например, для соединения частей линзы можно применять адгезив. Примером такой адгезионной системы является ConciseTM, выпускаемая фирмой 3M (St. Paul, Minnesota).
Альтернативным выполнением контактной линзы в соответствии с этим аспектом настоящего изобретения является линза, имеющая камеру на периферийном участке в отличие от камеры в центральной части линзы (фиг. 11, 12). Такая конструкция линзы показана на фиг.13 и 14. Как показано на этих фигурах, линза 150 состоит из передней части 160 и задней половины 170, которые соединены таким же образом, как и линза, показанная на фиг. 11 и 12. По этому варианту камера 182 находится в промежуточной части 180 линзы 150. На фиг.14 показана линза, у которой камера 182 находится в промежуточной части 180 линзы 150, она образована частью пространства задней поверхности 162 передней половины 160 линзы 150, которая имеет более крутой радиус кривизны, чем у оставшейся части задней поверхности передней части 160 линзы 150. Как и в случае предыдущего варианта контактной линзы с камерой, объем энзима или агента, которые могут содержаться в линзе и таким образом вводиться субъекту, в значительной степени определяется радиусом кривизны задней поверхности 162 передней половины 160 линзы 150 в промежуточной части 180 линзы, а также радиусом кривизны передний поверхности 172 задней половины 170 линзы 150 в промежуточной части 180 линзы.
Задняя половина 170 линзы 150 также снабжена отверстиями 190 в промежуточной части 180 линзы. Эти отверстия служат для передачи содержимого камеры 182 из этой камеры в глаз субъекта. Число и размер отверстий 190 в значительной степени определяют скорость поступления энзима или агента в глаз. Хотя варианты выполнения линз, показанные на фиг. 11-14, изготовлены соединением передней и задней половин линзы, специалисту в данной области очевидно, что возможны и другие методы образования вышеописанных камер.
Описанные линзы, применяемые в энзим-ортокератологии, могут использоваться для ношения днем и/или ночью. Роговица обычно смягчается и меняет свою форму в течение промежутка времени от нескольких часов до нескольких дней, ускорение изменения формы достигается обычными методами.
Линза 10 по настоящему изобретению может использоваться для коррекции близорукости (миопии) (фиг. 3A), астигматизма (фиг. 4A-D) и гиперопии. Гиперопию корректируют (фиг. 5A-B) при помощи линз, показанных на фиг. 5C-D и фиг. 15 и 16.
В соответствии с дальнейшим методом введения агентов согласно данному изобретению экран 22 мягкой линзы (фиг. 6) пропитывают определенным количеством энзима/агентов. Затем мягкая линза вставляется в глаз и носится в течение нескольких часов для введения энзима и/или агента в роговицу. После того, как энзим и/или агент смягчат строму роговицы в достаточной степени, мягкая линза или снимается или растворяется. Один тип мягкой линзы, используемый по указанному методу, изготавливается из коллагена, который имеет тенденцию впитывать сравнительно большой объем раствора, содержащего энзим и/или агент, и выделять их сравнительно медленно. Такой материал может быть высокочистым бычьим коллагеном. Диаметр, предпочтительно, равен 13,5-16,0 мм. Радиус кривизны равен 8,0-9,5 мм. DK (мера проницаемости кислорода) должен быть равен ~50 и степень гидратации H2O должна быть ~83%. Конечно, энзим или агент, используемый по этому варианту, не должен разрушать коллаген, как, например, коллагеназа.
Примером линзы, которая, как было установлено, хорошо подходит для осуществления этого метода, является MedilensТМ - экран, выпускаемый Chiron Opthalmics, Inc. of Irvine, California, MedilensTM представляет собой прозрачную, гибкую, тонкую пленку, изготовленную из бычьей ткани. Эта ткань содержит высокий процент коллагена, чем напоминает молекулы коллагена человеческого глаза. MedilensTM - экран обеспечивает защиту и смазку поверхности глаза, постепенно растворяясь в течение 24 часов. Сухой вес линзы равен ~5,5 мг, а вес в мокром состоянии (когда линза пропитана энзимом по данному изобретению) равен ~34 мг. Пропитку осуществляют погружением линзы в раствор, как описано выше, примерно на 60 мин при комнатной температуре. Величина поглощения линзой равна ~28,5 мг, а степень гидратации ~84%. В единицах объема величина поглощения линзой равна ~200-300 мкл (микролитров). Это эквивалентно примерно 4-6 каплям раствора или 28 мг при концентрации 150 ед/мл.
Другие типы материалов для мягких линз имеют тенденцию поглощать меньшее количество раствора, содержащего энзим или агент, а также выделять их более быстро. Примерами таких материалов являются обычно гидрофильные материалы для мягких линз, например, этафилкон A (etafilcon A) и фемфилкон A (phemfilcon A), поставляемые Vistacon and Wesley Jessen. Эти линзы могут быть различных видов - съемные и для длительной носки. Было установлено, что для данного метода пригодны линзы с содержанием воды, равным 58-70. После того, как мягкая линза 22 или другое средство выделит энзим и/или агент на роговицу, что приведет к ее смягчению, на роговицу надевается жесткая контактная линза, не содержащая энзима.
Жесткая контактная линза приводит к быстрому изменению формы смягченной роговицы. Используют контактную линзу с таким радиусом кривизны задней поверхности, который изменит форму передней части роговицы до такой кривизны, которая необходима для эмметропии. Процесс изменения формы может длиться от нескольких часов до нескольких дней.
Согласно предпочтительному варианту жесткая контактная линза надевается на центральную часть мягкой контактной линзы, содержащей энзим или агент, в то время, когда эта мягкая контактная линза находится в глазу пациента. Вследствие внутриглазного давления смягчившаяся роговица стремится к более крутому радиусу кривизны. Если в случае гиперопии это является желательным, то в случае лечения миопии и других дефектов этот процесс следует контролировать. И даже при лечении гиперопии степень увеличения кривизны роговицы следует контролировать. Следовательно, желательно помещать жесткую контактную линзу на мягкую линзу, выделяющую энзим и/или агент, для того, чтобы контролировать изменение формы роговицы, а не одевать жесткую контактную линзу прямо на роговицу, чтобы изменить ее форму.
Наиболее предпочтительно наплавлять жесткую линзу на центральную часть мягкой контактной линзы, которая служит для введения энзима или агента в роговицу. Таким путем можно избежать ошибок вследствие неправильной установки жесткой линзы на мягкую линзу.
В соответствии с дальнейшим вариантом настоящего изобретения используется контактная линза 24 типа "сатурн" (saturn), например, SoftpermTM, продаваемая фирмой Sola Barnes Hynds-Pilkington (фиг.7). Этот тип линзы включает линзу с жестким центром 26 и периферическую часть 28 мягкой линзы. Жесткий, предпочтительно, газопроницаемый центр 26 не содержит энзима и/или агента, в то время как часть 28 мягкой линзы пропитана раствором, содержащим энзим и/или агент.
Периферическая часть 28 линзы 24 типа "сатурн" может быть изготовлена из сополимера synergicon A, поставляемого Precision-Cosmet. Жесткий негидрофильный центр 26 обычно имеет диаметр 5,5-6,5 мм и содержит только 0,2% абсорбированной воды (фиг. 7). Внешняя периферическая часть 28 полимеризуется, образуя мягкую гидрофильную полость, расположенную по окружности вокруг внешней периферии центра 26, и имеет ширину 3,0-4,0 мм и степень поглощения воды, равную ~25%. Изгиб линзы типа "сатурн" равен 7,2-8,2 мм.
Когда пациент носит линзу 24 типа "сатурн", энзим/агенты выделяются в роговицу из мягкой периферической рубашки 28, смягчая роговицу в течение нескольких часов. Жесткий центр 26 линзы немедленно начинает изменять форму смягчившейся роговицы. Изменение формы длится от нескольких часов до нескольких дней. Часть 28 мягкой линзы является более удобной, меньше режет глаз, что способствует протеканию процесса Ортокератологии.
Энзим и/или агент выходят из роговицы через несколько дней и роговица затем "затвердевает", приобретя новую форму. Линза 24 или другая жесткая линза носится, предпочтительно, в течение нескольких дней для стабилизации новой формы. Затем линзу вынимают.
Для введения энзима и/или агента в роговицу и одновременного изменения ее формы можно также использовать систему 34 контактных линз с "вплавленной мягкой линзой" (фиг. 8A и 8B). По этому варианту кольцо 30 из материала, применяемого для мягких линз, вплавляется во внутреннюю промежуточную изогнутую часть и периферическую изогнутую часть жесткой газопроницаемой контактной линзы 32. Полученная вплавленная (мягкая) линза 34 пропитывается раствором энзима/агентов, и энзим удерживается в части 30 мягкой линзы. Затем энзим выделяется в роговицу, смягчая ее.
Жесткий, предпочтительно, газопроницаемый центр 32 имеет заднюю центральную изогнутую поверхность 35, которая изменяет форму кривизны передней поверхности роговицы, придавая ей конфигурацию, исправляющую дефекты преломления, предпочтительно, конфигурацию, которая делает глаз эмметропным. Центр 35 жесткой контактной линзы предпочтительно выполнять из кремнийсодержащего полифторакрилата с Dk около 60-92. Диаметры колеблются от 7,5 мм до 10,5 мм, а радиус кривизны 35 жесткой линзы 32 может быть равен ~7,5-9,0 мм. "Наплавленная" часть 30 мягкой линзы выполнена из гидрофильного материала для мягких линз, например, etafilcon'a A или phemfilcon'a A.
Соединение кольцевой части 30 с жесткой контактной линзой 32 осуществляется склеиванием. Ширина мягкой кольцевой части 30 меняется от 0,75 до 1,5 мм с каждой стороны.
III. Процедура энзим-ортокератологии.
Согласно методу энзим-ортокератологии контактная линза должна плотно прилегают к передней поверхности роговицы.
Когда надевается контактная линза с камерой, энзим и/или агент выделяются во времени и проходят через эпителий роговицы и мембрану Bowman'a, достигая в конце концов стромы (substantia propria).
В случае миопии (фиг.3A) роговица обычно имеет позитивную форму, более крутую в центре 33 и более плоскую на периферии 36. После того, как жесткая газопроницаемая линза помещается на глаз, нажим век и движение линзы вызывают сплющивание центральной изогнутой части 37 роговицы. Внутреннее давление в глазу заставляет парацентрическую роговицу 38 выдвигаться или становиться более выпуклой. Роговица становится сферической, с меньшим радиусом кривизны центральной части (37, 38). Свет, попадающий на роговицу, отражается поэтому меньше, то есть назад, ближе к сетчатке глаза (фиг.3B). Это уменьшает или исправляет миопию, что вызывает большую степень отражения света и таким образом приводит к фокусированию изображения впереди роговицы (фиг.3C).
Как только достигается соответствующая форма роговой оболочки, энзим и/или агент рассеиваются из роговицы и последняя "отверждается". Кроме того, можно вводить в этот момент ингибитор для ускорения процесса отверждения. Затем в течение короткого периода времени (обычно нескольких дней) носят фиксирующую контактную линзу для стабилизации формы роговицы, затем эту линзу вынимают. Фиксирующая линза может иметь те же параметры жесткой контактной линзы, которые упомянуты при описании линзы на фиг.1 и 2. Фиксирующая линза не содержит энзима и является последней в системе лечения методом энзим-ортокератологии. Задняя изогнутая поверхность этой линзы помогает обработанной роговице удерживать новую форму. Выравнивание восстановленных или замещенных мукополисахаридных цепей и коллагеновых фибрилл соответствует новой форме, созданной при помощи жесткой линзы. Структурные компоненты роговицы удерживают эту форму при помощи новой "памяти", хранящей только новую форму. Стабильность и постоянство поддерживаются без фиксирующей линзы.
После удаления линз после энзим-ортокератологии не требуется ношения линз или очков. С использованием прежних методов ортокератологии без применения энзимов после удаления фиксирующих контактных линз роговица имела тенденцию к возвращению старой формы, как резиновая лента. Это происходит потому, что неизменившиеся мукополисахариды и коллагеновые фибриллы сахраняют "память" о форме роговицы до лечения методом ортокератологии.
Метаболические процессы в роговице в значительной степени ускоряются при повышенной температуре. Изменение формы происходит более быстро, если метаболизм ускоряется под воздействием тепла.
Если желательно, при энзим-ортокератологии можно применять тепловую радиацию и другие методы нагрева роговицы. Однако, применение тепла для изменения формы роговицы необязательно.
A. Образцы жестких контактных линз.
Одним из вариантов жестких контактных линз, созданных для энзим-ортокератологии, является линза, изготовленная из кремнийсодержащего полимера фторакрилата (сополимер метилметакрилата с дифторитаконатсилоксанилом), производимого Paragon Optical. Высокая проницаемость по кислороду DK 60-DK 92x10-11, позволяет пациенту спать с надетыми линзами, если это необходимо. Линза имеет отличную смачиваемость с низким углом смачивания, равным 26. Основная кривая линза колеблется от 6,5 до 9,0 мм, в зависимости от кривизны центральной части роговицы. Общий диаметр линзы равен размеру основной кривой в мм +1,3-1,8 мм и амплитуда составляет 7,5-10,5 мм (общий диаметр на фиг.1).
Центральная оптическая зона 18 (фиг.1) является прозрачной и корректирует дефекты преломления глаза для получения прекрасной остроты зрения. Диаметр оптической зоны равен 6,5-9,0 мм. Промежуточная зона 19 содержит камеру для энзима и/или агента 11 для выделения раствора в роговицу. Ширина промежуточной зоны 19 равна 0,35-1,0 мм. Промежуточная кривая 15 может быть более крутой или более плоской, чем основная кривая 14 линзы в зависимости от дефекта преломления периферическая кривая 17 является более плоской, чем основная кривая 14 линзы. Ширина периферической зоны 20 равна 0,35-1,0 мм. Периферические кривые 17 создают условия для циркуляции слез и обмена кислорода при моргании.
Сила линзы основана на дефектах зрения пациента и отношения радиусов кривизны линзы и центрального участка роговицы. Толщина линзы равна 0,20 мм в случае 0 силы; 0,01 мм следует вычитать на каждую диоптрию минусовой коррекции и 0,02 мм следует прибавлять на каждую плюсовую диоптрию. Внутренняя кривизна оптической зоны (14 на фиг.2) (основная кривая) рассчитывается, предпочтительно, так, чтобы глаз был эмметропным, когда роговица имеет форму этой кривой. Этого можно достичь при помощи одной-трех линз.
Передняя кривая оптической зоны (12 на фиг.2) имеет радиус, рассчитанный таким образом, чтобы у субъекта не было дефектов преломления и добавилось 20/20 остроты зрения при ношении линзы. Последняя линза будет иметь нулевую преломляющую силу. Все параметры жестких контактных линз зависят в значительной степени от дефектов зрения пациента, радиуса кривизны и размера роговицы и методики подбора, как хорошо известно в данной области.
Эта конструкция линзы без энзима также может быть использована для изменения формы роговицы после ее смягчения при помощи уже упомянутых выше методов введения энзима.
Дальнейший вариант жесткой контактной линзы, специально созданный для лечения гиперопии, показан на фиг.15 и 16. Такая контактная линза должна быть жесткой, как вышеописанные линзы, изготовленные из кремнийсодержащего полифторакрилата. У этого образца линзы вогнутая (задняя) половина линзы 200 выполнена с периферической частью 210, которая имеет асферическую базисную кривую. Центральная часть 230 линзы 200 выполнена так, что вогнутая поверхность центральной части 230 имеет такую форму, которая создает эмметропию. Центральная часть 230 имеет базисную кривую, которая на 2-5 диоптрий круче, чем основная кривая периферической части 210 линзы 200 и имеет радиус кривизны, который круче на 1 мм, чем периферическая часть 210. Базисная кривая центральной части 230 линзы 200 может быть изготовлена так, чтобы обеспечить желаемый радиус кривизны роговицы, который не делает роговицу эмметропной, но который все же делает более изогнутой основную кривую роговицы.
В. Методика лечения миопии методом энзим-ортокератологии
В случае миопии обычно имеется роговица позитивной формы (более крутая в центре 33 и более плоская парацентрально 36), см. фиг.3A. Базисная кривая контактной линзы 14 (фиг.2) должна обычно быть более плоской, чем изогнутая центральная часть 33 роговицы меняет форму на более плоскую кривую 37, а более плоская парацентрическая кривая 36 становится более круто изогнутой формы 38. В результате образуется сферическая роговица из центра к парацентральной части с более плоской центральной кривой. Это снимает миопию, потому что свет преломляется дальше на сетчатке (фиг.3B), а не впереди сетчатки (фиг.3C) и имеет место менее сферическая аберрация.
Как очевидно для специалиста в данной области, для лечения миопии могут использоваться другие образцы линз, имеющие различные диаметры, базисные кривые и толщины. К таким образцам относятся контактные линзы, имеющие асферические базисные кривые и периферические кривые, и линзы, имеющие сферические базисные кривые и асферические периферические кривые.
Следующий пример иллюстрирует метод коррекции миопии при помощи энзим-ортокераталогии. В этом примере у пациента наблюдается 20/300 UVA или миопия в 3 диоптрии; самая плоская центральная часть кривой соответствует 45 диоптриям или 7,5 мм; и парацентрическая кривая - 40 диоптриям и роговица имеет позитивную форму +0,30. Первоначальная жесткая газопроницаемая контактная линза (фиг.1 и 2) содержит энзим по данному изобретению в полой камере 11. Базисная кривая 14 соответствует 42 диоптриям или 8,0 мм (более плоская на 3 диоптрии, чем центральная кривая). Ширина оптической зоны 18 равна 8,0 мм. Сила линзы равна 0. Размер линзы равен 9,6 мм (8,0+1,6 мм). Толщина линзы равна 0,20 мм. Радиус промежуточной кривой 15 равен 7,5 мм или 45 диоптриям (более крутая на 3 диоптрии, чем основная кривая) с шириной 0,50 мм. Периферическая кривая 17 имеет радиус 10,0 мм при ширине 0,3 мм. В линзу загружают определенное количество гиалуронидазы (приблизительно 2-4 капли) с активностью 500 ед/мкл инъекцией под давлением через одно из отверстий 16 при помощи микроскопической иглы. Для загрузки энзима в линзу можно использовать ультразвук. Контактную линзу надевают на роговицу и энзим выделяется в течение промежутка времени от нескольких минут до нескольких дней. Энзим проникает сквозь эпителий и мембрану Боумана (Bowman) в строму, где смягчает слой мукополисахарида. Смягченная, более гибкая роговица меняет форму своей передней центральной кривой (45 диоптрий) на форму базисной кривой 14 задней части линзы (42 диоптрии). Новая передняя базисная кривая роговицы приобретает 42 диоптрии (вместо первоначальных 45). Парацентрическая передняя часть роговицы (40 диоптрий) приобретает 42 диоптрии = 8,0 мм. Теперь роговица имеет сферическую форму. Первоначальные три диоптрии миопии теперь уменьшены и острота естественного зрения улучшилась до нормальной - с 20/300 до 20/20.
Энзим выделяется из роговицы в течение промежутка времени от нескольких часов до нескольких дней, а роговица "отверждается", принимая новую форму, глаз становится эмметропным (коррекции не требуется), с нормальным естественным зрением (20/20). Ингибиторы или другие средства "отверждения" роговицы также могут быть использованы для фиксации изменения формы роговицы. Последняя из серии линз в процедуре по методу энзим-ортокератологии остается в глазу на тот промежуток времени, который необходим для фиксации желаемой новой вычисленной формы кривизны для коррекции зрения после того, как роговица "отверждалась", и действует как фиксирующая линза. Затем она удаляется. Новые контактные линзы надеваются только в том случае, если нужно стабилизировать новую форму роговицы в течение еще нескольких дней, при этом время ношения в течение дня систематически уменьшается, пока не наступит момент, когда линзы больше не нужны. Новая система памяти изменившейся роговицы "помнит" только новую форму, поэтому роговица не восстанавливает старую форму в отсутствие контактных линз.
C. Методика лечения астигматизма методом энзим-ортокератологии.
В случае астигматизма центральный участок роговицы является неровным, что приводит к тому, что изображение на сетчатке растягивается (фиг.4A). Горизонтальный и вертикальный центральный меридианы представляют собой различные кривые 40, 42 (фиг.4B). Контактные линзы для лечения астигматизма могут использовать тороидальную и асферическую базисные кривые 40, 42 (фиг. 4C), промежуточные кривые и периферические кривые, которые могут образовывать призму и/или округление (усечение) 47 (фиг.4C). Первоначально более плоский центральный меридиан глаза 40 меняет форму, становясь более круто изогнутой кривой 44, а первоначально более выгнутый центральный меридиан 42 меняет форму, становясь более плоской кривой 46. Этот процесс приводит к изменению формы центрального участка роговицы, она становится сферической и астигматизм исчезает.
Для коррекции астигматизма используют следующую методику энзим-ортокератологии. Согласно предпочтительному варианту изобретения материалом для изготовления линзы служит кремнийсодержащий полифторакрилат. Базисные кривые 41 (6,0-8,0 мм) могут быть задними тороидальными, передними тороидальными и битороидальными. Самый плоский участок центральной части роговицы выравнивается с более круто изогнутой базисной кривой. Самый круто изогнутый центральный участок роговицы выравнивается с более плоской базисной кривой. Можно использовать асферические или сферические базисные кривые, а также периферические. Диаметр линзы равен базисному изгибу в мм +1,3-1,8 мм. Диапазон величин диаметров равен 7,5-11,5 мм. Диаметр оптической зоны 18 равен базисной кривой в мм и меняется от 6,5 до 9,5 мм. Радиус промежуточной кривой 43 является более плоским, чем базисная кривая (на 1-2 диоптрии). Ширина равна 0,35-1,0 мм. Периферические кривые 45 являются более плоскими, чем базисная кривая (на 2-4 диоптрии), ширина равна 0,35-1,0 мм. Промежуточная 43 и периферическая кривые 45 могут быть асферическими. Призма и/или усечение 47 используется для того, чтобы удерживать линзу в соответствующем положении для изменения формы астигматической роговицы.
Толщина линзы зависит от ее силы. Если нулевая сила линзы = 0,20 мм, следует вычитать 0,01 мм на каждую минусовую диоптрию и прибавлять 0,02 мм на каждую плюсовую диоптрию. Сила линзы рассчитывается, исходя из дефектов зрения пациента и отношения базисная кривая/кривизна роговицы. Астигматические линзы могут включать энзим/агенты в камере 11 или использоваться без энзима после того, как роговица смягчилась.
D. Методика лечения гиперопии энзим-ортокератологией
В случае гиперопии центральная кривая роговицы должна стать более круто изогнутой кривой 60 (фиг.5B). Свет, входящий в глаз, должен преломляться в большей степени, потому что изображение, проектируемое через роговицу, фокусируется за сетчаткой, должно быть перемещено вперед на сетчатку с большим преломлением, то есть больше света изгибается у роговицы. Базисная кривая линзы (50 на фиг.5C и 5D) может быть превращена в более крутую, чем кривая центрального участка роговицы при помощи более плоской асферической промежуточной 52 и периферической 54 кривых. Отверстие 56 в центре линзы может быть использовано для создания пространства для более крутого изгиба центрального участка 51 роговицы. Кроме того, для коррекции гиперопии можно использовать контактную линзу, показанную на фиг.15 и 16.
Для исправления гиперопии с использованием энзим-ортокератологии применяют следующую методику.
По предпочтительному варианту для линзы используют кремнийсодержащий полифторакрилат (фиг.5С). Отверстие 56 диаметром от 2,5 до 4,5 мм находится в центре. Базисная кривая 50 линзы является более круто изогнутой, чем кривая центрального участка роговицы. Базисные кривые 50 изменяются от 5,5 до 8,0 мм, диаметр равен базисной кривой в мм +1,0-1,5 мм (интервал значений 6,5-9,5 мм) используются меньшие диаметры, так как изгиб линз круче, чем у центрального участка роговицы. Промежуточная 52 и периферическая 54 кривые должны быть несферическими и на 1,0-3,0 диоптрии более плоскими, чем базисная кривая 50. Ширина этих кривых равна 0,35-1,0 мм. Оптическая зона 50,56-5,5-8,0 мм. Толщина линзы зависит от оптической силы, необходимой для коррекции. При гиперопии линзы будут толще. Если оптическая сила 0, толщина = 0,20 мм, затем следует добавить 0,02 мм на каждую плюсовую диоптрию. Оптическая сила линзы рассчитывается, исходя из дефектов зрения пациента и отношения радиусов кривизны базисной кривой и поверхности раговицы. Линзы могут включать энзимы/агенты в камере 11 или использоваться без энзима после смягчения роговицы.
По другому варианту лечения гиперопии методом энзим-ортокератологии, энзим или агент вначале вводят в роговицу, как в случае вышеописанных вариантов данного изобретения. Как только роговица начала смягчаться, ей позволяют вначале менять форму, не применяя жестких контактных линз. Благодаря внутриглазному давлению радиус кривизны роговицы будет становится больше без использования контактной линзы, вызывающей такое изменение. Это естественное увеличение радиуса кривизны роговицы происходит, пока не будет достигнута нужная величина. В этот момент осуществляют ингибирование энзима или агента, использованного для смягчения роговицы, и затем жесткая линза, задняя поверхность которой имеет нужный радиус кривизны, надевается на смягчившуюся роговицу, она играет роль фиксирующей линзы, пока роговица не приобретет структурную целостность и "твердость".
По этой методике энзим-ортокератологии желаемую форму роговицы можно получить без применения жесткой контактной линзы, хотя такую линзу желательно использовать для сохранения желаемой формы.
IV. Другие области терапевтического использования энзим-ортокератологии
В дополнение к коррекции дефектов преломления в общем нормально функционирующего глаза данные методы изменения формы роговицы можно использовать и для других терапевтических целей. Одно предполагаемое терапевтическое применение этих методов заключается в восстановлении недостатков роговицы и исправлении дефектов преломления, возникающих вследствие таких болезней, как кератоконусность, искривление роговицы, вызванное контактными линзами, или манипуляций с роговицей, включая хирургическое вмешательство, такое как радиальная кератотомия, фоторефрактивная кератектомия, пересадка роговицы и хирургия катаракты.
Одной из наиболее распространенных причин неудач, встречающихся при хирургических операциях в клиниках, таких как пересадка роговицы, является, например, наличие остаточного дефекта преломления, например, нерегулярного астигматизма, которым сопровождается в остальном удачное хирургическое вмешательство. Следовательно, данные методы можно использовать для коррекции дефектов преломления, которые возникает в результате болезни, хирургического вмешательства и тому подобное.
Повышение гладкости и ровности роговицы, придание роговице соответствующей формы, уменьшение неровностей на поверхности роговицы - все это дополнительные преимущества применения методов по данному изобретению. Например, поверхность роговицы, являющаяся неровной, может стать более гладкой при использовании агента, смягчающего роговицу с последующим приданием нужной конфигурации при помощи формы или контактной линзы. Придание роговице соответствующей формы, особенно у пациентов, подвергшихся хирургическим операциям, например, пересадке роговицы, также можно осуществить согласно данному изобретению.
Таким образом, исправление дефектов преломления глаза проходит более успешно и могут быть исправлены любые изменения формы роговицы, вызванные хирургическим вмешательством.
Для того, чтобы использовать вышеописанные методы энзим-ортокератологии для клинических целей, прежде всего необходимо выявление лиц с роговицей неправильной формы или тех, кто подвергался хирургическому вмешательству. Затем для изменения формы роговицы пациента используют вышеописанные методы энзим-ортокератологии.
Следующие примеры иллюстрируют варианты данного изобретения. Примеры являются иллюстративными и не ограничивают объем изобретения.
Пример 1.
Определение дозировки экзогенного энзима.
Новозеландских белых кроликов анестезируют при помощи кетамина и ксизалина. У каждого кролика роговица одного глаза используется как контрольная. Эта роговица обрабатывается только физиологическим раствором. Роговицу другого глаза каждого кролика обрабатывают энзимом для выявления его способности смягчать роговицу. Измеренное количество раствора, содержащего испытуемый экзогенный энзим, вводится инъекцией в роговицу кролика. Через определенный промежуток времени проверяют роговицы обоих глаз для определения смягчающего действия испытуемого энзима. Для определения эффекта смягчения сравнивают результаты следующих испытаний роговицы каждого глаза:
1) Пахиметрии - для измерения толщины роговицы;
2) кератометрии - для измерения радиуса кривизны центрального участка роговицы;
3) компьютерной топографии - для оценки поверхностного топографического изменения роговицы;
4) исследования при помощи щелевой лампы - для оценки прозрачности роговицы, передней камеры и зрачка;
5) тонометрии - для измерения внутриглазного давления в глазу каждого кролика;
6) фондоскопического исследования оптического нерва и сетчатки;
7) ретиноскопии для измерения дефекта преломления и
8) окраска при помощи флуоросцеина или Бенгальской Розы для определения повреждения эпителия роговицы.
Эти исследования затем повторяют через определенный промежуток времени для определения продолжительности и действия дозы энзима, который был использован.
Пример 2.
Использование инактиватора ингибитора эндогенного энзима
Приблизительно 0,25 г иодацетамида растворяют в 100 мл физиологического раствора для получения раствора иодацетамида 25%-ной концентрации. Примерно 1-2 капли этого раствора вводят каждый час в течение 4-х часов субъекту.
Пример 3.
Использование ингибитора энзима
Ингибитор ЭДТА (этилендиаминтетрауксусную кислоту) растворяют в физиологическом растворе, чтобы получить раствор ~0,01%-ной концентрации. 1-2 капли раствора закапывают 2-3 раза в день. Эта обработка продолжается несколько дней для того, чтобы прекратить смягчающее действие энзимов на роговицу, сказывающееся в разрушении протеогликановых или коллагеновых компонентов роговицы.
Фигуры, параметры, константы и концентрации, указанные выше в этом описании, приведены в качестве примеров, не являющихся единственными или ограничивающими изобретения.
Поскольку в вышеописанных конструкциях линз и в способах лечения многое можно изменить, не выходя за рамки изобретения, все, содержащееся в описании или показанное на фигурах, следует интерпретировать как иллюстрирующий, но не лимитирующий изобретение материал.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ И УСТРОЙСТВО ДЛЯ УСКОРЕННОЙ ОРТОКЕРАТОЛОГИИ (ВАРИАНТЫ) | 1999 |
|
RU2214200C2 |
| ИСПОЛЬЗОВАНИЕ КОНТАКТНЫХ ЛИНЗ ПРИ ЛЕЧЕНИИ ОФТАЛЬМОЛОГИЧЕСКОГО НАРУШЕНИЯ | 2013 |
|
RU2647783C2 |
| ЦЕНТРАЛЬНАЯ ОПТИЧЕСКАЯ ЗОНА ПОВЫШЕННОЙ ЖЕСТКОСТИ В МЯГКИХ КОНТАКТНЫХ ЛИНЗАХ ДЛЯ КОРРЕКЦИИ АСТИГМАТИЗМА | 2013 |
|
RU2540932C2 |
| ИНТРАОКУЛЯРНАЯ ЛИНЗА С РАСШИРЕННОЙ ГЛУБИНОЙ ФОКУСА | 2009 |
|
RU2523130C2 |
| ЭЛЕМЕНТ В ВИДЕ ЛИНЗЫ | 2019 |
|
RU2768515C1 |
| МНОГОФОКУСНЫЕ КОНТАКТНЫЕ ЛИНЗЫ | 2007 |
|
RU2439635C2 |
| ИНТРАОКУЛЯРНАЯ ЛИНЗА | 2006 |
|
RU2339341C2 |
| ДИНАМИЧЕСКИЕ ЖИДКОСТНЫЕ ЗОНЫ В КОНТАКТНЫХ ЛИНЗАХ | 2013 |
|
RU2535658C2 |
| КОНСТРУКЦИЯ ОФТАЛЬМОЛОГИЧЕСКИХ ЛИНЗ ДЛЯ КОНТРОЛЯ БЛИЗОРУКОСТИ | 2010 |
|
RU2575048C2 |
| ЭЛЕМЕНТ В ВИДЕ ЛИНЗЫ | 2019 |
|
RU2769091C2 |

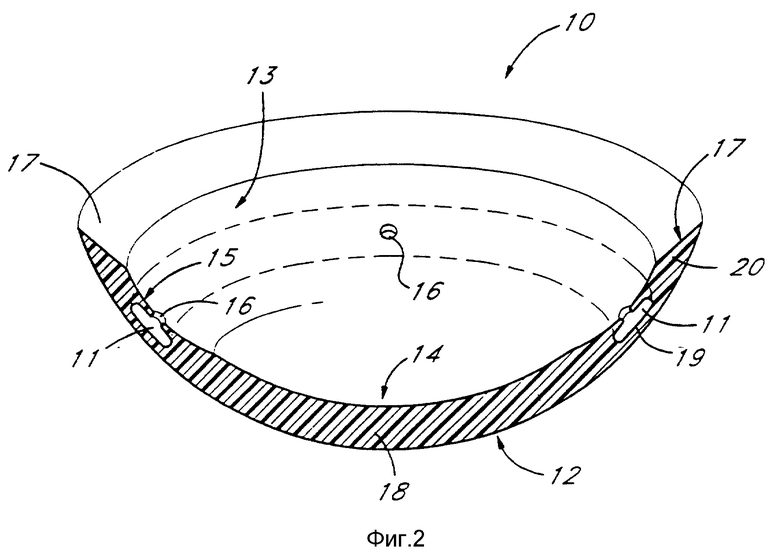
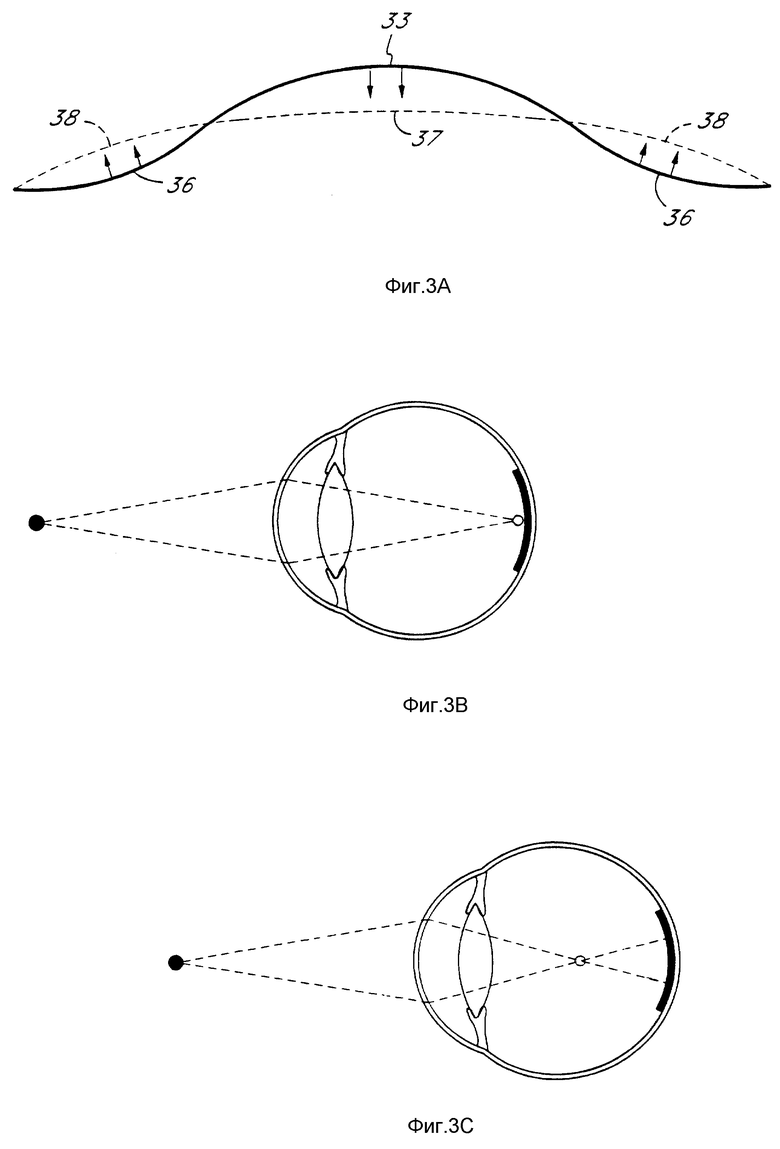


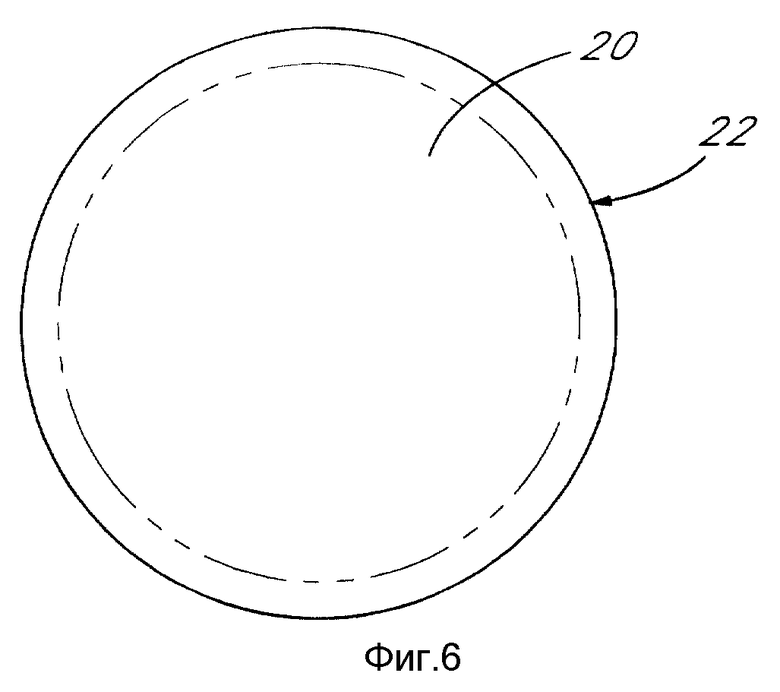
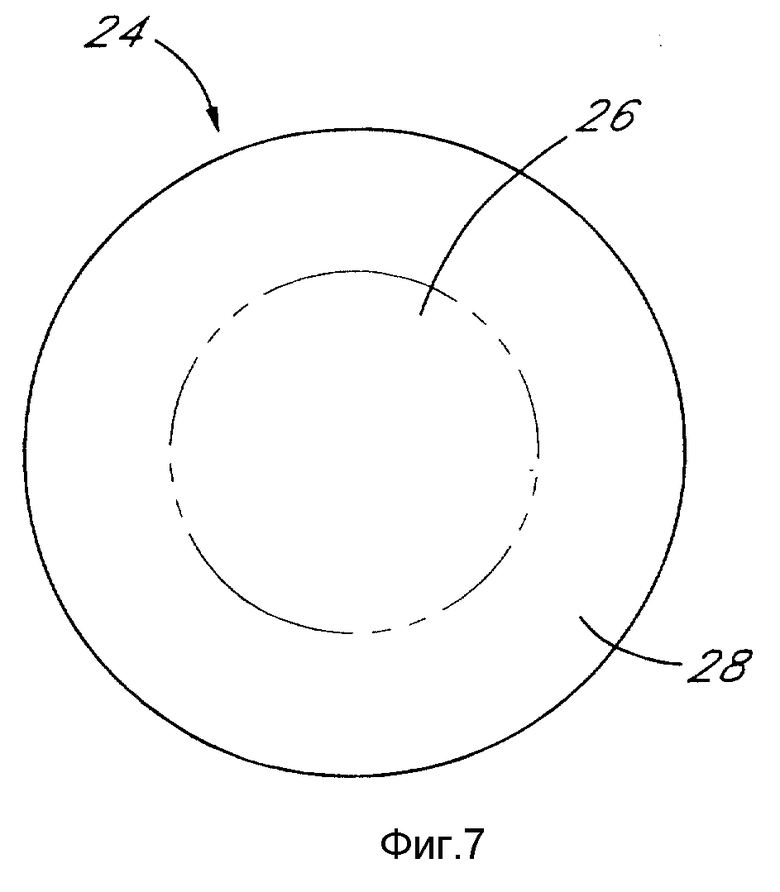
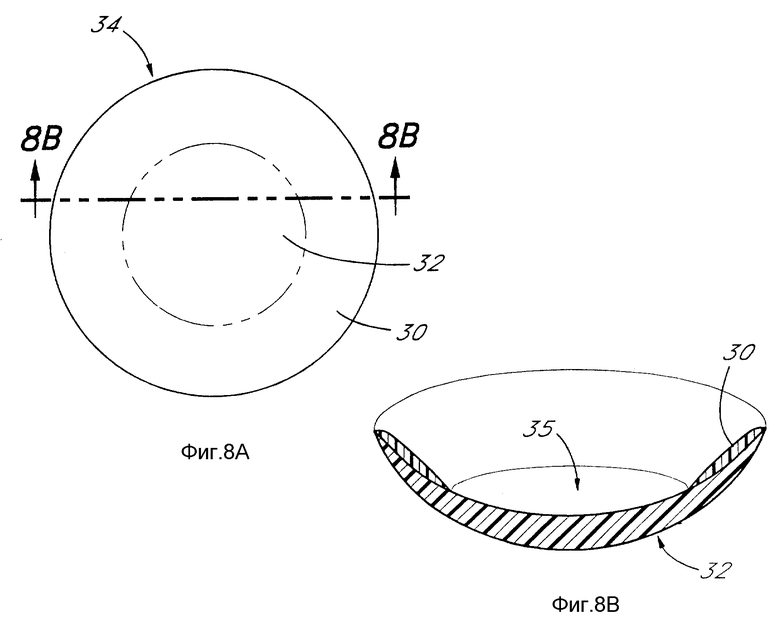
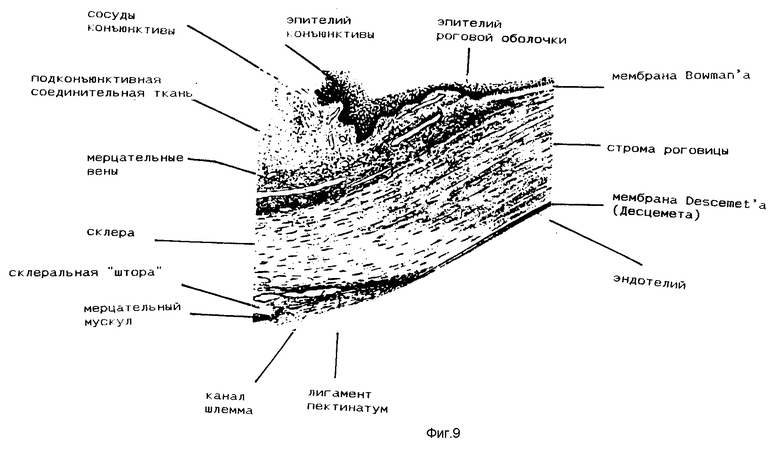

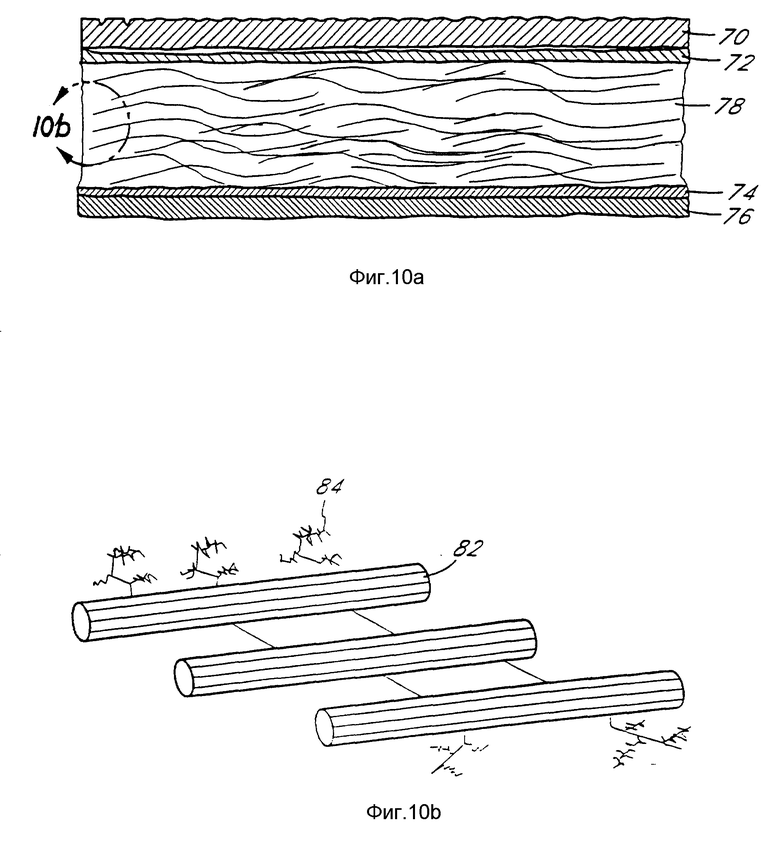
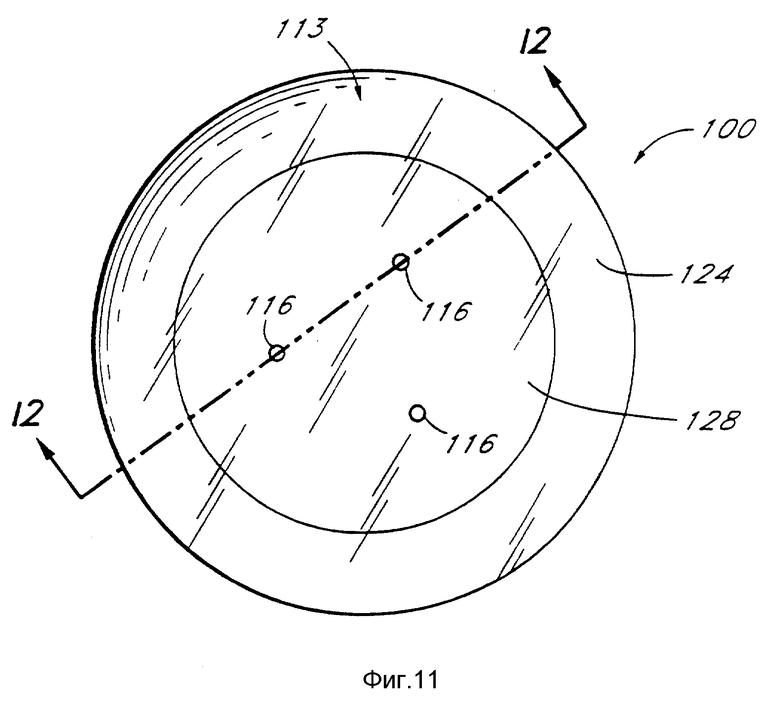
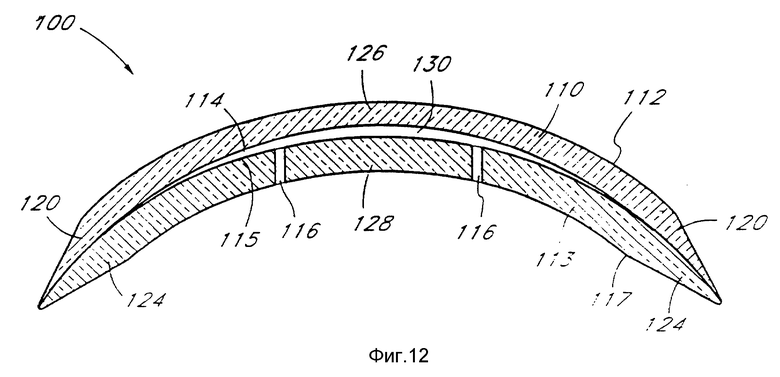
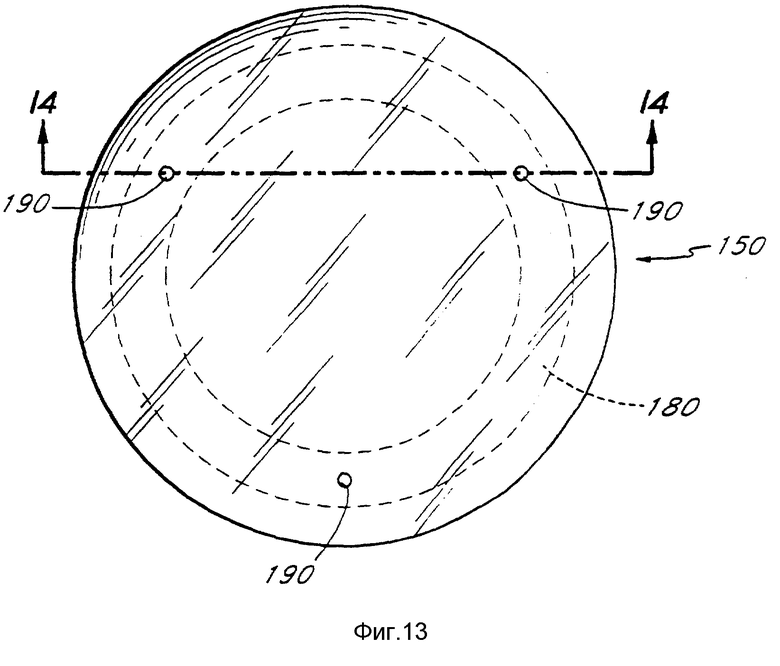
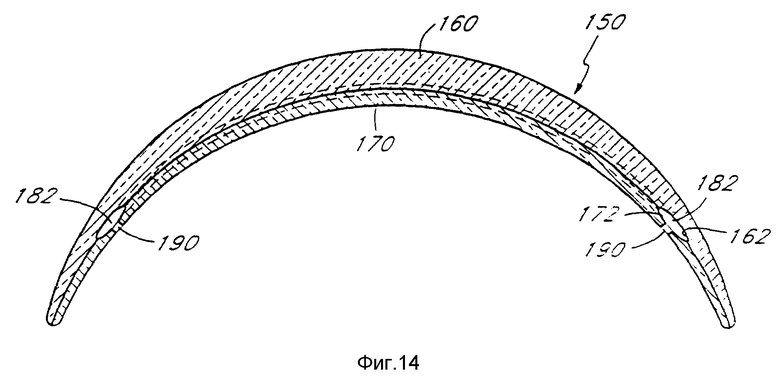
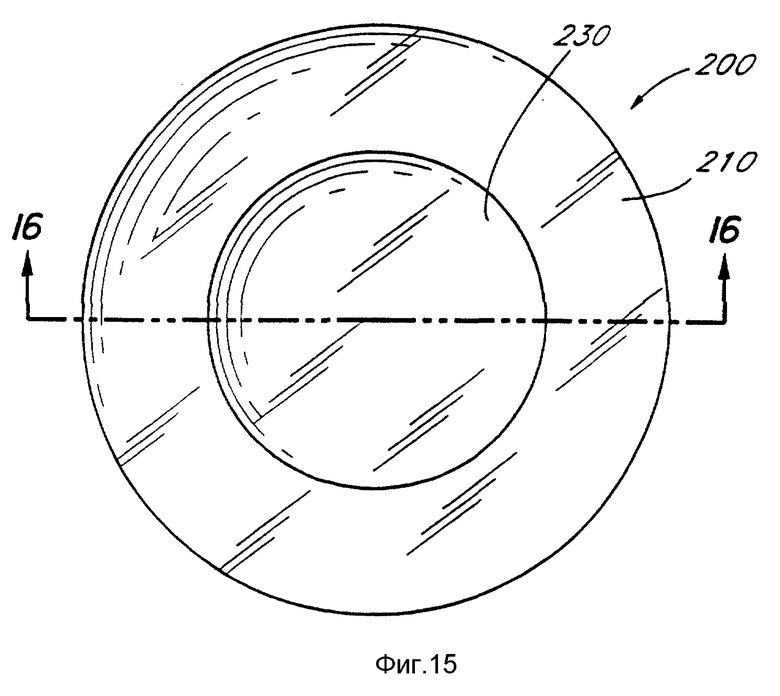
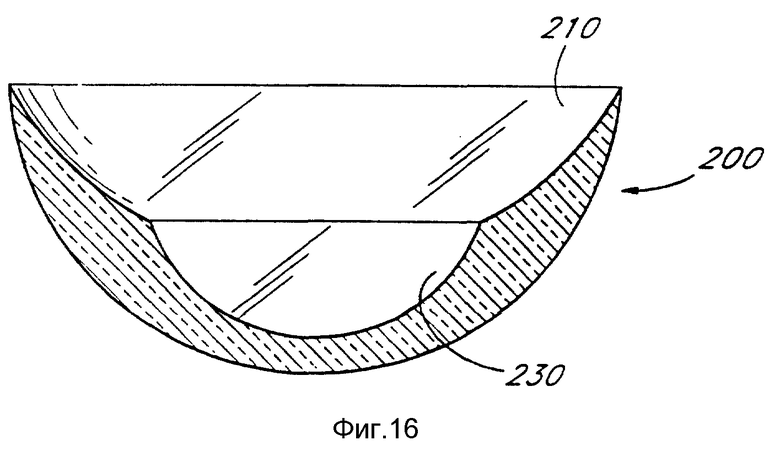
Изобретение относится к способам и устройству ускоренного изменения формы роговой оболочки глаза с целью уменьшения или устранения дефектов преломления глаза. Ускоренное изменение формы ткани роговой оболочки осуществляют введением в глаз одного или более энзимов и/или других агентов, которые временно смягчают роговицу. Затем на роговицу надевают жесткую контактную линзу или серию линз, которые имеют вогнутый профиль, который будет корректировать дефект преломления. Смягчившаяся роговица затем быстро изменяет форму выпуклой кривизны на вогнутую форму кривизны контактной линзы или серии линз, придавая глазу эмметропность. Энзимы и/или другие агенты затем выделяются из роговицы и роговица "отверждается", сохраняя новую эмметропную форму. После того, как "отверждение" произошло, линза, обеспечивающая глазу эмметропность, удаляется. Технический результат: изобретение позволяет нехирургическим путем исправлять большие дефекты преломления глаза и обеспечивает устойчивые результаты за более короткий промежуток времени. 8 с. и 35 з.п. ф-лы, 2 табл., 27 ил.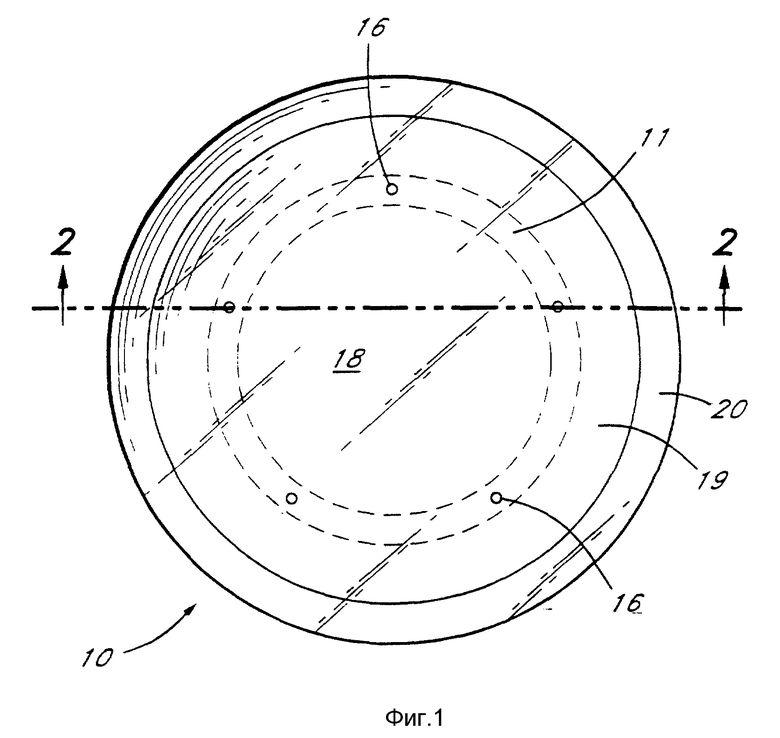
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Э.С.Аветисов | |||
| Близорукость | |||
| М.: Медицина, 1986, с.176 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ лечения прогрессирующей близорукости | 1987 |
|
SU1621921A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Актуальные вопросы контактной коррекции зрения | |||
| Сборник научных работ | |||
| Механизм для сообщения поршню рабочего цилиндра возвратно-поступательного движения | 1918 |
|
SU1989A1 |
Авторы
Даты
1999-09-20—Публикация
1992-10-15—Подача