Изобретение относится к области медицины.
Нарушение деятельности почек может наступить вследствие их заболевания, травмы или отравления нефротоксическими ядами (7, 9, 11 ,12, 18). Обратимое, быстро развивающееся нарушение функции почек называется острой почечной недостаточностью (ОПН), необратимое, формирующееся постепенно в течение месяцев и лет - хронической почечной недостаточностью (ХПН), а в последней стадии - терминальной уремией (7, 8, 12).
При ОПН и ХПН прекращается полностью или частично выведение из организма воды, азотистых шлаков, кислот и электролитов, которые накапливаются в крови и тканях организма, вызывая интоксикацию, жидкостную перегрузку и нарушение функций жизненно важных органов, отек легких и отек мозга, анемию, гипертонию, сердечную недостаточность вплоть до остановки сердца (7, 8, 11, 12). Продолжительность жизни при полностью неработающих почках составляет 6-8 суток (12).
Единственно эффективным методом лечения почечной недостаточности является гемодиализ (очищение крови) при помощи аппарата "Искусственная почка". Гемодиализ проводится 4-6-часовыми сеансами ежедневно или через день до восстановления функции почек при ОПН и пожизненно или до пересадки донорской почки при терминальной уремии (7, 8, 11, 12,). Гемодиализ - биохимическая операция. Очищение крови от избытка жидкости, азотистых шлаков, кислот и электролитов осуществляется путем их ультрафильтрации, диффузии и осмоса через полупроницаемую мембрану из ацетатцеллюлозы, купрофана, полиакрилметакрилата или других материалов в диализирующий (очищающий) раствор, аналогичный по своему электролитному и кислотно-щелочному составу плазме крови здорового человека. Устройство, в котором происходит собственно процесс очищения крови, называется диализатором (7). Клиренс (очищающая способность) и ультрафильтрация (способность к удалению жидкости) диализатора зависят от вида полупроницаемой мембраны, ее площади, толщины, количества пор на единицу поверхности, а также от режима проведения сеанса, то есть от скорости кровотока через диализатор, от величины отрицательного трансмембранного давления, подаваемого на мембрану специальным вакуумным насосом и от времени гемодиализа (2, 7).
Одна из основных задач врача, проводящего гемодиализ - квалифицированно подобрать необходимый данному больному по клиренсу и коэффициенту ультрафильтрации диализатор и назначить соответствующий режим проведения процедуры, обеспечивая тем самым максимально возможное для данного пациента очищение организма от азотистых шлаков и избыточной жидкости. На практике это означает снижение концентрации мочевины и креатинина в плазме крови до субнормальных значений, нормализацию уровней плазменного калия и кальция и удаление 1 - 6 литров жидкости за 4 - 6-часовой сеанс. Выполнение этих условий систематически от диализа к диализу позволяет добиться ликвидации угрожающих жизни расстройств при ОПН и уменьшения клинических проявлений уремии при ХПН. Однако выполнению этой задачи препятствуют следующие побочные эффекты и осложнения гемодиализа:
- синдром нарушенного равновесия (dysequilibrimn-syndrome) развивающийся из-за резких метаболических сдвигов во время гемодиализа - темп удаления мочевины из крови в диализирующий раствор превышает темп поступления ее из головного мозга в кровь вследствие плохой проницаемости для мочевины гематоэнцефалического барьера; в результате концентрация мочевины в мозгу может превысить концентрацию ее в крови, что создает осмотический градиент и вызывает перемещение жидкости в мозг, отек и набухание мозга, проявляющийся клинически некупируемыми медикаментозно головными болями, рвотой, судорогами, дезориентацией и острым психозом (4, 7, 14, 21);
- гемодинамические расстройства в виде
снижения системного артериального давления вплоть до коллапса из-за резкого опустошения сосудистого русла при удалении жидкости;
повышения системного артериального давления вплоть до гипертонического криза из-за резкого спазма сосудов в ответ на удаление жидкости и электролитные сдвиги;
усиления симптомов сердечной недостаточности в виде одышки в покое, цианоза, усиленного сердцебиения и нарушений сердечного ритма с возможным развитием кардиального отека легких (4, 5, 7, 10, 20, 23);
- усиление артериальной гипоксемии и общей гипоксии организма из-за нарушения вентиляционно-перфузионных отношений в легких вследствие гемодинамических расстройств во время гемодиализа и диффузии газов крови в диализирующий раствор (1, 6, 10, 15).
Для предотвращения возможных осложнений или купирования развившихся, применяется сокращение времени диализа и уменьшение интенсивности, что автоматически снижает его эффективность, введение гипертонических растворов глюкозы, глюконата кальция, препаратов крови и кровезаменителей, кардиотонических и гипотензивных препаратов, ингаляции кислорода или оксигенация крови во время диализа, а также гипербарическая оксигенация тотчас после его окончания (4, 5, 6, 10, 14, 15).
Необходимо подчеркнуть, что для больного с хроническим заболеванием почек развитие терминальной уремии и необходимость применения гемодиализа является безусловным психотравмирующим фактором (12, 17, 22, 25). Вынужденное прекращение профессиональной деятельности, нарушение жизненных планов, появление бытовых проблем и постоянная зависимость от аппарата "Искусственная почка" становятся причинами глубокой депрессии у 50-60% диализных больных (17, 22). K ней добавляется специфическая обстановка диализного зала, негативная информация от больных, плохо переносящих диализ или перенесших неудачную трансплантацию почки. В результате формируется стойкое чувство бесполезности проводимого лечения, напряженное ожидание худшего и отказ от сотрудничества с врачом. Устойчивая адаптация к процедуре гемодиализа наступает через 2-4 месяца лечения лишь у 23% больных, остальные во время и тотчас после диализа жалуются на необъяснимый дискомфорт, доходящий иногда до психоэмоционального и психомоторного возбуждения, сердцебиение и перебои в деятельности сердца, чувство нехватки воздуха, повышенную потливость, мигренеподобные головные боли при том, что объективная симптоматика (повышение или снижение артериального давления, снижение сократительной способности миокарда или признаки его ишемии) отсутствуют (17). Опыт показывает, что такая субъективная гиперреактивность без соответствующей медикаментозной коррекции к середине сеанса переходит в достоверную объективную реакцию на диализ вплоть до гипертонического криза, кардиальной астмы, некупируемых головных болей, заставляющих преждевременно прекращать сеанс (17, 22, 25). Из медикаментозных средств в таких ситуациях рекомендуются седативные и транквилизаторы (13).
Между тем, главная задача программного гемодиализа - ликвидация клинических проявлений уремии, компенсация состояния больного, отмена диетических ограничений, перевод больного на амбулаторный вариант лечения и возвращение ему трудоспособности - достижима лишь при условии достаточной для данного пациента длительности и интенсивности очищения крови. Реализация этой задачи означает для больного безусловное повышение "качества жизни" с возвратом в привычную микросоциальную среду, а часто и возвращение к профессиональной деятельности.
Актуальность и значимость настоящей разработки определяются существенным влиянием на качество гемодиализа таких побочных эффектов процедуры, как дизаквилибриум-синдром, гемодинамические реакции, усиление гипоксии и стресс, тяжесть течения которых определяется интенсивностью и длительностью лечения. Отсутствие четких рекомендаций затрудняет профилактику и коррекцию указанных выше побочных эффектов диализа.
Целью изобретения является практическое использование фармакологического средства, предупреждающего развитие побочных эффектов гемодиализа, или снижающего их интенсивность. Поставленная цель достигается совместным приемом внутрь реланиума с натрия оксибутиратом перед началом процедуры гемодиализа. В предлагаемом средстве обозначаемом далее "рецептура РОН", вместо реланиума (Польша) могут быть использованы его фармакоаналоги, в частности седуксен (Венгрия) или сибазон (Россия).
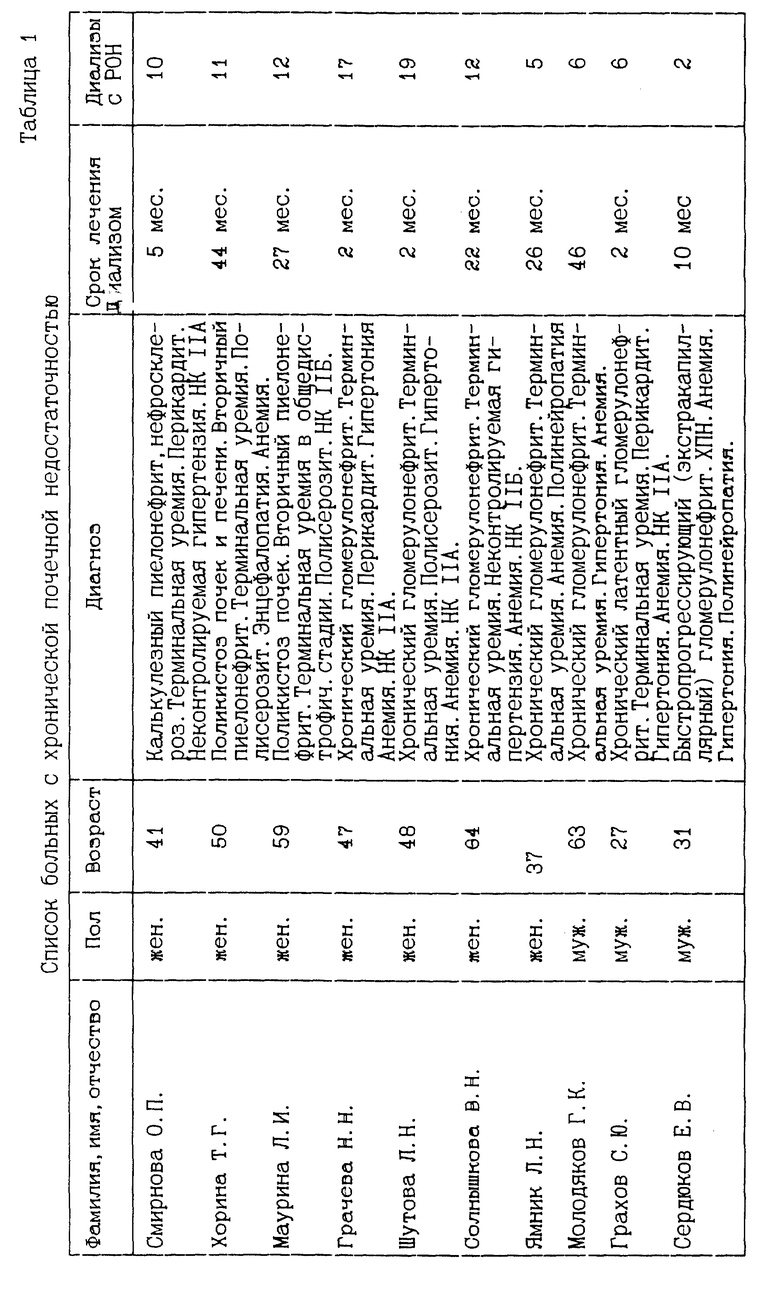
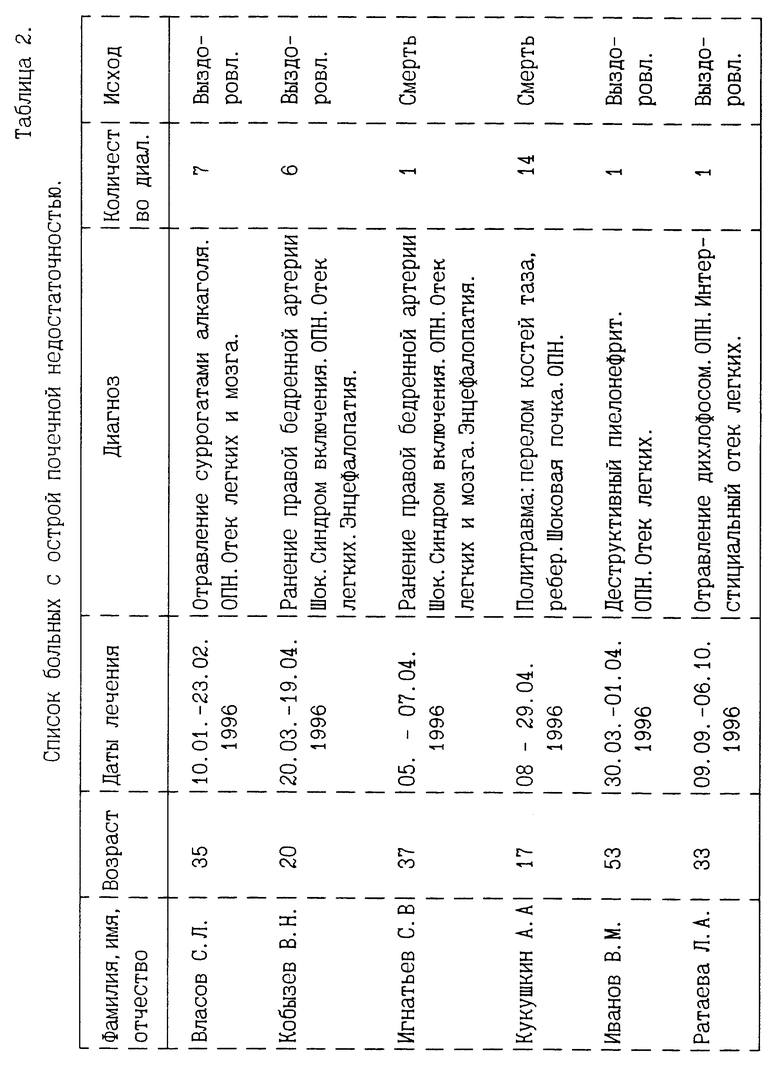
Средство применено в виде премедикации перед гемодиализом в лечении 10 больных с ХПН (таблица 1) и 6 больных с ОПН (таблица 2). Больные с ХПН за 20 минут до подключения к аппарату "Искусственная почка" получали внутрь через рот 1-2 мл реланиума (5-10 мг) совместно с 5-10 мл 20% натрия оксибутирата (1-2 г) в 50 мл дистиллированной воды. Больным с ОПН 2-4 мл реланиума (10-20 мг) и 10-20 мл 20% натрия оксибутирата (2-4 г) вводились внутривенно капельно в 400 мл физиологического раствора хлорида натрия.
Наблюдения проводились в течение 2-х месяцев. Для 5 больных с ХПН это был период введения в программный гемодиализ, у остальных стаж лечения составлял 22-46 месяцев, но ввиду запущенности основного заболевания имели место недостаточность кровообращения, неконтролируемая гипертония, непрерывно рецидивирующий пиелонефрит, затруднявшие адаптацию к диализу. Всего проведено 85 гемодиализов с премедикацией РОН (II группа). Контроль - 90 диализов без премедикации тем же больным (I группа).
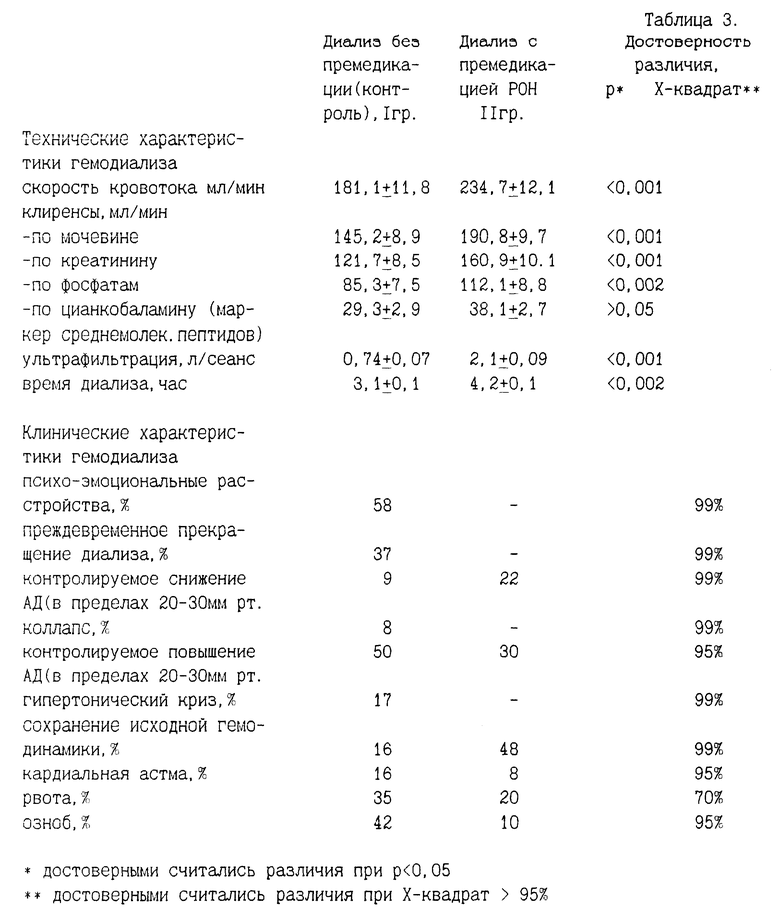
Результаты работы представлены в таблице 3. Общее время диализа, величина ультрафильтрации и скорость кровотока измерялись автоматически аппаратом "Искусственная почка", клиренсы мочевины, креатинина, фосфатов и цианкобаламина определялись по паспортной номограмме применяемого диализатора в соответствии с установленной скоростью кровотока. Все данные обработаны статистически с применением критерия Стьюдента и X-квадрат.
Оказалось, что время гемодиализа во II группе статистически достоверно на 26,2%, а объем удаленного ультрафильтрата - на 23,8% больше, чем в I группе. При этом во II группе на протяжении всего сеанса скорость кровотока и клиренсы мочевины, креатинина, фосфатов и цианкобаламина были достоверно выше, чем в I группе, в среднем на 24-25%. Несмотря на более интенсивный режим и большее время проведения процедуры гемодиализа во II группе достоверно реже фиксировались кардиальная астма, озноб и болевой синдром, колебания артериального давления достоверно чаще было контролируемым, а в половине диализов сохранялась исходная гемодинамика. Случаев коллапса или гипертонического криза, психоэмоциональных расстройств и преждевременного прекращения сеанса во II группе не зафиксированно.
Таким образом, применение премедикации рецептурой РОН обеспечивает проведение гемодиализа в необходимом данному пациенту режиме при минимальном риске развития осложнений и побочных эффектов, по-видимому, благодаря таким хорошо известным свойствам компонентов рецептуры, как стресс-протективный эффект, противоотечное и антигипоксическое действие (3, 16, 19). Полученные результаты позволяют рекомендовать премедикацию РОН перед началом гемодиализа следующим группам больных:
-всем эмоционально лабильным больным для профилактики и лечения психоэмоциональных расстройств;
- больным с ОПН, имеющим угрожающие жизни расстройства гомеостаза и потому требующим интенсивного ежедневного гемодиализа;
- больным с ХПН, находящимся на программном гемодиализе при декомпенсации уремии, развитии ее осложнений (перикардит, неконтролируемая гипертония, сердечная недостаточность) или сопутствующих заболеваний, ухудшающих переносимость гемодиализа.
Экономическая эффективность. В I группе без премедикации РОН общее время одного сеанса гемодиализа было на 26,2% меньше. Преждевременно прекращенных диализов в I группе оказалось 37%, во второй таких диализов не было (таблица 3). Себестоимость 4-часового гемодиализа больному с ХПН составляет 100 долларов США, прекращение такого диализа на час раньше необходимого времени процедуры означает потерю 25 долларов. В месяц одному больному с ХПН требуется 12 диализов, в год - 150. Таким образом, если за месяц преждевременно прекращается 4 диализа (37% от 12), а за год 55 (37% от 150), то на одном больном теряется соответственно 100 долларов в месяц и 1375 долларов в год.
Себестоимость одного гемодиализа больному с ОПН составляет 135 долларов США, сокращение времени его на 25% означает потерю 34 долларов. В среднем 1 больной с ОПН до восстановления функции собственных почек получает 4,6 ± 0,42 диализа (Дубров А.И. "Гипербарическая оксигенация в комплексном лечении острой почечной недостаточности у хирургических больных". Диссертация на соискание ученой степени кандидата медицинских наук, Ярославль, 1992, 139 с. ). Преждевременное прекращение 1,7 из них (37% от 4,6) означает потерю 58 долларов на одном больном с ОПН.
Литература
1. БАГРЯНЦЕВА С. Ю. Кислородно-транспортная функция крови у больных с гемотрансфузионными осложнениями. // Автореф. дисс. к.б.н. M., 1980.
2. БАЕВА Л. Б. Мембранные методы внепочечного очищения крови и аллотрансплантация трупной почки. // Дисс. д.м.н. 1984.
3. БЕЛЯКОВ В.А. Клиническая фармакология седуксена. // Анестезиол. и реаниматология, 1980, N 4, с. 57-61.
4. ДАНИЛКОВ А.П. Осложнения гемодиализа. // Дисс. к.м.н. М., 1972.
5. ДЖАВАД-ЗАДЕ М.Д., МАЛЬКОВ П.С., СУЛТАНОВ Ф.М. Осложнения гемодиализа. // Азерб. мед. журнал, 1975, N 9, с. 3-8.
6. ДУБРОВ А.И. Гипербарическая оксигенация в комплексном лечении острой почечной недостаточности у хирургических больных. // Дисс. к.м.н. Ярославль, 1992.
7. ЕРМОЛЕНКО В.М. Хронический гемодиализ. М., 1986.
8. КЛАР С., МАССРИ С.Г. Современная нефрология (пер. с англ.). М., 1984.
9. КОМАРОВ Б. Д. Хирургические методы лечения острых отравлений. M., 1981.
10. КОНОВАЛОВ Г. А. Реанимационные аспекты последовательной ультрафильтрации и гемодиализа. // Дисс. к.м.н. М., 1982.
11. КУЛАКОВ Г.П. Острая почечная недостаточность при некронефрозах. // Дисс. д.м.н. M., 1975.
12. ЛОПАТКИН Н.А., КУЧИНСКИЙ И.Н. Лечение острой и хронической почечной недостаточности. М., 1972.
13. МАЛЫШЕВ В.Д. Интенсивная терапия острых водно-электролитных нарушений. М., 1985.
14. МЕЛИКЯН А.М. Клиника и лечение острой почечной недостаточности после септического аборта. // Дисс. к.м.н, 1971.
15. МОРОЗ В.В., КОЗЛЕЧКОВ Ю.А. Профилактика гипоксии при проведении экстракорпорального гемодиализа. /Нарушения гемодинамики. Диагностика, профилактика, коррекция. // Тезисы докладов научной конференции 11-12 декабря 1980 г. М., 1981.
16. Оксибутират натрия. Нейрофармакол. и клинич. исследование. / Под ред. действ. члена АМН СССР Закусова В.В. - М., 1968.
17. СНЕТКОВ Д.И. Оценка уровня омаге-потенциала при проведении гемодиализа. // Материалы рабочего совещания нефрологов, С-Петербург, 13-15 декабря 1995 г., с.28.
18. ШИМАНКО И.И. Поражение почек при острых экзогенных отравлениях. М., 1977.
19. ЯСНЕЦОВ В.В., НОВИКОВ В.Е. Фармакотерапия отека головного мозга. М., 1994.
20. BERGSTROM J.M.D. Changes in blood pressure and hemodinamics during ultrafiltraition and dialysis. // Dialysis and Transplantaition, November, 1978, N 11, p. 1087-1092.
21. CERRA F., ANTONE R., ANTONE S. Colloid osmotic pressure flutuations and the dyseqilibrium syndrom during hemodialysis. // Nephron, 1974, N 3, p. 245-252.
22. DINGSALL R. Psycho-social aspects of dialysis. // Nephrology symposium in Moskau 26-30.05.95, p. 174-181.
23. HURVICH В.G. Dialysis fistula and heart falure. // Ann. Int. Mod., 1974, p. 80.
24. TECHERT F. Dialysis Quality and Adacuansy. // Nephrology symposium 26-30.05.95, p. 187-195.
25. ZUCOHELLI P. Dialysis Complications: Antmia and Cardiovascular Problems. // Nephrology symposium 26-30.05.95, p. 15-16.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ И ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ С ПОМОЩЬЮ ФЕТАЛЬНЫХ СТВОЛОВЫХ И ПРОГЕНИТОРНЫХ КЛЕТОК | 2007 |
|
RU2373942C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ | 1998 |
|
RU2154499C2 |
| ПРИМЕНЕНИЕ СОЛЕЙ ЛИТИЯ ДЛЯ ЛЕЧЕНИЯ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2008 |
|
RU2409373C2 |
| СПОСОБ ЭКСПЕРТИЗЫ КАЧЕСТВА ВНЕПОЧЕЧНОГО ОЧИЩЕНИЯ КРОВИ | 1998 |
|
RU2155074C2 |
| СПОСОБ ЛЕЧЕНИЯ ГИПЕРГОМОЦИСТЕИНЕМИИ У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ, ПОЛУЧАЮЩИХ ЛЕЧЕНИЕ ГЕМОДИАЛИЗОМ ИЛИ ГЕМОФИЛЬТРАЦИЕЙ | 2004 |
|
RU2261702C1 |
| СРЕДСТВО, ПОВЫШАЮЩЕЕ РЕЗИСТЕНТНОСТЬ ОРГАНИЗМА К ПЕРЕГРЕВАНИЮ | 1994 |
|
RU2096035C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ У ДОМАШНИХ ЖИВОТНЫХ С ПРИМЕНЕНИЕМ ПРОЦЕДУРЫ ГЕМОДИАЛИЗА | 2018 |
|
RU2693241C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ УРЕМИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2004 |
|
RU2272562C1 |
| СПОСОБ "СИМБИОТИЧЕСКОЙ" КОМПЕНСАЦИИ ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ (ХПН) У ЧЕЛОВЕКА | 2012 |
|
RU2506956C2 |
| Способ предупреждения почечного повреждения у больных первично выявленной секретирующей множественной миеломой | 2017 |
|
RU2652082C1 |
Изобретение относится к медицине и может быть использовано для предупреждения или уменьшения интенсивности побочных эффектов и осложнений гемодиализа, применяемого для лечения больных с почечной недостаточностью. Изобретение заключается в том, что средство содержит реланиум (10-20 мг) и 10-20 мл 20% натрия оксибутирата (2-4 г). В предлагаемом средстве вместо реланиума (Польша) могут быть использованы его фармакоаналоги, в частности седуксен (Венгрия) или сибазон (Россия). Разовая доза реланиума и его фармакоаналогов может колебаться в терапевтическом диапазоне от 5 до 20 мг. Изобретение предупреждает развитие побочных эффектов и осложнений гемодиализа или снижает их интенсивность за счет стресспротективного, противоотечного и антигипоксического действия его компонентов. 3 табл.
Средство, оптимизирующее проведение гемодиализа при почечной недостаточности, представляющее собой комбинацию реланиума или одного из его фармакоаналогов с натрия оксибутиратом в терапевтических дозах при соотношении 1 : 200.
| Машковский М.Л.Лекарственные средства | |||
| - М.: Медицина, ч.1, 1993, С.89, 136 | |||
| Лопаткин Н.А., Кучинская И.Н | |||
| Лечение острой и хронической недостаточности | |||
| Контрольный висячий замок в разъемном футляре | 1922 |
|
SU1972A1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ВЛИЯЮЩЕЕ НА ПРОЦЕССЫ ОБМЕНА ВЕЩЕСТВ | 1996 |
|
RU2114618C1 |
| СПОСОБ ИНГАЛЯЦИОННОЙ АНЕСТЕЗИИ И ОБОРУДОВАНИЕ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2183476C2 |
| US 4647500 A, 03.03.87. | |||
Авторы
Даты
1999-10-10—Публикация
1997-04-09—Подача