Изобретение относится к порошкообразным препаратам, содержащим медицински полезные полипептиды.
Предшествующий уровень техники
Полипептидные порошки, содержащие медицински полезные полипептиды и фармацевтически приемлемые носители или разбавители, могут быть приготовлены для введения путем ингаляции или иным образом. Полипептидные порошкообразные препараты для ингаляции описаны в WO 95/00197 и WO 95/00128. Они используются для стабилизации различных лекарств в процессе производства и хранения и для доведения количества приготовленных из порошка унифицированных доз - в основном, порошковые ингаляторы способны выделять лекарственное вещество с хорошей точностью дозирования только при определенных размерах доз, в то время как различные лекарства имеют различные активности и поэтому необходимо, чтобы они выделялись в различных количествах. Так как эти количества часто слишком малы, чтобы гарантировать надлежащую точность дозирования, добавляют разбавители до получения желательного размера дозы.
Ранее в полипептидных порошкообразных препаратах в качестве разбавителей использовались редуцирующие сахара, такие как лактоза и глюкоза. Они, однако, имеют тенденцию реагировать с полипептидами и являются поэтому неудовлетворительными.
В WO 95/00127 и WO 95/00128, относящихся к полипептидным порошкам для ингаляции, указывается, что нередуцирующие сахара, такие как рафиноза, мелецитоза, лактит, мальтит, трегалоза, сахароза, маннит и крахмал, могут быть предпочтительными добавками к полипептидным порошкам.
В настоящее время найдено, что мелецитоза является исключительно хорошим разбавителем, по сравнению с другими возможными разбавителями на основе нередуцирующих сахаров, для полипептидных порошкообразных препаратов, так как при ингаляции она дает неожиданно высокую вдыхаемую фракцию порошка.
Сущность изобретения
Соответственно, настоящее изобретение относится к порошкообразным препаратам для введения медицински полезных полипептидов, содержащих медицински полезный полипептид с мелецитозой в качестве разбавителя.
Предпочтительно введение путем ингаляции.
Мелецитоза может содержать, например, D-мелецитозу (α-D- мелецитозу), β-D- глюкопиранозид O-α-D- глюкопиранозид-1,3 _β-D- фруктофуранозил (β-D- мелецитозу) или изомелецитозу. Мелецитоза может быть, например, в форме моногидрата или дигидрата.
Выявлено, что порошкообразный препарат настоящего изобретения является очень эффективным при пероральной ингаляции, так как дает превосходную фракцию вдыхаемых частиц по сравнению с порошкообразными препаратами с другими разбавителями, как здесь описано. В результате более высокая фракция вдыхаемого порошка может достигать легких и более высокая фракция полипептида утилизируется.
Порошкообразный препарат настоящего изобретения пригоден также для использования путем ингаляции через нос.
Порошкообразный препарат настоящего изобретения пригоден как для системного, так и для местного лечения. Когда желательно местное воздействие в дыхательных путях, нет необходимости в других ингредиентах в порошкообразном препарате. Когда требуется системное воздействие, в препарат должен быть включен, в основном, усилитель, т.е. вещество, которое улучшает абсорбцию полипептида в дыхательных путях. Такие вещества включены в WO 95/00127 и WO 95/00128, приводимые здесь ссылкой. В некоторых случаях малые полипептиды абсорбируются в дыхательных путях без помощи усилителя. В таких случаях усилитель может быть исключен из препаратов мелецитозы и медицински полезного полипептида. Таким образом, в различных воплощениях настоящее изобретение представляет порошок, содержащий медицински полезный полипептид и мелецитозу; порошок, содержащий медицински полезный полипептид и мелецитозу и специфически включающий усилитель, и порошок, содержащий медицински полезный полипептид и мелецитозу, специфически исключающий усилитель. Порошок в соответствии с настоящим изобретением, исключающий усилитель, является наиболее полезным, (а) когда желательно местное воздействие полипептида, или (б) когда желательно системное воздействие более мелких полипептидов, которые абсорбируются в дыхательных путях без вспомогательной добавки усилителя. Полипептиды, которые абсорбируются в дыхательных путях без вспомогательной добавки усилителя, могут быть установлены с использованием обычных клеточных или, предпочтительно, животных моделей, в последнем случае путем сравнения уровней полипептида в плазме после введения, например, с помощью аппарата Wright Dust Feed, порошков с усилителем или без него. Порошок, специфически включающий усилитель в соответствии с настоящим изобретением, является наиболее полезным, когда желательно системное воздействие полипептидов, которые не абсорбируются в дыхательных путях без вспомогательной добавки усилителя.
Предпочтительные усилители включают C8-16 жирные кислоты и их соли, соли желчных кислот, фосфолипиды и алкил-сахариды.
Из жирных кислот и их солей предпочтительны соли C8-16 жирных кислот. Примерами предпочтительных солей жирных кислот являются натриевые, калиевые и лизиновые соли каприлата (C8), каприната (C10), лаурата (C12) и миристата (C14). Так как природа противоиона не имеет особого значения, потенциально пригодны любые из солей жирных кислот. Особенно предпочтительной солью жирной кислоты является капринат натрия.
Подходящими солями желчных кислот могут быть, например, соли холевой кислоты, хенодезоксихолевой кислоты, гликохолевой кислоты, таурохолевой кислоты, гликохенодезоксихолевой кислоты, таурохенодезоксихолевой кислоты, дезоксихолевой кислоты, гликодезоксихолевой кислоты, тауродезоксихолевой кислоты, литохолевой кислоты и урсодезоксихолевой кислоты.
Из солей желчных кислот предпочтительны соли тригидроксижелчных кислот. Более предпочтительными солями являются соли холевой, гликохолевой и таурохолевой кислот. Наиболее предпочтительной солью желчных кислот является таурохолат натрия.
Подходящими фосфолипидами могут быть, например, одноцепочечные фосфолипиды, например, лизофосфатидилхолины, лизофосфатидилглицерины, лизофосфатидилэтаноламины, лизофосфатидилинозиты и лизофосфатидилсерины, или двухцепочечные фосфолипиды, например, диацилфосфатидилхолины, диацилфосфатидилглицерины, диацилфосфатидилэтаноламины, диацилфосфатидилинозиты и диацилфосфатидилсерины.
Из фосфолипидов предпочтительны диацилфосфатидилглицерины и диацилфосфатидилхолины, например, диоктаноилфосфатидилглицерин и диоктаноилфосфатидилхолин.
Подходящими алкил-сахаридами могут быть, например, алкилглюкозиды или алкилмальтозиды, такие как децилглюкозид и додецилмальтозид.
Наиболее предпочтительными усилителями являются соли желчных кислот.
Полипептид может быть любым медицински или диагностически полезным пептидом или белком малого до среднего размеры, например, вплоть до молекулярной массы (MW) около 40 кД. Предполагается, что полипептиды, имеющие молекулярную массу вплоть до 30 кД, должны быть наиболее полезными в настоящем изобретении, такие как полипептиды, имеющие молекулярную массу вплоть до 25 кД или вплоть до 20 кД, или особенно вплоть до 15 кД, вплоть до 10 кД или вплоть до 5 кД.
Полипептид является предпочтительно пептидным гормоном, таким как инсулин, глюкагон, C-пептид инсулина, вазопрессин, десмопрессин, коктикотропин (ACTH), кортикотропин-высвобождающий гормон (CRH), гонадотропин-высвобождающий гормон (GnRH), агонисты и антагонисты гонадотропин-высвобождающего гормона, гонадотропин (лютеинизирующий гормон или LHRH), кальцитонин, паратиреоидный гормон (PTH), биоактивные фрагменты PTH, такие как PTH(34) и PTH(38), соматотропный гормон (GH) (например соматотропный гормон человека (hGH), соматотропин-высвобождающий гормон (GHRH), соматостатин, окситоцин, предсердный натриуретический фактор (ANF), тиротропин-высвобождающий гормон (TRH), дизоксирибонуклеаза (DNаза), пролактин и фолликулостимулирующий гормон (FSH) и аналоги любого из вышеупомянутых.
Другие возможные полипептиды включают факторы роста, интерлейкины, полипептидные вакцины, ферменты, эндорфины, гликопротеины, липопротеины и полипептиды, вовлеченные в путь коагуляции крови.
Предпочтительным полипептидом является инсулин.
В порошкообразном препарате настоящего изобретения мелецитоза может присутствовать в количестве вплоть до почти 100% от общей массы порошка. Например, мелецитоза может присутствовать в количестве между 20% и почти 100%, например, между 30% и почти 100% или между 40% и почти 100%, или между 50% и почти 100%, например, между 60% и почти 100% или между 65% и почти 100%, таком как между 65% и 99% или между около 70% и около 99%, таком как между 80% и 98% по массе от общей массы порошка.
Как и во всех фармацевтических препаратах, некоторые добавки, например, для регулирования pH, например, органические или неорганические соли, для придания вкуса или для повышения устойчивости, например, консерванты, углеводы, аминокислоты, пептиды или белки, могут быть также включены в препарат.
Когда порошкообразный препарат настоящего изобретения предназначается для пероральной ингаляции, полипептид должен состоять из (а) первичных частиц, имеющих диаметр менее, чем около 10 микрон, например между 0,01 и 10 микронами и предпочтительно между 0,1 и 6 микронами, например, между 0,01 и 5 микронами, или (б) агломератов указанных частиц. Предпочтительно по меньшей мере 50% полипептида состоит из частиц в желательных пределах размеров. Например, по меньшей мере 60%, предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 80% и наиболее предпочтительно по меньшей мере 90% полипептида состоит из частиц в желательных пределах размеров, когда желательна пероральная ингаляция.
Мелецитоза в препарате для пероральной ингаляции может, в основном, состоять из частиц, имеющих диаметр менее чем около 10 микрон, так что полученный порошок в целом состоит из необязательно агломерированных первичных частиц, имеющих диаметр менее чем около 10 микрон; альтернативно, мелецитоза может, в основном, состоять из более крупных частиц ("грубые частицы"), так что "упорядоченная смесь" может быть образована между активными соединениями и мелецитозой. В упорядоченной смеси, альтернативно известной как интерактивная или адгезивная смесь, полипептидные частицы могут быть довольно случайно распределены на поверхности грубой мелецитозы. Предпочтительно в этом случае, чтобы активные соединения не были в форме агломератов до образования упорядоченной смеси. Грубые частицы могут иметь диаметр более 20 микрон, например, более 60 микрон. Выше этих более низких пределов диаметр грубых частиц не является критически важным, так что различные размеры грубых частиц могут быть использованы при желании в соответствии с практическими требованиями порошкообразного препарата. Нет необходимости, чтобы грубые частицы в упорядоченной смеси были того же размера, но грубые частицы могут преимущественно быть подобного размера внутри упорядоченной смеси. Предпочтительно грубые частицы имеют диаметр 60-800 микрон.
Размер частиц менее важен при ингаляции через нос, хотя желательны маленькие частицы. Упорядоченная смесь обычно не должна использоваться для ингаляции через нос.
Полезный механизм для доставки порошка в дыхательные пути пациента обеспечивается через портативный ингалятор, пригодный для ингаляции сухого порошка. На рынке имеется много таких устройств, обычно сконструированных для доставки антиастматических и противовоспалительных средств в дыхательную систему.
Описанный порошкообразный препарат может быть приготовлен различными путями с использованием обычных технологий. Частицы требуемого диапазона размеров могут быть получены любым известным способом, например, способами сушки вымораживанием или регулируемой кристаллизации, например, кристаллизацией с использованием надкритических жидкостей; или способами микронизации. Например, можно смешать в сухом состоянии порошки полипептида и мелецитозы (и необязательного улучшителя), а затем микронизировать вещества вместе; альтернативно, вещества могут быть микронизированы отдельно, а затем смешены. Когда соединения, которые должны быть смешены, имеют различные физические свойства, такие как твердость и хрупкость, их сопротивление микронизации отличается, и они могут требовать различных давлений для разрушения до подходящих размеров частиц. Поэтому при совместной микронизации размер полученных частиц одного из компонентов может быть неудовлетворительным. В таком случае было бы предпочтительно микронизировать разные компоненты отдельно, а затем смешать их.
Возможно также, когда не намереваются приготовить упорядоченную смесь, вначале растворить компоненты в подходящем растворителе, например, в воде, чтобы достигнуть смешения на молекулярном уровне. Эта процедура позволяет также довести величину pH до желательного уровня. Для получения порошка растворитель удаляют способом, который сохраняет биологическую активность полипептида. Подходящие способы сушки включают концентрирование в вакууме, открытую сушку, сушку при распылении и сушку вымораживанием. Следует избегать воздействия температур выше 40oC в течение более, чем нескольких минут, так как может происходить некоторое разложение полипептида.
После стадии сушки твердый материал, если необходимо, измельчают для получения грубого порошка, затем, если необходимо, микронизируют.
Если желательно, порошок до введения в устройство, предназначенное для ингаляции, перерабатывают для улучшения реологических свойств, например, сухим гранулированием до образования сферических агломератов с превосходными свойствами для обращения с ними. В таком случае устройство должно иметь такую конфигурацию, чтобы обеспечивать существенную деагломерацию агломератов перед выходом из их устройства с тем, чтобы входящие в дыхательные пути пациента, были, в основном, в желательном диапазоне размеров.
Когда желательна упорядоченная смесь, активное соединение перерабатывают, например, путем микронизации, чтобы получить, если желательно, частицы в определенных пределах размеров. Мелецитозу также перерабатывают, например, чтобы получить желательные размеры и желательные поверхностные свойства, такие как определенное отношение поверхности к массе или определенная шероховатость, и чтобы обеспечить оптимальные адгезионные силы в упорядоченной смеси. Такие физические требования к упорядоченной смеси хорошо известны, как и различные средства для получения упорядоченной смеси, которая отвечает указанным требованиям, и могут быть легко определены специалистом согласно определенным обстоятельствам.
Порошки настоящего изобретения пригодны для местного или системного лечения заболеваний и могут быть введены, например, через верхние и нижние дыхательные пути, включая введение через нос. Таким образом, настоящее изобретение предоставляет также указанный порошок для применения в терапии; применение порошка в производстве медикамента для лечения заболеваний через дыхательные пути и способ лечения пациента, который нуждается в лечении, включающий введение указанному пациенту терапевтически эффективного количества порошка настоящего изобретения.
Заболеваниями, которые можно лечить порошком настоящего изобретения, являются некоторые из тех, которые можно лечить порошкообразным полипептидом в каждом случае; например, порошки, содержащие инсулин, соответствующие настоящему изобретению, могут быть использованы, например, при лечении диабетов; порошки, содержащие кортикотропин, могут быть использованы, например, при лечении воспалительных заболеваний; порошки, содержащие GnRH, могут быть полезными, например, при лечении мужского бесплодия. Показания для всех упомянутых полипептидов хорошо известны. Порошки настоящего изобретения могут быть также использованы в профилактических мероприятиях.
Хотя порошки настоящего изобретения относятся, в особенности, к полипептидным порошкам для ингаляции из устройств для ингаляции сухого порошка, полипептидные порошки могут быть также включены в композицию для других форм введения, например в инъекционные растворы и аэрозольные препараты.
Вдыхаемую фракцию при пероральной ингаляции порошков настоящего изобретения определяют способом, описанным здесь в примерах.
Некоторые воплощения изобретения иллюстрируются в следующих примерах, которые не следует считать ограничением:
Пример 1
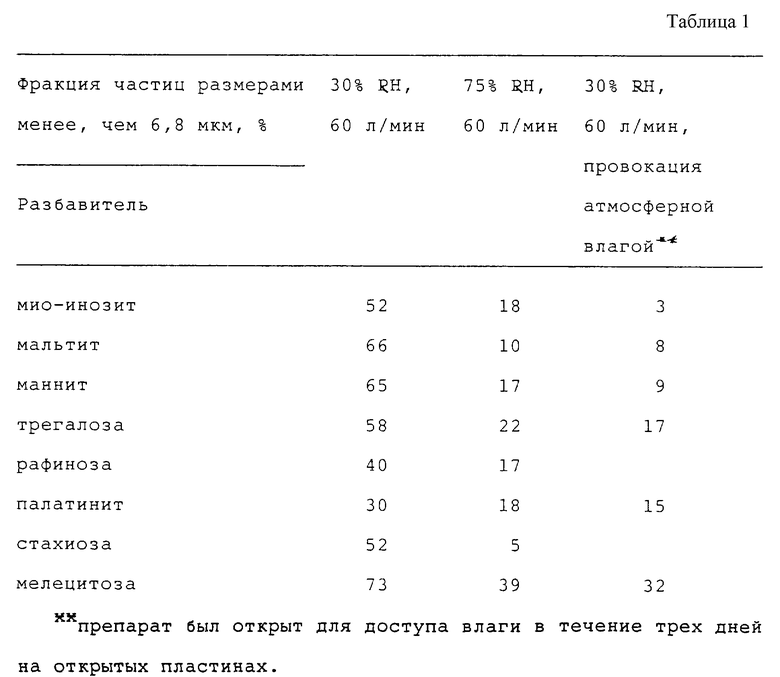
Инсулин (0,6 г) растворяют в дистиллированной воде (50 мл). Разбавитель (14,4 г) добавляют и растворяют и pH доводят до 7,4. Полученный твердый осадок измельчают, просеивают и микронизируют в струйной мельнице. Микронизированные порошки агломерируют и загружают в пульверизатор сухого порошка Turbuhaler® (зарегистрированный товарный знак) и дозу выпускают при скорости воздушного потока 60 л/мин при изменяющихся условиях.
Распыленную дозу собирают, используя многоступенчатый импинджер; содержание инсулина на каждой ступени импинджера определяют, используя жидкостную хроматографию с детектированием при 235 нм. Результаты представлены в табл. 1.
Ясно видно, что мелецитоза дает наибольшую фракцию вдыхаемых частиц во всех случаях. Более того, вдыхаемая фракция не зависит от внешних факторов, когда мелицитоза является разбавителем.
Пример 2
Инсулин (12 частей) растворяют в дистиллированной воде. Добавляют таурохолат натрия (усилитель, 4 части). Добавляют различные разбавители (84 части) и растворяют и pH доводят до 7,4. Раствор концентрируют испарением воды. Полученный твердый осадок измельчают, просеивают и микронизируют в струйной мельнице. Микронизированный порошок агломерируют и загружают в пульверизатор сухого порошка Turbuhaler® и дозу выпускают при скорости воздушного потока 60 л/мин при изменяющихся условиях.
Распыленную дозу собирают, используя многоступенчатый импинджер; содержание инсулина на каждой ступени импинджера определяют, используя жидкостную хроматографию с детектированием при 235 нм. Результаты представлены в табл. 2.
Результаты показывают, что препарат с мелицитозой значительно менее подвержен воздействию высокой влажности воздуха.
Пример 3
Микронизированные препараты, содержащие DNазу, поверхностно-активное вещество (таурохолат натрия или диоктаноилфосфатидилглицерин) и мелецитозу (отношение DNаза: поверхностно-активное вещество: мелецитоза - 1:0,33:98,67, общая масса 50 мг), добавляют к пропелланту (газу-носителю) 134a или пропелланту 227 (приблизительно 10 мл) в покрытом пластиком стеклянном пузырьке. Препараты смешивают с помощью ultra turrax приблизительно 10 минут.
Идентичные препараты готовят с добавлением 5% этанола перед смешиванием в течение приблизительно 10 минут с помощью аппарата ultraturrax.
Качество полученных суспензий оценивают сразу же или после 20 часов. Во всех случаях наблюдаются хорошие суспензии.
Это показывает, что содержащие мелецитозу препараты настоящего изобретения пригодны для применения в препаратах иных, чем для ингаляции сухого порошка, в данном случае в аэрозольных препаратах.

Порошкообразный препарат для введения медицинских полезных полипептидов, содержащий медицинский полезный полипептид с мелецитозой в качестве разбавителя. Изобретение относится к химико-фармацевтической промышленности и касается порошкообразного препарата, содержащего медицинские полезные полипептиды. Изобретение заключается в том, что порошкообразный препарат, содержащий полипептид с мелецитозой в качестве разбавителя, вводят путем ингаляций. Также изобретение заключается в способе производства порошкообразного препарата. Изобретение обеспечивает возможность использования хорошего разбавителя, по сравнению с другими разбавителями на основе нередуцирующих сахаров, для полипептидных порошкообразных препаратов, т.к. при ингаляции она дает неожиданно высокую вдыхаемую фракцию порошка. 3 с. и 49 з.п. ф-лы, 2 табл.
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА АМПИОКСА НАТРИЯ | 1988 |
|
SU1672627A1 |
| US 4788221 A, 29.11.88 | |||
| ВЛАГОМЕР ДЛЯ ИЗМЕРЕНИЯ ВЛАЖНОСТИ ДРЕВЕСИНЫ | 2000 |
|
RU2180746C1 |
Авторы
Даты
2000-01-27—Публикация
1995-12-19—Подача