Изобретения относится к области медико-биологических измерений и могут найти применение в лабораторной практике для биологических исследований и в медицине для диагностических целей.
Изобретения позволяют наблюдать спонтанную деоксигенацию пробы исследуемой крови и измерять скорость внутреннего потребления кислорода эритроцитами и могут быть использованы в медицинской практике для контроля за состоянием крови больного и подготавливаемой к переливанию донорской крови, а также для лабораторных исследований процессов оксигенации и деоксигенации крови.
Известен способ измерения внутреннего потребления кислорода эритроцитами, основанный на методе измерения дыхания тканей Варбурга [Умбрейт В.В., Буррис Р.Х., Штауффер Дж.Ф. Макрометрические методы изучения тканевого обмена. М., Изд. иностр. лит. 1951, 360 с.]. Согласно известному способу скорость потребления кислорода тканями определяется по изменению давления в замкнутой системе за счет выделения или поглощения изучаемыми тканями газообразного продукта. Устройство для осуществления способа (прибор Варбурга) состоит из термостатируемых замкнутых сосудиков, соединенных с манометром и равномерно покачиваемых для обеспечения равновесия между газовой средой и инкубируемыми тканями.
Зная объем замкнутого пространства, измеряя начальное давление в сосудиках и его изменение, рассчитывают объем выделившегося или поглощенного газа и скорость его выделения или поглощения.
Недостатком указанного решения являются ограничения по применению, обусловленные, во-первых, скоростью диффузии кислорода из заполняющей сосудики газовой среды в жидкую среду, в которой суспензированы исследуемые клетки (например, при изучении потребления дыхания эритроцитов - в плазму крови или физиологический раствор); во-вторых, выделением клетками в процессе дыхания углекислого газа. Для ускорения диффузии кислорода в жидкую среду сосудики равномерно встряхивают для улучшения газообмена и увеличивают парциальное давление кислорода в сосудиках.
Однако увеличение парциального давления кислорода в газовой среде изменяет условия газообмена между исследуемой тканью и средой инкубации, поскольку содержание газов в среде инкубации отличается от состояния in vivo.
При этом невозможно проконтролировать, находится ли жидкая среда в равновесии с газообразной по кислороду. Для удаления углекислого газа в сосудики помещают поглотитель - щелочь. Однако отсутствие углекислого газа полностью не контролируется, кроме того, при его отсутствии условия дыхания также могут изменяться по сравнению с нативными.
Недостатками указанных решений являются также необходимость использования относительно больших объемов исследуемых тканей (десятки миллилитров суспензий), невозможность проведения измерений в первые 10-15 мин после начала эксперимента из-за установления температурного равновесия в системе, невозможность проведения непрерывных измерений и, главное, недостаточная достоверность результатов, обусловленная визуальным характером наблюдения за показаниями прибора и обработкой их с помощью специальных таблиц.
Более совершенным по сравнению с вышеизложенным методом и прибором Варбурга являются способ и устройство для определения скорости внутреннего потребления кислорода с использованием респирометра, в котором предусматривается автоматическая регистрация показаний капиллярного манометра с помощью фотоэлемента, подающего импульсы на регистрирующее устройство, в котором сигналы в виде штриховых меток наносятся на ленту с частотой, зависимой от скорости поглощения кислорода [Шахбазов В.Г., Ена Л.Д. Респирометр для изучения дыхания мелких организмов, например, семян. Авт.свид N 178198 от 12.09.64, бюлл. "Открытия, изобретения, промышленные образцы, товарные знаки", 1966] , и при использовании микрореспирометра, в котором непрерывная регистрация потребления тканями кислорода осуществляется с помощью механоэлектронного преобразователя, соединенного с гидравлической системой, реагирующей на изменение давления в замкнутом пространстве, и показания которого регистрируются соответствующей аппаратурой [А.Л.Азин, Г.А.Вишковский. Микрореспирометр для определения количества потребленного тканями кислорода. Физиологический журнал СССР им. И.М.Сеченова, 1981, N 4, с. 618].
Эти решения в отличие от классического метода Варбурга позволяют вести непрерывные измерения и использовать образцы массой от 20 мг, однако в них по-прежнему остается неконтролируемым состав газовой среды в процессе эксперимента и условия диффузии кислорода между исследуемой тканью, средой инкубации и газовой средой. Соответствие содержания кислорода в газовой среде нативным параметрам контролируется с помощью полярографического электрода, комбинированного с прибором Варбурга [Э.С.Маилян, Е.А.Коваленко, Л.Б.Буравкова. Комбинированный метод изучения тканевого дыхания в условиях естественного газового гомеостаза. Патологическая физиология и экспериментальная терапия. 1981, N 4, с.85].
Вместе с тем ограничения, накладываемые удалением углекислого газа, процессами диффузии газов между исследуемой тканью, средой инкубации и газовой средой и невозможностью измерений в первые 10-15 мин, остаются.
Известны способы измерения внутреннего потребления кислорода эритроцитами, основанные на полярографическом методе [Руководство по изучению биологического окисления полярографическим методом. Под.ред. Г.М.Франка, М., Наука, 1973, 221 с.; Э.С.Маилян, Е.А.Коваленко, Л.Б.Буравкова. Комбинированный метод изучения тканевого дыхания в условиях естественного газового гомеостаза. Патологическая физиология и экспериментальная терапия. 1981, N 4, с. 85] . Указанный способ заключается в проведении электролиза исследуемого раствора в электрохимической ячейке и предусматривает определение внутреннего потребления кислорода на основании интерпретации зависимости между силой тока, характеризующей скорость электрохимического процесса, и потенциалом электрода или приложенным напряжением. Устройство для осуществления данного способа включает в себя схему питания, электроды в полярографической ячейке и регистратор.
Полярографическим методом можно непосредственно измерить напряжение (концентрацию) кислорода в растворе или суспензии. Ограничения на применения этого метода накладывается процессами диффузии кислорода между исследуемой тканью и средой инкубации и диффузии кислорода к электроду, "отравлением" электрода продуктами электролиза, либо, если поверхность электрода защищена газопроницаемой мембранной, его инерционностью и снижением чувствительности метода. Причем каждой конкретной цели измерения должна соответствовать определенная конструкция кислородного электрода.
Обуславливаемые налагаемыми ограничениями недостатки известных решений не позволяют успешно использовать их для исследования внутреннего потребления кислорода эритроцитами.
Близкими к заявляемому устройствами для исследования свойств крови, которые могут считаться устройствами - прототипами, являются устройства для контроля кислородно-транспортной функции крови [М.В.Фок, А.Р.Зарицкий, Г.А. Прокопенко, В.И.Грачев, М.И.Умаров "Способ определения оксигенационных свойств крови и устройство для определения кривой диссоциации оксигемоглобина крови", Авторское свидетельство СССР N 1608583 от 23.11.90, бюлл. N 43, МКИ G 01 N 33/49].
Известное устройство для контроля кислородно-транспортной функции крови содержит герметичную термо- и влагостатируемую камеру, подсоединенную к системе подачи газовой смеси с регулятором парциального давления кислорода в газовой смеси, регулятором парциального давления кислорода в газовой смеси, установленный в камере газообменник, оптический оксиметр с чувствительным элементом для оптической связи с исследуемой кровью и регистратор, подключенный к оксиметру. В этом известном решении имеет место принудительная оксигенация или деоксигенация пробы крови, происходящая в результате кислородного обмена крови с газовой средой, находящейся в контакте с кровью, на фоне спонтанной деоксигенации. При его использовании необходимыми элементами конструкции являются узлы и детали, обеспечивающие контакт поверхности крови с газовой средой для газообмена между средой и плазмой крови.
Известное устройство не обеспечивает возможности измерения скорости спонтанной деоксигенации крови, на фоне которой происходит принудительная оксигенация или деоксигенация, и, следовательно, не позволяет определить скорость внутреннего потребления кислорода эритроцитами.
Проведенные исследования обнаружили способность эритроцитов изменять проницаемость мембраны более, чем на три порядка величины в цикле кровообращения, причем структура мембраны претерпевает глубокие изменения, что в свою очередь воздействует на функционирование мембранных белков, в том числе ионных насосов и ферментов. Нарушения в механизме циклического изменения проницаемости эритроцитарной мембраны влекут за собой нарушения в выполнении эритроцитами их газотранспортной функции и, как следствие, вызывают патологическое состояние организма в целом. Показано, что для энергетического обеспечения процесса изменения мембранной проницаемости наряду с анаэробным гликолизом в эритроцитах должно существовать анаэробное усвоение глюкозы. Скорость внутреннего потребления кислорода эритроцитами в процессе спонтанной деоксигенации прямо пропорциональна интенсивности аэробного усвоения глюкозы, то есть количеству действующих ферментов. Таким образом, скорость внутреннего потребления кислорода эритроцитами является параметром, характеризующим энергетическое состояние исследуемой крови, в связи с чем заявляемое изобретение может быть использовано для контроля энергетического состояния крови, отражающего состояние организма в целом.
Использование заявленных изобретений позволяет, наблюдая спонтанную деоксигенацию пробы крови, измерять скорость внутреннего потребления кислорода эритроцитами и, соответственно, осуществлять контроль энергетического состояния крови.
Указанный технический результат при реализации изобретения по способу определения скорости внутреннего потребления кислорода эритроцитами крови, заключающемуся в заполнении сосуда исследуемой пробой крови, размещении сосуда с исследуемой пробой крови в термостатируемой камере и непрерывном измерении степени насыщенности кислородом исследуемой пробы крови, достигается тем, что в качестве сосуда используют емкость из газонепроницаемого материала, заполнение сосуда пробой крови производят полностью, без газовых включений, и перед размещением в термостабилизируемой камере сосуд герметично закрывают, при этом по изменению степени насыщенности крови кислородом определяют скорость ее спонтанной деоксигенации и скорость внутреннего потребления кислорода эритроцитами рассчитывают по формуле
где V - скорость внутреннего потребления кислорода кровью (в литрах кислорода на литр крови в мин);
α(t) - степень насыщенности крови кислородом в момент времени t (в %);
Q - количество гемоглобина в литре крови (в граммах), способного обратимо присоединить кислород;
dα/dt - - скорость спонтанной деоксигенации крови (в мин-1).
Точность измерения повышается, если для предотвращения оседания эритроцитов в процессе измерения пробу крови в сосуде перемешивают.
Необходимая точность измерения достигается и при другом варианте осуществления способа определения скорости внутреннего потребления кислорода эритроцитами, при котором измерение степени насыщенности кислородом крови начинают после оседания эритроцитов на дно сосуда.
Достижение указанного технического результата при реализации изобретения по заявляемому устройству для определения внутреннего потребления кислорода эритроцитами крови обеспечивается тем, что устройство содержит сосуд для размещения исследуемой пробы крови, помещенный в термостатируемую камеру, и регистратор степени насыщенности крови кислородом и отличается тем, что сосуд для крови выполнен в виде емкости из газонепроницаемого материала, имеет приспособление для заполнения его кровью исследуемой пробы полностью, без газовых включений, и для герметичного закрывания после заполнения его кровью. Конструкция устройства исключает газообмен крови с внешней газовой средой как в результате непосредственного контакта крови и газовой среды, так и в результате диффузии кислорода сквозь стенки сосуда.
Частным случаем осуществления устройства является такой, при котором регистратор степени насыщенности крови кислородом выполнен полярографически с чувствительными элементами для погружения в пробу крови.
В другом варианте исполнения устройства регистратор степени насыщенности крови кислородом выполнен в виде оптического оксиметра, чувствительный элемент которого размещен внутри сосуда для крови или вне его.
В случаях, если сосуд для размещения пробы крови выполнен из светопрозрачного материала, чувствительный элемент оксиметра может быть размещен снаружи сосуда.
В случаях, если сосуд для размещения пробы крови выполнен из светонепрозрачного материала, чувствительный элемент оксиметра снабжен световодами для обеспечения оптической связи с исследуемой пробой крови в сосуде.
Изобретение предусматривает различные модификации устройства, при которых исключается оседание эритроцитов, что увеличивает точность измерения.
В одном из частных случаев реализации устройства оно имеет механизм для перемешивания крови в сосуде.
В другом случае исключение оседания эритроцитов обеспечивается тем, что устройство снабжено механизмом вращения сосуда вокруг его горизонтальной оси.
Возможно также исполнение устройства, в котором для исключения оседания эритроцитов механизм перемешивания крови может быть выполнен в виде активатора, размещенного в сосуде и связанного с приводом его движения, размещенным вне сосуда.
Во всех случаях осуществления изобретения сосуд для размещения пробы крови выполняется в виде емкости из газонепроницаемого материала и имеет приспособления для его герметизации для исключения газообмена крови с окружающей газовой средой.
В частном случае сосуд для размещения крови может быть выполнен в виде стеклянного цилиндра, снабженного приспособлением для его заполнения кровью, которое может быть выполнено в виде поршня, размещенного в одном его торце, в то время как другой его торец оборудован полой иглой для забора крови, которая после заполнения сосуда закрывается колпачком (крышкой, пробкой, запечатывается чем-то типа воска, пицеина).
В другом исполнении в качестве сосуда для размещения крови может быть использован стеклянный капилляр, смонтированный с возможностью вращения вокруг его горизонтальной оси.
Необходимая точность измерения достигается и в следующем варианте исполнения устройства, при котором сосуд для крови выполняется в виде плоской камеры из светопрозрачного газонепроницаемого материала, внутренняя полость которой имеет столь малую глубину, что эритроциты пробы крови оседают на дно за время, много меньшее времени, необходимого для проведения измерений, после чего оседание эритроцитов прекращается и не вносит более искажений в измеряемую величину оптического сигнала, что исключает необходимость перемешивания. Обоснование возможности получения указанного выше результата при использовании заявленных изобретений заключается в следующем.
Энергетическое состояние эритроцита в основном определяется концентрацией в их цитоплазме макроэргических молекул аденозинтрифосфорной кислоты и работой ионных насосов, поддерживающих трансмембранный потенциал эритроцитов. Молекулы аденозинтрифосфорной кислоты гидролизуются в процессе деятельности калий-натриевых насосов, в результате деятельности которых на мембране клеток устанавливается и поддерживается трансмембранный потенциал. Поддержание трансмембранного потенциала на необходимом уровне является определяющим фактором для функционирования механизма изменения проницаемости мембраны для низкомолекулярных соединений, играющего важнейшую роль в осуществлении эритроцитами их кислородно-транспортной функции и нарушения которого приводят к тяжелым для организма последствиям. В частности, в низкоэнергетическом состоянии эритроцитов, характером для консервированной крови, их мембрана теряет способность уменьшать проницаемость - "закрываться" - при высоких степенях оксигенации, что приводит как к чрезмерному снабжению кислородом клеток в органах и тканях, где его требуется мало, так и к недостатку кислорода в тех тканях, где его нужно много. Кроме того, работа ионных насосов, регулирующих суммарные потоки ионов и воды из плазмы крови в цитоплазму эритроцитов и наоборот, в высокоэнергетическом (нативном) состоянии эритроцита сказывается на потоках воды и ионов солей через базальные мембраны капилляров тканей. При нарушении работы ионных насосов, имеющем место при переходе эритроцитов в низкоэнергетическое состояние, потоки воды и осмотических частиц через базальные мембраны капилляров изменяются, что вызывает нарушения водно-солевого обмена между кровью и тканями.
Наличие соответствия между скоростью производства аденозинтрифосфорной кислоты, ее концентрацией и скоростью расхода кислорода в эритроците (степень оксигенации крови является параметром, по скорости изменения которого можно судить о скорости усвоения клеткой кислорода), позволяет судить и о том, в каком энергетическом состоянии находится кровь.
Таким образом, выявлен критерий обнаружения патологии крови по указанным признакам, отражающим энергетическое состояние крови, с помощью предлагаемого способа определения скорости внутреннего потребления кислорода эритроцитами крови.
Как известно, здоровая кровь, будучи перенесенной в условия, адекватные условиям ее нахождения в организме человека, имеет определенные, принятые за эталонные при реализации изобретения, оптические характеристики, т.е. в каждый произвольно заданный момент времени процесса спонтанной деоксигенации состояние крови характеризуется определенным оптическим сигналом.
Об оптических свойствах любой среды: отражательной способности, поглощательной способности, вращении плоскости поляризации и др. - судят по интенсивности световых пучков, полученных в тех или иных условиях. Количественно эти свойства характеризуются: коэффициентами поглощения и преломления, удельным коэффициентом вращения плоскости поляризации и др. Причем эти величины обнаруживают дисперсию, т.е. зависят от длины волны света. Однако, как правило, непосредственно на опыте они не измеряются. Сигналы ϕ являются функциями указанных выше величин и естественной мерой оптических свойств крови. Сигналы ϕ отождествляются с оптическими характеристиками среды. Оптические характеристики (ϕ), являясь функциями перечисленных выше величин (коэффициентов поглощения, преломления и др.), также проявляют дисперсию - зависимость от длины волны. При поглощении или отдаче кровью кислорода (т.е. изменении степени оксигенации α) оптические свойства крови меняются, соответственно меняются оптические характеристики ϕ. Поэтому для реализации способа пригоден любой оптический прибор, способный регистрировать оптические характеристики крови, имеющие однозначную монотонную связь с количеством связанного гемоглобином крови кислорода, т.е. ее степенью оксигенации α, в виде показаний прибора ϕ во всем диапазоне изменений α от 0 до 100%, причем имеется взаимно однозначное соответствие между величинами α и ϕ для всех ϕ, принадлежащих отрезку [ϕmin; ϕmax]. В процессе измерения используется такой спектральный диапазон излучения, при котором ϕ однозначно связан со степенью оксигенации α. Например, в диапазоне 950 ± 10 нм поглощение кровью света при оксигенации растет и, следовательно, регистрируемый оптический сигнал монотонно уменьшается, а в диапазоне 650 ± 10 нм, наоборот, поглощение падает и соответственно монотонно растет регистрируемый сигнал.
Это свойство используется в предлагаемом способе, при реализации которого под оптическими характеристиками крови понимается именно величина ϕ, которая монотонно и однозначно связана с абсолютной степенью оксигенации крови α.
Сущность заявленных изобретений поясняется графическими материалами.
На фиг. 1 приведена принципиальная схема устройства для определения скорости внутреннего потребления кислорода эритроцитами крови, которое может быть использовано для осуществления способа определения скорости внутреннего потребления кислорода эритроцитами крови.
На фиг. 2 изображен один из вариантов монтажа сосуда для размещения в нем исследуемой пробы крови, предусматривающий предотвращение оседания эритроцитов.
На фиг. 3 представлена зависимость степени оксигенации крови от времени α(t) при спонтанной деоксигенации, наблюдаемой в предлагаемом устройстве.
На фиг. 4 представлена зависимость скорости внутреннего потребления кислорода кровью V(α).
Устройство для определения скорости внутреннего потребления кислорода эритроцитами крови, представленное на фиг. 1, включает следующие элементы.
Сосуд 1 для размещения в нем исследуемой пробы крови, снабженный приспособлениями для заполнения его кровью и последующей герметизации (и то, и другое на фиг. 1 не показано).
Термостабилизирующая камера 2 с установленным в ней сосудом 1 обеспечивает термостабилизацию крови и измерительных (чувствительных) элементов.
Система управления температурой в камере включает регулятор 3, подключенный к установленному в камере 2 датчику 4 и исполнительному механизму (на фиг. 1 не показан).
Для исключения оседания эритроцитов в сосуде, вызывающего искажения оптического сигнала в процессе измерений, устройство снабжено приводом 5 движения либо самого сосуда 1, либо перемешивателя внутри него.
Измерение временной зависимости степени насыщенности исследуемой пробы крови кислородом в процессе ее спонтанной деоксигенации, происходящем в сосуде 1, осуществляется с помощью регистратора 6, чувствительный элемент 7 которого может быть размешен внутри сосуда или вне его.
Выход регистратора 6 подключен к блоку 8 - отображение полученной информации.
Сосуд 1 для размещения исследуемой пробы крови выполняется из газонепроницаемого материала для исключения газообмена крови с внешней средой.
Для исключения отрицательного воздействия на химический состав крови сосуд 1 выполняется из материала, не травмирующего кровь.
В частном случае выполнение устройства сосуд для размещения крови 1 представляет собой заполненный кровью цилиндрический сосуд или капилляр, смонтированный в термостабилизирующей камере 2 с возможностью вращения вокруг горизонтальной оси сосуда 1 для предотвращения оседания эритроцитов.
В другом частном случае выполнения устройства сосуд для крови 1 выполняется в виде плоской камеры из светопрозрачного газонепроницаемого материала, внутренняя полость которой имеет столь малую глубину, что эритроциты пробы крови оседают на дно за время, много меньшее времени, необходимого для проведения измерений, после чего оседание эритроцитов прекращается и не вносит более искажений в измеряемую величину оптического сигнала. В этом случае исключается необходимость перемешивания пробы крови.
Средство для исключения оседания эритроцитов может иметь различные варианты исполнения.
В частном случае реализации устройства сосуд 1 для размещения пробы крови имеет форму цилиндра, узел крепления которого (не показан) соединен с приводом 5 его вращения вокруг горизонтальной оси.
При выполнении механизма перемешивания крови в виде активатора, погруженного в кровь, последний связывается с приводом 5 его движения, размещенным вне сосуда 1. В этом варианте исполнения сосуд 1 снабжен герметизирующими элементами для исключения газообмена крови с окружающей газовой средой (не показаны).
Для исключения отрицательного воздействия на химический состав крови перемешиватель выполняется из материала, не травмирующего кровь, или покрывается слоем такого материала.
Для реализации своих функций измерительный блок 6 может иметь различные варианты исполнения.
Измерение степени насыщенности крови кислородом может производиться полярографически, в таком случае чувствительные элементы 7 погружены в кровь, а сосуд 1 для размещения крови снабжен дополнительными элементами для исключения его разгерметизации и газообмена между кровью и окружающей средой.
В случае исполнения регистратора 6 в виде оптического оксиметра чувствительный элемент 7 может быть размещен внутри сосуда 1 для крови или вне его.
Сосуд 1 для размещения исследуемой пробы крови может быть выполнен из светопрозрачного материала, например стекла; в этом случае чувствительный элемент 7 оксиметра 6 может быть установлен снаружи сосуда 1.
В случаях выполнения сосуда 1 из светонепрозрачного материала, чувствительный элемент 7 может быть размещен как внутри, так и снаружи сосуда 1, снабженного дополнительными элементами, исключающими нарушение герметичности сосуда, влекущее за собой взаимодействие крови с кислородом газовой среды. В последнем случае чувствительный элемент 7 имеет световоды для оптической связи с исследуемой пробой крови в сосуде 1, конструкция сопряжения которых с сосудом исключает разгерметизацию сосуда.
В другом варианте исполнения предлагаемое устройство может быть выполнено следующим образом.
Сосуд 1 для размещения крови может представлять собой стеклянный цилиндр, в том числе тонкостенный капилляр, заполняемый кровью и герметично закрываемый.
Сосуд 1 помещается между чувствительными элементами 7 оксиметра 6 и закрепляется горизонтально в термостабилизирующей камере 2. Вращением сосуда 1 от привода 5 предотвращается оседание эритроцитов.
Регуляцию температуры в термостабилизирующей и, при необходимости, светоизолирующей камере 2, можно осуществить с помощью серийно выпускаемого термостата, вода из которого прокачивается по трубопроводу внутри термостатирующего кожуха. Температура крови при этом может контролироваться термопарой или термометром.
В качестве оптического оксиметра 6 может быть использован один из стандартных приборов, выпускаемых промышленностью, датчики (чувствительные элементы) которых по своим габаритам/параметрам позволяют осуществление оптической связи с кровью, находящейся в сосуде 1. Оптические чувствительные элементы 7, имеющие оптическую связь с кровью, могут быть стандартными светочувствительными элементами, например фотодиодами, солнечными батареями, ФЭУ и др.
На фиг. 2 изображен сосуд 1 цилиндрической формы, выполненный из светопрозрачного материала, горизонтально закрепленный в термостабилизирующей камере с помощью зажима 9, соединенного с приводом 5. Чувствительные элементы 7 в данном случае являются фотоэлементами, снабженными светофильтрами, и расположены так, что осуществляют оптическую связь между исследуемой пробой крови и оксиметром 6.
Вместо блока 8 отображения информации может быть использована и более сложная система, в том числе с использованием ЭВМ.
Согласно изобретению измерение скорости внутреннего потребления кислорода эритроцитами крови должно осуществляться путем проведения необходимых исследований в процессе спонтанной деоксигенации крови.
Для осуществления заявленного способа, а именно для наблюдения за процессом спонтанной деоксигенации, кровь должна быть насыщена кислородом, то есть либо пробу крови предварительно насыщают кислородом, либо исследуют насыщенную кислородом в организме артериальную кровь. Насыщение пробы крови кислородом проводится в сосуде 1 пропусканием над поверхностью крови или через ее объем газовой смеси, насыщенной кислородом. Для ускорения подготовки кровь при этом следует перемешивать. Подготовку крови проводят при той же температуре, при которой будут проводиться измерения.
Процесс поглощения кислорода кровью производится до полного насыщения и контролируется с помощью оптического оксиметра 6, чувствительный элемент 7 которого оптически связан с исследуемой кровью, либо полярографически.
При достижении кровью требуемого содержания кислорода процесс газообмена при подготовке исследуемой пробы крови прекращается.
После подготовки крови приступают непосредственно к определению скорости внутреннего потребления кислорода кровью путем исследования спонтанной деоксигенации пробы крови в заявленном устройстве, получения временных зависимостей оптических характеристик крови и их анализа.
Готовят устройство к работе - устанавливают необходимую для измерений температуру в камере 2, в которой находится сосуд 1.
Пробу крови, имеющую ту же температуру, помещают в сосуд 1. После установления температурного равновесия между камерой 2, сосудом 1 и пробой крови включают регистратор 6 и фиксируют сигналы с чувствительного элемента 7 на протяжении всего процесса измерения, длительность которого контролируется измерителем времени регистратора 8. Одновременно приводится в движение механизм перемешивания крови от привода 5. Контроль за процессом спонтанной деоксигенации крови осуществляется во времени в течение всего процесса измерения. Сигналы, поступающие с чувствительных элементов 7, являются количественной мерой оптических характеристик крови.
Полученную зависимость оптических либо полярографических характеристик от времени наблюдения спонтанной деоксигенации исследуемой крови φ(t) регистратором 8 преобразуют в зависимость степени оксигенации крови α(t) рассчитывают и анализируют зависимость скорости ее изменения  (в мин-1) и скорость внутреннего потребления кислорода кровью V (в литрах кислорода на литр крови в мин) по формуле
(в мин-1) и скорость внутреннего потребления кислорода кровью V (в литрах кислорода на литр крови в мин) по формуле
где V - скорость внутреннего потребления кислорода кровью (в литрах кислорода на литр крови в мин);
α(t) - степень насыщенности крови кислородом в момент времени t (в %);
Q - количество гемоглобина в литре крови (в граммах), способного обратимо присоединять кислород;
dα/dt - скорость спонтанной деоксигенации крови (в мин-1).
В качестве примеров реализации такого анализа могут быть приведены следующие.
На фиг. 3, 4 представлены результаты исследования крови на предлагаемом устройстве заявленным способом.
Предварительная подготовка крови заключалась в добавлении физиологической нормы глюкозы, установлении физиологических значений кислотно-щелочного баланса (pH) крови и ее оксигенации. 40%-ный раствор глюкозы добавляли в количестве, необходимом для питания эритроцитов в течение 5 часов. Величину pH крови доводили до 7.3-7.4 с помощью изотонических растворов щелочи и кислоты: NaOH и HCl. Кровь помещали в термостат с to=27oC, при этой температуре кровь находилась в течение всего эксперимента. После добавления глюкозы кровь до начала оксигенации инкубировали в течение 30 мин. Затем кровь оксигенировали в течение 1 часа в воздушной атмосфере, либо в атмосфере, либо в атмосфере, состоящей из аргона (Ar) и кислорода (O2) в соотношении Ar:O2 93.5:6.5 по объему до установления равновесия крови с газовой средой. Напряжение кислорода в плазме крови pO2 (а также pH и напряжение углекислого газа pCO2) контролировали полярографически с помощью прибора ABC-Radiometer. Степень оксигенации крови определялась из величины pO2 с помощью расчетной линейки BGCI и после оксигенации в присутствии 6.5% кислорода составляла около 90%.
Подготовленную кровь помещали в сосуд заявляемого устройства объемом 2 мл. Сосуд закрепляли в устройстве для предотвращения оседания эритроцитов внутри термостатируемой камеры, в которой предварительно устанавливали температуру 27oC, равную температуре крови, между фотоэлектронными датчиками, сигнал с которых подавался на регистратор и с него на ЭВМ. Затем включали мотор, вращающий устройство для предотвращения оседания эритроцитов. Регистрировали сигнал с оптических датчиков, получая зависимость степени насыщенности крови кислородом от времени.
На фиг. 3 представлены зависимости степени оксигенации от времени α(t) при спонтанной деоксигенации крови, оксигенированной в процессе предварительной подготовки до 97% в воздушной атмосфере (фиг. 3, кривая а), и крови, оксигенированной в процессе предварительной подготовки до 90% в атмосфере Ar:O2 (фиг. 3, кривая б).
На фиг. 4 представлены зависимости скорости внутреннего потребления кислорода кровью V(α) от степени оксигенации α при спонтанной деоксигенации крови, оксигенированной в процессе предварительной подготовки до 97% в воздушной атмосфере (фиг. 4, кривая а), и крови, оксигенированной в процессе предварительной подготовки до 90% в атмосфере Ar:O2 (фиг. 4, кривая б). Видно, что во втором случае при степенях оксигенации 78-80% скорость внутреннего потребления кислорода резко возрастает.
Результаты проведенных испытаний, представленных на фиг. 3-4, и изложенное выше описание работы устройства свидетельствуют о реализуемости заявленного способа и работоспособности предлагаемого устройства.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНТРОЛЯ КИСЛОРОДНО-ТРАНСПОРТНОЙ ФУНКЦИИ КРОВИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2060501C1 |
| СПОСОБ ДИАГНОСТИКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ОРГАНИЗМА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2002 |
|
RU2218085C2 |
| СПОСОБ ДИАГНОСТИКИ ОРГАНИЗМА, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ДИАГНОСТИКИ И ИССЛЕДОВАНИЙ СТЕПЕНИ ТЯЖЕСТИ ДИАБЕТА, И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2010 |
|
RU2453272C2 |
| Способ определения оксигенационных свойств крови и устройство для определения кривой диссоциации оксигемоглобина крови | 1988 |
|
SU1608583A1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ КИСЛОРОДНО-ТРАНСПОРТНОЙ ФУНКЦИИ КРОВИ У СУБЪЕКТА И ЕЕ ОТКЛОНЕНИЙ ОТ НОРМЫ | 2018 |
|
RU2703510C1 |
| СПЕКТРАЛЬНОЕ УСТРОЙСТВО ДЛЯ КОНТРОЛЯ И МОНИТОРИНГА ПРОЦЕССА ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2000 |
|
RU2169590C1 |
| СПОСОБ НЕИНВАЗИВНОГО ИЗМЕРЕНИЯ НАСЫЩЕНИЯ КРОВИ КИСЛОРОДОМ | 2000 |
|
RU2173082C1 |
| УСТРОЙСТВО ДЛЯ НЕИНВАЗИВНОГО ИЗМЕРЕНИЯ НАСЫЩЕНИЯ КРОВИ КИСЛОРОДОМ | 2002 |
|
RU2221485C2 |
| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОЙ РЕГИСТРАЦИИ ОСАЖДЕНИЯ КРОВИ | 1997 |
|
RU2128945C1 |
| ПУЛЬСОВОЙ ОКСИМЕТР (ВАРИАНТЫ) | 1999 |
|
RU2152030C1 |



Изобретения относятся к области медико-биологических измерений и могут быть использованы для биологических исследований и диагностических целей. Использование изобретений позволяет с высокой точностью контролировать энергетическое состояние крови и тем самым диагностировать различные заболевания людей. Указанный результат достигается при осуществлении способа определения скорости внутреннего потребления кислорода эритроцитами, заключающегося в заполнении сосуда из газонепроницаемого материала пробой исследуемой крови полностью, без газовых включений, герметизации сосуда и размещении его в термостатируемой камере, непрерывном измерении степени насыщенности кислородом исследуемой пробы крови, определении по изменению степени насыщенности крови кислородом скорости ее спонтанной деоксигенации и вычислении скорости внутреннего потребления кислорода эритроцитами. Указанный результат достигается при осуществлении устройства, содержащего сосуд из газонепроницаемого материала для размещения исследуемой пробы крови, помещенный в термостатируемую камеру, оборудованный приспособлениями для заполнения его кровью полностью, без газовых включений и для герметичного закрывания после заполнения его кровью, и регистратор с чувствительными элементами. 2 с. и 11 з.п.ф-лы, 4 ил.
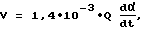
где V - скорость внутреннего потребления кислорода эритроцитами, л кислорода на 1 л крови в мин;
α(t) - степень насыщенности крови кислородом в момент времени t, %;
Q - количество гемоглобина в литре крови, способного обратимо присоединять кислород, г;
dα/dt - скорость спонтанной деоксигенации крови, мин-1.
| Оксигенатор крови | 1983 |
|
SU1217419A1 |
| US 4639353 A, 27.01.87. | |||
Авторы
Даты
2000-02-27—Публикация
1995-08-01—Подача