Изобретение относится к способам количественного анализа биологически (физиологически) активных веществ в пробах различной природы, а именно к способам радиоиммунохимического анализа с использованием метки йод-125. Способы радиоиммунохимического анализа известны.
Так, известен способ радиоиммунохимического анализа с использованием йода-125 (см. справочник "Радиоиммунохимические методы исследования", Г.А. Ткачева, М.И. Балаболкин, И.П. Ларичева, Медицина, М., 1983 г., стр. 76-96, статья "Радиотестирование in-vitro"), суть которого заключается в приготовлении реакционной смеси, ее инкубации, выделении продуктов реакции, определении суммарной интенсивности фотонного излучения, регистрируемого с помощью сцинтилляционного детектора в выделенных продуктах реакции, построении калибровочной кривой анализа, по которой находят количественное содержание определяемого вещества в пробе. Этот способ имеет недостаток, указанный в том же справочнике на стр. 80 - "эффективность детектирования излучения зависит также от объема измеряемой пробы, поэтому... объем проб и положение пробирок в колодезном счетчике (колодезном сцинтилляционном детекторе - авт. ) должны быть совершенно одинаковыми...". Следует отметить, что речь здесь, в сущности, идет о необходимости соблюдения идентичного для всех исследуемых проб взаиморасположения выделенных продуктов реакции и детектора, в противном случае возникает погрешность анализа, однако, это условие при реализации современных модификаций способа не может быть выполнено, поскольку выделенные продукты являются твердой фазой, распределены по стенке пробирки и имеют неконтролируемую геометрию.
Еще известен способ радиоиммунохимического анализа с использованием йода-125 (прототип) (см. прилагаемую Инструкцию по применению набора реактивов для радиоиммунологического определения тироксина РИА-Т4-СТ), заключающийся в приготовлении реакционной смеси, ее инкубации, выделении продуктов реакции, определении суммарной интенсивности фотонного излучения, регистрируемого с помощью сцинтилляционного детектора в выделенных продуктах реакции, построении калибровочной кривой анализа, по которой находят количественное содержание определяемого вещества в пробе.
Этап приготовления реакционной смеси заключается, например, в том, что в ряд пробирок с иммобилизованной на их стенке связывающей системой (в рассматриваемом конкретном примере, иммобилизованными антителами к определяемому веществу - гормону тироксину) с помощью тех или иных дозирующих устройств, например пипеточных дозаторов, вносят в некоторые из пробирок заранее известные, но различные количества определяемого вещества (стандарты), например, в виде одинаковых объемов (20 мкл) растворов с известной концентрацией определяемого вещества (тироксина), соответственно 0, 10, 20, 50, 150, 400 нмоль/л. В остальные пробирки вносят исследуемые пробы (например, определенные объемы (20 мкл) сыворотки крови пациентов), затем во все пробирки вносят одинаковое количество (500 мкл) раствора меченого йодом-125 аналога определяемого вещества (в данном примере меченый йодом-125 тироксин).
После инкубации, заключающейся во встряхивании пробирок с внесенными реагентами в течение 1 часа при температуре 18-25oC, производят выделение продуктов реакции в каждой из пробирок путем аспирации жидкой фазы из каждой пробирки.
Таким образом, получен ряд пробирок, содержащих меченые продукты реакции, иммобилизованные на стенках этих пробирок. Количество меченых продуктов реакции в той или иной пробирке обратно пропорционально количественному содержанию определяемого вещества, внесенного в данную пробирку. Однако при существующих технологиях приготовления иммобилизованных связывающих систем, а также в связи с неуправляемостью местоположения инициации иммунохимической реакции, формирование продуктов реакции происходит неравномерно по поверхности пробирки. Это явление - неоднозначность положения (распределения) продуктов реакции в реакционном сосуде (пробирке) имеет также и другие причины, связанные, в частности, и с конкретной технологией выполнения анализа и присуще всем другим модификациям радиоиммунохимического анализа, использующим в качестве выделенных продуктов реакции твердую фазу - т.е. всем современным модификациям анализа.
Далее в каждой из пробирок производят определение суммарной интенсивности фотонного излучения, регистрируемого с помощью сцинтилляционного детектора. Эта технология наиболее прогрессивна и применяется во всех устройствах для реализации радиоиммунохимического анализа, а сам детектор выполняется на основе монокристалла NaI (Tl).
Распад йода-125 происходит посредством К-захвата (в 100% актов распада) и поясняется схемой на фиг. 1.
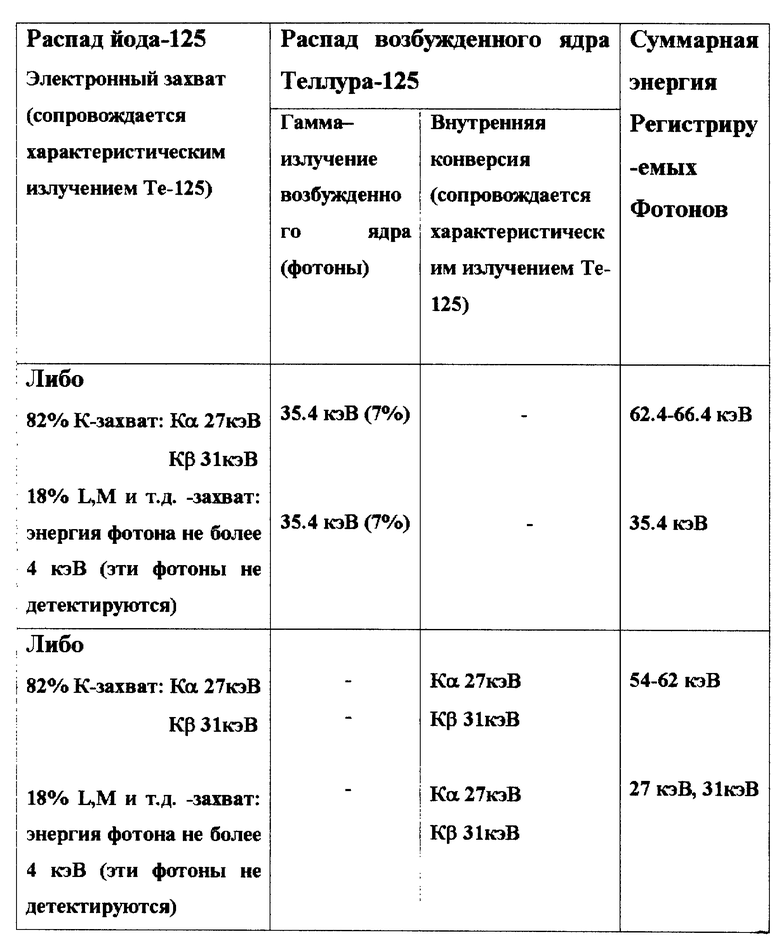
При распаде излучаются либо фотоны характеристического рентгеновского излучения с энергиями Кα = 27 кэВ или Кβ =31 кэВ (в 82% актов К-захвата), либо при захвате электрона с оболочек L, М,... (18% случаев) фотоны с энергией около 4 кэВ, которые полностью поглощаются лучевым окном и другими элементами сцинтилляционного детектора установок для радиоиммунохимического анализа и не регистрируются.
Ядро дочернего атома теллура-125 находится в возбужденном состоянии с периодом полураспада этого состояния 1,6 нс. Переход этого ядра в стабильное состояние происходит либо путем излучения гамма-кванта (фотона) с энергией 35,4 кэВ в 7% случаев, либо путем внутренней конверсии, в ходе которой при замещении образовавшихся вакансий в электронных оболочках излучаются фотоны с энергиями, соответствующими уровням Кα или Кβ (соответственно 27 и 31 кэВ).
Происходящие процессы в суммарном виде отражены в таблице.
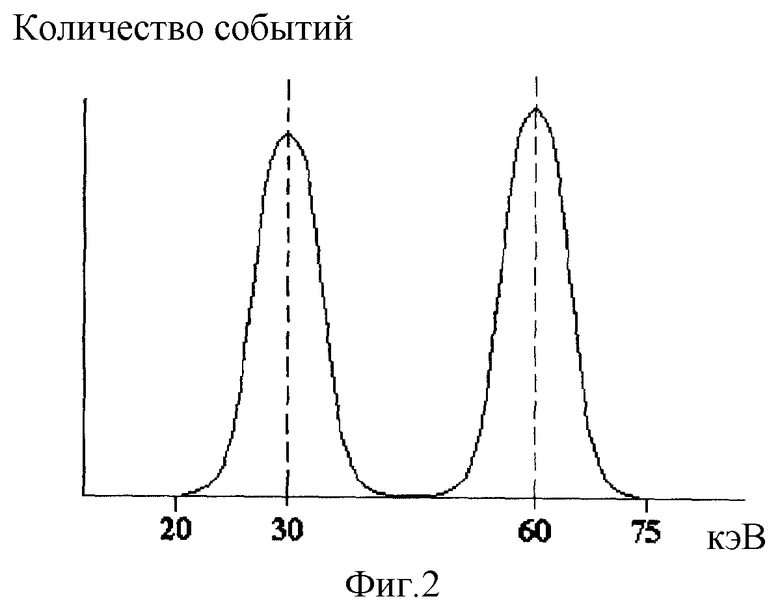
Учитывая свойства сцинтилляционного детектора NaI, а именно разрешающую способность во времени и вышеуказанный энергетический порог получим, что приборный спектр фотонного излучения йода-125 имеет вид, изображенный на фиг. 2.
Пик в области меньших энергий обусловлен фотонами с энергиями 27,31 и 35.4 кэВ, а пик в области больших энергий парами фотонов с энергиями 35,4 и 27 кэВ, или 35,4 и 31 кэВ, или 27 и 27 кэВ, или 27 и 31 кэВ (регистрируемых, как совпадающие во времени из-за недостаточного временного разрешения сцинтилляционного детектора).
В известном способе радиоиммунохимического анализа используется определение суммарной интенсивности фотонного излучения, регистрируемого сцинтилляционным детектором, т. е. суммарное количество событий, зарегистрированных в первом и втором пиках. Обычно энергетическое окно, используемое практически во всех известных установках для реализации анализа, составляет 20-75 кэВ. Тем самым преследуется цель обеспечить регистрацию практически всех фотонов, попавших в чувствительный объем детектора. Однако количество фотонов, попавших в чувствительный объем детектора, зависит от взаиморасположения продуктов реакции и детектора, таким образом, вышеуказанная неоднозначность положения (распределения) продуктов реакции в пробирках опосредуется детектором и приводит к позиционной погрешности определения интенсивности суммарного фотонного излучения в пробе. Исключить указанную погрешность, непосредственно влияющую на точность анализа, теоретически возможно, регистрируя фотоны, излученные исследуемой пробой в телесный угол, равный 4π.
Однако на практике создание такого детектора с истинной 4π-геометрией и полным сбором фотонного излучения пробы, независимо от геометрических особенностей распределения продуктов реакции в пробе, не представляется возможным. Реально ограничиваются колодезными конструкциями детекторов, регистрирующих (для лучших конструкций) 80-85% фотонного излучения точечной пробы, расположенной на дне колодца. При изменении пространственного взаиморасположения пробы и детектора или при изменении геометрии активной зоны пробы доля зарегистрированного излучения изменяется. При этом позиционная погрешность для стандартных конструкций таких детекторов (нормируемая для проб с протяженностью активной зоны 0-15 мм), применяемых в большинстве зарубежных установок для радиоиммунохимического анализа, составляет 12-15%. В современных установках (например, Наркотест, Гамма-НТ, Иммунотест, разработанных и выпускаемых ЗАО ВНИИМП-ВИТА) применяется конструкция колодезного детектора с компенсацией позиционной погрешности (авторское свидетельство СССР N 1345403), позволяющая при прочих равных условиях снизить величину этой погрешности до 5%.
Полученные данные о суммарной интенсивности фотонного излучения в каждой из пробирок (первичная диагностическая информация) используют для построения калибровочной кривой анализа. Например, откладывают на графике по оси абсцисс в логарифмическом масштабе содержание исследуемого вещества в пробах с известным содержанием вещества (стандартах), а по оси ординат соответствующее значение процентного отношения суммарной интенсивности фотонного излучения в каждой из этих проб к суммарной интенсивности фотонного излучения пробы с отсутствием определяемого вещества (коэффициент связывания). По полученным точкам проводят интерполяцию или находят ту или иную кривую регрессии.
В общем случае калибровочная кривая анализа - зависимость коэффициента связывания от содержания исследуемого вещества в пробе является существенно нелинейной (гиперболой). Для построения этой кривой по полученным точкам применяются различные математические методы, использующие гипотезу о ходе протекающих иммунохимических реакций или не опирающиеся на модель.
С помощью построенной калибровочной кривой находят количественное содержание определяемого вещества в исследуемых пробах, откладывая по оси ординат величину коэффициента связывания для данной пробы и считывая по оси абсцисс содержание определяемого вещества в ней.
Как видно из вышеприведенного описания способа анализа, ошибки в определении суммарного фотонного излучения в выделенных продуктах реакции приводят к искажению результатов анализа - снижению его точности. При этом рассматриваемый источник погрешности остается одним из основных факторов, ограничивающих точность радиоиммунохимического анализа (на этапах дозирования сегодня достигается точность порядка долей процента), даже при использовании детекторов с компенсацией позиционной погрешности. Недостаточная точность анализа особенно проявляется в тех пологих областях калибровочной кривой, где незначительные погрешности в определении интенсивности излучения приводят к существенной погрешности в количественной оценке содержания определяемого вещества в пробе.
Влияние позиционной погрешности на результат анализа может быть снижено путем постановки анализа с использованием нескольких репликатов одной и той же пробы и усреднением полученных результатов (обычно используют два репликата). Однако этот путь сопровождается расходом реагентов, трудозатрат и удорожает анализ. Наличие позиционной погрешности приводит также к недостаточности динамического диапазона анализа, поскольку для расширения диапазона измерения содержания определяемого вещества необходимо увеличивать площадь пробирки, на которой иммобилизовывается связывающая система, а это сопровождается резким увеличением позиционной погрешности (даже при использовании детекторов с компенсацией). Другой путь расширения динамического диапазона - анализ в области пологой части калибровочной кривой также неприемлем без снижения позиционной погрешности.
Следует отметить, что расширение динамического диапазона анализа является особо актуальным при измерении ряда гормонов у женщин в ходе суперовуляции при проведении экстракорпорального оплодотворения, в частности, эстрадиола, хорионического гонадотропина, прогестерона.
Вышеописанный способ радиоиммунохимического анализа имеет множество модификаций, касающихся используемых реагентов, последовательности внесения реагентов и проб при приготовлении реакционной смеси, методов выделения продуктов реакции, методов построения калибровочной кривой, не изменяющих данный способ анализа по существу.
Предлагаемое изобретение решает задачи повышения точности, расширения динамического диапазона анализа и снижения его стоимости путем исключения влияния неоднозначности положения (распределения) выделенных продуктов реакции в пробирке на результат анализа (неоднозначности взаиморасположения выделенных продуктов реакции и детектора).
Решение поставленной задачи достигается тем, что в способе радиоиммунохимического анализа и использованием йода-125, заключающемся в приготовлении реакционной смеси, ее инкубации, выделении продуктов реакции, построении калибровочной кривой анализа, по которой находят количественное содержание исследуемого вещества в пробе, согласно предлагаемому изобретению с помощью сцинтилляционного детектора в выделенных продуктах реакции определяют интенсивность Aоф однофотонного излучения и интенсивность Aс временных совпадений излучаемых фотонов, рассчитывают параметр G по формуле
G=(Aоф+2Aс)2/Aс,
который используют при построении калибровочной кривой.
Таким образом сущность настоящего изобретения заключается в том, что благодаря вышеописанному техническому решению повышается точность, расширяется динамический диапазон анализа и снижается его стоимость путем исключения влияния неоднозначности взаиморасположения выделенных продуктов реакции и детектора на результат анализа.
Изложенная сущность изобретения поясняется на примере конкретного анализа гормона эстрадиола в сыворотке крови с помощью набора (описание прилагается) готовых реагентов фирмы IMMUNOTECH (кат. N 1663). В комплект набора входят 100 шт. одинаковых пробирок, содержащих иммобилизованные на стенде антитела к эстрадиолу, 7 стандартов, содержащих эстрадиол в количестве 0, 10, 40, 140, 500, 1500, 5000 пг/мл соответственно, называемых B0, B1, B2... B6, и раствор эстрадиола меченого йодом-125. В первые 7 пробирок внесем соответственно по 100 мкл стандарта: в первую пробирку B0, во вторую B1 и т.д. Далее в оставшиеся пробирки последовательно вносят исследуемые пробы Bx1, Bx2 и т.д. Затем в каждую из пробирок вносят по 500 мкл раствора, содержащего меченый йодом-125 эстрадиол. Затем инкубируют пробирки с полученной реакционной смесью в течение 3 часов при непрерывном встряхивании при комнатной температуре. Для этой цели можно использовать, в частности, смешиватель вибрационный для радиоиммунохимического анализа СВ-3, выпускаемый ЗАО "ВНИИМП-ВИТА". После указанной инкубации производят выделение продуктов реакции в каждой из пробирок путем аспирации жидкой фазы, например, с помощью пастеровской пипетки, подключенной к водоструйному насосу. Таким образом получен ряд пробирок B0, B1. . . B6, Bx1, Bx2 ..., содержащих выделенные продукты реакции, иммобилизованные на стенках пробирок. Далее в каждой из пробирок с помощью сцинтилляционного детектора определяют интенсивность однофотонного излучения и интенсивность временных совпадений излучаемых фотонов.
Этот процесс выполняют, например, с помощью установки для радиоиммунохимического анализа седьмого поколения "ПОЛИТЕСТ-2000", образцы которой разработаны ЗАО "ВНИИМП-ВИТА", а ее серийное освоение запланировано на 4 кв. 1999 г. Установка содержит 12 сцинтилляционных детекторов, так что одновременно измеряется 12 пробирок, помещенных каждая в свой детектор. Сигналы детекторов подвергаются амплитудной селекции и последующему подсчету. Таким образом, определяется интенсивность однофотонного излучения (площадь пика в области меньших энергий) и интенсивность временных совпадений излучаемых фотонов (площадь пика в области больших энергий). Пусть A - суммарная интенсивность излучения фотонов в телесный угол 4π в продуктах реакции, содержащихся в какой-либо пробирке (рассматриваем только те фотоны энергия, которых позволяет зарегистрировать их сцинтилляционным детектором). Обозначим доли фотонного излучения, попавшего в чувствительный объем детектора и зарегистрированного в нем, как q1, q2 и q3 для фотонов с энергиями 27, 31, 35,4 кэВ соответственно. Ввиду близости энергий этих фотонов величины q1, q2 и q3 различаются между собой менее чем на 1% (для реальных конструкций сцинтилляционных детекторов с лучевым окном из алюминия толщиной 0,2 мм), поэтому можно принять q1 = q2 = q3 = q. Величина q существенно зависит от распределения выделенных продуктов реакции в пробирке (от взаиморасположения этих продуктов и детектора) и эта зависимость предопределяет величину позиционной ошибки. Обозначим вероятность излучения фотона в ходе К-захвата как p1, а вероятность излучения фотона в ходе распада возбужденного ядра теллура-125 (гамма-излучение возбужденного ядра или излучение при заполнении вакансий в электронных оболочках) как p2.
Тогда интенсивность A1 регистрируемого однофотонного излучения при К-захвате будет
A1=qp1A-q2p1p2A,
где q2p1p2A - учитывает долю совпадающих событий.
Аналогично интенсивность A2 регистрируемого однофотонного излучения в ходе распада возбужденного ядра теллура-125 будет
A2=qp2A-q2p1p2A
Интенсивность Aоф регистрируемого однофотонного излучения составит тем самым
Aоф = A1+A2 - qp1A + qp2A - 2q2p1p2A; (1)
Интенсивность Aс временных совпадений излучаемых фотонов составит
Aс=q2p1p2A; (2)
Решение системы уравнений (1), (2) относительно A дает
A = (p1p2/(p1 + p2)2) [(Aоф+2Aс)2/Aс] (3)
Иначе A = KG, где
К = p1p2/(p1 + p2)2;
G=(Aоф+2Aс)2/Aс; (4)
Величина A, расчитанная по формуле (3), не зависит от значения q и тем самым не зависит от распределения выделенных продуктов реакции в пробирке (взаиморасположения выделенных продуктов и детектора). Учитывая, что К - константа (можно показать, что значение К ≈ 0,92) величина G также не зависит от значения q и тем самым не зависит от распределения выделенных продуктов реакции в пробирке (взаиморасположения выделенных продуктов и детектора).
Калибровочная зависимость строится на основании значений G, вычисленных по формуле (4) для каждой пробы B0, B1, B2...B6 по измеренным для этой пробы величинам Aоф и Aс.
Калибровочная зависимость может быть, например, построена в следующей системе координат: G/G0 - по оси ординат и logC по оси абсцисс, где G/G0 -коэффициент связывания - процентное отношение значения G к величине G0, вычисленной для пробы B0, а C - концентрация определяемого вещества.
Калибровочная зависимость может быть построена, например, с использованием интерполяционного кубического сплайна (этот широко распространенный метод и его алгоритм приведены, в частности, в "Инструкции оператора установки для радиоиммунохимического анализа Гамма-800, Наркотест тА0.005.022И"). Далее с помощью построенной калибровочной зависимости находят содержание определяемого вещества - эстрадиола в каждой из исследуемых проб Bx1, Bx2 и т. д. , рассчитывая для каждой из этих проб соответствующее значение GBxi/G0, откладывая это значение на оси ординат и считывая с помощью калибровочной зависимости искомое содержание вещества в пробе по оси абсцисс.
Проведенные испытания полностью подтвердили преимущества заявленного способа перед известными. Так, в силу независимости результата анализа от расположения выделенных продуктов реакции в пробирке (взаиморасположения выделенных продуктов и детектора) существенно повышается точность анализа: снижается коэффициент вариации между репликатами пробы. Это можно характеризовать следующими значениями, в частности, коэффициент вариации между 20 репликатами референтных проб (воспроизводимость внутри анализа) для вышеприведенного анализа эстрадиола при реализации известного способа на установке "Политест-2000" составил для проб с содержанием эстрадиола 5,2; 360; 4600 пг/мл соответственно 12,3; 7,6 и 14,8%, а при анализе тех же проб на той же установке, но в режиме реализации предлагаемого способа 3,2; 2,3 и 3,8% (в обоих случаях измерения производились при уровне статистической погрешности, не превышающей 1%).
Аналогично для тех же проб при анализе с использованием 6 различных серий данного диагностического набора были получены следующие величины коэффициента вариации (воспроизводимость между анализами) соответственно для известного способа 15,2; 12,1; 19,6% и для предложенного - 4,8; 3,5; 5,2%.
Столь существенное уменьшение коэффициента вариации позволяет реально отказаться от репликации проб при проведении анализа, что приводит к существенному снижению стоимости анализа. Значительное снижение коэффициента вариации в области как низких так и, особенно, высоких концентраций позволяет расширить динамический диапазон анализа, как на стадии измерения проб, так и на стадии изготовления диагностического набора, поскольку на этой стадии становится возможным увеличить поверхность иммобилизации связывающего агента на стенке пробирки.
Проведенный эксперимент показал, что при существенном изменении взаиморасположения пробирки с продуктами реакции и сцинтилляционного детектора (пробирка приподнималась на 20 мм (!!!) над дном колодца детектора глубиной 37 мм), результат анализа при концентрации эстрадиола в пробе 360 пг/мл изменялся менее чем на 1,5% в предлагаемом способе и в 2,2 раза (!!!) в известном.
Дополнительным достоинством предлагаемого способа является снижение требований к сцинтилляционному детектору: нет необходимости усложнения конструкции для компенсации позиционной погрешности, кроме того, разброс параметров детекторов не влияет на результаты анализа, что особенно важно для многодетекторных установок.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАДИОИММУНОХИМИЧЕСКОГО АНАЛИЗА | 1999 |
|
RU2154831C1 |
| СПОСОБ СТАНДАРТИЗАЦИИ ДАННЫХ ПОЛИМЕРНОЙ ЦЕПНОЙ РЕАКЦИИ С РЕГИСТРАЦИЕЙ НАКОПЛЕНИЯ ПРОДУКТОВ РЕАКЦИИ ПО ФЛУОРЕСЦЕНЦИИ НЕПОСРЕДСТВЕННО ВО ВРЕМЯ РЕАКЦИИ (ПЦР "В РЕАЛЬНОМ ВРЕМЕНИ") | 2006 |
|
RU2294532C1 |
| СПОСОБ КОНТРОЛЯ ОБОГАЩЕНИЯ УРАНА В ПОРОШКАХ | 1996 |
|
RU2100856C1 |
| Способ флуоресцентного рентгенорадиометрического анализа состава вещества и устройство для его осуществления | 1983 |
|
SU1083100A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ГАДОЛИНИЯ В ТВЭЛе | 2001 |
|
RU2194271C2 |
| МОБИЛЬНЫЙ РЕНТГЕНОВСКИЙ ПЛОТНОМЕР | 2015 |
|
RU2617001C1 |
| СПОСОБ КОРРЕКЦИИ СИГНАЛОВ СЦИНТИЛЛЯЦИОННОГО ДЕТЕКТОРА | 2010 |
|
RU2418306C1 |
| Устройство непрерывного контроля обогащения и содержания оксида гадолиния в пресспорошке ядерного топлива при его засыпке в устройство прессования топливных таблеток | 2016 |
|
RU2629371C1 |
| РЕНТГЕНОФЛУОРЕСЦЕНТНЫЙ АНАЛИЗАТОР СОСТАВА И СКОРОСТИ ГАЗОЖИДКОСТНОГО ПОТОКА НЕФТЯНЫХ СКВАЖИН | 2008 |
|
RU2379666C1 |
| РЕНТГЕНОФЛУОРЕСЦЕНТНЫЙ АНАЛИЗАТОР КОМПОНЕНТНОГО СОСТАВА И СКОРОСТИ ТРЕХКОМПОНЕНТНОГО ПОТОКА НЕФТЯНЫХ СКВАЖИН | 2008 |
|
RU2379667C1 |
Изобретение относится к способам количественного анализа биологически активных веществ в пробах различной природы ,а именно к способам радиоиммунохимического анализа с использованием метки йод-125. Способ радиоиммунохимического анализа с использованием йода-125 заключается в приготовлении реакционной смеси, ее инкубации, выделении продуктов реакции, построении калибровочной кривой анализа, по которой находят количественное содержание исследуемого вещества в пробе. С помощью сцинтиляционного детектора в выделенных продуктах реакции определяют интенсивность Аоф однофотонного излучения и интенсивность Ас временных совпадений излучаемых фотонов, рассчитывают параметр G по формуле G(Аоф + 2Ас)2/Ас, который используют при построении калибровочной кривой. Использование изобретения позволяет повысить точность анализа. 2 ил, 1 табл.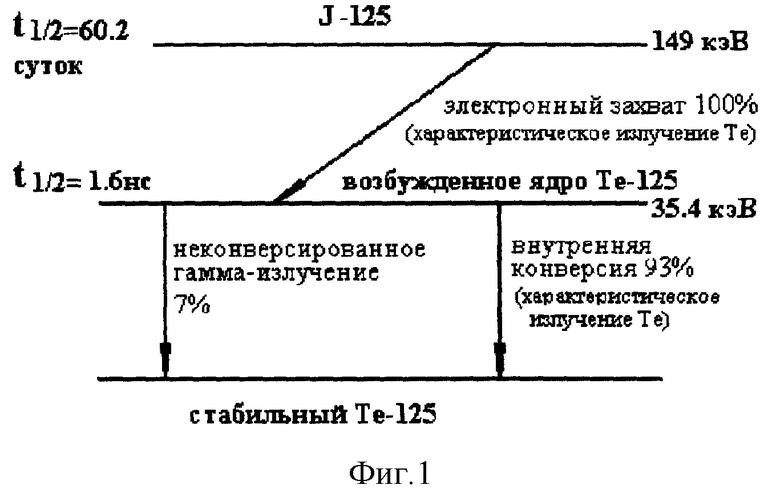
Способ радиоиммунохимического анализа с использованием йода-125, включающий приготовление реакционной смеси, ее инкубацию, выделение продуктов реакции, регистрацию информационного параметра, построение калибровочной зависимости, с использованием которой определяют количественное содержание исследуемого вещества в пробе, отличающийся тем, что с использованием сцинтилляционного детектора в выделенных продуктах реакции определяют для различных проб с известным содержанием исследуемого вещества интенсивность Аоф однофотонного излучения и интенсивность Ас временных совпадений излучаемых фотонов, рассчитывают параметр G по формуле G = (Аоф + 2Ас)2/Ас для каждой измеренной пробы, строят калибровочную зависимость по рассчитанным значениям, а в качестве информационного параметра для пробы с неизвестным содержанием исследуемого вещества используют величину G.
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ α -ФОТОПРОТЕИНА | 1990 |
|
RU2009506C1 |
| СПОСОБ ДИАГНОСТИКИ ПИЛОРИЧЕСКОГО ГЕЛИКОБАКТЕРИОЗА | 1991 |
|
RU2009507C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ГОРТАНИ У ЛИЦ МУЖСКОГО ПОЛА | 1991 |
|
RU2024022C1 |
Авторы
Даты
2000-05-20—Публикация
1999-06-28—Подача