Изобретение касается способа проведения гидролиза галактоманнанов, содержащихся в жидком кофейном экстракте.
В патенте США N 2801920 раскрыт способ проведения гидролиза галактоманнанов, содержащихся в кофейном экстракте, с получением бета-маннаназ с целью предотвращения образования геля при застывании этого экстракта.
В журнале Food Review, 8/9, 37 - 39 (1984), раскрыт способ промышленного использования бета-маннаназ для понижения вязкости жидкого кофейного экстракта, чем обеспечивается возможность концентрирования его с достижением высоких содержаний сухого вещества.
Однако этот способ промышленного использования бета-маннаназ обладает некоторыми недостатками. Например, фермент бесполезно расходуется, поскольку используется только один раз. Наличие фермента в конечном продукте также является нежелательным.
Настоящее изобретение направлено на устранение недостатков, свойственных прежнему уровню техники.
Для этого в способе проведения гидролиза галактоманнанов жидкого кофейного экстракта согласно настоящему изобретению этот экстракт подвергают гидролизу при температуре в области 20 - 80oC совместно в иммобилизованными бета-маннаназами.
Бета-маннаназы предпочтительно иммобилизуют посредством ковалентного связывания на субстрате или посредством полимеризации бета-маннаназ, адсорбированных на носителе.
Изобретение, следовательно, характеризуется тем преимуществом, что обеспечивает сохранность ферментов.
Другое преимущество состоит в том, что не происходит высаливание бета-маннаназы с субстрата.
Другое преимущество состоит в том, что обеспечивается возможность работы при такой температуре, при которой не наблюдается бактериальное загрязнение.
Поразительное преимущество настоящего изобретения состоит в том, что бета-маннаназы не теряют свою активность после ковалентного связывания на носителе или после полимеризации молекул, абсорбированных на носителе. Аналогичным образом, ферментативная активность иммобилизованной бета-маннаназы является сравнительно постоянной во времени.
И, наконец, настоящее изобретение обладает еще и другим преимуществом, которое состоит в том, что кофейный экстракт может быть подвергнут гидролизу в реакторе типа бака с мешалкой и в реакторе, содержащем неподвижный или псевдоожиженный слой иммобилизованных бета-маннаназ, несмотря на вязкость кофейного экстракта.
В последующем описании термин "реактор типа бака с мешалкой" относится к системе, в которой происходит механическое перемешивание суспензии, состоящей из иммобилизованных бета-меннаназ.
Аналогичным образом, под термином "неподвижный слой иммобилизованных бета-маннаназ" понимают бета-маннаназы, иммобилизованные на или в носителе, который уплотнен в реакторе, предназначенном для непрерывной обработки жидкого кофейного экстракта.
Под термином "псевдоожиженный слой иммобилизованных бета-маннаназ" понимают бета-маннаназы, иммобилизованные на носителе, который содержится без уплотнения в реакторе, предназначенном для непрерывной обработки жидкого кофейного экстракта. Поток кофейного экстракта, циркулирующий от днища к верху, затем переводит частицы носителя в состояние суспензии. Этот тип реактора, известного как "реактор с псевдоожиженным слоем", является особенно предпочтительным для обработки сред, содержащих твердое вещество в состоянии суспензии.
Термины "маннобиоза" и "маннотриоза" соответственно означают димер или тример маннозы, и термин "манносахарид" распространяется на полимер, состоящий по крайней мере из двух манноз.
Единица активности бета-маннаназы определяется как количество бета-маннаназы, которое высвобождает из смолы кароб-дерева количество восстанавливающихся сахаров, эквивалентное одному микромолю маннозы за минуту при pH 5 и 30oC.
Для осуществления изобретения бета-маннаназа, следовательно, может быть, к примеру, иммобилизована ковалентным связыванием на поверхности традиционного носителя или может быть иммобилизована проведением полимеризации бета-маннаназы, предварительно адсорбированной на поверхности традиционного носителя.
Жидкий кофейный экстракт может быть, к примеру, затем подвергнут гидролизу при 40 - 70oC совместно с этими ферментами, претерпевшими иммобилизацию.
В этом случае предпочтительно следует использовать бактериальную или грибковую бета-маннаназу, например бета-маннаназу, экстрагированную из Aspergillus niger, особенно очищенную бета-маннаназу из Aspergillus niger, известную под зарегистрированной торговой маркой Гаманаза (фирма Ново-Нордиск, Дания).
Кроме того, жидкий кофейный экстракт может быть получен перколяцией экстрагирующей жидкости через ячейки, заполненные молотым обжаренным кофе. Эта экстракция может быть осуществлена противоточным способом, т.е. воду под давлением, развиваемым при температуре, которая может находиться в области от 150 до 180oC, подают в ячейку с загрузкой молотого обжаренного кофе, которая в значительной мере уже является здесь отработанной, поскольку она уже претерпела N экстракций. Жидкий экстракт, выходящий из этой экстракционной ячейки, затем пропускают через экстракционную ячейку, содержащую загрузку кофе, которая была уже использована (N-1) раз, и т.д. до пропускания жидкого экстракта через ячейку, которая только что была заполнена свежим молотым обжаренным кофе. Конечный экстракт, который используют, выходит из последней ячейки с температурой порядка 100oC. Можно, следовательно, провести различие между ступенью, находящейся под давлением и образованной ячейками, которые содержат наиболее отработанное кофе, и атмосферной ступенью, образованной ячейками, которые содержат менее отработанный кофе.
Жидкий кофейный экстракт может быть также получен перколяцией экстрагирующей жидкости через ячейки, заполненные молотым обжаренным кофе, которые находятся под давлением. При осуществлении этого процесса, известного как "расщепительная экстракция", причем этот термин будет использоваться в остальной части описания, используют две экстракционные жидкости, причем экстракционные ячейки подразделяют на ступень, работающую под давлением, и атмосферную ступень, где экстракция на каждой ступени производится своей собственной экстракционной жидкостью. Кофе, находящееся в атмосферной ступени, экстрагируют первой экстракционной жидкостью при умеренных температурных и сжимающих условиях, тогда как кофе, находящийся в ступени, работающий под давлением, экстрагируют второй экстракционной жидкостью при условиях со значительно более высокими температурой и давлением. Результатом сказанного является получение двух различных жидких экстрактов, которые, к примеру, после частичного упаривания экстракта, выходящего из ступени, работающей под давлением, могут быть соединены друг с другом и затем превращены в порошок общеизвестными способами.
В настоящем изобретении, следовательно, может быть, в частности, использован экстракт со ступени, работающей под давлением, который получают при проведении расщепительной экстракции молотого обжаренного кофе и который еще не подвергнут частичному упариванию.
По этой причине предпочтительно следует использовать экстракт со ступени, работающей под давлением, который раскрыт, например, в патенте EP 0538512.
Согласно настоящему изобретению носитель может быть также пористым носителем, в частности, к примеру, обладать порами с размером в области 20 - 200 нм.
В частности, пористый носитель может быть выбран из группы, образованной частицами диоксида кремния, стекла, акрилового полимера, особенно акрилового полимера с зарегистрированной торговой маркой Ойпергит-C (фирма Рем, Германия), и фенольного полимера, особенно фенолоформальдегидной смолы с зарегистрированной торговой маркой Дюолит (фирма Супелко, США), к примеру, смола Дюолит S-761.
Бета-маннаназу предпочтительно иммобилизуют ковалентным связыванием на поверхности акрилового полимера с зарегистрированной торговой маркой Ойпергит-C. Последний обладает эпоксидными группами, делающими возможной иммобилизацию бета-маннаназ. По этой причине оказывается возможным, к примеру, иммобилизовать по крайней мере 1900 ед. бета-маннаназ на 1 г Ойпергита-C.
Бета-маннаназы предпочтительно следует иммобилизовать полимеризацией бета-маннаназ, адсорбированных на поверхности частиц фенольной смолы Дюолит. Можно, например, использовать глутаральдегид в качестве полимеризационного агента.
В первом предпочтительном варианте осуществления настоящего изобретения кофейный экстракт гидролизуют в реакторе типа бака с мешалкой, делая это в присутствии бета-маннаназы, иммобилизованной либо посредством ковалентного связывания с носителем, либо посредством полимеризации маннаназ, адсорбированных на носителе. Система может быть автоматизирована и может действовать в полунепрерывном режиме с последовательным проведением трех стадий. На первой стадии, к примеру, бак заполняют кофейным экстрактом, который должен быть подвергнут обработке, затем проводят гидролиз с механическим перемешиванием, после чего по прошествии определенного времени бак опорожняют. Удерживание фермента в реакторе может быть осуществлено применением фильтра, установленного в нижней части бака. Этот фильтр может задерживать, к примеру, все частицы с диаметром выше 40 мкм.
При этом способе проведения гидролиза оказывается, что бета-маннаназы, иммобилизованные ковалентным связыванием с носителем, обладают хорошей стабильностью, поскольку они могут сохранять более 60% своей ферментативной активности после проведения, к примеру, по крайней мере 500 последовательных циклов гидролиза кофейного экстракта.
Во втором предпочтительном варианте осуществления настоящего изобретения жидкий кофейный экстракт непрерывно гидролизуют в реакторе, содержащем неподвижный слой бета-маннаназ, иммобилизованных либо проведением ковалентного связывания с носителем, либо проведением полимеризации бета-маннаназ, адсорбированных на носителе. При работе по этому варианту иммобилизованные бета-маннаназы сохраняют хорошую стабильность, удерживая более 80% своей ферментативной активности после непрерывного проведения гидролиза в течение, к примеру, более 20 ч.
В третьем предпочтительном варианте осуществления настоящего изобретения жидкий кофейный экстракт непрерывно гидролизуют в реакторе, содержащем псевдоожиженный слой бета-маннаназ, иммобилизованных ковалентным связыванием с носителем.
Следующие примеры иллюстрируют способ согласно настоящему изобретению. В этих примерах использована бета-маннаназа, известная под торговой маркой Гаманаза, которая обладает удельной активностью в 65000 ед. на 1 г белков, и в некоторых из этих примеров в качестве модельного субстрата использован 2%-ный раствор растворимого кофе в дистиллированной воде или раствор галактоманнанов, полученных из смолы кароб-дерева, что является очень хорошей иллюстрацией результатов, которые могут быть получены с кофейным экстрактом.
Этим примерам предшествуют информация по проведению хроматографического анализа экстрактов и описание чертежей.
Тонкослойная хроматография высокого разрешения
Олигосахариды, присутствующие в жидком кофейном экстракте, определяли качественно и количественно, проводя хроматографию без предварительной очистки этого экстракта. Тем самым эту методику можно было использовать в различных тестах, таких как, например, установление ферментативной кинетики гидролиза галактоманнанов и измерение остаточной ферментативной активности гидролизованных кофейных экстрактов.
С этой целью использовали пластинки из диоксида кремния, предназначенные для проведения высокоэффективной тонкослойной хроматографии "силикагель 60" (фирма Мерк, тип 5631/5641). Наносили эквивалент из 80 мкг сухого кофейного экстракта и последовательно осуществляли три проявления с использованием растворителя, состоящего из хлороформа, уксусной кислоты и воды, взятых в соотношении 30: 35:11. Пластинку при 110oC в течение 30 мин подвергали воздействию реактива, содержащего 4 мл анилина, 4 г дифениламина, 200 мл ацетона и 30 мл 85%-ной фосфорной кислоты.
Тем самым обеспечивалась возможность качественного определения олигосахаридов, присутствующих в экстракте, например свободной маннозы, маннобиозы, маннотриозы и других манносахаридов со степенями полимеризации менее 8.
Обеспечивалась также возможность определения содержания различных олигосахаридов в экстракте, что достигалось сопоставлением плотности окрашивания пластинки, отвечающей олигосахариду из экстракта, с плотностью окрашивания пластинки, отвечающей этому олигосахариду, нанесенному на пластинку при известной концентрации. Считали также, что гидролиз галактоманнанов проходит на 100%, когда остаются только маннобиоза и маннотриоза, поскольку они представляют собой конечные продукты реакции, которые фермент уже не способен расщеплять.
Фиг. 1 (a и b) характеризует гидролиз галактоманнанов в реакторе с неподвижным слоем, содержащим бета-маннаназу, иммобилизованную на Дюолите S-761. Изображены выраженная в процентах глубина протекания гидролиза в зависимости от времени пребывания (1a) и относительная активность фермента в зависимости от времени (1b).
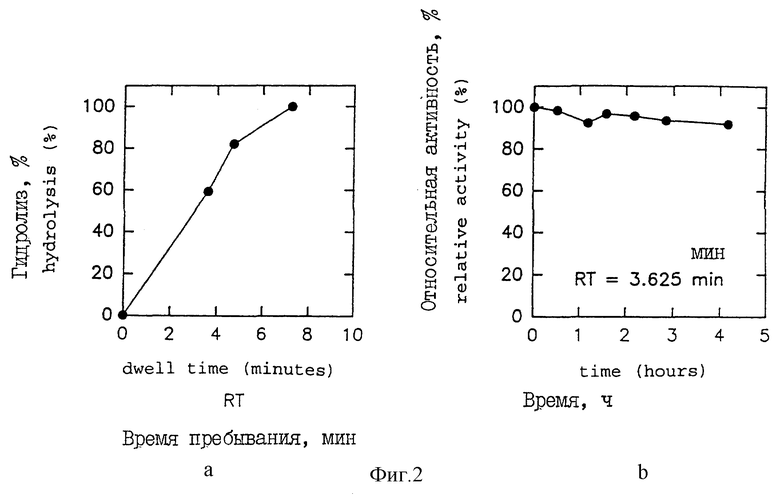
Фиг. 2 (a и b) характеризует гидролиз галактоманнанов в реакторе с неподвижным слоем, содержащим бета-маннаназу, иммобилизованную на шариках из диоксида кремния. Изображены выраженная в процентах глубина протекания гидролиза в зависимости от времени пребывания (2a) и относительная активность фермента в зависимости от времени (2b).
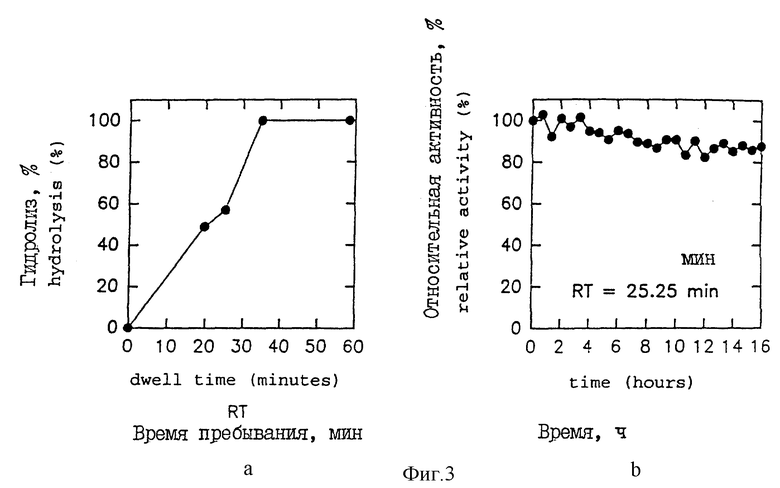
Фиг. 3 (a и b) характеризует гидролиз галактоманнанов в реакторе с неподвижным слоем, содержащем бета-маннаназу, иммобилизованную на материале Ойпергит-С. Изображены выраженная в процентах глубина протекания гидролиза в зависимости от времени пребывания (3a) и относительная активность фермента в зависимости от времени (3b).
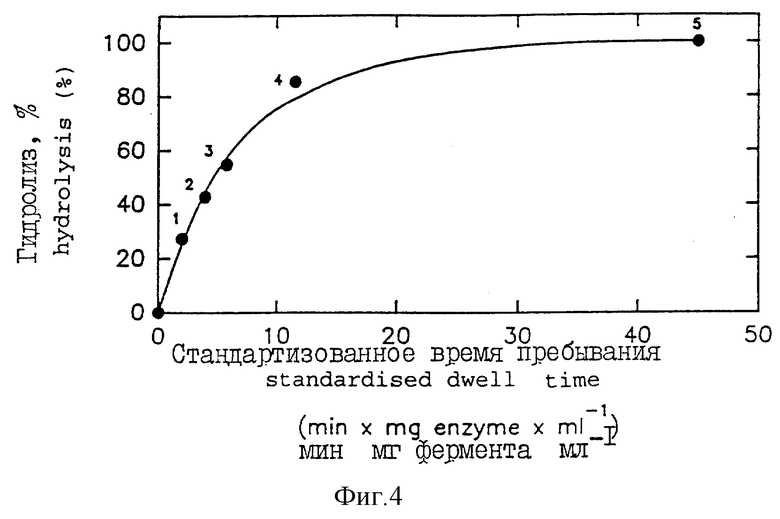
Фиг. 4 характеризует гидролиз кофейного экстракта в псевдоожиженном слое бета-маннаназой, иммобилизованной на материале Ойпергит-С. Изображена выраженная в процентах глубина протекания гидролиза в зависимости от стандартизованного времени пребывания.
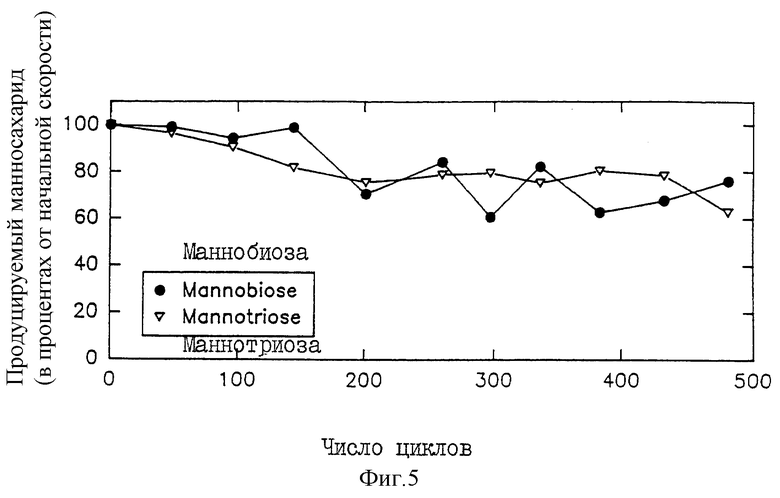
Фиг. 5 характеризует гидролиз кофейного экстракта в баке с перемешиванием бета-маннаназой, иммобилизованной на материале Ойпергит-С. Изображено процентное содержание получаемого манносахарида в зависимости от числа циклов гидролиза.
Пример 1.
Бета-маннаназу иммобилизовали адсорбцией и полимеризацией в фенольном полимере, для чего поступали следующим образом.
Использовали смолу с зарегистрированной торговой маркой Дюолит-S - 761 (фирма Супелко, США), имеющую поры размером порядка 60 км. Эту смолу просеивали, получая частицы размером 0,2 - 0,4 мм, обрабатывали в течение 1 ч 0,5 н. раствором NaOH, затем промывали водой, далее обрабатывали в течение 30 мин 0,25 н. раствором HCl и, наконец, промывали дистиллированной водой до pH 4. К 5 г обработанной смолы добавляли 25 мл раствора, состоящего из 5 мл Гаманазы (зарегистрированная торговая марка) и 20 мл 0,1 М буферного раствора фосфата натрия с pH 6, и Гаманазе давали адсорбироваться на смоле, оставляя ее на 12 ч при 22oC в условиях осторожного перемешивания. Препарат затем промывали дистиллированной водой и адсорбированные ферменты полимеризовали, воздействуя раствором 2,5%-ного глутаральдегида в течение 3 ч при 22oC, после чего препарат, наконец, промывали дистиллированной водой.
Раствор галактоманнанов готовили также нагреванием 3 г смолы из кароб-дерева до 80oC в 1 л 0,1 М ацетатного буферного раствора с pH 5 и растворимую часть раствора использовали для проведения следующих тестов.
Иммобилизованный фермент тестировали тем самым в обычном реакторе с неподвижным слоем. Этот реактор представляет собой трубчатый стеклянный корпус и два найлоновых фильтра (70 мкм), образующих горизонтальную поверхность на каждом конце корпуса. Реактор погружен в водяную баню с температурой 30oC, и раствор галактоманнанов прокачивали обычным перистальтическим насосом, затем нагревали до 30oC перед пропусканием через реактор.
В первом примере раствор галактоманнанов прокачивали с различными скоростями через реактор. Затем обычным способом измеряли количество восстанавливающих сахаров, появляющихся в элюате, в зависимости от времени пребывания (RT) экстракта в реакторе. Затем определяли выраженную в процентах глубину протекания гидролиза галактоманнанов в функции от времени пребывания экстракта в реакторе. Считали, что гидролиз проходит на 100%, если количество восстанавливающих сахаров, получаемых при этом, оказывается равным тому, которое получается в отдельном тесте проведением полного гидролиза субстрата неиммобилизованной Гаманазой. Полученные результаты показаны на фиг. 1a.
Во втором примере раствор галактоманнанов непрерывно подавали в реактор. В этом случае время пребывания (RT) в начале проведения эксперимента выбирали таким, при котором глубина протекания гидролиза оказывается менее 100%. Затем регулярно измеряли количество восстанавливающих сахаров, появляющихся в элюате. Установлено, что это количество понижается в функции от времени, что, возможно, происходит из-за потери ферментом активности. Именно по этой причине относительную активность (%) фермента определяли в функции от времени, соотнося количество восстанавливающих сахаров, получаемых при этом, с количеством, наблюдаемым в начале теста. Полученные результаты показаны на фиг. 1b.
Некоторые характеристики субстрата: Гаманаза, иммобилизованная на Дюолите S- 761:
Температура, oC - 30
Высота слоя, мм - 19
Объм слоя, мл - 2,15
Белки, мг/г субстрата - 37,2
Пример 2
Бета-маннаназу иммобилизовали ковалентным связыванием на шариках из диоксида кремния марки Х-030 LS (фирма Сепракор, Франция) диаметром 0,1-0,3 мм и размером пор порядка 60 нм, поступая следующим образом.
Шарики из диоксида кремния предварительно обрабатывали гамма-аминопропилтриэтоксисиланом, для чего использования способ силанизации в водной среде, описанной Уитоллом (H. H.Weetall Methods in Enz., 44, 135-148, 1976). Шарики из диоксида кремния в количестве 5 г, обработанные 50 мл 2,5%-ного глутаральдегидного раствора в 0,1 М буферном растворе фосфата натрия с pH 7, подвергали воздействию в течение 1 ч вакуума, а затем в течение 2 ч атмосферного давления. Частицы затем последовательно промывали дистиллированной водой, раствором из 0,5 М NaCl и 0,1 М буферного раствора фосфата натрия с величиной pH 6. К активированному субстрату затем добавляли 25 мл раствора, содержащего 5 мл Гаманазы и 20 мл буферного раствора фосфата натрия с величиной pH 6, затем оставляли взаимодействовать при 4oC в течение 12 ч в среде гелия. Шарики, наконец, обильно промывали дистиллированной водой, затем 0,1 М буферным раствором фосфата натрия с pH 6.
Этот препарат затем тестировали в реакторе с неподвижным слоем, делая это так, как и в случае примера 1. Тем самым определяли выраженную в процентах глубину протекания гидролиза галактоманнанов в функции от времени пребывания субстрата в реакторе (фиг. 2a), а также относительную активность фермента в функции от времени (фиг. 2b).
Некоторые характеристики использованного субстрата: Гаманаза, иммобилизованная на шариках из диоксида кремния:
Температура, oC - 30
Высота слоя, мм - 20
Объем слоя, мм - 2,26
Белки, мг/г субстрата - 34,4
Пример 3
Бета-маннаназу иммобилизовали ковалентным связыванием на шариках из акрилового полимера Ойпергит (фирма Рем, Германия) с размером пор порядка 35 нм, содержащего реакционноспособные эпоксидные группы, для чего поступали следующим образом.
Раствор в количестве 37,5 мл, состоящий из 7,5 мл Гаманазы и 30 мл 0,5 М буферного раствора фосфата калия с pH 7, добавляли к 5 г Ойпергита-С и оставляли взаимодействовать при осторожном перемешивании в течение 48 ч при температуре окружающей среды. Препарат затем промывали 0,5 М буферным раствором фосфата калия с pH 7.
Этот препарат затем тестировали в реакторе с неподвижным слоем, поступая так же, как это описано в примере 1. Тем самым обеспечивалась возможность определения выражаемой в процентах глубины протекания гидролиза галактоманнанов в функции от времени пребывания субстрата в реакторе (фиг. 3a), а также относительной активности фермента в функции от времени (фиг. 3b). Можно видеть, что на этом субстрате стабильность фермента является особенно хорошей, поскольку иммобилизованная бета-маннаназа сохраняет более 80% своей ферментативной активности по истечении 16 ч непрерывного протекания гидролиза.
Можно также видеть, что со временем не происходит высаливание фермента из субстрата в элюат. Отсутствуют изменения при инкубировании элюата в течение нескольких часов при 30oC, если судить по результатам измерения содержания восстанавливающих сахаров.
Некоторые характеристики использованного носителя: Гаманаза, иммобилизованная на Ойпергите-С:
Температура, oC - 30
Высота слоя, мм - 24
Объем слоя, мл - 2,74
Белки, мг/г субстрата - 31,4
Пример 4
Иммобилизацию проводили ковалентным связыванием на частицах обычного стекла (5 г) с проверенным размером пор, составляющим примерно 70 нм, которые также содержали аминопропильные группы (Сигма G5019), фиксированные тем же способом, что и использованный в случае шариков из диоксида кремния в примере 2.
Этот препарат затем тестировали в реакторе с неподвижным слоем, описанным в примере 1, в условиях использования обычного растворимого кофейного экстракта (зарегистрированная торговая марка Нескафе, фирма Нестле) при содержании 2% в дистиллированной воде.
Скорость течения кофейного экстракта изменяли и выходящий из реактора экстракт и анализировали проведением высокоэффективной тонкослойной хроматографии. Можно видеть, что при временах пребывания 64 и 81 с реакционные продукты в основном состоят из маннобиозы и маннотриозы. Проявляются при этом следы олигомеров, содержащих 4 и 5 манноз. При повышении времени пребывания до 105 с единственными олигосахаридами, присутствующими в экстракте, являются маннобиоза и маннотриоза, свидетельствуя о полном гидролизе галактоманнанов.
Некоторые характеристики использованного субстрата: Гаманаза, иммобилизованная на стекле с установленным размером пор:
Температура, oC - 30
Высота слоя, мм - 15
Объем слоя, мм - 1,69
Белки, мг/г субстрата - 32,2
Пример 5
Жидкий кофейный экстракт из полученной под давлением ступени в результате расщепительной экстракции молотого обжаренного кофе, приготовленного по способу, описанному в патенте EP 0538512, непрерывно подавали в реактор с неподвижным слоем, описанный в примере 1, который находился пи 50oC.
Реактор содержал Гаманазу, иммобилизованную на материале Ойпергит-С по способу, описанному в примере 3. Расход устанавливали таким, чтобы время пребывания составляло 8 мин. Пробы отбирали регулярно на протяжении 48 ч и по ним проведением высокоэффективной тонкослойной хроматографии оценивали олигосахариды.
Имел место полный гидролиз галактоманнанов экстракта, поскольку единственными олигосахаридами в обработанном экстракте были маннобиоза и маннотриоза.
Пример 6.
Несколько гидролизов кофейного экстракта, описанного в примере 5, провели в обычной вертикальной колонке, содержащей псевдоожиженный слой Гаманазы, иммобилизованной на материале Ойпергит-С.
Носитель содержал 28,6 мг белков на 1 г носителя, иммобилизованных так, как это описано в примере 3. Тесты проводили при 65oC.
Количество маннобиозы, присутствующей в элюате в каждом тесте, измеряли затем хроматографическим методом, поступая так, как это описано выше. Затем определяли выраженную в процентах глубину протекания гидролиза галактоманнанов в функции от стандартизованного времени пребывания экстракта в реакторе (отнесенное к миллилитрам произведение минут на миллиграммы белков). На фиг. 4 показаны результаты, полученные при проведении этих тестов.
Экспериментальные условия у различных тестов и полученные результаты приведены в таблице.
Пример 7
Примерно 500 последовательных гидролизов экстракта, описанного в примере 5, проводили в баке с перемешиванием, содержащем суспензию Гаманазы, иммобилизованной на материале Ойпергит-С.
Ферменты иммобилизовали добавлением 37,5 мл раствора, состоящего из 7,5 мл Гаманазы и 30 мл 1,25 М буферного раствора фосфата калия с pH 7, к 5 г материала Ойпергит-С. Смесь оставляли взаимодействовать при осторожном перемешивании в течение 72 ч при температуре окружающей среды.
Каждая операция гидролиза отвечала циклу в 30 мин, на протяжении которого насосом подавали экстракт в бак в течение первых двух минут, экстракт оставляли взаимодействовать при перемешивании в течение последующих 26 мин и насосом отсасывали гидролизованный экстракт из основания бака в течение остальных двух минут. Иммобилизованные ферменты удерживались фильтром (40 мкм), помещенным на основание бака, бак был термостатирован при температуре, находящейся в области до 60oC; и часть каждого элюата анализировали хроматографическим методом с проведением высокоэффективной тонкослойной хроматографии, что делали так, как это описано выше. Затем измеряли плотности окрашивания, отвечающие маннобиозе и маннотриозе.
На фиг. 5 изображены относительные количества маннобиозы и маннотриозы, продуцированные в функции от числа циклов гидролиза. Можно видеть, что фермент теряет свою ферментативную активность особенно медленно, поскольку иммобилизованная бета-маннаназа удерживает более 60% своей ферментативной активности после проведения 500 последовательных циклов гидролиза кофейного экстракта.
Экспериментальные условия: Гаманаза, иммобилизованная на Ойпергите-С; последовательный гидролиз в баке с перемешиванием:
Температура, oC - 60
Обработанный объем, мл - 38
Продолжительность цикла, мин - 30
Белки, мг/г подложки - 47,3
Мокрый иммобилизованный фермент, мг - 400

Способ проведения гидролиза галактоманнанов жидкого кофейного экстракта предусматривает гидролиз при 20-80°С с использованием иммобилизованных бета-маннаназ. Иммобилизованные бета-моннаназы ковалентно связаны с носителем или адсорбированы на нем с последующей полимеризацией и сохраняют ферментативную активность после 20 ч непрерывного гидролиза. Жидкий кофейный экстракт получают под давлением в результате расщепительной экстракции молотого кофе. Процесс гидролиза ведут непрерывно в реакторе с неподвижным или псевдоожиженным слоем иммобилизованных бета-маннаназ или периодически с суспензией бета-маннаназ. Способ является более экономичным. 11 з.п. ф-лы, 5 ил., 1 табл.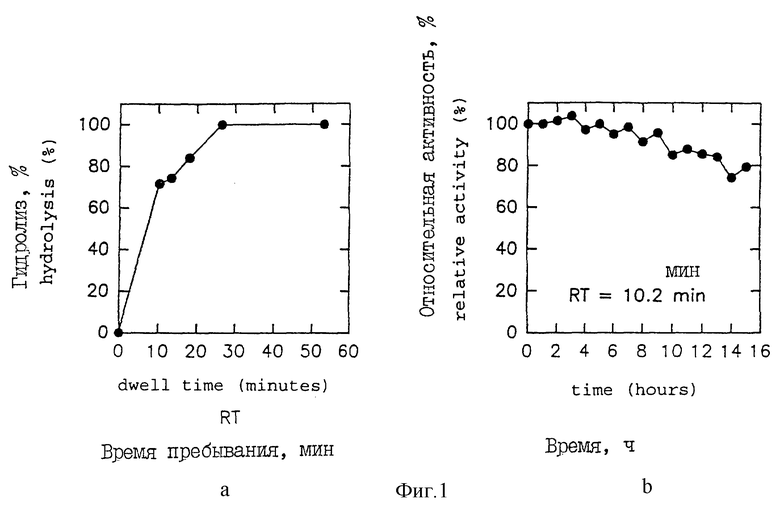
| Food Roview | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| Дифференциальный сверхпроводящий детектор | 2022 |
|
RU2801920C1 |
Авторы
Даты
2000-10-10—Публикация
1995-04-05—Подача