Настоящее изобретение относится к новым фармацевтическим препаратам для перорального приема, предназначенным для профилактики и лечения нарушений желудочно-кишечного тракта, связанных с приемом средств нестероидной противовоспалительной терапии - СНПТ (NSAID). Препараты по настоящему изобретению содержат кислоточувствительный ингибитор протонного насоса в сочетании с одним или несколькими средствами нестероидной противовоспалительной терапии в виде новой дозированной лекарственной формы, в частности таблетированной лекарственной формы.
Предпосылки изобретения
Средства нестероидной противовоспалительной терапии (СНПТ), в частности ацетилсалициловая кислота, являются наиболее часто прописываемыми и принимаемыми лекарственными препаратами в мире. Несмотря на лечебные достоинства СНПТ, их применение часто приходится ограничивать из-за большой вероятности возникновения побочных эффектов, главным образом, нарушений в верхнем отделе желудочно- кишечного тракта, таких как пептические язвы и расстройство пищеварения.
Вероятность образования язвы желудка во время лечения СНПТ увеличилась в 40-50 раз, а вероятность образования язвы двенадцатиперстной кишки увеличилась в 8-10 раз (McCarty DM. Gastroenterology 1989; 96:662). Вероятность возникновения осложнений, вызванных язвой, таких как кровотечение и перфорация язвы желудка, увеличилась в 1,5-5 раз (Hawkey C. BMJ 1990; 300:278). Кроме того, симптомы расстройства пищеварения наблюдаются у 30-60% субъектов, проходящих курс лечения СНПТ (Larkai EN. AmJGas 1987; 82:1153).
По свидетельству службы здравоохранения, в Великобритании на СНПТ приходится 25% случаев вредных реакций, вызываемых лекарственными средствами, а в США этот показатель равен 21%. Поэтому необходимы методы лечения, позволяющие избежать побочных эффектов, возникающих в желудочно-кишечном тракте под действием СНПТ.
Попытки изменить структуру СНПТ с тем, чтобы устранить такие побочные эффекты, все еще остаются безуспешными. Наиболее эффективным решением проблемы лечения и профилактики заболеваний верхнего отдела желудочно-кишечного тракта, вызываемых СНПТ, таких как язвы и расстройство пищеварения у субъектов, нуждающихся в постоянном лечении СНПТ, является прием СНПТ в сочетании с проти- воязвенными лекарственными средствами, рекомендованными для лечения и/или профилактики побочных эффектов, вызываемых СНПТ в желудочно-кишечном тракте, таким как аналоги простагландина, антагонисты H2-рецепторов или ингибиторы протонного насоса.
Факторами риска, способствующими возникновению побочных эффектов в верхнем отделе желудочно-кишечного тракта под действием СНПТ, являются, например, преклонный возраст, имевшаяся раньше пептическая язва и/или кровотечение, высокие дозы СНПТ, одновременное лечение стероидами и антикоагулянтами. Это значит, например, что ослабленные и престарелые субъекты, страдающие таким серьезным осложнением, как кровотечение или перфорация, должны пройти профилактический курс лечения в связи с приемом СНПТ.
Средства нестероидной противовоспалительной терапии используют главным образом для лечения хронических заболеваний, таких как ревматоидный артрит и остеоартрит, которыми чаще всего страдают старые люди. Подобный режим лечения особенно важен для престарелых и ослабленных субъектов, у которых особенно велика вероятность возникновения опасных для жизни осложнений, связанных с лечением СНПТ, таких как кровотечение или перфорация. Известно, что 50% всех смертей от пептической язвы приходится на субъекты, принимающие СНПТ, и 68% этих субъектов являются людьми старше 75 лет (Catford: Health Trends 1986; 18:38). Это подтверждено другим исследованием, которое позволяет сделать вывод о том, что СНПТ вызывает прежде всего смерть людей старше 75 лет (Guess. J Clin Epidemiol 1988; 41:35). Важность подобного режима лечения далее подтверждается открытием того, что у большинства пептических язв, вызываемых приемом СНПТ, отсутствуют какие-либо симптомы до самого момента их возникновения.
Установлено, что омепразол, являющийся известным ингибитором протонного насоса, способен предотвратить эрозию желудка и двенадцатиперстной кишки у здоровых добровольцев во время лечения ацетилсалициловой кислотой. Клинические исследования показали, что омепразол позволяет излечивать язвы желудка и двенадцатиперстной кишки как у субъектов, постоянно принимающих СНПТ, так и у субъектов, не принимающих этот препарат (Walan A. N Engl J Med 1989; 320: 69). Эти результаты стали основой для пересмотра рекомендаций относительно прописываемых доз омепразола для лечения язв желудка и двенадцатиперстной кишки во время приема СНПТ, одобренных службами здравоохранения в Великобритании и Швеции.
Недавно проведенные исследования подтверждают, что омепразол значительно снижает вероятность образования язв желудка, язв двенадцатиперстной кишки, а также расстройства пищеварения у субъектов, постоянно принимающих СНПТ.
В европейском патенте N 0426479 описываются таблетированные композиции, содержащие СНПТ, такой как ибупрофен, и средство, ингибирующее образование кислоты в желудке, такое как циметидин и т.д. В этих композициях не предусмотрена защита активного вещества, если ингибитором кислоты в желудке является кислоточувствительное соединение, такое как ингибитор протонного насоса.
В предлагаемых схемах лечения с использованием СНПТ и кислоточувствительного ингибитора протонного насоса разные активные вещества вводят отдельно. Хорошо известно, что соблюдение больным режима и схемы лечения является основным фактором достижения хорошего результата в процессе консервативного лечения. Поэтому прием двух или большего количества разных таблеток создает определенные неудобства для нуждающегося субъекта и не позволяет получить наиболее оптимальные результаты. Настоящим изобретением предусматриваются новые лекарственные препараты для перорального приема, содержащие два или больше разных активных веществ в виде одной дозированной лекарственной формы, предпочтительно таблетки.
Некоторые противоязвенные препараты, такие как ингибиторы протонного насоса, подвержены разрушению и трансформации в кислых и нейтральных средах, как указывалось выше. С точки зрения стабильности очевидно, что одно из активных веществ, которым является ингибитор протонного насоса, должно быть защищено от соприкосновения с кислым желудочным соком при помощи энтеросолюбильного покрытия. Описаны разные препараты с энтеросолюбильным покрытием, содержащие ингибиторы протонного насоса (см., например, заявку на патент США N 4786505 (AB Hassle)).
Сложно получить дозированную лекарственную форму, содержащую достаточно большое количество активного вещества. Объединение в одном препарате активных веществ с разными физическими свойствами создает дополнительные проблемы. При изготовлении лекарственных форм в виде таблеток со сложной структурой особые проблемы возникают тогда, когда гранулы с энтеросолюбильным покрытием, содержащие кислоточувствительный ингибитор протонного насоса, прессуют в таблетки. Если энтеросолюбильное покрытие не выдерживает давления, создаваемого в процессе прессования гранул в таблетки, то чувствительное активное вещество разрушается в результате соприкосновения с кислым желудочным соком, то есть кислотостойкость энтеросолюбильного слоя гранул оказывается недостаточной после прессования таблетки.
Краткое изложение существа изобретения
Настоящее изобретение относится к дозированным лекарственным формам для перорального приема, т.е. к таблетированным лекарственным формам со сложной структурой, таблеткам с энтеросолюбильным покрытием, многослойным таблеткам или капсулам, заполненным несколькими фармацевтически активными веществами. Активными соединениями предпочтительно являются кислоточувствительный ингибитор протонного насоса и одно или несколько средств нестероидной противовоспалительной терапии, при этом, по крайней мере, ингибитор протонного насоса защищен энтеросолюбильным покрытием. Эти новые лекарственные формы упрощают схему лекарственного лечения и облегчают соблюдение больным режима и схемы лечения.
Описание фигур
Фиг. 1 изображает поперечное сечение таблетированной лекарственной формы со сложной структурой, содержащей кислоточувствительный ингибитор протонного насоса в виде гранул (1) с энтеросолюбильным покрытием в смеси с быстро распадающимся гранулированным веществом, содержащим СНПТ (2). На таблетку нанесено пленочное покрытие (13).
Фиг. 2 - поперечное сечение таблетированной лекарственной формы со сложной структурой, содержащей кислоточувствительный ингибитор протонного насоса в виде гранул (1) с энтеросолюбильным покрытием и СНПТ в виде циклодекстринового комплекса (3) в быстро распадающемся гранулированном веществе (4). На таблетку нанесено пленочное покрытие (13).
Фиг. 3 - поперечное сечение таблетки с двумя разными слоями, из которых один слой содержит кислоточувствительный ингибитор протонного насоса в виде гранул (1) с энтеросолюбильным покрытием в смеси с эксципиентами (5), а другой слой содержит СНПТ (6) в гелеобразующей матрице с пролонгированным действием. Разные слои отделены друг от друга разделительным слоем (12), и на таблетку нанесено пленочное покрытие (13).
Фиг. 4 - поперечное сечение таблетированной лекарственной формы со сложной структурой, содержащей кислоточувствительный ингибитор протонного насоса в виде гранул (1)с энтеросолюбильным покрытием и СНПТ в виде гранул (7) с энтеросолюбильным покрытием в смеси с эксципиентами (5). На таблетку нанесено пленочное покрытие (13).
Фиг. 5 - поперечное сечение таблетки с энтеросолюбильным покрытием, содержащей кислоточувствительный ингибитор (8) протонного насоса в смеси с одним или несколькими СНПТ (9) и эксципиентами (5). На таблетку нанесено энтеросолюбильное покрытие (11), а между сердцевиной таблетки и энтеросолюбильным слоем расположен разделительный слой (10).
Фиг. 6 - таблетку, сердцевина которой состоит из кислоточувствительного ингибитора протонного насоса в виде гранул (1) с энтеросолюбильным покрытием в смеси с быстро распадающимся гранулированным веществом (4) и покрыта слоем СНПТ и гранулированного вещества (2). На таблетку нанесено пигментированное пленочное покрытие (13).
Подробное описание изобретения
Целью данного изобретения является создание таблетированной лекарственной формы со сложной структурой для перорального приема, содержащей противоязвенное средство, предпочтительно кислоточувствительный ингибитор протонного насоса в виде отдельных структурных единиц с энтеросолюбильным покрытием, спрессованное в таблетку с одним или несколькими СНПТ и эксципиентами. Энтеросолюбильное покрытие, защищающее отдельные структурные единицы кислоточувствительного ингибитора протонного насоса, обладает такими свойствами, что прессование указанных структурных единиц в таблетку не оказывает существенного влияния на кислотостойкость отдельных структурных единиц с энтеросолюбильным покрытием. Кроме того, таблетированная лекарственная форма со сложной структурой обеспечивает хорошую стабильность активных веществ во время длительного хранения.
Альтернативно полученная таблетка состоит из разных слоев, из которых один слой содержит кислоточувствительный ингибитор протонного насоса в виде спрессованных структурных единиц с энтеросолюбильным покрытием, а другой слой содержит одно или несколько СНПТ.
Новая дозированная лекарственная форма предпочтительно представляет собой таблетированную лекарственную форму со сложной структурой, содержащую структурные единицы кислоточувствительного вещества с энтеросолюбильным покрытием и другое гранулированное активное вещество (или несколько активных веществ), образующее остальную часть прессованной таблетка, как показано на фиг. 1.
Альтернативно разные активные вещества могут быть смешаны друг с другом и спрессованы в обычную таблетку с энтеросолюбильным покрытием, см. фиг. 5, либо оба активные вещества имеют форму гранул с энтеросолюбильным покрытием, спрессованных в таблетированную форму со сложной структурой вместе с предпочтительно быстро распадающимися гранулами инертных эксципиентов, как показано на фиг. 4.
Другими возможными вариантами являются описанные в примерах лекарственные формы со сложной структурой, которые содержат ингибитор протонного насоса в виде отдельных структурных единиц с энтеросолюбильным покрытием и СНПТ в виде а) комплекса с целью достижения лучшей биологической доступности, см. фиг. 2, или b) гелеобразующей матрицы, позволяющей получить препарат с пролонгированным высвобождением СНПТ, см. фиг. 3. Другим вариантом является лекарственная форма со сложной структурой, содержащая ингибитор протонного насоса в виде отдельных структурных единиц с энтеросолюбильным покрытием, спрессованных в таблетку, на которую нанесен распылением отдельный слой СНПТ. Эту таблетку покрывают пигментированным пленочным покрытием для защиты СНПТ, см. фиг. 6, так как некоторые СНПТ являются светочувствительными и требуют нанесения светозащитного покрытия.
В соответствии с другим вариантом разные активные вещества смешивают в сухом состоянии и заполняют ими капсулу. В последнем препарате кислоточувствительный ингибитор протонного насоса имеет форму структурных единиц с энтеросолюбильным покрытием, а СНПТ имеет форму гранул или альтернативно форму структурных единиц с измененным режимом высвобождения, таких как структурные единицы с энтеросолюбильным покрытием или структурные единицы с покрытием, обеспечивающим регулируемое высвобождение.
СНПТ можно получить в виде препаратов с немедленным действием, отсроченным или пролонгированным действием. Альтернативно из составляющих компонентов может быть получен растворимый шипучий препарат. Кроме того, поскольку некоторые СНПТ являются светочувствительными веществами, препарат предпочтительно защищают пигментированным пленочным покрытием, как показано на фиг. 6, или посредством включения пигмента в одно из покрытий, наносимых на таблетированную лекарственную форму.
Другой целью данного изобретения является создание делимой лекарственной формы, такой как делимые таблетки.
Еще одной целью данного изобретения является создание таблетированной лекарственной формы со сложной структурой, которая является делимой и простой в обращении. Некоторые таблетированные лекарственные формы со сложной структурой можно диспергировать в слегка кислой водной жидкости и давать субъектам с нарушениями глотания и маленьким детям. Такую суспензию диспергированных структурных единиц гранул соответствующего размера можно использовать для перорального введения, а также для кормления через назогастральный зонд.
Ниже описываются другие активные компоненты, используемые в лекарственных формах по настоящему изобретению.
Активные вещества
Противоязвенным средством предпочтительно является кислоточувствительный ингибитор протонного насоса. Такими ингибиторами протонного насоса являются, например, соединения общей формулы I: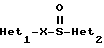
в которой
Het1 обозначает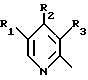 или
или 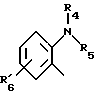
Het2 обозначает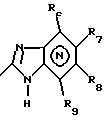 или
или 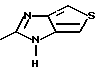 или
или 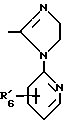
X=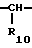 или
или 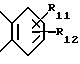
где N в бензимидазольной части означает, что один из атомов углерода, замещенных R6-R9, необязательно можно заменить атомом азота без каких-либо заместителей;
R1, R2 и R3 имеют одинаковые или разные значения, и их выбирают из группы, включающей водород, алкил, алкокси, необязательно замещенный фтором, алкилтио, алкоксиалкокси, диалкиламино, пиперидино, морфолино, галоген, фенил и фенилалкокси;
R4 и R5 имеют одинаковые или разные значения, и их выбирают из водорода, алкила и аралкила;
R'6 является водородом, галогеном, трифторметилом, алкилом и алкокси;
R6-R9 имеют одинаковые или разные значения, их выбирают из группы, включающей водород, алкил, алкокси, галоген, галогеналкокси, алкилкарбонил, алкоксикарбонил, оксазолил, трифторалкил, либо смежные группы R6-R9 образуют кольцевые структуры, которые могут быть далее замещены;
R10 является водородом или образует алкиленовую цепь вместе с R3; и
R11 и R12 имеют одинаковые или разные значения, и их выбирают из группы, включающей водород, галоген или алкил, алкильные группы, алкоксильные группы и их части, они могут быть разветвленными или прямыми C1-C9 цепями либо могут обозначать циклические алкильные группы, такие как циклоалкилалкил.
Примерами ингибиторов протонного насоса формулы I являются: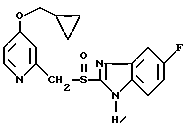
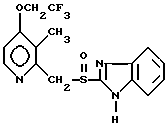 Ланзопразол
Ланзопразол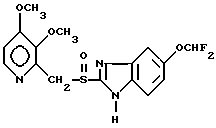 Пантопразол
Пантопразол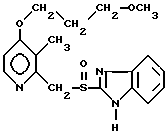 Парипразол
Парипразол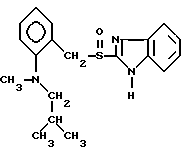 Леминопразол
Леминопразол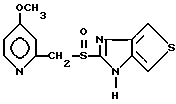
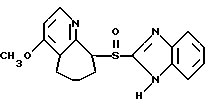
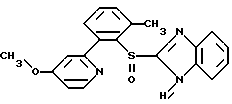
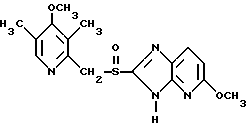
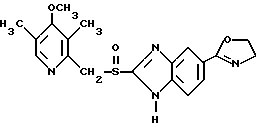
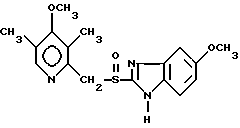 Омепразол
Омепразол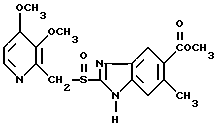
Кислоточувствительные ингибиторы протонного насоса, входящие в состав лекарственных форм по данному изобретению, можно использовать в нейтральной форме или в форме соли щелочного металла, такой как, например, соли Mg2+, Ca2+, Na+, К+ или Li+, предпочтительно соли Mg2+. Кроме того, приведенные выше соединения можно использовать, при желании, в виде рацемической смеси, в виде чистого энантионера или солей щелочных металлов отдельных энантиомеров.
Пригодные ингибиторы протонного насоса рассматриваются, например, в заявках на европейский патент EP-A1-0005129, EP-A1-174726, EP-A1-166287, в заявке Великобритании N 2163747 и заявках WO 90/06925, WO 91/19711, WO 91/19712, а другие особенно пригодные соединения описываются в заявках WO 95/01977 и WO 94/27988.
В дозированных лекарственных формах по настоящему изобретению можно использовать целый ряд СНПТ в сочетании с пригодным ингибитором протонного насоса и необязательно с фармацевтически приемлемыми эксципиентами. Такие СНПТ включают, например, производные пропионовой кислоты, оксикамы, производные уксусной кислоты и ацетамида, производные салициловой кислоты и производные пиразолидина.
Кроме того, препарат по настоящему изобретению может содержать другие средства нестероидной противовоспалительной терапии, например, СНПТ, избирательные в отношении циклооксигеназы 2 и NO-высвобождающие СНПТ (de Soldato P, NO-releasing NSAD:s, A new class of safer antiinflammatory analgesic and anti-pyrretic agents; The IV International meeting on side-effects of antiifinflammatory drugs 7-9, 1995).
В следующих примерах приведены некоторые пригодные СНПТ: ацетилсалициловая кислота, индометацин, диклофенак, пироксикам, теноксикам, ибупрофен, напроксен, кетопрофен, набуметон, кеторолак, азапропазон, мефенамовая кислота, толфенамовая кислота, сулиндак, дифлунизал, тиапрофеновая кислота, производные подофиллотоксина, ацеметацин, ацеклофенак, дроксикам, оксапрозин, флоктафенин, фенилбутазон, проглуметацин, флурбипрофен, толметин и фенбуфен.
Активные СНПТ можно использовать в стандартной форме или в виде солей, гидратов, сложных эфиров и т.д. Можно использовать комбинацию из двух или большего количества вышеуказанных лекарственных средств. Предпочтительными СНПТ для новой дозированной лекарственной формы являются диклофенак, ибупрофен, напроксен и пироксикам.
Предпочтительную таблетированную лекарственную форму со сложной структурой, содержащую ингибитор протонного насоса (в виде рацемата, соли щелочного металла или одного из его отдельных энантиомеров) и один или несколько СНПТ, можно охарактеризовать следующим образом. Отдельные структурные единицы с энтеросолюбильным покрытием (маленькие шарики, гранулы или пилюли), содержащие ингибитор протонного насоса и необязательно щелочной реагент, смешивают с СНПТ и обычными эксципиентами для таблеток. СНПТ и эксципиенты для таблеток предпочтительно имеют форму гранулированного вещества. Сухую смесь, состоящую из структурных единиц с энтеросолюбильным покрытием, гранул СНПТ и необязательно эксципиентов, прессуют с получением таблетированных лекарственных форм со сложной структурой. Выражение "отдельные структурные единицы" означает маленькие шарики, гранулы или пилюли, которые далее определяются как гранулы кислоточувствительного ингибитора протонного насоса.
Процесс прессования (уплотнения) с целью получения таблетированной лекарственной формы со сложной структурой не должен существенно влиять на кислотостойкость гранул с энтеросолюбильным покрытием, содержащих кислоточувствительный ингибитор протонного насоса. Другими словами, механические свойства, как пластичность и твердость, а также толщина энтеросолюбильного покрытия должны отвечать требованиям, предъявляемым фармакоцеей США к изделиям с энтеросолюбильным покрытием, в соответствии с которыми кислотостойкость не должна уменьшаться более чем на 10% во время прессования гранул в таблетки.
Кислотостойкость определяется количеством ингибитора протонного насоса в таблетках или гранулах после воздействия на них искусственным желудочным соком по определению фармакопеи США или 0,1 М раствором HCl (водный раствор) по сравнению соответственно с не подвергнутыми воздействию таблетками и гранулами. Испытание выполняют следующим образом. Отдельные таблетки или гранулы погружают в искусственный желудочный сок при температуре 37oC. Таблетки быстро распадаются и высвобождают гранулы с энтеросолюбильным покрытием в эту среду. Через два часа гранулы с энтеросолюбильным покрытием удаляют и анализируют на содержание ингибитора протонного насоса при помощи жидкостной хроматографии высокого разрешения.
Далее описываются другие характерные компоненты, используемые в дозированных лекарственных формах по настоящему изобретению.
Вещество сердцевины - для гранул и структурных единиц с энтеросолюбильным покрытием
Вещество сердцевины для отдельных гранул с энтеросолюбильным покрытием можно получить различными способами. В качестве вещества сердцевины, подвергаемого дальнейшей обработке, можно использовать затравочные кристаллы, на которые нанесен ингибитор протонного насоса необязательно в смеси со щелочными веществами.
Затравочные кристаллы, на которые наносят ингибитор протонного насоса, могут быть не растворимыми в воде кристаллами, представляющими собой разные оксиды, целлюлозы, органические полимеры и другие материалы, используемые отдельно или в виде смесей, либо они могут быть водорастворимыми кристаллами, представляющими собой разные неорганические соли, сахара, совершенные кристаллы и другие материалы, используемые отдельно или в виде смесей. Кроме того, затравочные кристаллы могут содержать ингибитор протонного насоса в виде кристаллов, агломератов, спрессованных веществ и т.д. Размер указанных кристаллов не имеет существенного значения для настоящего изобретения и может изменяться от примерно 0,1 до 2 мм. Кристаллы, покрытые ингибитором протонного насоса, получают путем нанесения покрытия из порошка или раствора/суспензии, например, при помощи оборудования для нанесения покрытия распылением.
Прежде чем нанести ингибитор протонного насоса на кристаллы, его, при желании, смешивают с другими компонентами. Такими компонентами могут быть связующие вещества, поверхностно-активные вещества, наполнители, дезинтеграторы, щелочные добавки или тому подобные и/или фармацевтически приемлемые ингредиенты, используемые отдельно или в виде смесей. Связующими веществами являются, например, такие полимеры, как гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидон или сахара, крахмалы или другие фармацевтически приемлемые вещества, обладающие когезионными свойствами. Пригодными поверхностно-активными веществами являются фармацевтически приемлемые неионные или ионные поверхностно-активные вещества, такие как, например, лаурилсульфат натрия.
Альтернативно вещество сердцевины можно получить из ингибитора протонного насоса, смешанного со щелочными веществами, а затем с приемлемыми компонентами. Указанное вещество сердцевины можно получить путем экструзии и сферообразования, комкования или прессования при помощи известного технологического оборудования. Вещество сердцевины получают в размере от около 0,1 до 4 мм, предпочтительно от 0,1 до 2 мм. На полученное вещество сердцевины можно далее нанести дополнительные ингредиенты, содержащие ингибитор протонного насоса, и/или использовать для дальнейшей обработки.
Ингибитор протонного насоса смешивают с фармацевтическими компонентами, чтобы получить необходимые для обращения и обработки свойства и требуемую концентрацию вещества в конечном препарате. Можно использовать такие фармацевтические компоненты, как наполнители, связующие вещества, смазки, дезинтеграторы, поверхностно-активные вещества и другие фармацевтически приемлемые добавки.
Кроме того, ингибитор протонного насоса может быть смешан со щелочным фармацевтически приемлемым веществом (или веществами). Такими веществами являются, но не ограничиваются ими, натриевые, калиевые, кальциевые, магниевые и алюминиевые соли фосфорной кислоты, угольной кислоты, лимонной кислоты или других приемлемых слабых неорганических или органических кислот; копреципитат гидроксида алюминия и бикарбоната натрия; вещества, обычно используемые в антацидных препаратах, такие как гидроксиды алюминия, кальция и магния; оксид магния и композиционные вещества, такие как Al2O3 • 6MgO • CO2 • 12H2O, (Mg6Al2(OH)16 CO3 • 4H2O), MgO • Al2O3 • 2SiO2 • nH2O или аналогичные соединения; органические pH-буферные вещества, такие как тригидроксиметиламинометан, основные аминокислоты и их соли или другие подобные фармацевтически приемлемые pH-буферные вещества.
Альтернативно вышеуказанное вещество сердцевины можно получить методом сушки или замораживания распылением.
Энтеросолюбильное покрытие
Прежде чем нанести энтеросолюбильное покрытие на вещество сердцевины в виде отдельных гранул, эти гранулы можно покрыть одним или несколькими разделительными слоями, состоящими из фармацевтических эксципиентов, необязательно содержащих щелочные соединения, такие как pH-буферные соединения. Такой разделительный слой отделяет вещество сердцевины от наружных слоев, представляющих собой энтеросолюбильные покрытия. Разделительный слой, защищающий вещество сердцевины из ингибитора протонного насоса, должен быть водорастворимым или быстро распадающимся в воде.
Один или несколько разделительных слоев можно нанести на вещество сердцевины при помощи методов нанесения покрытий или пленок с применением соответствующего оборудования, такого как устройство для нанесения покрытий, гранулятор для нанесения покрытий или аппарат с псевдоожиженным слоем, в котором для нанесения покрытий используют воду и/или органические растворители. В качестве возможного варианта один или несколько разделительных слоев можно нанести на вещество сердцевины при помощи метода нанесения покрытия из порошкового материала. Для разделительных слоев используют фармацевтически приемлемые соединения, такие как, например, сахар, полиэтиленгликоль, поливинилпирролидон, поливиниловый спирт, поливинилацетат, гидроксипропилцеллюлоза, метилцеллюлоза, этилцеллюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза, водорастворимые соли полимеров для энтеросолюбильных покрытий и тому подобные, применяемые отдельно или в виде смесей. В разделительный слой могут быть включены такие добавки, как пластификаторы, красители, пигменты, наполнители, вещества, препятствующие слипанию, и антистатики, такие как, например, стеарат магния, диоксид титана, тальк и другие добавки.
Необязательный разделительный слой, наносимый на вещество сердцевины, может иметь различную толщину. Максимальная толщина разделительного слоя обычно ограничивается лишь условиями технологического процесса. Разделительный слой может служить в качестве барьера диффузии и быть pH-буферной зоной. pH-Буферные свойства разделительного слоя можно далее усилить введением в него веществ, выбираемых из группы соединений, обычно используемых в антацидных препаратах, таких как, например, оксид, гидроксид или карбонат магния, гидроксид, карбонат или силикат алюминия или кальция; композиционные соединения алюминия и магния, такие как, например, Al2O3 • 6MgO • CO2 • 12H2O, (Mg6Al2 (OH)16CO3 • 4H2O), Mg•Al2O3 • 2SiO2•nH2O, копреципитат гидроксида алюминия и бикарбоната натрия или подобные соединения; либо другие фармацевтически приемлемые pH-буферные соединения, такие как, например, натриевые, калиевые, кальциевые, магниевые и алюминиевые соли фосфорной, угольной, лимонной кислот или других приемлемых слабых неорганических или органических кислот; или приемлемые органические основания, в том числе основные аминокислоты и их соли. Можно добавить тальк или другие соединения, чтобы увеличить толщину слоя и, таким образом, сделать более прочным барьер диффузии. Необязательный разделительный слой не имеет существенного значения для данного изобретения. Однако разделительный слой может улучшить химическую стабильность активного вещества и/или физические свойства новой таблетированной лекарственной формы со сложной структурой.
Альтернативно разделительный слой можно получить на месте в результате взаимодействия энтеросолюбильного полимерного покрытия, нанесенного на вещество сердцевины, со щелочным реагентом в веществе сердцевины. Полученный таким образом разделительный слой представляет собой водорастворимую соль, образовавшуюся в результате взаимодействия полимеpa, входящего в состав энтеросолюбильного покрытия, со щелочным реагентом, находящимся в месте образования соли.
На вещество сердцевины или на вещество сердцевины с разделительным слоем наносят одно или несколько энтеросолюбильных покрытий при помощи пригодного метода нанесения покрытия. Вещество энтеросолюбильного покрытия может быть диспергировано или растворено в воде или в приемлемых органических растворителях. В качестве одного или нескольких полимеров для энтеросолюбильного покрытия, применяемых отдельно или в сочетании, можно использовать следующие вещества, например, растворы или дисперсии сополимеров метакриловых кислот, ацетофталата целлюлозы, фталата гидроксипропилметилцеллюлозы, ацетосукцината гидроксипропилметилцеллюлозы, фталата поливинилацетата, ацетотримеллитата целлюлозы, карбоксиметилэтилцеллюлозы, шеллака и других приемлемых полимеров для энтеросолюбильного покрытия.
Энтеросолюбильные покрытия могут содержать фармацевтически приемлемые пластификаторы, используемые для получения требуемых механических свойств, таких как пластичность и твердость энтеросолюбильных покрытий. Такими пластификаторами являются, но не ограничиваются ими, например, триацетин, сложные эфиры лимонной кислоты, сложные эфиры фталевой кислоты, дибутилсебацат, цетиловый спирт, полиэтиленгликоли, полисорбаты или другие пластификаторы.
Количество пластификатора должно быть оптимальным для каждой структурной формулы энтеросолюбильного покрытия в зависимости от выбранного полимера для энтеросолюбильного покрытия, выбранного пластификатора и используемого количества указанного полимера, с тем чтобы механические свойства, т.е. пластичность и твердость энтеросолюбильного покрытия, например, выраженные в виде твердости по Виккерсу, можно было отрегулировать с таким расчетом, чтобы кислотостойкость гранул с энтеросолюбильным покрытием существенно не ухудшалась во время прессования гранул в таблетки. Количество пластификатора обычно составляет более 10 вес. % от количества полимера для энтеросолюбильного покрытия, предпочтительно это количество равно 15-50% и более предпочтительно 20-50%. Энтеросолюбильное покрытие может также содержать такие добавки, как диспергаторы, красители, пигменты, полимеры, например, поли(этилакрилат, метилметакрилат), вещества, препятствующие слипанию, и противовспениватели. Для увеличения толщины пленки и уменьшения диффузии кислого желудочного сока в кислоточувствительное вещество могут быть добавлены другие соединения. Чтобы защитить кислоточувствительное вещество, в частности, ингибитор протонного насоса, и получить приемлемую кислотостойкость лекарственной формы по данному изобретению, толщина энтеросолюбильного покрытия должна быть равна, по крайней мере, около 10 мкм, предпочтительно более 20 мкм. Максимальная толщина нанесенного энтеросолюбильного покрытия обычно ограничивается лишь условиями технологического процесса и требуемым профилем растворения.
Энтеросолюбильное покрытие можно также использовать для нанесения слоя СНПТ. Альтернативно энтеросолюбильное покрытие, описанное выше, можно также использовать в качестве энтеросолюбильного покрытия для обычных таблеток, содержащих композицию из ингибитора протонного насоса и одного или нескольких СНПТ, причем сердцевина таблетки может быть также покрыта одним из вышеописанных разделительных слоев, который позволяет отделить сердцевину таблетки от энтеросолюбильного покрытия.
Защитное покрытие
На гранулы с энтеросолюбильным покрытием можно дополнительно нанести одно или несколько защитных покрытий. Защитное покрытие должно быть водорастворимым или быстро распадающимся в воде. Защитное покрытие может быть нанесено на гранулы с энтеросолюбильным покрытием при помощи методов нанесения покрытий или пленок на соответствующем оборудовании, таком как устройство для нанесения покрытий, гранулятор для нанесения покрытий или аппарат с псевдоожиженным слоем, в котором для нанесения покрытий или пленок используют воду и/или органические растворители. Вещества для защитных покрытий выбирают из фармацевтически приемлемых соединений, таких как, например, сахар, полиэтиленгликоль, поливинилпирролидон, поливиниловый спирт, поливинилацетат, гидроксипропилцеллюлоза, метилцеллюлоза, этилцеллюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза и другие, используемые отдельно или в виде смесей. Защитное покрытие может также содержать такие добавки, как пластификаторы, красители, пигменты, наполнители, вещества, препятствующие слипанию, антистатики, такие как, например, стеарат магния, диоксид титана, тальк и другие добавки. Указанное защитное покрытие может далее препятствовать возможной агломерации гранул с энтеросолюбильным покрытием, оно может защищать энтеросолюбильное покрытие от растрескивания во время прессования и улучшать процесс таблетирования. Максимальная толщина нанесенного защитного покрытия обычно ограничивается лишь условиями технологического процесса и требуемым профилем растворения. Защитное покрытие можно также использовать в качестве пленочного покрытия таблетки.
Получение средства нестероидной противовоспалительной терапии (СНПТ)
Активное вещество, представляющее собой одно или несколько средств нестероидной противовоспалительной терапии (СНПТ), смешивают в сухом состоянии с инертными эксципиентами, при этом один или несколько наполнителей возможно являются дезинтегратором. Полученную смесь смачивают гранулирующей жидкостью и перемешивают. Мокрую массу сушат предпочтительно до потери при сушке менее 3 вес.%.
После этого сухую массу измельчают с получением гранул требуемого размера, в частности, менее 4 мм и предпочтительно менее 1 мм. Приемлемыми инертными эксципиентами для гранулированного СНПТ являются, например, гликолят натриевого крахмала, кукурузный крахмал, сшитый поливинилпирролидон, низкомолекулярная замещенная гидроксипропилцеллюлоза, микрокристаллическая целлюлоза, маннит и безводный коллоидный диоксид кремния (Aerosil®) и тому подобные. Сухую смесь, содержащую СНПТ, смешивают с приемлемой гранулирующей жидкостью, которая может содержать, например, поливинилпирролидон, гидроксипропилцеллюлозу, полиэтиленгликоль, гидроксипропилцеллюлозу и необязательно смачивающие вещества, такие как лаурилсульфат натрия, растворенный в дистиллированной воде, приемлемом спирте или их смеси.
В некоторых случаях можно прибегнуть к механической обработке, чтобы получить комплекс между СНПТ и комплексным пенообразователем, таким как бета- гидроксипропилциклодекстрин, подобным тому, который описывается в приводимом ниже примере 3. Известно, что циклодекстриновые комплексы СНПТ увеличивают биологическую доступность СНПТ, см., например. Drug Dev. Ind. Pharm. 19(7), 843-852, (1993).
Кроме того, СНПТ может быть смешан во время грануляции с гелеобразователем, таким как гидрофильный полимер. Приемлемыми гелеобразующими гидрофильными полимерами являются, например, гидроксипропилметилцеллюлоза, полиоксиэтилен (полиэтиленгликоль), гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза и ксантан. Гранулы могут также содержать буферные вещества. См., например, приводимый ниже пример 4. Некоторые СНПТ вызывают раздражение слизистой оболочки желудка, поэтому на них лучше наносить защитное энтеросолюбильное покрытие и получать в виде гранул с энтеросолюбильным покрытием.
Таблетки со сложной структурой
Гранулы с энтеросолюбильным покрытием, содержащие ингибитор протонного насоса, смешивают с гранулами, содержащими СНПТ, и эксципиентами для таблеток. Из этой смеси прессуют таблетированную лекарственную форму со сложной структурой. На прессованную таблетку можно нанести пленочное покрытие, чтобы сделать поверхность таблетки гладкой и увеличить ее стабильность во время упаковки и транспортировки. Такое пленочное покрытие таблетки может далее содержать такие добавки, как вещества, препятствующие слипанию, красители и пигменты или другие добавки, придающие таблетке привлекательный внешний вид и защищающие от света светочувствительные компоненты.
Гранулы с энтеросолюбильным покрытием, имеющие защитное покрытие или без него, и гранулы СНПТ смешивают с такими эксципиентами для таблетки, как наполнители, связующие вещества, дезинтеграторы, смазки и другие фармацевтически приемлемые добавки, и прессуют в таблетки. Приемлемыми смазками в процессе таблетирования являются, например, стеарилфумарат натрия, стеарат магния и тальк.
Альтернативно СНПТ можно смешивать в сухом состоянии с гранулами с энтеросолюбильным покрытием, содержащими ингибитор протонного насоса, возможно вместе с инертными эксципиентами, и прессовать в таблетки (прямое прессование), либо из разных активных веществ можно сформировать отдельные слои, причем СНПТ может входить в состав слоя с регулируемым высвобождением.
Кроме того, как СНПТ, так и ингибитор протонного насоса в виде гранул с энтеросолюбильным покрытием можно смешивать с инертными эксципиентами и прессовать в таблетку. На прессованную таблетку можно нанести пленочное покрытие, чтобы придать ей привлекательный вид.
В качестве другого возможного варианта на таблетированную лекарственную форму со сложной структурой, содержащую ингибитор протонного насоса, можно нанести покрытие распылением из суспензии или раствора, содержащего СНПТ. На полученную таблетку затем наносят пигментированное пленочное покрытие.
Доля гранул с энтеросолюбильным покрытием составляет менее 75 вес.% от общей массы таблетки, предпочтительно менее 60%. Увеличивая в лекарственной форме со сложной структурой количество гранул, содержащих СНПТ, в ней можно уменьшить долю гранул с энтеросолюбильным покрытием, содержащих ингибитор протонного насоса. Выбирая для препарата по настоящему изобретению маленькие гранулы с энтеросолюбильным покрытием, можно увеличить количество гранул в каждой таблетке, что, в свою очередь, позволяет делить таблетку с сохранением точности дозирования.
Таким образом, предпочтительная таблетка со сложной структурой состоит из гранул с энтеросолюбильным покрытием, содержащих одно активное вещество в виде кислоточувствительного ингибитора протонного насоса, необязательно в смеси с одним или несколькими щелочными реагентами, которые спрессованы в таблетку вместе с гранулами, содержащими СНПТ, и необязательно эксципиентами для таблеток. К ингибитору протонного насоса необязательно добавлять щелочной реагент, но такое вещество может еще больше увеличить стабильность ингибитора протонного насоса, к тому же некоторые щелочные реагенты могут взаимодействовать на месте с веществом энтеросолюбильного покрытия, образуя разделительный слой. Энтеросолюбильное покрытие препятствует растворению гранул лекарственной формы в кислых средах, но позволяет им распадаться/растворяться в почти нейтральных и щелочных средах, таких как, например, жидкости, присутствующие в проксимальном отделе тонкой кишки, где желательно растворение ингибитора протонного насоса. СНПТ может высвобождаться в желудке. На гранулы с энтеросолюбильным покрытием может быть далее нанесено защитное покрытие, прежде чем они будут спрессованы в таблетку, при этом они могут иметь один или несколько разделительных слоев между веществом сердцевины и энтеросолюбильным покрытием.
Способ получения
Дополнительным объектом данного изобретения является способ получения лекарственной формы. После получения гранул методом распыления ингибитора протонного насоса на затравочные кристаллы либо путем экструзии и сферообразования или грануляции, например, путем ротационной грануляции однородных гранул, на эти гранулы сначала необязательно наносят разделительный слой, а затем энтеросолюбильное покрытие либо разделительный слой формируют на месте в результате взаимодействия между щелочным веществом сердцевины и веществом энтеросолюбильного покрытия. Покрытие наносят так, как описано выше, и в приводимых далее примерах. Способ получения гранул, содержащих СНПТ, и гранул СНПТ с энтеросолюбильным покрытием также описан выше и в примерах. Методы получения фармацевтических препаратов предпочтительно должны полностью осуществляться на водной основе.
Гранулы с энтеросолюбильным покрытием, имеющие защитное покрытие или без него, смешивают с предварительно полученными гранулами СНПТ, эксципиентами и другими фармацевтически приемлемыми добавками и прессуют в таблетки. Альтернативно разные активные вещества в виде порошков можно смешивать в сухом состоянии до однородного состояния с эксципиентами для таблеток, смачивать и прессовать в обычные таблетки до нанесения необязательного разделительного слоя и энтеросолюбильного покрытия. СНПТ можно также ввести в покрытие, наносимое на лекарственную форму со сложной структурой, содержащую ингибитор протонного насоса, либо СНПТ и ингибитор протонного насоса в виде гранул с энтеросолюбильным покрытием смешивают с инертными эксципиентами для таблеток и прессуют в таблетированную лекарственную форму со сложной структурой.
Из разных активных веществ можно также сформировать два отдельных слоя, из которых один слой, содержащий СНПТ, может быть препаратом с регулируемым высвобождением. В качестве другого возможного варианта кислоточувствительный ингибитор протонного насоса в виде гранул с энтеросолюбильным покрытием может быть введен в капсулу вместе с СНПТ в виде гранул или гранул с энтеросолюбильным покрытием, при желании в смеси с фармацевтическими эксципиентами.
Применение препарата
Лекарственные формы по данному изобретению особенно эффективны для лечения побочных эффектов, вызываемых СНПТ в желудочно-кишечном тракте, которые обычно возникают при постоянном приеме средств нестероидной противовоспалительной терапии. Новые лекарственные формы принимают один или несколько раз в день, предпочтительно один или два раза в день. Обычная суточная доза активных веществ может быть различной в зависимости от таких факторов, как индивидуальные потребности нуждающихся субъектов, режим приема и характер заболевания. Как правило, каждая лекарственная форма содержит 0,1- 200 мг ингибитора протонного насоса и 0,1-1000 мг СНПТ. Каждая лекарственная форма предпочтительно содержит 10-80 мг ингибитора протонного насоса и 10-800 мг СНПТ, более предпочтительно 10-40 мг ингибитора протонного насоса и 10-500 мг СНПТ. Особенно предпочтительные препараты содержат, например, 10 мг омепразола и 50 мг диклофенака, 10 мг омепразола и 250 мг напроксена, 10 мг омепразола и 10 мг пироксикама или 10 мг омепразола и 400 мг ибупрофена.
Таблетированный препарат со сложной структурой можно также диспергировать в воде со слегка кислым показателем рН перед пероральным приемом или вводить через назогастральный зонд.
Данное изобретение более подробно иллюстрируется следующими примерами.
Примеры
Пример 1
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая магний-омепразол и ибупрофен.
Вещество сердцевины
Магний-омепразол - 12,00 кг
Совершенные кристаллы - 12,00 кг
Гидроксипропилметилцеллюлоза - 1,8 кг
Дистиллированная вода - 35,4 кг
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 23,50 кг
Гидроксипропилцеллюлоза - 2,35 кг
Тальк - 4,03 кг
Стеарат магния - 0,34 кг
Дистиллированная вода - 48,00 кг
Энтеросолюбильное покрытие
Гранулы с разделительным слоем (в соответствии с вышеуказанным) - 38,70 кг
Сополимер метакриловых кислот (30% суспензия) - 38,70 кг
Триэтилцитрат - 3,48 кг
Моно- и диглицериды (NF) - 0,58 кг
Полисорбат 80 - 0,06 кг
Дистиллированная вода - 22,68 кг
3ащитное покрытие
Гранулы с энтеросолюбильным покрытием (в соответствии с вышеуказанным) - 44,7 кг
Гидроксипропилметилцеллюлоза - 0,58 кг
Стеарат магния - 0,017 кг
Дистиллированная вода - 11,6 кг
Таблетки - мг/таблетка
Гранулы с защитным покрытием, содержащие омепразол - 47,85
Ибупрофен - 400
Микрокристаллическая целлюлоза - 273,6
Сшитый поливинилпирролидон - 100,4
Поливинилпирролидон К-25 - 33,3
Лаурилсульфат натрия - 26,7
Дистиллированная вода - 297
Стеарилфумарат натрия - 4,0
Суспензионное покрытие получают в аппарата с псевдоожиженным слоем. Магний-омепразол наносят распылением на инертные совершенные кристаллы из водной суспензии, содержащей растворенное связующее вещество.
На полученное вещество сердцевины в аппарате с псевдоожиженным слоем наносят разделительный слой из раствора гидроксипропилцеллюлозы, содержащего тальк и стеарат магния. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, триэтилцитрата и полисорбата, наносят распылением на гранулы (с нанесенным разделительным слоем) в аппарате с псевдоожиженным слоем. В аппарате такого же типа на гранулы с энтеросолюбильным покрытием наносят покрытие из суспензии гидроксипропилметилцеллюлозы и стеарата магния. Полученные гранулы сортируют грохочением.
Гранулирующую жидкость для таблеток получают, растворяя 26,7 частей лаурилсульфата натрия и 33,3 части поливинилпирролидона К-25 в 267 частях дистиллированной воды. 400 частей ибупрофена, 226 частей микрокристаллической целлюлозы и 10,4 части сшитого поливинилпирролидона смешивают в сухом состоянии. К порошкообразной смеси добавляют гранулирующую жидкость и полученную массу смешивают в мокром состоянии. Добавляют 30 частей воды до требуемого количества.
Мокрую массу сушат в печи при температуре 60oC в течение примерно 6 часов. Сухие гранулы измельчают так, чтобы они проходили через сито с ячейками размером 0,8 мм.
Гранулы омепразола с энтеросолюбильным покрытием, измельченные гранулы ибупрофена, 47,6 части микрокристаллической целлюлозы, 4,0 части стеарилфумарата натрия и 90 частей сшитого поливинилпирролидона смешивают и прессуют в таблетки при помощи таблеточной машины с 15 мм пуансонами. Твердость таблеток массой 886 мг, измеренная в аппарате Шленигера, составляет от 5,3 до 5,9 кП. Время распадаемости, определяемое в искусственном желудочном соке (фармакопея США, без ферментов), равно 49-52 сек (n = 2).
Пример 2
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая магниевую соль S-омепразола и напроксен
Вещество сердцевины
Магниевая соль S-омепразола - 120 г
Совершенные кристаллы - 150 г
Полисорбат 80 - 2,4 г
Гидроксипропилметилцеллюлоза - 18 г
Дистиллированная вода - 562 г
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 200 г
Гидроскипропилцеллюлоза - 30 г
Тальк - 51,4 г
Стеарат магния - 4,3 г
Дистиллированная вода - 600 г
Энтеросолюбильное покрытие
Гранулы с разделительным слоем (в соответствии с вышеуказанным) - 250 г
Сополимер метакриловых кислот, 30% суспензия - 333,7 г
Триэтилцитрат - 30 г
Моно- и диглицериды (NF) - 5,0 г
Полисорбат 80 (=Твин 80) - 0,5 г
Дистиллированная вода - 195,8
Защитное покрытие
Гранулы с энтеросолюбильным покрытием - 371 г
Натрийкарбоксилметилцеллюлоза - 5,0 г
Дистиллированная вода - 191 г
Таблетки - мг/таблетка
Гранулы с защитным покрытием, содержащие 55 магниевую соль S- омепраэола - 55
Напроксен - 250
Микрокристаллическая целлюлоза - 150
Гидроксипропилцеллюлоза, низкомолекулярная замещенная - 40
Поливинилпирролидон К-90 - 5,0
Дистиллированная вода - 250
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Магниевую соль S-омепразола наносят распылением на инертные кристаллы сахара (совершенные кристаллы) из водной суспензии, содержащей растворенное связующее вещество и полисорбат 80.
На полученное вещество сердцевины в аппарате с псевдоожиженным слоем наносят разделительный слой из раствора гидроксипропилцеллюлозы, содержащего тальк и стеарат магния. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, триэтилцитрата и полисорбата, наносят распылением на гранулы (с разделительным слоем) в аппарате с псевдоожиженным слоем. В аппарате подобного типа на гранулы с энтеросолюбильным покрытием наносят раствор натрийкарбоксиметилцеллюлозы. Гранулы с защитным покрытием сортируют грохочением.
5 частей поливинилпирролидона К-90 растворяют в 150 частях дистиллированной воды с получением гранулирующей жидкости. Напроксен, микрокристаллическую целлюлозу и низкомолекулярную замещенную гидроксипропилцеллюлозу смешивают в сухом состоянии. К порошкообразной смеси добавляют гранулирующую жидкость и полученную массу перемешивают в мокром состоянии. Добавляют 100 частей воды до требуемого количества.
Мокрую массу сушат в печи при температуре 60oC в течение примерно 5-6 часов. Сухие гранулы измельчают так, чтобы они проходили через сито с ячейками размером 1,0 мм.
Гранулы с энтеросолюбильным покрытием смешивают с измельченными гранулами и прессуют в таблетки при помощи таблеточной машины с 18х8,5 мм пуансонами. Средняя твердость таблеток массой 500 мг, измеренная (вдоль наибольшей оси) в аппарате Шленигера, равна 9,4 кП. Время распадаемости, определяемое в дистиллированной воде при температуре 37oC, равно 15-30 секундам (n = 2).
Пример 3
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая пантопразол и пироксикам- -β- гидроксипропилциклодекстрин.
Вещество сердцевины
Пантопразол - 100 г
Совершенные кристаллы - 200 г
Гидроксипропилметилцеллюлоза (LF) - 25 г
Дистиллированная вода - 607 г
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 200 г
Гидроксипропилцеллюлоза (LF) - 20 г
Тальк - 34,3 г
Стеарат магния - 2,9 г
Дистиллированная вода - 400 г
Энтеросолюбильное покрытие
Гранулы с разделительным слоем (в соответствии с вышеуказанным) - 200 г
Сополимер метакриловых кислот, 30% суспензия - 333 г
Триэтилцитрат - 30 г
Моно- и диглицериды (NF) - 5,0 г
Полисорбат 80 - 0,5 г
Дистиллированная вода - 281,5 г
Таблетки - мг/таблетка
Гранулы, содержащие пантопразол - 133
Пироксикам - 20
β Гидроксипропилциклодекстрин, (90%) - 72
Микрокристаллическая целлюлоза - 276
Сшитый поливинилпирролидон - 36,8
Дистиллированная вода - ≤ 2
Стеарилфумарат натрия - 3,9
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Пантопразол наносят распылением на инертные кристаллы сахара (совершенные кристаллы) из водной суспензии, содержащей растворенное связующее вещество.
На полученное вещество сердцевины в аппарате с псевдоожиженным слоем наносят разделительный слой из раствора гидроксипропилцеллюлозы, содержащего тальк и стеарат магния. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, триэтилцитрата и полисорбата, наносят распылением на гранулы (с разделительным слоем) в аппарате с псевдоожиженным слоем. Гранулы сортируют грохочением.
Пироксикам добавляют к β--гидpoкcипpoпилциклoдекстрину во время механической обработки и смачивания водой. Полученную массу сушат в сушильной печи при температуре 50oC, а затем измельчают так, чтобы она проходила через сито с ячейками размером 0,8 мм.
Пироксикам -β- -гидроксипропилциклодекстрин, микрокристаллическую целлюлозу, сшитый поливинилпирролидон и стеарилфумарат натрия смешивают в сухом состоянии, после чего эту смесь смешивают с гранулами пантопразола. Таблетки прессуют в таблеточной машине с 18х8,5 мм пуансонами. Средняя твердость таблеток массой 577 мг, измеренная в аппарате Шленигера вдоль наибольшей оси, равна 16,7 кП, причем она может изменяться от 14,8 до 18,7 кП. Время распадаемости, определяемое в воде, равно примерно 4 минутам.
Таблетки покрывают пигментированной дисперсией так же, как в примере 7.
Пример 4
Двухслойная таблетированная лекарственная форма, в которой один слой является быстро распадающейся частью и содержит 20 мг ланзопразола в виде гранул с энтеросолюбильным покрытием, а другой слой обладает пролонгированным действием и выполнен в виде матрицы гидрофильного геля, содержащей 250 мг напроксена.
Гранулы ланзопразола с энтеросолюбильным покрытием
Вещество сердцевины
Ланзопразол - 400 г
Совершенные кристаллы - 400 г
Гидроксипропилметилцеллюлоза (LF) - 80 г
Лаурилсульфат натрия - 3 г
Дистиллированная вода - 1360 г
Промежуточное покрытие
Вещество сердцевины (в соответствии с вышеуказанным) - 100 г
Гидроксипропилметилцеллюлоза - 9 г
Полиэтиленгликоль 6000 - 1 г
Этанол, 95% - 250 г
Дистиллированная вода - 250 г
Энтеросолюбильное покрытие
Гранулы с промежуточным покрытием (в соответствии с вышеуказанным) - 100 г
Фталат гидроксипропилметилцеллюлозы - 39,9 г
Ацетилтрибутилцитрат - 8 г
Цетанол - 2,1 г
Этанол, 95% - 162 г
Ацетон - 378 г
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Ланзопразол наносят распылением на инертные совершенные кристаллы из водной суспензии, содержащей растворенное связующее вещество и смачивающее вещество.
На полученное вещество сердцевины в специально оснащенном аппарате с псевдоожиженным слоем Вюрстера наносят промежуточное покрытие из талька, суспендированного в растворе гидроксипропилметилцеллюлозы и полиэтиленгликоля. Полиэтиленгликоль выполняет также функцию пластификатора гидроксипропилметилцеллюлозы.
Энтеросолюбильное покрытие наносят в аналогичном аппарате из раствора веществ, образующих энтеросолюбильный слой, в органических растворителях.
Таблетки - мг/таблетка
Гранулы, содержащие ланзопразол - 94
Микрокристаллическая целлюлоза - 181,8
Сшитый поливинилпирролидон - 18,2
Напроксен - 250
Полиоксиэтилен (молекулярная масса примерно равна 4000000) - 200
Алюмосиликат натрия - 50
L-аргинин - 190
Этанол, 95% (в отношении веса к объему), примерно - 280
Напроксен, полиокс WSR 301®, L-аргинин и алюмосиликат натрия смешивают в сухом состоянии. К порошкообразной смеси добавляют гранулирующую жидкость и этанол, после чего полученную массу перемешивают в мокром состоянии. Мокрую массу сушат в печи при температуре 60oC в течение примерно 8 часов. Сухие гранулы измельчают так, чтобы они проходили через сито с ячейками размером 1,0 мм.
В процессе изготовления таблеток сначала предварительно прессуют 690 мг гранул, содержащих напроксен, после чего на верхнюю поверхность этого слоя наносят из расчета на одну таблетку 281 мг смеси, содержащей 81 мг гранул ланзопразола, 181,8 мг микрокристаллической целлюлозы и 18,2 мг сшитого поливинилпирролидона. Эти вещества затем прессуют в таблеточной машине Диафа с 9х20 мм пуансонами с получением двухслойных таблеток. Твердость таблетки, измеренная в аппарате Шленигера вдоль наибольшей оси, равна примерно 14 кП.
Растворимость напроксена испытывали в фосфатном буфере с pH 6,8. Получены следующие результаты:
1 час растворилось - 14%
3 часа растворилось - 34%
5 часов растворилось - 58%
7 часов растворилось - 79%
24 часа растворилось - 102%
Пример 5
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая магний-омепразол и пироксикам.
Вещество сердцевины (омепразол)
Магний-омепразол - 5,00 кг
Совершенные кристаллы - 10,00 кг
Гидроксипропилметилцеллюлоза - 0,75 кг
Дистиллированная вода - 19,65 кг
Разделительный слой (омепразол)
Вещество сердцевины (в соответствии с вышеуказанным) - 14,60 кг
Гидроксипропилцеллюлоза - 1,46 кг
Тальк - 2,5 кг
Стеарат магния - 0,21 кг
Дистиллированная вода - 29,2 кг
Энтеросолюбильное покрытие (омепразол)
Гранулы с разделительным слоем (в соответствии с вышеуказанным) - 9,00 кг
Сополимер метакриловых кислот (30% суспензия) - 15,00 кг
Триэтилцитрат - 1,35 кг
Моно- и диглицериды (NF) - 0,22 кг
Полисорбат 80 - 0,02 кг
Дистиллированная вода - 8,8 кг
Защитное покрытие (омепразол)
Гранулы с энтеросолюбильным покрытием - 9,0 кг
Гидроксипропилметилцеллюлоза - 0,18 г
Стеарат магния - 0,005 кг
Дистиллированная вода - 3,6 кг
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Магний-омепразол наносят распылением на инертные кристаллы сахара (совершенные кристаллы) из водной суспензии, содержащей растворенное связующее вещество.
На полученное вещество сердцевины в аппарате с псевдоожиженным слоем наносят разделительный слой из раствора гидроксипропилцеллюлозы, содержащего тальк и стеарат магния. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, триэтилцитрата и полисорбата, наносят распылением на гранулы с промежуточным покрытием в аппарате с псевдоожиженным слоем. В аппарате такого же типа на гранулы с энтеросолюбильным покрытием наносят покрытие из суспензии гидроксипропилметилцеллюлозы и стеарата магния. Гранулы с защитным покрытием сортируют грохочением.
Вещество сердцевины (пироксикам)
Пироксикам, очень тонко измельченный - 35 г
Кристаллы сахара - 100 г
Гидроксипропилметилцеллюлоза, 6 сантипуаз - 25 г
Дистиллированная вода - 250 г
Этанол 99% (в отношении веса к объему) - 250 г
Энтеросолюбильное покрытие (пироксикам)
Гранулы пироксикама (в соответствии с вышеуказанным) - 100 г
На гранулы пироксикама наносят покрытие из суспензии следующего состава с получением продукта, содержащего 163 мг/г активного вещества:
Ацетосукцинат гидроксипропилметилцеллюлозы (LF) - 14,38 части
Триэтилцитрат - 2,87 части
Лаурилсульфат натрия - 0,43 части
Тальк - 4,32 части
Дистиллированная вода - 183,3 части
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Очень тонко измельченный пироксикам наносят распылением на инертные совершенные кристаллы из водной суспензии, содержащей растворенное связующее вещество.
Энтеросолюбильное покрытие, состоящее из ацетосукцината гидроксипропилметилцеллюлозы, триэтилцитрата, лаурилсульфата натрия и талька, наносят распылением на гранулы пироксикама в аппарате с псевдоожиженным слоем.
Таблетки (на 1000 штук)
Гранулы, содержащие омепразол - 95,7 г
Гранулы, содержащие пироксикам - 122,7 г
Микрокристаллическая целлюлоза - 240 г
Сшитый поливинилпирролидон - 20 г
Гидроксипропилцеллюлоза, низкомолекулярная замещенная - 40 г
Стеарилфумарат натрия - 4,6 г
Микрокристаллическую целлюлозу, низкомолекулярную замещенную гидроксипропилцеллюлозу и сшитый поливинилпирролидон смешивают до однородного состояния. После этого смешивают гранулы с энтеросолюбильным покрытием двух типов. Затем добавляют стеарилфумарат натрия, используемый в качестве смазки, и эту смесь прессуют в таблетки при помощи таблеточной машины с 8,5х16 мм пуансонами. Твердость таблеток массой 523 мг, измеренная в аппарате Шленигера, составляет от 8 до 9 кП. Время распадаемости, определяемое в воде при температуре 37oC, равно менее 1 минуты.
На эти таблетки наносят покрытие из пигментированной дисперсии так же, как в примере 7.
Пример 6
Быстро распадающаяся таблетка с энтеросолюбильным покрытием, содержащая магний-омепразол и диклофенак.
Таблетки (на 2000 штук)
Магний-омепразол (соответствует 20 мг омепразола) - 45,0 г
Натрий-диклофенак (соответствует 20 мг диклофенака) - 43,2 г
Микрокристаллическая целлюлоза - 110 г
Сшитый поливинилпирролидон - 50 г
Гидроксипропилцеллюлоза, низкомолекулярная замещенная - 50 г
Стеарилфумарат натрия - 8, 6 г
Дистиллированная вода, примерно - 170 г
Омепразол, диклофенак, микрокристаллическую целлюлозу, низкомолекулярную замещенную гидроксипропилцеллюлозу, 30 г сшитого поливинилпирролидона и 5,6 г стеарилфумарата натрия смешивают и, продолжая перемешивать, добавляют воду. Гранулированное вещество сушат в сушильной печи при температуре 60oC в течение примерно 1,5 часов. Сухое гранулированное вещество измельчают так, чтобы оно проходило через сито с ячейками размером 1,0 мм.
Измельченные гранулы смешивают с 20 г сшитого поливинилпирролидона и 3,0 г стеарилфумарата натрия. Из этой смеси прессуют таблетки массой 153 мг при помощи таблеточной машины с 7 мм пуансонами. Средняя твердость таблетки равна 7,4 кП (n = 6). Время распадаемости в воде при температуре 37oC равно 1 минуте 20 секундам (n = 1).
В специально оснащенном аппарате с псевдоожиженным слоем Вюрстера на таблетки наносят разделительный слой, состоящий из гидроксипропилметилцеллюлозы и талька.
Нанесение разделительного слоя
Таблетки 7 мм - 100,1 г
Дисперсия для нанесения покрытия:
Гидроксипропилметилцеллюлоза, 6 сантипуаз - 5,5 г
Тальк - 1,15г
Et OH 99% (в отношении веса к объему) - 46,7 г
Дистиллированная вода - 46,7 г
На полученные таблетки с покрытием далее наносят энтеросолюбильное покрытие в аналогичном аппарате.
Нанесение энтеросолюбильного покрытия
Таблетки с разделительным слоем - 100 г
Дисперсия для нанесения покрытия:
Сополимер метакриловых кислот, 30% суспензия - 26,4 г (7,92 г сухого вещества)
Полиэтиленгликоль 400 - 0,9 г
Диоксид титана - 0,83 г
Оксид железа, красновато-коричневый - 0,28 г
Дистиллированная вода - 55,1 г
На стадии нанесения энтеросолюбильного покрытия масса таблетки увеличивается примерно на 11 мг/таблетку, что соответствует примерно 7% массы загруженных таблеток.
Пигменты, входящие в состав энтеросолюбильного покрытия, защищают активные вещества от воздействия света.
Пример 7
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, состоящая из магний-омепразола, внутреннего покрытия, содержащего натрий-диклофенак, и защитного пигментированного покрытия, защищающего активные вещества от воздействия света.
Гранулы магний-омепразола с энтеросолюбильным покрытием по примеру 5.
Таблетки - мг/таблетка
Гранулы, содержащие омепразол - 83,3
Микрокристаллическая целлюлоза - 181,4
Сшитый поливинилпирролидон - 3,7
Стеарилфумарат натрия - 0,4
Гранулы получают так же, как в примере 5.
Микрокристаллическую целлюлозу, сшитый поливинилпирролидон и гранулы, содержащие омепразол, смешивают в сухом состоянии. 3атем к полученной смеси добавляют стеарилфумарат натрия.
Эту смесь прессуют в таблетки при помощи таблеточной машины с 9 мм пуансонами. Твердость таблеток Массой 269 мг, измеренная в аппарате Шленигера, составляет от 8 до 9 кП.
На таблетки наносят покрытие в псевдоожиженном слое из приведенного ниже раствора, пока средняя масса таблетки не становится равной 298 мг.
Натрий-диклофенак - 20,0 вес. частей
Гидроксипропилметилцеллюлоза, 6 сантипуаз - 11,4 вес.части
Этанол, 99% (в отношении веса к объему) - 113,6 вес.части
Дистиллированная вода - 113,6 вес.части
На последней стадии на эти таблетки наносят покрытие из пигментированной суспензии в том же аппарате. Суспензия для нанесения покрытия имеет следующий состав:
Гидроксипропилметилцеллюлоза, 6 сантипуаз - 10,0 вес.частей
Полиэтиленгликоль, молекулярная масса 6000 - 2,5 вес.части
TiO2 - 1,83 вес.части
Оксид железа, желтый - 0,40 вес.части
Этанол, 99% (в отношении веса к объему) - 85 вес.частей
Дистиллированная вода - 85 вес.частей
Средняя масса полученной таблетки равна 303 мг. Время распадаемости, определяемое в воде при температуре 37oC, составляет менее 4 минут (n = 4).
Пример 8
Капсулированный препарат, содержащий магний-омепразол и пироксикам.
Капсулы
Гранулы омепразола с энтеросолюбильным покрытием (способ получения и композиция в соответствии с примером 5) - 95,7 мг/капсулу
Гранулы пироксикама с энтеросолюбильным покрытием (способ получения и композиция в соответствии с примером 5) - 122,7 мг/капсулу
Полученными гранулами заполняют твердые желатиновые капсулы, размер 3. Прежде чем заполнить капсулы гранулами, к ним необязательно добавляют небольшое количество смазки. Количество омепразола в каждой капсуле составляет примерно 20 мг, а количество пироксикама составляет примерно 20 мг.
Пример 9
Капсулированный препарат, содержащий магниевую соль S-омепразола и напроксен.
Капсулы
Гранулы с энтеросолюбильным покрытием (способ получения и композиция в соответствии с примером 2) - 55,2 мг/капсулу
Гранулированный напроксен (способ получения и композиция в соответствии с примером 2) - 445 мг/капсулу
Полученными гранулами и гранулами с энтеросолюбильным покрытием заполняют твердые желатиновые капсулы, размер 00. Прежде чем заполнить капсулы гранулами, к ним необязательно добавляют небольшое количество смазки. Количество S-омепразола в каждой капсуле составляет примерно 10 мг, а количество напроксена составляет примерно 250 мг.
Пример 10
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая магний-омепразол и натрий-диклофенак.
Вещество сердцевины
Магний-омепразол - 5 кг
Сферические кристаллы сахара - 10 кг
Гидроксипропилметилцеллюлоза - 0,75 кг
Дистиллированная вода - 19,7 кг
Разделительный слой
Вещество сердцевины - 10,2 кг
Гидроксипропилцеллюлоза - 1,02 кг
Тальк - 1,75 кг
Стеарат магния - 0,146 кг
Дистиллированная вода - 21,4 кг
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем - 11,9 кг
Сополимер метакриловых кислот (30% суспензия) - 19,8 кг
Триэтилцитрат - 1,79 кг
Моно- и диглицериды (NF) - 0,297 кг
Полисорбат 80 - 0,03 кг
Дистиллированная вода - 11,64 кг
Защитное покрытие
Гранулы с энтеросолюбильным покрытием - 20,0 кг
Гидроксипропилметилцеллюлоза - 0,238 кг
Стеарат магния - 0,007 кг
Дистиллированная вода - 6,56 кг
Таблетки
Гранулы с защитным покрытием, содержащие омепразол - 82,4
Натрий-диклофенак - 50,0
Микрокристаллическая целлюлоза - 261
Сшитый поливинилпирролидон - 5,6
Стеарилфумарат натрия - 0,56 \\2 Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Магний-омепразол наносят распылением на сферические кристаллы сахара из водной суспензии, содержащей растворенное связующее вещество. Размер сферических кристаллов сахара равен 0,25-0,35 мм. Полученное вещество сердцевины покрывают раствором гидроксипропилцеллюлозы, содержащим тальк и стеарат магния. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, триэтилцитрата и полисорбата, наносят распылением на гранулы, покрытые разделительным слоем, в аппарате с псевдоожиженным слоем. В аналогичном аппарате на гранулы с энтеросолюбильным покрытием наносят покрытие из раствора гидроксипропилметилцеллюлозы, содержащего стеарат магния. Гранулы с защитным покрытием сортируют грохочением.
Гранулы с энтеросолюбильным и защитным покрытиями, натрий-диклофенак, микрокристаллическую целлюлозу, сшитый поливинилпирролидон и стеарилфумарат натрия смешивают в сухом состоянии и прессуют в таблетки при помощи таблеточной машины с эксцентриком и 11 мм пуансонами. Количество омепразола в каждой таблетке составляет примерно 10 мг, а количество натрий-диклофенака составляет примерно 50 мг. Измеренная твердость таблетки равна 80 Н.
Пример 11
Быстро распадающаяся таблетированная лекарственная форма со сложной структурой, содержащая магний-омепразол и пироксикам.
Вещество сердцевины
Магний-омепразол - 10,00 кг
Сферические кристаллы сахара - 10,00 кг
Гидроксипропилметилцеллюлоза - 1,5 кг
Дистиллированная вода - 29,9 кг
Разделительный слой
Вещество сердцевины - 20,00 кг
Гидроксипропилцеллюлоза - 2,0 кг
Тальк - 3,43 кг
Стеарат магния - 0,287 кг
Дистиллированная вода - 41,0 кг
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем - 24,5 кг
Сополимер метакриловых кислот (30% суспензия) - 32,7 кг
Триэтилцитрат - 2,94 кг
Моно- и диглицериды (NF) - 0,49 кг
Полисорбат 80 - 0,049 кг
Дистиллированная вода
Защитное покрытие
Гранулы с энтеросолюбильным покрытием - 37,8 кг
Гидроксипропилметилцеллюлоза - 0,49 кг
Стеарат магния - 0,0245 кг
Дистиллированная вода - 11,6 кг
Таблетки - мг/таблетка
Гранулы с защитным покрытием, содержащие омепразол - 94,9
Пироксикам - 20,0
Микрокристаллическая целлюлоза - 280
Сшитый поливинилпирролидон - 5,6
Стеарилфумарат натрия - 0,56
Гранулы магний-омепразола с энтеросолюбильным и защитным покрытиями получают так же, как в примере 10.
Гранулы с энтеросолюбильным и защитным покрытиями, пироксикам, микрокристаллическую целлюлозу, сшитый поливинилпирролидон и стеарилфумарат натрия смешивают в сухом состоянии и прессуют в таблетки при помощи таблеточной машины с эксцентриком и 11 мм пуансонами. Количество омепразола в каждой таблетке составляет примерно 20 мг, а количество пироксикама составляет примерно 20 мг. Измеренная твердость таблетки равна 110 Н.
Результаты
"Кислотостойкость", то есть % активного вещества, оставшегося после воздействия 0,1 н раствором HCl в течение 2 часов - Таблетки
Пример 1 - 95%
Пример 2 - 95%
Пример 3 - 99%
Пример 4 - 91%
Пример 5 - 92%
Пример 6 - 96%
Пример 7 - 93%
Пример 10 - 91%
Пример 11 - 91%
Наиболее предпочтительным вариантом осуществления настоящего изобретения являются лекарственные формы, описанные в примерах 5, 7 и 10.
Гранулы с энтеросолюбильным покрытием, содержащие ингибитор протонного насоса, можно также получить так, как описано в следующих примерах.
Пример 12
Получение гранул с энтеросолюбильным покрытием путем экструзии и сферообразования.
Вещество сердцевины
Магний-омепразол - 600 г
Маннит - 1000 г
Микрокристаллическая целлюлоза - 300 г
Гидроксипропилцеллюлоза - 100 г
Лаурилсульфат натрия - 6 г
Дистиллированная вода - 802 г
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 400 г
Гидроксипропилметилцеллюлоза - 48 г
Дистиллированная вода - 960 г
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (в соответствии с вышеуказанным) - 200 г
Сополимер метакриловых кислот - 100 г
Триэтилцитрат - 30 г
Моно- и диглицериды (NF) - 5 г
Полисорбат 80 - 0,5 г
Дистиллированная вода - 309 г
Лаурилсульфат натрия растворяют в дистиллированной воде с получением гранулирующей жидкости. Магний-омепразол, маннит, микрокристаллическую целлюлозу и гидроксипропилцеллюлозу смешивают в сухом состоянии. К порошкообразной смеси добавляют гранулирующую жидкость и полученную массу перемешивают в мокром состоянии.
Мокрую массу пропускают через экструдер, снабженный сотами с размером ячеек 0,5 мм. Экструдату придают сферическую форму на фрикционной плите в сферообразующем аппарате. Вещество сердцевины сушат в сушилке с псевдоожиженным слоем и сортируют. В аппарате с псевдоожиженным слоем полученное вещество сердцевины покрывают разделительным слоем из раствора гидроксипропилметилцеллюлозы и воды.
Энтеросолюбильное покрытие наносят на гранулы, покрытые разделительным слоем, из водной дисперсии сополимера метакриловых кислот, пластифицированного триэтилцитратом, к которой добавлена дисперсия моно- и диглицеридов и полисорбата. Гранулы сушат в аппарате с псевдоожиженным слоем.
Пример 13
Получение гранул с энтеросолюбильным покрытием путем нанесения порошка на сферические кристаллы сахара.
Вещество сердцевины
Магний-омепразол - 1500 г
Сферические кристаллы сахара - 1500 г
Гидроксипропилметилцеллюлоза - 420 г
Аэрозил ® - 8 г
Дистиллированная вода - 4230 г
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 500 г
Гидроксипропилцеллюлоза - 40 г
Тальк - 67 г
Стеарат магния - 6 г
Дистиллированная вода - 800 г
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (в соответствии с вышеуказанным) - 500 г
Сополимер метакриловых кислот - 200 г
Триэтилцитрат - 60 г
Дистиллированная вода - 392 г
Магний-омепразол, часть гидроксипропилметилцеллюлозы и аэрозил ® смешивают в сухом состоянии с получением порошка. На сферические кристаллы сахара (0,25-0,40 мм) наносят порошок в центробежном грануляторе для нанесения покрытия в псевдоожиженном слое при одновременном распылении раствора гидроксипропилметилцеллюлозы (6 вес.% отношении).
Полученное вещество сердцевины сушат и покрывают разделительным слоем в центробежном грануляторе для нанесения покрытия в псевдоожиженном слое. Энтеросолюбильное покрытие наносят в аппарате с псевдоожиженным слоем.
Пример 14
Получение гранул с энтеросолюбильным покрытием на основе кристаллов диоксида кремния.
Вещество сердцевины
Магний-омепразол - 8,00 кг
Диоксид кремния - 8,00 кг
Гидроксипропилметилцеллюлоза - 1,41 кг
Лаурилсульфат натрия - 0,08 кг
Дистиллированная вода - 28,00 кг
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 10,00 кг
Гидроксипропилметилцеллюлоза - 0,80 кг
Дистиллированная вода - 10,00 кг
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (в соответствии с вышеуказанным) - 300 г
Сополимер метакриловых кислот - 124 г
Полиэтиленгликоль 400 - 25 г
Моно- и диглицериды (NF) - 3 г
Полисорбат 80 - 1 г
Дистиллированная вода - 463 г
Суспензионное покрытие получают в аппарате с псевдоожиженным слоем. Магний-омепразол наносят распылением на кристаллы диоксида кремния из водной суспензии, содержащей растворенное связующее вещество и поверхностно-активное вещество. Полученное вещество сердцевины покрывают разделительным слоем из раствора гидроксипропилметилцеллюлозы в аппарате с псевдоожиженным слоем. Энтеросолюбильное покрытие, состоящее из сополимера метакриловых кислот, моно- и диглицеридов, полиэтиленгликоля 400 и полисорбата, наносят распылением на гранулы, покрытые разделительным слоем, в аппарате с псевдоожиженным слоем.
Пример 15
Получение гранул с энтеросолюбильным покрытием
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (способ получения и композиция в соответствии с примером 12) - 500 г
Сополимер метакриловых кислот - 250 г
Полиэтиленгликоль 6000 - 75 г
Моно- и диглицериды (NF) - 12,5 г
Полисорбат 80 - 1,2 г
Дистиллированная вода - 490 г
Пример 16
Получение гранул с энтеросолюбильным покрытием.
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (способ получения и композиция в соответствии с примером 1) - 500 г
Фталат гидроксипропилметилцеллюлозы - 250 г
Цетанол - 50 г
Этанол, 95% - 1000 г
Ацетон - 2500 г
Пример 17
Получение гранул с энтеросолюбильным покрытием.
Вещество сердцевины
Омепразол - 225 г
Маннит - 1425 г
Гидроксипропилцеллюлоза - 60 г
Микрокристаллическая целлюлоза - 40 г
Безводная лактоза - 80 г
Лаурилсульфат натрия - 5 г
Дигидрат динатрийфосфата - 8 г
Дистиллированная вода - 350 г
Разделительный слой
Вещество сердцевины (в соответствии с вышеуказанным) - 300 г
Гидроксипропилцеллюлоза - 30 кг
Тальк - 51 г
Стеарат магния - 4 г
Энтеросолюбильное покрытие
Гранулы, покрытые разделительным слоем (в соответствии с вышеуказанным) - 300 г
Сополимер метакриловых кислот - 140 г
Триэтилцитрат - 42 г
Моно- и диглицериды (NF) - 7 г
Полисорбат 80 - 0,7 г
Сухие ингредиенты, предназначенные для получения вещества сердцевины, тщательно смешивают в смесителе. Добавляют гранулирующую жидкость, после чего полученную смесь перемешивают и гранулируют до получения требуемой консистенции. Мокрую массу продавливают через сито экструдера и полученным гранулам придают сферическую форму в сферообразователе. Вещество сердцевины сушат в аппарате с псевдоожиженным слоем и отсортировывают частицы требуемого размера, например 0,5-1,0 мм. На вещество сердцевины наносят разделительный слой и энтеросолюбильное покрытие в соответствии с описанием, приведенным в предыдущих примерах.
Получение активного вещества
Магний-омепразол, используемый в некоторых примерах, получают в соответствии со способом, описанным в заявке WO/95/01977, отдельные энантиомеры солей омепразола получают так, как описано в заявке WO/94/27988, и омепразол получают в соответствии со способом, описанным в заявке на европейский патент N EP-A10005129. Эти документы включены в это описание изобретения в качестве справочных материалов.
Изобретение относится к фармацевтической лекарственной форме для перорального приема, содержащей ингибитор протонного насоса и одно или несколько средств нестероидной противовоспалительной терапии в виде дозированного препарата, в котором ингибитор протонного насоса защищен энтеросолюбильным покрытием, к средству нестероидной противовоспалительной терапии, к способу получения дозированной лекарственной формы и к способу лечения побочных эффектов, возникающих в желудочно-кишечном тракте вследствие лечения средствами нестероидной противовоспалительной терапии. Дозированный препарат имеет форму таблетки с энтеросолюбильным покрытием, капсулы или таблетированной лекарственной формы со сложной структурой. Лекарственные формы со сложной структурой являются наиболее предпочтительными. Новый дозированный препарат особенно полезен для лечения побочных эффектов, возникающих в желудочно-кишечном тракте вследствие лечения средствами нестероидной противовоспалительной терапии. 6 с. и 22 з.п.ф-лы.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Автоматическая акустическая блокировка | 1921 |
|
SU205A1 |
Авторы
Даты
2000-10-27—Публикация
1996-12-20—Подача