Изобретение относится к медицине, а именно к хирургии, и может быть использовано для лечения неосложненных форм наружных брюшных грыж, исключая послеоперационные. Известны способы эндовидеохиругического лечения паховых, бедренных, запирательных, пупочных, спигелиевых грыж, заключающиеся в полном или частичном удалении грыжевого мешка, интра- или экстраперитонеальном размещении синтетического сетчатого трансплантата, фиксации его металлическими скрепками (Тимошин А.Д., Галингер Ю.И., 1993; Седов В.М. и соавт., 1995; Рутенбург Г.М. и соавт., 1997; Gedebou Т.М., Neubauer W., 1998; Haith L.R. Jr. et al., 1998).
Указанные способы имеют ряд общих недостатков. А именно: дороговизна синтетического трансплантата, степлера и металлических скрепок; необходимость фиксации трансплантата вблизи подвздошных и семенных сосудов, семявыносящего протока, бедренного нерва ("рокового треугольника" и "треугольника боли") - опасно их повреждением; вправление грыжевого мешка при экстраперитонеальной герниопластике, а не его удаление сохраняет основной патологический субстрат грыжи, что может закончиться ее рецидивом.
Наиболее близкими к предлагаемому являются способ интраперитонеальной герниопластики паховых грыж, описанный И.В. Федоровым, Е. И. Сигал, В.В. Одинцовым (1998). Последний заключается в рассечении париетальной брюшины вдоль паховой связки электроножом или ножницами, отсепаровке ее, удалении грыжевого мешка, помещении протеза в сформированном окне, фиксации его степлером вдоль паховой и гребешковой связок, лонной кости, поперечной и прямой мышц, ушивании брюшины. Недостатками его, помимо перечисленных выше, являются: ненадежная фиксация протеза; кишечная непроходимость в связи со спайкообразованием в неушитом брюшинном окне; возможность появления гематом и сером в зоне грыжевого мешка при ненадежном гемостазе; отторжение трансплантата или образование "meshom" (больших гранулем в зоне сетчатого протеза) как следствие неучитывания стадийности раневого процесса; рассеченная брюшина ушивается без перемещения, оставляя скомпрометированную, участвующую в образовании грыжевого мешка часть в зоне грыжевых ворот.
Задача изобретения: устранение грыжевого дефекта путем формирования в его зоне равномерного соединительно-тканного рубца за счет местной индуцированной стимуляции фазы репаративной регенерации раневого процесса.
Поставленная задача решается путем выделения грыжевого мешка, выворачивания его в брюшную полость и фиксации к париетальной брюшине либо ушивания и резекции у шейки его в пределах здоровых тканей; дренирования ретроперитонеальной зоны грыжевых ворот через контрапертуру "дренажем-ирригатором с памятью барьерной формы"; имплантации в указанную зону на 7-е сутки послеоперационного периода 0,8 г препарата "Фибриноген", растворенного в 70-100 мл физиологического раствора.
Изобретение поясняется следующими фигурами.
Фиг. 1 - изображен выделенный, вывернутый в брюшную полость грыжевой мешок прямой паховой грыжи, фиксированный швами к париетальной брюшине.
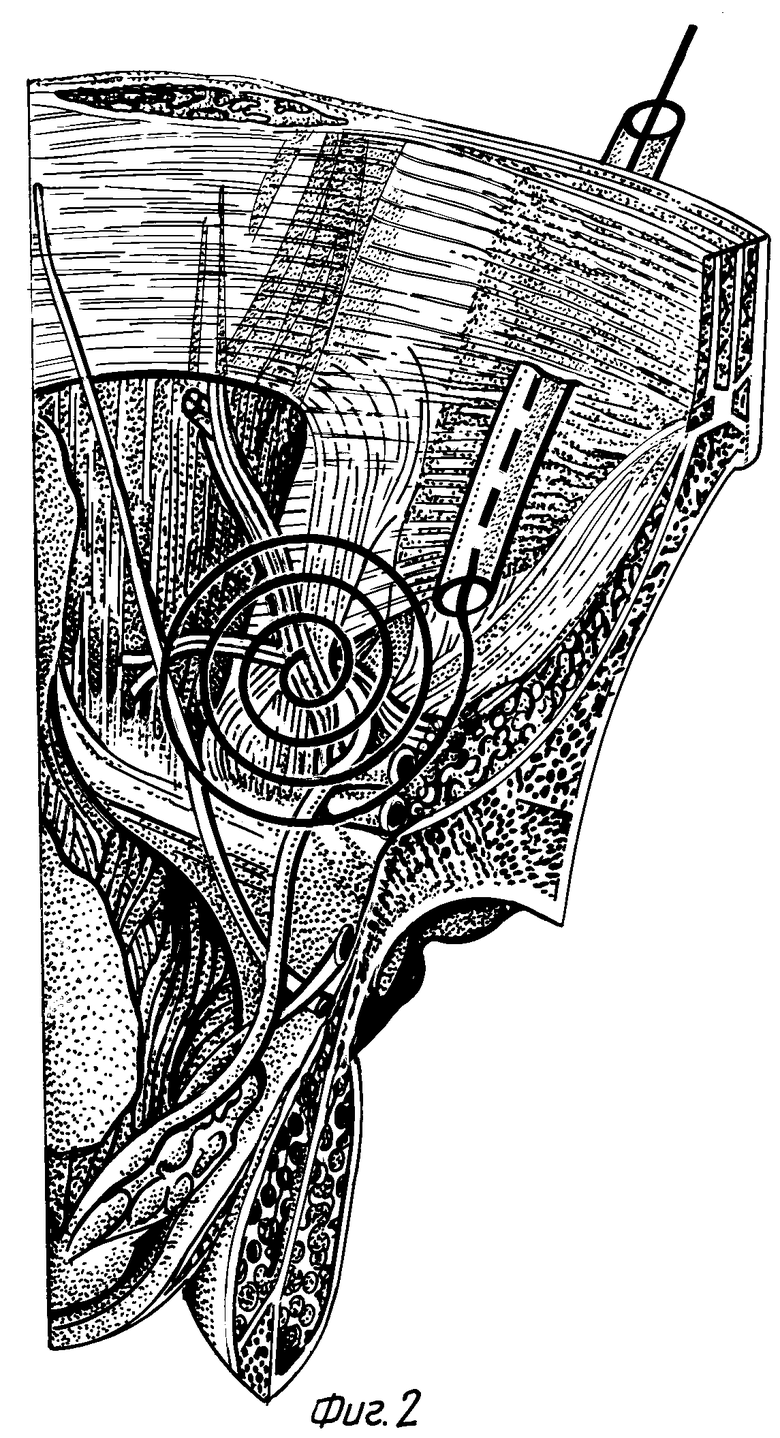
Фиг. 2 - изображено дренирование ретроперитонеальной зоны грыжевых ворот через контрапертуру дренажем-ирригатором.
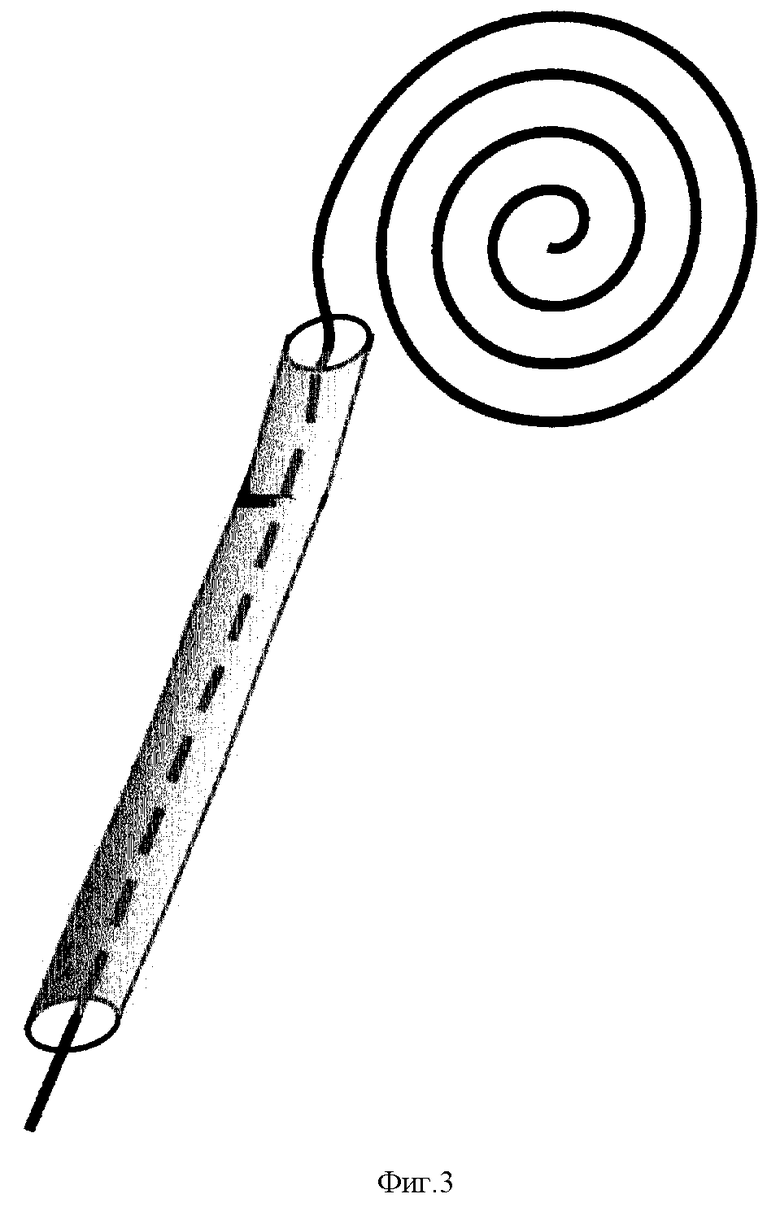
Фиг. 3 - изображен дренаж-ирригатор с памятью барьерной формы.
Заявленный способ заключается в том, что грыжевой дефект устраняется за счет перемещения в эту область нескомпрометированной брюшины путем выворачивания грыжевого мешка в брюшную полость с фиксацией к париетальной брюшине или ушивания и пересечения его у шейки; дренирования ретроперитонеальной зоны грыжевых ворот через контрапертуру "дренажем-ирригатором с памятью барьерной формы", который в фазе воспаления раневого процесса выполняет эвакуаторную и защитную функции, а в фазе репаративной регенерации - каркасную и транспортную, по которому на 7-е сутки послеоперационного периода имплантируется 0,8 г препарата "Фибриноген", растворенного в 70-100 мл физиологического раствора, с целью формирования прочного соединительнотканного рубца.
Способ выполняется следующим образом. Дренаж-ирригатор с памятью барьерной формы изготавливается индивидуально, стерилизуется непосредственно перед оперативным вмешательством методом "холодной" стерилизации. Для осуществления этого полихлорвиниловый катетер внутренним диаметром 1-1,4 мм наматывается на 5 последовательно одеваемых друг на друга металлических полуколец с желобом на наружной поверхности диаметром от 1 до 5 см. Противоположный конец дренажа остается прямым на расстоянии до 10 см. Образовавшуюся конструкцию помещают в кипящую воду на 3-5 минут, затем быстро охлаждают проточной холодной водой. Катетер снимают с колец, на одном из концов его получается плоская спираль, легко расправляющаяся и сворачивающаяся вновь. Вмешательство выполняют под общим обезболиванием с использованием ИВЛ. Накладывается пневмоперитонеум. Параумбиликально вводится троакар и лапароскоп. Дополнительно вводятся два троакара для инструментов, причем один из них, на стороне грыжи, располагается забрюшинно. Дно грыжевого мешка захватывается эндохирургическим зажимом и подтягивается в брюшную полость. В эабрюшинное пространство вводится лопаточка или анатомический зажим, брюшина отсепаровывается, обнажая зону грыжевых ворот, дополнительно помогая тракциям мешка. При невозможности его выделения, что бывает при косых паховых грыжах, ушивают у шейки кисетным швом, отсекают электроножом, дефект брюшины ушивают кисетным швом в пределах нескомпрометированных участков. Для этого троакар из забрюшинного пространства временно переводят в брюшную полость. Вывернутый грыжевой мешок фиксируют к париетальной брюшине 3-4 швами у дна и по краям. Под контролем лапароскопа через гильзу ретроперитонеального троакара в зону грыжевых ворот помещают трубчатый дренаж внутренним диаметром 5-7 мм, по которому вводится тонкий дренаж, с постепенно скручивающейся спиралью. Диаметр спирали варьирует в зависимости от размеров грыжевого дефекта, обязательно превышая его. Извлекаются инструменты, дренаж фиксируется. Первые 1-3 суток по нему эвакуируется раневое отделяемое. На 6-7 сутки послеоперационного периода, в фазе репарации раневого процесса, препарат "Фибриноген", заготавливаемый в условиях Станции переливания крови, массой 0,8 грамм растворяется 70-100 мл физиологического раствора. В стерильных условиях фибриноген вводится в зону грыжевого дефекта по тонкому дренажу с одновременным извлечением его. Спираль при этом раскручивается, вводимый препарат распределяется равномерно, повторяя ее ход, занимает всю указанную зону. Избыток последнего изливается по толстому дренажу, который также удаляется.
Исходя из представлений о стадийности раневого процесса каждой из них присущ определенный клеточный субстрат. Переход пролиферативной стадии воспаления в фазу репаративной регенерации, отмечаемый на 5-7 сутки, для ран, заживающих первичным натяжением, характеризуется преобладанием популяции фибробластов, выполняющих рубцово-образовательную функцию путем синтеза коллагена, от качественного и количественного состава которого зависит прочность рубца, замещающего грыжевой дефект. Фибриноген-фибрин образует матричную основу для фибробластов, а продукты его распада стимулируют их деятельность.
Перемещение брюшины в зоне грыжевых ворот как фактор укрепления не требует дополнительной аргументации. Не вызывают возражений эвакуаторная, защитная (барьерная), транспортная и каркасная функции сконструированного дренажа-ирригатора. Гипотеза о стимулирующем воздействии фибриногена на репарацию, индуцирование коллагенопэза требовала дополнительного обоснования.
С этой целью выполнено экспериментальное исследование. У 3 кроликов породы "Шиншилла" был осуществлен забор крови, из которой, по стандартной технологии, методом плазмафереза и последующего фракционирования было заготовлено, фасовано и консервировано 0,5 г сухого фибриногена. 33 кроликам той же породы произведены трансректальные лапаротомии в мезогипогастральной области с удалением участка прямой мышцы живота площадью 6 см2, ушиванием брюшины и передней стенки влагалища прямой мышцы, дренированием безмышечной зоны. На 7-е сутки послеоперационного периода, после разведения сухой массы фибриногена 75 мл физиологического раствора, 27 кроликам имплантировано по 1 мл раствора фибриногена. Вывод животных из эксперимента осуществляли 3-мя группами: 9 особей - на 7-е сутки; 9 - на 21-е; 15 - на 31-е (9 - экспериментальной группы, 6 - контрольной). Забор материала производили путем иссечения зоны вмешательства вместе с окружающими тканями, после макроскопической оценки его плотности и однородности осуществлялось гистологическое исследование серийных и ступенчатых срезов. Срезы окрашивались гематоксилином и эозином, пикрофуксином по Ван Гизон, для оценки гистохимического состава межклеточного матрикса ставилась ШИК-реакция, для выявления аргирофильных волокон использовали импрегнацию азотнокислым серебром по Данилину.
Гистологические и гистохимические исследования области формирующегося рубца выявили существенные особенности репаративных процессов при использовании фибриногена в сравнении с контрольной серией, принципиально заключающиеся в раннем наступлении фаз организации и ремоделирования соединительной ткани, создании анатомической целостности апоневротического регенерата, отсутствии в раннем периоде выраженных экссудативных и воспалительных явлений, что приводит к выводу об оптимальном с биомеханической точки зрения характере репарации фасциальных и апоневротических структур, с установлением их анатомической целостности и непрерывности в условиях введения фибриногена.
Компрессирующего воздействия индуцированного рубца на сосудистые и протоковые образования не обнаружено.
Таким образом, можно предположить, что поставленная задача устранения грыжевого дефекта путем формирования в его зоне равномерного соединительнотканого рубца за счет местной индуцированной стимуляции фазы репаративной регенерации раневого процесса достигнута за счет того, что устраняется основной патологический субстрат - грыжевой мешок; на его месте оказывается непораженная брюшина; дренирование зоны грыжевых ворот в фазе воспаления устраняет отрицательные проявления экссудации, плазмо- и геморрагии; спиралевидня форма дренажа придает ему барьерную функцию в раннем послеоперационном периоде; введение фибриногена в зону грыжевого дефекта в фазе репаративной регенерации раневого процесса индуцирует формирование прочного соединительно-тканного рубца, а спиралевидная форма дренажа-ирригатора создаст равномерность поступления препарата; исключается необходимость использования дополнительных пластических материалов; возможно применение разработанного способа для эндоскопического хирургического лечения неосложненных грыж паховой, бедренной, тазовой, пупочной и белой линии, спигелиево-дугласовой, поясничной локализаций.
СПИСОК ЛИТЕРАТУРЫ
1. Сравнительная характеристика различных методов эндо-видеохирургической и "традиционной" герниопластики. /Рутенбург Г.М., Протасов А.В., Виноградов А.В., Пономарев В.А.// Эндоскопическая хирургия. 1997. N 1. С. 91.
2. Лапароскопическая герниопластика при паховых грыжах. /Седов В.М., Гуслев А. Б., Стрижелецкий В. В. и соавт./ С.-Петербург. 1995. 50-е.
3. Тимошин А.Д., Галингер Ю.И. Лапароскопическое грыжесечение с использованием полипропиленовой сетки для закрытия внутреннего кольца пахового канала. //Тез. межд. конгресса "Лапароскопическая хирургия". М. 1993. С. 92- 97.
4. Федоров И. В. , Сигал Е.И., Одинцов В. В. Эндоскопическая хирургия //М.: ГЭОТАР МЕДИЦИНА. 1998. 352-С.
5. Gedebou Т. М., Neubauer W. Laparoskopic repair of bila-teral spigelian and inguinal hernias./ Surg.-Endosk. 1998. Vol. 12. N 12. P. 1424- 1425.
6. Obturator hernia: laparoscopic diagnosis and repair. //Haith L.R. Jr. , Simeone M.R., Reilly K.J. et al. //J-Soc-Laparoendosc-Surg. 1998. Vol.2 N 2. P. 191-193.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ГЕРНИОПЛАСТИКИ РЕЦИДИВНЫХ СКОЛЬЗЯЩИХ ПАХОВЫХ ГРЫЖ | 1992 |
|
RU2072796C1 |
| СПОСОБ ПЛАСТИКИ ПРИ ГРЫЖАХ ПЕРЕДНЕЙ БРЮШНОЙ СТЕНКИ | 2009 |
|
RU2407456C1 |
| СПОСОБ ЛЕЧЕНИЯ ГИГАНТСКИХ ВЕНТРАЛЬНЫХ ГРЫЖ | 1997 |
|
RU2127554C1 |
| Способ фиксации сетчатого трансплантата при лапароскопической герниопластике паховой грыжи | 2019 |
|
RU2704780C1 |
| СПОСОБ ПРЕДБРЮШИННОЙ ГЕРНИОПЛАСТИКИ ГРЫЖ ПАХОВОЙ ЛОКАЛИЗАЦИИ | 2000 |
|
RU2160562C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ЛАПАРОСКОПИЧЕСКОЙ ГЕРНИОПЛАСТИКИ | 2010 |
|
RU2435528C1 |
| СПОСОБ МИНИИНВАЗИВНОЙ ЛАПАРОСКОПИЧЕСКОЙ ПАХОВОЙ ГЕРНИОПЛАСТИКИ С ТРАСГЕРНИАЛЬНОЙ ФИКСАЦИЕЙ ИЗБИРАТЕЛЬНО АДГЕЗИВНОГО АЛЛОТРАСПЛАНТАТА | 2015 |
|
RU2580974C1 |
| СПОСОБ ОПЕРАТИВНОГО ЛЕЧЕНИЯ ПАХОВЫХ И БЕДРЕННЫХ ГРЫЖ КОСОПОПЕРЕЧНЫМ ПАХОВЫМ ПРЕДБРЮШИННЫМ МИНИДОСТУПОМ | 2004 |
|
RU2313292C2 |
| ВАРИАНТ "НЕНАТЯЖНОЙ" ГЕРНИОПЛАСТИКИ ПРИ СРЕДНИХ И БОЛЬШИХ ПОСЛЕОПЕРАЦИОННЫХ ГРЫЖАХ | 2007 |
|
RU2355328C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ | 2003 |
|
RU2279251C2 |
Изобретение относится к медицине, хирургии, может быть использовано при лечении наружных брюшных грыж. Устраняют грыжевой дефект. При этом перемещают здоровую брюшину и устанавливают дренаж-ирригатор в форме плоской спирали. В фазу репарации вводят по дренажу фиброноген с извлечением дренажа. Способ позволяет устранить грыжевой дефект путем формирования в зоне дефекта равномерного соединительного рубца. 3 ил.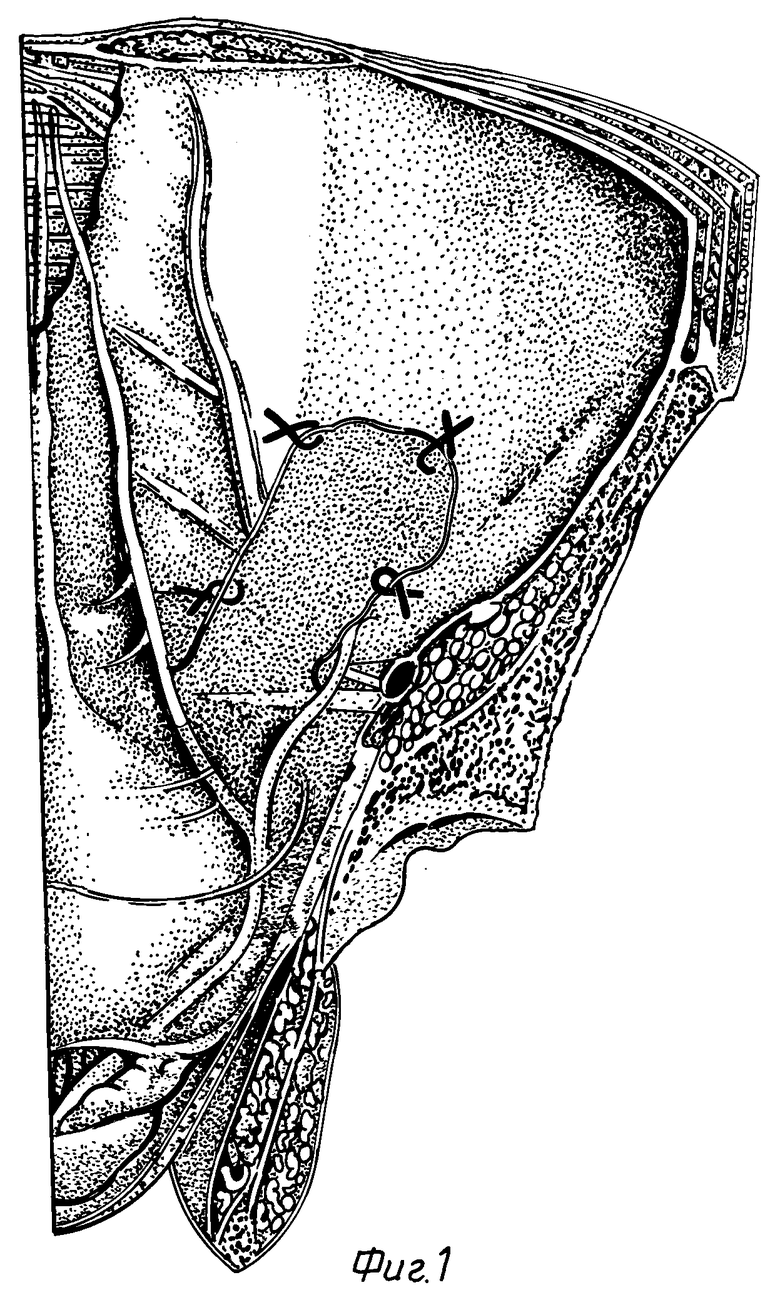
Способ лечения наружных брюшных грыж, отличающийся тем, что грыжевой дефект устраняют путем перемещения здоровой брюшины и установки дренажа-ирригатора в форме плоской спирали, а в фазу репарации вводят по нему фибриноген с извлечением дренажа.
| СПОСОБ ЛЕЧЕНИЯ ПАХОВЫХ ГРЫЖ У ДЕТЕЙ | 1994 |
|
RU2086189C1 |
Авторы
Даты
2001-02-27—Публикация
1999-10-18—Подача