Изобретение относится к медицине, а конкретно к хирургическим способам, и касается пластики дефекта нервного ствола.
Известно много различных способов, направленных на предотвращение спаек и рубцового сдавления трансплантата, являющегося одной из главных причин неблагоприятных исходов пластики нервных стволов. В известном по а.св. N 515511 способе оперативного лечения сухожилий и нервов конечностей используется полиэтиленовая трубка, в которую помещается поврежденный участок нерва. Однако полиэтиленовая трубка предотвращает образование рубцов только на время заживления раны, после чего она удаляется. В соответствии со способом хирургического лечения повреждений нервов нижней трети предплечья по а.св. N 1572560 восстановленный участок нерва помещают во вновь образованное мышечное ложе. Недостатком этого способа является невозможность применения его при обширных дефектах нервного ствола.
Наиболее близким к предлагаемому техническому решению является способ пластики дефекта нервного ствола, описанный В.Ковачевым с соавторами в ст. "Реконструкция обширных стволовых дефектов при помощи свободных васкуляризованных нервных трансплантатов", "Ортопедия и травматология", Т. XXVII 1990, кн. 4, с. 23.
Этот способ осуществляют путем формирования сосудисто-нервного комплекса из венозной магистрали вместе с паравазальными тканями и икроножным нервом. Далее этот комплекс переносится в дефект восстанавливаемого нервного ствола, выполняется шов трансплантата с концами нервного ствола, анастомозируется вена трансплантата с артерией реципиентной области.
Недостатком этого способа является возможность рубцового сдавления трансплантата вследствие рубцевания паравазальной клетчатки, особенно в условиях рубцовоизмененного ложа.
Задачей, не решение которой направлено предлагаемое техническое решение, является профилактика рубцового сдавления трансплантата.
Эта задача решается за счет того, что на первом этапе формируют трансплантат, заключая сосудисто-нервный комплекс в середину манжеты, образованной выкроенным из подлежащей собственной фасции голени фасциально-клетчаточным островковым лоскутом с сохранением его связей с икроножным нервом и веной и длиной, равной длине дефекта нервного ствола, пересекают икроножный нерв ниже дистального конца манжеты, а пересеченную на уровне основания пятой плюсневой кости вену анастомозируют с выделенной и пересеченной тыльной артерией стопы, а на втором этапе осуществляют разрез в проекции поврежденного нервного ствола с освобождением из рубцов его концов и в образовавшийся дефект переносят выделенный трансплантат с оставлением на его манжете фасциально-рубцового слоя и сосудистую ножку в виде артериализованной вены с последующим анастомозированием ее дистального конца с одной из магистральных артерий, а проксимального конца - с тыльной подкожной веной оперированной области.
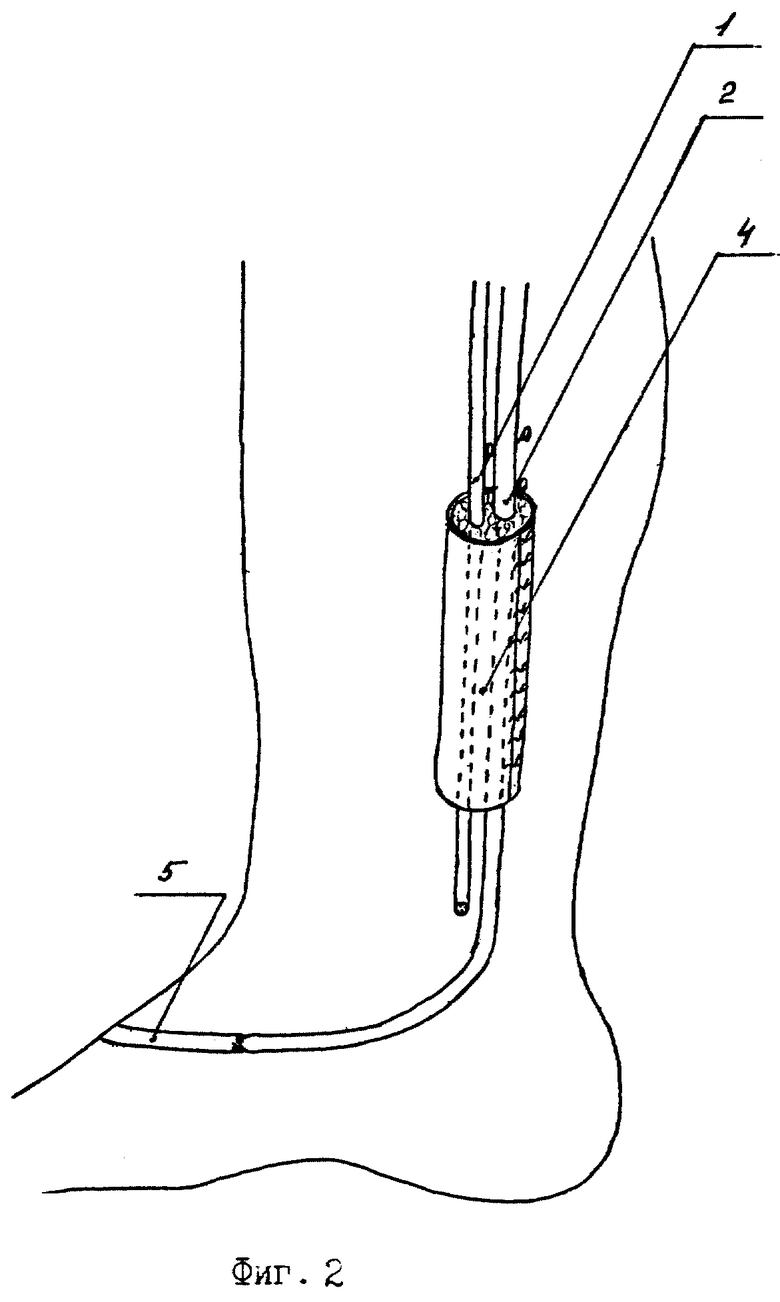
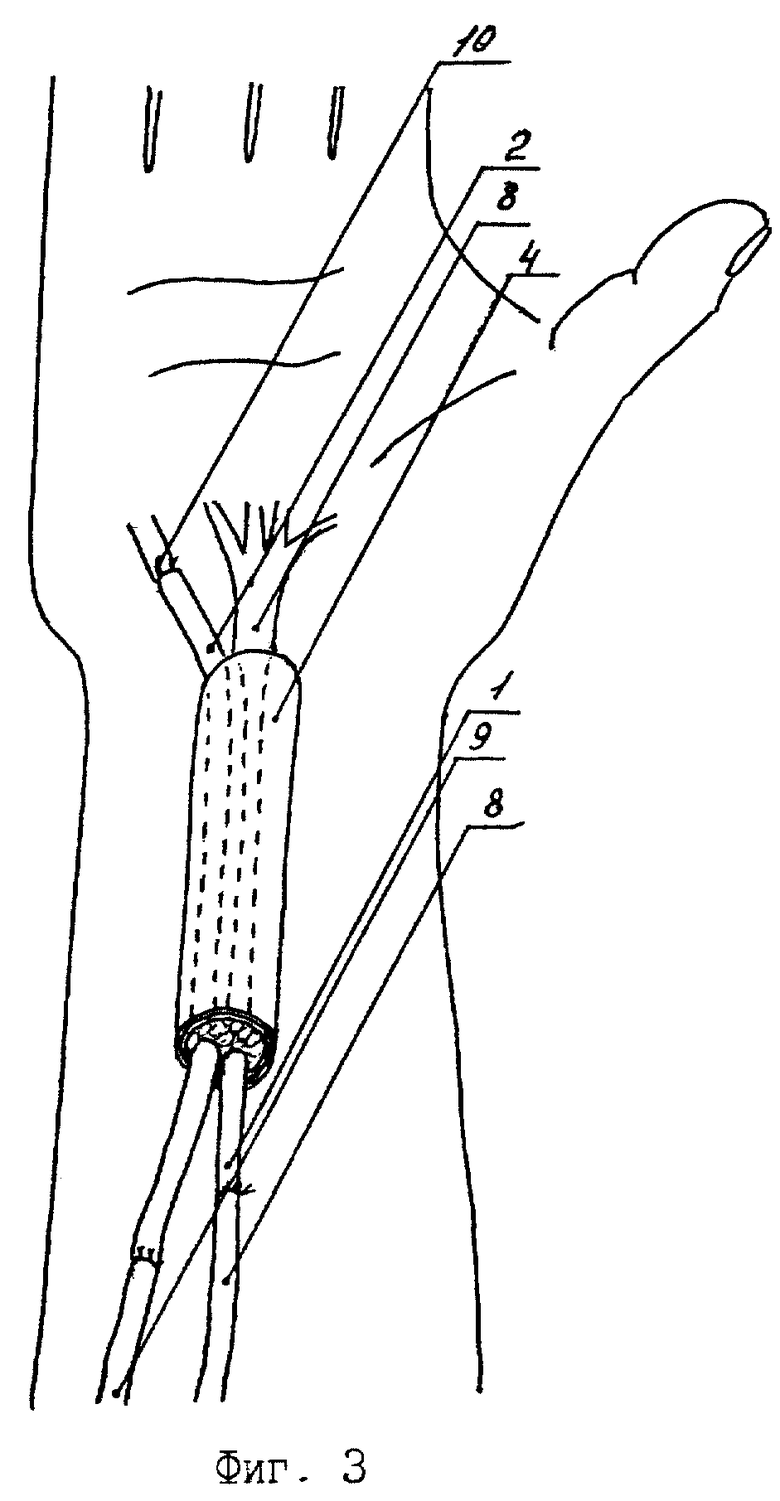
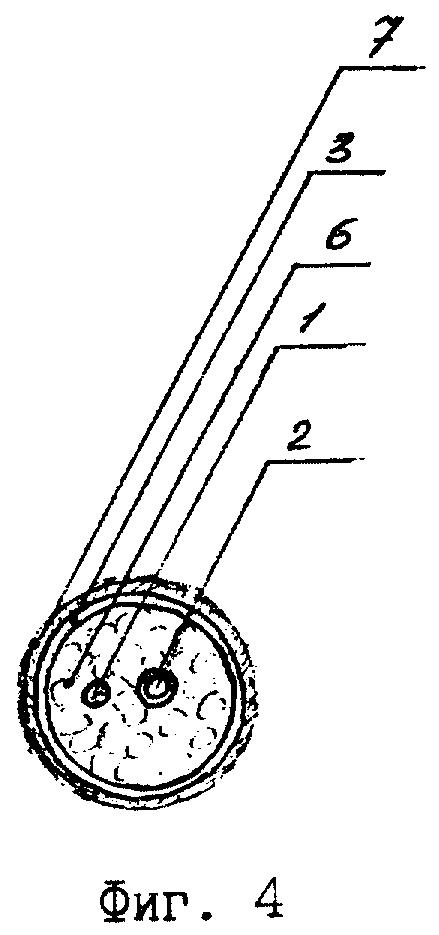
Сущность изобретения поясняется чертежами, где на фиг. 1 изображен I этап пластики, формирование фасциально-клеточного островкового лоскута, пересечение икроножного нерва, на фиг. 2 - I этап пластики, формирование манжетки из фасциально-клетчаточного лоскута с включением в нее икроножного нерва и вены, анастомозирование центрального конца вены с тыльной артерией стопы, на фиг. 3 - II этап пластики, пересадка сформированного комплекса в дефект нервного ствола, анастомозирование сосуда и икроножного нерва комплекса с соответствующими структурами реципиентной области, на фиг. 4 - II этап пластики, поперечный срез комплекса тканей, пересаженного в дефект нервного ствола.
Способ осуществляют следующим образом.
На I этапе формируют трансплантат. Для этого выполняют разрез кожи и подкожной клетчатки в проекции икроножного нерва по наружной поверхности голени и стопы. Икроножный нерв (1) и малая подкожная вена (2) выделяются единым блоком без нарушения сосудистых связей. Далее этот сосудисто-нервный комплекс заключают в середину манжеты (4), образованной выкроенным из подлежащей собственной фасции голени фасциально-клеточным островковым лоскутом (3) с сохранением его связей с икроножным нервом и веной и длиной, равной длине дефекта нервного ствола. Пересекают нерв ниже дистального конца манжеты, а вену - на уровне основания пятой плюсневой кости. На передней поверхности стопы выполняют послойный разрез кожи, выделяется и пересекается тыльная артерия стопы. Центральный конец вены проводится в подкожном тоннеле и выводится в рану, где анастомозируется с периферическим концом артерии (5). Рана послойно зашивается. Через 3 месяца после нормализации кровоснабжения в тканевом комплексе выполняется II этап операции - собственно пересадка сформированного трансплантата в дефект нервного ствола на предплечье. После выполнения разреза кожи по послеоперационному рубцу из рубцов выделяют трансплантат и сосудистую ножку, представленную артериализованной веной (2), причем на манжете (4) оставляют рубцовый слой. Таким образом, манжета становится трехслойной, состоящей из клетчаточного (6), фасциального (3) и рубцового (7) слоев. Пересекают икроножный нерв на уровне проксимального конца трубки, пересекают вену дистальнее и проксимальнее трубки. В случае наличия дефекта магистральной артерии на предплечье длина вены должна равняться длине недостающей части сосуда. Далее на предплечье выполняют разрез кожи в проекции поврежденного нервного ствола, выделяют из рубцов его концы (8) и в образовавшийся дефект нервного ствола переносят трансплантат. Сшивают между собой центральный и периферический концы нервного ствола и трансплантата, восстанавливают кровоток в трансплантате путем анастомозирования дистального конца вены (2) трансплантата с одной из магистральных артерий, а его проксимального конца - с тыльной подкожной веной кисти. При наличии дефекта магистрального сосуда центральный его конец (9) анастомозируется с дистальным концом вены (2), а периферический (10) - с проксимальным концом вены (2). Зашивают донорскую и реципиентную раны. Конечность иммобилизируют гипсовой лонгетой на 4 недели. Предлагаемым способом оперировано 8 больных.
Клинический пример.
Б-ой С-в Ю.С., 1952 г.р., находился в Нижегородском НИИТО по поводу дефекта лучевого края правой кисти, срединного нерва и локтевого сосудисто-нервного пучка, перерыва сухожилий сгибателей 2-5 пальцев на уровне средней трети предплечья.
При поступлении отмечается отсутствие первого пальца вместе с пястной костью, выпадение чувствительности 2-5 пальцев по ладонной поверхности, невозможность активного сгибания пальцев. Кроме того, определяется атрофия собственных мышц кисти. Предварительно у больного были восстановлены лучевой край кисти, сухожилия сгибателей пальцев и локтевой нерв. Первый этап пластики дефекта срединного нерва по разработанному способу выполнен 2.03.94 г., а второй этап - 13.05.94 г. При этом на втором этапе восстановлены срединный нерв и локтевая артерия путем пластики ее дефекта сосудистой ножкой трансплантата. Послеоперационное течение гладкое. Раны зажили первичным натяжением.
В отдаленные сроки после операции (до 1 года) определяется отчетливая пульсация на локтевой артерии. Отмечается также восстановление всех видов чувствительности в зоне иннервации срединного нерва, что значительно улучшило функциональные возможности кисти.
Во всех случаях применения способа достигнута адекватная чувствительность в зоне иннервации восстановленных нервов, не было отмечено признаков рубцового сдавления трансплантата.
Таким образом, использование для изоляции трансплантата от окружающих тканей хорошо кровоснабжаемой артериализованной манжеты предотвращает рубцовое перерождение трансплантата.
Пересадка трансплантата в два этапа обеспечивает переадаптацию его кровообращения к новым условиям функционирования, что повышает жизнестойкость тканей, в том числе и манжеты. Кроме того, при выполнении операции в 2 этапа на манжете формируется еще дополнительный рубцовый слой, что повышает ее каркасность и, соответственно, препятствует сдавлению трансплантата рубцами. При этом сам нервный трансплантат свободен от рубцов и окружен жировой клетчаткой на всем протяжении, что сохраняет его экстра-интраорганное кровоснабжение.
Кроме того, предлагаемый способ позволяет одновременно с восстановлением нерва восстановить и магистральную артерию предплечья, что улучшает кровоснабжение донорского ложа и условия регенерации нерва.
Перечисленные преимущества делают способ наиболее показанным в условиях рубцовых изменений тканей донорской области.
Способ достаточно прост, эффективен и может быть реализован в отделениях хирургии кисти, микрохирургии и травматологических, нейрохирургических клиниках, имеющих соответствующее оборудование.
Изобретение относится к медицине, в частности к хирургии, и может быть использовано при замещении дефекта нервного ствола. Формируют на первом этапе трансплантат с заключением сосудисто-нервного комплекса в середину манжеты. В комплекс включают икроножный нерв с малой подкожной веной в одном блоке. Манжету образуют из выкроенного из подлежащей собственной фасции голени фасциально-клетчаточного островкового лоскута. Лоскут выкраивают с сохранением его связей с икроножным нервом и веной и равной длине дефекта нервного ствола длиной. Затем пересекают икроножный нерв ниже дистального конца манжеты. Пересеченную на уровне основания пятой плюсневой кости вену анастомозируют с выделенной и пересеченной тыльной артерией стопы. На втором этапе осуществляют разрез в проекции поврежденного нервного ствола и освобождают из рубцов его концы. В дефект переносят выделенный трансплантат. При этом сохраняют на манжете фасциально-рубцовый слой и сосудистую ножку в виде артериализованной вены. Выполняют швы концов нервного ствола с соответствующими концами нерва трансплантата. Восстанавливают кровоток в трансплантате соединением вены трансплантата с реципиентной артерией. Способ позволяет профилактировать рубцовое сдавление трансплантата. 4 ил.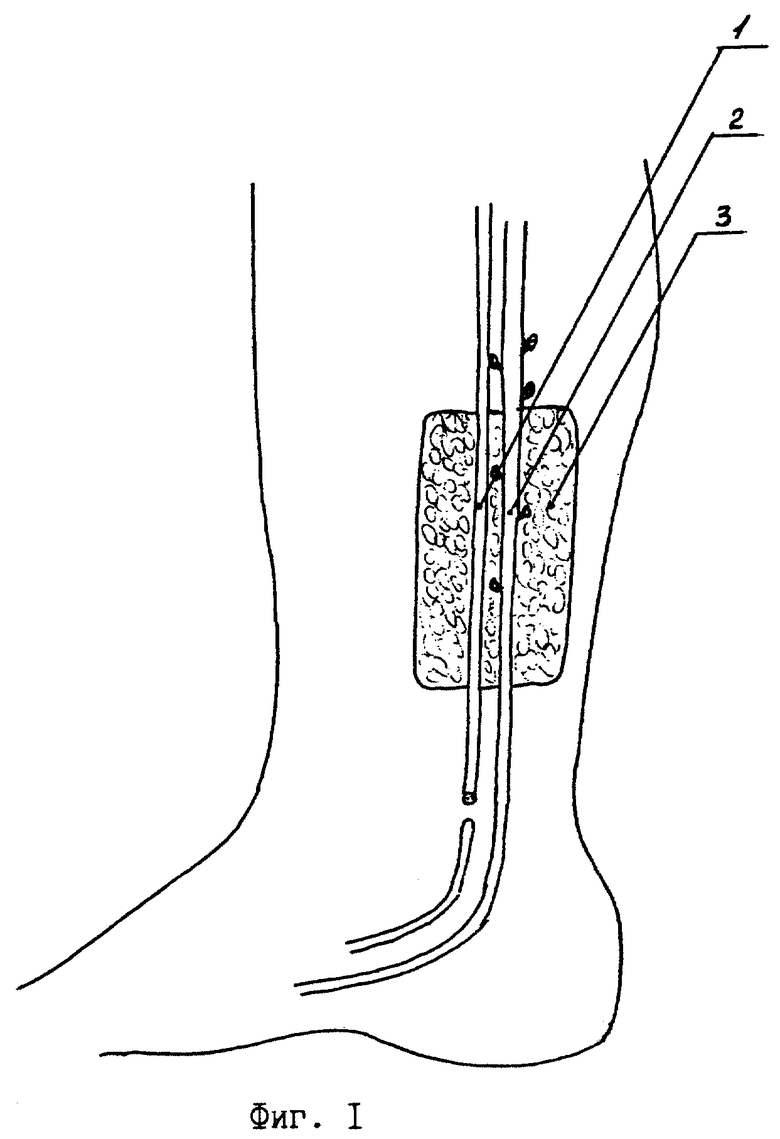
Способ пластики дефекта нервного ствола путем выделения трансплантата в виде сосудисто-нервного комплекса из икроножного нерва с малой подкожной веной в одном блоке, перенесения его в дефект нервного ствола с предварительным пересечением вены и икроножного нерва на дистальном и проксимальном уровнях и шва концов нервного ствола с соответствующими концами трансплантата и вены трансплантата с реципиентной артерией, отличающийся тем, что на первом этапе формируют трансплантат, заключая сосудисто-нервный комплекс в середину манжеты, образованной выкроенным из подлежащей собственной фасции голени фасциально-клетчаточным островковым лоскутом с сохранением его связей с икроножным нервом и веной и длиной, равной длине дефекта нервного ствола, пересекают икроножный нерв ниже дистального конца манжеты, а пересеченную на уровне основания пятой плюсневой кости вену анастомозируют с выделенной и пересеченной тыльной артерией стопы, а на втором этапе осуществляют разрез в проекции поврежденного нервного ствола с освобождением из рубцов его концов, в образовавшийся дефект переносят выделенный трансплантат с оставлением на его манжете фасциально-рубцового слоя и сосудистую ножку в виде артериализованной вены и восстанавливают кровоток в трансплантате.
| МИНДЕРИС М.В | |||
| Васкуляризованные трансплантаты нервов нижней конечности | |||
| Проблемы микрохирургии: Тезисы III Всесоюзного симпозиума | |||
| - Саратов, 1989, с.157-158 | |||
| 1979 |
|
SU825025A1 | |
| Способ лечения поврежденного периферического нерва | 1989 |
|
SU1804800A1 |
| Способ лечения вазоренальной гипертензии | 1987 |
|
SU1404063A1 |
| СПОСОБ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЯ ПЕРИФЕРИЧЕСКОГО НЕРВА | 1990 |
|
RU2028088C1 |
| САПИН М.Р | |||
| Анатомия человека, в 2-х тт | |||
| - М.: Медицина, 1993, т.2, с.190. | |||
Авторы
Даты
2001-12-10—Публикация
1998-10-21—Подача