Эта заявка является частичным продолжением патентной заявки США, серийный N 08/369786, поданной 6 января 1995 г., которая является частичным продолжением заявки, серийный N 08/234738, поданной 28 апреля 1994 г.
Предпосылки создания изобретения
Область изобретения
Это изобретение относится к аппаратам и процессам для использования паров перекиси водорода для стерилизации таких вещей, как медицинские инструменты, и более конкретно к использованию неорганического комплекса перекиси водорода для такого процесса.
Описание имеющего отношение к делу предшествующего уровня техники
Медицинские инструменты традиционно стерилизовались с использованием нагревания, такого, которое обеспечивается паром, или химических веществ, таких как формальдегид или окись этилена в газообразном состоянии или в виде пара. Каждый из этих методов имеет недостатки. Многие медицинские устройства, такие как устройства с оптическим волокном, эндоскопы, инструменты с энергопитанием и т.д., чувствительны к нагреванию, влаге или к тому и другому. Формальдегид и окись этилена - оба являются токсическими газами, которые представляют потенциальную опасность для работников здравоохранения. Проблемы, связанные с окисью этилена, особенно тяжелы, так как ее использование требует длительной аэрации для удаления газа из устройств, которые были простерилизованы. Это делает время цикла стерилизации нежелательно длительным. Кроме того, как формальдегид, так и окись этилена требует присутствия существенного количества влаги в системе. Таким образом, устройства, которые подлежат стерилизации должны увлажняться перед введением химического вещества, или химическое вещество и влага должны вводиться одновременно. Влага имеет значение при стерилизации с помощью ряда других химических соединений в газообразном состоянии или в виде пара, кроме окиси этилена или формальдегида, что показано в таблице 1.
Стерилизация с использованием паров перекиси водорода, как было показано, имеет некоторые преимущества над другими процессами химической стерилизации (смотрите, например, патенты США NN 4169123 и 4169124), а комбинация перекиси водорода с плазмой дает дополнительные преимущества, что раскрыто в патенте США 4643876. Как раскрыто в этих описаниях, пары перекиси водорода продуцируются из водного раствора перекиси водорода, что обеспечивает присутствие влаги в системе. Раскрытие в этих описаниях вместе с данными, обобщенными в таблице 1, указывают, что увлажнение необходимо для того, чтобы перекись водорода была эффективна в фазе пара или для проявления максимальной спороцидной активности. Однако использование водных растворов перекиси водорода для получения пара перекиси водорода для стерилизации может вызывать определенные трудности. При более высоком давлении, таком как атмосферное давление, избыток воды в системе может приводить к конденсации. Таким образом, необходимо снижать относительную влажность в стерилизационной емкости перед введением пара водной перекиси водорода.
Стерилизация изделий, содержащих области ограниченной диффузии, такие как длинные узкие просветы, представляет особое противопоказание для применения пара перекиси водорода, который получают из водного раствора перекиси водорода, так как:
1. Вода обладает более высоким давлением, чем перекись водорода, и будет испаряться быстрее, чем перекись водорода из водного раствора.
2. Вода имеет более низкий молекулярный вес, чем перекись водорода и будет быстрее диффундировать, чем перекись водорода в парообразном состоянии.
Из-за этого, когда водный раствор перекиси водорода выпаривается, вода первой достигает предметов, подлежащих стерилизации, и в более высокой концентрации. Водяной пар поэтому становится барьером для проникновения пара перекиси водорода в области ограниченной диффузии, такие как небольшие щели и длинные узкие просветы. Нельзя решить проблему путем удаления воды из водного раствора и использования более концентрированной перекиси водорода, так как концентрированные растворы перекиси водорода, т.е. больше 65% по весу, могут быть опасными из-за окислительной природы раствора.
В патентах США 4642165 и 4744951 предприняты попытки решить эту проблему. В первом раскрывается измерение небольшого добавления раствора перекиси водорода на нагретой поверхности для подтверждения того, что каждое добавление испаряется до того, как добавляется следующее количество. Хотя это помогает устранить различие в давлении паров и летучести между перекисью водорода и водой, это не направлено на тот факт, что вода диффундирует быстрее, чем перекись водорода в парообразном состоянии.
В последнем патенте описан процесс концентрации перекиси водорода из относительно разбавленного раствора перекиси водорода и воды и подача концентрированной перекиси водорода в форме пара в стерилизационную камеру. Процесс включает выпаривание основной части воды из раствора и удаление водяного пара, образованного перед инжекцией пара концентрированной перекиси водорода в стерилизационную камеру. Предпочтительный интервал для концентрированного раствора перекиси водорода находится в пределах от 50% до 80% по весу. Этот процесс имеет недостаток, состоящий в работе с растворами, которые находятся в опасном интервале, т.е. более 65% перекиси водорода, а также в том, что не удаляется вся вода из парообразного состояния. Так как вода все еще присутствует в растворе, она будет испаряться первой, диффундировать быстрее и достигать предметов, подлежащих стерилизации, первой. Этот эффект будет особенно выраженным в длинных узких просветах.
В патенте США 4943414 раскрывается процесс, в котором сосуд, содержащий небольшое количество выпариваемого жидкого стерилизующего раствора располагается в просвете, и стерилизующий раствор выпаривается и стекает прямо в просвет предмета, так как давление снижается во время цикла стерилизации. Эта система обладает тем преимуществом, что пары воды и перекиси водорода проталкиваются через просвет существующим дифференциалом давления, повышая скорость стерилизации для просветов, но она имеет тот недостаток, что нужно, чтобы сосуд примыкал к каждому просвету, который нужно простерилизовать. Кроме того, вода выпаривается быстрее и предшествует пару перекиси водорода в просвете.
В патенте США N 5008106 раскрывается, что по существу безводный комплекс ПВП и H2O2 применим для снижения количества микробов на поверхностях. Комплекс в виде тонкого белого порошка используется для получения антимикробных растворов, гелей, мазей и т.д. Он также может наноситься на марлю, ватные тампоны, губку и тому подобное. H2O2 выделяется при контакте с водой, присутствующей на поверхностях, содержащих микробы. Таким образом, при этом методе тоже необходимо присутствие влаги для эффекта стерилизации.
Сообщалось о некоторых неорганических комплексах перекиси водорода, включая примеры из следующих классов: карбонаты щелочных металлов и аммония, оксалаты щелочных металлов, фосфаты щелочных металлов, пирофосфаты щелочных металлов, фториды и гидроксиды. В патенте СССР N SU 1681860 (Никольская и др. ) раскрывается, что поверхности могут быть обеззаражены, хотя не обязательно простерилизованы, при применении пероксигидрата фтористого аммония (H4F • H2O2). Однако этот неорганический пероксидный комплекс обеспечивает обеззараживание только в очень узком интервале температур - 70-86oC. Даже в этом интервале время обеззараживания было достаточно продолжительным, необходимо, по крайней мере, два часа. Кроме того, известно, что фтористый аммоний разлагается на аммоний и фтористоводородную кислоту при температурах выше 40oC. Из-за ее токсичности и реактогенности фтористоводородная кислота является нежелательной в большинстве систем для стерилизации. Кроме того, у Николаевской и др. раскрывается, что несмотря на выделение из него 90% перекиси водорода при 60oC, NH4F H2O2 неэффективен при обеззараживании поверхностей при этой температуре. Таким образом, по-видимому другой фактор, а не перекись водорода ответственен за отмеченное обеззараживание.
Перекись водорода способна к образовыванию комплексов как с органическими, так и с неорганическими соединениями. Связи в этих комплексах относятся к водородным связям между богатыми электронами функциональными группами в комплексообразующем соединении и перекисью водорода. Эти комплексы применяли при коммерческом и промышленном использовании в качестве отбеливающих средств, дезинфектантов, стерилизующих средств, окисляющих реагентов при органическом синтезе и катализаторов для реакций полимеризации, индуцируемых свободными радикалами.
В основном, эти типы соединений были получены путем кристаллизации комплекса из водного раствора. Например, комплекс мочевины и перекиси водорода был получен Lu et al (J.Am. Chem Soc. 63(1):1507-1513 (1941)) в жидкой фазе путем добавления раствора мочевины к раствору перекиси водорода, и затем комплексу давали кристаллизоваться в соответствующих условиях. В патенте США N 2986448 описывается получение комплекса карбоната натрия и перекиси водорода путем обработки насыщенного водного раствора Na2CO3 раствором 50-90% H2О2 в закрытой циклической системе при 0-5oC в течение 4-12 часов. Совсем недавно в патенте США N 3870783 раскрыто получение комплекса карбоната натрия и перекиси водорода путем реакции водных растворов перекиси водорода и карбоната натрия в кристаллизаторе с непрерывным процессом или с периодической загрузкой. Кристаллы отделяются путем фильтрования или центрифугирования и жидкости используются для получения раствора карбоната натрия еще раз. Титова и др. (Журнал неорг.хим., 30: 2222-2227, 1985) описывают синтез пероксигидрата карбоната калия (K2CO3 • 3H2O2) путем реакции твердого карбоната калия с водным раствором перекиси водорода при низкой температуре с последующей кристаллизацией комплекса из этанола. Эти методики хорошо работают в отношении пероксидных комплексов, причем образуются стабильные кристаллические свободно текучие продукты из водного раствора.
В патентах США NN 3376110 и 3480557 раскрывается получение комплекса перекиси водорода с полимерным N-винилгетероциклическим соединением (ПВП) из водного раствора. Полученные в результате комплексы содержали различные количества перекиси водорода и существенные количества воды. В патенте США N 5008093 указывается, что свободно текучие, стабильные, в значительной степени безводные комплексы ПВП и H2O2 могли быть получены путем реакции суспензии ПВП и раствора H2O2 в безводном органическом растворителе, подобном этилацетату. Совсем недавно в патенте США N 5077047 описан коммерческий процесс получения продукта ПВП-перекиси водорода путем добавления тонко измельченных капелек 30-80% по весу водного раствора перекиси водорода к ожиженному слою ПВП, поддерживаемому при температуре от комнатной до 60oC. Как было обнаружено, полученный в результате продукт является стабильным, по существу безводным, свободно текучим порошком с концентрацией перекиси водорода 15-24%.
В патенте США N 5030380 описывается получение твердого полимерного электролитного комплекса с перекисью водорода путем сначала образования комплекса в водном растворе, а затем высушивания продукта реакции под вакуумом или путем распылительной сушки при достаточно низкой температуре, чтобы исключить термическое разрушение продукта.
Во всех этих предыдущих методах получения комплексов перекиси водорода используются растворы перекиси водорода. Или комплекс образуется в растворе, содержащем перекись водорода, или капельки раствора перекиси водорода распыляются в ожиженном слое реагирующего материала.
Реакции в паровой фазе или газообразной фазе - хорошо известные методы синтеза. Например, в патенте США N 2812244 раскрывается процесс взаимодействия твердого вещества и газа для дегидрогенизации, термического расщепления и деметанирования. Fujimoto et al. (J.Cotalisis, 133: 370-382 (1992)) описали карбоксилирование метанола в паровой фазе. Zellers et al. (Anal. Chem. , 62: 1222-1227 (1990)) рассмотрели реакцию стиренового пара с прямоугольно-плоским органоплатиновым комплексом. Эти предшествующие реакции в паровой и газообразной фазе, однако, не использовались для получения комплексов перекиси водорода.
Краткое изложение изобретения
Один аспект этого изобретения относится к аппарату для стерилизации предметов перекисью водорода. Этот аппарат включает контейнер для помещения предмета, подлежащего стерилизации, при давлении менее (50 Торр) 6,65 кПа. Предпочтительно давление равно менее (20 Торр) 2,66 кПа и более предпочтительно - менее (10 Торр) 1,33 кПа. Аппарат также включает источник пара перекиси водорода в жидкостной коммуникационной линии с контейнером. Источник включает неорганический комплекс перекиси водорода при температуре более 86oC и устроен так, что пар перекиси может контактировать с предметом для осуществления стерилизации. Источник может быть расположен внутри контейнера, или же иначе, аппарат может включать закрытое пространство, расположенное снаружи контейнера, в котором располагаются комплекс и входное отверстие, обеспечивающее движение жидкости между контейнером и закрытым пространством, так что пар, выделенный из комплекса, проходит через выходное отверстие и поступает в контейнер для осуществления стерилизации. Неорганический комплекс перекиси водорода может быть комплексом карбоната натрия, пирофосфата калия или оксалата калия. Предпочтительно, аппарат также включает нагреватель, расположенный внутри контейнера, посредством чего комплекс помещается на нагреватель и нагревается для того, чтобы облегчить выделение паров из комплекса. Такой нагреватель может нагреваться перед контактом с комплексом. Аппарат может также включать вакуумный насос в жидкостной коммуникационной линии с контейнером для опорожнения контейнера. В некоторых вариантах воплощения аппарат включает электрод, приспособленный для получения плазмы вокруг предмета. Такой электрод может быть внутри контейнера или может помещаться вне контейнера и приспособлен для направления потока генерируемой плазмы по направлению к предмету и вокруг него. В предпочтительном варианте воплощения комплекс находится в твердой фазе.
Другой аспект данного изобретения относится к способу стерилизации предметов парами перекиси водорода. Этот способ включает помещение предмета в контейнер и контактирование предмета с парами перекиси водорода, выделяемыми из неорганического комплекса перекиси водорода при нагревании комплекса со скоростью, по крайней мере, 5oC/мин для контакта с предметом и его стерилизации. Предпочтительно, скорость нагревания составляет, по крайней мере, 10oC/мин, более предпочтительно, по крайней мере, 50oC/мин и еще более предпочтительно, по крайней мере, 1000oC/мин. Комплекс предпочтительно содержит менее 10% воды. Комплекс может нагреваться предпочтительно до температуры более 86oC, чтобы облегчить выделение паров из комплекса. Газ из контейнера можно откачивать перед введением паров в контейнер при давлении менее (50 Торр) 6,65 кПа, более предпочтительно - менее (20 Торр) 2,66 кПа и еще более предпочтительно - менее (10 Торр) 1,33 кПа. По желанию плазма может генерироваться вокруг предмета после введения пара в контейнер. Плазма может генерироваться или внутри или снаружи контейнера. Данное изобретение также включает способ стерилизации предметов парами перекиси водорода, при котором используемый неорганический комплекс перекиси водорода является комплексом, который не разлагается с выделением галогеноводородной кислоты.
Еще один аспект данного изобретения относится к способу стерилизации предметов перекисью водорода с использованием самостерилизующейся ограниченной емкости. При этом способе предмет помещается в закрытый объем, содержащий неорганический комплекс перекиси водорода, ограниченная емкость герметически закрывается, и эту емкость оставляют при температуре ниже 70oC на время, достаточное для выделения пара перекиси водорода из комплекса и осуществления стерилизации предмета. Хотя и необязательно, емкость оставляют стоять при давлении менее атмосферного давления или при температуре выше комнатной температуры (23oC). Таким образом емкость оставляют при температуре ниже примерно 40oC. Может использоваться любой вид емкости, например мешок, контейнер, камера или комната. Предпочтительно комплекс перекиси водорода представлен в форме порошка или таблетки. Стадия герметизации может включать герметизацию ограниченной емкости газонепроницаемым материалом, таким как ТYVEKTM, обертка CSR или бумага.
Данное изобретение также относится к герметизируемой емкости, содержащей стерильный продукт и неорганический комплекс перекиси водорода, способный выделять пар перекиси водорода.
В данное изобретение включается также калийпирофосфатный комплекс перекиси водорода.
Еще один аспект изобретения касается способа стерилизации перекисью водорода предметов, имеющих внешний и узкий просвет в них. Этот способ включает соединение сосуда, содержащего неорганический пероксидный комплекс с просветом предмета, помещение предмета в контейнер, причем сосуд остается соединенным с просветом, снижение давления в контейнере и контакт просвета предмета с парами перекиси водорода, выделяемыми из неорганического комплекса перекиси водорода при температуре менее 70oC.
Краткое описание рисунков
ФИГУРА 1 является схематическим изображением аппарата для паровой стерилизации согласно данному изобретению.
ФИГУРА 2 является схематическим изображением аппарата для паровой стерилизации согласно данному изобретению, который включает электрод, который произвольно используется для генерации плазмы.
ФИГУРА 3A является схематическим изображением устройства, которое может использоваться для нагревания пероксидных комплексов.
ФИГУРА 3B является схематическим изображением предпочтительного контейнера для помещения источника пероксида для стерилизации по данному изобретению.
ФИГУРА 4 является графиком, показывающим выделение паров перекиси водорода из неустойчивого в вакууме неводного комплекса перекиси водорода.
ФИГУРА 5 является схематическим изображением системы регуляции давления, состоящей из сканирующего калориметра (ДСК), используемого для определения выделения перекиси водорода или свойств к разложению неорганических пероксидных комплексов по данному изобретению.
ФИГУРА 6 является графиком, показывающим действие давления на выделение перекиси водорода из калийоксалатного пероксидного комплекса.
ФИГУРА 7A является схематическим изображением гофрированной трубки для инжекции пара пероксида в камеру по данному изобретению перед инжекцией пара пероксида.
ФИГУРА 7B является схематическим изображением гофрированной трубки с фигуры 7A, показывающим нагреваемую плоскость в контакте с пероксидным комплексом во время инжекции.
Детальное описание изобретения
В стерилизаторах перекисью водорода, которые использовали в прошлом, неизменно применяли водный раствор перекиси водорода в качестве источника стерилизующего вещества в них. Эти стерилизаторы обладают недостатками, причиной которых служит наличие воды в системе. При более высоком давлении, таком как атмосферное давление, избыток воды в системе может приводить к конденсации. Это требует, чтобы производилась дополнительная стадия по снижению относительной влажности атмосферы в емкости, в которой производится стерилизация, до приемлемого уровня, перед тем как вводится пар перекиси водорода. Эти стерилизаторы также имеют недостатки, причина которых состоит в том факте, что вода, имеющая более высокое давление паров, испаряется более быстро, чем перекись водорода из водного раствора, и вода, имеющая меньший молекулярный вес, диффундирует быстрее, чем перекись водорода. Когда медицинское устройство или что-то подобное заключается в стерилизатор, первоначальное стерилизующее вещество из источника перекиси водорода, которое достигает устройства, разбавляется по сравнению с концентрацией в источнике. Разбавленное стерилизующее вещество может быть барьером для стерилизующего вещества, которое поступает позднее, особенно если устройство, подлежащее стерилизации, является предметом, таким как эндоскоп, который имеет узкие просветы. Использование концентрированного раствора перекиси водорода в качестве источника при попытке преодолеть эти недостатки является неудовлетворительным, так как такие растворы являются опасными.
В данном изобретении недостатки стерилизаторов на основе перекиси водорода предшествующего уровня техники преодолеваются путем использования по существу неводного (т.е. по существу безводного) источника перекиси водорода, который выделяет по существу безводные пары перекиси водорода. В предпочтительном варианте воплощения по существу безводный пар перекиси водорода продуцируется непосредственно из по существу неводного комплекса перекиси водорода. Однако по существу безводный пар перекиси водорода может также генерироваться из водного комплекса, который обрабатывается при выпаривании с целью удаления воды таким способом, как вакуум. Так, если используется водный комплекс перекиси водорода, водный комплекс может превращаться в по существу неводный комплекс перекиси водорода во время проведения процесса данного изобретения. Предпочтительно, по существу безводные комплексы перекиси водорода содержат менее примерно 20% воды, более предпочтительно - не более примерно 10% воды, еще более предпочтительно - не более примерно 5% воды и наиболее предпочтительно - не более примерно 2% воды.
Как видно из предпочтительного процентного содержания воды, в по существу неводных комплексах перекиси водорода, использованных в данном изобретении, как представлено выше, наиболее предпочтительный комплекс перекиси водорода и пар перекиси водорода, продуцируемый из него, по существу безводны. Тем не менее, как также видно из этих фигур, некоторое количество воды может присутствовать в этой системе. Некоторое количество этой воды может получаться от разложения перекиси водорода с образованием воды и кислорода в качестве побочных продуктов, и может происходить некоторое связывание этой воды водородной связью с этим комплексом.
Воздействие воды измерялось в серии тестов с помощью стерилизационной камеры с поддерживаемой различной относительной влажностью. Условия испытания были такими, какие описаны в примере 1, ниже, со спорами, содержащимися на пластинках из нержавеющей стали (НС) в просветах в нержавеющей стали 3 мм х 50 см. Как показано в таблице 2, в условиях испытания 5%-ная относительная влажность не влияет на эффективность, но 10%-ная относительная влажность снижает скорость стерилизации. Этот пример показывает, что небольшое количество влаги допустимо в системе с перекисью водорода, генерируемой из неводного пероксидного комплекса, и присутствие воды в системе может быть преодолено путем увеличения времени экспозиции.
Первичным критерием для композиции источника перекиси водорода является отношение между его стабильностью и скоростью выпаривания перекиси водорода как функцией температуры и давления. В зависимости от параметров процесса стерилизации, например давления, температуры и т.д., может быть предпочтительна более высокая или более низкая скорость выпаривания пероксида и нагревание источника пероксида может быть либо необходимо, либо ненужно. Необходимость нагревания пероксидного комплекса зависит от давления пара комплекса. Некоторые пероксидные комплексы обладают достаточно высоким давлением паров, таким, что значительное количества пара перекиси водорода может выделяться без нагревания комплекса. В основном нагревание комплекса увеличивает давление пара перекиси водорода и ускоряет выделение пероксида из комплекса.
Чтобы обеспечить желаемую высокую скорость испарения источник должен предпочтительно иметь большую площадь поверхности. Так, источник может быть тонко измельченным порошком или покрытием на материале, который имеет большую площадь поверхности. Конечно, безопасность, доступность и стоимость материала также являются важными критериями. Оценивали выделение перекиси водорода из комплексов перекиси водорода с мочевиной, поливинилпирролидоном, нейлоном-6, глициновым ангидридом и 1,3-диметилмочевиной. Комплексы перекиси водорода с мочевиной, поливинилпирролидоном, нейлоном-6 и глициновым ангидридом являются твердыми веществами. Комплекс 1,3-диметилмочевины и пероксида является жидкостью. Комплекс глицинангидрида и перекиси водорода является менее стабильным комплексом при пониженном давлении, чем другие оцениваемые комплексы, и в условиях вакуума большая часть перекиси водорода может выделяться из комплекса без необходимости дополнительного нагревания.
Комплекс мочевины и перекиси водорода можно приобрести в таблетированной форме у Fluka Chemical Corp., Ronkonkoma, NY и в порошкообразной форме у Aldrich Chemical Co. , Milwaukee, WI. Этот комплекс также известен как мочевины пероксид, комплекс перекиси водорода и мочевины, пероксид-мочевина, продукт соединения пероксида и мочевины, продукт соединения мочевины и пероксида, перкарбамид, карбамида пергидрат и карбамида пероксид. Как он использован здесь, термин "мочевины пероксид" охватывает все из предыдущих терминов.
Поливинилпирролидон-перекисноводородный комплекс (ПВП-H2O2) может быть получен с помощью метода, раскрытого в Международной патентной публикации N WO 92/17158. Или же комплексы с ПВП, с нейлоном-6, с 1,3-диметилмочевиной и с глицинангидридом, а также с другими органическими и неорганическими соединениями могут быть получены по методу, описываемому детально ниже.
Достижение соответствующих скоростей образования пара безводного пероксида из источника может облегчаться с помощью повышенных температур и/или пониженного давления. Таким образом, нагреватель для пероксидного источника и/или вакуумный насос для откачивания из стерилизационной камеры предпочтительно являются частями стерилизатора. Предпочтительно, источник покрывается слоем газопроницаемого материала, такого как ТYVЕКTM, нетканый полиэтиленовый материал, нетканый полипропиленовый, такой как SPUNGUARDTM, или подобный материал, который пропускает пары пероксида, но не пропускает образующий пероксидный комплекс материал. В качестве покрытия также мог бы использоваться перфорированный алюминий или другой подходящий перфорированный материал.
На фигуре 3А показано устройство 80, которое может использоваться для измерения выделения пероксида из комплексов перекиси водорода в условиях разных температур. В этом устройстве алюминиевый лоток 90 покрыт газопроницаемым слоем 92, таким как слой ТYVЕКTM медицинской марки. Лоток 90 помещен наверху нагревающего лотка 94, который помещается в пирексном лотке 96. Термопарный термометр 98 помещается снаружи лотка 90, примерно в 1 сантиметре от его дна.
Предпочтительный контейнер 99 для помещения источника пероксида показан на фигуре 3B. Контейнер 99 состоит из металлической пластины 100, например алюминиевой пластины с произвольным присоединенным нагревателем, используемым для нагревания твердого пероксидного комплекса. Индикатор температуры 101, такой как термометр, может помещаться на пластине 100 для контроля температуры, пероксидный комплекс помещается непосредственно на пластине 100. Или же, чтобы обеспечить равномерное нагревание всего пероксидного комплекса, пероксидный комплекс может помещаться между одним или более алюминиевыми экранами 102, 104, помещенными сверху пластины 100. Алюминиевые экраны 102, 104 обеспечивают большую площадь поверхности и равномерное нагревание комплекса, когда нужно использовать большие количества пероксидного комплекса. Пероксидный комплекс или экран или экраны 102, 104 затем покрывают слоем газопроницаемого материала 106, таким как слой материала медицинской марки ТYYЕКTM или SPUNGUARDTM, так что перекись водорода, выделяемая комплексом, проходит через покрытие 106 перед диффузией в остальную часть камеры. Перфорированная алюминиевая пластинка по желанию помещается сверху слоя ТYVEKTM или SPUNGUARDTM 106 для обеспечения давления для удерживания комплекса в контакте с нагреваемой пластиной 100 и для обеспечения равномерного нагревания пероксидного комплекса.
Описанное выше устройство обеспечивает равномерное прогревание комплекса, что дает в результате повышенное количество пара перекиси водорода, выделяющегося из пероксидного комплекса.
На фигуре 1 схематически изображен аппарат данного изобретения для стерилизации парами перекиси водорода. Камера 10 вмещает предмет 12, который нужно простерилизовать, и который для удобства помещен на полку 14. Дверь 16 обеспечивает доступ во внутреннюю часть камеры 10. Неводный источник перекиси водорода 18 помещается на произвольный нагреватель 20, который настраивается регулятором температуры 22. Концентрация пероксида может контролироваться с помощью произвольного детектора 24. Если желательно, из камеры 10 можно производить откачивание, используя насос 26, однако стерилизация может выполняться при атмосферном давлении.
Контейнер, в котором помещаются предметы, подлежащие стерилизации, может быть обычной стерилизационной камерой, из которой производится откачивание, или он может быть контейнером (или комнатой) с атмосферным давлением.
Время, необходимое для стерилизации предметов, зависит от природы, числа и упаковки предметов и их размещения в камере. Как альтернатива, может быть необходимо простерилизовать саму камеру (или внутреннее пространство комнаты). В любом случае оптимальное время стерилизации может быть определено эмпирически.
Применение пульсации давления для увеличения проникновения и антимикробного действия стерилизующих газов, которое известно в области стерилизации, также может применяться при процессе с неводной перекисью водорода. Как описано более детально здесь ниже, для дополнительного повышения активности может также использоваться плазма.
В заключение процесса стерилизации избыток перекиси водорода может быть удален из устройств, которые имеют сродство к пероксиду путем замены воздуха, контактирующего с этими устройствами. Это может быть осуществлено путем продувки теплого воздуха над устройствами в течение продолжительного времени или путем откачивания камеры.
Предметы, которые предварительно были простерилизованы воздействием паров перекиси водорода, можно также подвергать воздействию плазмы для удаления остаточной перекиси водорода, которая может сохраняться на предметах. Так как перекись водорода разлагается на нетоксичные продукты во время обработки плазмой, простерилизованные предметы могут использоваться без необходимости любых дополнительных стадий.
Может быть желательно изолировать источник пероксида от стерилизатора после того, как пары пероксида выделились, чтобы избежать реабсорбции паров или, когда используется плазма, для исключения экспозиции источника с плазмой. Изоляция также благоприятна, когда используемый комплекс нестабилен в вакууме. Изоляция может выполняться с использованием клапанов или других изолирующих устройств, хорошо известных в этой области техники.
На фигуре 2 схематически изображена система данного изобретения для стерилизации плазмой перекиси водорода. Стерилизация может достигаться с применением плазмы или без этого. Плазма может применяться для повышения спороцидной активности паров пероксида и/или для удаления какого-либо остаточного количества перекиси водорода, сохраняющегося на простерилизованных предметах.
Стерилизация проводится в камере 30, которая имеет дверь или отверстие 32, через которые могут вводиться предметы, подлежащие стерилизации. Камера 30 имеет выходное отверстие 34 для вакуумного насоса 36, через которое производится откачивание из камеры. Выходное отверстие 34 имеет клапан 38 для изоляции камеры от вакуумного насоса 36. Камера 30 также имеет входное отверстие 40, соединенное с отгороженной емкостью 42, которая содержит комплекс перекиси водорода. Входное отверстие имеет клапан 44, который позволяет изолировать емкость 42 от камеры. Система стерилизации также имеет входное отверстие 41, которое соединяет емкость 42 и вакуумный насос 36, который имеет клапан 43. Эта система дает возможность одновременного откачивания как из емкости 42, так и из камеры 30 или независимого откачивания из емкости 42 или камеры 30. Откачивание регулируется с помощью открывания и закрывания клапанов 38, 44 и 43. Как будет ясно специалисту, в этой системе можно было бы использовать два насоса, по одному для каждой камеры.
Емкость 42 содержит произвольный нагреватель 49, соединенный с регулятором температуры 46 для регуляции температуры комплекса перекиси водорода. Концентрация комплекса перекиси водорода в парообразном состоянии может контролироваться с помощью произвольного детектора пероксида 48. Внутри камеры имеется радиочастотный (РЧ) электрод 50, который присоединен к соответствующей сети 52 и РЧ источнику энергии 54. Обычной формой для электрода является перфорированный цилиндр, окружающий образцы и открытый с обоих концов. Обычная операция данного процесса состоит в следующем:
1. Предметы 56, подлежащие стерилизации, помещают в камеру 30.
2. Камера 30 может находиться при атмосферном давлении или же может быть откачана для облегчения проникновения перекиси водорода. Откачивание выполняется с помощью открывания клапана 38 и включения вакуумного насоса 36. Или же как камера 30, так и емкость 42 можно откачивать с помощью открывания клапанов 38 и 44 и/или 43.
3. Клапаны 38 и 43 закрываются для изоляции вакуумного насоса 36 от камеры 30 и емкости 42, а клапан 44 открывается. Пары перекиси водорода поступают в камеру 30 из источника перекиси водорода, который может нагреваться для облегчения выделения паров перекиси водорода. По желанию могут также добавляться воздух или инертный газ.
4. Предметы 56, подлежащие стерилизации, обрабатывают или парами пероксида до полной стерилизации, или предварительно обрабатывают парами пероксида в камере 30 до того, как генерируется плазма с достаточной энергией для стерилизации. Если необходимо, камера 30 может быть откачена в это время для облегчения получения плазмы. Продолжительность периода предплазменной выдержки зависит от типа использованной упаковки, природы и числа предметов, подлежащих стерилизации, и расположения предметов в камере. Оптимальное время определяется эмпирически.
5. Предметы 56 подвергаются воздействию плазмы с помощью подведения энергии от источника РЧ энергии 54 к РЧ электроду 50. РЧ энергия, применяемая для генерации плазмы, может быть пульсирующей или непрерывной. Предметы 56 остаются под воздействием плазмы на срок для проведения полной стерилизации и/или для удаления остаточной перекиси водорода. При некоторых осуществлениях применяется 5-30 минутное воздействие плазмы. Однако оптимальное время может быть определено эмпирически.
Когда в данном описании и формуле изобретения используется термин "плазма", подразумевается, что он включает обозначение любого количества газа или пара, который содержит электроны, ионы, свободные радикалы, диссоциированные и/или возбужденные атомы или молекулы, продуцируемые в результате приложенного электрического поля, включая любое сопутствующее облучение, которое могло бы быть получено. Налагаемое поле может охватывать широкую полосу частот; однако обычно используются радиочастоты или микроволны.
Система подачи неводной перекиси водорода, раскрытая в данном изобретении, может также применяться с плазмами, генерируемыми по методу, раскрытому в ранее упомянутом патенте США N 4643876. Или же она может применяться с плазмами, описанными в патенте США N 5115166 или 5087418, в которых предметы, подлежащие стерилизации, помещаются в камеру, которая отделяется от источника плазмы.
Устройство, описанное выше, дает особые преимущества, когда используются пероксидные комплексы, нестабильные в условиях вакуума. Существует, по крайней мере, два возможных метода, которые могут использоваться для снижения до минимума потери перекиси водорода во время стадии вакуумирования. Во-первых, небольшая камера может быть вакуумирована независимо. Во-вторых, если используется достаточно небольшая камера, совсем нет необходимости откачивать небольшую камеру.
Одним из таких нестабильных неводных пероксидных комплексов является глицинангидрид-пероксид. Это соединение выделяет пары перекиси водорода при помещении в условия вакуума. Фигура 4 является графиком, иллюстрирующим выделение паров перекиси водорода из глицинангидридпероксидного комплекса в условиях вакуума. Процедура, используемая для выделения перекиси водорода из глицинангидридного комплекса, состоит в следующем: (1) основную камеру 30 откачивали при закрытых клапанах 43 и 44. (2) Камеру 42, содержащую комплекс перекиси водорода, откачивали при закрытых клапанах 38 и 44 и открытом клапане 43. (3) Клапан 43 закрывали и клапан 44 открывали и давали парам перекиси водорода заполнить камеру 30.
Как продемонстрировано с помощью графика, пары перекиси водорода выделяются из комплекса по мере того, как давление снижается даже без дополнительного нагревания. Как показано на фигуре 4, выделение паров пероксида значительно повышается при нагревании комплекса до более высокой температуры. Таким образом, даже нестабильные пероксидные комплексы применимы при методе стерилизации данного изобретения.
Данное изобретение дает, по крайней мере, четыре преимущества над более ранними системами стерилизации перекисью водорода:
1. Позволяет обойтись без использования концентрированных потенциально опасных растворов перекиси водорода.
2. Устраняется необходимость предварительно снижать относительную влажность мест, подлежащих стерилизации, с целью предотвращения конденсации.
3. Вода по существу устраняется из системы, так что существует слабая конкуренция между водой и перекисью водорода по диффузии в длинные узкие просветы.
4. Часто может быть исключена необходимость соединения со специальными сосудами для доставки стерилизующих газов в длинные узкие просветы.
То, что стерилизация может производиться с использованием паров перекиси водорода при значительном отсутствии влаги - является одним из неожиданных открытий данного изобретения. Предшествующий опыт в данной области показывает, что присутствие воды необходимо для достижения стерилизации при процессах стерилизации химическими веществами в газообразном или парообразном состоянии. Преимущество состоит в том, что по данному изобретению вода по существу удаляется из системы, что дает в результате более быструю, более эффективную и рациональную стерилизацию.
Эффективность стерилизации различными неводными комплексами перекиси водорода определяли, как описано ниже в примерах 1-4.
Пример 1
Данные по эффективности были получены относительно паров перекиси водорода, выделяемых из по существу безводного мочевинопероксидного комплекса с использованием спор Bacillus subtilis var (niger) в просветах в металле или пластике TEFLONTM в качестве биологической пробы.
А. Процедуры испытания
1. Оборудование
Четыре грамма раздробленной таблетки продукта соединения перекиси водорода и мочевины (Fluka Chemical Corp., Ronkonkoma, NY) помещали на алюминиевый лоток 90, который показан на фигуре 3A. Сверху лоток 90 покрывали ТYVEKTM 92 медицинской марки (прессуемый штапельного плетения полиэтиленовый материал), так что любое количество перекиси водорода, выделившееся из комплекса должно пройти через покрытие ТYVEKTM, перед диффузией в остальные части камеры. Алюминиевый лоток 90 помещали на нагревающую пластину 94 в пирексной тарелке 96, расположенной на дне алюминиевой стерилизационной камеры (смотрите фигуру 1). Стерилизационная камера, которая имела примерный объем 173 литра, также содержала:
- детектор перекиси водорода для измерения концентрации перекиси водорода в паровой фазе,
- регулятор температуры для регулирования температуры нагревающей пластины,
- отверстие для введения, через которое в камеру могла бы вводиться жидкая перекись водорода,
- металлическую полку, на которую помещали пластиковый поднос, содержащий устройства с просветами для испытания,
- электрические обогреватели снаружи стенок камеры, которые поддерживали температуру в камере на уровне 45oC во время испытаний эффективности.
2. Биологическая проба и испытание
Для оценки эффективности системы доставки неводного пероксида биологическую пробу, состоящую из 1,04 • 106 спор B. subtilis var. (niger), на лезвии скальпеля из нержавеющей стали помещали на одинаковом расстоянии от каждого конца просветов в нержавеющей стали с размерами 3 мм ВД х 40 см длины, 3 мм ВД х 50 см длины и 1 мм ВД х 50 см длины. Эти ВД и длины являются типичными для просветов в металле, используемых в медицинских устройствах. Отделение в середине каждого просвета, которое содержало часть биологической пробы, имело размеры 13 мм ВД х 7,6 см длины. В биологическом испытании с просветами в металле, в целом, оценивали 9 просветов на испытание. В это число входило 3 просвета из каждого из 3 разных наборов ВД и длин, имеющихся в наличии.
Сходные тесты проводили с биологическими пробами, состоящими из 4,1 • 105 спор B.subtilis var (niger), на бумажной полоске (6 мм х 4 мм бумаги для хроматографии Ватман # 1), помещенной на одинаковом расстоянии от концов просветов в ТефлонеТМ с размерами 1 мм ВД х 1 метр в длину, 1 мм ВД х 2 метра в длину, 1 мм ВД х 3 метра в длину, 1 мм ВД х 4 метра в длину. Центральный отдел этих просветов, который содержал часть биологической пробы, имел размеры 15 мм ВД х 7,6 см в длину. При биологическом испытании с просветами в ТефлонеТМ оценивалось в целом 12 просветов на испытание, 3 просвета на каждую из 4 различных представленных длин.
Просветы, содержащие образцы биологической пробы помещали на пластиковый поднос, который затем помещали на полку
в стерилизационной камере. Дверь камеры затем закрывали и камеру вакуумировали до давления (0,2 Торр) 26,6 Па с помощью вакуумного насоса. Алюминиевый лоток, содержащий продукт соединения перекиси водорода и мочевины, затем нагревали до 80-81oC в течение 5 минут, что измеряли с помощью термопары термометра, помещенной на стороне стенки алюминиевого лотка примерно в 1 см от дна лотка. В течение этого времени концентрация перекиси водорода в камере увеличивалась до 6 мг/л, что измеряли с помощью детектора пероксида.
Образцы для биологического испытания выдерживали в парах перекиси водорода в течение сроков, равных 5, 10, 15, 20 и 25 минутам. После экспозиции в парах перекиси водорода образцы для биологического испытания асептически переносили в 15 мл триптиказного соевого бульона, содержащего 277 единиц каталазы, для нейтрализации остаточной перекиси водорода, которая может оставаться на испытуемых образцах. Все образцы инкубировали в течение 7 дней при 32oC и просматривали на наличие роста.
Провели также сравнительные исследования, в которых в стерилизационную камеру вводили 50% водный раствор перекиси водорода и выпаривали из нагреваемого инжектора (нагреваемая металлическая поверхность). Вводимый объем раствора перекиси водорода создавал концентрацию перекиси водорода в паровой фазе, равную 6 мг/л. Образцы просветов для испытания и биологические пробы в этих испытаниях были идентичными тем, которые использовались при тестах с неводной перекисью водорода. Работа с образцами для биологических испытаний после экспозиции с перекисью водорода также была идентичной.
В. Результаты испытаний
Результаты этих испытаний с просветами в нержавеющей стали и ТефлонеТМ представлены в таблицах 3 и 4 соответственно, и показывают преимущества системы доставки неводного пероксида в отношении обработки просветов как в металле, так и в неметаллическом материале. В целом гибель спор бактерий достигалась в течение 5 минут с помощью системы доставки неводного пероксида для просветов с наименьшим БД и наибольшей длины. В то же время полная гибель не достигалась даже через 25 минутный срок диффузии при применении 50% раствора перекиси водорода.
Тот факт, что может производиться быстрая стерилизация в отсутствие существенных количеств воды, является неожиданным в свете того факта, что влага обычно присутствовала во время химической стерилизации другими различными стерилизующими веществами в газовой/паровой фазе, а не перекисью водорода. Так как в системах стерилизации перекисью водорода в паровой фазе использовались растворы перекиси водорода, в этих системах также присутствовала влага.
Для определения эффективности стерилизации различными другими пероксидными комплексами были выполнены следующие эксперименты.
Примеры 2, 3 и 4
Для определения эффективности комплекса поливинилпирролидона с перекисью водорода (пример 2), комплекса нейлона 6 и перекиси водорода (пример 3) и комплекса 1,3-диметилмочевины и перекиси водорода (пример 4) использовался аппарат примера 1. Эти соединения были синтезированы по методу, описанному ниже в примерах 12 и 13. Параметры испытания были следующими (см. пример в конце описания).
В каждом случае носителями спор были субстраты в виде полосок бумаги 6 мм х 4 мм в просветах в пластике и лезвия из нержавеющей стали. Результаты этого испытания эффективности представлены ниже в таблице 5.
Результаты, представленные в таблице 5, показывают, что каждый из испытанных комплексов пероксида водорода продуцирует пар пероксида, который обеспечивает достаточную стерилизацию только через пять минут экспозиции.
Температура, необходимая для выделения пара перекиси водорода из твердого комплекса, которая представлена выше, является температурой, измеренной с помощью термопарного термометра, расположенного на наружной стороне алюминиевого лотка примерно в 1 сантиметре от дна лотка. Дополнительное испытание с использованием термометра, такого как флюороптический термометр, помещенного на внутренней стороне дна лотка, показало, что температура на дне лотка была примерно на 30-35oC выше, как описано в примере 5, ниже. Таким образом, в предыдущем примере температура на дне лотка была примерно 110-115oC, когда термопарный термометр показывал 80oC, а температура на дне лотка была примерно 140-145oC, когда термопарный термометр показывал 110oC.
Пример 5
Чтобы определить температуру на дне алюминиевого лотка, использованного для помещения твердого пероксидного комплекса, флюороптический термометр присоединяли к внутренней стороне дна алюминиевого лотка. Термопарный термометр ОмегаТМ помещали на наружной стороне алюминиевого лотка примерно в 1 см от дна лотка. Снимали три разные показания термометров. Каждый раз лоток нагревали до желаемой температуры, показываемой термометром, помещенным сбоку лотка, давали остыть и затем снова нагревали до желаемой температуры. Зарегистрированные температуры перечислены ниже (см. табл. А).
Результаты показывают, что температура на дне алюминиевого лотка была примерно на 30-35oC выше, чем температура, показываемая термопарным термометром, расположенным сбоку лотка.
Кроме того, испытание проводили для сравнения данных по эффективности, полученных с использованием водного и неводного источников пероксида в открытой системе (без просветов). Эксперименты описаны более детально ниже.
Пример 6
Аппарат из примера 1 использовали с биологической пробой, которая состояла из 6,8 • 105 спор B subtilis var (niger) на полоске 6 мм х 4 мм хроматографической бумаги Ватман # 1, упакованной в конверт из ТYVEKTM/MYLARTM (TYVEKTM является газопроницаемой тканью, изготовленной из полиэтилена. MYLARTM является газонепроницаемым полиэфирным материалом). Упакованные полоски биологической пробы помещали перед, в середине и сзади полифениленоксидного подноса, на котором помещался гибкий волоконно-оптический сигмоидоскоп. Поднос помещали в полифениленоксидный контейнер, который имел отверстие наверху и два отверстия на дне для обеспечения распространения пара. Отверстия диаметром в четыре дюйма (10,16 см) были покрыты пропускающим газы полипропиленовым упаковочным материалом (SPUNGUARDTM обертка для строгорежимной стерилизации, Kimberly-Clark, Dollas, TX) для сохранения стерильности содержимого контейнера после стерилизации. Контейнер помещали в аппарат из примера 1 и давление в камере снижали до (0,2 Торр) 26,6 Па. Затем алюминиевый лоток, содержащий 2 грамма продукта соединения перекиси водорода и мочевины (Fluka Chemical corp.), нагревали до 80-81oC, что измеряли с помощью термопары, помещенной на наружной стороне алюминиевого лотка примерно в 1 см от дна алюминиевого лотка, в течение 5 минут для получения 3 мг/л паров перекиси водорода в камере. Образцы для биологического испытания выдерживали в парах перекиси водорода в течение сроков 5 и 10 минут. После экспозиции с испытуемыми образцами обращались так же, как и с образцами в примере 1.
Проводили также сравнительные исследования, в которых в стерилизационную камеру вводили 50% водный раствор перекиси водорода и выпаривали из нагретого инжектора. Вводимый объем раствора перекиси водорода создавал концентрацию в паровой фазе, равную 3 мг/л. Форма испытания, состав образцов для биологического испытания и работа с образцами для биологического испытания после экспозиции были идентичны тем, которые использовались в испытаниях с неводной перекисью водорода. Результаты этих испытаний представлены в таблице 6.
Результаты этих испытаний показывают более высокую эффективность процесса с неводной по сравнению с водной перекисью водорода в "открытой" системе, в которой биологический образец не помещается в просвет. К тому же неожиданно было обнаружено, что неводная система обеспечивала превосходную стерилизацию, даже когда не нужна диффузия перекиси водорода в длинные и узкие просветы. Это наводит на мысль, что способ действия перекиси водорода не одинаков для систем с водой и без нее.
Проводилось дополнительное испытание для определения эффективности паров неводного пероксида при нормальном, несниженном давлении. Это испытание детализировано ниже.
Пример 7
Испытания по эффективности проводили с парами перекиси водорода, выделяемыми комплексом мочевины и пероксида в открытой системе при атмосферном давлении. При этом испытании биологическую пробу из 1,04 • 106 спор B.subtilis var. (niger) на хирургических лезвиях из нержавеющей стали упаковывали в конверт из TYLEKTM/MYLARTM. Упакованные лезвия с биологической пробой помещали перед, в середине и сзади подноса из полифениленоксида. Поднос помещали в аппарат из примера 1 и дверь камеры закрывали. Алюминиевый лоток, содержащий 4,0 г пероксидмочевины (Fluka Chemical corp.), нагревали до 80-81oC, что измерялось с помощью термопарного термометра, помещенного сбоку алюминиевого лотка примерно в 1 см от дна лотка, в течение всего этого испытания. Образцы биологического теста выдерживали в парах перекиси водорода в течение сроков, равных 5, 10, 20 и 30 минутам. После экспозиции с испытуемыми образцами работали таким же образом, как и в примере 1. Результаты этих испытаний представлены в таблице 7, и они показывают эффективность процесса с неводным пероксидом в открытой системе при атмосферном давлении.
Проводились дополнительные испытания для определения примерного количества пероксида, выделяемого из комплекса перекиси водорода и мочевины при различных температурах. Это испытание описано в примере 8.
Пример 8
Порошок пероксидмочевины, полученный при дроблении коммерчески доступных таблеток (Fluka Chemical corp.), помещали между двумя алюминиевыми экранами в аппарате по фигуре 3B, имеющими размеры 12,7 см х 12,7 см. Алюминиевую пластинку затем нагревали и температуру контролировали, используя термометр, расположенный у угла алюминиевой пластинки. В таблице 8 перечислено примерное процентное количество, выделяемое при разных температурах после нагревания в течение пяти минут. Данные показывают, что примерно 100% пероксида выделяется при более низких температурах.
Пероксидные комплексы, обладающие способностью выделять пары перекиси водорода при комнатной температуре и атмосферном давлении, такие как комплекс мочевины и перекиси водорода, позволяют им быть эффективными для использования при различном применении для стерилизации. Они могут использоваться не только в аппарате для стерилизации данного изобретения, описанном выше, соединения данного изобретения могут также использоваться как часть самостерилизующих упаковочных материалов или применяться на носителях, таких как марля, губка, вата и тому подобное. Эти соединения дают возможность стерилизации запаянных упаковок при комнатной температуре или при повышенных температурах и особенно полезны для стерилизации упакованных медицинских и хирургических изделий.
Конкретное применение соединений данного изобретения описано в примерах, которые следуют ниже. Пероксидным комплексом, использованным в следующих примерах, была пероксидмочевина в форме таблеток (Fluka Chemical corp.) или в форме порошка, полученного путем дробления таблеток.
Пример 9
Самостерилизующий мешочек был устроен следующим образом: хирургический скальпель, имеющий 3,8 • 10 спор B.subtilis var. niger на поверхности, помещали в стерильную чашку Петри. Чашку помещали в большую чашку Петри вместе с 1 г мочевинопероксидного комплекса в таблетированной или в порошковой форме. Большую чашку Петри помещали в мешок, сделанный из TYVEKTM/MYLARTM (газопроницаемый, таблица 9), MYLARTM/MYLARTM (газонепроницаемый, таблица 10) или бумага/MYLARTM (газопроницаемый, таблица 10). Затем пакет запечатывали.
Каждый пакет выдерживали при разных температурах в течение разных периодов времени, как показано в таблицах 9 и 10, ниже. Образцы для биологического испытания оценивали на стерилизацию, как описано в примере 1. Результаты включены в таблицы 9 и 10, причем знак "+" показывает бактериальный рост.
В таблице 10 перечисляются данные по эффективности самостерилизующих пакетов с (бумага/MYLARTM) газопроницаемым барьером и без него (MYLARTM/MYLARTM). Пакеты устроены, как описано выше, однако источником пара перекиси водорода была пероксидмочевина только в порошковой форме.
Результаты этого испытания показывают, что комплекс мочевины и пероксида данного изобретения, заключенный в пакете с газопроницаемым барьером или без него, обеспечивает эффективную стерилизацию для предмета внутри пакета в отсутствие влаги при комнатной температуре и атмосферном давлении через всего 2-3 часа. При более высоких температурах стерилизация осуществляется через всего один час.
Для определения эффективности стерилизационной системы данного изобретения в закрытом контейнере, выполнялся следующий эксперимент.
Пример 10
Самостерилизующий контейнер был устроен следующим образом: подложку из нержавеющей стали, имеющую 3,8 • 105 спор B.subtilis var.niger на ее поверхности (таблица 11) или имеющую 9,2 • 105 спор B.subtilis var. niger на ее поверхности (таблица 12), помещали внутри небольшого полиэтиленового (ПЭ) сосуда, имеющего 20 отверстий (размером 3/16")на его поверхности. Сосуд помещали в больший ПЭ сосуд, который покрывали или воздухонепроницаемой крышкой или газонепроницаемым слоем SPUNGUARD® (CSR обертка). Больший полиэтиленовый сосуд также заключал в себе второй ПЭ сосуд, также имеющий 20 отверстий (размером 3/16") на его поверхности. Этот сосуд содержал 1 г пероксидмочевины или в виде порошка, или в виде таблетки и был запечатан в пакет или из SPUNGUARDTM (CSR обертка) или из TYVEKTM.
Каждый контейнер выдерживали при разных температурах в течение разных отрезков времени, что показано в таблицах 11 и 12 ниже. Образцы для биологического испытания оценивали на стерилизацию, как описано в примере 1. Результаты включены в таблицы 11 и 12, причем знак "+" показывает бактериальный рост.
Результаты этого испытания показывают, что неводный комплекс мочевины и пероксида, заключенный в контейнере с газопроницаемым барьером и без него, обеспечивает эффективную стерилизацию при комнатной температуре через всего 3-4 часа. При более высоких температурах стерилизация осуществляется за такой малый срок, как полчаса.
Неводные пероксидные комплексы, которые выделяют пары пероксида, как было обнаружено, применимы для стерилизации предметов при комнатной температуре и более эффективны при повышенных температурах. Эти комплексы можно помещать в пакеты, контейнеры, камеры, комнаты или любые емкости, которые можно герметично изолировать, где они выделяют пары пероксида, которые эффективно стерилизуют предметы. Комплексы можно нагревать для облегчения выделения паров и для обеспечения стерилизации за время, которое меньше срока, необходимого для стерилизации при комнатной температуре. Соединения данного изобретения поэтому применимы в целом ряде случаев, когда желательна стерилизация. Стерилизация может достигаться просто путем помещения комплекса в герметично изолированную емкость, заключающую предметы, подлежащие стерилизации. В противоположность предыдущим способам здесь нет необходимости контакта с влагой для обеспечения активации перекиси водорода.
Чтобы подтвердить, что стерилизация может осуществляться с использованием неводных пероксидных комплексов за меньший срок при более низком давлении, были выполнены следующие эксперименты.
Пример 11
Самостерилизующий контейнер был устроен следующим образом: подложку из нержавеющей стали, имеющую 9,2 • 105 спор B.subtilis var. niger на ее поверхности, помещали внутри небольшого ПЭ сосуда, имеющего 20 отверстий (размером 3/16") по поверхности. Сосуд помещали в ПЭ сосуд большего размера, который закрывали газопроницаемым слоем из обертки CSB (SPUNGUARDTM). Сосуд большего размера также заключен во второй ПЭ сосуд, также имеющий 20 отверстий (размером 3/16") на поверхности. Этот сосуд содержал 1 г пероксидмочевины в виде порошка или в виде таблетки. Сосуд затем герметично упаковывали в упаковочный материал CSR или пакет из TYVEKTM.
Большие сосуды помещали или в 4,5 л стерилизационную камеру, или в 173 л стерилизационную камеру. Каждый контейнер выдерживали при давлении 13,3 Па (100 Торр) и температуре 23oC в течение 2 часов, как показано в таблице 13. Образцы для биологического испытания оценивали на стерилизацию, как описано в примере 1. Результаты включены в таблицу 13.
Эти результаты показывают, что неводный комплекс мочевины и пероксида, заключенный в контейнер с воздухопроницаемым барьером, обеспечивает эффективную стерилизацию при 13,3 Па и комнатной температуре через всего 2 часа. Эти результаты при сравнении с результатами таблицы 12, демонстрируют, что пероксидные комплексы данного изобретения обеспечивают стерилизацию при пониженном давлении через меньшее время, чем то, которое необходимо для осуществления стерилизации при атмосферном давлении.
Таким образом, комплексы перекиси водорода данного изобретения могут обеспечивать эффективную стерилизацию через значительно более короткие периоды времени. Кроме того, как обсуждалось выше, плазму также можно использовать для повышения действенности стерилизации парами перекиси водорода. Предметы, подлежащие стерилизации, подвергаются воздействию плазмы после экспозиции с парами перекиси водорода и остаются в плазме в течение отрезка времени, достаточного для осуществления полной стерилизации.
Предметы, которые были простерилизованы путем экспозиции в парах перекиси водорода, могут выдерживаться под воздействием плазмы для удаления остаточной перекиси водорода, сохраняющейся на предметах. Так как остаточная перекись водорода разлагается на нетоксичные продукты во время обработки плазмой, простерилизованные предметы готовы для использования после обработки без необходимости каких-либо дополнительных стадий.
Неводные пероксидные комплексы применимы в целом ряде случаев, включая такое применение, как в качестве компонента самостерилизующей упаковки. Кроме того, эти комплексы пригодны для использования при различных способах стерилизации предметов парами, таких как способ, раскрытый в патенте США N 4943414. В этом патенте раскрывается процесс, при котором сосуд, содержащий небольшое количество испаряемого жидкого стерилизующего раствора, подсоединяется к просвету и стерилизующий раствор испаряется и протекает непосредственно в просвет предмета, так как давление снижено во время цикла стерилизации. Способ, раскрытый в патенте, может быть модифицирован, чтобы дать возможность применения неводного пероксидного соединения. Соединение помещается в сосуд и он соединяется с просветом предмета, подлежащего стерилизации. Предмет затем помещается в контейнер, и контейнер откачивают. Просвет предмета и наружная часть предмета контактируют с парами перекиси водорода, выделяемыми неводным соединением. По желанию может генерироваться плазма и использоваться для усиления стерилизации и/или для удаления какого-либо остаточного количества перекиси водорода с предмета.
Использование неводных пероксидных комплексов в системе, только что описанной, позволяет преодолеть тот недостаток, что вода из водного раствора испаряется быстрее и предшествуем парам перекиси водорода в просветах. Таким образом достигается более эффективная стерилизация, и необходимо меньшее время для осуществления стерилизации. Комплексы перекиси водорода, такие как глицинангидридные, обладают особыми преимуществами, так как они выделяют значительное количество перекиси водорода при пониженном давлении без необходимости дополнительного нагревания комплекса.
Синтез неводных комплексов перекиси водорода
Данное изобретение, кроме того, представляет процесс получения неводных комплексов перекиси водорода, которые применимы в качестве источника для стерилизатора парами перекиси водорода или в качестве компонента самостерилизующей упаковки, как было описано выше. Конечно комплексы перекиси водорода могут использоваться в других целях, таких как для отбеливающих средств, для растворов для контактных линз, для катализаторов и для другого применения, которое хорошо известно специалистам.
Общая процедура получения комплексов перекиси водорода этого изобретения состоит в следующем:
(1) Поместить реагирующий материал в камеру
Материал, который должен прореагировать с перекисью водорода может быть твердым веществом в разных формах (например, порошок, кристаллический, пленка и т.д., причем предпочтительно имеет большую площадь поверхности для повышения скорости реакции). Реагирующий материал может также присутствовать в виде раствора в воде или другом растворителе, если дается достаточное время для выпаривания растворителя после того, как давление в камере снижается. Этот материал может также быть жидкостью, температура кипения которой выше, чем температура кипения перекиси водорода (150oC). Так как скорость реакции больше при повышенной температуре, камеру предпочтительно нагревают или перед тем, как вводится смесь реагентов, или после этого. Однако температура не должна быть настолько высокой, чтобы реагенты кипели или выпаривались.
Реагирующая композиция может помещаться в любой контейнер, который обеспечивает выход парам перекиси водорода. Если она находится в форме порошка или другой форме, которая может распространяться, когда камера откачивается, тогда реагент может оставаться в проницаемом контейнере, который позволяет перекиси водорода диффундировать в контейнер.
(2) Откачать камеру
Предпочтительно камеру откачивают до давления, которое ниже давления паров перекиси водорода (которое зависит от ее концентрации и температуры), чтобы гарантировать то, что вся перекись водорода находится в фазе пара. Давление паров повышается с повышением температуры и снижается при увеличении концентрации пероксида. Для большинства экспериментов камеру откачивают до примерно (0,2 Торр) 26,6 Па, а температура была комнатной или выше.
(3) Генерировать пары перекиси водорода
Пары перекиси водорода могут генерироваться из раствора перекиси водорода или из по существу безводного комплекса перекиси водорода. Последний дает сухую перекись водорода в парообразном состоянии, которая имеет преимущества, если или материал должен реагировать с парами, или комплекс, который должен образоваться, является гигроскопическим. Другое преимущество генерации паров перекиси водорода из по существу безводного комплекса состоит в том, что процент перекиси водорода в комплексе, который будет образовываться, выше, чем тогда, когда пар генерируется из водного раствора H2O2. Это возможно связано с конкуренцией между молекулами воды и молекулами H2O2 за места связывания в комплексе, когда для генерации паров H2O2 используется водный раствор.
Пары пероксида могут генерироваться в той же самой камере, которая вмещает реагирующий материал, или в другой камере, отделенной от нее вакуумным клапаном.
(4) Дать прореагировать реагирующему материалу с перекисью водорода
Время, необходимое для реакции, зависит, конечно, от скорости реакции реагента с перекисью водорода. Оно может быть определено эмпирически путем контроля давления, которое снижается при связывании пероксида с реагирующим материалом. Обычно время реакции составляет примерно 5-30 минут. Концентрация парообразной перекиси водорода и вес исходного материала определяют процент пероксида по весу в конечном продукте реакции. Когда весовое отношение реагента к перекиси водорода повышается, весовой процент перекиси водорода в комплексе снижается. Реакция может повторяться много раз для увеличения концентрации перекиси водорода в комплексе.
(5) Откачать камеру снова
В конце реакционного периода камеру дополнительно откачивают до примерно (2 Торр) 266 Па для удаления какого-то количества непрореагировавшей перекиси водорода.
(6) Открыть камеру и забрать комплекс перекиси водорода
Механизм, с помощью которого перекись водорода образует комплекс с материалом реагента, полностью неясен. Образование комплекса, как полагают, включает образование водородной связи между перекисью водорода и богатыми электронами функциональными группами, содержащими кислород и/или азот, в реагирующем веществе. Неизвестно, является ли это единственным видом связи; однако вещества с широким рядом функциональных групп, как было обнаружено, образуют комплексы с перекисью водорода.
Преимущества реакции с паровой фазой над предыдущими способами образования комплекса перекиси водорода включают:
1. Отношение перекиси водорода к реагирующему материалу может точно контролироваться путем изменения количества перекиси водорода, присутствующего в парообразном состоянии, или количества реагирующего материала, подвергающегося действию паров.
2. Необходимость удалять растворитель из продукта реакции исключается.
3. Могут образовываться пероксидные комплексы, которые являются жидкими или твердыми веществами, такими как порошки, кристаллы, пленки и т.д.
4. Можно получать пероксидные комплексы гигроскопических материалов. Синтез неводных пероксидных комплексов по данному изобретению, кроме того, описан в следующих примерах. Многие из этих соединений применяются в качестве катализаторов, в дополнение к использованию, описанному более детально здесь, что легко будет осознано специалистами. Примеры представляют осуществление получения композиций и процессов этого изобретения, но они никаким образом не предназначены для ограничения объема этого изобретения.
Пример 12
Комплекс перекиси водорода с глицинангидридом получали следующим образом: 1 г образца глицинангидрида (Aldrich Chemical Co., Milwaukee, WI) помещали на алюминиевый поднос в 173-литровой камере, в которой поддерживалась температура в 45oC. Сверху алюминиевый поднос покрывали нетканым материалом TYVEKTM, который предотвращал потерю глицинангидрида с подноса, когда давление в камере снижалось, но был газопроницаемым и не абсорбировал перекись водорода. Дверь камеры закрывали и давление в камере снижали до (0,2 Торр) 26,6 Па путем откачивания камеры с помощью вакуумного насоса. Концентрацию перекиси водорода, равную 10 мг/л, создавали путем выпаривания соответствующего объема 70% водного раствора перекиси водорода (FMC Corp., Philadelphia, РА) в камере. Контакт паров перекиси водорода с глицинангидридом поддерживали в течение 20 минут. В конце реакционного периода давление в камере снижали до 266 Па (2 Торр) и затем возвращали к атмосферному давлению. Продукт реакции удаляли из камеры и анализировали на процентное содержание перекиси водорода по весу с помощью следующих реакций иодометрического титрования.
H2O2 + 2Kl+H2SO4-->I2+K2O4+2H2O
I2+2Na2S2O3--->Na2S4O6+ 2NaI
При реакции титрования иода тиосульфатом натрия использовали крахмальный индикатор для усиления изменения окраски в конечной точке. Процент по весу перекиси водорода рассчитывали по следующему уравнению:
Вес. % H2O2= [(мл Na2S2O3] (нормальность Na2S2O3)1,7]/(вес образца в граммах).
Весовой процент перекиси водорода в глицинангидридном комплексе, как было обнаружено, составлял 24,3%.
Пример 13
Комплексы перекиси водорода из широкого ряда органических и неорганических комплексов получали, используя процедуру из примера 12. В каждом случае условия реакции были такими же, что и условия в примере 12, за исключением того, что 1,0 г каждого из соединений, представленных в таблице 14, использовали вместо глицинангидрида.
Образованные органические комплексы включают следующий ряд соединений с функциональными группами, которые способны к образованию водородных связей с перекисью водорода: спирты, эфиры, кетоны, кислоты, аминокислоты, сложные эфиры, органические соли, амины, амиды, полиамиды, полиуретаны, мочевины и биурет. Неорганические комплексы включают карбонаты с катионами натрия, калия и рубидия, а также бикарбонат натрия. Кроме того, были также получены комплексы перекиси водорода с гидроксидом кальция и тетранатрий-пирофосфатом. Исходные материалы были тонко измельченными порошками или слегка более крупными кристаллическими веществами, за исключением нейлона 6,6, который обрабатывался в виде пленки толщиной 0,12 мм, и поливиниметилового эфира, который был в виде 50% по весу водного раствора.
Комплексы перекиси водорода, полученные с этими материалами в условиях опыта, были твердыми веществами, за исключением поливинилпирролидона, гистамина, поливинилметилового эфира, поливинилметилкетона, пропионамида и 1,3-диметилмочевины. Комплексы перекиси водорода с 1,3-диметилмочевиной и пропионамидом были свободнотекучими жидкостями, которыми легко оперировали в процессе синтеза с паровой фазой, так как не нужно было удалять растворитель для получения конечного продукта. Комплексы с гистамином, поливинилпирролидоном, поливинилметиловым эфиром и поливинилметилкетоном были липкими материалами, с которыми не так легко было работать.
В примерах 14 и 15 описаны дополнительные исследования с поливинилпирролидоном при различных условиях процесса получения пероксидного комплекса в виде свободнотекучего твердого продукта.
Пример 14
Были получены комплексы перекиси водорода с поливинилпирролидоном, в которых процент перекиси водорода в поливинилпирролидоновом комплексе менялся путем изменения отношения веса поливинилпирролидона к концентрации перекиси водорода в парообразном состоянии. Условия в этих опытах были идентичны условиям в примере 12, за исключением того, что вес поливинилпирролидона повышался с 1,0 г до 3 г и до 5 г. Во всех опытах концентрация перекиси водорода поддерживалась постоянной на уровне 10,0 мг/л объема камеры. Результаты этих исследований представлены в таблице 15.
Пример 15
Получали комплекс перекиси водорода с ПВП, для которого перекись водорода производилась из комплекса перекиси водорода с мочевиной. Когда перекись водорода производится таким образом, она по существу безводна. В этом исследовании 5 г ПВП помещали в реакционную камеру и в реакционную камеру поставляли 10 мг H2O2/литр объема камеры путем нагревания примерно 7 г 35% комплекса H2O2 с мочевиной до температуры примерно 110oC в течение примерно 5 минут. Остальные условия этого опыта были теми же самыми, что и условия в примере 12. Процент перекиси водорода в ПВП комплекса и физическое состояние комплекса представлены в таблице 15.
Результаты этих экспериментов показывают, что свободно-текучее твердое вещество может быть получено в случае ПВП комплекса перекиси водорода путем регулировки отношения ПВП к перекиси водорода в парообразном состоянии и, альтернативно, путем использования по существу безводного источника пара перекиси водорода.
Неорганические комплексы перекиси водорода
Неорганические комплексы перекиси водорода также пригодны для использования в качестве стерилизующих веществ, как описано детально здесь выше для органических комплексов перекиси водорода. Пары пероксида могут выделяться из этих неорганических органических комплексов при атмосферном давлении и комнатной температуре. Однако, как описано более детально ниже, существенные количества паров перекиси водорода могут выделяться из неорганических пероксидных комплексов при быстром нагревании до конкретных температур выделения при пониженном давлении. Для успешного выделения перекиси водорода из неорганических пероксидных комплексов скорость нагревания неорганических пероксидных комплексов составляет предпочтительно, по крайней мере, 5oC/мин; более предпочтительно она составляет, по крайней мере, 10oC в минуту; еще более предпочтительно, по крайней мере, 50oC/мин; и наиболее предпочтительно она составляет, по крайней мере, 1000oC в минуту.
Перечисление типичных представителей этих неорганических пероксидных комплексов и весовой процент перекиси водорода представлены в таблице 16. Процедура титрования, используемая для определения весового процента H2О2 в комплексах, была такой же, как и описанная в примере 12. Натрийкарбонатный комплекс H2O2 закупали у Fluka Chemical Corp. Процедура синтеза с парообразной фазой, использованная для синтеза неорганических пероксидных комплексов была той же самой, что и описанная в примере 12, за исключением того, что использовали 10 г твердого неорганического образца вместо 1-5 г и проводили два реакционных цикла вместо одного.
Пример 16
Процедура реакции для жидкофазного синтеза неорганических комплексов перекиси водорода была по существу такой же, какая описана Jones et al. (J. Chem. Soc. Dalton, 12: 2526-2532, 1980). Вкратце, неорганические твердые вещества сначала растворяли в 30% водном растворе перекиси водорода до получения насыщенного раствора, с последующим добавлением по каплям этанола. В случае комплексов оксалата калия и карбоната рубидия образовывались белые осадки пероксида по мере того, как возрастало количество добавляемого этанола. В случае карбоната калия, пирофосфата калия и пирофосфата натрия насыщенные растворы инкубировали при -10oC в течение нескольких часов, чтобы облегчить образование кристаллического пероксидного комплекса. Комплексы отделяли от жидкости с помощью вакуумной фильтрации, промывали этанолом, по крайней мере, три раза и сушили под вакуумом.
Для определения выделения H2O2 или способности неорганических пероксидных комплексов разлагаться использовали дифференциальный сканирующий калориметр (ДСК) (модель PDS С 2920, ТА instruments). ДСК работал при линейном нагревании 10oC/мин и в интервале температур от 30oC до 200oC как при атмосферном, так и при различных условиях разрежения. Со ссылками на фигуру 5, ДСК включает камеру для образца 110, нагревающую пластину 112 и систему контроля давления. Система контроля давления включает датчик давления 114, соединенный с манометром 116. Манометр 116 соединен с регулятором 118, который, в свою очередь, соединен с клапаном регулировки давления 120. Датчик давления 114 подвижно связан с клапаном регулировки давления 120 и с насосом 122.
Комплекс оксалата калия и перекиси водорода, синтезированный, как описано здесь выше, помещали в ДСК и подвергали воздействию температур в интервале от 50 до 170oC при конкретном пониженном давлении. Как можно видеть на фиг. 6, большее выделение H2O2 дает эндотермический процесс, происходящий при пониженном давлении, тогда как экзотермическое разложение H2O2 преобладает при высоких давлениях. Частичное снижение давления предпочтительно до менее (20 Торр) 2,66 кПа и наиболее предпочтительно до менее (10 Торр) 1,33 кПа. Действительное давление в камере для образца несколько выше, чем измеряемое прибором, и действительная температура в камере несколько ниже, чем измеряемая температура металлической пластины и алюминиевого столика. Не желая связывать себя какой-либо конкретной теорией работы, предполагают, что действительное давление, используемое в стерилизационном аппарате, должно быть меньше давления пара неорганического пероксидного комплекса при действительной температуре в камере для того, чтобы обеспечить то, что комплекс будет выделять пары перекиси водорода по существу без разложения. Однако обычно применяемое давление предпочтительно менее (50 Торр) 6,65 кПа, более предпочтительно менее (10 Торр) 1,33 кПа. При некоторых осуществлениях этого изобретения, при которых давление пара пероксидного комплекса ниже, давление предпочтительно менее (5 Торр) 0,665 кПа.
При применении неорганических пероксидных комплексов для стерилизации определяющим для стабильности комплекса является то, что нагревание происходит быстро, что может производиться путем предварительного нагревания алюминиевой пластинки перед контактом с композицией неорганического пероксида. При использовании неорганических пероксидных соединений также предпочтительно, чтобы температура была выше 86oC.
Как обсуждалось выше, предпочтительно, чтобы неорганический комплекс перекиси водорода нагревался быстро, т.е. с такой скоростью, как 1000oC/мин или более. Это может быть осуществлено путем контактирования пероксида с предварительно нагретой нагревающей пластинкой. Предпочтительное осуществление для выполнения такого быстрого нагревания показано на фигурах 7A и 7B. Со ссылками на фигуру 7A показан аппарат 125 для инжекции паров пероксида в стерилизационную камеру 131 в закрытом положении. Неорганический комплекс перекиси водорода заключается в пероксидный диск 132. Диск 132 включает пять слоев: три слоя обертки CSR, порошок пероксидного комплекса и алюминиевую фольгу, покрытую полипропиленом. Диск 132 теплоизолирован по краю с целью сохранения порошка пероксидного комплекса. Пероксидный диск 132 помещается под перфорированной алюминиевой пластинкой 130, которая соединена с корпусом 150 с помощью соединяющих алюминиевых элементов 142. Диск 132 свободно удерживается на месте между O-кольцами 151. Перед введением паров пероксида в камеру нагретый алюминиевый столик 134 находится в стороне от пероксидного диска 132 и соединен с алюминиевой пластиной 136. Пружина (не показана) внутри мембранной коробки 138 удерживает пластину 136 внизу в закрытом положении. Когда камера 131 откачивается мембранная коробка 138 также откачивается. Пластина 136 помещается против О-колец 148, отделяя таким образом камеру для выделения пероксида 152 от пропускного канала 158. Аппарат удерживается на месте и соединяется со стерилизационной камерой 131 болтами 144, 146, 154 и 156.
Со ссылками на фигуру 7B, чтобы привести столик 134 в контакт с пероксидным диском 132, мембранная коробка 138 откачивается. Если давление повышается, мембранная коробка 138 движется вверх, тем самым продвигая нагретый алюминиевый столик 134 в положение против пероксидного диска 132. В предпочтительном осуществлении алюминиевый столик 134 предварительно нагревается до 175oC; однако могут использоваться другие температуры. Затем из порошка через слои CSR выделяется пар пероксида, проходит через отверстия 160 в перфорированной алюминиевой пластинке 130 и поступает в камеру для выделения пероксида 152. Движение вверх нагретого алюминиевого столика 134 также открывает камеру для выделения пероксида 152, позволяя парам пероксида пройти в каналы 158, которые подвижно связаны со стерилизационной камерой.
Неорганическими пероксидными комплексами, использованными в следующих двух примерах для определения количества выделения пероксида и эффективности стерилизации, были пирофосфат калия (К4P2О7 • 3H2О2:ПК), оксалат калия (К2С2О4 • 1H2O2:OK) и карбонат натрия (Na2СО3 • 1,5 H2О2:KH).
Пример 17
Выделение пероксида из KH, OK и ПК
Идеальная температура, при которой H2О2 выделяется из KH, OK и ПК определяли с помощью ДСК. Действительное количество H2O2 выделившегося из 2 г каждого из этих комплексов определяли при разных температурах с использованием 75-литровой камеры и аппарата с фигур 7A и 7B. Количество H2О2, выделенного из ПК при 175oC, было больше, чем для KH и OK. Хотя KH выделял, по крайней мере, количество H2О2 при 175oC, значительно большее выделение наблюдалось, когда количество образца увеличивалось (Табл.17).
Пример 18
Испытание эффективности с использованием KH, OK и ПК
2 • 106 спор B.subtilis var. niger помещали на лезвие из HC. Три обсемененные лезвия сначала помещали в положениях впереди, в середине и сзади завернутого в Spunquard полифениленоксидного подноса 10'' х 21'' х 3,5''. Завернутый поднос затем помещали в 75-литровую вакуумную камеру, имеющую первоначальное давление разрежения (0,2 Торр) 26,6 Па. Пероксидный диск 5,5'' был изготовлен путем термоизоляции порошков KH, OK или ПК неорганических пероксидов между тремя слоями Spunquard и одним слоем алюминиевой фольги, покрытой полипропиленовой пленкой. Пероксид выделялся с помощью контакта диска в течение 2 минут с алюминиевой пластиной, которая была предварительно нагрета до 175oC, с последующим дополнительным временем диффузии, равным 8 минутам до общего времени экспозиции, равного 10 минутам. После обработки три лезвия раздельно помещали в триптиказный соевый бульон (ТСБ) при 32oC на 7 дней и учитывали бактериальный рост. Результаты суммированы в таблице 18.
Как можно видеть из таблицы никакого роста спор не наблюдалось, за исключением эксперимента с 2 г KH (1/3). Однако, когда количество KH, подвергаемое испарению, увеличивали до 3 г, бактериального роста не наблюдалось. Эти результаты подтверждают эффективность стерилизации с использованием соединения неорганического вещества с перекисью водорода.
Неорганические комплексы перекиси водорода могут легко включаться в процедуры стерилизации, описанные здесь выше в сочетании с органическими пероксидными комплексами. Например, неорганические комплексы могут использоваться в сочетании с методом стерилизации плазмой, или в сочетании с самостерилизующей оболочкой, где пероксид медленно выделяется из комплекса. Подобным же образом неорганические комплексы могут также использоваться при стерилизации предметов, имеющих узкие просветы, причем сосуд, содержащий неорганический пероксидный комплекс подсоединяется к просвету. Дополнительно может применяться пульсирование давления паров из неорганических пероксидных комплексов. Другие примеры использования неорганических комплексов для стерилизации будут очевидны специалисту при обращении к данному описанию.



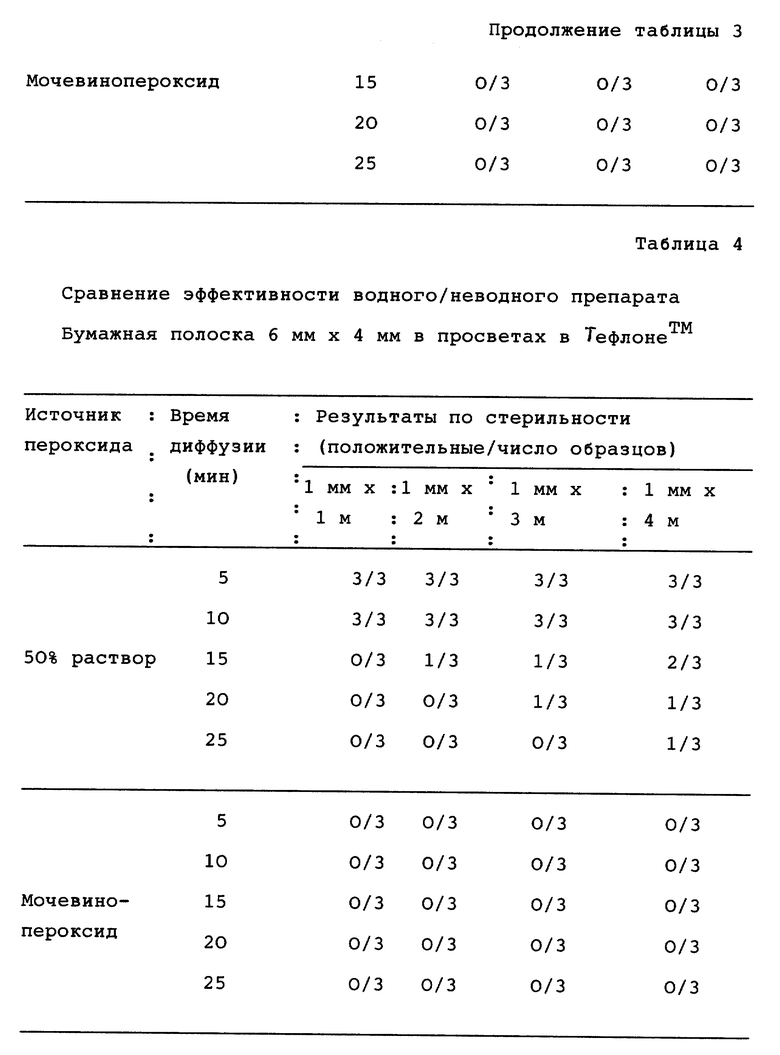

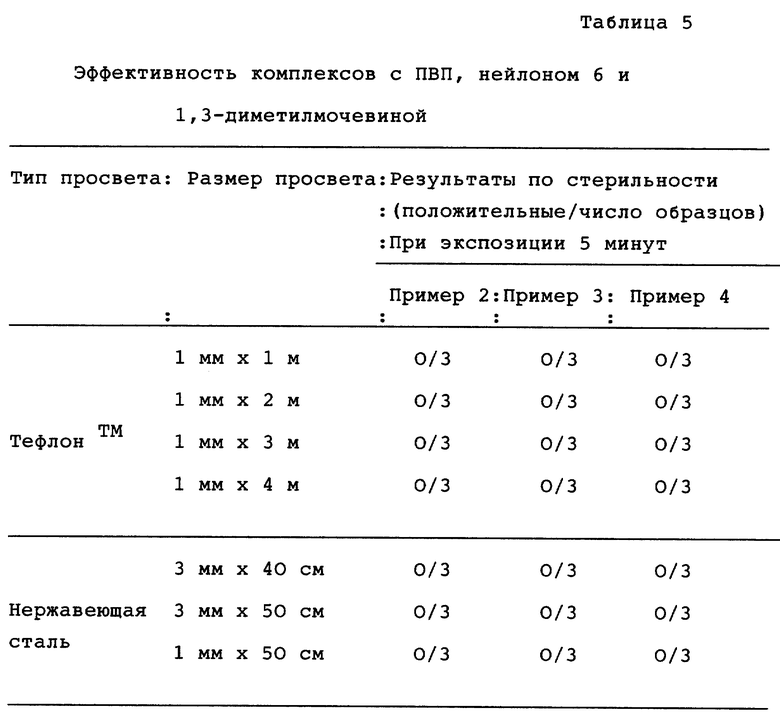

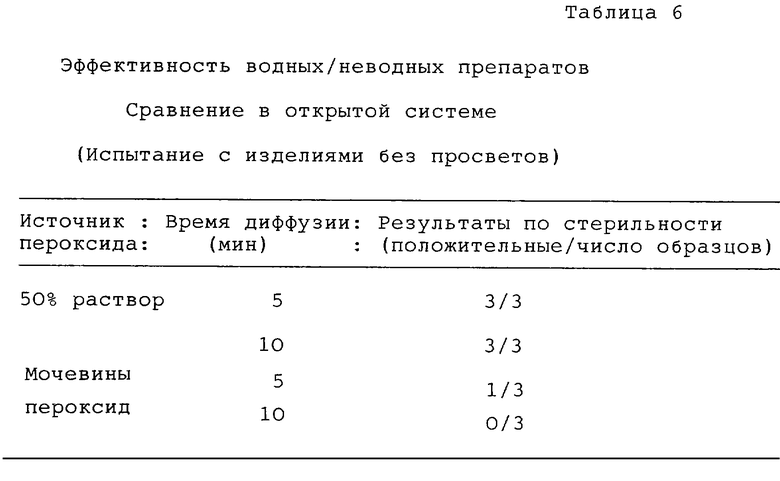
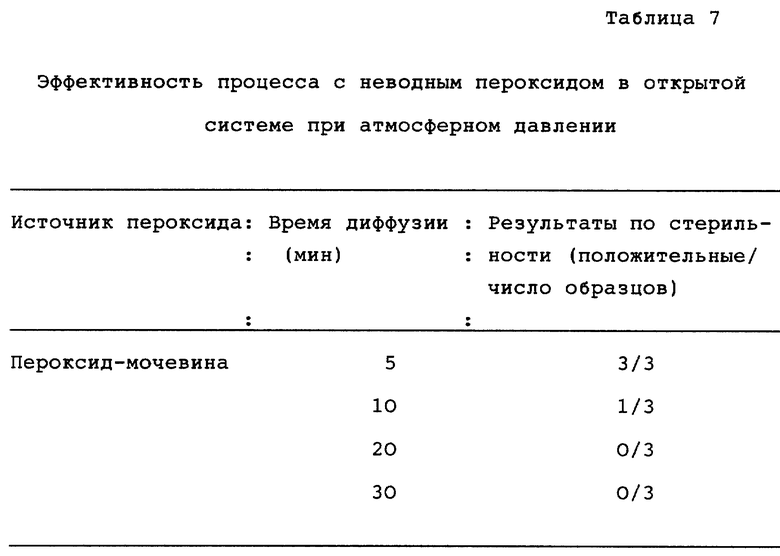

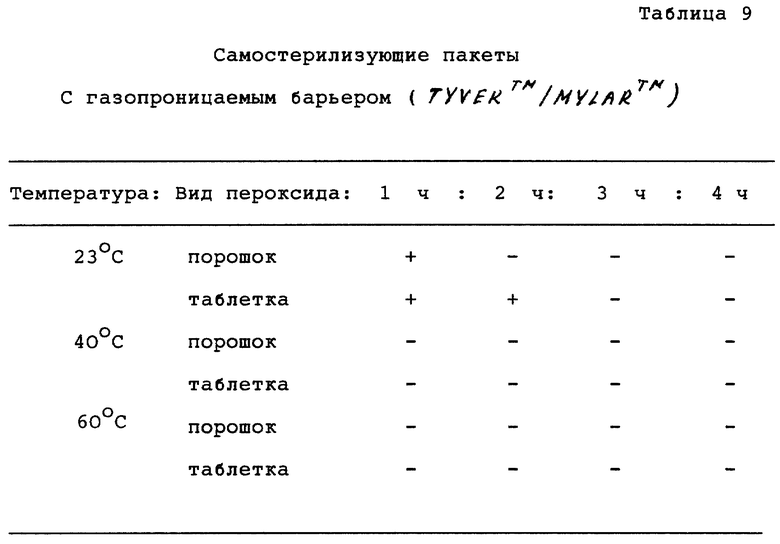
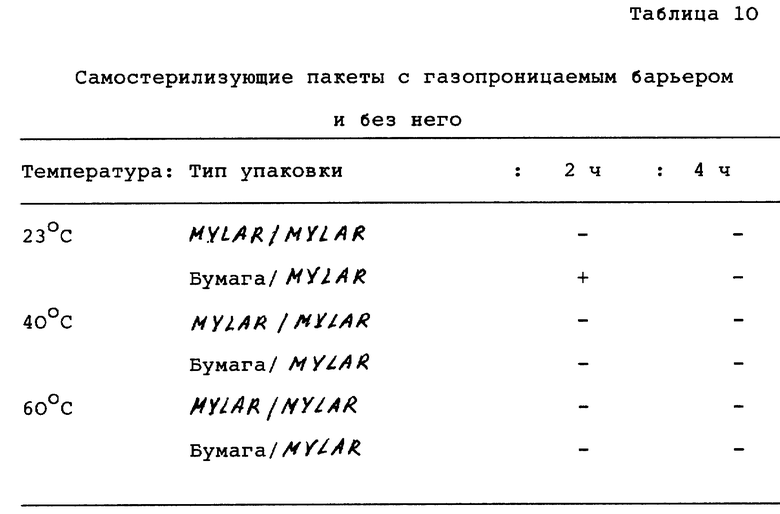











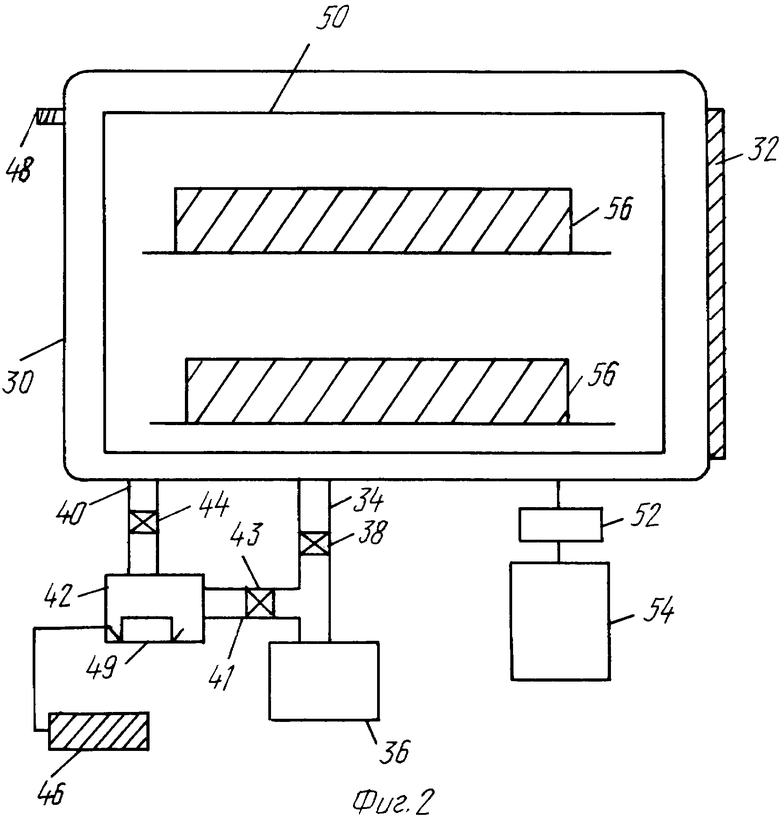
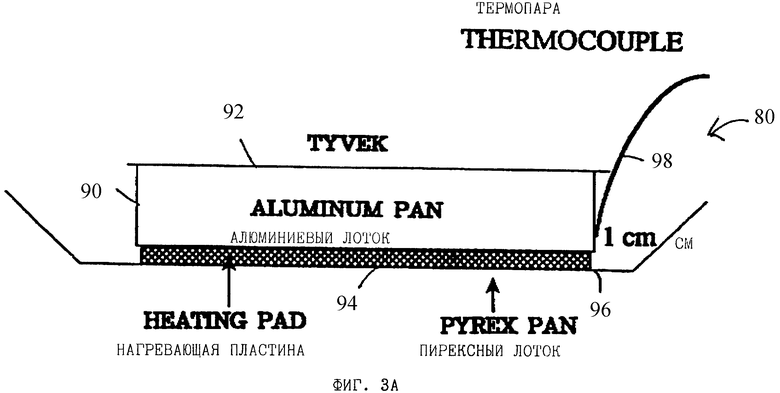
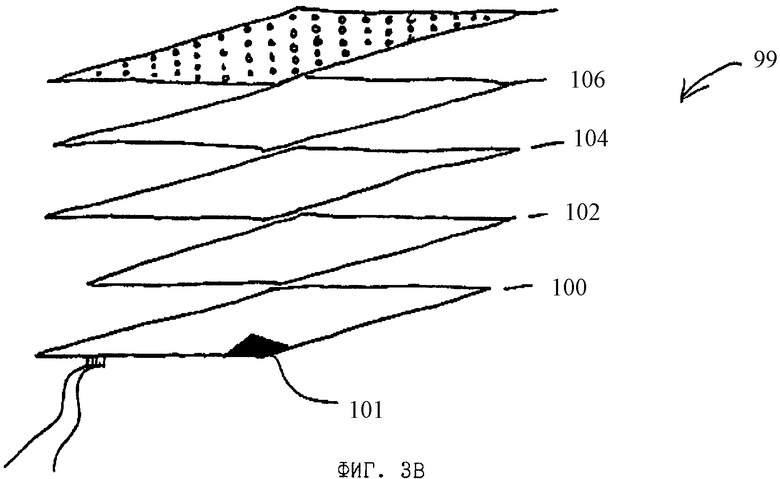
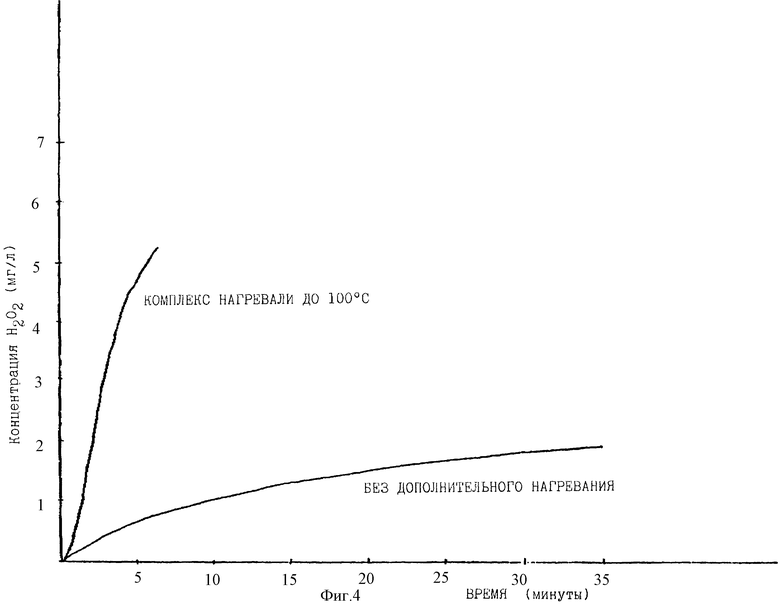
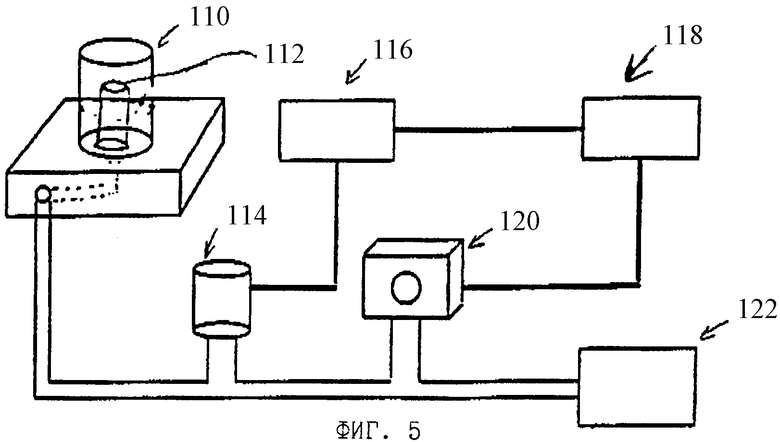
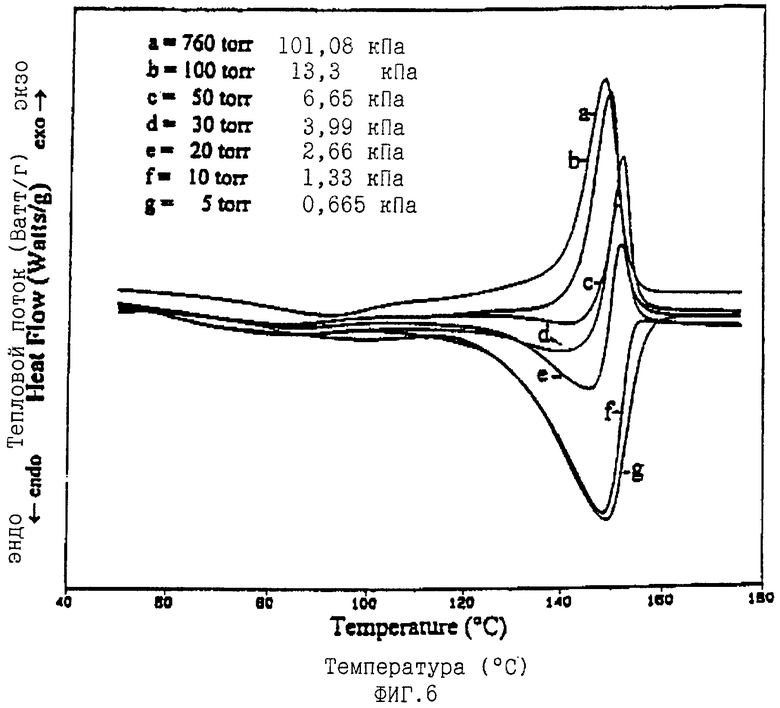
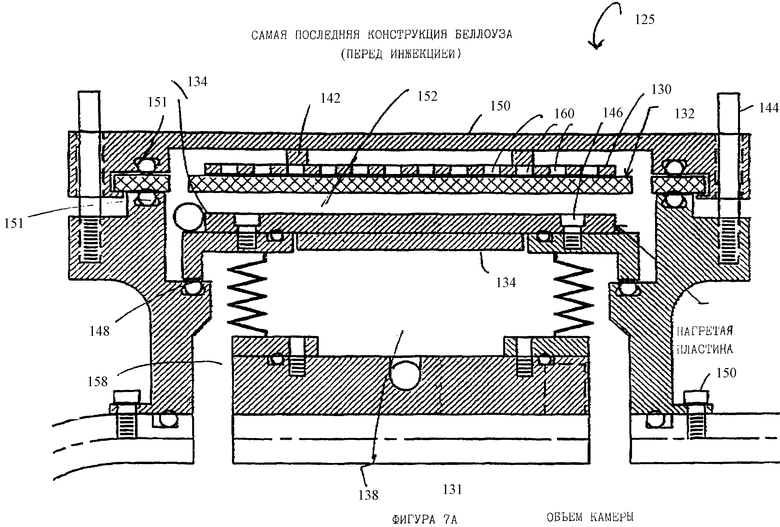
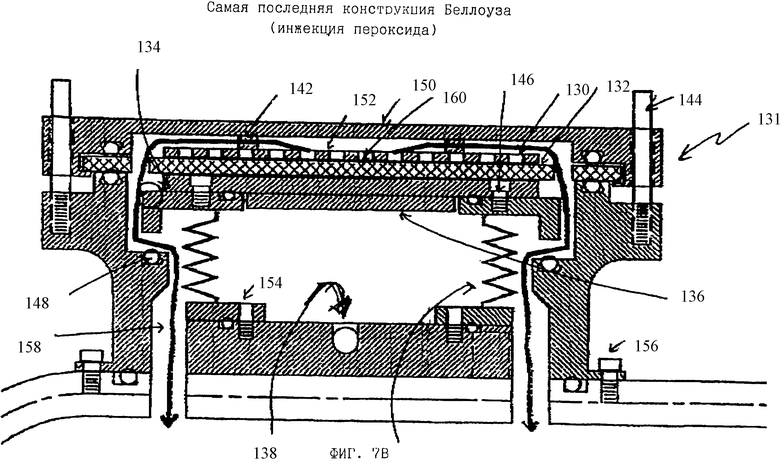
Изобретение относится к аппарату и способу стерилизации паром перекиси водорода медицинских инструментов и подобных устройств. Пар перекиси водорода выделяют из неводного неорганического комплекса перекиси водорода. Пар перекиси может выделяться при комнатной температуре и атмосферном давлении, однако используемое давление может быть менее (50 Торр) 6,65 кПа, а температура - более 86oС для облегчения выделения пара перекиси водорода. Скорость нагревания может быть более 5oС/мин. По желанию в сочетании с паром может использоваться плазма. Изобретение позволяет повысить эффективность стерилизации. 6 с. и 33 з.п.ф-лы, 18 табл., 7 ил.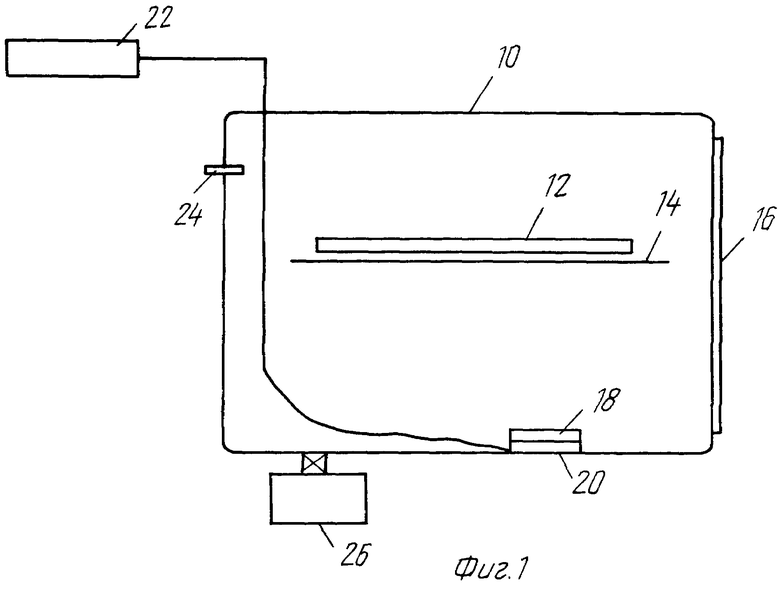
| US 4643876 А, 17.02.1987 | |||
| US 4744951 А, 17.05.1988 | |||
| US 5087418 А, 11.02.1992 | |||
| US 5115166 А, 19.05.1992. |
Авторы
Даты
2001-12-10—Публикация
1996-10-25—Подача