Изобретение относится к области охраны окружающей среда при переработке отходов гальванического производства, в частности к способам переработки вторичного медного, никелевого и хромового сырья, и может быть использовано при переработке отработанных электролитов.
Известен способ возврата отработанных электролитов в производство путем стабилизации раствора за счет осуществления непрерывной его циркуляции через систему аппаратов ([1], с. 358). Она представляет собой систему фильтров для задержания взвешенных и органических веществ, систему электролизеров, теплообменник. Данная система не является универсальной, для каждого электролита подбирается определенный набор фильтров и аппаратов очистки.
Это является основным сдерживающим фактором при внедрении таких систем в производстве. Кроме того, целесообразность использования таких систем находится в случае концентрации основных компонентов в электролите менее 100 г/л.
Чаще в отработанных электролитах концентрация по основному металлу бывает более 100 г/л.
В процессе работы происходит засоление раствора кислотными остатками SO4 -2, NO3 -, Cl-. Это ведет к использованию ионообменных фильтров, что усложняет процесс регенерации и очистки электролита.
Без устранения высокого солесодержания повторное использование таких растворов возможно не более 1-2 раз. Кроме того, в данном методе не решен вопрос регенерации фильтров. Это ведет к накоплению отходов в виде фильтрующих загрузок.
Другой известный способ обезвреживания отработанных растворов заключается в добавлении их в сточные воды и очистке на локальных очистных сооружениях ([5] , с. 223) и ([1], с. 366), ([3], с. 8). Сбросы отработанных растворов в сточные воды составляют 2-3% от объема стоков, а по содержанию загрязнений достигают 40-70%. Залповый характер таких сбросов нарушает режим работы очистных сооружений, приводит к безвозвратным потерям ценных материалов.
Следующий известный метод обезвреживания отработанных электролитов сводится к их нейтрализации путем смешивания кислых и щелочных отработанных растворов ([1], с. 367). В этом случае образующиеся осадки гидроксидов металлов обычно не могут быть утилизированы.
Методы нейтрализации отработанных электролитов с помощью реагентов гидроксида кальция, кальцинированной соды, доломита не дают необходимой степени очистки до предельно-допустимой концентрации ионов металлов.
Такие растворы после обезвреживания должны проходить очистку на локальных очистных сооружениях. Осадки в виде гидроксидов металлов и солей кальция и магния обычно не могут быть утилизированы. Чаще всего эти шламы выводятся на специальные площадки или сбрасываются в водоемы, леса или на городские свалки ([2], с. 20).
Известен способ обработки кислых железосодержащих сточных вод (4), заключающийся в нейтрализации и осаждении щелочным реагентом, окислении образующегося гидроксида железа (II) до гидроксида железа (III) перекисью водорода с последующим отделением осадки и его сушкой. Нейтрализацию и осаждение проводят при pH 9-10, а в качестве щелочного реагента используют раствор гидроксида калия. Данный способ имеет узкую область применения, так как сточные воды имеют нейтральный показатель pH среды; основными загрязнениями сточных вод в процессах гальванического производства являются ионы меди, никеля, хрома, цинка, а железо идет как сопутствующий компонент.
В результате применения гидроксида калия произойдет осаждение не только гидроксидов железа, но и гидроксидов других металлов, находящихся в сточных водах. Из таких осадков получить желозоокисные пигменты как основу для приготовления красок практически невозможно, т.к. химический состав, согласно ГОСТам на различные железоокисные пигменты (желтые, коричневые, красные), ограничивает количество и виды примесей.
В качестве прототипа выбран способ очистки вод от ионов тяжелых металлов, (6) заключающийся во введении соединений железа и щелочного реагента с непрерывным перемешиванием и последующим отделением осадка. В качестве соединений железа используют свежеприготовленную гидроокись трехвалентного железа при отношении количества Fe3+ к сумме ионов тяжелых металлов не менее 5: 1, а в качестве щелочного реагента используют раствор гидроксида калия и перемешивание осуществляют при pH 9-10.
Жидкая фаза идет на приготовление удобрений.
К недостаткам этого способа относится:
1. Невозможность применения данного способа на предприятиях с непрерывной подачей воды на очистные сооружения, где часовой расход составляет 50 м3/час и выше. У сточных вод в отличие от электролитов сравнительно небольшое солесодержание, которое является основой для производства удобрений, т. е. потребуются выпарные агрегаты большой мощности, чтобы сконцентрировать растворы калийных солей. Экономически нецелесообразно выпаривать 40000 м3/смену сточных вод, чтобы повысить солесодержание раствора.
2. Осадки, образующиеся после данного метода, содержат множество основных металлов: Fe, Cr, Al, Cu, Ni, Sn, Pb, и примесей в виде взвешенных и органических веществ. И это делает невозможным использование осадков для приготовления ферритов и красителей, к которым согласно ГОСТам предъявляются высокие требования по химической чистоте и однородности.
3. Кроме того, сброс таких сточных вод в промышленную и хоз.-бытовую канализацию невозможен, т.к. pH 9-10. Разрешается сбрасывать сточные воды с pH 6,5-7,5.
Таким образом, данный метод не может найти реализацию в реальных условиях гальванического производства.
Задача изобретения - возвращение ценных металлов в производство и исключение попадания ионов тяжелых металлов в окружающую среду, а также расширение функциональных возможностей способа.
При использовании настоящего изобретения достигается следующий технический результат:
1. Получаемая жидкая фаза после утилизации электролитов содержит высокое содержание солей калия 200 г/л и выше и является само по себе жидким концентрированным минеральным удобрением, служащим основой для получения комплексного минерального удобрения.
2. В ходе утилизации получаются два вида сравнительно "чистых" и однородных вида осадков:
1 вид - гидрооксиды основного металла;
2 вид - осадки, содержащие соединения железа.
Второй вид осадков используется для изготовления красителей на основе железа.
3. В процессе утилизации отсутствуют сливы в канализацию, также не требуется полигонов для хранения отходов, т.е. отсутствует нагрузка на окружающую природную среду.
4. Получаемые в процессе утилизации изделия и продукты обладают товарной стоимостью и приносят прибыль в процессе реализации.
5. Данный способ позволяет утилизировать не только концентрированные отработанные растворы, но и сточные воды.
Для решения поставленной задачи и достижения указанного технического результата в известном способе переработки отработанных растворов, заключающемся в нейтрализации с последующим выделением твердой фазы в виде гидроксидов металлов, согласно изобретению необходимо гидроксиды металлов перевести в оксиды путем нагрева до температуры не менее 900oС с последующим восстановлением при температуре, превышающей температуру плавления металлов. Восстановление оксидов металлов проводят в интервале температур 1200-2000oС в среде углерода.
Сущность данного метода заключается в проведении следующих операций.
1. Принятие отработанных растворов на утилизацию предпочтительно по видам: растворы никелирования, меднения, хромирования (допускается принимать смешанные отработанные медные и никелевые растворы).
2. Проведение химической нейтрализации каждого вида электролита.
Нейтрализация кислых растворов 20-25% раствором КОН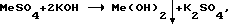

где Me - металл. В качестве него может быть медь, никель, хром.
В результате проведения нейтрализации образуются гидроксиды Cu(OH)2, Ni(OH)2, СR(OH)3, которые высушиваются и собираются по видам.
3. При накоплении необходимого объема осадков одного вида (объем зависит от загрузки печи) проводится нагрев его в печи при температуре 900-1000oС.
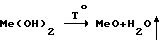
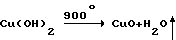
В результате проведения данной реакции происходит образование оксидов металлов.
4. Восстановление оксидов до металлов углеродом при Тo, превышающей To плавления металлов в интервале температур 1200-2000oC в зависимости от вида восстанавливаемого металла.
Реакция происходит по формуле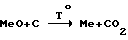
Тo=1200-1300oC для восстановления меди
Тo=1000-1600oC для восстановления никеля
Тo=2000oС для восстановления хрома.
В зависимости от химического состава осадков получают металлы или сплавы различной степени чистоты. Выход металла при этом составляет более 98%.
5. Полученную жидкую фазу дорабатываем следующим образом. Доочистка жидкой фазы электролита необходима потому, что электролит не является железосодержащим, а нейтрализация просто щелочью не дает очистки раствора от ионов металлов до предельно-допустимых концентраций.
В этом случае используют свежеприготовленную гидроокись трехвалентного железа Fe(OH)3, как в (6), или же обработкой раствора FeSO4 пероксидом водорода стр. 22 (3). Или же готовят железосодержащую суспензию из железного купороса, едкого натра и азотнокислого натрия. Для приготовления l м3 суспензии необходимо
60 кг едкого натра,
21,3 кг азотнокислого натрия,
208,5 кг железного купороса, стр. 169 (5).
Коагулянты, приготовленные таким образом, дозируются в очищаемый фильтрат. После отстаивания и фильтрации фильтрат может быть использован для приготовления комплексных концентрированных удобрений. Железосодержащий осадок используется для приготовления красителей.
Предложенный способ реализуется следующими примерами:
Пример 1.
Из привозимых на утилизацию отработанных электролитов меднения с помощью 25%-ного раствора КОН осадили гидроксид меди Сu(ОН). Осадок промыли и высушили до 20% влажности. 12 кг данного осадка прокалили в печи при Тo=900oС в течение 12 часов до получения оксида СuО. Полученный оксид смешали с 1,5 кг графита и поместили в печь на 2 часа при Тo=1250-1300oC. В результате получили 8 кг медного сплава с процентным содержанием меди 99,5%.
Пример 2.
Из 15 кг высушенного осадка, содержащего 90% гидроксида никеля и 10% гидроксида меди, прокалив в печи 12 часов при температуре 900oC, получили смесь оксидов никеля и меди (NiO и CuO). В полученные оксиды добавили 2 кг графита и поместили в печь на 4 часа при Тo=1600oС. В результате получили 9 кг медно-никелевого сплава, общее содержание которых в образце 99%. Заявляемым способом могут перерабатываться электролиты хромирования.
Жидкую фазу в каждом примере обрабатывают, как было описано ранее, т.е. свежеприготовленным гидроксидом трехвалентного железа, или железосодержащей суспензией, или смесью раствора железного купороса с пероксидом водорода. Полученный фильтрат идет на приготовление комплексных минеральных удобрений, а осадок, содержащий железо, используют для приготовления красителей.
Данный способ позволяет возвращать в производство ценные металлы, что дает большой экономический эффект, который будет зависеть от объема растворов, приходящих на утилизацию.
На предприятии-заявителе создана утилизационная установка, на которой проводится нейтрализация электролитов. В процессе работ на установке получены комплексные минеральные удобрения марки "Саров" ТУ113-08-00209438-134-92. Получены образцы медного и медно-никелевого сплава, образцы цветной брусчатки и облицовочных кирпичей красного, коричневого и зеленого цвета.
Источники информации
1. Справочник "Гибкие автоматизированные гальванические линии". Под общей редакцией З.А. Зубченко. Москва. "Машиностроение" 1989.
2. Журнал "Гальванотехника и обработка поверхности". Том. 2. 1, I993, Москва.
3. Д.Н. Смирнов, В.Е. Генкин. Очистка сточных вод в процессах обработки металлов. Москва, "Металлургия, 1989.
4. Патент РФ 2019524. МКИ С 02 F 1/64 Опубл. в БИ 17. 1994.
5. Приложение: к журналу "Гальванотехника и обработка поверхности". С.С. Виноградов. Экономически безопасное гальваническое производство. Выпуск 3, г. Москва, "Глобус 1998".
6. Патент РФ 2060962. МКИ С 02 F 1/62, опубл. в БИ 15, 1996.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1992 |
|
RU2060962C1 |
| СПОСОБ ОБРАБОТКИ КИСЛЫХ ЖЕЛЕЗОСОДЕРЖАЩИХ СТОЧНЫХ ВОД | 1991 |
|
RU2019524C1 |
| СПОСОБ ПОДГОТОВКИ ПОВЕРХНОСТИ ИЗДЕЛИЙ ИЗ НЕРЖАВЕЮЩЕЙ СТАЛИ ПЕРЕД ГАЛЬВАНИЧЕСКИМ НИКЕЛИРОВАНИЕМ | 2000 |
|
RU2201478C2 |
| РАСТВОР ДЛЯ ИЗГОТОВЛЕНИЯ СТЕКЛЯННЫХ МИКРОСФЕР | 2001 |
|
RU2205802C2 |
| СПОСОБ УДАЛЕНИЯ НАКИПИ | 1995 |
|
RU2117077C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДНЫХ СОЕДИНЕНИЙ ОБЩЕЙ ФОРМУЛЫ LIMO, ГДЕ M=FE, И/ИЛИ CO, И/ИЛИ NI | 2000 |
|
RU2183587C2 |
| СПОСОБ УТИЛИЗАЦИИ ЖИДКИХ ОРГАНИЧЕСКИХ ОТХОДОВ | 1996 |
|
RU2138087C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКИХ ОБРАЗЦОВ ТВЕРДЫХ РАСТВОРОВ ПОЛУТОРНЫХ ОКСИДОВ ВАНАДИЯ И ХРОМА | 2001 |
|
RU2206539C1 |
| СПОСОБ ПЕРЕРАБОТКИ И ЗАХОРОНЕНИЯ ОТРАБОТАВШИХ ФИЛЬТРОВ | 1999 |
|
RU2174260C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЗВОДНОГО ИОДИДА СКАНДИЯ | 2000 |
|
RU2189358C2 |
Используется при переработке отходов гальванического производства. Способ комплексной переработки отработанных растворов гальванического производства включает нейтрализацию с последующим выделением твердой фазы в виде гидроксидов металлов. Гидроксиды металлов переводят в оксиды путем нагрева до температуры не менее 900oС с последующим восстановлением при температуре, превышающей температуру плавления металлов, а полученную жидкую фазу обрабатывают свежеприготовленной гидроокисью трехвалентного железа, или железосодержащей суспензией, или смесью раствора железного купороса с пероксидом водорода, отстаивают и фильтруют. Восстановление оксидов проводят при 1200-2000oС в среде углерода. Изобретение позволяет возвращать в производство ценные металлы. 2 з.п. ф-лы.
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1992 |
|
RU2060962C1 |
| Неорганические соединения хрома | |||
| Справочник | |||
| - Л.: Химия, 1981, с.9-18 | |||
| Роде | |||
| Т.В | |||
| Кислородные соединения хрома и хромовые катализаторы | |||
| - М.: Издательство Академии наук СССР, 1962, с | |||
| Затвор для дверей холодильных камер | 1920 |
|
SU182A1 |
| Химическая энциклопедия, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - М.: Советская энциклопедия, 1990, с | |||
| Приспособление для указания нагревания подшипников | 1919 |
|
SU669A1 |
| Химическая энциклопедия, т | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| - М.: Советская энциклопедия, 1990, с.245 | |||
| Металлургия меди, никеля и кобальта, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - М.: Металлургия, 1977, с.122 | |||
| ЕР 0457988 А1, 10.10.1990 | |||
| DE 4019052 А1, 19.12.1991. | |||
Авторы
Даты
2002-02-20—Публикация
1999-09-23—Подача