Изобретение относится к области медицины и может быть использовано в ортопедической стоматологии и хирургии при восстановлении зубных рядов посредством мостовидных протезов с опорой на имплантаты, а также путем непосредственного применения имплантатов.
В настоящее время в хирургической и терапевтической стоматологии наиболее широко применяются при зубном протезировании металлические, преимущественно титановые, керамические, стеклокерамические, стеклоиономерные, полимерные и композиционные имплантаты. Основным требованием, предъявляемым к имплантационным материалам стоматологического назначения, является их биологическая и физиологическая совместимость с костными и мягкими тканями челюстной части лицевого скелета и полости рта.
Наиболее сложными по конструкции и самыми совершенными по комплексу механических и биологических свойств являются титановые дентальные имплантаты, которые могут иметь различную конструкцию внутрикостной части. Усложнение внутрикостной части титановых дентальных имплантатов преследует две главные цели:
- увеличение площади опоры имплантата в костной ткани и его надежную фиксацию;
- создание оптимальных условий для остеогенеза при срастании кости с имплантатом.
Последнее условие обеспечивается наличием каналов и отверстий в имплантате, нанесением на его поверхность биоактивных покрытий на основе костного минерала - гидроксиапатита Са10(РO4)6(ОН)2 или созданием шероховатости или пористости поверхностей имплантата, находящихся в тесном контакте с костным ложем.
Известен дентальный имплантат, состоящий из внутрикостной части, соответствующий конфигурации корня удаленного зуба и выполненный из биоинертного пористого материала и коронковой части, состоящей из наружней и внутренней частей (RU 2023437, С1, опубл. 30.11.94, Бюл. 22).
Материалом для изготовления внутрикостной части данного имплантата служит титан, а внекостной части - пористый титан или пористая корундовая керамика на основе оксида алюминия.
Известен дентальный имплантат, содержащий штифт в виде головной и корневой частей, в котором корневая часть выполнена цилиндрической формы и покрыта слоем волластонитапатитовой керамики со сквозной проницаемостью и размером пор 300...500 мкм (RU 2109493 С1, опубл. 27.04.98, Бюл. 12) (прототип).
Накопленный клинический опыт применения титановых дентальных имплантатов разных типов позволил выявить ряд недостатков, к которым относятся следующие:
- слабо выраженный остеогенез при срастании костной ткани с имплантатом;
- смещение, поворот или отторжение имплантата;
- отскок неорганических и титанонеорганических покрытий от поверхности имплантатов и нарушение их контакта с костным ложем;
- разрушение кортикальных, плотных поверхностей зубных корневых каналов и установка внутрикостной части имплантатов в относительно мягкую внутричелюстную губчатую кость.
Известен композиционный материал, включающий гидроксиапатит и трикальцийфосфат (RU 2074702 С1, опубл. 10.03.97, Бюл. 7). Известный материал применяют для заполнения костных полостей и сохранения костной структуры, обеспечивая ее заростания, но он не пригоден для изготовления имплантатов.
Задачей, на решение которой было направлено создание данного изобретения, является получение конструкции дентального имплантата, по возможности приближенного естественным анатомическим и функциональным особенностям зубочелюстной системы человека.
Технический результат, достигаемый в процессе решения поставленной задачи, заключается в воссоздании имплантата, имеющего внешнюю конфигурацию удаленного зуба или его корня, который устанавливается непосредственно в лунку удаленного зуба без ее разрушения, обеспечивая при этом периодонтальный тип сращения материала имплантата со стенками зубной альвеолы.
Технический результат достигается за счет того, что дентальный имплантат содержит корневую пористую, внутреннюю (центральную) и коронковую части, выполненные как единое целое на единой остеокондуктивной силикатной матрице с градиентом пористости, дифферинцированным по высоте имплантата от 5...10% до 60% за счет распределения фосфатов кальция, при этом градиент пористости коронковой части составляет 5...10%, внутренней (центральной) - 20...50% и корневой 40...60%.
Технический результат достигается также за счет того, что композиционный материал для изготовления имплантата включает гидроксиапатит, трикальцийфосфат, фторапатит и остеокондуктивную силикатную матрицу при общем содержании компонентов в матрице от 40 до 60 мас.%, в том числе:
Гидроксиапатита - 15,0...25,0
Трикальцийфосфата - 15,0...20,0
Фторапатита - 10,0...15,0
Сущность заявляемого изобретения поясняется графическими материалами, где на фиг.1 представлена структура апатитосиликатного биоактивного корневого имплантата, на фиг.2-5 показаны варианты применения предлагаемых дентальных корневых имплантатов.
Дентальный имплантат состоит из верхней части 1, внутренней части 2 и корневой части 3(фиг. 1). Имплантат изготовлен из силикокальцийфосфатного остеокондуктивного биокомпозиционного материала. Основным биологически активным компонентом данного материала являются фосфаты кальция, содержание которых по высоте имплантата может изменяться от 40 до 60 мас.%. На рисунке видно, что корневые каналы зуба полностью сохранены и хирургические повреждения костной ткани минимальны. С точки зрения состава и структуры разработанный остеокондуктивный корневой имплантат представляет собой полиминеральный композит на основе силикатной гидрофильной ячеистой матрицы с дифференцированным распределением в ней минералов группы апатита по высоте, изготовляемых из него дентальных имплантатов.
Верхняя часть апатитосиликатного корневого имплантата выполнена из резистивного плотного слаборезорбирующего в физиологической среде ротовой полости фторапатита Са10(РO4)6Р2 в силикатной матрице, что соответствует естественной зубной эмали. Эта часть имплантата представляет собой своего рода прочную и непроницаемую коронку, составляющую единое целое с телом имплантата. Она выполняется по принятым в стоматологии технологиям с учетом архитектоники соседних и контактных зубов противоположной челюсти. Пористость верхней части имплантата составляет 5...10%.
Внутренняя часть 2 корневого имплантата выполнена из гидроксиапатита Са10(РO4)6(ОН)2 с сохранением силикатной матрицы. Пористость этой части составляет 20...50%.
Внутрикостная корневая часть 3 состоит из ячеистой проницаемой силикатной матрицы, в которой диспергирован гидроксиапатит в сочетании с низкотемпературной модификацией трикальцийфосфата. Пористость этой части имплантата составляет примерно 40-60% при размере открытых ячеек от 50 до 400 мкм, что достаточно для размещения колоний костных клеток.
Срастание кости с имплантатом за счет ее оппозиционного роста осуществляется колонизацией открытых ячеек на поверхности и в объеме материала костными клетками в сочетании с последовательной резорбцией трикальцийфосфата и гидроксиапатита с образованием прямых химических связей с костью при взаимодействии гидроксильных ОН-групп силикатной матрицы Si-ОН и гидроксиапатита с полярными, в том числе ОН-группами белковых молекул, коллагена, образующегося белкового матрикса молодой костной ткани и минерального матрикса открытых стенок корневого канала.
Внутрикостная корневая часть имплантата, находящаяся в плотном контакте с костным ложем корневого канала, имеет общую с головкой силикатную матрицу, но с более высокой остеопроводимостью за счет повышения пористости. Биоактивными компонентами этой части корневого имплантата являются трикальцийфосфат и резорбируемый гидроксиапатит с атомным Са/Р отношением не более 1.66. Эта активная часть имплантата обеспечивает необходимые условия для протекания процесса остеогенеза и срастание стенок корневого канала с имплантатом с образованием единой костной структуры.
Морфологические и клинические испытания ячеистого апатитосиликатного остеокондуктивного материала показали, что первым продуктом остеогенеза на поверхности и в объеме изготовленных из него имплантатов является коллаген в виде переплетенных волокон, образующих на открытых поверхностях ячеек и каналов материала сплошной слой. Кальцинация белкового матрикса с образованием зрелых костных балочек отмечается на третьей неделе после имплантации. Кристаллизация костного гидроксиапатита отмечается образованием его кристаллов на поверхности волокон коллагена. Через 3 месяца после имплантации содержание зрелой минерализованной костной ткани в имплантате превышает 30%.
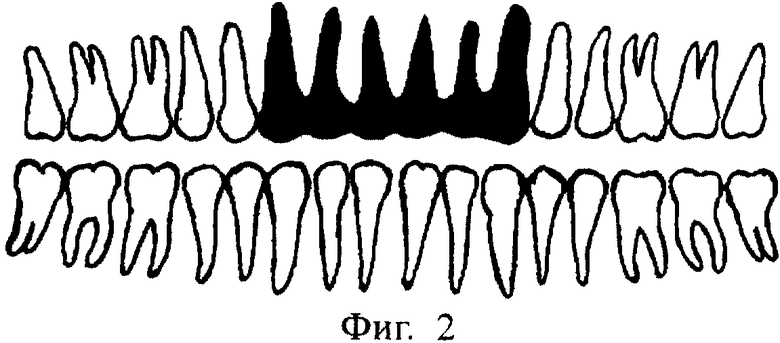
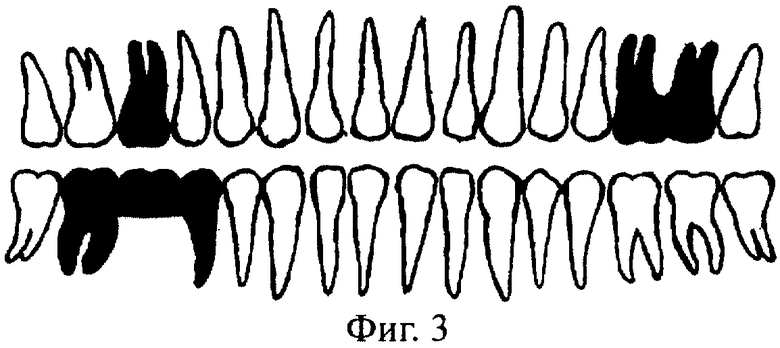
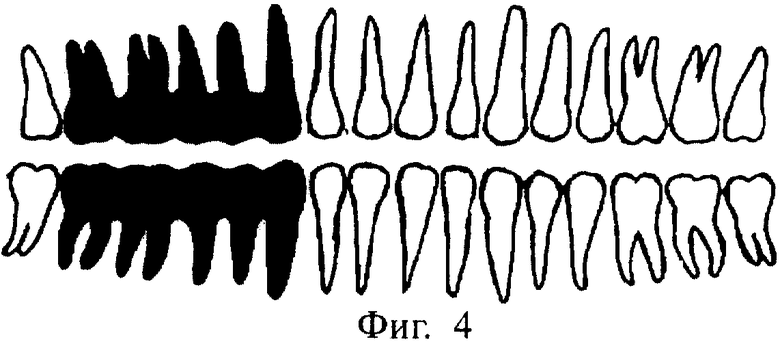
На фиг.2-5 показаны варианты применения предлагаемых дентальных корневых имплантатов. При использовании многокорневого имплантата на 8 и более - до 16 зубов не все корневые каналы могут быть использованы. Тогда имплантат без внутрикостной корневой части по своей сути представляет собой несъемный мост (фиг.5), опирающийся на имплантаты.
Корневые имплантаты могут устанавливаться как по одному, так и группами с использованием всех свободных от зубов альвеол. При полном отсутствии зубов возможно их восстановление как группами от 2 до 6, так и в виде полной зубной дуги до 16 имплантатов, соединенных в единое целое.
Корневая часть имплантата может быть выполнена удлиненной для более надежной фиксации в кости, при этом высверливаются или рассверливаются корневые каналы альвеолярного гребня.
Использование предлагаемых корневых дентальных имплантатов предполагает как индивидуальный подход в лечении больных с различными формами адентии, так и серийный с применением заранее изготовленных заготовок. В последнем случае внутрикостная корневая часть имплантата, преимущественно многорядного, выполняется в виде прямой, трапецеидальной или клиновой сплошной дуги. При установке такого имплантата обточка его корневой части проводится непосредственно врачом-стоматологом с учетом размеров зубов, глубины, направления и форм корневых каналов больного. К достоинствам предлагаемых корневых имплантатов следует отнести совмещение их установки с операцией по удалению поврежденных зубов.
Методика установки предлагаемых корневых имплантатов включает проведение следующих подготовительных операций:
а) точное установление направления, формы и размеров корневых каналов отсутствующих или удаляемых зубов с применением панорамной рентгенографии и томографии;
б) моделирование верхней части головки имплантата одинарного или многорядного с целью определения ее размеров и рельефа рабочей контактной поверхности;
в) изготовление имплантата по точной модели зуба (зубов) и их подгонка;
г) очистка корневых каналов с удалением эпителия для открытия костного ложа;
д) плотная установка имплантата одного или многокорневого в корневые каналы;
е) временная фиксация установленного имплантата в зависимости от показаний сроком на 2,5-3 недели;
ж) снятие фиксаторов.
При установке предлагаемых дентальных корневых имплантатов используются применяемые в хирургической стоматологии методики, технологии, инструменты и лекарственные препараты. Следует отметить, что материал имплантата гидрофилен, проницаем и перед установкой может быть пропитан раствором антибиотиков пролонгированного действия с заполнением до 40-50% его объема. Материал имеет среднюю объемную массу 1250 кг/м3, что близко к плотности твердой костной ткани, рентгеноконтрастен, что в свою очередь обеспечивает наблюдение за процессом вживления. Предлагаемые корневые дентальные имплантаты можно протезировать на верхнюю и нижнюю челюсти.
Материал корневых имплантатов прочный, машинообрабатываемый и позволяет производить установку на его верхней части коронок и мостов из металлов, сплавов, корундовой и кварцевой керамики, композитов, стеклоиономеров и других материалов, применяемых в современной стоматологии при зубном протезировании. Отличие от известных имплантатов состоит в том, что колонизированный колониями костных клеток апатитосиликатный корневой имплантат васкуляризирован и является живой тканью, единой с костной структурой реставрируемой челюсти.
К достоинствам предлагаемых дентальных имплантатов, изготовленных из предлагаемого материала, следует отнести не только их биологическую совместимость с костными тканями, но и их биоэнергетическую совместимость, поскольку их спектральные характеристики совпадают со спектральными характеристиками минерального матрикса плотной костной ткани. Их применение не нарушает естественное биополе головного мозга.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДЕНТАЛЬНЫЙ ИМПЛАНТАТ ХАСАНОВА, УСТРОЙСТВО, СОСТАВ, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И УСТАНОВКИ | 2004 |
|
RU2271172C1 |
| ЗУБНОЙ ИМПЛАНТАТ | 2011 |
|
RU2479281C2 |
| Способ изготовления дентального имплантата с использованием композитного нанопокрытия | 2018 |
|
RU2765921C1 |
| НАБОР БИОСОВМЕСТИМЫХ АПАТИТО-СИЛИКАТНЫХ ЗАГОТОВОК ИМПЛАНТАТОВ ДЛЯ ВОССТАНОВИТЕЛЬНОЙ И ЗАМЕСТИТЕЛЬНОЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ | 1995 |
|
RU2074672C1 |
| Способ изготовления дентального имплантата из нанотитана с использованием лазерного структурирования поверхности и наноструктурированного композитного покрытия и имплатат | 2019 |
|
RU2724437C1 |
| ПОРИСТЫЕ МИКРОСФЕРЫ НА ОСНОВЕ БИОФОСФАТОВ КАЛЬЦИЯ И МАГНИЯ С РЕГУЛИРУЕМЫМ РАЗМЕРОМ ЧАСТИЦ ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2012 |
|
RU2497548C1 |
| СТОМАТОЛОГИЧЕСКИЙ ИМПЛАНТАТ "ДИВАТАЛ" | 2001 |
|
RU2199973C1 |
| СПОСОБ НЕПОСРЕДСТВЕННОЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ У ПАЦИЕНТОВ С ВКЛЮЧЕННЫМИ ДЕФЕКТАМИ ЗУБНЫХ РЯДОВ | 2010 |
|
RU2447859C1 |
| СПОСОБ КОСТНОЙ ПЛАСТИКИ ПРИ НЕПОСРЕДСТВЕННОЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2008 |
|
RU2366378C1 |
| ЗУБНОЙ ИМПЛАНТАТ И КОМПЛЕКТ ДЛЯ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2017 |
|
RU2661019C1 |

Изобретение относится к области медицины и может быть использовано в ортопедической стоматологии и хирургии при восстановлении зубных рядов посредством мостовидных протезов с опорой на имплантаты, а также путем непосредственного применения имплантатов. Технический результат, достигаемый в процессе решения поставленной задачи, заключается в воссоздании имплантата, имеющего внешнюю конфигурацию удаленного зуба или его корня, который устанавливается непосредственно в лунку удаленного зуба без ее разрушения, обеспечивая при этом периодонтальный тип сращивания материала имплатата со стенками зубной альвеолы. Имплантат содержит корневую пористую, внутреннюю и коронковые части, выполненные как единое целое на единой остеокондуктивной силикатной матрице с градиентом пористости, дифференцированным по высоте имплантата от 5-10 до 60% за счет распределения фосфатов кальция, при этом градиент пористости коронковой части составляет 5-10%, внутренней - 20-50% и корневой - 40-60%. Композиционный материал для изготовления имплантата включает гидроксиапатит, трикальцийфосфат, фторапатит и остеокондуктивную силикатную матрицу при общем содержании компонентов в матрице от 40-60 мас. %, в том числе: гидроксиапатит 15,0-25,0; трикальцийфосфат 15,0-20,0; фторапатит 10,0-15,0. 2 с.п. ф-лы, 5 ил.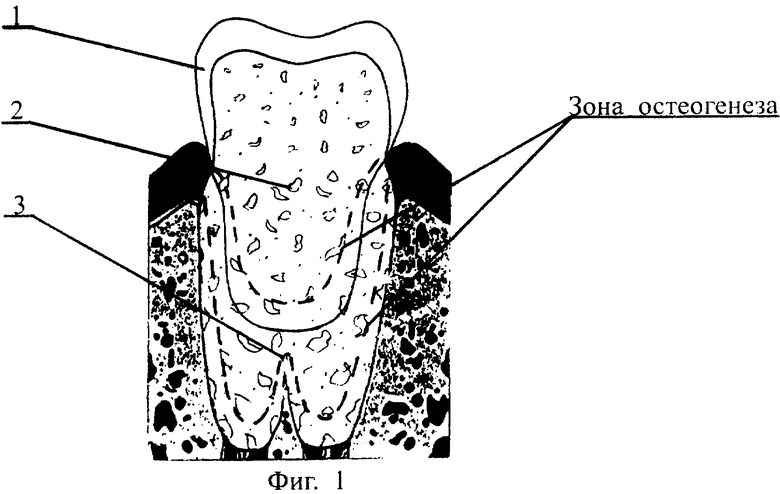
Гидроксиапатита - 15,0 - 25,0
Трикальцийфосфата - 15,0 - 20,0
Фторапатита - 10,0 - 15,0
| ЗУБНОЙ ИМПЛАНТАТ | 1996 |
|
RU2109493C1 |
| МАТЕРИАЛ ДЛЯ ВОССТАНОВЛЕНИЯ КОСТНОЙ ТКАНИ | 1994 |
|
RU2074702C1 |
| ПОРИСТЫЙ ПРОТЕЗ ТАЗОБЕДРЕННОГО СУСТАВА | 1996 |
|
RU2137442C1 |
| US 4051598 А, 04.10.1977 | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
Даты
2002-05-27—Публикация
2001-07-19—Подача