Изобретение относится к области медицины, а именно к хирургии, и может быть использовано в хирургическом лечении заболеваний щитовидной железы.
Из практики медицины известен способ аутотрансплантации ткани щитовидной железы в подкожную жировую клетчатку передней брюшной стенки (Шевердин Ю.П. Субоперационная аутоимплантация щитовидной железы при тиреотоксикозе в профилактике послеоперационного гипотиреоза. - Автореферат дисс. канд. мед. наук. - Харьков, 1979, 17 с. ), которая не обладает развитой сосудистой сетью, обеспечивающей процессы реваскуляризации и раннего приживления аутотрансплантатов.
Известен способ трансплантации ткани щитовидной железы с фрагментами целлоидина - культивирование тканей в организме по Ф.М.Лазаренко (Дунаев П.В., Соловьев Г. С. , Гинковер А.Г. Нервно-тканевые отношения и васкуляризация в имплантатах различных органов//Сб. Нервно-сосудистое обеспечение тканевых процессов. - М.: 1979, с. 21-24), при котором аутотрансплантация осуществляется так же в подкожную клетчатку в создаваемый очаг асептического воспаления. При этом наряду с процессами приживления трансплантата происходят процессы воспалительной деструкции и рубцевания, приводящие к ускоренному замещению аутотрансплантата соединительной тканью, быстрой потере функции ткани.
Наиболее близким к предлагаемому, является способ трансплантации ткани щитовидной железы в мышцы предплечья (Исмаилов С.И., Нугманова Л.Б., Костенко Л.Н. Аллотрансплантация криоконсервированной ткани щитовидной железы в лечении послеоперационного гипотиреоза//Вопросы клинической хирургии органов эндокринной системы. - Л.: 1987, с. 57-62). Однако известный способ так же имеет следующие недостатки:
- трансплантаты, находящиеся вне сосудистых связей с реципиентным ложем, до начала их реваскуляризации питаются путем диффузии, которая в скелетной мышечной ткани затруднена вследствие концентрации микроциркуляторной сосудистой сети преимущественно в эндомизии, на протяжении всей длины мышечного волокна;
- сроки реваскуляризации зависят от расположения трансплантатов по отношению к эндомизию и сухожильным структурам мышцы - в случае преобладания опорных структур мышечной ткани в области реципиентного ложа, реваскуляризация задерживается и в ткани трансплантата преобладают деструктивные процессы;
- несмотря на интенсивный кровоток в мышечной ткани, расположение элементов системы микроциркуляции, особенно артериоло-венулярных анастомозов, обеспечивающих перераспределение потока крови, не соответствует площади поверхности аутотрансплантатов ткани щитовидной железы, в связи с чем требуется дополнительное время для перестройки сосудистого русла в месте трансплантации, увеличиваются сроки ишемии и деструктивные процессы в ткани щитовидной железы;
- сокращение поперечно-полосатой мышечной ткани в период приживления трансплантатов способствует их смещению, травматизации и усилению процессов деструкции и рубцевания трансплантатов;
- используется трансплантация аллогенной ткани железы, которая подвержена воздействию иммунологических процессов, реакции отторжения, способствует сенсибилизации реципиента и ускоренному отторжению трансплантатов при последующих пересадках, которые устраняются в предлагаемом изобретении.
Целью предлагаемого изобретения является улучшение результатов аутотрансплантации ткани щитовидной железы в эксперименте путем создания оптимальных условий питания трансплантатов в ближайшем послеоперационном периоде путем диффузии и полноценной реваскуляризации фрагментов ткани.
Поставленная цель достигается тем, что ложе для трансплантатов ткани щитовидной железы формируется в подслизистом слое передней стенки желудка путем рассечения серозного и мышечного слоев без вскрытия просвета желудка, погружаются подготовленные трансплантаты и накладываются серозно-мышечные узловые швы, восстанавливающие целостность стенки желудка.
Восстановление сосудистого русла трансплантатов должно происходить в кратчайшие после операции сроки. Питание ткани путем диффузии до формирования сосудистого обмена более интенсивно происходит в условиях развитой сосудистой сети, которая хорошо выражена в подслизистом слое стенки желудка. Формирование сосудистой системы трансплантатов ткани щитовидной железы, их приживление и дальнейшее изолированное существование также зависит от условий кровоснабжения.
Левым параректальным разрезом от реберной дуги на протяжении 5-6 см, послойно вскрывается брюшная полость, в рану выводится передняя стенка желудка. В средней трети тела желудка, ближе к большой кривизне, как наиболее подвижной части желудка, рассекаются серозный и мышечный его слои на протяжении 1-2 см. Тупым и острым путем отслаивается слизистая оболочка - формируется ложе для трансплантатов. При этом стараются не повреждать крупные сосуды, залегающие в подслизистом слое стенки желудка. Кровотечение обычно бывает незначительным и легко останавливается прижатием на 1-2 мин салфетки, смоченной горячим физиологическим раствором - 50-60oС. После этого в подготовленное ложе погружаются трансплантаты ткани щитовидной железы в количестве соответствующем задачам эксперимента и рана желудка ушивается одним рядом узловых серозно-мышечных швов. Накладываются послойные швы на переднюю брюшную стенку (фиг.1).
Кровоснабжение желудочной стенки весьма интенсивное, наибольшее количество сосудов сосредоточено в подслизистом слое, а артериоло-венулярные анастомозы сосудистой системы желудочной стенки обеспечивают быструю ее адаптацию к новым условиям. Использование подслизистого слоя желудочной стенки для аутотрансплантации отличается от применения мышечной ткани в качестве ложа наличием рыхлой волокнистой соединительной ткани, обеспечивающей плотный контакт с питающим ложем, диффузионный тип питания трансплантатов в раннем послеоперационном периоде и интенсивную реваскуляризацию.
Аутотрансплантация ткани щитовидной железы в эксперименте и клинических условиях выполняется с целью коррекции уровня гормонального гомеостаза после радикальных операций на щитовидной железе при заболеваниях неопухолевой природы. Основной задачей этой операции является быстрое и наиболее полное приживление ткани, обеспечивающей требуемый уровень тиреоидных гормонов.
Отмеченное в экспериментах сохранение ткани щитовидной железы и формирование сосудов по периферии и в самих трансплантатах свидетельствует о соответствии предлагаемого для аутотрансплантации ткани железы подслизистого слоя желудочной стенки задачам данного метода сберегательного хирургического лечения заболеваний щитовидной железы. Отмечено снижение количества коллоида и десквамация фолликулярного эпителия в аутотрансплантированной ткани щитовидной железы: мерокриновый тип секреции, свойственный нормальной щитовидной железе взрослого человека сменяется преобладающим голокриновым типом секреции (у детей в 20% случаев в перинатальном периоде встречается такой же тип секреции, что расценивается как адаптационная перестройка ткани - "десквамативный" тип ткани железы) (Волкова О.В., Пекарский М.И. Эмбриогенез и возрастая гистология внутренних органов человека. - М.: 1976, с. 244). Поэтому отсутствие коллоида в большей части трансплантатов, сохраняющих фолликулярный рисунок, стромальные элементы, может расцениваться как особенность строения ткани щитовидной железы при аутотрансплантации в условиях резкого снижения общего количества функционирующей тиреоидной ткани. В этих условиях свободный трансплантат щитовидной железы является единственным источником гормонов. При сохранении части ткани удаляемой щитовидной железы в области верхнего полюса, культя органа подвергается регенераторной гипертрофии, а дистрофические изменения трансплантатов в подслизистом слое желудочной стенки выражены в меньшей степени.
Технически данный способ достаточно прост. Выполнение лапаротомии из небольшого доступа и рассечение стенки желудка после тиреоидэктомии не является существенной дополнительной травмой, поскольку аутотрансплантация ткани щитовидной железы позволяет обеспечить достаточное для сохранения гормонального гомеостаза количество функционирующей ткани в условиях развитого сосудистого русла с восстановлением в последующем интенсивного кровотока в самом трансплантате. Последнее условие является решающим в выборе предлагаемого способа.
Изложенная сущность изобретения поясняется чертежами, где:
фиг. 1 - сформированное реципиентное ложе с трансплантатами в подслизистом слое стенки желудка (схема);
фиг.2 - микропрепарат - аутотрансплантат щитовидной железы через 3 месяца после субтотальной билатеральной резекции (увеличение •70, окраска гематоксилином и эозином);
фиг. 3 - микропрепарат культи щитовидной железы через 3 месяца после субтотальной билатеральной резекции (увеличение •70, окраска гематоксилином и эозином);
фиг.4 - микропрепарат - аутотрансплантат щитовидной железы через 3 месяца после тиреоидэктомии (увеличение •70, окраска гематоксилином и эозином).
Предложенный способ был успешно апробирован экспериментально на 12 лабораторных собаках в Центральной научно-исследовательской лаборатории Астраханской государственной медицинской академии и отработан на 5 трупах людей в течение 1998-99 гг. Ниже приводятся результаты апробации.
Пример 1.
Собака 2, возраст 1 год, мужского пола, масса тела 12,5 кг. Под эндотрахеальным наркозом произведена субтотальная билатеральная резекция щитовидной железы. Оставлены участки ткани щитовидной железы 5•5•5 мм в верхней полюсе каждой доли. После подготовки трансплантатов путем рассечения ткани каждой доли щитовидной железы на поперечные фрагменты толщиной 0,5-1 мм и отмывания их в физиологическом растворе с гепарином 1:200, произведена левосторонняя параректальная лапаротомия разрезом длиной 5 см от реберной дуги, в рану выведена передняя стенка желудка. В средней трети тела желудка вблизи большой кривизны сделан продольный разрез серозного и мышечного слоев длиной 2 см. Тупым и острым путем сформировано ложе в подслизистом слое. При этом обращали особое внимание на сохранение целостности слизистой оболочки и тщательную остановку незначительного кровотечения, поскольку кровяной сгусток является препятствием для врастающих сосудов и средой для развития инфекционного воспаления с последующим рубцеванием ткани щитовидной железы.
В сформированное ложе погрузили 10 фрагментов ткани щитовидной железы 5•3•1 мм и рана стенки желудка была ушита атравматическими узловыми серозно-мышечными швами шелком 1 черного цвета, для визуализации данного участка желудочной стенки при заборе препарата. Послойные швы на рану передней брюшной стенки.
Срок наблюдения - 1 мес. Клинические признаки послеоперационного гипотиреоза: слабость, медлительность, снижение аппетита, брадикардия до 70-80 уд/мин, очаговая потеря волос, наблюдались до 14 суток после операции.
Забор препаратов производился под эндотрахеальным наркозом. Произведена лапаротомия и резекция участка желудочной стенки с препаратами щитовидной железы, локализация которых была определена по наличию шовного материала и пальпаторно. Выполнено иссечение культи щитовидной железы слева от трахеи - при ревизии ложа щитовидной железы выявлено, что культи обеих долей щитовидной железы округлой формы, размеры их 10•8•8 мм, полнокровные. На поперечном разрезе препарата желудочной стенки, в подслизистом слое определялась ткань розоватого цвета, окруженная рубцом, вокруг которой сохранялась неизмененная стенка желудка.
При гистологическом исследовании (фиг.2 - микропрепарат, окраска гематоксилином и эозином, увеличение •100), определяется ткань щитовидной железы, окруженная соединительнотканной капсулой, с лимфоидной и макрофагальной инфильтрацией, единичные фибробласты. Фолликулярный эпителий местами десквамирован, однако структура его в целом сохранена, коллоид сохранен лишь в единичных периферических участках трансплантата преобладает голокриновый тип секреции. Деструктивные изменения более выражены в центральных отделах трансплантата, по периферии на фоне фолликулярного рисунка имеются участки лейкоцитарной инфильтрации, развитые сосуды.
При гистологическом исследовании культи щитовидной железы (фиг.3 - микропрепарат, окраска гематоксилином и эозином, увеличение •100) отмечено сохранение типичной структуры ткани. Фолликулярный эпителий местами десквамирован, высота его неоднородная, имеется чередование участков нормального эпителия и соединительно-тканного перерождения ткани, структура имеющихся фолликулов в основном сохранена, имеются скопления коллоида как в фолликулах, так и в сформированных полостях, преимущественно на периферии.
Пример 2.
Собака 5, возраст 1,5 года, женского пола, масса тела 10 кг. Под эндотрахеальным наркозом произведена тиреоидэктомия. После подготовки трансплантатов описанным выше способом, произведена параректальная лапаротомия, в рану выведена передняя стенка желудка. В средней трети тела желудка вблизи большой кривизны сделан продольный разрез серозного и мышечного слоев длиной 2 см. Тупым и острым путем сформировано ложе в подслизистом слое. В сформированное ложе погрузили 15 фрагментов ткани щитовидной железы 5•3•1 мм и рана стенки желудка была ушита атравматическими узловыми серозно-мышечными швами шелком 1 черного цвета. Послойные швы на рану передней брюшной стенки.
Срок наблюдения - 6 мес. Клинические признаки послеоперационного гипотиреоза наблюдались в течение 1 месяца после операции.
Забор препаратов производился под эндотрахеальным наркозом. Произведена лапаротомия и резекция участка желудочной стенки с препаратами щитовидной железы. На поперечном разрезе препарата в подслизистом слое определялась ткань щитовидной железы, окруженная рубцом.
При гистологическом исследовании (фиг.4 - микропрепарат, окраска гематоксилином и эозином, увеличение •100) определяется ткань щитовидной железы, окруженная соединительнотканной капсулой, с участками лимфоидной и макрофагальной инфильтрации. Структура фолликулярного эпителия определяется в периферических и центральных участках трансплантата, скопления коллоида, соответствующие интактной структуре железы не определяются, имеются полости, содержащие коллоид в единичных участках на периферии транстантата. Организованная соединительная ткань на границе с донорским участком желудка, лимфоцитарные и плазмоклеточные инфильтраты в центральных и периферических отделах трансплантата.
Предлагаемым способом аутотрансплантации ткани щитовидной железы достигается хороший контакт между трансплантатами, находящимися вне сосудистых связей с реципиентным ложем, и до начала их реваскуляризации питающихся путем диффузии. Сроки реваскуляризации не приводят к развитию избыточных деструктивных процессов в ткани трансплантатов, что соответствует основной задаче операции - сохранению функционально активной ткани щитовидной железы. Моторика желудочной стенки в период приживления трансплантатов не способствует дополнительной травматизации и усилению процессов деструкции и рубцевания трансплантатов. Аутотрансплантация ткани железы, которая подвержена воздействию иммунологических процессов после хирургического воздействия, не является причиной для развития реакции отторжения, не способствует сенсибилизации реципиента и ускоренному отторжению трансплантатов.
Рекомендуется использовать данный способ в практике работы лабораторий экспериментальной хирургии, занимающихся проблемами заболевании щитовидной железы, а также возможно его использование в хирургических отделениях стационаров.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОВРЕЖДЕНИЙ СЕЛЕЗЕНКИ В ЭКСПЕРИМЕНТЕ | 1994 |
|
RU2113017C1 |
| СПОСОБ АУТОТРАНСПЛАНТАЦИИ ТКАНИ СЕЛЕЗЕНКИ | 1992 |
|
RU2062606C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ЖЕЛУДОЧНОГО АНАСТОМОЗА | 2009 |
|
RU2408304C1 |
| СПОСОБ ПЛАСТИКИ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ АОРТЫ В ЭКСПЕРИМЕНТЕ | 1998 |
|
RU2147419C1 |
| СПОСОБ ПЛАСТИЧЕСКОГО УКРЫТИЯ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ НИЖНЕЙ ПОЛОЙ ВЕНЫ | 2004 |
|
RU2283622C2 |
| СПОСОБ АУТОТРАНСПЛАНТАЦИИ ПАРАЩИТОВИДНЫХ ЖЕЛЕЗ | 2010 |
|
RU2457795C2 |
| СПОСОБ ФОРМИРОВАНИЯ АУТОТРАНСПЛАНТАТА | 2009 |
|
RU2398529C2 |
| СПОСОБ ЗАКРЫТИЯ КУЛЬТИ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ ПРИ РЕЗЕКЦИИ ЖЕЛУДКА ПО ПОВОДУ ПЕНЕТРИРУЮЩЕЙ В ПОДЖЕЛУДОЧНУЮ ЖЕЛЕЗУ ЯЗВЫ С АРРОЗИЕЙ ПАНКРЕАТИЧЕСКОГО ПРОТОКА | 1991 |
|
RU2016548C1 |
| СПОСОБ ФАРИНГОПЛАСТИКИ В УСЛОВИЯХ ДЕФИЦИТА ПЛАСТИЧЕСКОГО МАТЕРИАЛА | 2010 |
|
RU2427339C1 |
| СПОСОБ ФОРМИРОВАНИЯ ТОНКОКИШЕЧНО-БРЫЖЕЕЧНОГО АУТОТРАНСПЛАНТАТА | 2010 |
|
RU2426503C1 |



Изобретение относится к медицине, а именно к хирургии. Подготавливают аутотрансплантат ткани щитовидной железы. Ложе для трансплантата формируют в подслизистом слое передней стенки желудка рассечением серозного и мышечного слоев без вскрытия просвета желудка. Погружают трансплантаты в ложе. Восстанавливают целостность стенки желудка наложением серозно-мышечных узловых швов. Способ позволяет улучшить результаты аутотрансплантации щитовидной железы. 4 ил.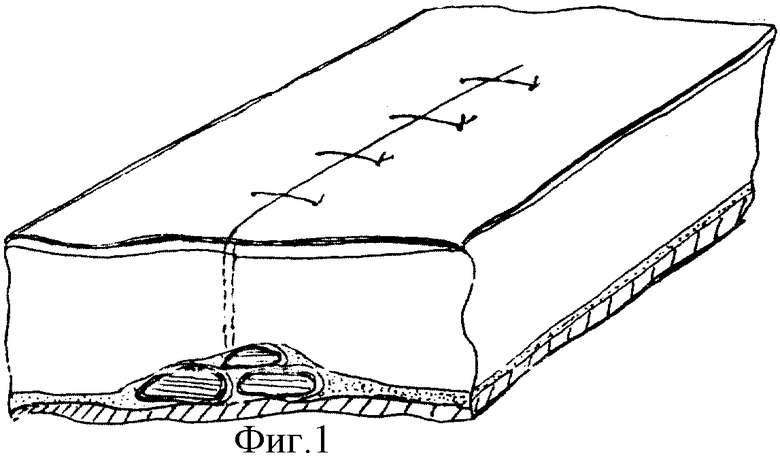
Способ аутотрансплантации ткани щитовидной железы в эксперименте, состоящий в подготовке трансплантатов, формировании ложа для трансплантатов, погружении трансплантатов и ушивании раны, отличающийся тем, что ложе для трансплантатов ткани щитовидной железы формируется в подслизистом слое передней стенки желудка путем рассечения серозного и мышечного слоев без вскрытия просвета желудка, погружаются подготовленные трансплантаты и накладываются серозно-мышечные узловые швы, восстанавливающие целостность стенки желудка.
| ИСМАИЛОВ С.И | |||
| Аутотрансплантация криоконсервированной ткани щитовидной железы в лечении послеоперационного гипотиреоза | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
| ШЕВЕРДИН Ю.П | |||
| и др | |||
| Аутоимплантация ткани щитовидной железы с целью профилактики послеоперационного гипотиреоза | |||
| - Вестник хирургии, 1977, №5, с.8-11 | |||
| Способ хирургического лечения диффузного токсического зоба | 1977 |
|
SU936890A1 |
Авторы
Даты
2002-07-10—Публикация
1999-12-23—Подача