Изобретение относится к препарату, например, в виде капсулы с мягким покрытием, содержащему в качестве действующего вещества циклоспорин. В частности, настоящее изобретение относится к препарату в виде капсулы с мягким покрытием, содержащему циклоспорин в качестве действующего вещества, пропиленкарбонат или полиэтиленгликоль или их смесь, одно соединение или смесь двух или нескольких соединений, выбранного(ых) из группы, включающей эфир жирной кислоты и первичного спирта, триглицерид жирной кислоты со средней длиной цепи и моноглицерид жирной кислоты, в качестве замасливателя и поверхностно-активное вещество, имеющее значение ГЛБ (гидрофильно-липофильный баланс) от 8 до 17.
Циклоспорин представляет собой определенное макромолекулярное (молекулярная масса 1202,64) циклическое пептидное соединение, состоящее из 11 аминокислот и обладающее широким спектром ценных фармакологических действий, в частности иммуносупрессорной активностью и противовоспалительной активностью. Поэтому циклоспорин применялся для подавления врожденных иммунологических реакций живого организма, вызываемых трансплантацией ткани и органа, например, трансплантацией сердца, легкого, печени, почки, панкреатической железы, костного мозга, кожи и роговицы, и прежде всего трансплантацией чужеродных тканей и органов. Кроме того, циклоспорин пригоден для лечения гематологических нарушений, таких, как анемия, различных аутоиммунных болезней, таких, как системная красная волчанка, идиопатический синдром мальабсорбции и т.д., и воспалительных болезней, таких, как артрит, ревматоидные заболевания и т.д. Циклоспорин полезен при лечении болезней, вызванных простейшими, таких, как малярия, шистосомоз и т.д., а в настоящее время его, кроме того, также применяют в химиотерапии.
Циклоспорин является высоко липофильным и гидрофобным соединением. Поэтому циклоспорин слабо растворим в воде и растворим в органических растворителях, таких, как метанол, этанол, ацетон, простой эфир, хлороформ и т.д. Вследствие того, что циклоспорин обладает вышеуказанными характеристиками слабой растворимости в воде, то биологическая доступность циклоспорина при введении его оральным путем является чрезвычайно низкой, и на нее могут оказывать сильное влияние индивидуальные особенности пациента. Поэтому очень трудно поддерживать его эффективную в терапевтическом отношении концентрацию. Кроме того, циклоспорин может оказывать значительные побочные действия, такие, как нефротоксичность. Вследствие низкой растворимости циклоспорина в воде очень трудно изготавливать на его основе препараты для орального введения. В связи с этим были проведены обширные исследования, направленные на создание пригодного для эффективного введения циклоспорина оральным путем препарата, который мог бы обеспечить приемлемую стандартную дозу и соответствующую биологическую доступность.
Согласно известным из уровня техники решениям препараты, пригодные для орального введения слабо растворимого в воде циклоспорина, обычно изготавливали в форме предварительно концентрированной эмульсии.
Один из обычных способов применения такой комбинации предложен в патенте US 4388307, выданном 14 июня 1983 г. В этом патенте описана жидкая композиция на основе циклоспорина с использованием этанола. Согласно способу, изложенному в описании к этому патенту, для получения жидкой композиции циклоспорин объединяют с носителем, содержащим этанол в качестве вторичного поверхностно-активного вещества, оливковое масло в качестве растительного масла и продукт переэтерификации триглицерида природного растительного масла и полиалкиленполиола в качестве поверхностно-активного вещества.
Однако полученную жидкую композицию вводят в форме водных разбавленных растворов, что сильно затрудняет адаптацию индивидуума к ее введению и приготовление стандартной дозы для орального введения.
Для уменьшения неудобства, связанного с растворением жидкой композиции на основе циклоспорина в воде, перед оральным введением жидкую композицию в форме предварительно приготовленного эмульсионного концентрата вносили в капсулу с мягким покрытием, и такой препарат в настоящее время поступает в продажу под названием Sandimmune (зарегистрированный товарный знак). В этом случае в состав содержащей циклоспорин капсулы с мягким покрытием входит этанол, что обусловлено требованиями, связанными с растворимостью циклоспорина. Однако поскольку этанол может проникать через желатиновую оболочку капсулы, так как он является летучим даже при нормальной температуре, для предотвращения испарения этанола из композиций в виде капсул с мягким покрытием при хранении и продаже такие композиции в виде капсул с мягким покрытием могут быть заключены в оболочку из специального упаковочного материала, например, в блистерную упаковку типа алюминий-алюминий.
Недавно оказалось возможным создать препарат на основе циклоспорина, который сохраняет стабильность в течение всего расчетного периода хранения и, кроме того, практически не изменяет биологическую доступность, которая является одинаковой для отдельных пациентов, вследствие чего биологическое действие циклоспорина может поддерживаться на постоянном уровне. Один из препаратов, разработанных для этой цели, описан в корейской выложенной заявке 93-113. Этот препарат поступает в продажу под торговым знаком Sandimmun Neoral. Однако поскольку в этом препарате также используется этанол, он может иметь некоторые недостатки в отношении стабильности при хранении и в нем может изменяться содержание этанола, что характерно для содержащих этанол препаратов-прототипов.
Поэтому авторами изобретения было исследовано большое количество комбинаций различных поверхностно-активных веществ, замасливателей, вторичных поверхностно-активных веществ и т.д. с целью создания композиции на основе циклоспорина, которая являлась бы стабильной и с точки зрения своих фармакокинетических характеристик обеспечивала бы более высокую биологическую доступность и меньшее различие концентраций в крови у отдельных пациентов, чем препараты-прототипы на основе циклоспорина. В результате было обнаружено, что определенная композиция на основе циклоспорина, включающая указанные ниже компоненты, может удовлетворить вышеуказанным требованиям, и тем самым решает положенную в основу настоящего изобретения задачу.
Таким образом, объектом настоящего изобретения является композиция, пригодная для приготовления капсул с мягким покрытием, включающая циклоспорин в качестве действующего вещества, гидрофильное вещество полиэтиленгликоль или негидрофильное вещество пропиленкарбонат либо их смесь, замасливатель, как он определен ниже, и поверхностно-активное вещество.
Следующим объектом настоящего изобретения является препарат в виде капсулы с мягким покрытием, содержащий композицию, которая включает циклоспорин в качестве действующего вещества, гидрофильное вещество полиэтиленгликоль, негидрофильное вещество пропиленкарбонат либо их смесь, одно соединение или смесь двух или более соединений, выбранного(ых) из группы, включающей эфир жирной кислоты и первичного спирта, триглицерид жирной кислоты со средней длиной цепи (при необходимости) и моноглицерид жирной кислоты, в качестве замасливателя и поверхностно-активное вещество, имеющее значение ГЛБ (гидрофильно-липофильный баланс) от 8 до 17.
Еще одним объектом настоящего изобретения является способ изготовления указанного выше препарата в виде желатиновых капсул с мягким покрытием.
Хотя настоящее изобретение описано применительно к желатиновым капсулам с мягким покрытием, следует отметить, что в его объем включена и сама композиция, которая может применяться, например, в виде раствора для питья, например, как Sandimmun Neoral, или в виде иных стандартных дозируемых форм.
Один из объектов настоящего изобретения относится к содержащей циклоспорин капсуле, которая обладает высокой стабильностью при хранении, так что с течением времени происходит лишь незначительное изменение композиции, и повышенной биологической доступностью и которая содержит композицию, включающую циклоспорин в качестве действующего вещества, гидрофильное вещество полиэтиленгликоль или негидрофильное вещество пропиленкарбонат либо их смесь в качестве второго компонента, замасливатель, как он определен ниже, и поверхностно-активное вещество.
Для изготовления такого препарата в виде капсулы с мягким покрытием, содержащей композицию на основе циклоспорина, необходимо использовать желатиновую оболочку. Однако, если капсулу с мягким покрытием изготавливают с использованием обычной капсульной оболочки, содержащей в качестве пластификатора глицерин, то препарат в виде капсулы с мягким покрытием имеет определенные недостатки, связанные с тем, что эмульсионное состояние предварительно приготовленного эмульсионного концентрата может изменяться вследствие проникновения глицерина в эмульсию, что приводит к существенному снижению растворимости циклоспорина и в результате этого к осаждению циклоспорина из эмульсии.
Поэтому в настоящем изобретении в качестве оболочки капсулы с мягким покрытием предпочтительно выбирают желатиновую оболочку, в которой в качестве пластификатора используют смесь пропиленгликоля и полиэтиленгликоля, а не глицерин, что позволяет решить проблему, связанную с проникновением глицерина.
Однако, если ленту оболочек капсул, содержащую пропиленгликоль и полиэтиленгликоль согласно настоящему изобретению, изготавливают методом водяного охлаждения, который обычно применяют для барабанных холодильников, то ее трудно извлечь из барабана. Такую извлекаемость ленты оболочек капсул из охлаждающего барабана можно улучшить путем переохлаждения барабанного холодильника с помощью непрерывной циркуляции воды для понижения температуры ленты приблизительно до 17oС. Однако лента оболочек капсул, охлажденная до более низкой температуры, может обладать плохой способностью к герметичному запечатыванию в процессе капсулирования, что может привести к снижению производительности.
Поэтому в способе изготовления ленты не содержащих глицериновый пластификатор оболочек капсул по настоящему изобретению вместо применяемого в прототипах метода водяного охлаждения используют метод воздушного охлаждения, при котором ленту оболочек капсул охлаждают до оптимальной температуры путем подвода воздуха от вентилятора, что позволяет легко извлечь ее из барабанного холодильника, и при котором ленту в дальнейшем выдерживают при оптимальной температуре приблизительно 21oС для улучшения способности герметично запечатываться в процессе капсулирования, что обеспечивает высокую производительность.
Как указано выше, продукты по настоящему изобретению могут быть изготовлены с использованием не содержащей глицерин желатиновой оболочки капсулы и с применением метода воздушного охлаждения композиции, которая не содержит этанол, являющийся летучим растворителем с низкой температурой кипения, и поэтому она обладает высокой стабильностью при хранении, так что с течением времени происходит лишь незначительное изменение композиции, и повышенной биологической доступностью.
Более конкретно настоящее изобретение относится к препарату на основе циклоспорина, содержащему композицию, включающую
1) циклоспорин в качестве действующего вещества,
2) полиэтиленгликоль или пропиленкарбонат либо их смесь,
3) одно соединение или смесь двух или более соединений, выбранного(ых) из группы, включающей эфир жирной кислоты и первичного спирта, триглицерид жирной кислоты со средней длиной цепи (при необходимости) и моноглицерид жирной кислоты, в качестве замасливателя и
4) поверхностно-активное вещество, имеющее значение ГЛБ (гидрофильно-липофильный баланс) от 8 до 17, и, например, заключенную в желатиновую оболочку, содержащую в качестве пластификатора полиэтиленгликоль или пропиленгликоль. Другим объектом настоящего изобретения является препарат на основе циклоспорина, который содержит композицию, включающую
1) циклоспорин в качестве действующего вещества и
2) пропиленкарбонат.
Еще одним объектом настоящего изобретения является указанная композиция, не содержащая полиэтиленгликоля.
Такая композиция, также являющаяся композицией по изобретению, может необязательно дополнительно включать любой другой компонент, представленный в настоящем описании, при необходимости в количествах, указанных в настоящем описании.
Циклоспорин, используемый в качестве фармацевтически активного вещества в композиции по настоящему изобретению, представляет собой циклическое пептидное соединение, обладающее описанной выше ценной иммуносупрессорной и противовоспалительной активностью. Хотя в качестве циклоспоринового компонента по настоящему изобретению также могут использоваться циклоспорин А, В, С, D, G и т.п., наболее предпочтительным является циклоспорин А, поскольку его клиническая эффективность и фармакологические свойства хорошо известны в данной области.
В качестве второго компонента композиции по настоящему изобретению, который может действовать как вторичное поверхностно-активное вещество, могут применяться пропиленкарбонат или полиэтиленгликоль либо их смеси.
В качестве негидрофильного вещества может использоваться пропиленкарбонат, который имеет высокую температуру кипения (приблизительно 242oС), является нелетучим, обладает слабой гигроскопичностью и проницаемостью через оболочку и в котором хорошо растворим циклоспорин.
В альтернативном варианте в качестве гидрофильного вещества также может применяться полиэтиленгликоль, который имеет высокую температуру кипения, является нелетучим, не проникает через желатиновую оболочку капсулы с мягким покрытием и в котором хорошо растворим циклоспорин. Хотя в композиции по настоящему изобретению может применяться любой полиэтиленгликоль, который может быть разжижен, предпочтительно следует применять полиэтиленгликоль (ПЭГ) с молекулярной массой от 200 до 600 (в частности ПЭГ 200).
В настоящем изобретении также может использоваться смесь негидрофильного вещества и гидрофильного вещества, как определено выше. Если в качестве компонента по настоящему изобретению применяют смесь полиэтиленгликоля и пропиленкарбоната, они обычно могут быть объединены в массовом соотношении 1: 0,1-5, предпочтительно 1:0,1-3, наиболее предпочтительно 1:0,2-2.
В настоящем изобретении за счет применения полиэтиленгликоля и пропиленкарбоната достигаются определенные преимущества. Так, например, улучшается стабильность при хранении композиции, содержащей циклоспорин, и, следовательно, содержание входящих в нее компонентов сохраняется практически на постоянном уровне. Кроме того, применение пропиленкарбоната может даже увеличить растворимость циклоспорина как действующего вещества и ингибировать проникновение воды из оболочки желатиновой капсулы в композицию, повышая тем самым стабильность композиции.
В композиции по настоящему изобретению второй компонент предпочтительно применяют в соотношении от 0,1 до 10 мас.частей, более предпочтительно от 0,5 до 8 мас. частей и наиболее предпочтительно от 1 до 5 мас.частей в пересчете на 1 мас.часть циклоспорина.
Третьим компонентом, применяемым в предварительно приготовленном эмульсионном концентрате по настоящему изобретению, является замасливатель. В качестве замасливателя по настоящему изобретению может применяться одно соединение либо смесь двух или более соединений, выбранное(ых) из группы, включающей эфир жирной кислоты и первичного спирта, триглицериды жирной кислоты со средней длиной цепи (если они присутствуют) и моноглицериды жирной кислоты. Эфир жирной кислоты и первичного спирта, который может применяться согласно настоящему изобретению, может включать эфир жирной кислоты с 8-20 атомами углерода и первичного спирта с 2-3 атомами углерода, например, изопропилмиристат, изопропилпальмитат, этиллинолеат, этилолеат и т.д., при этом особенно предпочтительным является эфир линолевой кислоты и этанола. Кроме того, в качестве триглицерида жирной кислоты со средней длиной цепи (если он присутствует) может применяться триглицерид насыщенной жирной кислоты, имеющей от 8 до 10 атомов углерода, при этом наиболее предпочтительно использовать в качестве триглицерида насыщенной жирной кислоты и растительного масла триглицерид каприловой/каприновой кислоты. Моноглицерид жирной кислоты, который также может применяться в качестве замасливателя согласно настоящему изобретению, включает моноглицерид жирной кислоты, имеющей от 18 до 20 атомов углерода, в частности моноглицерид олеиновой кислоты.
В предварительно приготовленном эмульсионном концентрате по настоящему изобретению замасливатель может применяться в соотношении от 1 до 10 мас. частей, предпочтительно от 2 до 6 мас.частей на 1 мас.часть циклоспорина.
Предпочтительно в качестве замасливателя моноглицерид жирной кислоты и эфир жирной кислоты присутствуют, например, в соотношении от 1:1 до 1:2, например, от 1:1 до 1:1,2.
Необязательно также присутствует триглицерид каприловой/каприновой кислоты, например, в соотношении от 1:0,1 до 1:0,2 к этиллинолеату.
В масляной смеси, применяемой в качестве замасливателя по настоящему изобретению, массовое соотношение в смеси моноглицерид жирной кислоты/эфир жирной кислоты и первичного спирта/триглицерид жирной кислоты со средней длиной цепи (если он присутствует) обычно может находиться в интервале 1: 0,1-5:0,1-10, предпочтительно в 1:0,1-3,0:0,1-3,0.
Четвертым компонентом, применяемым в композиции по настоящему изобретению, является поверхностно-активное вещество. Пригодные для использования согласно настоящему изобретению поверхностно-активные вещества включают любые фармацевтически приемлемые поверхностно-активные вещества, значение ГЛБ (гидрофильно-липофильный баланс) которых составляет от 8 до 17 и которые обладают способностью стабильно эмульгировать липофильную часть композиции, включающую содержащий циклоспорин замасливатеь, и гидрофильную часть, включающую вторичное поверхностно-активное вещество, в воде с образованием стабильной микроэмульсии. Примеры предпочтительных поверхностно-активных веществ но настоящему изобретению включают полиоксиэтиленовые продукты гидрогенизированных растительных масел, эфиры полиоксиэтиленсорбитана и жирной кислоты и т.п., например, NIKKOL HCO-50, NIKKOL НСО-40, NIKKOL НСО-60, TWEEN 20, TWEEN 21, WEEN 40, TWEEN 60, TWEEN 80, TWEEN 81 и т.д. В частности, предпочтительно применение гидрогенизированного касторового масла с содержанием этиленоксидных звеньев 50 молей, поступающего в продажу под товарным знаком NIKKOL HCO-50 (фирма NIKKO Chemical Co., Ltd), и сорбитанмонолаурата с содержанием этиленоксидных звеньев 20 молей, поступающего в продажу под товарным знаком TWEEN 20 (фирма ICI Chemicals) и имеющего кислотное число приблизительно 48-56, гидроксильное число 45-55 и значение рН (5%) 4,5-7,0.
Поверхностно-активное вещество может включать либо одно любое из вышеуказанных поверхностно-активных веществ, либо предпочтительно комбинацию двух или более поверхностно-активных веществ, выбранных из вышеуказанных поверхностно-активных веществ. В композиции по настоящему изобретению поверхностно-активные вещества могут применяться в соотношении от 1 до 10 мас.частей, предпочтительно в соотношении от 2 до 8 мас.частей на 1 мас.часть циклоспорина.
Кроме того, если в композиции по настоящему изобретению используется смесь двух поверхностно-активных веществ, например, гидрогенизированного касторового масла, содержащего 50 молей этиленоксидных звеньев, и сорбитанмонолаурата, содержащего 20 этиленоксидных звеньев, принятое массовое соотношение гидрогенизированного касторового масла, содержащего 50 молей этиленоксидных звеньев, и сорбитанмонолаурата, содержащего 20 молей этиленоксидных звеньев, предпочтительно находится в диапазоне 1:0,1-5, более предпочтительно в диапазоне 1:0,5-4.
В композиции по настоящему изобретению четыре компонента предпочтительно присутствуют в массовом соотношении циклоспорин/второй компонент/замасливатель/поверхностно-активное вещество 1:0,1-10:1 -10:1 -10, более предпочтительно 1:0,5-8:2-6:2-8.
Помимо этой композиции, в качестве дополнительных предпочтительных композиций по настоящему изобретению можно отметить композиции, приведенные в следующих примерах.
Для орального введения композиция по настоящему изобретению, содержащая указанные выше компоненты, может быть изготовлена в виде капсулы с мягким покрытием. Поскольку в препарате в виде капсулы с мягким покрытием по настоящему изобретению не используется этанол в качестве летучего растворителя с низкой температурой кипения, этот препарат является стабильным с фармацевтической точки зрения и может удовлетворять требованиям по улучшению характеристик, в том числе по улучшению биологической доступности.
Однако может оказаться, что этой цели трудно добиться при использовании обычной оболочки капсул с мягким покрытием с помощью общепринятого способа изготовления капсул с мягким покрытием. Если капсулу с мягким покрытием изготавливают с использованием обычной оболочки, содержащей в качестве пластификатора глицерин, то изготовленная таким образом капсула с мягким покрытием может иметь определенные недостатки, заключающиеся в том, что эмульсионное состояние предварительно приготовленного эмульсионного концентрата может изменяться вследствие проникновения в эмульсию глицерина и происходящего в результате этого существенного понижения растворимости циклоспорина, что может привести к осаждению циклоспорина из эмульсии.
Поэтому согласно изобретению предусмотрено, что, если оболочку капсулы изготавливают, используя в качестве пластификатора смесь полиэтиленгликоля и пропиленгликоля, а не глицерин, то может быть получен препарат в виде капсулы с мягким покрытием, который сохраняет стабильность в течение длительного периода времени. Хотя в принципе в качестве пластификатора может применяться любой полиэтиленгликоль, который может быть разжижен, предпочтительно применять полиэтиленгликоль, имеющий молекулярную массу от 200 до 600.
В частности, предпочтительно использовать полиэтиленгликоль 200. В оболочке капсулы с мягким покрытием по настоящему изобретению предпочтительно используют смесь полиэтиленгликоля и пропиленгликоля в соотношении от 0,1 до 0,5 мас. частей, более предпочтительно от 0,1 до 0,4 мас.частей и наиболее предпочтительно от 0,2 до 0,3 мас.частей на 1 мас.часть желатина, используемого для изготовления оболочки капсулы. В смесь полиэтиленгликоля и пропиленгликоля, используемой в качестве пластификатора, пропиленгликоль входит предпочтительно в соотношении от 1 до 10 мас.частей, более предпочтительно в соотношении от 3 до 8 мас.частей и наиболее предпочтительно в соотношении от 3 до 6 мас.частей на 1 мас.часть полиэтиленгликоля.
С целью улучшить извлекаемость ленты для оболочек капсул из барабанного холодильника в способе изготовления ленты желатиновых оболочек капсул по настоящему изобретению применяют метод воздушного охлаждения вместо метода водяного охлаждения. При применении этого метода воздушного охлаждения, поскольку лента оболочек капсул не перегревается и легко может быть извлечена из барабанного холодильника, в котором поддерживается оптимальная температура приблизительно 21oС, способность герметично запечатываться в процессе капсулирования является высокой, что гарантирует высокую производительность, и, следовательно, эффективность осуществления предлагаемого способа достаточно высока.
При изготовлении капсулы с мягким покрытием по настоящему изобретению приемлемый объемный расход воздуха в барабанном холодильнике для охлаждения оболочки капсулы предпочтительно составляет от 5 до 15 м3/мин, наиболее предпочтительно приблизительно 10 м3/мин.
Поскольку в качестве второго компонента по настоящему изобретению пропиленкарбонат может быть использован индивидуально или в качестве его основного компонента, при изготовлении содержащего циклоспорин препарата в виде капсулы с мягким покрытием, сохраняющего стабильность в течение длительного периода времени, не требуется использовать определенный пластификатор для желатиновой оболочки.
В таких желатиновых оболочках можно использовать без каких-либо ограничений один или несколько пластификаторов, выбранных из группы, включающей глицерин, сорбит, гексантриол, пропиленкарбонат, гексангликоль, сорбитаны, простой эфир тетрагидрофурилового спирта, моноэтиловый эфир диэтиленгликоля, 1,3-диметил-2-имидазолидон, диметилизосорбид и т.д. Однако следует отметить, что пластификаторы, которые могут использоваться согласно настоящему изобретению, не ограничены перечисленными выше.
При изготовлении капсул с мягким покрытием, содержащих композицию по настоящему изобретению, препарат в виде капсулы при необходимости может дополнительно содержать фармацевтически приемлемые добавки, обычно применяемые при изготовлении капсул с мягким покрытием. Такие добавки включают, например, лецитин, регулятор вязкости, ароматизатор (например, масло мяты перечной и т.д.), антиоксидант (например, токоферол, витамин Е и т.д.), консервант (например, парабен и т.д.), краситель, аминокислоты и т.д.
Препарат в виде капсулы с мягким покрытием по настоящему изобретению может быть изготовлен путем тщательного смешения вторичного поверхностно-активного вещества, замасливателя и поверхностно-активного вещества, растворения при перемешивании в этой смеси циклоспорина и осторожного нагревания до температуры приблизительно 60oС и затем заполнения в машине для изготовления капсул с мягким покрытием с использованием метода воздушного охлаждения приготовленным концентратом с вышеуказанными фармацевтически приемлемыми добавками, обычно применяемыми при изготовлении капсул с мягким покрытием, или без этих добавок, пригодных для циклоспорина капсул с мягким покрытием, желатиновая оболочка которых содержит в качестве пластификатора полиэтиленгликоль и пропиленгликоль.
Композиции и препаративные формы по настоящему изобретению пригодны при таких же показаниях и могут вводиться таким же путем и в таком же диапазоне доз, что и известные композиции, содержащие циклоспорин, с применением при необходимости регулировки дозы на основе стандартных опытов по оценке биологической доступности на животных, например, на собаках, или на людях, например, как описано ниже.
Если составы каких-либо эксципиентов или компонентов не представлены конкретно в настоящем описании, их перечень можно найти в литературе, например, у Н.Р. Fiedler в Lexikon der Hilfsstoffe, изд-во Edito Cantor, Aulendorf, Германия, 4-е изд., 1996, в Handbook of Pharmaceutical Excipients, American Pharmaceutical Association, Washington, и в The Pharmaceutical Society, Лондон, 2-е изд., 1994, а также в заявке на корейский патент 94-29208, поданной 9.11.94.
Настоящее изобретение более подробно проиллюстрировано на следующих примерах. Однако следует подчеркнуть, что эти примеры никоим образом не ограничивают объем изобретения.
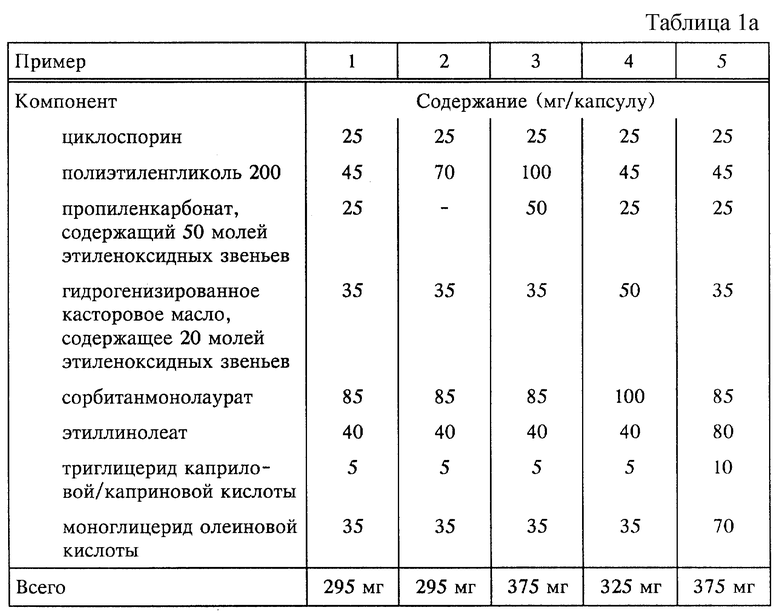
Примеры 1-5 представлены в табл.1а.
Пример 6
Препарат в виде капсулы с мягким покрытием, содержащий композицию из примера 1, изготавливали с использованием приведенной ниже композиции для оболочки капсулы и затем визуально наблюдали за изменением характеристик и состояния содержимого в результате проникновения глицерина.
6.1 (Контрольная группа)
Компонент - Массовое соотношение
желатин - 20
очищенная вода - 16
глицерин - 9
6.2. (Тестируемая группа)
Компонент - Массовое соотношение
желатин - 20
очищенная вода - 16
пропиленгликоль - 4
полиэтиленгликоль 200 - 1
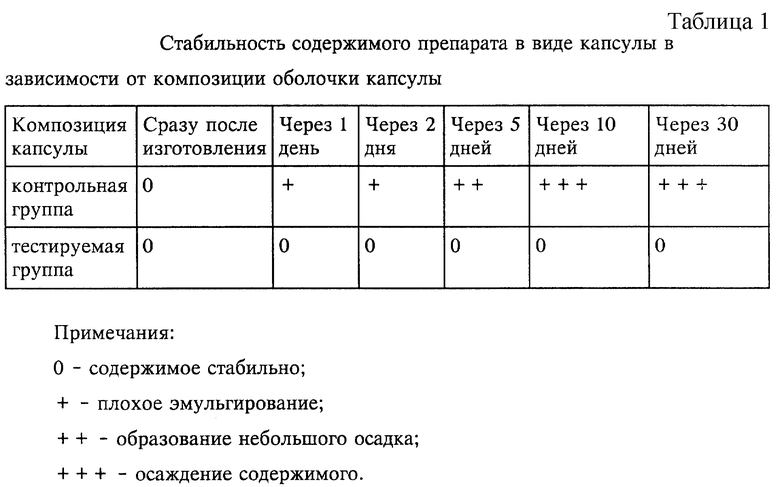
Полученные результаты представлены в таблице 1.
Как следует из результатов, представленных в таблице 1, препарат в виде капсулы, изготовленной с использованием композиции 6.1 (контрольная группа), содержащей в качестве пластификатора глицерин, имеет определенные недостатки, включающие образование осадка вследствие проникновения глицерина, тогда как препарат в виде капсулы, изготовленный с использованием композиции 6.2 (тестируемая группа), содержащей в качестве пластификатора полиэтиленгликоль и пропиленгликоль, сохраняет стабильное состояние.
Пример 7
Препарат в виде капсулы с мягким покрытием, содержащий композицию из примера 1, изготавливали с использованием композиции 6.2 (тестируемая группа) для оболочки капсулы, указанной в приведенном выше примере 6, с использованием соответственно метода водяного охлаждения (температура воды приблизительно 12oС) и метода воздушного охлаждения (объемный расход воздуха приблизительно 10 м3/мин).
В каждом случае оценивали и сравнивали извлекаемость ленты оболочек капсул из барабанного холодильника. Полученные результаты представлены в таблице 2.
Как следует из результатов, представленных в таблице 2, препарат в виде капсулы с мягким покрытием, изготовленный с использованием метода воздушного охлаждения по настоящему изобретению, обладает существенно лучшей извлекаемостью из барабанного холодильника по сравнению с таковым, изготовленным с использованием метода водяного охлаждения. В частности, обычно считается, что если величина угла, необходимая для извлечения ленты желатиновых оболочек из барабанного холодильника составляет приблизительно 70o или более, то извлекаемость является плохой, а если величина угла, необходимая для извлечения ленты желатиновых оболочек из барабанного холодильника меньше, приблизительно 70o, то извлекаемость является хорошей. Препарат в виде капсулы с мягким покрытием, полученный методом водяного охлаждения, неудовлетворительно извлекался из барабанного холодильника даже в том случае, если композицию извлекали под углом 100o или более.
В отличие от этого препарат в виде капсулы с мягким покрытием, изготовленный с использованием метода воздушного охлаждения по настоящему изобретению, может быть легко извлечен из барабанного холодильника при угле 50o и менее и, следовательно, может обеспечить хорошую прочность герметичного запечатывания и высокую производительность.
Пример 8
Биологическую доступность тестируемой препаративной формы, изготовленной путем капсулирования композиции из примера 1 в желатиновую оболочку, состав которой указан в разделе 6.2, сравнивали с биологической доступностью поступающего в продажу продукта SANDIMMUN Capsule, содержащего этанол, который использовали в качестве контрольного препарата для оценки влияния препарата на основе циклоспорина по настоящему изобретению на биологическую доступность циклоспорина и на ее различие для отдельных пациентов.
В этом эксперименте как тестируемый препарат, так и контрольный препарат вводили из расчета 300 мг циклоспорина на 1 кг веса кролика.
Кроликов содержали в течение 4 дней или более в одинаковых условиях в проволочных клетках на одинаковом корме, состоящем из твердой питательной композиции для кроликов. При проведении опытов по оральному введению препарата кроликов закрепляли на 48 ч в стальной клетке, ограничивающей движение, и в течение этого времени кролики имели свободный доступ к воде.
Назогастральный зонд диаметром 5 мм, поверхность которого была предварительно смазана вазелином для уменьшения трения, вводили в пищевод на глубину 30 см. Каждый из тестируемых препаратов и контрольный препарат эмульгировали с помощью 50 мл воды и затем вводили в шприц, присоединенный к назогастральному зонду. Ушные вены кроликов расширяли с использованием ксилола и затем с помощью обработанного гепарином одноразового шприца отбирали образцы крови из ушной вены каждого кролика до опыта и через 0,5, 1, 1,5, 2, 3, 4, 6, 10 и 24 ч. К 1 мл полученной таким образом крови добавляли 0,5 мл водного насыщенного раствора хлорида натрия и 2 мл простого эфира, а затем смесь встряхивали в течение 5 мин и центрифугировали в течение 10 мин при 5000 об/мин для отделения надосадочной жидкости (эфирный слой). Отбирали 1 мл надосадочной жидкости и подвергали обработке с использованием активированной двуокиси кремния типа sep-pak® (фирма Waters). Обработанный продукт sep-pak® промывали 5 мл н-гексана и элюировали 2 мл метанола. Элюат упаривали досуха в атмосфере азота при пониженном давлении. Остаток анализировали с помощью ЖХВР (жидкостная хроматография высокого разрешения) [условия ЖХВР: колонка μ-Bondpak®C18 (фирма Waters), подвижная фаза CH2CN:MeOН:H2O в соотношении 55:15:30, обнаружение при 210 нм, скорость потока 1,0 мл/мин, температура колонки 70oС, чувствительность 0,01 единиц спектральной поглощательной способности, объем инъекции 100 мкл].
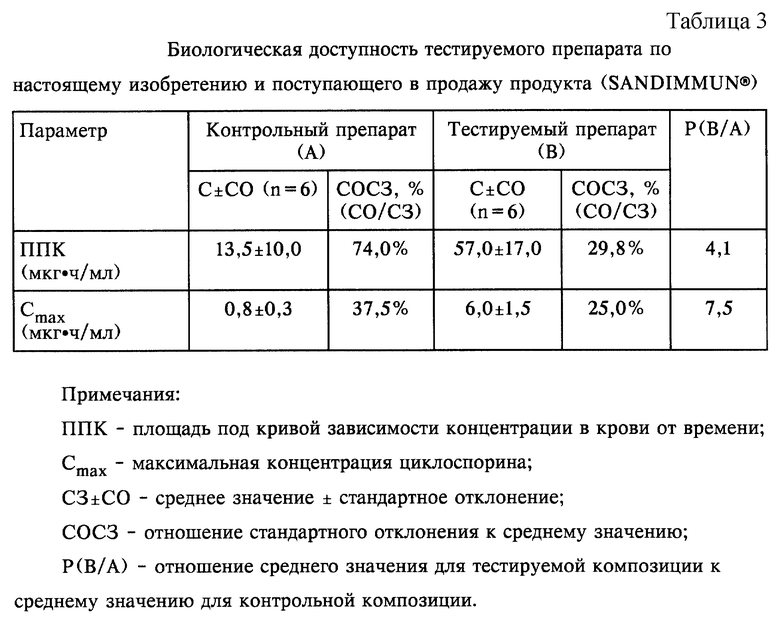
Результаты, полученные для тестируемого препарата и контрольного препарата, приведены в таблице 3.
Как следует из таблицы 3, тестируемый препарат имеет большие значения ППК-показателя и Сmax, которые превышают соответственно приблизительно в 4 раза и приблизительно в 7 раз таковые для контрольного препарата. Следовательно, можно считать, что биологическая доступность тестируемого препарата значительно выше биологической доступности контрольного препарата. Кроме того, тестируемый препарат по настоящему изобретению приводит к уменьшению различий в величине ППК приблизительно в 2 раза или более и в величине Сmax приблизительно в 1,5 раза между соответствующими подопытными животными (СОСЗ, %) по сравнению с контрольным препаратом.
Следовательно, можно считать, что при введении препарата в виде капсулы с мягким покрытием по настоящему изобретению пероральным путем она обладает приблизительно в 4 раза большей биологической доступностью циклоспорина по сранению с известным поступающим в продажу продуктом SANDIMMUN® Capsule, содержащим этанол, при этом также снижается различие между биологической доступностью циклоспорина для различных особей и в то же время сохраняется стабильность без какого-либо изменения в течение длительного периода хранения. Таким образом, очевидно, что препарат в виде капсулы с мягким покрытием по настоящему изобретению обладает существенно лучшими характеристиками среди известных в данной области препаратов в виде содержащих циклоспорин капсул с мягким покрытием.
Пример 9
Изготавливают мягкие гели, имеющие состав, представленный в табл.3а.
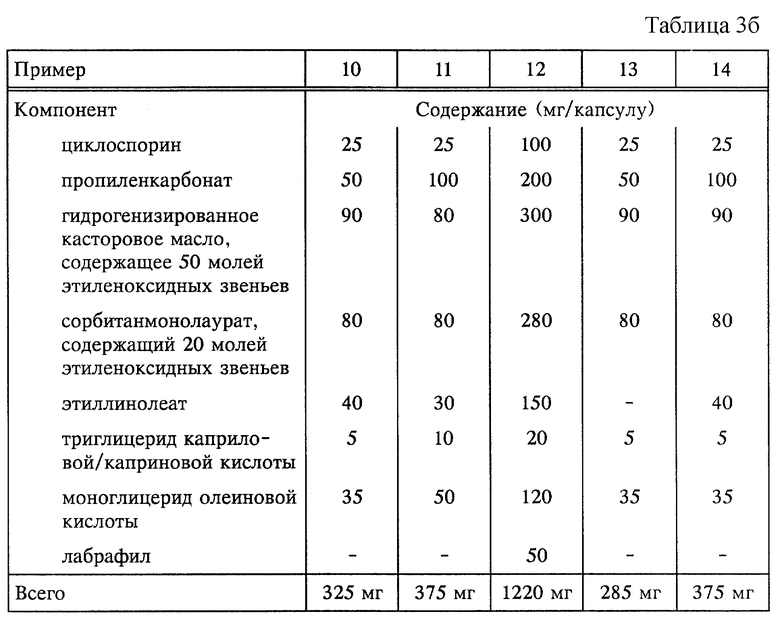
Примеры 10-14 (см. табл. 3б).
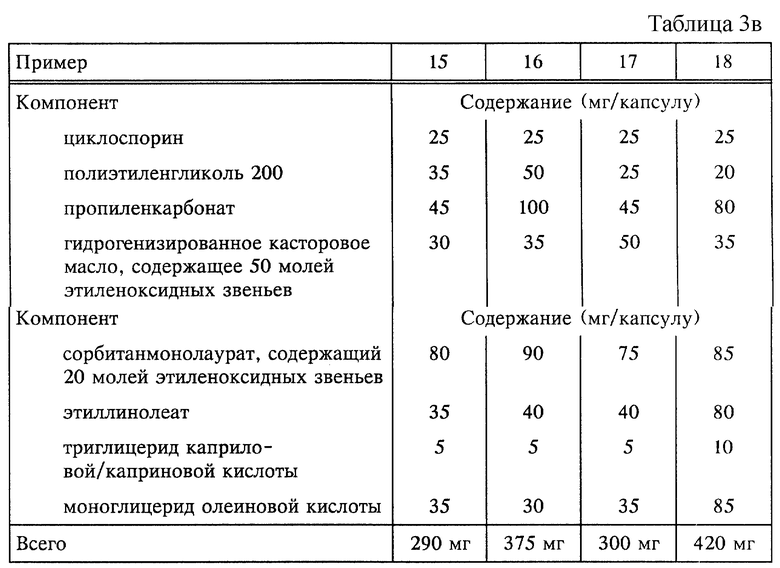
Примеры 15-18 (см. табл. 3в).
Пример 19
Биологическую доступность тестируемого препарата, изготовленного на основе композиции из примера 10, сравнивали с биологической доступностью поступающего в продажу продукта, содержащего этанол, а именно, SANDIММUN Capsule, который использовали в качестве контрольного препарата для оценки влияния содержащего циклоспорин препарата по настоящему изобретению на биологическую доступность циклоспорина и ее различие для отдельных особей.
Протокол эксперимента был таким же, как и описанный в примере 8.
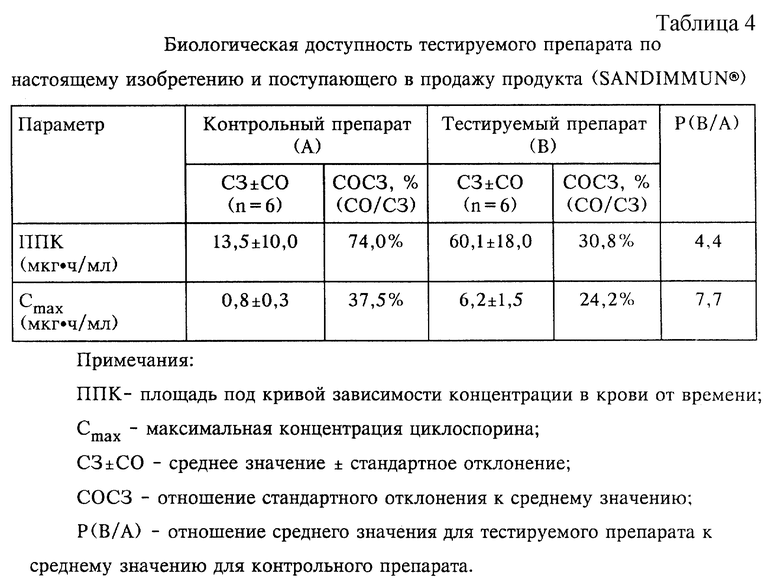
Результаты, полученные для тестируемого препарата и контрольного препарата, приведены в таблице 4.
Как следует из данных таблицы 4, тестируемый препарат имеет большие значения ППК-показателя и Сmax, которые превышают соответственно приблизительно в 4 раза и приблизительно в 7 раз или более таковые для контрольного препарата. Следовательно, можно считать, что биологическая доступность тестируемого препарата значительно выше биологической доступности контрольного препарата. Кроме того, тестируемый препарат по настоящему изобретению приводит к уменьшению различий в величине ППК приблизительно в 2 раза или более и в величине Сmax приблизительно в 1,5 раза между соответствующими подопытными животными (СОСЗ, %) по сравнению с контрольным препаратом.
Следовательно, можно считать, что при введении пероральным путем препарата в виде капсулы с мягким покрытием по настоящему изобретению он обладает приблизительно в 4 раза большей биологической доступностью циклоспорина по сравнению с известным поступающим в продажу продуктом SANDIMMUN® Capsule, содержащим этанол, а также дает уменьшение различия между биологической доступностью циклоспорина для различных особей, и в то же время сохраняется стабильность без какого-либо изменения в течение длительного периода хранения. Таким образом, очевидно, что препарат в виде капсулы с мягким покрытием по настоящему изобретению обладает существенно лучшими характеристиками среди известных в данной области препаратов в виде содержащих циклоспорин капсул с мягким покрытием.


Изобретение может быть использовано в фармации для изготовления препаратов циклоспорина, применяемых в медицине. Заявлен препарат, содержащий циклоспорин, пропиленкарбонат, поверхностно-активное вещество, имеющее величину гидрофильно-липофилного баланса 8-17, и по меньшей мере одно соединение, выбранное из группы, содержащей эфир жирной кислоты и первичного спирта, триглицерид жирной кислоты со средней длиной цепи и моноглицерид жирной кислоты в качестве замасливателя. Второй вариант препарата содержит циклоспорин и пропиленкарбонат. Изобретение позволяет получить лекарственные формы циклоспорина, сохраняющие стабильность в течение всего периода их хранения. Они не изменяют биодоступность, поэтому действие циклоспорина может поддерживаться на постоянном уровне. 2 с. и 8 з.п. ф-лы, 8 табл.
| RU 94046413 А1, 10.11.1996 | |||
| АНТИФРИКЦИОННАЯ КОМПОЗИЦИЯ | 2005 |
|
RU2295546C1 |
| US 5589455 А, 31.12.1996 | |||
| Устройство для регулирования относительного положения уровней в емкостях | 1978 |
|
SU711550A1 |
Авторы
Даты
2002-07-20—Публикация
1998-03-12—Подача