Изобретение относится к фармацевтическим композициям, полезным для защиты митохондриального генома и/или митохондрий от повреждений или для лечения заболеваний, связанных с такими повреждениями, причем эти композиции включают производное гидроксамовой кислоты формулы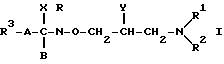
где R1 является атомом водорода или С1-5 алкильной группой,
R2 является атомом водорода, С1-5 алкильной группой, С3-8 циклоалкильной группой или фенильной группой, которая может быть замещена гидроксильной или фенильной группой, или R1 и R2 совместно с атомом азота, к которому они присоединены, образуют пяти - восьмичленное кольцо, которое может содержать еще один или более атом(ов) азота, кислорода или серы, и указанное кольцо может быть соединено с бензольным кольцом,
R3 является атомом водорода, фенильной группой, нафтильной группой или пиридильной группой, причем указанные группы могут быть замещены одним или более атомом(ами) галогена или C1-4 алкоксильной(ыми) группой(ами),
Y является гидроксильной группой,
Х является аминогруппой,
R образует с В химическую связь,
А является C1-4 алкиленовой группой или химической связью или группой формулы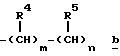
где R4 является атомом водорода или фенильной группой,
R5 является атомом водорода или фенильной группой,
m имеет значение 0,1 или 2,
n имеет значение 0, 1 или 2,
или его фармацевтически приемлемую кислотную аддитивную соль в качестве активного ингредиента.
HU-P 177578 и его эквивалент US-P 4308399 описывает производные гидроксамовой кислоты, относящиеся к группе соединений формулы I, которые являются полезными для лечения диабетической ангиопатии.
HU-P 207998 и его эквивалент Е-Р 417210 также описывают галогениды гидроксамовой кислоты, имеющие избирательный бета-блокирующий эффект, таким образом, являющиеся полезными для лечения диабетической ангиопатии.
Заявка HU-P 2385/92, опубликованная под T/66350, описывает другие производные гидроксамовой кислоты. Эти известные соединения могут быть использованы в лечении сосудистых деформаций, в основном, в терапии сахарного диабета.
Хорошо известно, что геном ядра человеческих клеток кодирует около 100000 генов, но в цитоплазме также существует небольшой, независимый митохондриальный геном /Wellace, D.C, Science, 256, 628-632 (1992)/.
Митохондриальный геном кодирует всего 13 генов /Clayton, D.A., Cell, 28, 693-705 (1982)/, но без них клетка не способна потреблять кислород, поэтому, как следствие повреждений митохондриального генома, клетка становится анаэробной. В отличие от ядерного генома митохондриальный геном не обладает способностью к репарации ДНК и митохондриальная ДНК (мтДНК) не стабилизирована гистонами, что делает митохондриальные гены гораздо более уязвимыми, чем гены, кодируемые ядром /Tzagoloff, A., Myer, A.M., Annu. Rev. Biochem., 55, 249-285 (1986)/. Поглощение более чем 90% кислорода клеткой происходит во внутренней митохондриальной мембране, где, помимо нормального оксидирования, также формируются свободные радикалы кислорода /Stryer, L., Biochemistry, 4 издание, W.H. Freeman and Co., New York, 1995/. Такие свободные радикалы могут легко модифицировать митохондриальную ДНК в непосредственной близости от их формирования. Формирование свободных радикалов реактивного кислорода значительно повышается, например во время реоксигенации вследствие ишемии, при которой повышенная концентрация свободных радикалов может приводить к значительным и необратимым повреждениям митохондриальной ДНК /Marklund, S.L., J. Mol. Cell. Cardiol., 20, (Приложение II), 23-30 (1988)/. Даже при нормальных условиях свободные радикалы причиняют малые, но кумулятивные повреждения мтДНК. Поэтому очевидно, что повреждения мтДНК повышаются с возрастом /Wellace, D.C., Annu. Rev. Biochem., 61, 1175-1212 (1992)/, хотя уровень таких повреждений зависит от индивидуального организма, и что такие повреждения мтДНК могут легко приводить к развитию кардиомиопатии и нейродегенеративных заболеваний у пожилых людей /Cortopassi, G.A., Arnheim, N., Nucleic Acids Res., 18, 6027-6033 (1990)/.
Из-за нарушений метаболизма энергии клетки повреждения митохондриального генома могут вызывать тяжелые заболевания, такие как миопатии /Luft, R., Proc. Natl. Acad. Sci. USA, 91, 8731-8738 (1994)/, расширенные или гипертрофические кардиомиопатии /Ozawa, Т. et al., Biochem. Biophys. Res. Commun., 170, 830-836 (1990)/, далее могут играть роль в усугубляющихся с возрастом числе нейродегенеративных заболеваний (таких как болезнь Паркинсона, болезнь Хантингтона, болезнь Альцгеймера) и в тяжелых симптомах диабета /Luft, R., процитированная публикация/.
К некоторым из вышеперечисленных заболеваний (например, миопатии) применимо лечение антиоксидантами (лечение коферментом Q и витамином С) /Shoffher, J. M., Wallace, D.C., Adv. Hum. Genet., 19, 267-330 (1990)/. Это лечение приносит результат только изредка. Были проведены другие лечебные эксперименты, чтобы избежать нарушений последовавшей после ишемии реоксигенации, применяя антиоксидантную и метаболическую терапию с использованием липоамидов. Липоамиды корригируют повреждения сердца, вызванные ишемией, с одной стороны, путем их антиоксидантного эффекта, с другой стороны, путем их положительного влияния на митохондриальный метаболизм /Sumegi, Balazs et al. , Biochem. J., 297, 109-113 (1994)/. Без глубокого знания процесса повреждения до сих пор не было разработано эффективной терапии.
Из вышесказанного следует, что существует потребность в разработке фармацевтического продукта, который может защитить митохондриальный геном от повреждений и, также, предотвратить такие повреждения.
Было обнаружено, что соединения формулы I способны защищать митохондриальный геном от повреждений, таким образом, они полезны для защиты митохондриального генома и/или митохондрий от повреждений или для лечения заболеваний, связанных с такими повреждениями.
Примеры заболеваний митохондриального происхождения:
KSS (синдром Кернса-Сайера),
MERRF (миоклональная эпилепсия и синдром шероховатого красного волокна),
LHON (наследственная оптическая нейропатия Лебера),
MJELAS (митохондриальная миопатия, энцефалопатия, лактозный ацитоз и паралич-подобные эпизоды),
Болезнь Лэя,
СРЕО (хроническая прогрессивная наружная фтальмофлегия),
Синдром Альпера.
Примеры зависимых от возраста дегенеративных заболеваний, при которых поврежден митохондриальный геном.
Нейродегенеративные заболевания:
Болезнь Альцгеймера,
Болезнь Паркинсона,
ALS (амиотрофный латеральный склероз)
HD (Болезнь Хантингтона),
Кардиомиопатии и другие миопатии.
Таким образом, изобретение относится к фармацевтическим композициям, содержащим от 0.1 до 95 мас.% производного гидроксамовой кислоты формулы I или его фармацевтически приемлемой кислотной аддитивной соли в качестве активного ингредиента в смеси с одним или более традиционным(и) носителем (носителями).
В описании и формуле С1-5 алкильной группой является, например, метильная, этильная, н-пропильная, изопропильная, н-бутильная или н-пентильная группа, предпочтительно метильная или этильная группа.
С3-8 циклоалкильной группой является, например, циклопропильная, циклопентильная, циклогексильная, циклогептильная или циклооктильная группа, предпочтительно, циклопентильная или циклогексильная группа.
Пяти - восьмичленным кольцом, содержащим один или более гетероатом(ов), может быть, например, пиррол, пиразол, имидазол, оксазол, тиазол, пиридин, пиридазин, пиримидин, пиперазин, морфолин, индол, хинолин и др. кольцо.
Атомом галогена является, например, атом фтора, хлора, брома или йода, предпочтительно, атом хлора или брома.
Фармацевтически приемлемыми кислотными аддитивными солями соединений формулы I являются кислотные аддитивные соли, образованные с фармацевтически приемлемыми неорганическими кислотами, такими как соляная, серная и другие, или с фармацевтически приемлемыми органическими кислотами, такими как уксусная кислота, фумаровая кислота, молочная кислота и другие.
Предпочтительная подгруппа соединений формулы I состоит из производных гидроксамовой кислоты формулы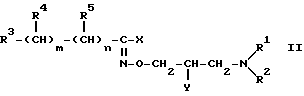
где R1, R2, R3, R4, R5, m и n таковы, как указано в отношении формулы I,
X представляет собой аминогруппу,
Y означает гидроксигруппу.
Особенно предпочтительными соединениями формулы II являются те, в которых R1 и R2, совместно с атомом азота, к которому они присоединены, образуют пиперидиновую группу, R3 означает пиридильную группу, m и n имеют значение О, Х является таким, как указано выше. Из этих соединений предпочтительным является следующее:
О-(3-пиперидино-2-гидрокси-1-пропил)никотинамидоксим (соединение "В")
Соединения формулы I могут быть приготовлены в соответствии со способами, известными из HU-P 177578.
Фармацевтическая композиция изобретения содержит от 0.1 до 95 мас.%, предпочтительней от 1 до 50 мас.%, особо предпочтительно от 5 до 30 мас.% производного гидроксамовой кислоты формулы I или его фармацевтически приемлемой кислотной аддитивной соли в качестве активного ингредиента и один или более традиционный носитель (носители).
Фармацевтические композиции изобретения могут быть полезны для перорального, парентерального или ректального введения или для местного применения и могут быть твердыми или жидкими.
Твердые фармацевтические композиции, подходящие для перорального введения, могут быть порошками, капсулами, таблетками, покрытыми пленкой таблетками, микрокапсулами и т.д. и могут содержать связывающие агенты, такие как желатин, сорбитол, поли(винилпирролидон) и т.д.; наполняющие агенты, такие как лактоза, глюкоза, крахмал, фосфат кальция и т.д.; дополнительные субстанции для таблетирования, такие как стеарат магния, тальк, поли(этиленгликоль), силикат и т. д.; увлажняющие агенты, такие как лаурилсульфат натрия и т.д. в качестве носителя.
Жидкими фармацевтическими композициями, подходящими для перорального введения, могут быть растворы, суспензии или эмульсии и могут содержать, например, суспендирующие агенты, такие как желатин, карбоксиметилцеллюлоза и т.д.; эмульгаторы, такие как моноолеат сорбитана и т.д.; растворители, такие как вода, масла, пропиленгликоль, этанол и т.д.; консерванты, такие как метил-п-гидроксибензоат и т.д. в качестве носителя.
Фармацевтическими композициями, подходящими для парентерального введения, в основном, являются стерильные растворы активного ингредиента.
Лекарственные формы, перечисленные выше, как и другие лекарственные формы, известны, см. , например, Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Co., Easton, USA (1990).
Фармацевтические композиции изобретения содержат, обычно, единичную дозу. Типичная ежедневная доза для взрослых пациентов составляет от 0.1 до 1000 мг соединения формулы I или его фармацевтически приемлемой кислотной аддитивной соли. Вышеупомянутая доза может быть введена в одной порции или в нескольких порциях. Реальная доза зависит от многих факторов и определяется врачом.
Фармацевтические композиции изобретения изготавливают путем смешивания соединения формулы I или его фармацевтически приемлемой кислотной аддитивной соли с одним или более носителем (носителями) и путем превращения полученной смеси в фармацевтическую композицию известным способом. Полезные способы известны из литературы, например, из Remington Pharmaceutical Sciences.
Другое воплощение изобретения заключается в применении соединения формулы I, где R, R1, R2, R3, X, Y, А и В таковы, как указано в отношении формулы I, или его фармацевтически приемлемой кислотной аддитивной соли, возможно, в смеси с одним или более носителем (носителями), часто используемым(ми) в фармацевтических композициях, для приготовления фармацевтической композиции, полезной для защиты митохондриального генома и/или митохондрии от повреждений.
Другое воплощение изобретения заключается в применении соединения формулы I, где R, где R1, R2, R3, X, Y, А и В таковы, как обозначено в отношении формулы I, или его фармацевтически приемлемой кислотной аддитивной соли, возможно, в смеси с одним или более носителем (носителями), часто используемым(ми) в фармацевтических композициях, для приготовления фармацевтической композиции, полезной для лечения заболеваний, связанных с повреждением митохондриального генома и/или митохондрии. Такие заболевания включают, особенно, миопатию, кардиомиопатию и нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Паркинсона или болезнь Хантингтона.
Предпочтительной реализацией изобретения является применение производных гидроксамовой кислоты формулы II, где R1, R2, R3, R4, R5, X, Y, m и n таковы, как указано в отношении формулы II, или их фармацевтически приемлемых кислотных аддитивных солей.
Наиболее предпочтительной реализацией изобретения является применение соединений формулы II, где R1 и R2, совместно с атомом азота, к которому они присоединены, образуют пиперидиновую группу, m и n имеют значение О, Х и Y такие, как указано в отношении формулы II, или их фармацевтически приемлемых кислотных аддитивных солей.
Особо предпочтительной реализацией изобретения является применение O-(3-пиперидино-2-гидрокси-1-пропил)никотинамидоксима или его фармацевтически приемлемой кислотной аддитивной соли.
Тесты in-vitro
Защитный эффект производных гидроксамовой кислоты формулы I на митохондриальный геном тестировали по их способности защищать окислительное фосфорилирование in vitro. Теоретическим основанием тестов является то, что энергия, необходимая для клеток, продуцируется аденозинтрифосфатом (АТФ), который синтезируется в митохондриях. Нарушения транспорта субстрата, цитратного пути, дефект респираторных комплексов и нарушение связи в окислительном фосфорилировании приводит к нарушению снабжения клетки энергией. В тесте окислительное фосфорилирование было повреждено путем обработки клеток дрожжей Saccharomyces cerevisiae и человеческих эритролейкемических клеток К562 тепловым шоком, и определяли защитный эффект соединения "В".
Известно, что один из повреждающих эффектов теплового шока, который развивается немедленно, т.е. в течение нескольких минут, затрагивает митохондрию путем отрыва дыхательной цепи от окислительного фосфорилирования. Тесты с использованием химических разъединителей показали, что протоны, внесенные ферментными комплексами дыхательной цепи во время электронного транспорта в пространство между внутренней и наружной мембранами митохондрий, попадают обратно во внутреннее пространство вследствие эффекта разъединителей, таким образом, АТФ не синтезируется. В результате теплового шока происходит сходный процесс, который приводит к быстрому снижению питания клеток энергией.
Материалы, использованные в тестировании
Культура клеток Saccharomyces cerevisiae. Гаплоидную клеточную линию дикого типа S288C культивировали в среде YPG, содержащей 1% дрожжевого экстракта, 2% пептона и 3% глицерина. Культуру выращивали при встряхивании в жидкой среде в водяной бане при 25oС, при аэробных условиях.
Культура К562.
Клеточную линию К562 эритролейкемического типа происхождения от клеток человеческой хронической миелогенной лейкемии культивировали в жидкой среде RPMI 1640 в присутствии 10% телячьей сыворотки при температуре 37oС, в смеси влажного газа, содержащей 95% воздуха и 5% диоксида углерода.
Олигомицин.
Производитель карбонилцианид-м-хлорофенилгидразона (CI-CCP):
Sigma Chemicals Co., St.Louis, USA).
Потребление кислорода измеряли следующим способом.
Клетки на их логарифмической фазе роста центрифугировали и, в случае Saccharomyces cerevisiae, брали в десятикратном количестве среды YPG, содержащей 1% маннозы вместо 2% глицерина. В случае К562 после разделения клетки брали в концентрации 4•106 клеток/мл в среде RPMI 1640, содержащей 20 мМ HEPES. Потребление кислорода измеряли в термостатированной кювете на 2 мл электродом Клэра. Детали метода описаны в следующей статье: Patriarca, E.J и Maresca, В. Experimental Cell Research, 190, 57-64 (1990). Стимуляция респираторного уровня представлена в % с использованием формулы:
[(VCI-ССР/VOlig)-1]•100
За один час до теплового шока, после сепарации, к среде добавляли, соответственно, 10-5, 2.5•10-5, 5•10-5 М соединения "В" и растворитель (PBS, т. е. физиологический раствор хлорида натрия, содержащий фосфатный буфер). Тепловой шок проводили, выдерживая культуру при 42oС в течение 5 мин вместо обычной температуры 25oС. В случае клеток К562 культуру выдерживали при 48oС в течение 10 мин вместо обычной температуры 37oС.
Во время экспериментов было отмечено, что тепловой шок значительно разъединял электронную транспортную цепь от синтеза АТФ как у клеток Saccharomyces cerevisiae, так и у клеток К562.
Полученные результаты показаны в табл. 1 и 2, где способ лечения показан вместе со стимуляцией в % и полученной защитой в %.
Данные табл. 1 и 2 демонстрируют, что использование соединения "В" неоспоримо обеспечивало повышенную защиту клеток путем предотвращения разъединения митохондриальных дыхательных комплексов.
В исследованном промежутке оптимальной концентрацией соединения "В" являлось 25 мкмоль. В дополнение к сохранению определенной клеточной функции, наиболее возможно непрямое предотвращение формирования свободных радикалов кислорода. Из этого мы можем заключить, что соединение "В" обеспечивает защиту против повреждений митохондриального генома.
Защита митохондрий от индуцированного тепловым шоком разъединения
При нормальных условиях дыхательные комплексы выталкивают протоны во время окисления NADH, создавая протонный градиент с двух сторон внутренней митохондриальной мембраны. Этот протонный градиент обеспечивает энергию для синтеза АТФ из АДФ и неорганического фосфата. Протоны способны вновь войти в пространство внутренней мембраны только через F1F0AТФазу, утилизируя энергию протонного градиента для синтеза АТФ из АДФ и неорганического фосфата (Pi). В отсутствие АДТ или Pi повышается протонный градиент, и дыхательные комплексы и митохондриальное потребление кислорода ингибируются. Однако, если существует какое-либо нарушение во внутренней мембране, протоны способны вновь войти в пространство внутренней мембраны, и энергия протонного градиента не утилизируется F1F0АТФазой, и, таким образом, митохондриальное окисление становится независимым от АДФ (митохондрии становятся разъединенными).
Хорошо известно, что тепловой стресс может индуцировать разъединение митохондриального окисления от продукции митохондриальной энергии (АТФ), что является последствием теплового стресса, индуцированного повреждением внутренней мембраны митохондрий. В поврежденных областях мембран протоны протекают обратно из межмембранного пространства к компартменту внутренней мембраны, таким образом, митохондриальное окисление становится независимым от АТФ.
Для теста митохондрии изолировали из контрольных крыс или из крыс, обработанных 40 мг/кг соединения "В" за 6 ч до получения препарата, которое осуществляли, как описано в Sumegi et al., J. Biol. Chem., 259, 8748 (1984). Потребление кислорода определяли электродом Кларка в камере при 37oС. Определяли уровень потребления кислорода в присутствии 5 мМ АДФ и в отсутствии АДФ, что показано в табл. 3 для необработанных митохондрий и для митохондрий, переинкубированных в течение 8 мин при 42oС.
Данные, указанные в табл. 3, являются средним значением ± стандартная ошибка по трем экспериментам.
Из табл. 3 видно, что при нормальных условиях митохондриальное окисление в присутствии АДФ происходит, примерно, в 6 раз быстрее, чем в среде, свободной от АДФ, демонстрируя хорошее объединение между митохондриальным окислением и синтезом АТФ. Однако тепловой стресс значительно понижает объединение митохондрий, и в контрольных случаях это значение понижалось (2.7), но в митохондриях из животных, предварительно обработанных соединением "В", все же сохранялся относительно высокий уровень объединения (5.1). Эти данные демонстрируют, что соединения формулы I и, особенно, соединение "В" защищали продукцию митохондриальной энергии (синтез АТФ) от повреждения, вызванного тепловым стрессом.
Защита холинэргических нейронов от клеточной дегенерации, индуцированной перекисью водорода
Хорошо известно, что перекись водорода наносит окислительное повреждение клеткам из-за образования в клетках свободных радикалов кислорода. Поэтому индуцированное перекисью водорода клеточное повреждение может быть использовано в качестве общей модели дегенерации нейронов. Были использованы гибрид SN6.10.2.2, клеточная линия септальных нейронов N18TG2 + ED15 /Hammond et al. , Science, 234, 1237 (1986)/ для изучения защитного эффекта соединений формулы I против свободных радикалов кислорода, вызывающих клеточное повреждение, что является главным механизмом большинства нейродегенеративных заболеваний.
Для теста клетки разделили на две группы на плате из 96 лунок. Одну из групп поддерживали в среде, содержащей соединение "В" (40 мг/л), другую поддерживали в основной среде. Обработку начинали через 24 ч после разделения. Обе группы обрабатывали средой, содержащей различные концентрации перекиси водорода. Тест на выживание проводили через 48 ч после периодов обработки.
Тест на выживание.
Удаляли среду из лунок, клетки промывали стерильным PBS и затем к каждой лунке добавляли 150 мкг субстрата щелочной фосфатазы, растворенного в 150 мкг свежего диэтаноламинного буфера (рН 9.8). Плашки инкубировали при 30oС и останавливали реакцию добавлением к каждой лунке 50 мкл гидрохлорида натрия. Поглощение измеряли при 405 нм ридером плат Dynatech ELISA, для определения фона использовали периферические лунки каждой платы, содержащие только среду. Полученные результаты показаны в табл. 4.
Табл. 4 показывает, что использование соединения формулы I (т.е. соединения "В") эффективно защищает холинэргические нейроны от индуцированного перекисью водорода лизиса клеток. Поскольку перекись водорода убивает клетки благодаря образованию большого количества свободных радикалов кислорода, соединение "В" способно защищать нейроны при любых заболеваниях, когда повреждение нейронов связано со свободными радикалами кислорода. Поэтому соединения формулы I могут успешно использоваться при болезни Паркинсона, амиотрофическом латеральном склерозе (ALS), болезни Хантингтона и при различном слабоумии смешанного происхождения /Life Sciences, 56, 1151-1171 (1995)/.
Тесты in vivo
Защитный эффект на митохондриальный геном производных гидроксамовой кислоты формулы I тестировали in vivo на крысах. Вистаровских крыс обрабатывали ежедневно AZT (3'-азидотимидином, производитель: Sigma Chemicals Inc.) в дозе 50 мг/кг в течение 14 дней. Определенные тестовые группы обрабатывали AZT в комбинации с соединением "В" (ежедневная доза 40 мг/кг). Проводили различные измерения во время и после обработки.
1) ЭКГ Schiller AT-6 использовали для мониторинга кардиологической функции животных, на всех четырех конечностях. Параметры ЭКГ оценивали, используя стандартный метод, описанный в технической литературе /Kawai, С., Takatsu, Т., New Engl. J. Med, 293, 592 (1975); Angelakos, E.T, Bernardini, P. J. Appl. Physiol., 18, 261-263 (1963)/. Мы определили интервалы RR, PR и TQ и точки депрессий J. Полученные результаты показаны в табл. 5, где значения представлены как средние 5 измерений ± стандартное отклонение.
Данные табл. 5 показывают, что в результате обработки AZT в сравнении с контрольной группой частота сердечных сокращений у животных была значительно увеличена (RR), и также были увеличены интервалы PQ. Далее, значение QT значительно увеличивалось и на пиках I и VL, которые представляют основную мускульную массу левого желудочка, были обнаружены значительные точки депрессии J (более 0.1 mV). Эти параметры характеризуют развивающуюся миокардиальную ишемию или нарушение потребления кислорода. Однако в случаях, когда в дополнение к AZT крысам вводили также соединение "В" в ежедневной дозе 40 мг/кг, параметры сердца возвращались к нормальному уровню, что свидетельствует о том, что соединение "В" защищает сердце от отклонений, индуцированных AZT.
2) Определяли дыхательную активность животных. Для этого определяли активности NADH: цитохром С оксидоредуктазы, цитохром оксидазы и цитрат синтазы методами, описанными в технической литературе /Sumegi, Balazs et al.; Clin. Chim. Acta. , 192, 9-18, (1990)/. (NADH: никотиновой кислоты аденин динуклеотид, восстановленная форма). Полученные результаты показаны в табл. 6,
В табл. 6 хорошо продемонстрировано, что обработка AZT значительно понижает активность дыхательных комплексов в митохондриях сердца. В этом случае AZT существенно понижает продукцию окислительной энергии в сердце, что может привести к состоянию, когда сердце неспособно должным образом осуществлять его основную функцию (см. табл. 5, данные ЭКГ). Кроме этого, пониженная емкость митохондриального дыхания может привести к нарушению митохондриального метаболизма, что может послужить причиной последующих повреждений сердца.
Когда AZT вводили животным в комбинации с соединением "В", эффект AZT, снижающий дыхательную активность, практически исчезал и значения дыхательной активности были близки к норме. Именно протестированные соединения формулы I значительно понижали индуцированные AZT повреждения митохондриальной мембраны путем защиты дыхательных комплексов.
3) Исследовали повреждения митохондриального генома. Повреждения митохондриального генома определяли при помощи метода ПЦР (ПЦР: полимеразная цепная реакция). Были отобраны праймеры путем амплифицирования набора от компонента I цитохром оксидазы до цитохрома В, чтобы определить делеции. (Праймеры были приобретены у Ransonhill BioScience Co.). Использованный метод описан в публикации Sumegi, Balazs et al./B.B.A. (1996)/, публикация находилась в стадии издания. Используя ПЦР праймеры в амплификации района с 4929 до 16298 митохондриального генома, было показано, что районы 0.5 и 1.5 тысяч пар оснований (т.п.о) значительно амплифицированы у крыс, обработанных AZT. В то же время амплификации таких коротких участков у животных контрольной группы не наблюдалось. Очевидно, что неповрежденный геном не амплифицирует короткие участки ДНК, как в этих тестах, когда праймеры расположены на более чем 11.3 т.п.о. друг от друга. Факт, что такие короткие участки ДНК амплифицируются у обработанных AZT крыс, показывает, что вследствие обработки AZT участки размером 10 т.п.о. делетированы из митохондриального генома, и именно в таких поврежденных геномах праймеры становятся ближе друг к другу на 0.5-1.5 т.п.о. Как следствие, такой участок ДНК может быть амплифицирован. Амплификация таких участков ДНК показывает повреждение митохондриального генома, которое является частичной или полной делецией генов, кодирующих подгруппы I, II и III цитохром оксидазы, генов, кодирующих АТФ 6 и 8, генов, кодирующих Комплекс I или NADH: убихинон оксидоредуктазу 2, 4, 4L, 5 и 6, и цитохром В.
Когда AZT вводили животным в комбинации с соединением "В", амплификация вышеупомянутых коротких участков ДНК значительно понизилась, и определенные фрагменты ДНК не могли быть определены.
Это означает, что соединение "В" защищало вышеупомянутые гены от индуцированных AZT повреждений или, по меньшей мере, значительно снижало эти повреждения. Необходимо отметить, что искусственные повреждения, индуцированные AZT, вышеупомянутым генам также могут появляться в результате ишемической кардиомиопатии или кардиомиопатии престарелых людей.
Влияние соединений формулы I на наследственные митохондриальные кардиомиопатии
Были проведены тесты с использованием крыс с наследственной митохондриальной кардиомиопатией, обработанных ежедневной дозой 40 мг/кг соединения "В" в течение 14 дней. Функцию сердца крыс оценивали по ЭКГ. Полученные данные ЭКГ контрольной группы и группы, обработанной соединением "В", показаны в табл. 7. Значения представлены как среднее 3 измерений ± стандартное отклонение.
Были проведены тесты на крысах с наследственной кардиомиопатией, которые имели нарушенные функции сердца. Этот факт хорошо виден из табл. 7. Эти кардиомиопатические крысы являются отличной моделью ишемической кардиомиопатии и кардиомиопатии престарелых людей. Как следствие влияния 14-дневной обработки соединением "В", функции сердца животных значительно улучшились и параметры ЭКГ вернулись к нормальному уровню.
Эти тесты показывают, что производные гидроксамовой кислоты формулы I способны защищать митохондриальный геном против различных повреждений. В случае использованных животных моделей, они, фактически, устранили индуцированные AZT повреждения сердца, и это может иметь большое значение в медицинской науке, принимая во внимание то, что в настоящее время более ста тысяч людей в мире получают лечение AZT.
Другим важным качеством этих соединений является то, что, в случае развивающейся кардиомиопатии (когда митохондриальные повреждения сходны с таковыми ишемической кардиомиопатии и кардиомиопатии престарелых людей), они устраняют отклонения функции сердца и восстанавливают нормальные параметры ЭКГ.
Основываясь на вышеприведенных тестах, можно сказать, что фармацевтические композиции изобретения, содержащие в качестве активного ингредиента соединение формулы I, способны защитить митохондриальный геном или митохондрии от повреждений, более того, с их помощью можно лечить заболевания с уже развившимися повреждениями такого типа.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОСМЕТИЧЕСКИЙ СОСТАВ И СПОСОБ ДЛЯ ЗАМЕДЛЕНИЯ ПРОЦЕССОВ СТАРЕНИЯ КОЖИ | 1996 |
|
RU2197954C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ СО СНИЖЕННЫМИ ПОБОЧНЫМИ ЭФФЕКТАМИ, СОДЕРЖАЩАЯ ПРОТИВООПУХОЛЕВЫЙ АГЕНТ И ПРОИЗВОДНОЕ ГИДРОКСАМОВОЙ КИСЛОТЫ | 1998 |
|
RU2214238C2 |
| СИНЕРГИЧНЫЙ ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ДИАБЕТА | 2002 |
|
RU2311907C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ УЛУЧШЕННЫМ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ И/ИЛИ СНИЖЕННЫМИ ПОБОЧНЫМИ ЭФФЕКТАМИ, СОДЕРЖАЩАЯ ПРОТИВООПУХОЛЕВЫЙ АГЕНТ И ПРОИЗВОДНОЕ ГИДРОКСАМОВОЙ КИСЛОТЫ | 1998 |
|
RU2254129C2 |
| УМЕНЬШЕНИЕ ИЗБЫТОЧНОЙ МАССЫ ТЕЛА ИЛИ ОЖИРЕНИЯ | 2007 |
|
RU2443417C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИПСИХОТИЧЕСКОЙ, АНТИДЕПРЕССАНТНОЙ ИЛИ ПРОТИВОЭПИЛЕПТИЧЕСКОЙ АКТИВНОСТЬЮ, СО СНИЖЕННЫМ ПОБОЧНЫМ ЭФФЕКТОМ | 2007 |
|
RU2440116C2 |
| ПРОИЗВОДНЫЕ АМИДОКСИМОВ ПРОПЕНКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2001 |
|
RU2264387C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ МИТОХОНДРИАЛЬНЫХ ЗАБОЛЕВАНИЙ | 1999 |
|
RU2279880C2 |
| КОМПОЗИЦИИ СЕЛЕНООРГАНИЧЕСКИХ СОЕДИНЕНИЙ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2665135C2 |
| МЯГКИЕ КАТИОННЫЕ МИТОХОНДРИАЛЬНЫЕ РАЗОБЩИТЕЛИ | 2010 |
|
RU2527519C2 |





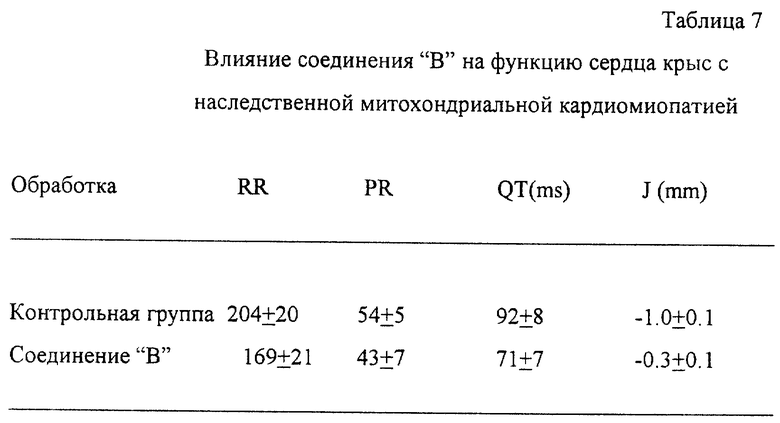
Изобретение относится к новому средству и к фармацевтическим композициям на его основе для защиты митохондриального генома и/или митохондрий от повреждений или для лечения заболеваний, связанных с этими повреждениями. Активным ингредиентом вышеупомянутых композиций предложено производное гидроксамовой кислоты формулы (I) или его фармацевтически приемлемая кислотная аддитивная соль. Вещество использовалось ранее для лечения диабета. Изобретение предлагает средство для лечения миопатии и/или кардиомиопатии или нейродегенеративных заболеваний с новым механизмом действия. 3 с. и 11 з.п.ф-лы, 7 табл. 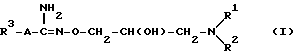
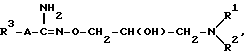
где R1 является атомом водорода или С1-5 алкильной группой;
R2 является атомом водорода, С1-5 алкильной группой, С3-8 циклоалкильной группой или фенильной группой, которая может быть замещена гидроксильной или фенильной группой, или R1и R2 совместно с атомом азота, к которому они присоединены, образуют пяти - восьмичленное кольцо, которое может содержать еще один или более атом(ов) азота, кислорода или серы, и указанное кольцо может быть соединено с бензольным кольцом;
R3 является атомом водорода, фенильной группой, нафтильной группой или пиридильной группой, причем указанные группы могут быть замещены одним или более атомом(ами) галогена или С1-4 алкоксильной(ыми) группой(ами),
А является С1-4 алкиленовой группой или химической связью или группой формулы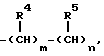
где R4 является атомом водорода или фенильной группой;
R5 является атомом водорода или фенильной группой;
m имеет значение 0, 1 или 2;
n имеет значение 0, 1 или 2,
или его фармацевтически приемлемую кислотную аддитивную соль в качестве активного ингредиента в смеси с одним или более традиционным(и) носителем(ями).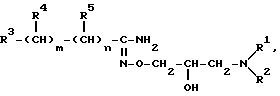
где R1, R2, R3, R4, R5 m и n такие, как указано в п.1,
или его фармацевтически приемлемая кислотная аддитивная соль.
| МЫШКИН В.А | |||
| и др | |||
| Исследования антиоксидантных свойств и ноотропного действия оксиметацина | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Биоантиоксидант | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Счетный сектор | 1919 |
|
SU107A1 |
| Жданюк Ю.И | |||
| Состояние перекисного окисления липидов у больных кардиомиопатиями и пути его коррекции биоантиоксидантами | |||
| Автореф | |||
| диссертации на соискание ученой степени кандидата медицинских наук | |||
| - Харьков, 1992, с.1-19 | |||
| US 4187220, 05.02.1980 | |||
| US 4308399, 29.12.1981. | |||
Авторы
Даты
2002-10-20—Публикация
1996-09-26—Подача