Изобретение относится к синергичному фармацевтическому составу, подходящему для профилактики или лечения преддиабетического состояния, метаболического Х-синдрома или сахарного диабета, а также нарушений, которые связаны с перечисленными выше состояниями, а именно эндогенных нарушений обмена веществ, инсулинорезистентности, дислипидемии, алопеции, распространенного выпадения волос (diffuse effluvium) и/или эндокринных нарушений у женщин, обусловленных преобладанием андрогенов.
В промышленно развитых странах все большее количество людей страдает от диабета. Например, развитие диабета 2 типа (т.е. инсулиннезависимого сахарного диабета, NIDDM - non-insulin-dependent diabetes mellitus) провоцируется дефектами как в продукции, так и в использовании инсулина. Генетические факторы и факторы окружающей среды в равной степени вносят вклад в развитие этого широко распространенного серьезного заболевания, сопровождающегося значительной смертностью. Пациент, которого лечат инсулином или другим противодиабетическим или антигиперлипидемическим агентом, фактически получает только паллиативное лечение, которое улучшает качество жизни, однако неизбежно появляются осложнения, сопровождающие диабет.
Цель настоящего изобретения состоит в том, чтобы предложить фармацевтический состав, пригодный для профилактики развития диабета или, по меньшей мере, осложнений, сопровождающих диабет, или, если такая профилактика более невозможна, для эффективного лечения указанных осложнений.
Обнаружили, что указанная выше цель достигается с помощью синергичного фармацевтического состава, включающего:
(a) первую фармацевтическую композицию, содержащую противодиабетический или антигиперлипидемический активный агент и один или более стандартных носителей, и
(b) вторую фармацевтическую композицию, содержащую производное гидроксамовой кислоты формулы
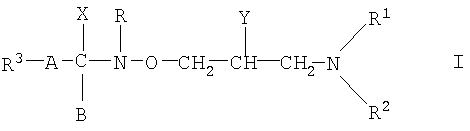
где R1 представляет собой атом водорода или C1-5-алкильную группу,
R2 обозначает атом водорода, C1-5-алкильную группу, С3-8-
циклоалкильную группу или фенильную группу, которые могут
быть замещены гидроксигруппой или фенильной группой, или
R1 и R2 вместе с атомом азота, к которому они присоединены,
образуют 5-8-членное кольцо, которое может содержать один
или более дополнительных атомов азота, кислорода или серы и
которое может быть сконденсировано с другим алициклическим
или гетероциклическим кольцом, предпочтительно бензольным,
нафталиновым, хинолиновым, изохинолиновым, пиридиновым или
пиразолиновым кольцом, причем гетероатом(ы) азота и/или серы
могут быть представлены в форме оксида или диоксида,
R3 обозначает атом водорода, фенильную группу, нафтильную группу
или пиридильную группу, где указанные группы могут быть
замещены одним или более атомами галогена или C1-4-
алкоксигруппами,
Y представляет собой атом водорода, гидроксигруппу, C1-24-
алкоксигруппу, которая может быть замещена аминогруппой, C2-24-
полиалкенилоксигруппу, содержащую от 1 до 6 двойных связей,
С1-25-алканоильную группу, С3-9-алкеноильную группу или группу
формулы R7-COO-, где R7 представляет собой С2-30-
полиалкенильную группу, содержащую от 1 до 6 двойных связей,
Х обозначает атом галогена, аминогруппу, С1-4-алкоксигруппу
или
Х образует с В атом кислорода, или
Х и Y вместе с атомом углерода, к которому они присоединены, и-
NR-О-СН2-группой, находящейся между указанными атомами
углерода, образуют кольцо формулы
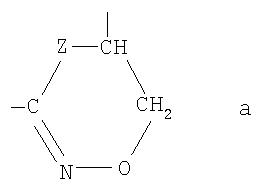
где
Z представляет собой атом кислорода или группу формулы -N= или -NH-,
R обозначает атом водорода или
R образует с В химическую связь,
А представляет собой C1-4-алкиленовую группу или химическую связь или группу формулы
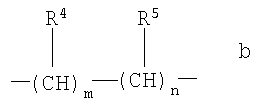
где
R4 представляет собой атом водорода, C1-5-алкильную группу, С3-8-
циклоалкильную группу или фенильную группу, которая может
быть замещена атомом галогена, C1-4-алкоксигруппой или C1-5-
алкильной группой,
R5 обозначает атом водорода, С1-4-алкильную группу или
фенильную группу,
m имеет значение 0, 1 или 2,
n имеет значение 0,1 или 2,
или его фармацевтически приемлемую соль присоединения кислоты и один или более стандартных носителей.
Изобретение основано на том, что производные гидроксамовой кислоты формулы I увеличивают чувствительность к инсулину. Поэтому в присутствии производного гидроксамовой кислоты формулы I или его фармацевтически приемлемой соли присоединения кислоты, противодиабетический или антигиперлипидемический активный агент, применяющийся для лечения патологического состояния, может вводиться в значительно меньшей дозе для достижения желаемого эффекта, при этом уменьшая или устраняя побочные эффекты, которые сопровождают традиционное лечение.
Производные гидроксамовой кислоты формулы I известны из Патента US 4308399 и ЕР 417210. Согласно этим документам эти соединения могут применяться для лечения диабетической ангиопатии, и часть из них оказывает избирательный бета-блокирующий эффект.
Согласно Венгерской патентной заявке №2385/92, опубликованной под № Т/66350, определенные производные гидроксамовой кислоты в пределах формулы I могут применяться для лечения сосудистых осложнений, обусловленных диабетом.
Известны также различные дополнительные биологические эффекты производных гидроксамовой кислоты формулы I, их применение для профилактики и лечения болезней митохондриального происхождения (WO 97/13504), для увеличения уровня стресс-белков в клетках (WO 97/16439), для замедления процессов старения кожи (WO 97/23198), против аутоиммунных болезней (WO 00/07580) и т.д.
Определение выражений, применяющихся в описании и формуле изобретения:
Фармацевтический состав представляет собой сочетание двух фармацевтически активных агентов, в котором:
1) либо каждый из активных агентов по отдельности был внесен в состав отдельной фармацевтической композиции с использованием одного или более стандартных носителей и любого из обычных способов производства лекарств, и в этом случае пациенту вводят две полученных фармацевтических композиции одновременно или одну после другой через промежуток времени;
2) либо два активных агента были внесены в состав одной фармацевтической композиции, которая может быть введена пациенту, нуждающемуся в ней. В последнем случае фармацевтическая композиция может содержать смесь двух активных агентов, или каждый активный агент может быть представлен в разных элементах фармацевтической композиции, например один из них находится в сердцевине таблетки, а другой в покрытии сердцевины таблетки. Конечно, для приготовления этой единой фармацевтической композиции применяют один или более стандартных носителей и любой из обычных способов производства лекарств.
Под противодиабетическим активным агентом подразумевают любые фармакологически активные агенты, обычно применяющиеся для лечения диабета. В основном эти агенты представляют собой следующие агенты:
- инсулин,
- инсулинсенсибилизирующие активные агенты,
- активные агенты, которые увеличивают продукцию инсулина,
- сульфамиды,
- производные бигуанидина и
- ингибиторы α-глюкозидазы.
Поскольку инсулин стоит на первом месте, то применяют человеческий инсулин, полученный рекомбинантными методами, который вводят, как правило, парентерально.
Инсулинсенсибилизирующие активные агенты усиливают эффект инсулина. Наиболее важные разновидности этих агентов представляют собой γ-агонисты PPAR (от англ. peroxisome proliferator-activated receptor, рецептор, активируемый пероксисомальным пролифератором), например производные тиазолидиндиона, такие как пиоглитазон [(±)-5-[[4-[2-(5-этил-2-пиридинил)этокси]фенил]метил]-2,4-тиазолидиндион], троглитазон [(±)-5-[[4-[(3,4-дигидро-6-гидрокси-2,5,7,8-тетраметил-2Н-1-бензопиран-2-ил)метокси]фенил]метил]-2,4-тиазолидиндион], циглитазон [5-[[4-[(1-метилциклогексил)-метокси]фенил]метил]-2,4-тиазолидиндион], росиглитазон [(±)-5-[4-[2-[N-метил-N-(2-пиридил)амино]этокси]бензил]-2,4-тиазолидиндион] и другие производные 2,4-тиазолидиндиона, а также их фармацевтически приемлемые соли присоединения кислот.
Активные агенты, которые увеличивает продукцию инсулина, представляют собой, например, следующие агенты: митиглинид [(αS,3аR,7аS)-октагидро-γ-оксо-α-(фенилметил)-2Н-изоиндол-2-масляную кислоту], репаглинид [(S)-2-этокси-4-[2-[[3-метил-1-[2-(1-пиперидинил)фенил]бутил]амино]-2-оксоэтил]бензойную кислоту], сенаглинид (т.е. натеглинид) [N-[[(транс-4-(1-метилэтил)циклогексил]карбонил]-D-фенилаланин] или их фармацевтически приемлемые соли присоединения кислот или фармацевтически приемлемые соли.
Из сульфамидов наиболее важными являются производные сульфонилмочевины, например толбутамид [N-[(бутиламино)карбонил]-4-метилбензолсульфамид], хлорпропамид [4-хлор-N-[(пропиламино)карбонил]бензолсульфамид], толазамид [N-[[(гексагидро-1Н-азепин-1-ил)амино]карбонил]-4-метилбензолсульфамид], ацетогексамид [4-ацетил-N-[(циклогексиламино)карбонил]бензолсульфамид] и т.д. в качестве сульфонилмочевин первого поколения, или, например, глибурид [5-хлор-N-[2-[4-[[[(циклогексиламино)карбонил]амино]сульфонил]-фенил]этил]-2-метоксибензамид], глипизид [N-[2-[4-[[[(циклогексиламино)карбонил]амино]сульфонил]фенил]этил]-5-метилпиразинкарбоксамид], гликлазид [N-[[(гексагидроциклопента[с]пиррол-2(1Н)-ил)амино]карбонил]-4-метилбензолсульфамид], глимепирид [транс-3-этил-2,5-дигидро-4-метил-N-[2-[4-[[[[(4-метилциклогексил)амино]карбонил]амино]сульфонил]фенил]этил]-2-оксо-1Н-пиррол-1-карбоксамид], гликвидон [N-[(циклогексиламино)карбонил]-4-[2-(3,4-дигидро-7-метокси-4,4-диметил-1,3-диоксо-2(1Н)-изохинолинил)этил]-бензолсульфамид], глиборнурид [N-[[(3-гидрокси-4,7,7-триметилбицикло[2.2.1]гепт-2-ил)амино]карбонил]-4-метилбензолсульфамид], глизоксепид [N-[2-[4-[[[[(гексагидро-1Н-азепин-1-ил)амино]-карбонил]амино]сульфонил]фенил]этил]-5-метил-3-изоксазолкарбоксамид], глибурид [5-хлор-N-[2-[4-[[[(циклогексиламино)карбонил]амино]сульфонил]фенил]этил]-2-метоксибензамид], глизентид [N-[2-[4-[[[(циклопентиламино)карбонил]амино]сульфонил]-фенил]этил]-2-метоксибензамид], глизоламид N-[2-[4[[[(циклогексиламино)карбонил]амино]-сульфонил]фенил]этил]-5-метил-3-изоксазолкарбоксамид], глибузол [N-[5-(1,1-диметилэтил)-1,3,4-тиадиазол-2-ил]бензолсульфамид], гликлопирамид [4-хлор-N-[(1-пирролидиниламино)-карбонил]бензолсульфамид] и т.д. в качестве сульфонилмочевин второго поколения и их фармацевтически приемлемые соли присоединения кислот.
Наиболее важные производные бигуанидина могут быть охарактеризованы формулой
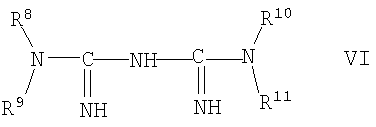
где
R8, R9, R10 и R11 независимо представляют собой атом водорода, C1-10-алкильную
группу, нафтильную группу, фенильную группу или фенил(С1-4-
алкильную) группу, где в обоих предыдущих случаях фенильная
группа может быть замещена 1-3 заместителями, которые
независимо могут представлять собой атом галогена, С1-4-
алкильную группу или С1-4-алкоксигруппу,
при условии, что один из R8, R9, R10 и R11 иной, чем атом водорода, или R8 и R9 вместе с соседним атомом азота, и/или R10 и R11 вместе с соседним
атомом азота образуют 5- или 6-членное, насыщенное,
ненасыщенное или ароматическое кольцо, которое может быть
сконденсировано с другим 5- или 6-членным насыщенным,
ненасыщенным или ароматическим кольцом, которое также может
содержать атом азота.
Особенно предпочтительными производными бигуанидина являются метформин [N,N-диметилимидкарбоимиддиамид], буформин [N-бутилимидкарбоимиддиамид] и фенформин [N-(2-фенилэтил)имиддикарбоимиддиамид].
Ингибиторы α-глюкозидазы ингибируют фермент α-глюкозидазу. Важными представителями их являются, например, миглитол [1,5-дидезокси-1,5-[(2-гидроксиэтил)имино]-D-глюцитол], акарбоза [O-4,6-дидезокси-4-[[[1S-(1α,4α,5β,6α)]-4,5,6-тригидрокси-(3-гидроксиметил)-2-циклогексен-1-ил]амино]-α-D-глюкопиранозил-(1→4)-O-α-D-глюкопиранозил-(1→4)-D-глюкоза], воглибоза [3,4-дидезокси-4-[[2-гидрокси-1-(гидроксиметил)этил]амино]-2-С-(гидроксиметил)-D-эпиинозитол] и т.д.
Под антигиперлипидемическим активным агентом подразумевают любой из фармакологически активных агентов, обычно применяющихся в терапии для снижения высокого уровня липидов в крови. Эти агенты представляют собой соединения, которые в основном могут быть классифицированы следующим образом:
производные арилоксиалкановой кислоты,
ингибиторы (ГМГ-КоА)-редуктазы (3-гидрокси-3-метилглутарил-коэнзим А-редуктазы),
производные никотиновой кислоты,
антациды желчных кислот.
Из производных арилоксиалкановой кислоты предпочтительными активными агентами являются, например, клофибрат [2-(4-хлорфенокси)-2-метилпропановой кислоты этиловый эфир], гемфиброзил [5-(2,5-диметилфенокси)-2,2-диметилпентановая кислота], симфибрат [2-(4-хлорфенокси)-2-метилпропановой кислоты 1,3-пропандииловый эфир], этофибрат [3-пиридинкарбоновой кислоты 2-[2-(4-хлорфенокси)-2-метил-1-оксопропокси]этиловый эфир], ципрофибрат [2-[4-(2,2-дихлорциклопропил)фенокси]-2-метилпропановая кислота], ронифибрат [3-пиридин-карбоновой кислоты 3-[2-(4-хлорфенокси)-2-метил-1-оксопропокси]пропиловый эфир] и т.д.
Из ингибиторов (ГМГ-КоА)-редуктазы наиболее важными активными агентами являются следующие: ловастатин [[1S-[1α(R*),3α,7β,8β(2S*,4S*),8αβ]]-2-метилмасляной кислоты 1,2,3,7,8,8α-гексагидро-3,7-диметил-8-[2-(тетрагидро-4-гидрокси-6-оксо-2Н-пиран-2-ил)этил]-1-нафталениловый эфир], флувастатин [[R*,S*-(E)]-(±)-7-[3-(4-фторфенил)-1-(1-метилэтил)-1Н-индол-2-ил]-3,5-дигидрокси-6-гептеновая кислота], правастатин[[1S-[1α(βS*,δS*),2α,6α,8β(R*),8аα]]-1,2,6,7,8,8а-гексагидро-β,δ,6-тригидрокси-2-метил-8-(2-метил-1-оксобутокси)-1-нафталингептановой кислоты мононатриевая соль], симвастатин [[1S-[1α,3α,7β,8β(2S*,4S*),8αβ]]-2,2-диметилмасляной кислоты 1,2,3,7,8,8а-гексагидро-3,7-диметил-8-[2-(тетрагидро-4-гидрокси-6-оксо-2Н-пиран-2-ил)этил]-1-нафталениловый эфир], аторвастатин [[R-(R*,R*)]-2-(4-фторфенил)-B,δ-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановая кислота] и т.д.
Из производных никотиновой кислоты применяют, например, следующие производные: аципимокс [5-метилпиразинкарбоновой кислоты 4-оксид], ницеритрол [3-пиридинкарбоновой кислоты 2,2-бис[[(3-пиридинилкарбонил)окси]метил]-1,3-пропандииловый эфир], никомол [сложный эфир 3-пиридинкарбоновой кислоты и (2-гидрокси-1,3-циклогександиилиден)-тетракис(метилена)], никоклонат [3-пиридинкарбоновой кислоты 1-(4-хлорфенил)-2-метилпропиловый эфир] и т.д.
Из антацидов, которые связывают желчные кислоты, важными являются следующие антациды: колестипол [основная анионообменная смола: N-(2-аминоэтил)-N′-[2-[(2-аминоэтил)амино]этил]-1,2-этандиаминовый полимер с (хлорметил)оксираном], холестирамин [синтетическая, сильно оснувная анионообменная смола, содержащая четвертичные аммониевые функциональные группы, которые присоединены к сополимеру стирен-дивинилбензол], полидексид [анионообменная смола, содержащая четвертичные аммониевые группы, которые связывают желчные кислоты в кишечнике] и т.д.
Противодиабетический и антигиперлипидемический активные агенты известны из литературы. Если необходимо и химически возможно, эти активные агенты могут применяться в форме их фармацевтически приемлемых солей присоединения кислот или в форме солей, образованных с фармацевтически приемлемыми основаниями.
В описании и формуле изобретения С1-4-алкильная группа представляет собой метальную, этильную, н-пропильную, изопропильную, н-бутильную, втор-бутильную, трет-бутильную или изобутильную группу.
C1-5-алкильная группа, кроме перечисленных выше групп, может также представлять собой, например, н-пентильную группу.
C1-4-алкоксигруппа может быть, например, метокси-, этокси-, н-пропокси- или н-бутоксигруппой.
Атом галогена представляет собой, например, атом фтора, хлора, брома или йода.
С3-8-циклоалкильная группа обозначает, например, циклопропильную, циклопентильную, циклогексильную, циклогептильную или циклооктильную группу.
5-8-членное кольцо, содержащее атом азота, и которое может содержать другой гетероатом, представляет собой, например, пиррольное, пиразольное, имидазольное, оксазольное, тиазольное, пиридиновое, пиридазиновое, пиримидиновое, пиперазиновое, морфолиновое, индольное, хинолиновое кольцо или тому подобное.
C1-24-алкоксигруппа может также представлять собой, кроме алкоксигрупп, перечисленных выше, например, н-пентокси-, децилокси-, додецилокси-, октадецилоксигруппу и т.д.
C1-25-алканоильная группа представляет собой, например, формильную, ацетильную, пропионильную, бутирильную, капроильную, пальмитоильную, стеароильную группу и т.д.
С3-9-алкеноильная группа представляет собой, например, акрилоильную, пентеноильную, гексеноильную, гептеноильную, октаноильную группу и т.д.
Когда Y представляет собой группу формулы R7-COO-, она может представлять собой, например, линоленоильную, линолоильную, докозагексаеноильную, эйкозапентаеноильную, арахидоноильную группу и т.д.
Когда R3 обозначает пиридильную группу, если необходимо, ее атом азота может быть представлен в форме N-оксида. Аналогично, когда R1 и R2 образуют с соседним атомом азота 5-8-членное кольцо, например пиперидильное кольцо, если необходимо, его атом азота может быть также представлен в форме N-оксида.
Под фармацевтически приемлемой солью присоединения кислоты подразумевают соль присоединения кислоты, образованную с фармацевтически приемлемой неорганической кислотой, такой как соляная кислота или серная кислота и тому подобное, или с фармацевтически приемлемой органической кислотой, такой как уксусная кислота, фумаровая кислота, молочная кислота и тому подобное.
Когда противодиабетический или антигиперлипидемический активный агент имеет химическую структуру, которая может образовывать соль с основанием, можно использовать также соль активного агента, образованную с фармацевтически приемлемым неорганическим или органическим основанием. Когда указанный выше активный агент может образовывать соль присоединения кислоты с кислотой, этот активный агент можно использовать также в форме его фармацевтически приемлемой соли присоединения кислоты.
В пределах производных гидроксамовой кислоты формулы I предпочтительный подкласс состоит из производных гидроксамовой кислоты формулы
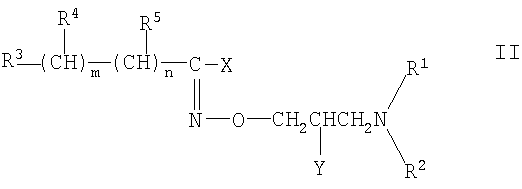
где
R1, R2, R3, R4, R5, m и n такие, как определены для формулы I, X обозначает атом галогена или аминогруппу, Y представляет собой гидроксигруппу, и их фармацевтически приемлемых солей присоединения кислот.
Производные гидроксамовой кислоты формулы II, где R и R вместе с соседним атомом азота образуют пиперидиновую группу, R3 представляет собой пиридильную группу, и m, и n имеют значение 0, Х такой, как определено выше, и их фармацевтически приемлемые соли присоединения кислот являются особенно предпочтительными. Из них O-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим и его фармацевтически приемлемые соли присоединения кислот, в частности моногидрохлорид или дигидрохлорид особенно предпочтительны.
Другой предпочтительный подкласс производных гидроксамовой кислоты формулы I состоит из соединений формулы
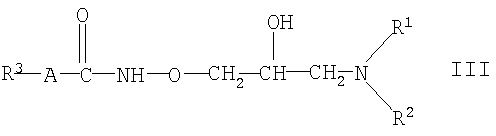
где
R1, R2, R3 и А такие, как определены для формулы I, и их фармацевтически приемлемых солей присоединения кислот.
Другой предпочтительный подкласс производных гидроксамовой кислоты формулы I состоит из циклических соединений формулы
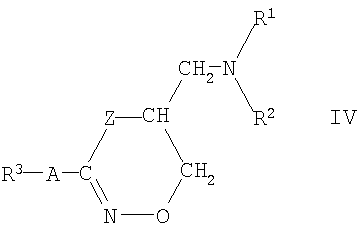
где R1, R2, R3 и А такие, как определены для формулы I, Z представляет собой атом кислорода или группу формулы -N=или -NH-, и их фармацевтически приемлемых солей присоединения кислот.
Еще один предпочтительный подкласс производных гидроксамовой кислоты формулы I состоит из соединений формулы
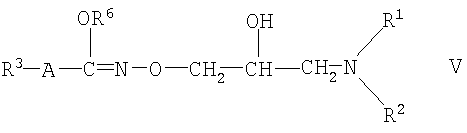
где R1, R2, R3 и А такие, как определены для формулы I, R6 обозначает С1-4-алкильную группу, и их фармацевтически приемлемых солей присоединения кислот.
Соединения формулы I могут быть получены по способам, известным из Патента US 4308399, ЕР 417210 и Венгерской патентной заявки, раскрытой под №7766350.
В синергичном фармацевтическом составе по настоящему изобретению массовое (или весовое) соотношение (а) противодиабетического или антигиперлипидемического активного агента или, если необходимо и химически возможно, его фармацевтически приемлемой соли присоединения кислоты или соли, образованной с фармацевтически приемлемым основанием, и (b) производного гидроксамовой кислоты формулы I или его фармацевтически приемлемой соли присоединения кислоты составляет в основном (1-100):(100-1). Одна или две фармацевтические композиции фармацевтического состава пригодны для перорального или парентерального введения и представляют собой твердые или жидкие композиции. Подходящие лекарственные формы и их изготовление, а также полезные носители известны из литературы, например из Remington′s Pharmaceutical Sciences, Mack Publishing Co., Easton, USA.
Предпочтительно, чтобы синергичный фармацевтический состав по настоящему изобретению содержал: (а) производное гидроксамовой кислоты формулы II или его фармацевтически приемлемую соль присоединения кислоты, и (b) противодиабетический или антигиперлипидемический активный агент или, если необходимо и химически возможно, его фармацевтически приемлемую соль присоединения кислоты, или соль, образованную с фармацевтически приемлемым основанием, где активные агенты представлены в отдельных фармацевтических композициях или в одной общей фармацевтической композиции. Противодиабетический или антигиперлипидемический активный агент может представлять собой, например, одно из соединений, перечисленных выше. Таким образом, предпочтительный синергичный фармацевтический состав по настоящему изобретению может содержать: (а) производное гидроксамовой кислоты формулы II, например O-(3-пиперидино-2-гидрокси-1-пропил)никотинамидоксим или его фармацевтически приемлемую соль присоединения кислоты, такую как дигидрохлорид или моногидрохлорид, а также (b1) противодиабетический активный агент, например инсулин, или инсулинсенсибилизирующий активный агент, такой как производное тиазолидиндиона, например пиоглитазон, троглитазон, циглитазон, росиглитазон, или активный агент, который увеличивает продукцию инсулина, такой как митиглинид, репаглинид, сенаглинид, или сульфамид, такой как толбутамид, хлорпропамид, толазамид, ацетогексамид, глибурид, глипизид, гликлазид, глимепирид, гликвидон, глиборнурид, глизоксепид, глибурид, глизентид, глизоламид, глибузол, гликлопирамид, или производное бигуанидина формулы VI, предпочтительно метформин, буформин, фенформин, или ингибитор α-глюкозидазы, такой как миглитол, акарбоза или воглибоза, или (b2) антигиперлипидемический активный агент, например производное арилоксиалкановой кислоты, такое как клофибрат, гемфиброзил, симфибрат, этофибрат, ципрофибрат, ронифибрат, или ингибитор (ГМГ-КоА)-редуктазы, такой как ловастатин, флувастатин, правастатин, симвастатин, аторвастатин, или производное никотиновой кислоты, такое как аципимокс, ницеритрол, никомол, никоклонат, или антацид желчных кислот, такой как колестипол, холестирамин, полидексид, или, если необходимо и химически возможно, фармацевтически приемлемую соль присоединения кислоты или соль, образованную с фармацевтически приемлемым основанием, соединений, представленных в (b1) и (b2).
Другой предпочтительный фармацевтический состав по настоящему изобретению содержит: (а) соединение формулы III, IV или V или его фармацевтически приемлемую соль присоединения кислоты, а также (b1) противодиабетический активный агент, например инсулин или инсулинсенсибилизирующий активный агент, такой как производное тиазолидиндиона, например пиоглитазон, троглитазон, циглитазон, росиглитазон, или активный агент, который увеличивает продукцию инсулина, такой как митиглинид, репаглинид, сенаглинид, или сульфамид, такой как толбутамид, хлорпропамид, толазамид, ацетогексамид, глибурид, глипизид, гликлазид, глимепирид, гликвидон, глиборнурид, глизоксепид, глибурид, глизентид, глизоламид, глибузол, гликлопирамид, или производное бигуанидина формулы VI, предпочтительно метформин, буформин, фенформин, или ингибитор α-глюкозидазы, такой как миглитол, акарбоза или воглибоза, или (b2) антигиперлипидемический активный агент, например производное арилоксиалкановой кислоты, такое как клофибрат, гемфиброзил, симфибрат, этофибрат, ципрофибрат, ронифибрат, или ингибитор (ГМГ-КоА)-редуктазы, такой как ловастатин, флувастатин, правастатин, симвастатин, аторвастатин, или производное никотиновой кислоты, такое как аципимокс, ницеритрол, никомол, никоклонат, или антацид желчных кислот, такой как колестипол, холестирамин, полидексид, или, если необходимо и химически возможно, фармацевтически приемлемую соль присоединения кислоты или соль, образованную с фармацевтически приемлемым основанием, соединений, представленных в (b1) и (b2).
Влияние состава по настоящему изобретению на чувствительность к глюкозе изучали с помощью следующих тестов. Все проводимые эксперименты соответствуют основным правилам Европейского Сообщества по содержанию и применению экспериментальных животных.
Для экспериментов использовали взрослых самцов белых новозеландских крыс весом 3-3,2 кг, помещенных в комнату для животных (12-часовые периоды света/темноты в день, температура 22-25°С, относительная влажность 50-70%), с одним животным на небольшой загон, получающим стандартную лабораторную пищу и водопроводную воду неограниченно. Животных оперировали по прошествии двухнедельного периода адаптации.
Операцию проводили в стерильных условиях. Крыс подвергали анестезии с помощью внутривенного болюса 10 мг/кг диазепама (Sigma, St. Louis, МО, USA) и 5 мг/кг кетамина (EGIS Pharmaceuticals Ltd., Budapest, Hungary). Лидокаин (EGIS Pharmaceuticals Ltd., Budapest, Hungary) вводили подкожно для местного обезболивания, как описано у Szilvassy Z. с соавт.(Br. J. Pharmacol., 112, 999-1001, 1994). Полиэтиленовые катетеры вводили в два основных ответвления яремной вены и левую сонную артерию. Катетеры выводили на поверхность через заднюю часть шеи. Эти трубки сохраняли открытыми, заполняя их раствором гепарина натрия (100 МЕ/мл).
Клэмп-исследования содержания глюкозы при гиперинсулинемической эугликемии
Обычный человеческий инсулин вводили с постоянной скоростью (13 мЕ/кг, NOVO Nordisk, Copenhagen) через один из венозных катетеров в течение 120 мин. Это вливание инсулина давало иммунореактивность плазматического инсулина 100±5 мкЕ/мл в стационарном состоянии. Это значение соответствует пятикратному значению нормального верхнего предела данной величины. Образцы крови (0,3 мл) брали из артериальной канюли для определения концентрации глюкозы через 10 мин интервалы. Концентрацию глюкозы в крови поддерживали на постоянном уровне (5,5±0,5 ммоль/литр) путем изменения скорости вливания глюкозы через вторую венозную канюлю. Когда концентрацию глюкозы в крови удавалось стабилизировать по меньшей мере на 30 мин, авторы определяли это состояние как стационарное. В стационарном состоянии отбирали дополнительные образцы крови (0,5 мл) для определения плазматического инсулина через интервалы 10 мин. Скорость вливания глюкозы (мг/кг/мин) во время стационарного состояния использовали для характеристики чувствительности к инсулину [DeFronzo R.A. et al., Am. J. of Physiol., 237. E 214-223 (1979)]. Тест-соединение(я) вводили, соответственно, здоровым и гиперхолестеринемичным животным перорально, в одну дозу, один раз в сутки в течение пяти дней, и определяемые скорости вливания глюкозы на 6-й день усредняли в пределах каждой тест-группы, состоящей из 6 животных. В качестве контроля брали одну группу здоровых и одну группу гиперхолестеринемичных животных. Полученные результаты представлены в Таблицах 1 и 2.
Чувствительность к инсулину (обратно пропорциональна инсулинорезистентности), охарактеризованная с помощью скорости вливания глюкозы в мг/кг/мин во время стационарного состояния
Норма = в этом тесте использовали здоровых животных;
BGP-15 = О-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим гидрохлорид.
В указанных выше тестах фактически было измерено количество глюкозы, введенной для получения постоянного уровня глюкозы в крови. Предпочтительно, чтобы при заданном постоянном уровне глюкозы в крови требовалось большее количество глюкозы, что свидетельствовало бы о повышенном эффекте инсулина. Поэтому измеряют более высокую скорость вливания глюкозы, получают более высокую эффективность в присутствии исследуемого соединения.
Пероральное введение метформина в дозе 100 мг/кг вызывало некоторое увеличение чувствительности к инсулину (т.е. снижение инсулинорезистентности), и еще большее снижение инсулинорезистентности достигалось при пероральном введении 30 мг/кг BGP-15, однако скорость вливания глюкозы, характерная для здоровых животных, все же не достигалась. Однако одновременное введение гаперхолестеринемичным животным обоих активных агентов в указанных выше дозах позволяло достичь скорости вливания глюкозы, находящейся в диапазоне, характерном для здоровых животных.
Также результаты, представленные в Таблице 1, свидетельствуют о том, что инсулинорезистентность у гиперхолестеринемичных животных практически не уменьшалась при пероральном введении более высоких доз (50 мг/кг и 100 мг/кг) BGP-15. Точно также не уменьшало инсулинорезистентность гиперхолестеринемичных животных и введение 300 мг/кг метформина по сравнению с введением дозы 100 мг/кг. Скорость вливания глюкозы, характерная для здоровых животных (т.е. состояние, характеризующееся отсутствием инсулинорезистентности), достигалась только при одновременном введении BGP-15 и метформина, даже при самых низких дозировках этих веществ.
Изобретение включает также способ лечения или профилактики преддиабетического состояния, метаболического Х-синдрома или сахарного диабета типа 2, а также нарушений, которые связаны с выше описанными состояниями, а именно эндогенных нарушений обмена веществ, инсулинорезистентности, дислипидемии и/или эндокринных нарушений у женщин, обусловленных преобладанием андрогенов, в соответствии с которым пациенту, предрасположенному или страдающему от указанных выше состояний, вводят терапевтически эффективное количество противодиабетического или антилипидемического активного агента или, если необходимо и химически возможно, его фармацевтически приемлемой соли присоединения кислоты, или соли, образованной с фармацевтически приемлемым основанием, и производного гидроксамовой кислоты формулы I, или его фармацевтически приемлемой соли присоединения кислоты.
Противодиабетический или антигиперлипидемический активный агент и производное гидроксамовой кислоты формулы I можно вводить одновременно или один после другого через короткий промежуток времени, длящийся, например, от нескольких секунд или минут, или более длительный промежуток времени, длящийся, например, от 10 до 30 минут.
Поскольку производное гидроксамовой кислоты формулы I синергично усиливает терапевтический эффект противодиабетического или ангигиперлипидемического активного агента, в способе по настоящему изобретению суточная доза противодиабетического или антигиперлипидемического агента ниже их обычной суточной дозы, использующейся в традиционном лечении, когда не вводят производное гидроксамовой кислоты формулы I.
Применяя способ по настоящему изобретению, можно, в частности, предупредить развитие следующих клинических состояний (или если они уже имеются, то можно их улучшить):
- преддиабетическое состояние, такое как непереносимость глюкозы или инсулинорезистентность,
- метаболический Х-синдром,
- оба типа диабета (инсулинзависимого сахарного диабета и инсулиннезависимого сахарного диабета),
- диабетические осложнения, особенно в отношении ретинопатии, нейропатии, нефропатии, синдрома поликистоза яичников, сахарного диабета беременных, артериальной гипертонии, дислипидемии, артериосклероза, ожирения, сердечной ишемии, ассоциированной с диабетом и т.д.
Таким образом, изобретение включает применение производного гидроксамовой кислоты формулы I или его фармацевтически приемлемой соли присоединения кислоты для приготовления фармацевтической композиции, которая синергично усиливает действие активного агента, особенно противодиабетического или антигиперлипидемического активного агента, применяющегося для профилактики или лечения преддиабетического состояния, метаболического Х-синдрома или сахарного диабета, а также нарушений, которые связаны с выше описанными состояниями, а именно эндогенных нарушений обмена веществ, инсулинорезистентности, дислипидемии, алопеции, распространенного выпадения волос и/или эндокринных нарушений у женщин, обусловленных преобладанием андрогенов. Следовательно, фармацевтическую композицию, содержащую в качестве активного агента производное гидроксамовой кислоты формулы I или его фармацевтически приемлемую соль присоединения кислоты, можно введить пациенту, которого лечат с помощью противодиабетического или антигиперлипидемического активного агента, для профилактики или лечения преддиабетического состояния, метаболического Х-синдрома или сахарного диабета, а также нарушений, которые связаны с выше описанными состояниями, а именно эндогенных нарушений обмена веществ, инсулинорезистентности, дислипидемии, алопеции, распространенного выпадения волос и/или эндокринных нарушений у женщин, обусловленных преобладанием андрогенов. Введение фармацевтической композиции, содержащей в качестве активного агента производное гидроксамовой кислоты формулы I или его фармацевтически приемлемую соль присоединения кислоты, приводит к применению более низкой дозы противодиабетического или антигиперлипидемического активного агента. Когда фармацевтическую композицию, содержащую в качестве активного агента производное гидроксамовой кислоты формулы I или его фармацевтически приемлемую соль присоединения кислоты, например О-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим или его фармацевтически приемлемую соль присоединения кислоты, такую как дигидрохлорид или моногидрохлорид, вводят пациенту, страдающему от диабета и получающему регулярное лечение инсулином, то суточная доза инсулина может быть уменьшена, и таким образом можно избежать развития инсулинорезистентности.
Дополнительные экспериментальные данные
При проведении следующих тестов применяли ту же процедуру, что описана выше, с той разницей, что использовали глибурид, ловастатин и симвастатин вместо метформина. Полученные результаты представлены в Таблицах 2, 3 и 4.
Чувствительность к инсулину (обратно пропорциональна инсулинорезистентности), охарактеризованная с помощью скорости вливания глюкозы в мг/кг/мин во время стационарного состояния
Норма = в этом тесте использовали здоровых животных;
BGP-15=О-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим гидрохлорид.
Скорость вливания глюкозы, характерная для здоровых животных, также определялась как соответствующее значение в контрольной группе, состоящей из нормальных кроликов.
Данные Таблицы 2 свидетельствуют о том, что скорость вливания глюкозы у гиперхолестеринемичных (контрольная группа) меньше, чем у здоровых (т.е. нормальных) животных (контрольная группа). Этот факт свидетельствует о значительной инсулинорезистентности в гиперхолестеринемичной группе. Значения, характерного для здоровых животных, не удавалось достичь с помощью увеличения дозы BGP-15. Введение гиперхолестеринемичным животным различных доз глибурида даже уменьшало скорость вливания глюкозы, т.е. увеличивало инсулинорезистентность. Скорости вливания глюкозы, характерной для здоровых животных, достигали только при одновременном введении BGP-15 и глибурида, причем даже в самых низких дозах.
Чувствительность к инсулину (обратно пропорциональна инсулинорезистентности), охарактеризованная с помощью скорости вливания глюкозы в мг/кг/мин во время стационарного состояния
Норма = в этом тесте использовали здоровых животных;
BGP-15 = О-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим гидрохлорид.
Скорость вливания глюкозы, характерная для здоровых животных, также определялась как соответствующее значение в контрольной группе, состоящей из нормальных кроликов.
Данные Таблицы 3 свидетельствуют о том, что скорость вливания глюкозы у гиперхолестеринемичных (контрольная группа) меньше, чем у здоровых (т.е. нормальных) животных (контрольная группа). Этот факт свидетельствует о значительной инсулинорезистентности в гиперхолестеринемичной группе. Значения, характерного для здоровых животных, не удавалось достичь с помощью увеличения дозы BGP-15. Введение гиперхолестеринемичным животным различных доз ловастатина даже уменьшало скорость вливания глюкозы, т.е., увеличивало инсулинорезистентность. Скорости вливания глюкозы, характерной для здоровых животных, достигали только при одновременном введении BGP-15 и ловастатина, причем даже в самых низких дозах.
Чувствительность к инсулину (обратно пропорциональна инсулинорезистентности), охарактеризованная с помощью скорости вливания глюкозы в мг/кг/мин во время стационарного состояния
Норма = в этом тесте использовали здоровых животных;
BGP-15 = O-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксим гидрохлорид.
Скорость вливания глюкозы, характерная для здоровых животных, также определялась как соответствующее значение в контрольной группе, состоящей из нормальных кроликов.
Данные Таблицы 4 свидетельствуют о том, что скорость вливания глюкозы у гиперхолестеринемичных (контрольная группа) меньше, чем у здоровых (т.е. нормальных) животных (контрольная группа). Этот факт свидетельствует о значительной инсулинорезистентности в гиперхолестеринемичной группе. Значения, характерного для здоровых животных, не удавалось достичь с помощью увеличения дозы BGP-15. Введение гаперхолестеринемичным животным различных доз симвастатина даже уменьшало скорость вливания глюкозы, т.е. увеличивало инсулинорезистентность. Скорости вливания глюкозы, характерной для здоровых животных, достигали только при одновременном введении BGP-15 и симвастатина, причем даже в самых низких дозах.
Ту же процедуру, что описана выше, применили для изучения эффекта различных доз метформина и глибурида на гиперхолестеринемических кроликов. Полученные результаты представлены в Таблице 5.
Чувствительность к инсулину (обратно пропорциональна инсулинорезистентности), охарактеризованная с помощью скорости вливания глюкозы в мг/кг/мин во время стационарного состояния
Данные, представленные в Таблице 5, свидетельствуют о том, что значение инсулинорезистентности, характерное для здоровых животных, не может быть достигнуто путем одновременного введения гиперхолестеринемичным кроликам 100 мг/кг метформина и 1 мг/кг глибурида.
В таблицах большая величина скорости вливания глюкозы соответствует большему эффекту увеличения чувствительности к инсулину.
Результаты показывают, что у гиперхолестеринемичных животных и глибурид, и ловастатин, и симвастатин при использовании только их, снижали эффект чувствительности к инсулину, однако комбинации BGP-15 и глибурида, комбинации BGP-15 и ловастатина и комбинации BGP-15 и симвастатина давали эффект увеличения чувствительности к инсулину, который был больше, чем эффект от BGP-15, таким образом доказывая, что имеет место синергизм.
Следует отметить, что глибурид является представителем таких противодиабетических агентов, как производные сульфонилмочевины (см. выше), метформин является представителем противодиабетических агентов бигуанидов (стр.10 описания); и ловастатин - представитель антигиперлипидемических агентов ингибиторов ГМГ-КоА редуктазы (см. выше).
Следовательно, экспериментальные данные демонстрируют, что между производными гидроксамовых кислот формулы I (т.е. BGP-15) и представителями очень разных групп противодиабетических и антигиперлипидемических агентов имеет место синергизм.
Это также, дополнительно, подтверждает изобретательский уровень заявленного изобретения.
Экспериментальные данные для комбинации BGP-15 и инсулина у крыс с резистентностью к инсулину
В экспериментах использовали взрослых самцов крыс Goto-Kakizaki массой 200-220 г. Крысы Goto-Kakizaki имеют резистентность к инсулину, таким образом давая модель животных, у которых количество глюкозы в крови регулируется не так эффективно, как у здоровых животных. Животных размещали в камере для животных (с периодами свет/темнота по 12 часов, 22-25°С, относительная влажность 50-75%), по два животных в секции, с кормлением пищей для лабораторных животных. Эксперимент проводили по прошествии периода адаптации, составлявшего две недели.
В этих экспериментах применяли метод быстрого тестирования чувствительности к инсулину (RIST). Животных (шесть животных в группе) анестезировали сначала внутрибрюшинной дозой тиопентал-натрия 50 мг/кг, поддерживая затем непрерывную анестезию внутривенной инфузией раствора тиопентал-натрия (1,5 мг/мл/100 г массы тела). В правую яремную вену помещали канюлю для введения инсулина с последующей инфузией глюкозы. На правой стороне формировали артериально-венозную петлю между сонной артерией и яремной веной для отбора образцов. Петлю поддерживали открытой, обрабатывая ее солевьм раствором гепарина.
Получили три стабильных последовательных уровня глюкозы в крови, затем, в тестах с инсулином, осуществляли внутривенное вливание человеческого инсулина 50 мЕд/кг (NOVO, Nordisk, Копенгаген) в течение пяти минут. Затем проводили вливание глюкозы с разной скоростью инфузии для поддержания фонового уровня глюкозы в крови. Готовили раствор глюкозы в солевом буфере (100 мг/мл). Чтобы избежать гипогликемии, вливание глюкозы начинали через 1 минуту после вливания инсулина с варьирующей скоростью 2,5-5 мг/кг/минута. Скорость вливания глюкозы регулировали так, чтобы она варьировала по концентрации глюкозы в артериальной крови, измеренной через 2-минутные интервалы, для поддержания фонового уровня глюкозы в крови. Общее количество введенной глюкозы рассматривается как мера чувствительности к инсулину, выраженная как индекс быстрого теста чувствительности к инсулину (RIST).
Для групп, обрабатываемых BGP-15, дозы 20 мг/кг O-(3-пиперидино-2-гидрокси-1-пропил)никотиновой кислоты амидоксима дигидрохлорида, растворенные в физиологическом растворе, вводили перорально один раз в сутки в течение пяти дней, и индекс RIST определяли на пятый день через 4-6 часов после последней обработки. Полученные результаты представлены в Таблице 6.
Чувствительность к инсулину, характеризуемая потреблением глюкозы, в мг/кг (индекс RIST)
Данные показывают, что одновременное введение BGP-15 и инсулина дают трехкратное увеличение потребления глюкозы по сравнению с обработкой одним инсулином у крыс, имеющих резистентность к инсулину. Следовательно, в присутствии BGP-15 инсулин может регулировать требуемый уровень глюкозы даже в случае потребления трехкратного количества сахара.
Результаты приведенных выше тестов подтверждают наличие синергизма между BGP-15 и использующимися в тестах активными веществами, т.е. метформином, глибуридом, ловастатином, симвастатином и инсулином. Эффект, который достигается в результате синергетического действия, не может быть получен при введении одного компонента даже при повышении дозы. Существование синергизма между BGP-15 и любым из остальных активных агентов является неожиданным, поскольку одновременное введение двух противодиабетических агентов (т.е. метформина и глибурида) не привело к достижению скорости вливания глюкозы, характеризующей здоровых (т.е. нормальных) животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| УМЕНЬШЕНИЕ ИЗБЫТОЧНОЙ МАССЫ ТЕЛА ИЛИ ОЖИРЕНИЯ | 2007 |
|
RU2443417C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИПСИХОТИЧЕСКОЙ, АНТИДЕПРЕССАНТНОЙ ИЛИ ПРОТИВОЭПИЛЕПТИЧЕСКОЙ АКТИВНОСТЬЮ, СО СНИЖЕННЫМ ПОБОЧНЫМ ЭФФЕКТОМ | 2007 |
|
RU2440116C2 |
| СПОСОБЫ ИСПОЛЬЗОВАНИЯ ДИАЦЕРЕИНА В ДОПОЛНИТЕЛЬНОМ ЛЕЧЕНИИ ДИАБЕТА | 2011 |
|
RU2563988C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ВАНАДИЯ, ОБЛАДАЮЩИЕ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2709491C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОДИАБЕТИЧЕСКОЙ, ГИПОЛИПИДЕМИЧЕСКОЙ, ГИПОГЛИКЕМИЧЕСКОЙ И ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ УКАЗАННЫХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2361581C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРА DPP-IV ДЛЯ СНИЖЕНИЯ ПРИСТУПОВ ГЛИКЕМИИ | 2006 |
|
RU2440143C2 |
| СПОСОБ СНИЖЕНИЯ ВЕСА | 2013 |
|
RU2664442C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА | 2004 |
|
RU2367423C2 |
| НОВОЕ ПРИМЕНЕНИЕ АГОНИСТОВ ПЕЧЕНОЧНОГО РЕЦЕПТОРА Х | 2006 |
|
RU2417078C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДИАБЕТА ИЛИ ОЖИРЕНИЯ, СОДЕРЖАЩАЯ СОЕДИНЕНИЕ, ИНГИБИРУЮЩЕЕ АКТИВНОСТЬ ДИПЕПТИДИЛПЕПТИДАЗЫ-IV, И ДРУГИЕ ПРОТИВОДИАБЕТИЧЕСКИЕ СРЕДСТВА ИЛИ СРЕДСТВА ПРОТИВ ОЖИРЕНИЯ В КАЧЕСТВЕ АКТИВНЫХ ИНГРЕДИЕНТОВ | 2009 |
|
RU2466727C1 |
Изобретение относится к лекарственным средствам и касается синергичного фармацевтического состава, включающего: (а) первую фармацевтическую композицию, содержащую противодиабетический активный агент, выбранный из группы, состоящей из инсулина, метформина и глибурида, или антигиперлипидемический активный агент, выбранный из группы, состоящей из ловастатина и симвастатина, и один или более стандартных носителей, и (b) вторую фармацевтическую композицию, содержащую O-(3-пиперидино-2-гидрокси-1-пропил)-никотинамидоксим или его фармацевтически приемлемую соль и один или более стандартных носителей. Фармацевтический состав пригоден для профилактики или лечения инсулинорезистентности, метаболического Х-синдрома или сахарного диабета типа 2. Состав по изобретения обладает высокой эффективностью при более низких дозах, что приводит к снижению токсичности лечения. 2 н. и 1 з.п. ф-лы, 5 табл.
a) первую фармацевтическую композицию, содержащую противодиабетический активный агент, выбранный из группы, состоящей из инсулина, метформина и глибурида, или антигиперлипидемический активный агент, выбранный из группы, состоящей из ловастатина и симвастатина, или, если необходимо и химически возможно, его фармацевтически приемлемую соль присоединения кислоты или соль, образованную с фармацевтически приемлемым основанием, и один или более стандартных носителей, и
b) вторую фармацевтическую композицию, содержащую O-(3-пиперидино-2-гидрокси-1-пропил)-никотинамидоксим или его фармацевтически приемлемую соль присоединения кислоты, и один или более стандартных носителей.
| WO 00/07580 A2 20.09.2001 | |||
| US 5328906 A 12.06.1994 | |||
| US 4308399 A 29.12.1981 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Новая волна, 2001, том I, с.448-451; том II, с.17-23. |
Авторы
Даты
2007-12-10—Публикация
2002-07-10—Подача