Изобретение относится к применению специфически модифицированного крахмала в качестве агента для получения термообратимого геля.
Для модификации крахмала известно много различных путей. В зависимости от проведенной модификации получают крахмалистые продукты, пригодные для различных применений. Многие из известных модификаций крахмала приводят к получению относительно вязких растворов, с которыми из-за этого трудно обращаться. В других случаях, действительно, может быть получена низкая вязкость, но тогда молекулярная масса существенно уменьшается, так что утрачиваются многие обычные для крахмала качества.
Другая проблема с продуктами из клейстеризованного крахмала - это ретроградация, при которой растворенные молекулы амилозы постепенно и необратимо становятся нерастворимыми. Не подверженный ретроградации раствор крахмала может быть получен с использованием крахмалов, в которых нет амилозы. С этой целью амилопектин и амилоза могут быть отделены от крахмала любого типа, но эти процедуры являются трудоемкими. Крахмалы без амилозы могут быть также извлечены из специальных культур, в которых амилоза не образуется. Тогда такие культуры должны быть выращены для этой цели. Не подверженные ретроградации крахмалы могут быть также получены путем химической дериватизации, но это вызывает введение посторонних групп, которые влияют на свойства крахмала. И наконец, ретроградацию можно также предотвратить путем повышения декстрозного эквивалента (ДЭ) раствора крахмала посредством ферментативного гидролиза, но тогда полимерный характер крахмала нарушается и иногда полностью утрачивается.
Кроме того, известно, что конкретные производные крахмала способны образовывать крахмальные гели, которые предоставляют различные возможности применения, но пока крахмальные гели могут быть получены при предпочтительно высоких концентрациях по меньшей мере 10%, как известно из Carbohydrate Polymeres 231 (1993), 243-248.
В настоящее время обнаружено, что крахмал, модифицированный особым образом, является исключительно подходящим для образования термообратимого геля.
В настоящее время обнаружено также, что крахмал, модифицированный таким образом, уже в низкой концентрации способен образовывать термообратимый гель.
Модифицированный крахмал для использования согласно изобретению характеризуется также низкой вязкостью в водном растворе, так что с продуктом легко обращаться и легко его перерабатывать, и такой водный раствор пригоден для различных применений.
Замечательно, что модифицированный крахмал для использования согласно изобретению по существу идентичен исходному материалу, что касается средней молекулярной массы, восстанавливающей способности (ДЭ) и процентной доли разветвления. Поэтому полимерные свойства сохраняются, к тому же не происходит увеличения мест, чувствительных к окислению (ДЭ остается практически неизмененным).
В соответствии с указанными выше целями изобретение характеризуется тем, что модифицированный крахмал, получаемый путем обработки содержащего амилозу крахмала в водной среде ферментом из группы α-1,4-α-1,4-глюкозилтрансфераз (ЕС 2.4.1.25) или ферментом, активность которого соответствует активности ферментов из указанной группы, - все эти ферменты будут кратко называться ниже как глюкозилтрансфераза - используют в качестве агента для образования термообратимого геля. Обычная и соответствующая этому активность глюкозилтрансфераз проявляется в том, что они способны расщеплять α-1,4 связь между двумя звеньями глюкозы так, чтобы впоследствии образовать новую α-1,4 связь.
Изобретение, кроме того, характеризуется применением модифицированного крахмала, как определено выше, в виде водного раствора, который, как установлено, имеет относительно низкую вязкость.
Как используется здесь, термин "крахмал" содержит как нативный крахмал, так и незамещенные производные крахмала. Под последними подразумевают крахмалы, полученные путем частичного расщепления нативного крахмала путем кислотного и/или ферментативного гидролиза до достижения ДЭ не более чем 5, потому что иначе полимерный характер крахмала утрачивается. Крахмал для использования в процессе превращения его глюкозилтрансферазой должен, как установлено, содержать амилозу, предпочтительно в количестве по меньшей мере 5 мас. %. Кроме того, исходный крахмал должен также содержать амилопектин, который, однако, естественно уже присутствует в крахмале. Поэтому нативные крахмалы, содержащие амилозу и амилопектин, такие как картофельный крахмал, кукурузный крахмал, пшеничный крахмал, рисовый крахмал и тапиоковый крахмал, а также их незамещенные производные, могут быть использованы в качестве исходного крахмала.
Глюкозилтрансферазы, которые должны быть использованы, могут быть получены из различных организмов. Из литературы известно, что эти ферменты встречаются в представителях Eukarya и Bacteria. Кроме того, известно, что глюкозилтрансферазы присутствуют также в представителях Archae. Предпочтительно используют глюкозилтрансферазу, которая является стойкой к высокой температуре, например температуре около 70oС. Примерами их являются глюкозилтрансферазы из Thermus thermophilus, Thermotoga maritima и из термофильных представителей Archae. Но и нетермостойкие глюкозилтрансферазы, например из картофеля или Escherichia coli, являются полезными при осуществлении изобретения. Если необходимо, фермент должен быть очищен от ферментативных компонентов, которые могут вызывать нежелательное повреждение или разрушение молекулы крахмала. Поэтому фермент должен быть по существу свободен от загрязняющей активности α-амилазы. Специалистам в этой области известно, как проводить такую очистку.
Ферментативное превращение глюкозилтрансферазой может быть проведено как с клейстеризованным крахмалом, так и с крахмалом, который еще находится в форме гранул, но затем в набухшем состоянии, или, иными словами, с таким, который только частично клейстеризован. В предыдущем случае глюкозилтрансфераза может быть добавлена к уже клейстеризованному раствору крахмала, после чего его охлаждают, например, до желательной температуры реакции. В последнем случае глюкозилтрансфераза может быть добавлена к суспензии крахмала в любой желательный момент.
Условия реакции для проведения ферментативного превращения зависят от используемой глюкозилтрансферазы и легко могут быть определены специалистами в этой области. На практике это обычно делают при рН или около рН, при котором фермент имеет оптимальную активность. Соответственно, чем больше фермента используют, тем более быстро протекает превращение, и также более высокая температура улучшает ожидаемое ферментативное превращение. Конечно, когда выбирают температуру, должна учитываться термостойкость используемой глюкозилтрансферазы. Когда используют преимущественно термостойкий фермент, ферментативное превращение предпочтительно проводят при температуре в диапазоне 60-75oС. Протекание реакции превращения может отслеживаться посредством уменьшения вязкости. После достижения желательного снижения вязкости реакцию превращения прекращают. Предпочтительно, однако, проводить реакцию превращения до тех пор, когда не будет происходить дальнейшего снижения вязкости.
После осуществления желательного ферментативного превращения фермент может быть дезактивирован, если желательно, путем нагревания реакционной смеси. Когда начинают с суспензии крахмала, она может быть затем также превращена в раствор. Если желательно, фермент, который может быть дезактивированным или недезактивированным, может быть также отделен от реакционной смеси методами, известными специалистам, такими как диализ. Фактически, для конкретных применений присутствие глюкозилтрансферазы недопустимо. Если желательно, полученный раствор крахмала может быть концентрирован или может быть извлечен сухой модифицированный крахмал в виде порошка. Кроме того, согласно потребности могут быть проведены обработки промыванием, например, холодной водой или растворами, имеющими повышающиеся концентрации этанола, после чего может иметь место сушка.
Водный раствор крахмала, модифицированного глюкозилтрансферазой, имеет свойство образовывать при охлаждении гель, который при повышении температуры переходит снова в раствор. Таким образом, это термообратимый гель, и изобретение как раз направлено на применение модифицированного крахмала, который может быть получен описанным способом, в качестве термообратимого геля. Это термообратимое поведение обычно наблюдается при низкой концентрации, например около 3 мас.%, модифицированного крахмала, так что когда используют это термообратимое поведение согласно изобретению, небольшое количество модифицированного крахмала уже может быть достаточным.
Как вкратце установлено выше, водный раствор крахмала, модифицированного глюкозилтрансферазой, имеет низкую вязкость. Фактически, водный раствор около 10 мас. % имеет значительно более низкую вязкость, чем 10 мас.%-ный раствор немодифицированного крахмала. Поэтому продукт очень легко перерабатывать. Более того, средняя молекулярная масса, восстанавливающая способность (ДЭ) и процентная доля разветвления сохраняются практически неизменными по отношению к исходному материалу. Отсюда можно сделать вывод, что между различными типами молекул крахмала имеет место взаимная перегруппировка без увеличения мест, чувствительных к окислению, или частей, имеющих восстановительную активность. Наконец, оказывается, что либо происходит незначительная ретроградация, либо ее нет вообще, так что рассматриваемый продукт является очень стабильным.
Крахмал, модифицированный ферментативным превращением указанным образом, пригоден для многих применений, где свойство образовывать термообратимый гель может быть полезным или важным, например в пищевых продуктах, косметике, фармацевтических препаратах, детергентах, адгезивах и бурильных жидкостях. Эти применения, как таковые, известны специалистам, так что нет необходимости обсуждать их здесь более подробно. Для этих применений стабильность модифицированного крахмала и тот факт, что ожидаемая термообратимая активность может быть достигнута уже при низкой концентрации, например только при около 3 мас.%, являются важными преимуществами. Какое количество дает оптимальную активность в конкретном случае, может быть легко определено специалистами путем эксперимента.
Изобретение далее будет пояснено на следующих примерах.
Пример 1
(Очистка термостойкой глюкозилтрансферазы из Thermus thermophilus)
Активность глюкозилтрансферазы определяют путем определения количества глюкозы, образовавшейся из мальтотриозы при 70oС и рН 6,5 в 50 мМ малеатном буфере. Активность выражают в мкмоль глюкозы в минуту на миллиграмм белка (единицах на мг).
Стадия 1. Термофильные грамотрицательные зубактерии Thermus thermohilus HB8 культивируют в ферментере вместимостью 40 л, имеющем рабочий объем 35 л. Питательная среда содержит (на литр): 50 г дрожжевого экстракта, 50 г касаминокислот, 10 г сахарозы, 2,5 г (NH4)2SО4, 0,2 г MgCl2, 6,2 г К2НРО4, 2,2 г NaH2PО4. Культивирование осуществляют при температуре 70oС и рН поддерживают при 7,0 с помощью 2 М NaOH. Для уменьшения пенообразования добавляют пеноподавитель. После ферментации клетки собирают путем фильтрования в поперечном потоке и центрифугирования. Клетки замораживают при -20oС. Перед очисткой 40 г клеток (влажная масса) оттаивают и добавляют 1 мг DNазы. Все это подвергают обработке ультразвуком 14•20 с, зонд 9 мм, 18 Вт. Остатки клеток удаляют путем центрифугирования (60 мин, 30000g). Супернатант осторожно сливают. Вязкую лепешку промывают снова 50 мМ Tris-НСl рН 7,5 и снова центрифугируют. Два супернатанта объединяют и используют как свободный от клеток экстракт (140 мл).
Стадия 2. Свободный от клеток экстракт распределяют на 10 пробирок и инкубируют 5 мин при 90oС. Осажденный материал удаляют посредством центрифугирования (15 мин, 17000g обор. в мин).
Стадия 3. Материал со стадии 2 переносят в 30% (насыщение) (NH4)2SO4 (23,0 г) и инкубируют 15 мин при 4oС. Осажденный материал удаляют посредством центрифугирования (15 мин, 17000g) и супернатант (150 мл) переносят в 60% (насыщение) (NH4)2SО4 (27,2 г). После 15 мин инкубирования при 4oС лепешку, полученную посредством центрифугирования (15 мин, 17000g), растворяют в 25 мМ Tris-HCl рН 7,5 и подвергают диализу в течение ночи против 1 л того же буфера.
Стадия 4. Диализованный материал со стадии 3 (40 мл) разделяют на две порции по 20 мл. Каждую порцию отдельно разделяют посредством анионообменной хроматографии MonoQ (HR 10/10) (Pharmacia). Несвязанные белки вымывают из колонки до тех пор, пока А280 элюента не станет ниже, чем 0,05. Связанные белки элюируют 240 мл с градиентом NaCl от 0 до 0,5 М в 20 мМ Tris-HCl рН 7,5 (4 мл/мин, фракция: 4 мл). Фракции двух ступеней разделения, в которых присутствует наивысшая активность глюкозилтрансферазы, объединяют.
Стадия 5. Материал со стадии 4 подвергают диализу в течение ночи против 1 мл 20 мМ Tris-HCl pH 6,8 с 0,25 М NaCl. Материал связывают с хелатирующей Superose HR (10/2) (Pharmacia), насыщенной ионами меди согласно предписанию производителя. Несвязанные белки вымывают из колонки до тех пор, пока A280 не станет ниже, чем 0,05. Связанные белки элюируют 30 мл с градиентом NH4Cl от 0 до 3,0 М в 20 мМ Tris-HCl pH 6,8, 0,25 М NaCl (1 мл/мин, фракция: 1 мл). Фракции, в которых присутствует наивысшая активность глюкозилтрансферазы, объединяют.
Стадия 6. Материал со стадии 5 переносят в колонку для гель-фильтрации Superdex 200 HR (26/60) (Pharmacia) и элюируют 20 мМ Tris-HCl pH 7,5, 0,1 М NaCl (2,5 мл/мин, фракция: 5 мл). Фракции, в которых присутствует наивысшая активность глюкозилтрансферазы, объединяют.
Стадия 7. Материал со стадии 6 переносят в 1,7 М (NH4)2SО4 и на алкил-Superose HR (5/5) (Pharmacia). Несвязанные белки вымывают из колонки до тех пор, пока А280 не станет ниже, чем 0,05. Связанные белки элюируют 25 мл с градиентом (NH4)2SО4 от 1/7 М до 0 М в 20 мМ Tris-HCl pH 7,5 (1 мл/мин, фракция: 1 мл). Фракции, в которых присутствует наивысшая активность глюкозилтрансферазы, объединяют и подвергают диализу в течение ночи против 25 мМ Tris-HCl pH 7,5 и хранят при 4oС.
Полученная таким образом глюкозилтрансфераза имеет максимальную активность при температуре 75oС и при pH 6,5. Молекулярная масса лежит между 43 и 54 кД, и фермент является активным как мономер. Определяют первые 35 N-концевых аминокислот. Последовательность определяют как: MELPRAFGLL LHPTSLPGPY GVGVLGQEAR DFLRF (1-буквенный код).
Пример 2
(Модификация клейстеризованного крахмала термостойким ферментом)
Суспензию картофельного крахмала (20 мас.% амилозы, 80 мас.% амилопектина, это также относится к следующим примерам, кроме иначе указанного) в 50 мМ цитрате натрия рН 6,5 (10 мас.% сухого вещества) клейстеризуют в струйном варочном аппарате при 150oС. Полученную вязкую суспензию охлаждают до 70oС и повторно доводят рН до 6,5. Затем 1 мг очищенной глюкозилтрансферазы, как полученная в примере 1, добавляют к 8 л суспензии. Затем раствор инкубируют в течение нескольких часов до тех пор, пока вязкость не достигнет постоянной величины (фиг. 1). Изменение вязкости отслеживают путем регистрации напряжения, необходимого для того, чтобы поддерживать постоянное число оборотов перемешивающего мотора.
Пример 3
(Модификация клейстеризованного крахмала термолабильным ферментом)
Картофельный крахмал клейстеризуют путем инкубирования 5%-ной суспензии крахмала в течение 10 мин при 100oС. Полученную вязкую суспензию охлаждают до 30oС и добавляют 40 мкг картофельного D-фермента к 5 мл суспензии. Реакционную смесь инкубируют в течение 48 часов при 30oС.
Пример 4
(Модификация разбухших крахмальных гранул термостойким ферментом)
5%-ную суспензию картофельного крахмала (5 мл) смешивают с 2 мкг глюкозилтрансферазы из T. thermophilus из примера 1 и нагревают до 70oС, после этого осуществляют инкубирование до тех пор, пока вязкость не станет постоянной (около 24 часов). При 70oС прекрасно видна гранулированная структура разбухшего крахмала. После действия глюкозилтрансферазы гранулированная структура полностью исчезает, хотя без глюкозилтрансферазы гранулированная структура все еще прекрасно видна (фиг.2 - это фаза - контрастная фотография (200х) картофельного крахмала (А) и модифицированного глюкозилтрансферазой картофельного крахмала (В) при 70oС).
Пример 5
(Характеристика крахмала, модифицированного глюкозилтрансферазой)
Проводят некоторые анализы модифицированного крахмала из примеров 2, 3 и 4. В качестве сравнения берут клейстеризованный (2%, 20 мин, 120oС) картофельный крахмал.
Йодные абсорбционные спектры продуктов, полученных в примерах 2, 3 и 4, являются идентичными друг другу, но что касается исходного материала (картофельного крахмала), его абсорбционный максимум сдвигается с 620 до 540 нм (фиг.3). Делают также сравнение с йодным абсорбционным спектром не содержащего амилозы картофельного крахмала (амилопектина).
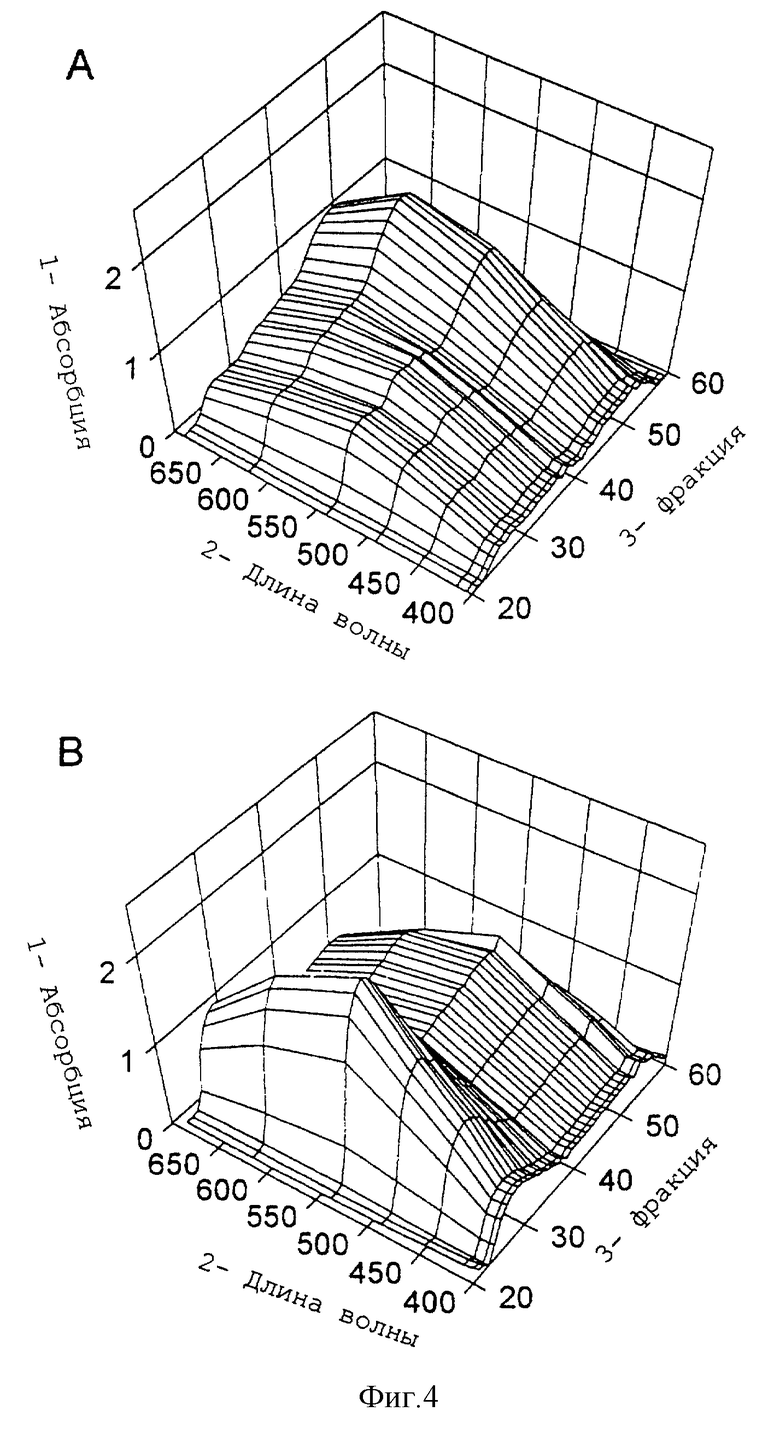
Распределение молекулярной массы растворимого картофельного крахмала, модифицированного глюкозилтрансферазой T. thermophilus из примера 1 (Merck), определенное посредством гель-фильтрующей хроматографии (Superdex 200) и йодного абсорбционного спектра (фиг.4, часть В), изменяется по отношению к исходному материалу (фиг.4, часть А). Наличие двух пиков в части В фиг.4 указывает, что имеет место превращение, хотя модифицированный продукт сохраняет высокую молекулярную массу.
Процентная доля разветвления (отношение между числом α-1,6 связей и числом α-1,4 связей, определенное с помощью фермента изоамилазы, которая расщепляет α-1,6 связи, так что образуется дополнительная восстанавливающая группа; увеличение числа восстанавливающих групп под действием изоамилазы является мерой числа α-1,6 связей или пунктов разветвления) и восстанавливающая способность только слегка изменяются по отношению к исходному материалу (процентная доля разветвления: 2,86% против 2,77% для исходного материала; содержание восстанавливающего: 0,00293 против 0,00288 для исходного материала). Распределение длины боковых цепей действительно изменяется по отношению к исходному материалу, как можно наблюдать после отщепления боковых цепей (фиг. 5 и 6). Фиг.5 показывает профиль элюирования картофельного крахмала после отщепления боковых цепей (А) и модифицированного глюкозилтрансферазой картофельного крахмала после отщепления боковых цепей (В). Олигосахариды отделяют путем ЖХВР на Dionex и определяют с помощью Импульсного Амперометрического Детектора. Числа над пиками указывают длину олигосахаридов. Фиг.6 показывает картину элюирования картофельного крахмала, освобожденного от боковых цепей, и модифицированного глюкозилтрансферазой картофельного крахмала, освобожденного от боковых цепей, который отделяют на колонке для гель-фильтрации (Superdex 200).
Пример 6
(Образование геля)
Раствор, полученный в примере 2, охлаждают до 4oС и затем инкубируют до тех пор, пока не образуется белый гель. Этот материал последовательно промывают водой и 25, 50, 75 и 100%-ным этанолом. Полученный таким образом материал сушат на воздухе и измельчают, чтобы получить порошок, имеющий средний размер частиц около 200 мкм. Получают около 500 г картофельного крахмала, модифицированного глюкозилтрансферазой.
Пример 7
(Термообратимость и образование геля)
С материалом, полученным согласно примеру 6, готовят 5%-ную водную суспензию, которую нагревают до 90oС, пока не получат прозрачный раствор. Этот раствор охлаждают в реометре до 4oС и отслеживают G' (G'') во времени (относительно G' и G'' смотри "Inleiding in de Reologie" 1991, ISBN 90 201 2557 5, pp. 177-189). После установления постоянной величины G' температуру повышают до 70oС и затем снова охлаждают до 4oС. Этот процесс повторяют три раза. В качестве контроля берут 3%-ный раствор картофельного крахмала. Фиг.7 дает гипотетическое изображение установленного изменения вязкости (G') модифицированного глюкозилтрансферазой картофельного крахмала (часть А) и картофельного крахмала (часть В) после трех циклов нагревания и охлаждения. Часть А ясно показывает поведение термообратимого геля.
Начиная с 5%-ной водной суспензии, как описано в этом примере, исследуют образование геля, в отношении которого устанавливают, что это происходит преимущественно при низких температурах порядка 15oС и ниже (фиг.8, которая показывает образование геля (повышение G') модифицированного глюкозилтрансферазой картофельного крахмала при различных температурах).






Описывается агент для образования термообратимого геля, представляющего собой модифицированный крахмал, получаемый путем обработки крахмала, содержащего амилозу, в водной среде ферментом из группы α-1,4-α-1,4-глюкозилтрансфераз (КФ 2.4.1.25) или ферментом, имеющим α-1,4-α-1,4-глюкозилтрансферазную активность, а также продукт в форме термообратимого геля, который в качестве гелеобразующего соединения содержит указанный модифицированный крахмал. Модифицированный крахмал характеризуется низкой вязкостью в водном растворе, что позволяет легко перерабатывать продукты, содержащие модифицированный крахмал. 2 с. и 5 з.п. ф-лы, 8 ил.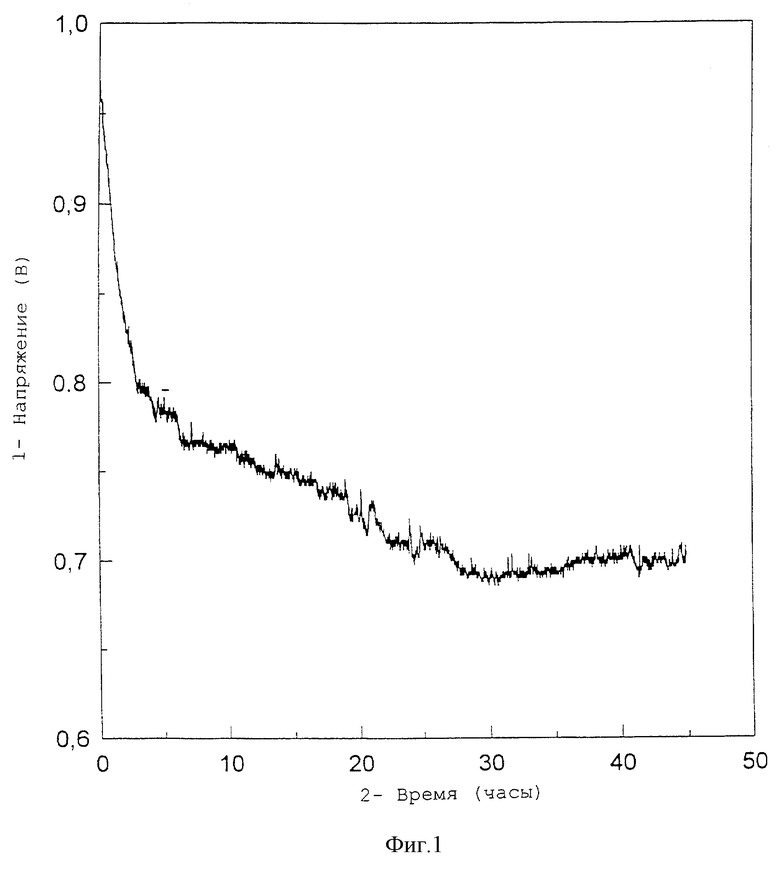
| ЕР 0355908 А, 1990 | |||
| Устройство для измерения зенитного угла скважин | 1978 |
|
SU690170A1 |
| US 3962465 А, 1976 | |||
| ЕР 0616778 А, 1994 | |||
| RU 94016162 А, 1995. | |||
Авторы
Даты
2002-11-27—Публикация
1997-10-06—Подача