Изобретение относится к ранее неизвестному классу соединений, проявляющих высокую активность в индуцировании дифференциации и ингибировании нежелательной пролиферации некоторых клеток, в том числе клеток кожи и раковых клеток, и обладающих иммуномодулирующим и антивоспалительным действиями. Данное изобретение относится также к фармацевтическим препаратам, содержащим эти соединения, к дозировочным единицам этих препаратов и их применению в лечении и/или профилактике заболеваний, характеризующихся ненормальной дифференциацией и/или пролиферацией клеток, например псориаза и других нарушений кератинизации, HIV-ассоциированных дерматозов, залечивании ран, раковых заболеваний, включая рак кожи; заболеваний, являющихся следствием нежелательных процессов в иммунной системе, таких как реакции организма-хозяина против трансплантата и трансплантата против организма-хозяина, а также отторжении трансплантата; аутоиммунных заболеваний, таких как дискоидальная и системная эритематозная волчанка, сахарный диабет и хронические дерматозы аутоиммунного типа, например склеродермия и обыкновенная пузырчатка; воспалительных заболеваний, таких как ревматоидный артрит и астма; а также ряд других патологических состояний, включающих гиперпаратиреоидизм, отчасти вторичный гиперпаратиреоидизм, связанный с почечной недостаточностью, нарушение распознавательной способности, старческое слабоумие (заболевание Альцгеймера (Aizheimers disease)) и другие нейродегенеративные заболевания, повышение артериального давления, кожные угри, выпадение волос, атрофия кожи, например вызванная стероидными гормонами, старение кожи, в том числе процессы старения, спровоцированные действием света. Данное изобретение относится также к использованию этих соединений как содействующих процессам остеогенеза и в лечении/профилактике остеопороза (разрежение костной ткани) и остеомаляции (размягчение костей).
Соединения настоящего изобретения составляют новый класс аналогов витамина D, представленный общей формулой I: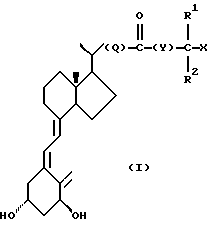
где Х представляет собой водород или гидрокси группу;
R1 и R2 представляют собой метил или этил, или, вместе с атомом углерода, несущим группу X, могут образовывать С3-С5-карбоцикл;
Q представляет собой или одинарную связь, или C1-C8-гидрокарбилен, в котором одна из метиленовых групп, не связанных непосредственно с карбонильной группой, может быть необязательно замещена атомом кислорода (или метил-гидрокси группой);
Y представляет собой или одинарную связь, или C1-С9-гидрокарбилен.
В контексте данного изобретения выражение "гидрокарбилен" обозначает бирадикал, полученный в результате удаления 2 атомов водорода из неразветвленного, разветвленного или циклического, насыщенного или ненасыщенного углеводорода.
Примеры Q и Y (если они не являются одинарной связью) включают, не ограничиваясь ими, следующие группы: метилен, этилен, СН=СН,  , триметилен, СН=СНСН2, СН2СН=СН,
, триметилен, СН=СНСН2, СН2СН=СН,  ,
, 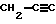 , аналогично полученные С4-(тетраметилен) и С5-бирадикалы, кроме того, Q может представлять собой следующие группы: О-СН2, O-CH2CH2, СН2-О-СН2СН2, СН2СН2-О-СН2, СН(OEt)-С=СН, СН(ОН)-СН2,
, аналогично полученные С4-(тетраметилен) и С5-бирадикалы, кроме того, Q может представлять собой следующие группы: О-СН2, O-CH2CH2, СН2-О-СН2СН2, СН2СН2-О-СН2, СН(OEt)-С=СН, СН(ОН)-СН2, 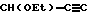 , a Y может являться фениленом (о-, м-, п-).
, a Y может являться фениленом (о-, м-, п-).
Соединения данного изобретения могут включать в себя более чем один диастереоизомер (например, Е или Z конфигурации, в случае присутствия двойной связи в группах Q или Y; R и S конфигурации, в случае присутствия разветвленной углеродной цепи). Данная заявка охватывает все эти диастереоизомеры в чистом виде или в виде их смесей. Кроме того, предшественники соединений, представленных формулой I, в которых одна из гидрокси групп или более замаскированы как группы, которые могут превращаться в гидрокси in vivo, также входят в объем настоящего изобретения.
Соединения формулы I могут быть получены в кристаллическом виде или непосредственно концентрацией из органического растворителя, или кристаллизацией или перекристаллизацией из органического растворителя или смеси упомянутого растворителя и сорастворителя, который может быть органическим или неорганическим, таким как вода. Кристаллы могут быть выделены или практически в свободном от растворителя виде, или в виде сольватов, таких как, например, гидраты. Данная заявка охватывает все кристаллические модификации и формы, а также их смеси.
Недавно было продемонстрировано, что ряд аналогов витамина D проявляют некоторую степень избирательности в отношении индуцирования клеточной дифференциации/ингибирования клеточной пролиферации in vitro по сравнению с воздействием на метаболизм кальция in vivo (что определяли по увеличению концентрации кальция в сыворотке и/или увеличению экскреции кальция с мочой), что лимитирует дозу, безопасную для введения. Один из первых таких препаратов, кальципотриол (INN) или кальципотриен (USAN), разработан на основе такой избирательности и сейчас широко известен в мире как эффективное и безопасное средство для решения такой злободневной проблемы, как лечение псориаза.
Изучение другого аналога (ЕВ 1089), выбранного на этой основе, позволило предложить концепцию, что систематическое введение аналогов витамина D может ингибировать пролиферацию раковых клеток дыхательных путей in vivo в субтоксических дозах (Colston K. W. et al, Biochem.Pharmacol. 44, 2273-2280 (1992)).
Иммуносупрессорная активность аналогов витамина D рассмотрена в обзоре (Binderup L. , Biochem.Pharmacol. 43, 1885 -1892 (1992)). Так, ряд 20-эпи-аналогов витамина D идентифицировали как потенциальные ингибиторы активации Т-лимфоцитов in vitro (Binderup L. et al., Biochem.Pharmacol. 42, 1569-1575 (1991)). Два из этих аналогов, МС 1288 и КН 1060, при систематическом введении проявляли иммуносупрессорную активность в экспериментальных животных моделях. При комбинировании с низкими дозами циклоспорина А наблюдали аддитивные или синергические эффекты. Также показано, что КН 1060, один или в комбинации с циклоспорином А, предотвращает аутоиммунную деструкцию трансплантированных островков у мышей с диабетом, не сопровождающимся ожирением (Bouillon R. et al., In: Vitamin D, Proceedings of the Ninth Workshop on Vitamin D, Orlando, Florida, Walter de Gruyter, Berlin, 1994, pp 551-552). MC 1288 обладал способностью продлевать выживание пересаженных сердечных тканей и тканей малого кишечника у крыс (Johnsson С. et al. In: Vitamin D, Proceedings of the Ninth Workshop on Vitamin D, Orlando, Florida, Walter de Gruyter, Berlin, 1994, pp 549-550). Однако во всех этих работах дозы аналогов, обладающие значительным иммуноподавляющим эффектом, вызывали увеличение уровня кальция в сыворотке. Следовательно, продолжает существовать потребность в новых аналогах, обладающих высокой эффективностью и приемлемой комбинацией пролонгированной терапевтической активности и минимального токсического эффекта.
Настоящее изобретение предоставляет ранее нераскрытые серии аналогов 20-эпихолекальциферола, которые характеризуются присутствием кето-функции в боковой цепи. Аналоги витамина D с кето-группой (карбонильная группа, связанная с двумя атомами углерода) в боковой цепи не являются новыми: например, Kureha Chemical Industries KK in Japanese Patent Application 210016/1983 раскрывает применение 23-оксо-1,25,-26-тригидроксихолекальциферола как антиопухолевого препарата. Norman, A.W. и Mayer E. из Калифорнийского Университета описали синтез 1,25-дигидрокси-24-оксо-витамина D3 и 1,23,25 -тригидрокси-24-оксо-витамина D3 (US 4,495,181, 1985). The Tejin Company раскрывает производные 24-оксо-витамина D3 как ингибиторы новообразований в Japanese Patent Application 067,423/1985. Hamma, N. et al. описывают фторированные производные витамина D3 и способ их получения (ЕР 250,755, 1988). McLane J.A. et al. раскрывают стабильные и активные метаболиты 1,25-дигидрокси-16-ен-холекальциферола (US 5,401,733, 1995). Пример 22-окса-24-кетона с активностью, способствующей клеточной дифференциации, описан в Chugai Pharmaceutical Company in Japanese Patent Application 8,559/1996. Однако надо заметить, что эти и другие ранее созданные соединения с кето группой в боковой цепи, которые были приведены в качестве примеров, характеризуются присутствием метильной группы природной конфигурации в С-20 положении витамина D. Более того, эти соединения содержат кето функцию, локализованную при втором или третьем атоме, считая от С-20 (позиция 23 или 24).
Соединения настоящего изобретения отличаются от ранее созданных соединений с кето группой в боковой цепи конфигурацией метильной группы в С-20 положении; она имеет β-проекцию, что показано общепринятым способом, используемым в формуле I. Кроме того, скелет другого С-20 заместителя (основа боковой цепи) не ограничивается ни алифатическим или шести-углеродным, ни локализацией кето группы, ограниченной вторым или третьим атомом, считая от С-20. Было обнаружено, что эти соединения обладают исключительно высокой иммуносупрессорной активностью и одновременно высокой способностью подавлять пролиферацию опухолевых клеток. Например, обнаружено, что соединение примера 4 (соединение 104) более активно, чем аналоги МС 1288 и КН 1060 (самые активные из тестированных прежде соединений), обсуждаемые в вышеупомянутом обзоре (Binderup, 1992), в ингибировании аллогенной активации Т-лимфоцитов (реакция смешанных лимфоцитов) in vitro, при том, что оно является менее кальцемичным in vivo. Далее было обнаружено, что соединение 104 как минимум в десять раз более активно в этой иммунологической тест-системе, чем его соответствующий изомер с нормальной конфигурацией при С-20 атоме (20R). Те же порядки активности наблюдали в других in vitro иммунологических тест-системах, таких как ингибирование пролиферативного ответа человеческих лимфоцитов, вызванного фитогемагглютинином (исследования проводили с помощью метода, описанного Piekoszewski, W. et al., Immunopharmacology and Immunotoxicology, 16, 389-401 (1994)). Было также обнаружено, что соединения примеров 1 и 2 (соединения 101 и 102) более чем в десять раз активнее, чем их 20-изомеры, которые были синтезированы для сравнительных целей. Кроме того, эти соединения были высоко активны в тесте дифференциации опухолевых клеток U937, о чем упоминалось в том же обзоре (Binderup, 1992), с соединениями настоящего изобретения, будучи приблизительно в десять раз активнее, чем их 20-изомеры.
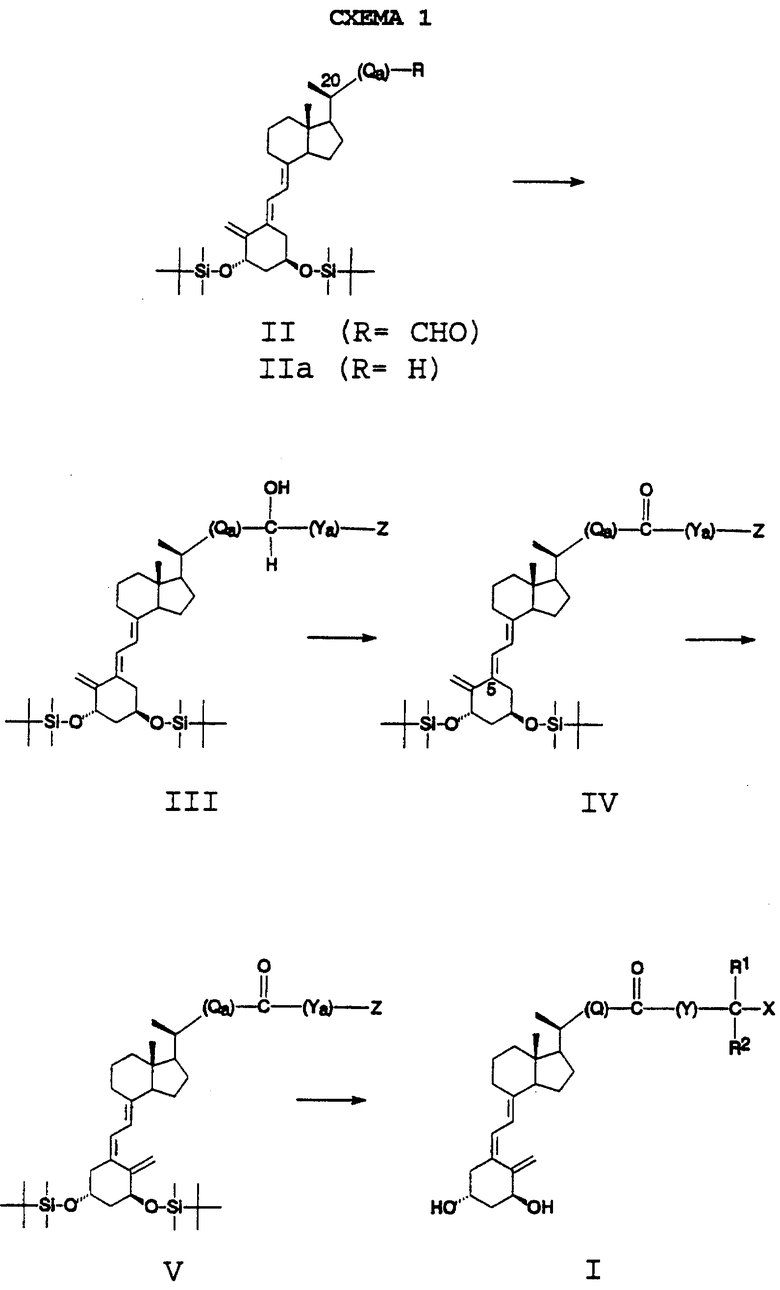
Соединение формулы I может быть получено с помощью общей процедуры, описанной в схеме 1. В этой схеме исходным веществом является альдегид II, ключевой строительный блок витамина D, в котором атом углерода альдегидной группы расположен так, чтобы превратиться в атом углерода кето группы боковой цепи целевого соединения I. Альдегид II представляет собой либо простое соединение, в котором Qa является одинарной связью, либо известным производным, либо новым производным, приготовленным с помощью стандартной последовательности реакций. Далее, символ Qa в соединении II обозначает связующую группу, которая может быть идентична Q в соединении I или альтернативно представлять собой группу, которая может быть превращена в Q в процессе одной из последовательных стадий синтеза. Более того, структура Qa может изменяться от одного промежуточного соединения к другому во время протекания реакции. Однако допустимость изменений станет ясной в результате детального описания.
Далее изложена схема синтеза:
1. соединение II взаимодействует с металлоорганическим реагентом, имеющим формулу Z-(Ya)-M (где радикал металла М необязательно представляет собой Li или Mg-Hal; Наl= Сl, Вr или I), полученным из боковой цепи строительного блока, имеющего формулу Z-(Ya)-H или Z-(Ya)-Hal, для того, чтобы установить углеродный скелет боковой цепи в промежуточном соединении III. Конфигурация спиртовой группы боковой цепи может быть R, S или смешанной и не имеет отношения к синтезу. Символ Ya используют для указания необязательности идентичности этой группы и группы, обозначаемой Y, и возможности ее превращения в Y (см. выше аналогичное применение символа Qa), а символ Z отражает аналогичные взаимоотношения с группой C(R1)(R2) (X). При получении промежуточного соединения III радикал металла (-М) замещает альдегидную группу (-СНО) в исходном веществе II, который взаимодействует со строительным блоком боковой цепи с альдегидной группой, имеющим формулу Z-(Ya)-CHO. Предшественник IIа металлизированного производного II (R=M) получают путем стандартной последовательности реакций из альдегида типа II.
Остальные стадии синтеза включают:
2. окисление спирта до кетона;
3. необязательное превращение группы Qa в Q;
4. необязательное превращение группы Ya в Y;
5. необязательное превращение группы Z в C(R1) (R2)(X);
6. триплет-чувствительная изомеризация триеновой структуры витамина D (5E в 5Z) и
7. удаление силильных защитных групп ядра витамина D.
Последовательность стадий от 1 до 7 может уменьшаться (т.к. стадия фотоизомеризации может предшествовать реакции (стадия 1) со строительным блоком боковой цепи), и некоторые стадии могут быть объединены (т.к. условия десилилирования (стадия 7) могут способствовать удалению защиты со спиртовой группы Х (стадия 5)). Примеры условий и реагентов для обозначенных реакций (т. е. для стадий 2, 6 и 7) хорошо известны в результате ранее проведенных синтезов аналогов витамина D. Альтернативные пути для любого из промежуточных соединений от II до V или соединения I доступны и очевидны специалистам в этой области.
Настоящие соединения можно использовать в фармацевтических композициях, которые применяют при лечении заболеваний человека и в ветеринарии, как описано выше.
Необходимое количество соединения формулы I (далее обозначаемых как активный ингредиент) для терапевтического эффекта варьирует в зависимости от особенностей соединения, способа введения и вида млекопитающего, подвергающегося лечению. Соединения данного изобретения можно вводить парентерально, внутрисуставно, внутрикишечно и местно. Они хорошо абсорбируются при внутрикишечном введении, и этот способ является предпочтительным при лечении системных заболеваний. При лечении кожных заболеваний, таких как псориазы, или глазных заболеваний предпочитают местный или внутрикишечный способ введения.
При лечении дыхательных заболеваний, таких как астма, предпочитают аэрозоли.
Хотя возможно вводить активный ингредиент один, как индивидуальное вещество, предпочтительно применять его в виде фармацевтических композиций. Желательно, чтобы активный ингредиент составлял от 0,1 части на млн до 0,1% по массе от состава композиции.
Под термином дозировочная единица понимают единичную, т.е. одинарную, дозу, которая обладает активностью при введении пациенту и которая может быть легко упакована, оставаясь физически и химически стабильной, единичная доза включает в себя или активный ингредиент как таковой, или смесь его с твердым или жидким фармацевтическим растворителем или носителем.
Композиции настоящего изобретения, предназначенные для применения как в ветеринарии, так и в медицине человека, включают в себя активный ингредиент в сочетании с фармацевтически приемлемым носителем и, в необязательном порядке, с другими терапевтическими ингредиентами. Носитель должен быть приемлемым, что подразумевает совместимость с другими ингредиентами композиции и отсутствие с его стороны вредного влияния на реципиента.
То есть композиции включают вещества в форме, удобной для орального, ректального, парентерального (в том числе подкожного, внутримышечного и внутривенного), внутрисуставного и местного введения.
Композиции могут быть представлены в форме дозировочных единиц, приготовленных любым способом, применяемым в фармацевтике. Все методы включают объединение активного ингредиента с носителем, состоящим из одного или более вспомогательных ингредиентов. Обычно композиции готовят путем равномерного и однородного смешивания активного ингредиента с жидким носителем, или тонко размельченным твердым, или с обоими, и затем, по необходимости, придают продукту нужную форму.
Композиции настоящего изобретения, предназначенные для орального введения, могут быть представлены в форме капсул, присыпок (sachets), таблеток или пастилок, содержащих определенное заранее количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; в виде эмульсий масло-в-воде или вода-в-масле. Активный ингредиент можно также вводить в виде шариков, лекарственной кашки или пасты.
Таблетки могут быть приготовлены прессованием или формованием активного ингредиента, возможно, в совокупности с одним или более дополнительными ингредиентами. Прессованные таблетки могут быть приготовлены в соответствующем аппарате прессованием активного ингредиента в свободно-текучей форме, такой как порошок или гранулы, необязательно смешанного с носителем, смазочным веществом, инертным растворителем, поверхностно-активным или диспергирующим агентом. Формованные таблетки могут быть приготовлены в соответствующем аппарате формованием смеси порошкообразного активного ингредиента и подходящего носителя, увлажненных инертным жидким разбавителем.
Композиции для ректального введения можно применять в виде свечей, включающих активный ингредиент и носитель, такой как кокосовое масло, или в виде клизмы.
Композиции для парентерального введения включают в себя стерильные масляные или водные препараты активного ингредиента, которые преимущественно представляют собой изотонические растворы по отношению к крови реципиента.
Композиции для внутрисуставного введения можно применять в виде стерильных водных препаратов активного ингредиента, который может находиться в микрокристаллической форме, например виде водной микрокристаллической суспензии. Для внутрисуставного и глазного применения могут также использоваться липосомные композиции, или биодеградируемые полимерныe системы.
Композиции для местного применения, в том числе для лечения глаз, включают жидкие или полужидкие препараты, такие как линименты, лосьоны, гели, накладки, масло-в-воде и вода-в-масле эмульсии, например кремы, мази или пасты, а также растворы или суспензии в виде капель.
Лечение астмы можно проводить посредством вдыхания порошка, самовведения или спрея композиций, приготовленных с помощью спрэй-баллона, распылителя или пульверизатора. При диспергировании размер частиц композиции преимущественно находится в интервале от 10 до 100 мкм.
Такие композиции наиболее предпочтительны в виде тонкоизмельченного порошка для легочного введения с помощью приспособления для вдыхания порошка или самовведения порошкообразных композиций. В случае самовведения композиций в виде растворов и спрэя можно достигнуть эффекта или с помощью выбора клапана, имеющего нужные характеристики (т. е. способного продуцировать спрэй, имеющий требуемый размер частиц), или посредством введения активного ингредиента в виде суспендированного порошка с контролируемым размером частиц. Такие композиции для самовведения могут представлять собой порошкообразные композиции или композиции с активным ингредиентом в виде капель раствора или суспензии.
Порошкообразные композиции для самовведения преимущественно содержат диспергированные частицы твердого активного ингредиента и жидкий носитель, имеющий точку кипения ниже 18oС при атмосферном давлении. Обычно носитель составляет от 45 до 99,9 мас.% от состава композиции, в то время как активный ингредиент составляет от 0,1 ч./млн до 0,1 мас.% от состава композиции.
В дополнение к вышеупомянутым ингредиентам композиции данного изобретения могут включать один или более дополнительных ингредиентов, таких как растворители, буфера, ароматизирующие агенты, связующие вещества, поверхностно-активные агенты, сгустители, смазочные вещества, предохраняющие средства, например метилгидроксибензоат (включая антиоксиданты), эмульгирующие агенты и другие. Кроме того, композиции могут содержать другие терапевтически активные соединения, обычно используемые в лечении упомянутых выше патологических состояний.
Настоящее изобретение касается также способа лечения пациентов, страдающих от одного из вышеперечисленных патологических состояний, упомянутый метод состоит во введении пациенту одного или более соединений формулы I в количествах, необходимых для эффективного лечения, которые можно комбинировать с одним или более соединениями, обладающими другой терапевтической активностью, обычно применяемыми в лечении упомянутых физиологических состояний. Лечение с помощью настоящих соединений и/или соединений с другой терапевтической активностью может быть непрерывным или с интервалами.
При лечении системных заболеваний дневные дозы вводимого соединения формулы I составляют от 0,1 до 100 мкг, предпочтительно от 0,2 до 25 мкг. При местном лечении кожных заболеваний применяют соединения формулы I в виде мазей, кремов или лосьонов, содержащих от 0,1 до 500 мкг/г, предпочтительно от 0,1 до 100 мкг/г активного ингредиента. Для местного применения в офтальмологии используют соединения формулы I в виде мазей, капель или гелей, содержащих от 0,1 до 500 мкг/г, предпочтительно от 0,1 до 100 мкг/г активного ингредиента. Композиции для орального введения, преимущественно в виде таблеток, капель или капсул, содержат от 0,05 до 50 мкг, предпочтительно от 0,1 до 25 мкг, соединения формулы I на дозировочную единицу.
Далее изобретение иллюстрируют с помощью нижеследующих нелимитирующих его способов получения и примеров:
Способы получения и примеры
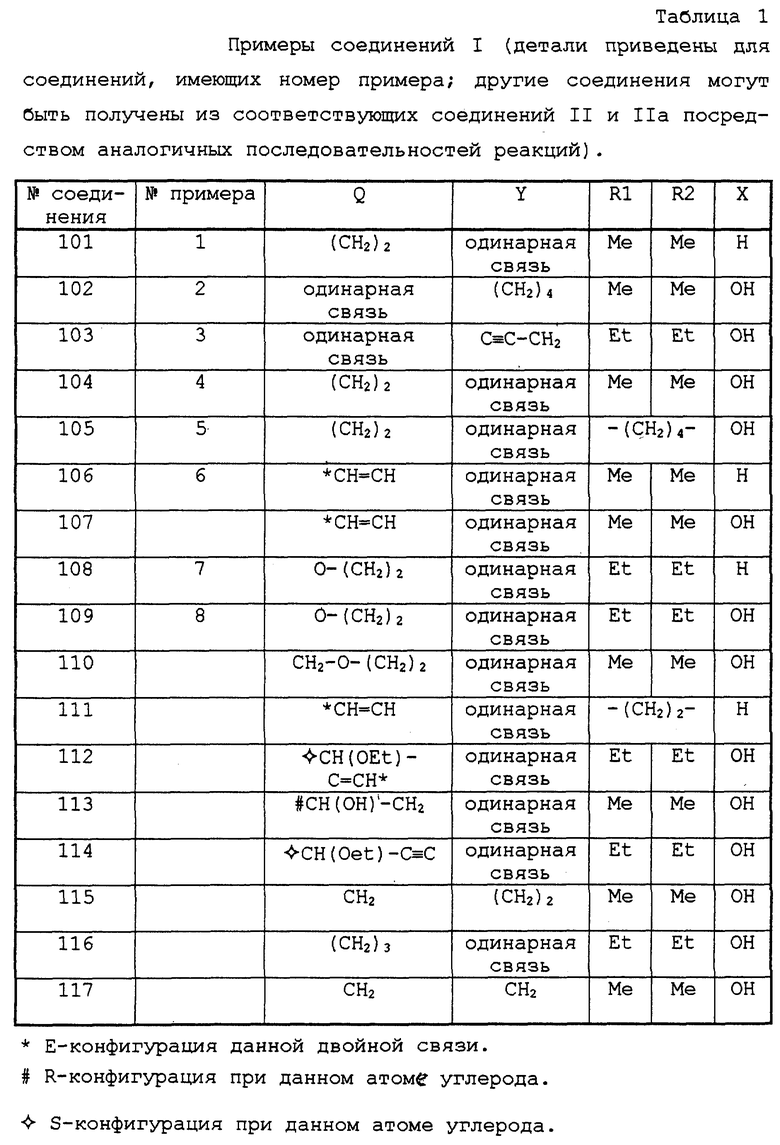
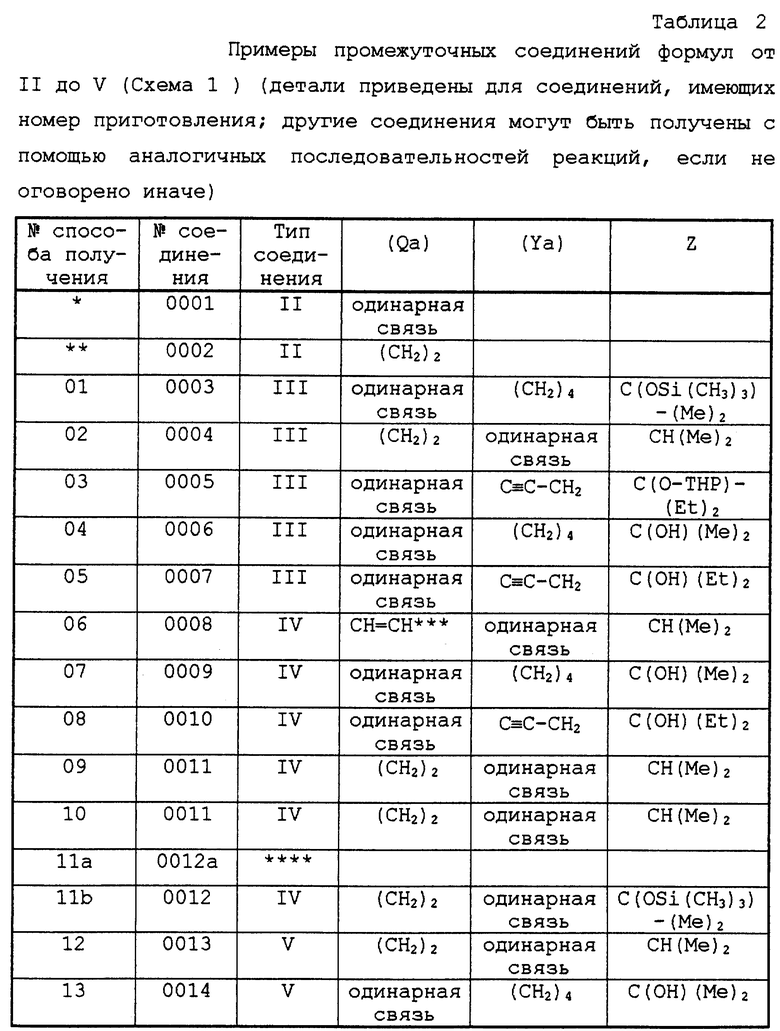
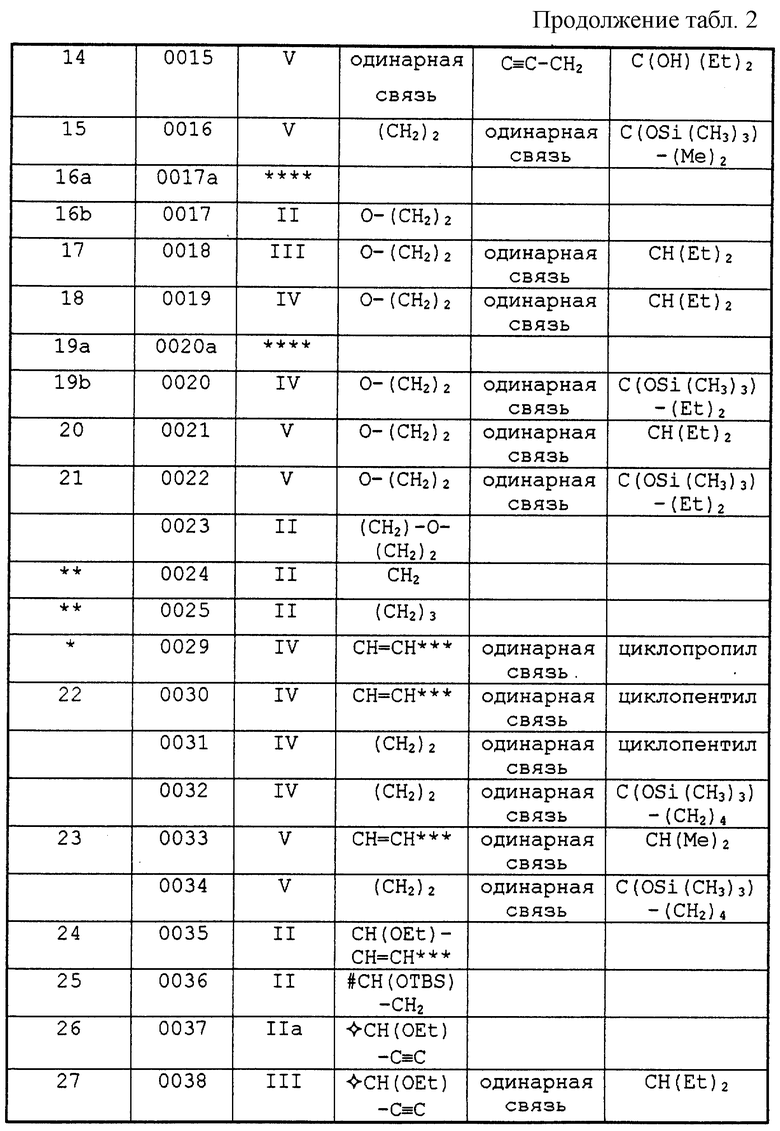
Примеры соединений I перечислены в табл.1, а исходные вещества и промежуточные соединения общих формул II, III, IV и V перечислены в табл.2.
Использовали следующие аббревиатуры стандартов: Me = метил; TBS = т-бутилдиметилсилил; ТНР = тетрагидро-4Н-пиран-2-ил; ТГФ = тетрагидрофуран.
Общее:
Под эфиром подразумевается диэтиловый эфир. Тетрагидрофуран (ТГФ) высушивали над натрием/бензофеноном. Реакции обычно проводили в атмосфере азота, если не оговорено иначе. В стандартной рабочей процедуре отделяли органический слой, промывали его насыщенным раствором хлорида натрия, высушивали над безводным сульфатом магния, концентрировали в вакууме и в результате получали продукт.
В спектрах 1H ядерного магнитного резонанса значения химических сдвигов (δ) (в м. д. ) приводятся, если не оговорено иначе, для растворов в дейтерохлороформе относительно внутреннего стандарта тетраметилсилана (δ=0,00) или хлороформа (δ=7,25). Значения для мультиплетов, как определенных (дублет (д), триплет (т), квартет (к)), так и для неопределенных (м), даны приблизительно в средней точке, если не указан интервал (с=синглет, шир=широкий).
Общая процедура 1 (способы получения 01, 02, 17)
К раствору реагента Гриньяра, приготовленного из магния (3,3 ммоля) и строительного блока боковой цепи (3 ммоля), в высушенном ТГФ (3 мл) при температуре около 5oС добавляют с помощью шприца раствор альдегида (1 ммоль) в высушенном ТГФ (5 мл). После перемешивания при той же температуре в течение 30 мин реакционную смесь распределяют между эфиром и насыщенным раствором хлорида аммония. Стандартная процедура приводит к получению маслянистого продукта.
Способ получения 01: соединение 0003
(Этот способ получения представляет собой модификацию без разделения изомеров синтеза, описанного в Calverley М. J. and Binderup, E.T. Novel vitamin D analogues. International Patent Application WO 9,100,271-A: (1991), способ получения 32:) Строительный блок боковой цепи: 6-бром-2-метил-2-(триметилсилилокси)гексан (0,80 г); альдегид: соединение 0001 (0,55 г, 0,96 ммоль); без дальнейшей очистки продукт, содержащий соединение, указанное в заголовке, использовали в следующей стадии.
Способ получения 02: соединение 0004
Строительный блок боковой цепи: 2-бромпропан (0,37 г); альдегид: соединение 0002 (0,60 г), продукт очищают на силикагеле (50 г) (элюент: 15% эфир в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.54 (3Н, с), 0.75-1.0 (9Н, м), 0.85 (9Н, с), 0.9- (9Н, с), 1.05-2.1 (20Н, м), 2.3 (1Н, шир.д), 2.55 (1H, дд), 2.87- (1H, шир. д), 3.31 (1H, м), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.81 (1H, д), 6.45 (1H, д).
Способ получения 03: соединение 0005
(Этот способ получения представляет собой модификацию без разделения изомеров синтеза, описанного в Bretting, C.A.S. and Grue-Serensen, G., International Patent Application WO 9,319,044-Al (1993), способ получения 13:). К раствору литиевого производного, приготовленного из н-бутирата лития и строительного блока боковой цепи, 4-этил-(4-тетра-гидропиранилокси)-гекс-1-ил (0,65 г, 3,1 ммоля) в высушенном ТГФ (5 мл) при температуре около -70oС, добавляют с помощью шприца раствор соединения 0001 (0,575 г, 1 ммоль) в высушенном ТГФ (2 мл). После перемешивания при той же температуре в течение 10 мин и затем при 0oС в течение 45 мин реакционную смесь распределяют между эфиром и водой. Стандартная процедура приводит к получению маслянистого продукта. Очищают методом хроматографии на силикагеле (50 г) (элюент: 30% эфир в петролейном эфире), получая соединение, указанное в заголовке, в виде масла.
Общая процедура 2 (способы получения 04, 05)
К раствору триметилсилилового эфира (0,96 ммолей) или ТНР эфира (0,22 ммоля) в ТГФ (2 мл) при температуре около 25oС добавляют пиридиний п-толуолсульфонат (0,010 г, 0,04 ммолей в случае использования триметилсилилового эфира, и 0,150 г, 0,6 ммолей в случае использования ТНР эфира) в этаноле (10 мл). После перемешивания при той же температуре в течение 15 мин (триметилсилиловый эфир), или 2 часов (ТНР эфир), реакционную смесь распределяют между этилацетатом и 5% раствором бикарбоната натрия. Стандартная процедура приводит к получению маслянистого продукта.
Способ получения 04: соединение 0006
Триметилсилиловый эфир: соединение 0003, неочищенный продукт соединения 0001 (0,96 ммолей); продукт очищают методом хроматографии на силикагеле (50 г) (элюент: 40% этилацетат в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.06 (12Н, м), 0.54 (3Н, с), 0.83 (3Н, д), 0.86 (9Н, с), 0.89 (9Н, с), 1.01-2.15 (24Н, м), 1.2 (6Н, с), 2.31 (1H, шир.д), 2.55 (1H, дд), 2.88 (1H, шир. д), 3.85 (1H, м), 4.21 (1H, M), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.83 (1H, д), 6.45 (1H, д).
Способ получения 05: соединение 0007
ТНР эфир: соединение 0005 (0,170 г, 0,217 ммолей); в следующей стадии используют продукт, содержащий соединение, указанное в заголовке.
δ = 0.05 (12Н, м), 0.55 (3Н, с), 0.85 (9Н, с), 0.88 (6Н, т), 0.89 (9Н, с), 1.03 (3Н, д), 1.15-2.1 (20Н, м), 2.31 (1H, шир.д), 2.37 (2Н, м), 2.54 (1H, дд), 2.87 (1H, м), 4.21 (1H, м), 4.52 (1H, м), 4.61 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.82 (1H, д), 6.44 (1H, д).
Способ получения 06: соединение 0008
К раствору соединения 0001 (0,481 г, 0,84 ммоля) в высушенном толуоле (3 мл) при температуре около 25oС добавляют строительный блок боковой цепи 2-пропилкарбонилметилентрифенилфосфоран (0,60 г, 1,72 ммоля). После перемешивания при той же температуре в течение 10 мин и затем при 110oС в течение 5 ч, реакционную смесь частично концентрируют в вакууме и разбавляют эфиром. Раствор оставляют кристаллизоваться и фильтруют. Фильтрат концентрируют под вакуумом, получая в результате масло. Очищают методом хроматографии на силикагеле (50 г) (элюент: 10% эфир в петролейном эфире), получая соединение, указанное в заголовке. Игольчатые кристаллы (needles) (из метанола), т. пл. 123-124oС;
δ = 0.05 (12Н, м), 0.5 (3Н, с), 0.85 (9Н, с), 0.89 (9Н, с), 1 (3Н, д), 1-1.82 (10Н, м), 1.09 (6Н, д), 1,95 (3Н, м), 2.25 (1Н, м), 2.3 (1H, шир.д), 2.54 (1H, дд), 2.81 (1H, м), 2.84 (1H, шир.д), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.97 (1Н, м), 5.81 (1H, д), 6.1 (1H, д), 6.43 (1H, д), 6.77 (1Н, дд).
Способ получения 07: соединение 0009
К раствору соединения 0006 (0,69 г, 0,1 ммоля) в высушенном дихлорметане (2 мл) при температуре около 25oС добавляют твердый хлорхромат пиридиния (0,04 г, 0,19 ммоля). После перемешивания при той же температуре в течение 1 часа реакционную смесь экстрагируют эфиром. Органический слой отделяют, фильтруют и концентрируют под вакуумом, получая в результате масло. Очищают методом хроматографии на силикагеле (15 г) (элюент: 20% этилацетат в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.06 (12Н, м), 0.51 (3Н, с), 0.85 (9Н, с), 0.88 (9Н, с), 1.02 (3Н, д), 1.1-2.1 (20Н, м), 1.2 (6Н, s), 2.31 (1H, шир.д), 2.5 (4Н, м), 2.85 (1H, м), 4.21 (1H, м), 4.51 (1H, м), 4.93 (1H, м), 4.97 (1H, м), 5.81 (1H, д), 6.43 (1H, д).
Общая процедура 3 (способы получения 08, 09, 18)
К раствору спирта (от 0,2 до 0,5 ммолей) в высушенном дихлорметане (10 мл) при температуре около 25oС добавляют порциями 1,1,1-триацетокси-1,1-дигидро-1,2-бензиодоксол-3-(1Н)-он (1,2 мол. эквивалентов). После перемешивания при той же температуре в течение 15 мин реакционную смесь распределяют между эфиром и 5% водным раствором бикарбоната натрия, содержащим также избыток тиосульфата натрия. В результате стандартной процедуры получают продукт в виде масла.
Способ получения 08: соединение 0010
Спирт: соединение 0007, неочищенный продукт из соединения 0005 (0,217 ммолей); очищают методом хроматографии на силикагеле (30 г) (элюент: 40% эфир в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.54 (3Н, с), 0.85 (9Н, с), 0.88 (9Н, с), 0.92 (6Н, т), 1.1-2.1 (14Н, м), 1.14 (3Н, д), 2.3 (1H, шир.д), 2.52 (2Н, м), 2.56 (2Н, с), 2.86 (1H, м), 4.21 (1H, м), 4.51 (1H, м), 4.93 (1H, м), 4.97 (1H, м), 5.81 (1H, д), 6.43 (1H, д).
Способ получения 09: соединение 0011
Спирт: соединение 0004 (0,322 г, 0,5 ммолей), продукт очищают хроматографией на силикагеле (30 г) (элюент: 5% эфир в петролейном эфире), получая соединение, указанное в заголовке. Игольчатые кристаллы (из метанола); т. пл. 95-96oС;
δ = 0.05 (12Н, м), 0.55 (3Н, с), 0.83 (3Н, д), 0.85 (9Н, с), 0.89 (9Н, с), 1.08 (6Н, д), 1.2-2.1 (16Н, м), 2.25-2.7 (5Н, м), 2.86 (1H, шир.д), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.81 (1H, д), 6.45 (1H, д).
Способ получения 10; соединение 0011 (альтернативный синтез)
К раствору соединения 0008 (1,15 г, 1,79 ммоля) в толуоле (50 мл) при температуре около 25oС добавляют водный раствор дитионита натрия (5,45 г, 31 ммоль), содержащего бикарбонат натрия (5,5 г) и хлорид метилтридециламмония (0,55 г). После интенсивного перемешивания при той же температуре в течение 5 мин и затем 3 часа при 80oС, реакционную смесь распределяют между эфиром и водой. В результате стандартной рабочей процедуры получают продукт в виде масла, продукт очищают хроматографией на силикагеле (30 г) (элюент: 30% эфир в петролейном эфире), получая соединение, указанное в заголовке. Игольчатые кристаллы (из метанола); т.пл. 95-96oС;
δ = 0.05 (12Н, м), 0.55 (3Н, с), 0.83 (3Н, д), 0.85 (9Н, с), 0.89 (9Н, с), 1.08 (6Н, д), 1.2-2.1 (16Н, м), 2.25-2.7 (5Н, м), 2.86 (1H, шир.д), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.81 (1H, д), 6.45 (1H, д).
Общая процедура 4 (способы получения На, 19а)
К раствору кетона (са. 0,5 ммолей) в высушенном дихлорметане (3 мл) при температуре около 5oС добавляют гексаметилдисилазан( 2 мол. эквивалентов) и затем иодтриметилсилан (0,6 мол. эквивалентов). После перемешивания при той же температуре в течение 1 часа и затем при -20oС в течение ночи реакционную смесь распределяют между эфиром и 5% водным раствором бикарбоната натрия. В результате стандартной процедуры получают продукт в виде масла.
Способ получения 11а: 24-триметилсилилокси-1(S), 3(R) -бис-(ТВS-окси)-20(S)-9,10-втор-холеста-5(Е),7(Е),10 (19),24-тетраен (соединение 0012а)
Кетон: соединение 0011 (0,395 г, 0,61 ммолей); продукт очищают хроматографией на силикагеле (30 г) (элюент: 1% эфир в петролейном эфире), получая соединение, указанное в заголовке. Игольчатые кристаллы (из метанола): т. пл. 69-71oС;
δ = 0.05 (12Н, м), 0.15 (9Н, с), 0.53 (3Н, с). 0.86 (3Н, д), 0.86 (9Н, с), 0.89 (9Н, с), 1-2.08 (17Н, м), 1.56 (3Н, с), 1.59 (3Н, с), 2.16 (1H, м), 2.3 (1H, шир. д), 2.55 (1H, дд), 2.86 (1H, шир.д), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.81 (1H, д), 6.45 (1H, д).
Общая процедура 5 (способы получения llb, 19b)
К раствору енолового эфира (са. 0,2 ммолей) в высушенном дихлорметане (5 мл) при температуре около 5oC добавляют твердую м-хлорпербензоевую кислоту (85%) (1,1 мол. эквивалентов). После перемешивания при той же температуре в течение 15 мин реакционную смесь распределяют между эфиром и 5% раствором бикарбоната натрия. В результате стандартной процедуры получают продукт в виде масла.
Способ получения llb; соединение 0012
Енольный эфир; соединение 0012а (0,152 г, 0,21 ммолей); продукт очищают хроматографией на силикагеле (15 г) (элюент: 5% эфир в петролейном эфире), получая соединение, указанное в заголовке. Игольчатые кристаллы (из метанола); т.пл. 82-84oС;
δ = 0.05 (12Н, м), 0.15 (9Н, с), 0.55 (3Н, с), 0.84 (3Н, д), 0.85 (9Н, с), 0.89 (9Н, с), 1.15-2.08 (16Н, м), 1.32 (6Н, с), 2.3 (1H, шир.д), 2.56 (1H, дд), 2.62 (2Н, м), 2.86 (1H, м), 4.21 (1H, м), 4.52 (1H, м), 4.93 (1H, м), 4.98 (1H, м), 5.81 (1H, д), 6.45 (1H, д).
Общая процедура 6 (способы получения от 12 до 15, 20, 21, 23)
Раствор 5Е - витаминa D (са 0,1 ммоль), антрацена (в способах получения 20 и 21 - 9-ацетилантрацена) (0,03 г) и триэтиламина (0,1 мл) в толуоле или дихлорметане (5 мл) в колбе Пирекса облучали светом ультрафиолетовой лампы высокого давления, тип TQ718Z2 (Hanau) при 10oС в течение 30 мин. Реакционную смесь частично концентрировали под вакуумом, получая в результате продукт в виде масла.
Способ получения 12: соединение 0013
5Е-витамин D: соединение 0011 (0,067 г, 0,104 ммоля); продукт очищают хроматографией на силикагеле (15 г) (элюент: 5% эфир в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.53 (3Н, с), 0.82 (3Н, д), 0.87 (18Н, с), 1.05-2.05 (16Н, м), 1.08 (6Н, д), 2.2 (1Н, дд), 2.3-2.67 (4Н, м), 2.81 (1H, м), 4.18 (1H, м), 4.36 (1H, м), 4.85 (1H, м), 5.17 (1H, м), 6.00 (1H, д), 6.22 (1H, д).
Способ получения 13; соединение 0014
5Е-витамин D: соединение 0009 (0,080 г, 0,116 ммолей) (в дихлорметане); продукт очищают хроматографией на силикагеле (15 г) (элюент: 30% этилацетат в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.49 (3Н, с), 0.87 (9Н, с), 0.87 (9Н, с), 1 (3Н, д), 1.19 (3Н, с), 1.19 (3Н, с), 2.2 (1H, дд), 2.3-2.7 (4Н, м), 2.81 (1H, м), 4.18 (1H, м), 4.36 (1H, м), 4.85 (1H, м), 5.17 (1H, м), 6 (1H, д), 6.22 (1H, д).
Способ получения 14: соединение 0015
5Е-витамин D; соединение 0010 (0,076 г, 0,109 ммолей) (в дихлорметане); продукт очищают хроматографией на силикагеле (15 г) (элюент: 50% эфир в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.53 (3Н, с), 0.87 (18Н, с), 0.92 (6Н, т), 1.14 (3Н, д), 2.2 (1H, дд), 2.4 (1H, дд), 2.53 (1H, м), 2.57 (2Н, с), 2.81 (1H, м), 4.18 (1H, м), 4.36 (1H, м), 4.85 (1H, м), 5.17 (1H, м), 6 (1H, д), 6.22 (1H, д).
Способ получения 15; соединение 0016
5Е-витамин D; соединение 0012 (0,062 г, 0,085 ммоля) (в толуоле); продукт очищают хроматографией на силикагеле (15 г) (элюент: 2% эфир в петролейном эфире), получая соединение, указанное в заголовке. Масло;
δ = 0.05 (12Н, м), 0.15 (9Н, с), 0.53 (3Н, с), 0.84 (3Н, д), 0.87 (18Н, c), 1.32 (3Н, с), 1.32 (3Н, с), 2.2 (1H, дд), 2.4 (1H, м), 2.62 (2Н, м), 2.81 (1H, м), 4.18 (1H, м), 4.36 (1H, м), 4.85 (1H, м), 5.17 (1H, м), 6 (1H, д), 6.22 (1H, д).
Способ получения 16а; (2-цианоэтокси-1(S),3(R)-бис-(TBS -окси)-9,10-20(R)-втор-прегна-5(Е), 7(Е),10(19),24-триен (соединение 0017а)
К раствору 20(R)-гидрокси-1(3), 3(R)-бис-(ТВS-окси)-9,-10-20(R)-втор-прегна-5(Е), 7(Е), 10(19), 24-триена (1,3 г, 2,32 ммоля) в дихлорметане (40 мл) при 25oС добавляют 40% водный раствор гидроксида тетрабутиламмония (20 мл, 15 ммолей) и затем акрилонитрил (4,84 г, 91 ммоль). После интенсивного перемешивания при той же температуре в течение ночи реакционную смесь распределяют между эфиром и водой. В результате стандартной рабочей процедуры получают продукт в виде масла. Продукт очищают хроматографией на силикагеле (80 г) (элюент 20% эфир в петролейном эфире), получая соединение, указанное в заголовке;
δ = 0.05 (м, 12Н), 0.56 (с, 3Н), 0.86 (с, 9Н), 0.88 (с, 9Н), 1.10 (д, 3Н), 1.10-2.20 (м, 13Н), 2.30 (шир.д, 1H), 2.55 (дд, 1H), 2.56 (т, 2Н), 2.87 (шир. д, 1H), 3.34 (м, 1H), 3.44 (м, 1H), 3.75 (м, 1H), 4.20 (м, 1H), 4.52 (дд, 1H), 4.92 (шир.т, 1H), 4.98 (шир.с, 1H), 5.79 (д, 1H), 6.45 (д, 1H).
Способ получения 16b: соединение 0017
К раствору соединения 0017а (0,9 г, 1,46 ммолей) в высушенном эфире (45 мл) при -70oС добавляют с помощью шприца диизобутилалюминий гидрид (1М в гексане; 2 ммоля). После перемешивания при той же температуре в течение 1 часа, реакционную смесь распределяют между эфиром и насыщенным раствором хлорида аммония. Полученный в результате стандартной рабочей процедуры продукт очищают хроматографией на силикагеле (50 г) (элюент: 30% эфир в петролейном эфире), получая соединение, указанное в заголовке, в виде масла;
δ = 0.05 (м, 12Н), 0.53 (с, 3Н), 0.86 (с, 9Н), 0.88 (с, 9Н), 1.09 (д, 3Н), 1.05-2.10 (м, 13Н), 2.30 (шир.д, 1H), 2.54 (дд, 1H), 2.62 (дт, 2Н), 2.86 (шир. д, 1H), 3.30 (м, 1H), 3.55 (м, 1H), 3.88 (м, 1H), 4.20 (м, 1H), 4.52 (дд, 1H), 4.93 (шир. т, 1H), 4.98 (шир.т, 1H), 5.79 (д, 1H), 6.44 (д, 1H), 9.78 (т, 1H).
Способ получения 17: соединение 0018(общая процедура 1)
Строительный блок боковой цепи: 3-бромпентан (0,45 г);
альдегид: соединение 0017 (0,49 г, 0,8 ммолей), продукт очищают хроматографией на силикагеле (50 г) (элюент: 20% эфир в петролейном эфире), получая соединение, указанное в заголовке, в виде разделенных изомеров, которые объединяют для использования в следующей стадии. Изомер, элюирующийся первым: масло;
δ = 0.05 (м, 12Н), 0.54 (с, 3Н), 1.85 (м, 6Н), 0.86 (с, 9Н), 0.88 (с, 9Н), 1.11 (д, 3Н), 1.10-2.15 (м, 20Н), 2.30 (шир.д, 1H), 2.54 (дд, 1Н), 2.86 (шир. д, 1Н), 3.18 (шир.с, 1H), 3.26 (м, 1Н), 3.49 (м, 1Н), 3.75 (м, 2Н), 4.21 (м, 1Н), 4.52 (дд, 1Н), 4.93 (шир.т, 1H), 4.98 (шир.с, 1Н), 5.79 (д, 1Н), 6.45 (д, 1Н);
Изомер, элюирующийся вторым: масло;
δ = 0.05 (м, 12Н), 0.55 (с, 3Н), 0.87 (м, 6Н), 0.86 (с, 9Н), 0.88 (с, 9Н), 1.09 (д, 3Н), 1.10-2.15 (м, 21Н), 2.30 (шир.д, 1H),
2.54 (дд, 1H), 2.86 (шир.д, 1H), 3.29 (м, 1H), 3.44 (м, 1H), 3.72 (м, 2Н), 4.21 (м, 1H), 4.52 (дд, 1H), 4.93 (шир.с, 1H), 4.98 (шир.с, 1H), 5.79 (д, 1Н), 6.45 (д, 1H).
Способ получения 18: соединение 0019(общая процедура 3)
Спирт: соединение 0018 (0,22 г, 0,32 ммолей), продукт очищают хроматографией на силикагеле (30 г) (элюент: 10% эфир в петролейном эфире), получая соединение, указанное в заголовке;
δ = 0.05 (м, 12Н), 0.54 (с, 3Н), 0.83 (т, 3Н), 0.84 (т, 3Н), 0.86 (с, 9Н), 0.89 (с, 9Н), 1.07 (д, 3Н), 1.05-1.80 (м, 16Н), 1.85-2.07 (м, 3Н), 2.25-2.35 (м, 2Н), 2.55 (м, 1H), 2.86 (шир.д, 1H), 3.29 (м, 1H), 3.46 (м, 1H), 3.79 (м, 1H), 4.21 (м, 1H), 4.51 (дд, 1H), 4.93 (м, 1H), 4.97 (м, 1H), 5.79 (д, 1H), 6.45 (д, 1H).
Способ получения 19а; (3-триметилсилилокси-4-этил-гекс-3-енил-окси) -1(S), 3 (R) -бис- (TBS-окси) -20 (R) -9,10-втор-прег-на-5(Е),7(Е),-10(19)-триен (соединение 0020а) (общая процедура 4)
Кетон: соединение 0019 (0,178 г, 0,25 ммолей); продукт очищают хроматографией на силикагеле (30 г) (элюент: 1% эфир в петролейном эфире), получая соединение, указанное в заголовке;
δ = 0.06 (м, 12Н), 0.55 (с, 3Н), 0.86 (с, 9Н), 0.90 (с, 9Н), 0.92 (т, 3Н), 0.93 (т, 3Н), 1.08 (д, 3Н), 1.16 (с, 9Н), 1.00-2.25 (м, 17Н), 2.31 (шир. д, 1H), 2.37 (м, 2Н), 2.55 (дд, 1H), 2.86 (шир.д, 1H), 3.31 (м, 2Н), 3.63 (м, 1H), 4.21 (м, 1H), 4.53 (м, 1H), 4.93 (м, 1H), 4.98 (м, 1H), 5.79 (д, 1H), 6.46 (д, 1H).
Способ получения 19b: соединение 0020 (общая процедура 5)
Еноловый эфир: соединение 0012а (0,1 г, 0,13 ммолей), продукт очищают хроматографией на силикагеле (15 г) (элюент: 5% эфир в петролейном эфире), получая соединение, указанное в заголовке;
δ = 0.06 (м, 12Н), 0.17 (с, 9Н), 0.55 (с, 3Н), 0.77 (т, 3Н), 0.78 (т, 3Н), 0.86 (с, 9Н), 0.89 (с, 9Н), 1.08 (д, 3Н), 1.00-2.15 (м, 17Н), 2.29 (шир. д, 1H), 2.55 (дд, 1H), 2.70-2.92 (м, 3Н), 3.30 (м, 1H), 4.45 (м, 1H), 3.78 (м, 1H), 4.21 (м, 1H), 4.53 (м, 1H), 4.93 (м, 1H), 4.98 (м, 1H), 5.79 (д, 1H), 6.45 (д, 1H).
Способ получения 20: соединение 0021 (общая процедура 6)
5Е-витамин D: соединение 0019 (0,06 г, 0,87 ммолей) (в толуоле); без дальнейшей очистки продукт, содержащий соединение, указанное в заголовке, используют на следующей стадии. δ соответствует структуре вещества.
Способ получения 21: соединение 0022 (общая процедура 6)
5Е-витамин D: соединение 0020 (0,07 г, 0,09 ммолей) (в толуоле); без дальнейшей очистки продукт, содержащий соединение, указанное в заголовке, используют на следующей стадии.
Для соединения, указанного в заголовке, могут быть приведены следующие сигналы:
δ = 0.06 (м, 12Н), 0.17 (с, 9Н), 0.56 (с, 3Н), 0.78 (т, Н), 0.79 (т, 3Н), 0.88 (с, 18Н), 1.08 (д, 3Н), 1.00-2.15 (м, 17Н), 2.22 (дд, 1Н), 2.45 (дд, 1Н), 2.80(м, 3Н), 3.30(м, 1Н), 3.45 (м, 1Н), 3.79 (м, 1H), 4.19 (м, 1H), 4.38 (м, 1H), 4.87 (м, 1H), 5.18 (м, 1H), 6.00 (д, 1H), 6.25 (д, 1H).
Способ получения 22; соединение 0030
Соединение, указанное в заголовке получают замещением строительного блока боковой цепи циклопентилкарбонилметилен-трифенилфосфорана на 2-пропилкарбонилметилен-трифенил-фосфоран.
Способ получения 23: соединение 0033
5Е-витамин D: соединение 0008 (0,09 г, 0,14 ммолей) (в дихлорметане); продукт очищают хроматографией на силикагеле (15 г) (элюент: 30% эфир в петролейном эфире), получая соединение, указанное в заголовке. δ соответствует структуре вещества.
Способ получения 24: соединение 0035
Соединение получают из соединения 0001 в результате последовательности: 1. СН2= СН-МgВr; 2. разделение изомеров методом хроматографии; 3. EtBr, KH; 4. SO2; 5. О3; 6. РРh3; 7. нагревание, NаНСО3; 8. Рh3РСНСО2Ме; 9. гидрид диизобутилалюминия; 10. 1,1,1-триацетокси-1,1-дигидро-1,2-бензиодоксол-3-(1Н)-он.
Способ получения 25: соединение 0036
Соединение получают из соединения 0001 в результате последовательности: 1. СН3СO2Et, LiN(SiMe3)2; 2. TBS-трифторме-тансульфонат, 2,6-лютидин; 3. гидрид диизобутилалюминия.
Способ получения 26: соединение 0037
Соединение получают из соединения 0001 в результате последовательности: 1. 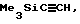 н-бутиллития, 2. EtBr, KH; 3. фторид тетрабутиламмония.
н-бутиллития, 2. EtBr, KH; 3. фторид тетрабутиламмония.
Способ получения 27: соединение 0038
К раствору литиевого производного, полученного из н-бутиллития (1,6М в гексане; 1 ммоль) и соединения 0037 (1 ммоль) в высушенном ТГФ (5 мл) при -70oС добавляют с помощью шприца 2-этилбутанал (1 ммоль) в высушенном ТГФ (2 мл). После перемешивания при той же температуре в течение 10 мин и затем при 0oС в течение 45 мин реакционную смесь распределяют между эфиром и водой. В результате стандартной рабочей процедуры получают продукт в виде масла. Очищают хроматографией на силикагеле (50 г) (элюент: 30% эфир в петролейном эфире), получая соединение, указанное в заголовке, в виде масла.
Общая процедура 7 (примеры)
К смеси раствора этилацетата (около 3 мл) TBS-эфира (са. 0,1 ммоль) в ацетонитриле (5 мл) при 25oС добавляют 48% водный раствор фтористоводородной кислоты (0,5 г, 12 ммолей). После перемешивания при той же температуре в течение 1 часа реакционную смесь распределяют между этилацетатом и 1N раствором гидроокиси натрия. Полученный в результате стандартной рабочей процедуры маслянистый продукт очищают хроматографией на силикагеле (15 г) (элюент: этилацетат), получая соединение, указанное в заголовке.
Пример 1: 24-oкco-l (S), 3 (R) -дигидрокси-20 (S)-9, 10-втор-холеста-5(Z), 7(Е),10(19)-триен (соединение 101)
TBS-эфир: соединение 0013 (0,050 г, 0,078 ммолей); соединение, указанное в заголовке: масло;
δ = 0.56 (3Н, с), 0.83 (3Н, д), 1.09 (6Н, д), 1.15-2.1 (18Н, м), 2.31 (1H, дд), 2.4 (1H, ддд), 2.5 (1H, м), 2.59 (1H, дд), 2.61 (1H, м), 2.82 (1Н, дд), 4.23 (1H, м), 4.43 (1H, м), 5 (1H, м), 5.32 (1H, м), 6.02 (1H, д), 6.37 (1H, д).
Пример 2: 1 (S), 3 (R) -дигидрокси-20 (R) - (6-гидрокси-6-метил-1-гептаноил)-9, 10-втор-прегна-5(Z), 7(Е),-10(19)-триен (соединение 102)
TBS-эфир: соединение 0014 (0,065 г, 0,095 ммолей); соединение, указанное в заголовке; масло;
δ = 0.52 (3Н, с), 1.02 (3Н, д), 1.1-2.05 (22Н, м), 1.21 (6Н, с), 2.3 (1H, с), 2.37-2.65 (4Н, м), 2.81 (1H, м), 4.22 (1H, м), 4.42 (1H, м), 4.99 (1H, м), 5.33 (1H, м), 6.01 (1H, д), 6.35 (1H, д).
Пример 3: 1(S), 3(R)-дигидрокси-20(R)-(5-гидрокси-5-этил-2-гептин-1-оил)-9, 10-втор-прегна-5(Z), 7(Е), 10(19)-триен (соединение 103)
TBS-эфир: соединение 0015 (0,07 г, 0,1 ммоль); соединение, указанное в заголовке: масло;
δ = 0.55 (3Н, с), 0.93 (6Н, т), 1.1-2.1 (20Н, м), 1.14 (3Н, д), 2.31 (1H, дд), 2.53 (1H, м), 2.57 (2Н, с), 2.59 (1H, м), 2.82 (1H, дд), 4.23 (1H, м), 4.42 (1H, м), 4.99 (1H, м), 5.33 (1H, м), 6.01 (1H, д), 6.36 (1H, д).
Пример 4: 24-оксо-1(S), 3(R), 25-тригидрокси-20(S)-9,10-втор-холеста-5(Z), 7 (Е), 10(19)-триен (соединение 104)
TBS-эфир: соединение 0016 (0,053 г, 0,073 ммолей); соединение, указанное в заголовке; масло;
δ = 0.57 (3Н, с), 0.85 (3Н, д), 1.2-2.1 (18Н, м), 1.39 (6Н, с), 2.31 (1H, дд), 2.55 (3Н, м), 2.83 (1H, м), 3.83 (1H, с), 4.23 (1H, м), 4.43 (1H, м), 5 (1H, м), 5.33 (1H, м), 6.02 (1H, д), 6.38 (1H, д).
Пример 5: 24-(1-гидрокси-циклопентил)-24-оксо-1(S),-3(R)-дигидрокси-20(S)-9,10-втор-хола-5(Z),-7(Е),10(19)-триен (соединение 105)
TBS-эфир: соединение 0034 (0,05 г, 0,066 ммолей); соединение, указанное в заголовке: масло;
δ = 0.57 (3Н, с), 0.85 (3Н, д), 1.2-2.1 (26Н, м), 2.31 (1H, дд), 2.55 (3Н, м), 2.83 (1H, м), 3.83 (1H, с), 4.23 (1H, м), 4.43 (1H, м), 5 (1H, м), 5.33 (1H, м), 6.02 (1H, д), 6.38 (1H, д).
Пример 6: 24-оксо-l (S), 3(R) -дигидрокси-20(R)-9,10-втор-холеста-5(Z), 7(Е),10(19),22(Е)-тетраен (соединение 106)
TBS-эфир: соединение 0033 (0,050 г, 0,078 ммолей); соединение, указанное в заголовке: масло;
δ = 0.56 (3Н, с), 1 (3Н, д), 1.09 (6Н, д), 1.15-2.1 (16Н, м), 2,25 (1H, м), 2.31 (1H, дд), 2.59 (1H, дд), 2.81 (1H, м), 2.82 (1H, дд), 4.23 (1H, м), 4.43 (1H, м), 5 (1H, м), 5.32 (1H, м), 6.02 (1H, д), 6.1 (1H, д), 6.37 (1H, д), 6.77 (1H, дд).
Пример 7: 1 (S), 3(R)-дигидрокси-20(R)-(3-оксо-4-этил-1-гексилокси)-9, 10-втор-прегна-5(Z), 7(Е), 10 (19)-триен (соединение 108)
TBS-эфир: соединение 0021, неочищенный продукт из способа получения 20; соединение, указанное в заголовке: масло;
δ = 0.55 (с, 3Н), 0.84 (т, 3Н), 0.85 (т, 3Н), 1.08 (д, 3Н), 1.10-1.80 (м, 15Н), 1.90-2.07 (м, 4Н), 2.25-2.35 (м, 2Н), 2.60 (шир.д, 1H), 2.75 (шир. к, 2Н), 2.82 (шир.д, 1H), 3.29 (м, 1H), 3.47 (м, 1H), 3.79 (м, 1H), 4.23 (м, 1H), 4.42 (м, 1H), 5.00 (шир.с, 1H), 5.33 (шир.с, 1H), 5.99 (д, 1H), 6.38 (д, 1H).
Пример 8: 1(S),3(R)-дигидрокси-20(R)-(3-оксо-4-гидрокси-4-этил-1-гексилокси)-9, 10-втор-прегна-5(Z), -7(Е), 10(19)-триен (соединение 109)
TBS-эфир: соединение 0022, неочищенный продукт из способа получения 21: соединение, указанное в заголовке: масло;
δ = 0.54 (с, 3Н), 0.77 (т, 3Н), 0.79 (т, 3Н), 1.07(д, 3Н), 1.05-2.10 (м, 19Н), 2.30 (дд, 1H), 2.58 (м, 2Н), 2.81 (м, 2Н), 3.28 (м, 1H), 3.50 (м, 1H), 3.83 (с, 1H), 3.85 (м, 1H), 4.22 (м, 1H), 4.41 (м, 1H), 4.98 (м, 1H), 5.31 (м, 1H), 5.98 (д, 1H), 6.37 (д, 1H).
Пример 7: Капсулы, содержащие соединение 104
Соединение 104 растворяют в арахисовом масле до конечной концентрации 1 мкг/мл. 10 весовых частей желатина, 5 весовых частей глицерина, 0,08 весовых частей сорбата калия и 14 весовых частей дистиллированной воды смешивают вместе при нагревании и формируют в мягкие желатиновые капсулы. Затем каждую из них наполняют 100 мкл масляного раствора соединения 104.
Пример 8: Дерматологический крем, содержащий соединение 104
Соединение 104 (0,05 мг) растворяют в миндальном масле (1 г). К этому раствору добавляют минеральное масло (40 г) и самоэмульгирующийся воск (20 г). Смесь нагревают до получения однородной массы (потери гетерогенности, liquifidation). После добавления горячей воды (40 мл) смесь хорошо встряхивают. Полученный крем содержит приблизительно 0,5 мкг соединения 104 на грамм крема.
ПРИЛОЖЕНИЕ 1.
Биологическая активность.
Мужские особи крыс - отъемышей (Holtzman Co,Madison,Wis.) помещали в подвешенные проволочные клетки и откармливали в волю кормом с низким содержанием кальция, витамина Д (дефицит), раскрытым в J.Nutr. 100,1049 (1970), в течение 2-3 недель до их использования в следующих исследованиях.
Интестинальный транспорт кальция
Крысы были разделены на шесть групп по шесть животных и каждому животному вводили путем интраюгулярной инъекции единичную дозу испытываемых соединений, растворенных в 0.05 мл 95% этанола. В таблице приведены вводимые дозы.
Группа 1, контрольная группа, получающая только растворитель (0.05 мл 95% этанола). Спустя 24 ч после инъекции крыс умерщвляют путем обезглавливания, извлекают двенадцатиперстную кишку для измерения активности транспорта кальция согласно методикам Мартина и ДеЛюка (Am.J.Physiol.216,1351 (1969)).
Результаты сведены в табл.3, приведенную ниже.
ПРИЛОЖЕНИЕ 2
Мобилизация кальция в кости (повышение концентрации кальция в сыворотке)
Крысам, откормленным так же, как описанно выше, и разделенным на группы из шести животных в каждой, вводили путем интраюгулярной инъекции по 0.05 мл 95% этанола (контрольная группа) или различные количества тестируемых соединений, указанных в табл.3, растворенных в 0.05 мл 95% этанола. Инъекцию делали в виде единичной дозы, за 6 или 24 ч перед их умервщлением. По истечении указанного времени крыс умервщляли обезглавливанием, их собирали кровь, которую центрифугировали, получая сыворотку. Аликвоту сыворотки (0.1 мл) смешивали с 1.9 мл 0.1% раствором хлористого лантана и измеряли концентрацию кальция в сыворотке (показание высвобождения костного кальция в ответ на тестируемое соединение) с помощью атомарного абсорбционного спектрофотометра (Perkin Elmer Model НО-214).
Результаты сведены в табл.4
Предлагаются дополнительные фармакологические данные, показывающие активность заявленных метаболитов витамина D3.
Показано клональное ингибирование пролиферации лейкозных, опухолевых клеток молочных желез и простаты. Были проведены эксперименты с соединениями витамина D3 и его соответствующего 24-оксо метаболита - соединения 104 согласно настоящему изобретению на их влияние на клональную пролиферацию лейкозных, двух типов опухолевых клеток молочной железы и простаты. Были определены дозы, требуемые для 50% ингибирования клональной пролиферации (ED50 нМ), которые сведены в таблицу. Исследования проводились на следующих клетках HL-60 (лейкозные, выделенные у пациентов с острой формой миелоидной лейкемии), MCF-7 и MDA-MB-436 (рак молочной железы, от пациентов с метастатической аденокарциномой молочной железы), LNCaP и DU-145 ( опухоль простаты).
Клетки, упомянутые выше, высевались трижды в лунки и выращивались в присутствии или отсутствии (контроль) испытываемых соединений. По истечении 3 дней измерялось распределение клеточного цикла. Результаты сведены в табл. 5.
Как видно из представленных данных, соединение согласно изобретению чрезвычайно активно в отношении указанных выше видов опухолей.
Кроме того, заявитель утверждает, что заявляемые соединения обладают значительной антипролиферативной активностью в отношении опухолевых клеток упомянутых выше. В частности, соединение 104 имеет значительную антипролиферативную активность в отношении MDA-MB-436 (ED50, 5 нМ). Это тем более замечательно, что известно, что опухолевые клетки молочной железы - MDA-MB-436 резистентны ко всем соединениям витамина D3.
Кроме того, клетки MCF-7 подвергаются апоптозу под действием соединений витамина D3 и его метаболитов, в частности соединение 104, причем апоптоз последнего значительно выше 23+ 1.6% по сравнению с 9.5 + 0.3% для его аналога 1,25 (ОН)2 -20-эпи-D3.




Изобретение относится к новым аналогам витамина D формулы I, где Х - Н или ОН, R1 и R2 - СН3 или С2Н5 или вместе с атомом углерода, несущим группу X, могут образовывать С3-С5 карбоцикл, Q - одинарная связь или С1-С8-гидрокарбилен, в которой одна из групп-CH2-, нe связанная с СО-группой, необязательно замещена ОН группой или заменена на атом кислорода, Y - одинарная связь или C1-C8-гидрокарбилен, или к их другим производным. Эти соединения обладают антивоспалительными и иммуномодулирующими эффектами, а также высокой активностью при индуцировании дифференциации и ингибировании нежелательной пролиферации некоторых клеток. 5 с. и 5 з.п. ф-лы, 5 табл.
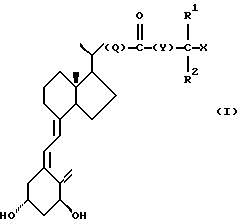
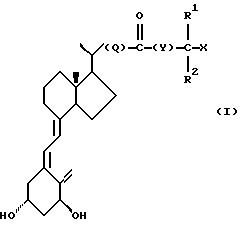
где Х представляет собой водород или гидроксигруппу;
R1 и R2 представляют собой метил или этил, или, вместе с атомом углерода, несущим группу X, могут образовывать С3-С5-карбоцикл;
Q представляет собой или одинарную связь, или C1-C8-гидрокарбилен, в котором одна из метиленовых групп, непосредственно не связанных с карбонильной группой, необязательно замещена гидроксильной или заменена на атом кислорода;
Y представляет собой или одинарную связь, или C1-C8-гидрокарбилен,
и производные формулы I, где одна или более гидроксигруппы замаскированы в виде групп, которые могут превращаться в гидроксигруппы in vivo.
| US 5274142, 28.12.1993 | |||
| ТРИНУС Ф.П | |||
| Химико-терапевтический справочник | |||
| - Киев: Здоровья, 1989, с.288 | |||
| Posner et al | |||
| "Stereocontrolled total synthesis of calcitriol derivatives", J of Org | |||
| Chem., v.59, № 25, (1994), p.7855-61. |
Авторы
Даты
2002-12-20—Публикация
1996-12-02—Подача