Изобретение относится к замещенным производным пропаноламина и их солям.
Уже описаны различные классы биологически активных веществ для лечения ожирения и нарушений липидного обмена:
- полимерные адсорберы, как, например, холестирамин;
- бензотиазепины (международная заявка WO 93/16055);
- димеры и конъюгаты желчной кислоты (европейский патент ЕР 0489423),
- амиды 4-амино-2-уреидопиримидин-5-карбоновой кислоты (европейский патент ЕР 00557879).
В основу изобретения положена задача получения других соединений, которые проявляют терапевтически пригодное гипо-липидемическое действие.
Изобретение относится поэтому к производным пропаноламина формулы (I)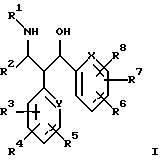
где R1 и R2, независимо друг от друга, означают циклоалкил с 3-8 атомами углерода в цикле, фенил, нафтил, фенантрил, пиридил, тиенил, фурил, пиримидил, индолил, тиазолил, имидазолил, кумаринил, фталиминил, хиноил, пиперазинил, тетразолил, триазолил, оксазолил и их тиено-, пиридино- или бензоанеллированные производные, причем циклоалкильное кольцо, ароматическое кольцо или гетероароматическое кольцо может быть от однократно до трехкратно замещено фтором, хлором, бромом, иодом, гидроксилом, СF3, -NO2, CN, (C1-C8)-алкоксилом, (С1-С8)-алкилом, аминогруппой, -NH-R9, -N(R9)R10, СНО, -СООН, -COOR11, -(C=O)-R12, (C1-C6)-алкил-ОН, (C1-C6)-алкил-(-ОН)-фенилом, (C1-C6) -алкилтрифторметилом, (C1-C6)-aлкилнитрогруппой, (C1-C6) -алкил-СN,
(С1-С6)-алкиламиногруппой, (С1-С6)-алкил-NН-R9, (С1-С6)-алкил-N((R9)R10,
(С1-С6)-алкил-СНО, (C1-C6)-алкил-СООН, (С1-С6)-алкил-СООR11, (С1-С6)-алкил-(С=O)-R12, -О-(C1-C6)-алкил-ОН, -О-(С1-С6)-алкил-СF3, -О-(C1-C6)-алкилнитрогруппой, -О-(C1-C6)-алкил-CN, -О-(С1-С6)-алкиламиногруппой, -O-(С1-С6)-алкил-NН-R9, -О-(С1-С6)алкил-N(R9)R10,
-O-(C1-C6)-алкил-СНО, -О-(C1-C6) -алкил-СООН, -О-(C1-C6) -алкил-COOR11, -O-(С1-С6)-алкил-(С=O)-R12, -N-SО3Н, SО2-СН3, -О-(C1-С6)-алкил-O-(C1-C6)-алкилфенилом, причем в алкильных остатках один или несколько атомов водорода могут быть заменены фтором;
R3-R8, независимо друг от друга, означают водород, фтор, хлор, бром, иод, гидроксил, СF3, -NO2, CN, (C1-C8)-алкоксил, (C1-C8)-алкил, аминогруппу, -NH-R9, -N(R9)R10, CHO, -СООН, -COOR11, -(C=O)-R12, причем в алкильных остатках один или несколько атомов водорода могут быть заменены фтором;
R9-R12, независимо друг от друга, означают водород, (C1-C8)-алкил,
Х означает СН, N;
Y означает СН, N;
при условии, что остатки R1, R2, Х и Y одновременно не означают: R1 - фенил; R2 - фенил; Х - СН; Y - CH;
а также к их физиологически приемлемым солям.
Предпочтительными являются соединения формулы (I), в которых один или несколько остатков имеют следующее значение:
R1 и R2, независимо друг от друга, означают циклоалкил с 3-8 атомами углерода в цикле, фенил, нафтил, тиенил, фурил, пиримидил, тиазолил, имидазолил, фталиминил, хиноил, пиперазинил, тетразолил, триазолил, оксазолил или их тиено-, пиридино-, или бензоанеллированные производные, причем циклоалкильное кольцо, ароматическое кольцо или гетероароматическое кольцо может быть от однократно до трехкратно замещено фтором, хлором, бромом, гидроксилом, СF3, -NO2, CN, (C1-С8)-алкоксилом, (С1-С8)-алкилом, аминогруппой, -NH-R9, -N(R9)-R10, -COOH, -COOR11, -(C=O)-R12, причем в алкильных остатках один или несколько атомов водорода могут быть заменены фтором;
R3-R8, независимо друг от друга, означают водород, фтор, хлор, бром, гидроксил, СF3, -NO2, CN, (С1-С8)-алкоксил, (С1-С8)-алкил, аминогруппу, -NH-R9, -N(R9)R10, COOH, -COOR11, -(C=O)-R12, причем в алкильных остатках один или несколько атомов водорода могут быть заменены фтором;
R9-R12, независимо друг от друга, означают водород, (С1-С8)-алкил;
Х означает СН, N;
Y означает СН, N;
при условии, что остатки R1, R2, Х и Y одновременно не означают: R1-фенил; R2-фенил; Х-СН; Y-СН;
а также их физиологически приемлемые соли.
Особенно предпочтительны соединения формулы (I), в которых один или несколько остатков имеют следующее значение:
R1 означает пиридил, пиримидил, тиенил, тиазолил, причем гетероароматическое кольцо может быть от однократно до трехкратно замещено фтором, хлором, бромом, иодом, гидроксилом, СF3, -NO2, CN, (C1-C8)-алкоксилом, (C1-C8)-алкилом, аминогруппой, -NH-R9, -N(R9)R10, СНО, -СООН, -COOR11, -(С= O)-R12;
R2 означает фенил, причем ароматическое кольцо может быть от однократно до трехкратно замещено фтором, хлором, бромом, гидроксилом, СF3, -NO2, CN, (C1-C8)-алкоксилом, (C1-С8)-алкилом, аминогруппой, -NH-R9, -N(R9)R10, -СООН, -COOR11, -(C=O)-R12;
R3-R8, независимо друг от друга, означают водород, фтор, хлор, бром, иод, гидроксил, СF3, -NO2, CN, (C1-C8)-алкоксил, (С1-С8)-алкил, аминогруппу, -NH-R9, -N(R9)R10, СНО, -СООН, -COOR11, -(C=O)-R12, причем в алкильных остатках один или несколько атомов водорода могут быть заменены фтором;
R9-R12, независимо друг от друга, означают водород, (C1-C8)-алкил;
Х означает СН;
Y означает N;
а также их физиологически приемлемые соли.
Под физиологически приемлемыми солями присоединения кислот понимают легко растворимые, растворимые или малорастворимые в воде соединения согласно определению, данному в книге "Немецкая Фармакопея" (9-е издание, 1986 г., официальное издание, Немецкое Медицинское Издательство, Штуттгарт) на странице 19. Предпочтительными являются гидрохлориды и сульфаты соединений.
Предметом изобретения являются как смеси изомеров формулы (I), так и также чистые энантиомеры формулы (I).
Изобретение относится далее к способу получения производных пропаноламина формулы (I):
Способ А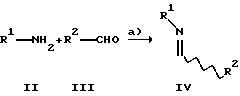
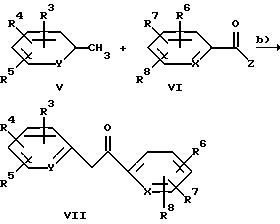
Способ Б
Способ А получения соединений формулы (I), отличающийся тем, что а) неизвестные из литературы, замещенные с помощью R1 и R2 имины, причем R1 и R2 имеют указанное для формулы (I) значение, получают известными из литературы способами из аминов типа II и альдегидов типа III. Для этого, например, амин типа II вводят во взаимодействие с альдегидом типа III в пригодном растворителе или в его отсутствие, таком как этанол, толуол или уксусная кислота, без добавки или с добавкой кислоты, как, например, п-толуолсульфокислота, при температурах от 20 до 150oС.
Замещенные остатками R3-R8 кетосоединения формулы (VII), причем R3-R8 имеют указанное для формулы (I) значение, получают известными из литературы способами или следуя таким способам. Так, например, производное пиколина формулы (V) металлируют с помощью пригодного основания, как, например, н-бутиллитий, и в тетрагидрофуране или в другом пригодном растворителе вводят во взаимодействие с соответствующими производными карбоновых кислот формулы (VI), например, как диалкиламиды или алкиловые эфиры карбоновых кислот, при температурах от -80oС до 20oС.
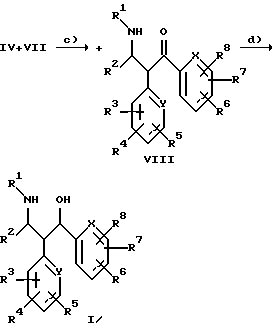
Соединения типа VIII получают тем, что имины типа IV вводят во взаимодействие с кетонами типа VII, которые могут быть замещены остатками R3-R8, причем R3-R8 имеют указанное для формулы (I) значение. Эту реакцию можно осуществлять, например, путем смешения обоих соединений в отсутствие их последующего нагревания или в пригодном растворителе, таком как этанол, толуол, диглим или тетрадекан, при температурах от 20 до 150oС (с).
Кетосоединения типа VIII в пригодном растворителе, таком как, например, метанол, тетрагидрофуран или смесь тетрагидрофурана с водой, восстанавливают с помощью NaBH4 или другого пригодного восстановителя, при температурах от -30oС до +40oС, до гидроксисоединений типа I, причем соединение формулы (I) может быть замещено остатками R3-R8 и R3-R8 имеют указанное для формулы (I) значение (d).
Соединения формулы (I) после вышеописанного восстановления получают в виде смеси изомеров. Различные рацематы можно отделять друг от друга путем фракционной кристаллизации или путем колоночной хроматографии. Чистые энантиомеры можно получать из рацематов соединений формулы (I) путем хроматографии на хиральном материале или путем известных из литературы способов с помощью оптически активных вспомогательных реагентов, как, например, описывается в J.Org.Chem., 44, 4891 (1979).
Способ Б получения соединений формулы (I), отличающийся тем, что имин формулы (IV) получают и выделяют не как в способе А, а соединения типа VIII, замещенные остатками R3-R8, синтезируют трехкомпонентной реакцией из кетонов VII, аминов II и альдегидов III. Для этого эти три компонента вводят во взаимодействие в отсутствие растворителя или в пригодном растворителе, как этанол, тетрадекан или толуол, при температурах от 20 до 150oС (е). Соединения формулы (VIII) восстанавливают до соединений формулы (I) (f), как описано в случае способа А, причем соединения формулы (VIII) можно использовать в виде очищенных кетонов, а также в виде полупродуктов, получаемых путем вышеописанной реакции.
Настоящее изобретение также относится к фармацевтическим композициям, которые наряду с нетоксическими, инертными, фармацевтически пригодными носителями содержат одно или несколько предлагаемых согласно изобретению биологически активных веществ или состоят из одного или нескольких, предлагаемых согласно изобретению биологически активных веществ, а также к способу получения этих композиций.
Под нетоксическими, инертными, фармацевтически пригодными носителями нужно понимать фармацевтически приемлемые, полутвердые или жидкие разбавители, наполнители или вспомогательные для приготовления лекарственных форм средства любого рода, которые после смешения с биологически активным веществом доводят его до пригодной формы применения.
В качестве пригодных лекарственных форм предлагаемых согласно изобретению соединений используют, например, таблетки, драже, капсулы, пилюли, водные растворы, суспензии и эмульсии, в случае необходимости стерильные растворы для инъекций, неводные эмульсии, суспензии и растворы, спреи, а также препаративные формы с пролонгированным высвобождением биологически активного вещества.
Терапевтически активные соединения в вышеуказанных фармацевтических композициях целесообразно должны находиться в концентрации примерно 0,1-99,0 мас.%, предпочтительно 0,5-70,0 мас.%, в расчете на общую смесь.
Применяемые концентрации для растворов, а также аэрозолей в форме спрея составляют в общем 0,1-20 мас.%, предпочтительно 0,5-5 мас.%.
Кроме предлагаемых согласно изобретению биологически активных веществ вышеуказанные фармацевтические композиции могут содержать также другие фармацевтические биологически активные вещества.
Указанные фармацевтические композиции получают обычным образом известными способами, например путем смешения биологически активного вещества или биологически активных веществ с носителем или носителями.
Биологически активные вещества или фармацевтические композиции можно вводить перорально, парентерально, интраперитонеально и/или ректально.
Используемые, например, в качестве гиполипидемических средств соединения настоящего изобретения и их соли можно применять для получения фармацевтических препаратов, которые содержат эффективное количество активного вещества вместе с носителями и которые пригодны для кишечного или парентерального введения. Предпочтительно используют таблетки или капсулы (желатиновые капсулы), которые содержат биологически активное вещество вместе с разбавителями, соответственно носителями, такими как, например, лактоза, декстроза, сахар-сырец, маннит, сорбит, целлюлоза, различные виды крахмала и/или глицин, и веществами, придающими скользкость, такими как кремнезем, тальк, стеариновая кислота или ее соли, как стеарат магния или стеарат кальция, и/или полиэтиленгликоль. Таблетки содержат также связующие, как карбонат магния, алюмосиликат магния, крахмал, желатина, трагант, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и/или поливинилпирролидон, и, если необходимо, красители, вещества, корригирующие неприятный вкус лекарства, и подслащивающие средства. Растворы для инъекций представляют собой предпочтительно изотонические водные растворы или суспензии, которые могут быть стерилизованы и могут содержать вспомогательные вещества, как консерванты, стабилизаторы, смачиватели и/или эмульгаторы, агенты растворения, соли для регулирования осмотического давления и/или буферные вещества. Предлагаемые согласно изобретению препараты, которые, если желательно, могут содержать другие фармакологически активные вещества, получают, например, обычными способами смешения-гранулирования и дражирования, и они содержат от 0,1% до предпочтительно 80%, предпочтительно примерно 5-65%, биологически активного вещества.
Пероральное введение осуществляют в виде фармацевтически обычных композиций, например в форме таблеток, драже или капсул, которые, например, содержат 5-1000 мг на суточную дозу, предпочтительно 20-200 мг, биологически активного вещества в смеси с обычным носителем и/или компонентом, причем можно вводить разовые дозы 5-200 мг, предпочтительно от одного до трех раз в день.
Однако может оказаться необходимым отклонение от указанных дозировок, а именно в зависимости от рода и массы тела излечиваемого объекта, рода и тяжести заболевания, вида композиции и способа введения лекарственного средства, а также от периода времени, соответственно интервала, в течение которого осуществляют прием лекарства. Так, в некоторых случаях может оказаться достаточным меньшее, чем вышеуказанное, количество биологически активного вещества, в то время как в других случаях нужно превышать вышеуказанное количество биологически активного вещества. Установить требующуюся в каждом случае оптимальную дозировку и способ введения биологически активных веществ легко может любой специалист, основываясь на своих специальных знаниях.
Соединения формулы (I) и их физиологически приемлемые соли представляют собой идеальное лекарственное средство для лечения нарушений липидного обмена, в особенности гиперлипидемии. Соединения формулы (I) также пригодны для влияния на уровень холестерина в сыворотке, а также для профилактики и лечения артериосклеротических явлений. Следующие данные подтверждают фармакологическую активность предлагаемых согласно изобретению соединений.
Биологическое испытание предлагаемых согласно изобретению соединений осуществляют путем определения ингибирования поступления [3H]-таурохолата в мембранные везикулы щеточной каймы подвздошной кишки кроликов. Тест на ингибирование осуществляют следующим образом:
1. Приготовление мембранных везикул щеточной каймы из подвздошной кишки кроликов.
Приготовление мембранных везикул щеточной каймы клеток тонкого кишечника осуществляют с помощью так называемого способа преципитации Мg2+. Самцов новозеландских кроликов (с массой тела 2-2,5 кг) умерщвляют путем внутривенной инъекции 0,5 мл T61®, водного раствора 2,5 мг тетракаингидрохлорида, 100 мл эмбутрамида и 25 мг мебезонийиодида. Тонкий кишечник извлекают и промывают охлажденным льдом физиологическим раствором хлорида натрия. Концевые 7/10 тонкого кишечника (измеряют в орально-ректальном направлении, т.е. концевая подвздошная кишка, которая содержит активную, Na+- зависимую транспортную систему желчной кислоты) используют для приготовления мембранных везикул щеточной каймы. Кишки замораживают в пакетах из синтетического материала в атмосфере азота при температуре -80oС. Для приготовления мембранных везикул замороженные кишки оттаивают при 30oС на водяной бане. Слизистую оболочку соскабливают и суспендируют в 60 мл охлажденного льдом 12 ммоль Трис/НСl-буфера (рН= 7,1)/300 ммоль маннита/5 ммоль этиленбис(оксиэтиленнитрило)-тетрауксусной кислоты/10 мг/л фенилметилсульфонилфторида /1 мг/л трипсинового ингибитора из соевых бобов (32 Ед/мг) /0,5 мг/л трипсинового ингибитора из легких крупного рогатого скота (193 Ед/мг) /5 мг/л бацитрацина. После разбавления до 300 мл с помощью охлажденной льдом дистиллированной воды гомогенизируют при охлаждении льдом с помощью аппарата Ультратурракс (18-стержневой, IKA Werk Staufen, Германия) в течение трех минут при 75% максимальной мощности. После добавления 3 мл 1 М раствора хлорида магния (конечная концентрация 10 ммоль) выдерживают точно одну минуту при температуре 0oС. Путем добавления Mg2+ агрегируют клеточные мембраны и осаждают за исключением мембран щеточной каймы. После центрифугирования в течение 15 минут при ускорении 3000 g (5000 оборотов в минуту, SS-34-ротор) осадок отбрасывают и супернатант, который содержит мембраны щеточной каймы, центрифугируют в течение 30 минут при ускорении 48000 g (20000 оборотов в минуту, SS-34-ротор). Супернатант отбрасывают, осадок снова гомогенизируют в 60 мл 12 ммоль Трис/НСl-буфера (рН=7,1)/60 ммоль маннита /5 ммоль этиленбис (оксиэтиленнитрило)-тетрауксусной кислоты с помощью гомогенизатора Поттер-Элвейгема (Браун, Мелсунген, 900 оборотов в минуту, 10 ходов). После добавления 0,1 мл 1 М раствора хлорида магния и времени инкубации 15 минут при температуре 0oС снова центрифугируют в течение 15 минут при ускорении 3000 g. Супернатант затем еще раз центрифугируют в течение 30 минут при ускорении 48000 g (20000 оборотов в минуту, SS-34-ротор ). Осадок обрабатывают с помощью 30 мл 10 ммоль Трис/Гепес-буфера (рН=7,4)/300 ммоль маннита и снова суспендируют путем 20 ходов в гомогенизаторе Поттер-Элвейгема при скорости 1000 оборотов в минуту. После центрифугирования в течение 30 минут при ускорении 48000 g (20000 оборотов в минуту, SS-34-ротор) осадок вносят в 0,5-2 мл Трис/Гепес-буфера (рН= 7,4)/280 ммоль маннита (конечная концентрация 20 мг/мл) и ресуспендируют с помощью туберкулинового шприца с иглой 27-го калибра. Везикулы либо используют непосредственно после приготовления для исследований транспортировки, либо хранят при температуре -196oС порциями по 4 мг в жидком азоте.
2. Ингибирование Nа+-зависимого поступления [3H]тaypoхолата в мембранные везикулы щеточной каймы подвздошной кишки.
Поступление субстратов в вышеописанные мембранные везикулы щеточной каймы определяют с помощью так называемого способа мембранной фильтрации. 10 мкл суспензии везикулы (100 мкг протеина) в виде капель наносят пипеткой на стенку инкубационной пробирки из полистирола (11•70 мм), которая содержит инкубационную среду с соответствующими лигандами (90 мкл). Инкубационная среда содержит 0,75 мкл = 0,75 мкКи [3H(G)]-таурохолата (удельная активность 2,1 Ки/ммоль)/0,5 мкл 10 мМ таурохолата/8,75 мкл натрийтранспортного буфера (10 ммоль Трис/Гепес (рН=7,4)/100 ммоль маннита/100 ммоль хлорида натрия) (Na-T-Б), соответственно 8,75 мкл калий-транспортного буфера (10 ммоль Трис/Гепес (рН=7,4)/100 ммоль маннита/100 ммоль хлорида калия) (К-Т-Б) и 80 мкл соответствующего раствора ингибитора, растворенного в зависимости от эксперимента в Na-T-буфере или К-Т-буфере. Инкубационную среду фильтруют через мембранный фильтр из поливинилиденфторида (SYHVLO 4NS, 0,45 мкм, диаметр 4 мм, фирма Миллипор, Эшборн, Германия). Путем смешения везикул с инкубационной средой начинают измерение транспортировки. Концентрация таурохолата в инкубационной смеси составляет 50 мкмоль. По истечении желательного времени инкубации (обычно 1 минута) транспортировку стопперируют путем добавления 1 мл охлажденного льдом раствора стоппера (10 ммоль Трис/Гепес (рН= 7,4) /150 ммоль КСl). Образующуюся смесь тотчас отфильтровывают под вакуумом 25-35 мбар через мембранный фильтр из нитрата целлюлозы (массовая единица 25, 0,45 мкм, диаметр 25 мм, Schleicher и Schuell, Дасселл, Германия). Фильтр дополнительно промывают с помощью 5 мл раствора стоппера.
Для определения поступления радиоактивно маркированного таурохолата мембранный фильтр растворяют в 4 мл сцинтиллятора Quickszint 361 (Zinsser Analytik GmbH, Франкфурт, Германия) и измеряют радиоактивность путем измерения сцинтилляции жидкости в измерительном приборе TriCarb 2500 (Канберра Паккард Гмбх, Франкфурт, Германия). Измеренные значения получают после калибровки прибора с помощью стандартных образцов и после коррекции возможно имеющейся хемилюминесценции в виде числа распадов в минуту.
В каждом случае определяют контрольные значения в Na-T-Б и К-Т-Б. Разница между поступлением в Na-T-Б и К-Т-Б дает Nа+-зависимую транспортную долю. В качестве ИК50 Na+ обозначают такую концентрацию ингибитора, при которой Na+-зависимая транспортная доля подавляется на 50%, в расчете на контроль.
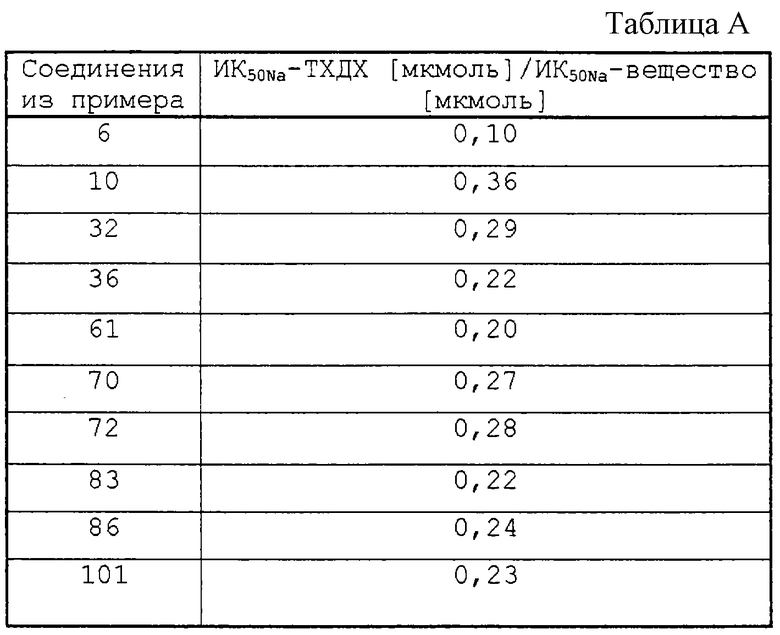
Фармакологические данные включают серию тестов, в которой исследуют взаимодействие предлагаемых согласно изобретению соединений с кишечной транспортной системой желчной кислоты в концевом тонком кишечнике. Результаты представлены в таблице А.
В таблице А приводятся данные измерения ингибирования поступления [3Н] -таурохолата в мембранные везикулы щеточной каймы подвздошной кишки кроликов. Показаны отношения значений ИК50Na стандартного вещества в виде таурохенодезоксихолата (ТХДХ) к соответствующему тестируемому веществу.
Нижеследующие примеры служат для более подробного пояснения изобретения, не ограничивая изобретение описанными в примерах продуктами и формами осуществления.
ПРИМЕР 1.
а.
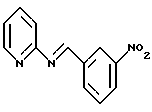
К раствору 25 г (266 ммоль) 2-аминопиридина и 40 г (265 ммоль) 3-нитро-бензальдегида в 300 мл толуола добавляют 0,7 г п-толуолсульфокислоты и смесь кипятят с обратным холодильником в течение 6 часов. После охлаждения половину растворителя удаляют в вакууме и смесь выдерживают в течение ночи. Выпавший осадок отсасывают, промывают холодным толуолом и высушивают в вакууме. Путем последующей перекристаллизации из смеси н-гептана с этилацетатом в соотношении 2:1 получают 48,8 г (81%) имина. С12Н9N3О2 (227,2); масс-спектр (бомбардировка быстрыми атомами): 228,2 М+Н+
b.

К раствору 50 г (0,54 моль) 2-пиколина в 770 мл тетрагидрофурана при температуре -55oС прикапывают 250 мл н-бутиллития (15%-ный в гексане) и перемешивают в течение 10 минут. Затем нагревают до 0oС и спустя следующие 30 минут охлаждают до -55oС. После этого медленно прикапывают раствор 77 г (0,52 моль) N,N-диметилбензамида в 570 мл тетрагидрофурана. После добавления нагревают до комнатной температуры и перемешивают в течение 1 часа. После добавления 500 мл воды и 35 мл концентрированной соляной кислоты органическую фазу отделяют, а водную фазу экстрагируют два раза этилацетатом. После высушивания над сульфатом магния органические фазы концентрируют в вакууме и остаток перегоняют в высоком вакууме. Температура кипения 134-136oС/0,3 мбар. Выход: 47,5 г (47%)кетона. С13Н11NО (197,2); масс-спектр (бомбардировка быстрыми атомами): 198,1 М+Н+.
с.
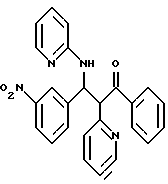
5,8 г (25,5 ммоль) имина из примера 1а и 5,0 г (25,4 ммоль) кетона из примера 1b хорошо перемешивают и нагревают на паровой бане. Спустя примерно 20 минут смесь начинает расплавляться и при дальнейшем нагревании кристаллизуется. После охлаждения остаток в 200 мл этилацетата нагревают до кипения, охлаждают, осадок отсасывают и высушивают в вакууме. Выход: 6,7 г (62%). C25H20N4O3 (424,2); масс-спектр (бомбардировка быстрыми атомами): 425,2 M+H+.
d.
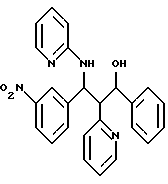
3,0 г (7,1 ммоль) кетосоединения из примера 1с растворяют в 50 мл смеси тетрагидрофурана с водой в соотношении 10:1, смешивают с 1,35 г (35,7 ммоль) боргидрида натрия и перемешивают в течение 1 часа при комнатной температуре. С помощью 2н. соляной кислоты доводят до pH=1 и перемешивают в течение 30 минут при температуре 50oС. После охлаждения реакционную смесь подщелачивают с помощью 2н. раствора гидроксида натрия и экстрагируют два раза этилацетатом. Органические фазы сушат над сульфатом магния и концентрируют. Остаток хроматографируют на силикагеле с помощью смеси гептана с этилацетатом в соотношении 6:4. Благодаря этому в виде продукта получают 2 рацемических соединения.
1-я Фракция: 1,26 г (42%) неполярного рацемата; С25Н22N4O3 (426,2); масс-спектр (бомбардировка быстрыми атомами): 427,2 М+Н+.
2-я Фракция: 1,15 г (38%) полярного рацемата; С25Н22N4O3 (426,2); масс-спектр (бомбардировка быстрыми атомами): 427,2 М+Н+.
е.

50 мг неполярного рацемата из примера Id путем препаративной высокоэффективной жидкостной хроматографии (ВЭЖХ) расщепляют на энантиомеры. Расщепление осуществляют на колонке с хиральной фазой CSP Chiralpak (фирма Daicel, Дюссельдорф) с помощью смеси н-гексана с пропан-2-олом в соотношении 50: 10 + 0,1% диэтиламина в качестве растворителя. В качестве 1-ой фракции получают 20 мг (-)-энантиомера и в качестве 2-ой фракции получают 20 мг (+)-энантиомера.
f.
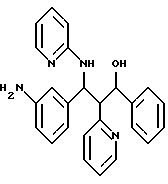
1,0 г (2,34 ммоль) неполярного рацемата из примера Id растворяют в 200 мл метанола и в присутствии примерно 20 мг 10%-ного палладия-на-угле гидрируют в атмосфере водорода в течение трех часов при комнатной температуре. Отфильтровывают от катализатора и раствор выпаривают. Остаток хроматографируют на силикагеле с помощью смеси этилацетата с н-гептаном в соотношении 4:1. Выход: 680 мг (73%) амина. C25H24N4O (396,2); масс-спектр (бомбардировка быстрыми атомами): 397,3 М+Н+.
g.
Из 2,0 г (4,69 ммоль) полярного рацемата из примера Id по описанному в примере 1f способу получают 1,2 г (65%) соответствующего амина. С25Н24N4O (396,2); масс-спектр (бомбардировка быстрыми атомами): 397,2 М+Н+.
ПРИМЕР 2.
а.
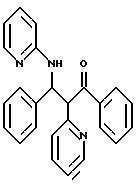
78,8 г (0,4 моль) кетона из примера 1b, 37,6 г (0,4 моль) 2-аминопиридина и 21,2 г (0,4 моль) бензальдегида растворяют в 1 л этанола и при интенсивном перемешивании кипятят с обратным холодильником в течение полутора часов. После этого дополнительно перемешивают в течение 4-х часов и выдерживают в течение ночи. Осадок отсасывают, промывают небольшим количеством этанола и высушивают в вакууме. Выход: 134 г (88%). С25Н21N3О (379,2); масс-спектр (бомбардировка быстрыми атомами): 380,1 М+Н+.
b.
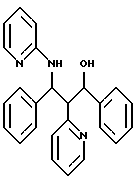
56,9 г (0,15 моль) кетона из примера 2а суспендируют в 1 л метанола и медленно порциями добавляют к 60 г NaBH4 в 100 мл воды; температура повышается от 22oС до 34oС. Спирт удаляют в вакууме, остаток смешивают примерно с 200 мл воды и экстрагируют три раза этилацетатом. Органические фазы сушат и выпаривают. Остаток хроматографируют на силикагеле с помощью смеси н-гептана с этилацетатом в соотношении 2:1. Получают два рацемических соединения.
1-я Фракция: 43 г (75%) неполярного рацемата; C25H23N3O (381); масс-спектр (бомбардировка быстрыми атомами): 382 М+Н+.
2-я Фракция: 14 г (24%) полярного рацемата; С25Н23N3О (381); масс-спектр (бомбардировка быстрыми атомами): 382 М+Н+.
с.
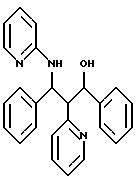
100 мг неполярного рацемата из примера 2b расщепляют по описанному в примере 1е способу. С помощью смеси н-гексана с пропан-2-олом в соотношении 25: 10+0,1% диэтиламина в качестве растворителя получают в качестве 1-ой фракции 40 мг (-)-энантиомера, а в качестве 2-ой фракции 30 мг (+)-энантиомера.
ПРИМЕР 3.
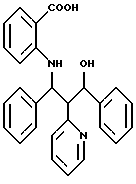
Неполярный рацемат из примера 47 в таблице 2 получают аналогично методике примера 2; 160 мг (0,36 ммоль) этого сложного метилового эфира растворяют в 20 мл этанола, смешивают с 1,6 мл 2н. водного раствора гидроксида натрия и перемешивают в течение 40 часов при комнатной температуре. Затем растворитель полностью удаляют, остаток растворяют в воде и с помощью 2н. соляной кислоты устанавливают в растворе рН=6,5. Экстрагируют два раза по 50 мл этилацетатом, органические фазы сушат и концентрируют. Хроматография остатка на силикагеле с помощью смеси н-гептана с этилацетатом в соотношении 1:1 дает 110 мг (71%) продукта. С27Н24N2О3 (424,2); масс-спектр (бомбардировка быстрыми атомами): 425,2 М+Н+.
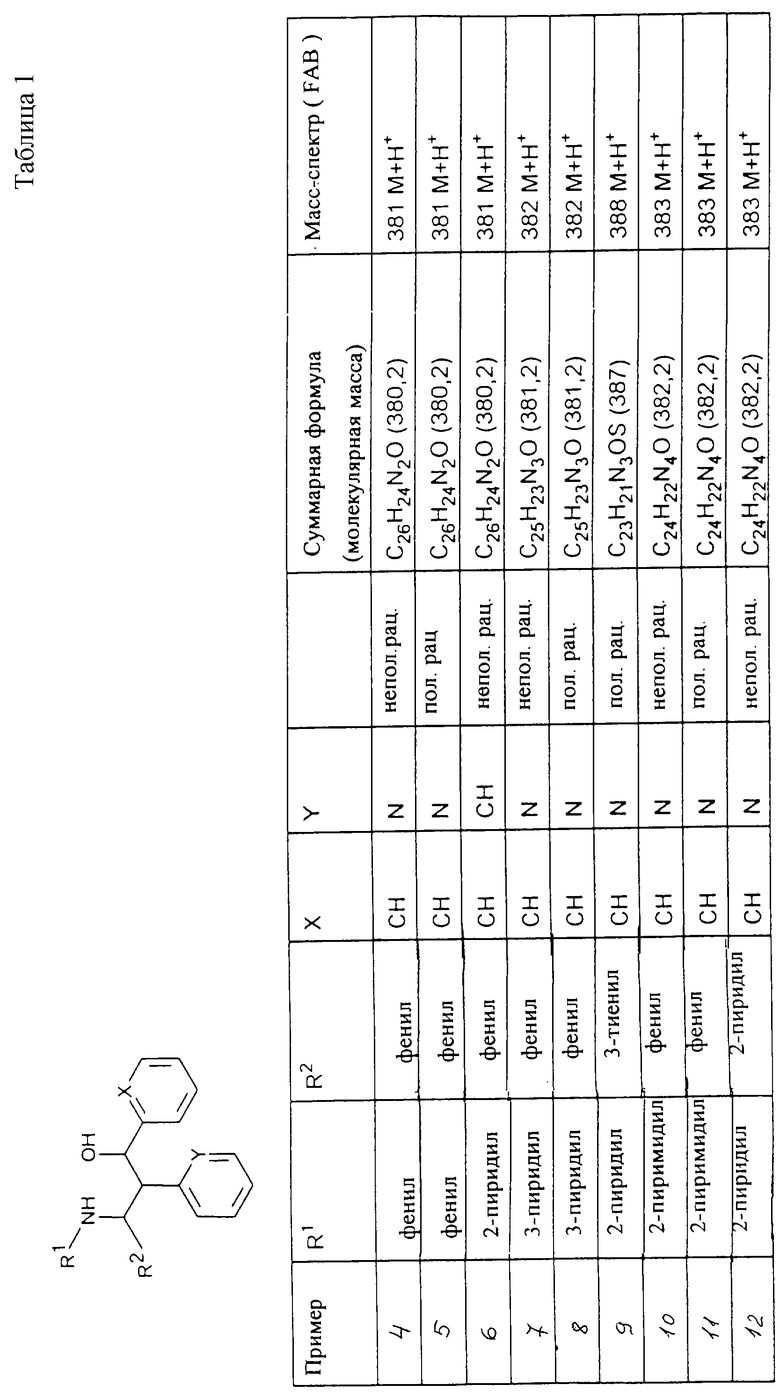
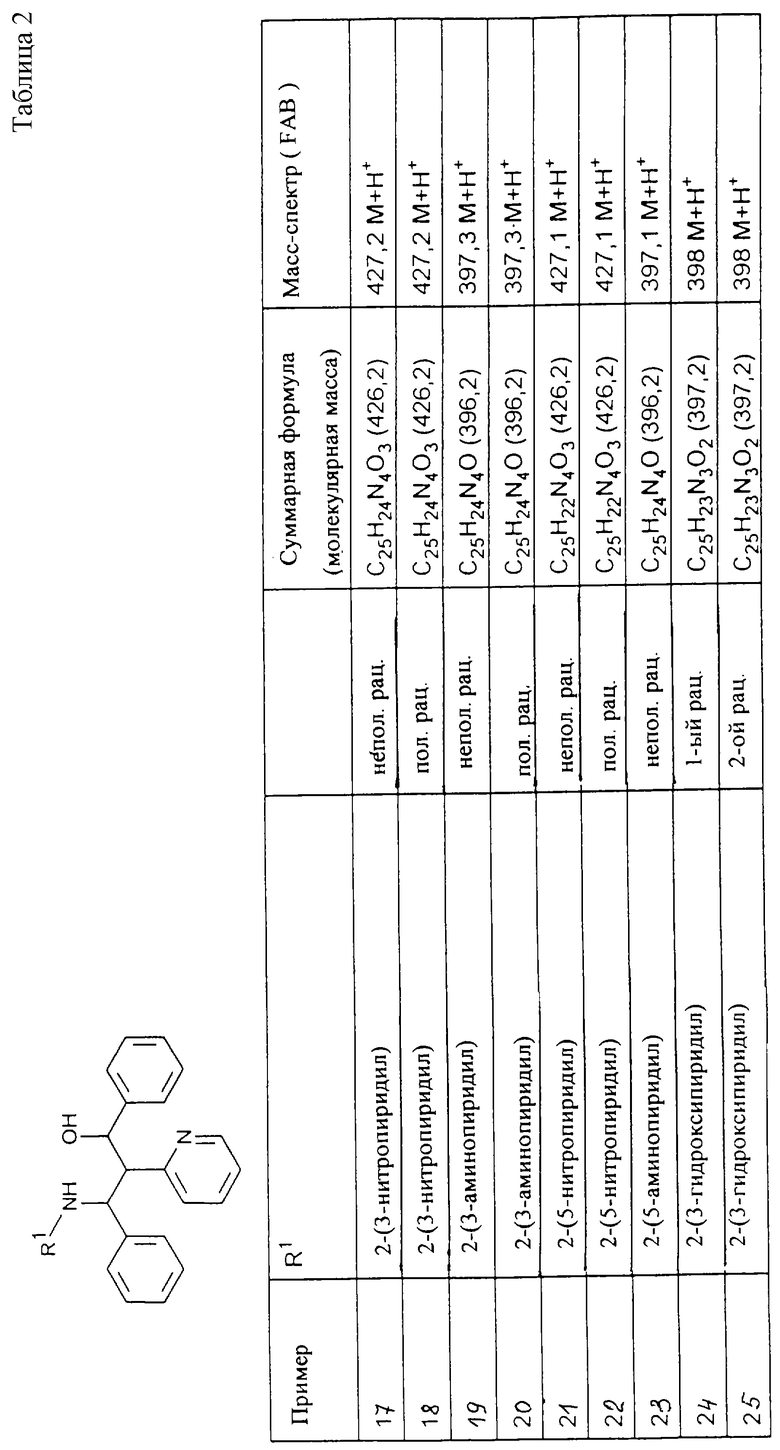
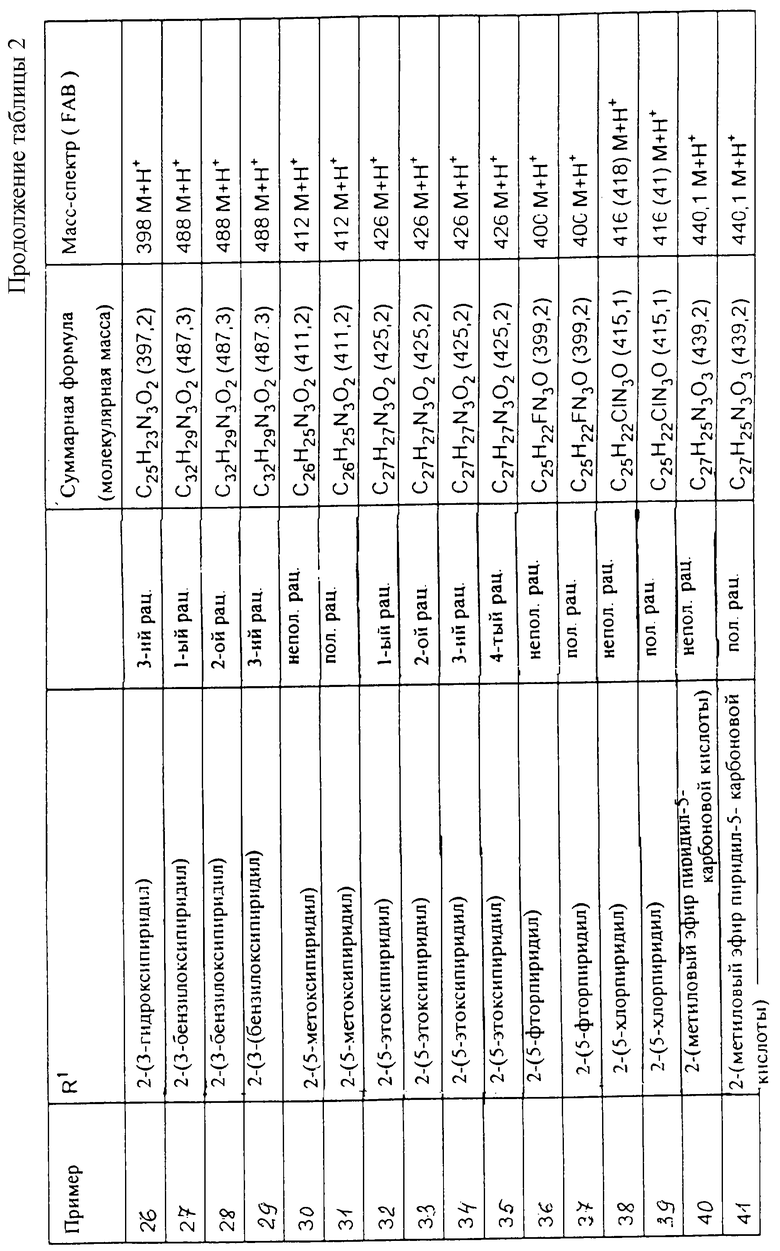
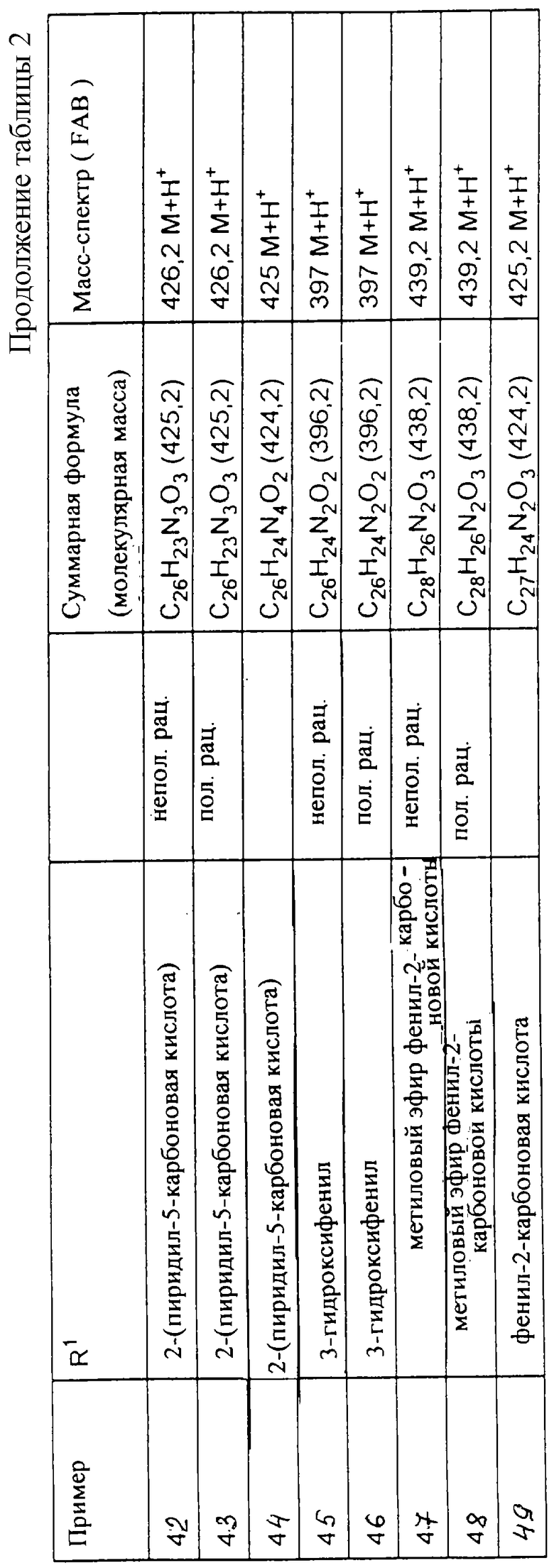
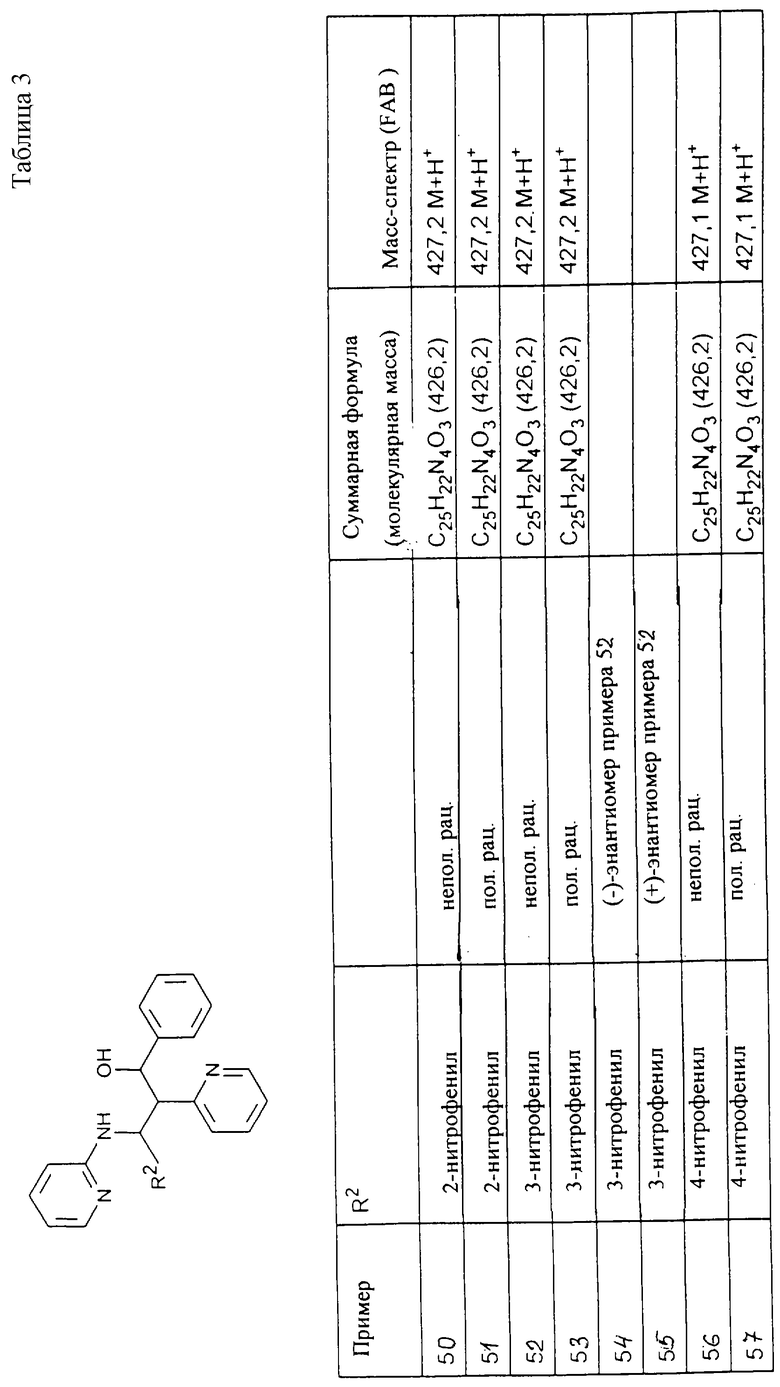
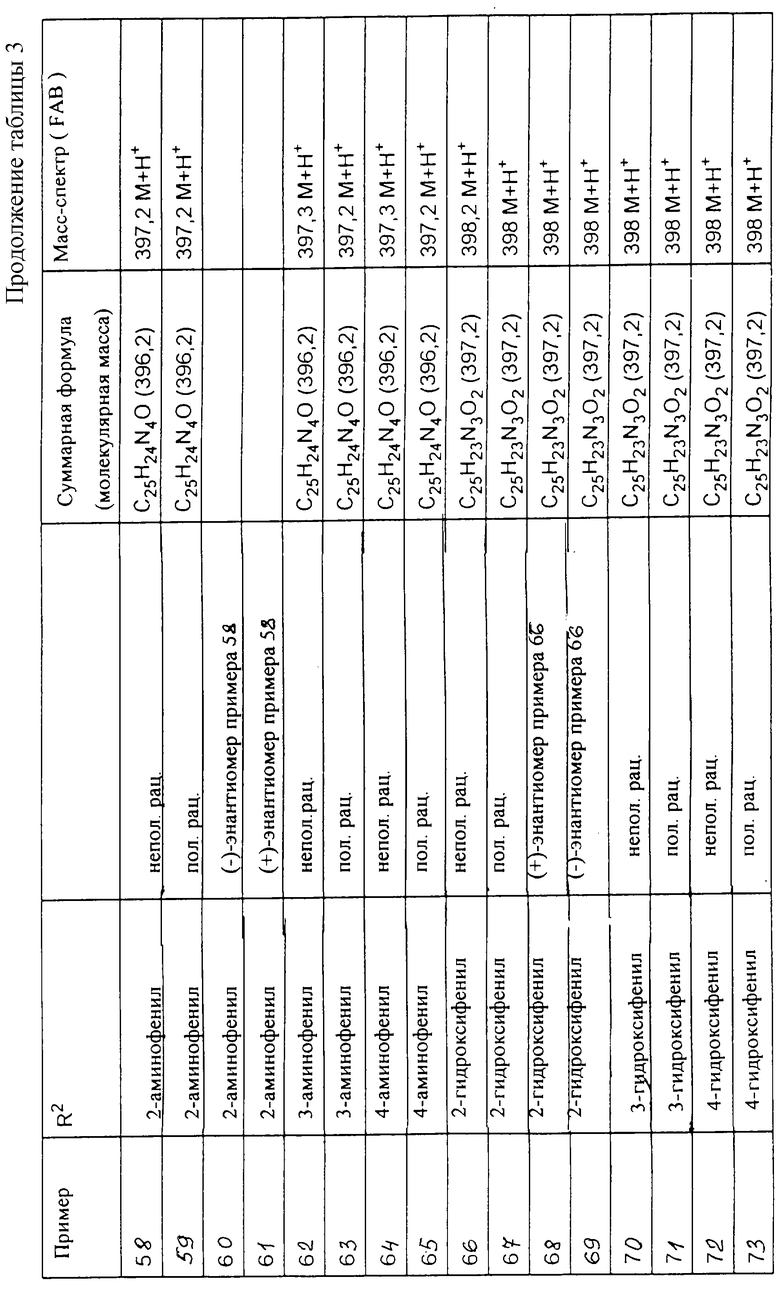
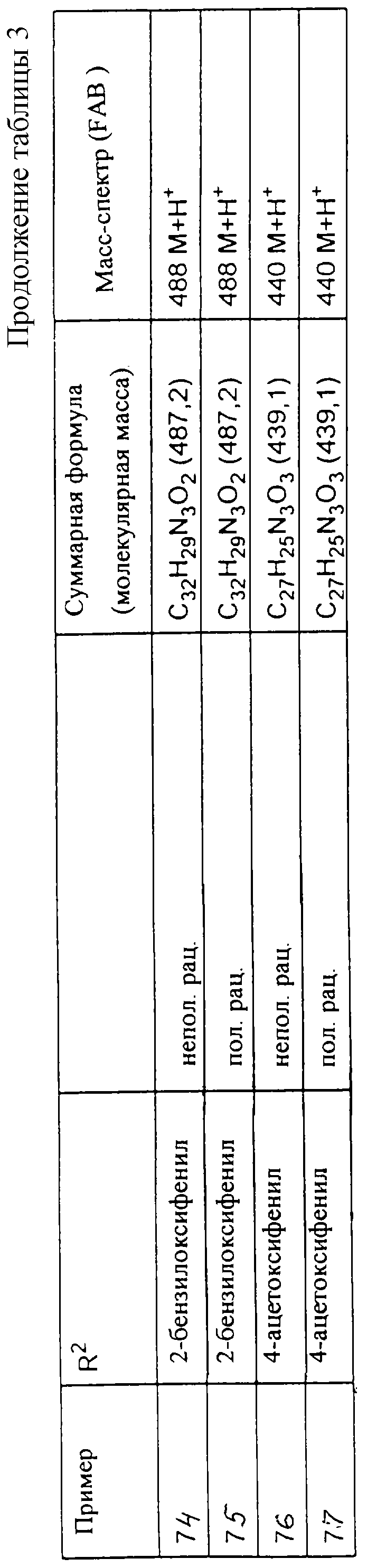
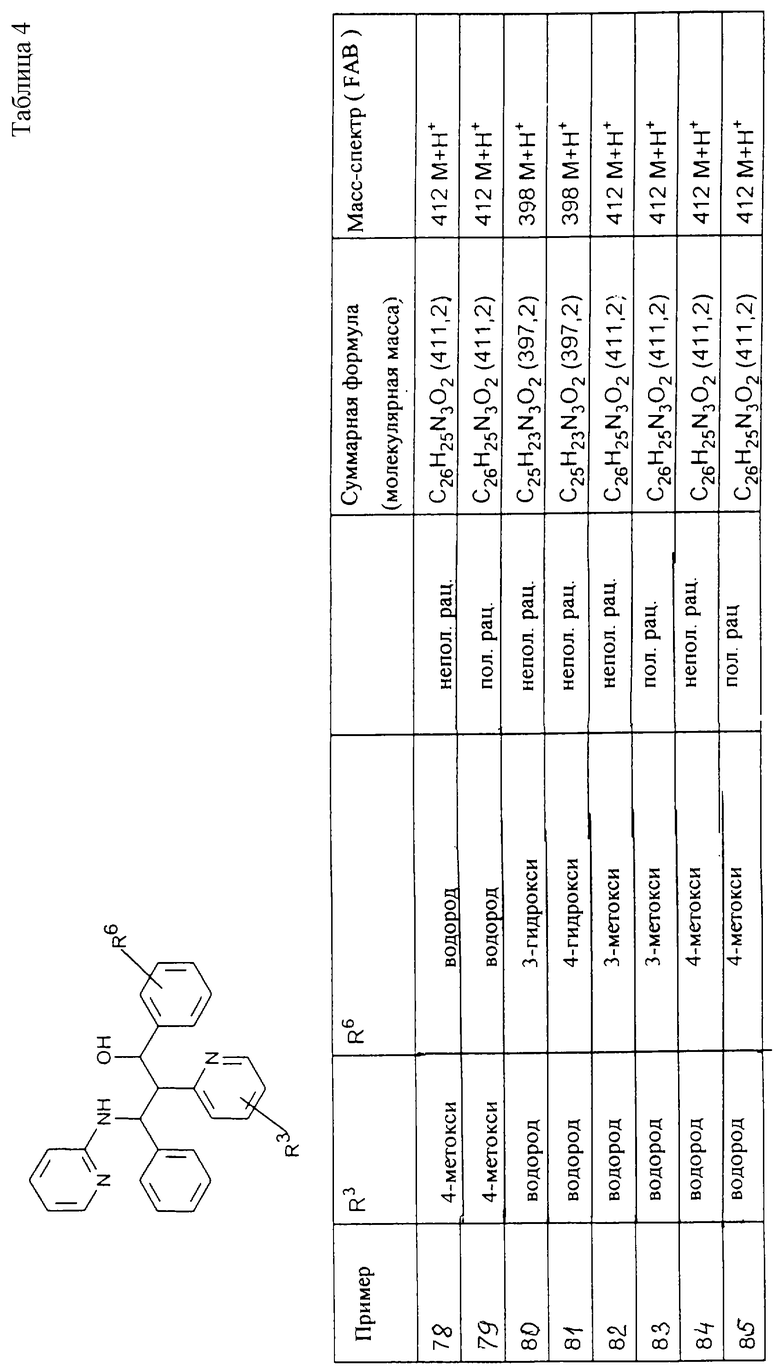
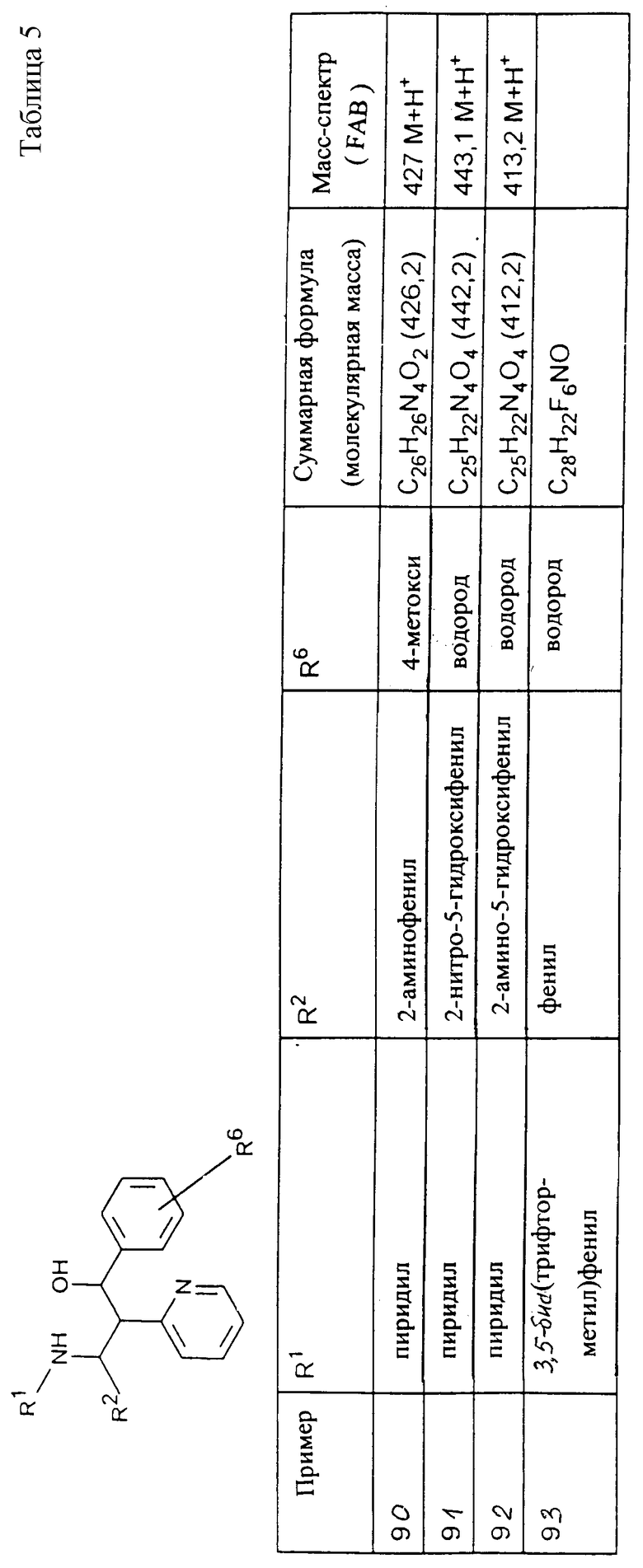
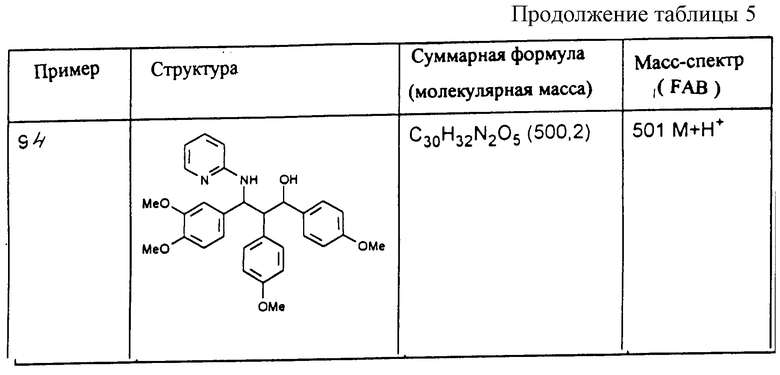
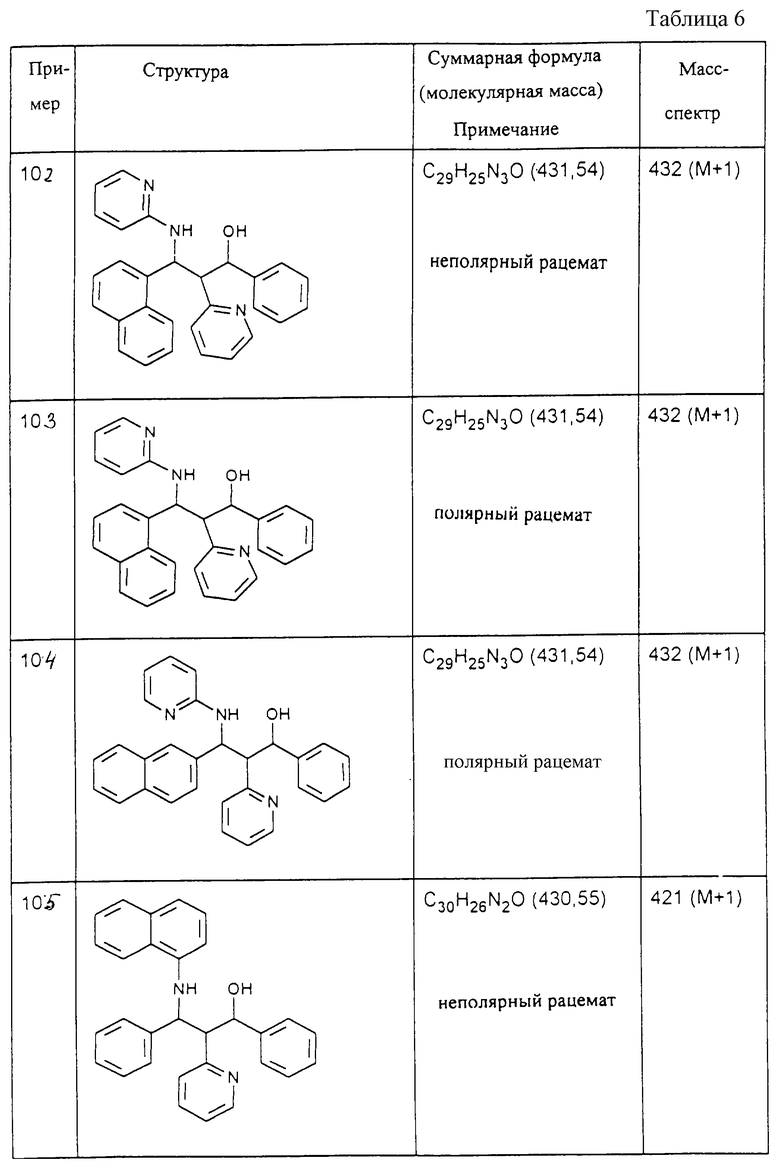
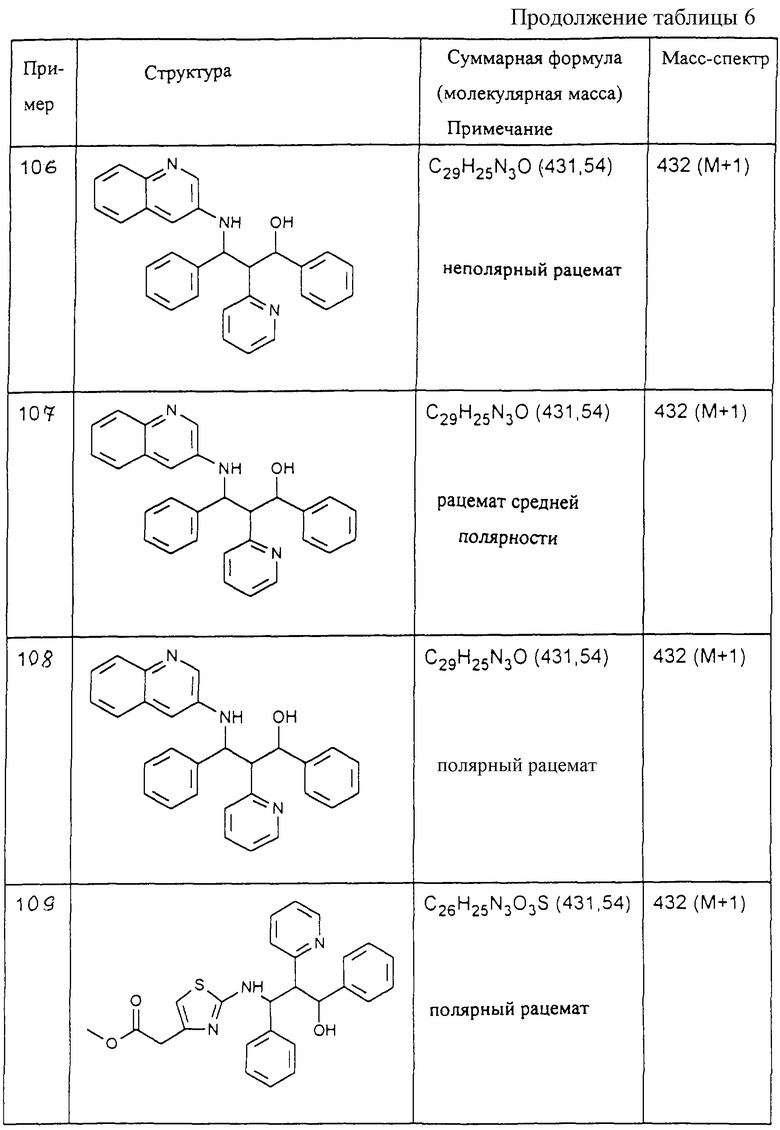
Исходя из соответствующих исходных соединений, получают указанные в примерах таблиц 1-5 соединения по описанным в примерах 1-3 способам.
ПРИМЕР 95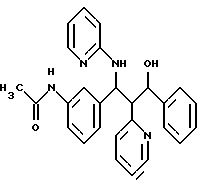
300 мг (0,76 ммоль) амина из примера 62 растворяют в 10 мл пиридина, смешивают с 75 мкл (0,80 ммоль) уксусного ангидрида и 5 мг диметиламинопиридина и перемешивают в течение двух часов при комнатной температуре. Затем добавляют 30 мл воды и экстрагируют три раза этилацетатом. Органические фазы сушат и концентрируют. Хроматография на силикагеле с помощью смеси н-гептана с этилацетатом в соотношении 4: 1 дает 200 мг (60%) продукта. C27H25N4O2 (438,2); масс-спектр (бомбардировка быстрыми атомами ): 439,2 М+Н+.
ПРИМЕР 96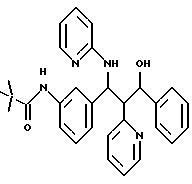
Аналогично методике примера 94 и при использовании хлорангидрида пивалиновой кислоты получают вышеуказанное соединение. С30Н32N4О2 (480,3); масс-спектр (бомбардировка быстрыми атомами): 481,3 М+Н+.
ПРИМЕР 97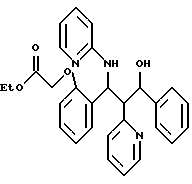
1,99 г (0,005 моль) соединения из примера 66 и 1 г порошкообразного карбоната калия вносят в 50 мл диметил-формамида. К раствору добавляют 0,7 мл (0,006 моль) этилового эфира бромуксусной кислоты и кипятят с обратным холодильником в течение 6 часов. Затем концентрируют в вакууме и остаток хроматографируют на силикагеле при использовании смеси н-гептана с этилацетатом в соотношении 2: 1. Выход: 1,94 г (80%). С29Н29N3O4 (483); масс-спектр (бомбардировка быстрыми атомами): 484 М+Н+.
ПРИМЕР 98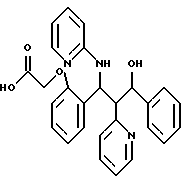
Целевое соединение примера 98 получают из соединения примера 97 по описанному в примере 3 способу. С27Н25N3О4 (455); масс-спектр (бомбардировка быстрыми атомами): 456 М+Н+.
ПРИМЕР 99.
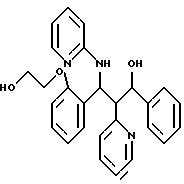
1,99 (0,005 моль) соединения из примера 66 и 8,8 г (0,1 моль) этиленкарбоната нагревают на масляной бане до 90-95oС (расплав). При этой температуре добавляют 0,14 г (0,001 моль) карбоната калия и перемешивают в течение 5 часов. После охлаждения полученный раствор отфильтровывают и концентрируют в вакууме. Хроматография на силикагеле с помощью смеси н-гептана с этилацетатом в соотношении 1:1 дает 1,5 г (68%) продукта. С27Н27N3О3 (441); масс-спектр (бомбардировка быстрыми атомами): 442 М+Н+.
ПРИМЕР 100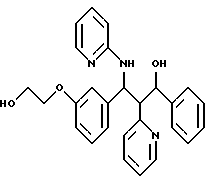
Целевое соединение примера 100 получают из соединения примера 70 по описанному в примере 99. способу. С27Н27N3О3 (441); масс-спектр (бомбардировка быстрыми атомами): 442 М+Н+.
ПРИМЕР 101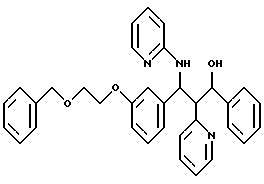
К раствору 1,83 г (12 ммоль) бензилоксиэтанола и 3,67 г (14 ммоль) трифенилфосфина в 100 мл безводного тетрагидрофурана в атмосфере аргона добавляют 4,04 г (20 ммоль) диизопропилазодикарбоксилата и затем 3,97 г (10 ммоль) соединения примера 70. После перемешивания в течение ночи растворитель удаляют и снова растворяют в этилацетате. Этот раствор встряхивают два раза с раствором карбоната натрия, затем сушат и концентрируют. Хроматография на силикагеле дает 3,85 г (72%) продукта. С34Н33N3О3 (531,3); масс-спектр (бомбардировка быстрыми атомами): 532 М+Н+.


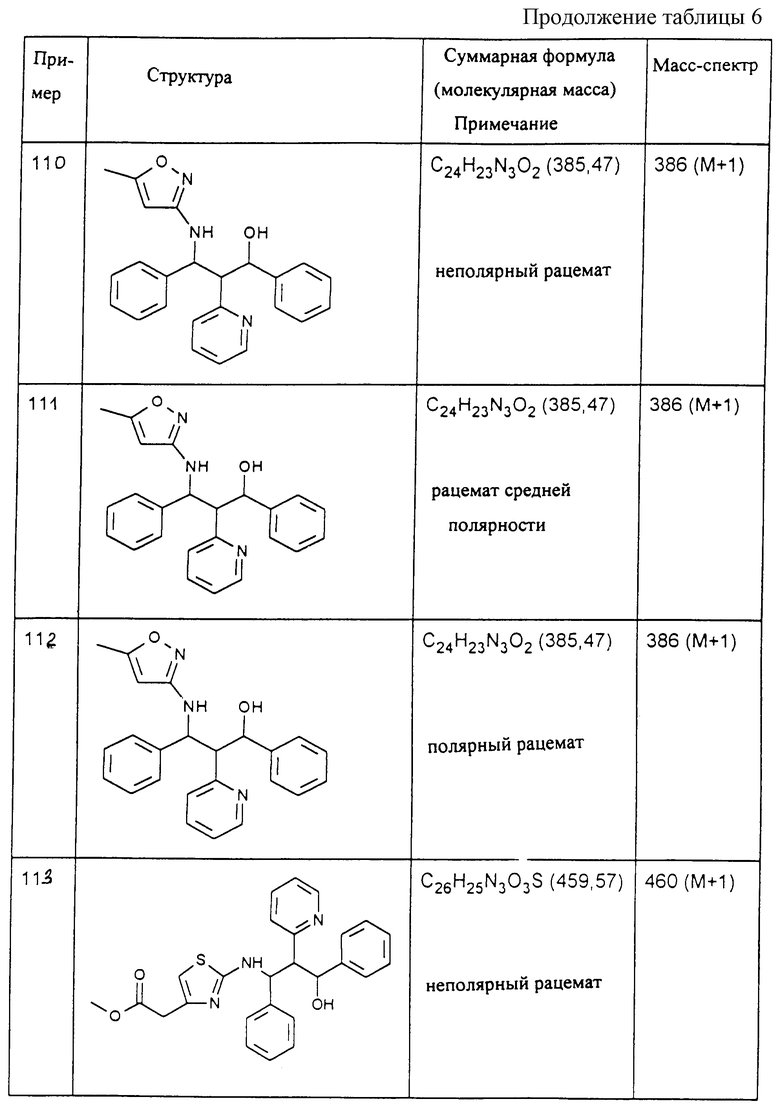
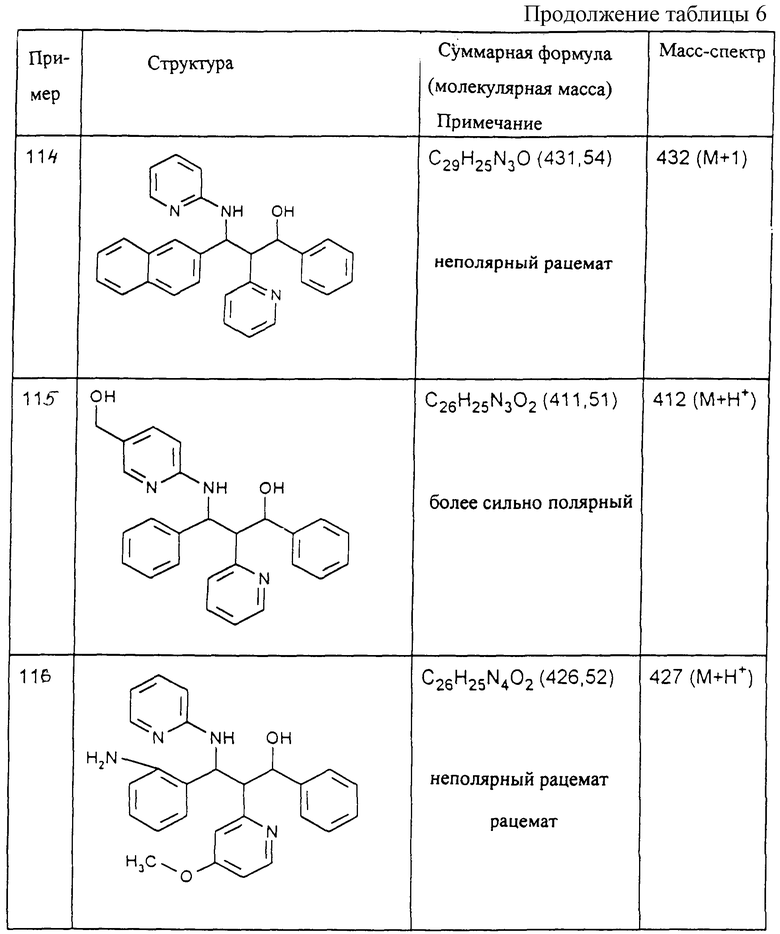
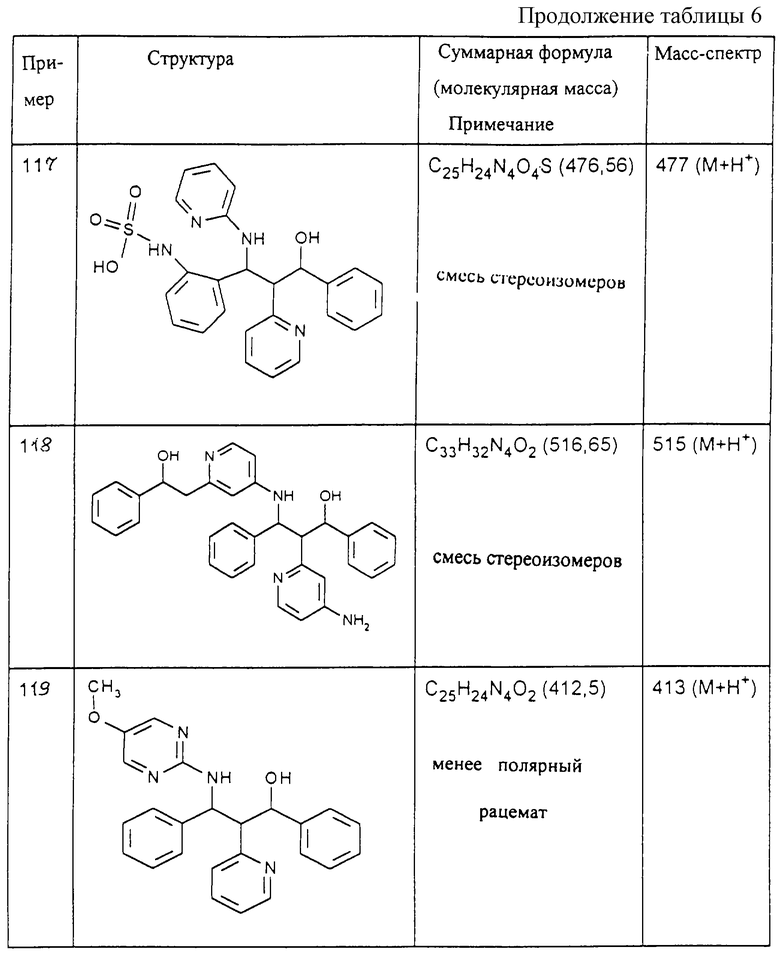
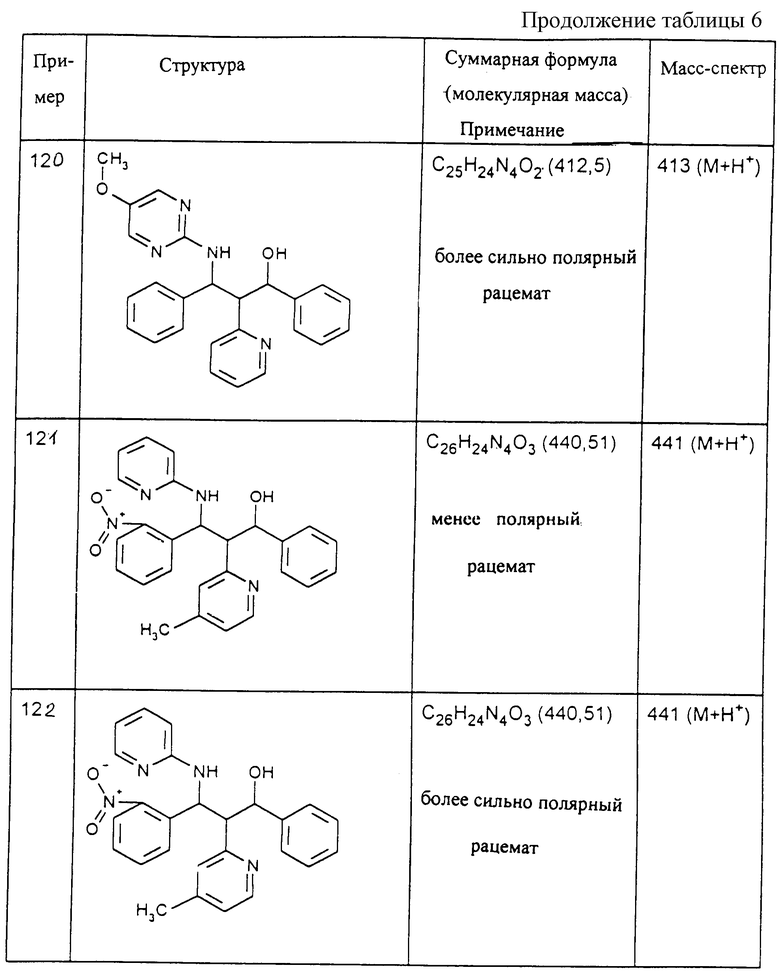
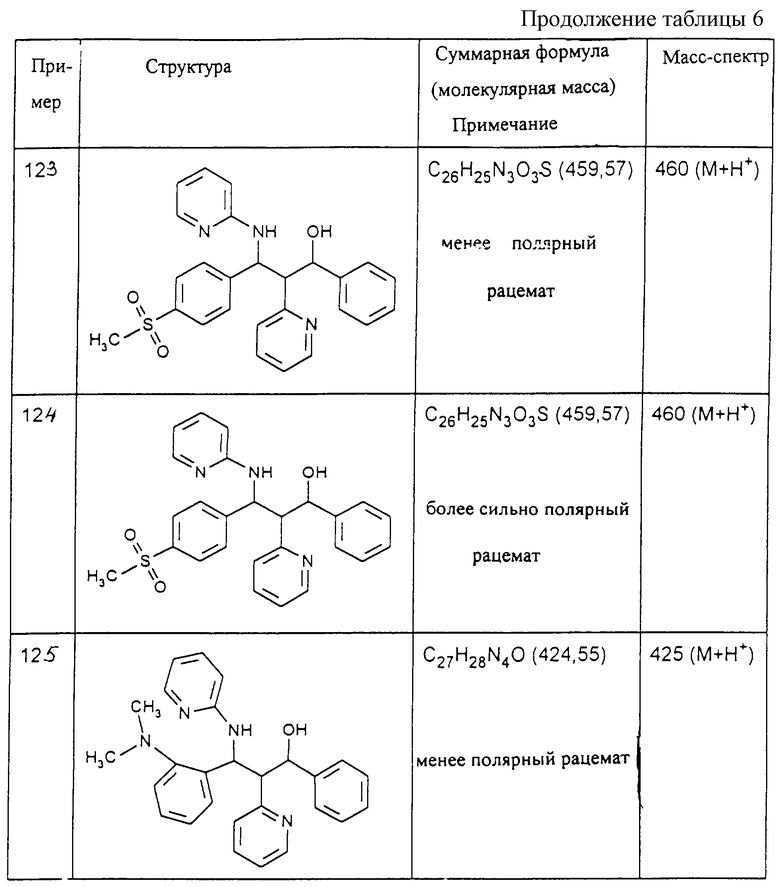
Изобретение относится к производным пропаноламина формулы (I) и их фармацевтически приемлемым солям, где R1 и R2 означают фенил, нафтил, пиридил, тиенил, пиримидил, тиазолил, хинолил, пиперазинил, оксазолил, которые могут быть замещены галогеном, ОН, NO2, NH2, COOH и др., R3-R8 означают водород, гидроксил, (С1-С8)-алкоксил, NH2, -NHR9, -N(R9)R10, R9-R10 означают водород или (С1-С8)алкил, Х означает СН или N, Y означает СН или N, при условии, что остатки R1, R2, X и Y одновременно не означают R1 - фенил, R2 - фенил, Х - СН, Y - СН. Соединения формулы (I) обладают ингибирующей поступление [3H] таурохолата активностью и могут найти применение в медицине. 3 с. и 3 з.п. ф-лы, 7 табл.
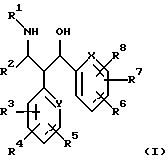
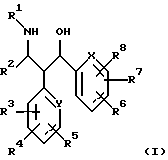
где R1 и R2, независимо друг от друга, означают фенил, нафтил, пиридил, тиенил, пиримидил, тиазолил, хинолил, пиперазинил, оксазолил, причем ароматическое или гетероароматическое кольцо может быть от однократно до трехкратно замещено фтором, хлором, бромом, иодом, гидроксилом, NO2, (С1-С8)-алкоксилом, NH2, -NHR9, -N(R9)R10, -СООН, -COOR11, (С1-С6)-алкил-ОН, (С1-С6)-алкил-(-ОН)-фенилом, (С1-С6)-алкил-СООН, (С1-С6)-алкил-СООR11,
-O-(С1-С6)-алкил-ОН, -N-SO3H, -SО2-СН3, -O-(С1-С6)-алкил-O-(С1-С6)-алкилфенилом,
R3-R8, независимо друг от друга, означают водород, гидроксил, (С1-С8)-алкоксил, NH2, -NHR9, -N(R9)R10;
R9-R11, независимо друг от друга, означают водород или (C1-C8)-алкил;
Х означает СН или N;
Y означает СН или N;
при условии, что остатки R1, R2, X и Y одновременно не означают R1 - фенил, R2 - фенил, Х - СН, Y - СН,
или их физиологически приемлемые соли присоединения кислот.
а) амин формулы (II)
R1-NH2, (II)
подвергают взаимодействию с альдегидом формулы (III)
R2-CHO, (III)
с получением имина формулы (IV)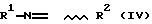
где R1 и R2 имеют указанные для соединений формулы (I) значения,
в) соединение формулы (V)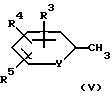
подвергают взаимодействию с производным карбоновой кислоты формулы (VI)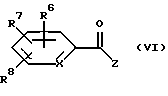
где Z обозначает удаляемую группу,
с получением кетосоединения формулы (VII)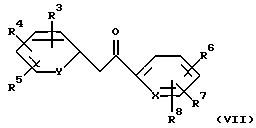
где X, Y и R3-R8 имеют указанные для соединений формулы (I) значения,
с) соединение формулы (IV), полученное на стадии (а), подвергают взаимодействию с соединением формулы (VII), с получением соединений формулы (VIII)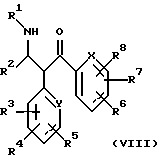
где X, Y, R1-R8 имеют указанные для соединений формулы (I) значения,
d) соединение формулы (VIII) восстанавливают до соединения формулы (I) в подходящем растворителе при температуре от -30 до 40oС.
Приоритет по пунктам и признакам:
04.04.1997 по пп.1-6;
26.01.1998 по пп.1-6, уточнение признаков.
| ЙНИЯ ЗАДЕРЖКИ | 0 |
|
SU345591A1 |
| RU 94031210 A1, 20.03.1996 | |||
| 3R,5S-(+)-7-[4-(4-ФТОРФЕНИЛ)-2,6- ДИИЗОПРОПИЛ-5-МЕТОКСИМЕТИЛ-ПИРИД-3-ИЛ]-3,5- ДИОКСИГЕПТЕНОВАЯ КИСЛОТА В ЭРИТРО-(E)-КОНФИГУРАЦИИ В ВИДЕ ФИЗИОЛОГИЧЕСКИ ПЕРЕНОСИМОЙ СОЛИ МЕТАЛЛА В КАЧЕСТВЕ ИНГИБИТОРА БИОСИНТЕЗА ХОЛЕСТЕРИНА | 1991 |
|
RU2026290C1 |
Авторы
Даты
2003-02-20—Публикация
1998-04-03—Подача