Предпосылки изобретения
Область изобретения
Изобретение относится к регулированию раскрытия и растяжения шейки матки использованием доноров и/или субстратов оксида азота или ингибиторов оксида азота.
Уровень техники
Роды (выход плода из матки) требуют как сокращения миометрия, гладкой мышцы матки, так и расслабления соединительной ткани шейки, так чтобы она была растянута и расширена достаточно, чтобы позволить плоду выйти. Это расслабление известно как "созревание".
В настоящее время предпочтительным методом созревания шейки является использование простагландина Е2. Его применяют как вагинальный гель или таблетки или как гель, помещаемый в шейку матки. Проблемой, связанной с использованием простагландина Е2, является то, что существует возможность гиперстимуляции матки, приводящей к исключительно сильным сокращениям миометрия до созревания шейки и до спокойных и безопасных родов.
Идеальный препарат должен расслаблять и разглаживать шейку, не вызывая миометральных сокращений. Это должно позволить последующие сокращения (вызываемые, если необходимо, небольшой дозой простагландина), чтобы ребенку родиться с минимальным сопротивлением. Есть хорошие свидетельства из экспериментов на животных, что антипрогестины, такие как RU486, должны отвечать таким требованиям, но проблема с этим лекарством в том, что оно имеет сопутствующую антиглюкокортикоидную активность, которая может повредить плоду.
Одним из наиболее значительных недавних успехов в биологии и медицине является открытие того, что оксид азота продуцируется эндотелиальными клетками и что он включается в регуляцию сосудистого тонуса, агрегации тромбоцитов, нейротрансмиссии и имунной активации (Фурхготт и Завадский, 1980; Монкада, Палмер и Хиггс, 1991; Ингарро, 1991). Оксид азота является важным медиатором релаксации гладкомышечной мышцы (Монтада, Палмер и Хиггс, 1991) и был прежде известен как EDRF (расслабляющий фактор, полученный из эндотелина) (Фурхготт и Завадский, 1980; Монкада, Палмер и Хиггс, 1991).
Оксид азота синтезируют окислительным деаминированием гуанидинового азота L-аргинина по меньшей мере различными изоформами флавинсодержащего фермента, синтазы оксида азота (Монтада, Палмер и Хиггс, 1991).
Оксид азота также можно генерировать, применяя различные доноры оксида азота, такие как нитропруссид натрия, нитроглицерин, тринитрат глицерина, SIN, мононитрат изосорбида, динтрат изосорбида и т.д.
Было показано, что синтез оксида азота полностью ингибируется аналогами L-аргинина; метиловым эфиром NG-нитро-L-аргинина (L-NAME), NG-моноэтил-L-аргинином (LMMA), N-иминоэтил-L-аргинином (L-N10), L-монометил-L-аргинином (L-NNMA), L-NG-метиларгинином (LNМА), NW-нитро-L-аргинином (L-NА) и аминогуанидином.
Обработка небеременных морских свинок L-NAME приводит к повышенной сократительной способности матки. Следовательно, ингибирование сократительной способности матки, стимулированное синтазой оксида азота, указывает, что тонизирующее выделение оксида азота поддерживает матку в неактивном состоянии. Подобно этому обработка беременных морских свинок L-NАМЕ вызывает преждевременные роды. С другой стороны, обработка полоски матки крыс in vitro L-аргинином ингибирует сокращения. Эти исследования показывают, что выработка оксида азота маткой ингибирует сократительную способность матки, а блокирование ее синтеза приводит к повышенной сократительной способности у беременных и небеременных животных. Следовательно, субстраты и доноры оксида азота могут быть использованы в терапии для предотвращения сократительной способности матки, а ингибиторы оксида азота - для эффективного стимулирования сокращений матки.
На основе предварительных изучений на макаках-резусах Дженнингс и др. (The Journal of Maternal - Fetal Medicine 2; 170-175 (1993)) предположили, что оксид азота может быть важным для неактивности матки во время беременности, а экзогенный оксид азота может быть полезен для контроля преждевременных родов.
Активность синтазы оксида азота (NOS) была продемонстрирована Натуцци и др. (Biochem. and Byophys. Aes.Commun. 194, 1, 128 (1993)) в многочисленных структурах матки беременных крыс, и они заключили, что NOS должна присутствовать в многочисленных структурах матки беременных крыс. Снижение активности NOS при родах предполагает, что NOS может вносить вклад в поддерживание сократительного спокойствия во время беременности.
Также морфологические изучения уже показали наличие NOS (NADPH-диафораза, гистохимический метод определения всех изоформ NOS) и ферментов, метаболизирующих NO, таких как супероксиддисмутаза в шейке матки (Папка и др. Neuroscience letters, 147 (1992); Шиотани и др. Acta Histochem Cytochem. 26; 57-64 (1993)).
Было обнаружено, что обработка L-NAME морских свинок подкожно на 48-49 после контакта (конечный день 67+3 дня) ведет к снижению растяжения матки и снижению расширения шейки матки.
У беременных крыс была обнаружена повышенная выработка оксида азота (параметр, выделение нитрита или нитрата in vitro) из шейки матки во время родов по сравнению с 18 днем беременности. Напротив, происходило снижение выработки маточного (миометрального) NО во время беременности крыс. Антипрогестин онапристон увеличивал выработку оксида азота в шейке матки беременных крыс еще больше, но ингибировал выработку NO в матке (миометрии). Введение той же самой дозы онапристона вызывало созревание матки у крыс.
Эти исследования свидетельствуют о том, что обработка ингибитором оксида азота, такого как L-NАМЕ, ингибирует созревание шейки, но стимулирует сокращения матки у беременных морских свинок;
выработка NO, который дает расслабляющий эффект на миометрии, уменьшается в беременной матке (миометрии) во время беременности, но она увеличивается в шейке матки во время нормальных или вызываемых антипрогестином родах у крыс;
расходящиеся эффекты ингибитора оксида азота, такого как L-NAME, на сократительную способность матки и шейки матки обусловлены либо различными действиями NО системы, либо присутствием различных изоформ фермента в миометрии и шейке, и
NO-система играет важную роль в регуляции шейки матки, причем выработка NО увеличивается в процессе созревания шейки.
Следовательно, можно заключить, что:
а) местное применение доноров и/или субстратов оксида азота может быть использовано, чтобы вызвать созревание шейки, или
б) местное применение ингибитора оксида азота может быть использовано, чтобы предотвратить или ингибировать созревание шейки, например, при лечении шеечной недостаточности (слишком раннего созревания шейки) или преждевременных родов.
Настоящее изобретение относится к применению доноров и/или субстратов оксида азота или ингибиторов оксида азота для производства лекарственного средства для регуляции раскрытия шейки матки и/или растяжения.
Настоящее изобретение включает применение или
а) по меньшей мере одного донора и/или субстрата оксида азота для производства лекарственного средства для местного применения (например, внутримышечно или внутривагинально) для вызывания созревания матки, или
б) по меньшей мере одного ингибитора оксида азота для производства лекарственного средства для местного применения (например, внутришеечно или внутривагинально) для ингибирования созревания матки при лечении шеечной недостаточности или преждевременных родов.
В качестве (а) доноров и/или субстратов оксида азота или (б) ингибиторов оксида азота в настоящем изобретении используют все соединения, известные профессионалам, как имеющие требуемые свойства; соединения, указанные в уровне техники, являются предпочтительными. Доноры и/или субстраты оксида азота (а) могут быть также использованы в комбинации с (i) по меньшей мере одним антипрогестином, простагландином и/или цитокином.
Антипрогестины выбирают из следующей группы соединений
онапристон
(11β-[4-(диметиламино) фенил] -17α-гидрокси-17β-(3- гидроксипропил)-13α-эстра-4,9-диен-3-он),
RU 486 (11β-[4-(диметиламино) фенил] -17β-гидрокси-17α-(1- пропенил)эстра-4,9-диен-3-он),
(Z)-11β-[4-(диметиламино) фенил] -17β-гидрокси-17α-(3-гидрокси-1-пропенил) эстра-4-ен-3-он (ЕР-А 0404283),
11β-(4-ацетилфенил)-17β- гидрокси-17α-(1-пропинил)эстра-4,9-диен-3-он (ЕР-А 0190759),
4', 5'-дигидро-11β-[4- (диметиламино)фенил]-6β-метилспиро[эстра-4,9-диен -17β,2'(3'Н)-фуран]-3-он,
4',5'-дигидро-11β-[4- (диметиламино)фeнил]-7β-метилспиро[эстра-4,9-диен- 17β,2'(3'Н)-фуран]-3-он,
11β-(4-ацетилфенил)-19, 24-динор-17,23-эпокси-17α-хола-4,9,20-триен-3-он,
(Е)-11β-[4-[[(ацетокси)имино] метал]фeнил]-17β-метокси-17α-(метоксиметил) эстра-4,9-диен-3-он,
(Е)-11β-[4-[[[(этоксикарбонил) окси)имино]метил]фенил]-17β-метокси-17α- (метоксиметил)эстра-4,9-диен-3-он.
и множество других соединений, имеющих конкурентную активность антагонистов прогестерона, и которые хорошо известны профессионалам.
Простагландины сульпростон (PGE2) или гемепрост могут быть использованы как пример.
Наиболее предпочтительными представителями цитокинов являются интерлейкин-8 или интерлейкин-1β.
Использование не ограничено вышеприведенными соединениями.
Ингибитор (б) оксида азота может быть также использован в комбинации с (ii) по меньшей мере одним прогрестином и/или ингибитором циклооксигеназы (например, ингибиторами СОХ-1 и СОХ-2).
В качестве прогрестинов предпочтительно применяют пригодный прогестерон, а также возможно использование одного или нескольких известных синтезированных прогестинов в качестве пероральных контрацептивов, например левоноргестрел, ципротеронацетат, гестоден, дроспиренон, дезогестрел, 3-кетодезогестрел, диеногест и т.д.
Ингибитором циклооксигеназы может быть, например, аспирин (ингибитор СОХ-1 и СОХ-2). Другие примеры ингибиторов СОХ-2 могут быть взяты из: Роберт Асланян, Николас 1, Карузерс, Джеймс Дж. Камински; циклооксигены 2: A Novel Target for Terapeutic Intervention, Exp. Opin.Invest.Drugs, 1994 3(12), 1323-1325, например соединения SС-58125 (GD Searle)/ DuP-697, флузолид [6-(2,4-дифторфенокси)-5-метилсульфониламино-1-инданон] , Sc-57666 (GD Searle) L-745337 (Merck Frosst), N-398 (Monsanto).
В первом аспекте изобретение относится к применению соединений изобретения (а) при рождении или абортах. При беременности шейка матки обрабатывается предварительно. Гормоны в течение беременности изменяют шейку матки, которая затем предрасположена отвечать эффективно на другие стимуляторы.
Далее изобретение относится к применению соединений (а) при хирургическом вмешательстве или диагностической процедуре. Следовательно, соединения (а) изобретения могут, возможно в комбинации с соединениями, указанными как (i), быть использованы для производства лекарственных средств, применяемых для:
А) вызывания родов в конце срока (время ожидаемого рождения при нормальном протекании беременности (препарат) можно комбинировать с последующей обработкой окситоцином или подобными средствами).
Б) вызывания родов в связи с патологической беременностью (например, порок развития плода; предпочтительно аборт во второй трехмесячный срок).
В) вызывания родов в связи с внутриматочной гибелью плода.
Г) при абортах (предпочтительно аборт в первый трехмесячный срок).
Д) вызывания преждевременных родов.
Е) при продолжительных родах вследствие дистоции, относящейся к шейке патологии.
Ж) вызывания созревания шейки матки небеременной женщины или беременой женщины при хирургической или диагностической процедуре и
З) вызывания созревания шейки матки у женщины, подвергнутой искусственному оплодотворению.
Во втором аспекте (б) изобретение относится к применению соединений изобретения в случаях, когда требуется предотвращение слишком раннего созревания шейки матки или где шейка должна поддерживаться жесткой. Следовательно, соединения (б) изобретения могут, возможно в комбинации с соединениями (ii), быть использованы для получения лекарственных средств для:
И) лечения шеечной недостаточности (шеечная функциональная недостаточность) и
К) лечения угрозы преждевременных родов.
В основном соединения могут быть применимы для женщин и самок животных. Человеческие особи являются предпочтительной группой для такого лечения.
Донор и/или субстрат оксида азота (а) или ингибитор оксида азота (б) могут быть введены любым путем, в котором, прямо или косвенно, он будет доходить до шейки. Следовательно, он обычно применяется интравагинально на шейку, то есть обычно как гель или крем. Он также может быть инъецирован в ткань шейки или тупой иглой в канал шейки. Он также может быть нанесен экстраамниотически, то есть между стенкой матки и амниотическим мешком, используя катетер.
Предпочтительной формой является гель или крем, но он также может быть нанесен в виде размягчающихся капсул, липосом или в составах замедленного выделения или в качестве водного раствора, например, физиологического или белоксодержащего раствора. Лекарственное средство может быть получено известными методами.
При комбинированном применении соединений, указанных выше как (а) и (i) антипрогестин может быть введен в композицию для системного или местного введения. Простагландин, как и цитокин, предпочтительно вводят в композицию для местного введения.
При комбинированном применении соединений, указанных выше как (б) и (ii), соединения (ii) могут быть введены в состав для системного и местного введения.
Композиции, включающие соединения (i) и (ii) получают известными методами.
Соединения (а) изобретения проявляют фармакологическую активность, вызывая созревание шейки матки и, следовательно, могут быть использованы в качестве лекарственных средств.
Соединения (б) изобретения проявляют фармакологическую активность, предотвращая созревание шейки матки и, следовательно, могут быть использованы в качестве лекарственных средств.
Измерение созревания шейки матки описано в примере 1.
Нитропруссид натрия и другие доноры влияют на созревание шейки матки при концентрации от примерно 0,03 мМ - 100 мМ (1,8 мкг - 6 мг/применение) при локальном введении беременным самкам морских свинок. В случаях, указанных ранее от (А) до (З), соответствующая дозировка будет изменяться в зависимости от, например, использованного соединения изобретения, хозяина, способа введения и природы и тяжести состояния. В общем, удовлетворительные результаты на животных, как показано, получены при концентрации от примерно 0,03-100 мМ для местного применения, предпочтительно при концентрации примерно 10 мМ.
Соединения изобретения могут быть введены за 6-48 часов до конечного созревания шейки матки. Следующие за созреванием роды могут быть вызваны введением окситоцитного соединения. Соединения можно вводить в одной или больше дозах, вводимых последовательно с разницей в несколько часов или один день. Соединения изобретения могут быть введены любым обычным путем, особенно в форме геля, мази или местной инъекции (при концентрации примерно 0,03-100 мМ).
Нитропруссид натрия и другие доноры оксида азота оказывают действие на созревание шейки матки при концентрации от примерно 0,03 мМ - 100 мМ (1,8 мкг - 6 мг/применение) при введении небеременным самкам морских свинок. В случаях, указанных ранее от (Ж) до (З), соответствующая дозировка будет изменяться в зависимости от, например, использованного соединения изобретения, хозяина, способа введения и природы и тяжести состояния. Однако, в общем, удовлетворительные результаты на животных, как показано, получены при концентрации от примерно 0,03 мМ - 100 мМ (1,8 мкг - 6 мг/применение) предпочтительно при концентрации примерно 10 мМ. Соединения изобретения могут быть введены за 24 или 48 часов до окончательного созревания шейки матки. Соединения можно вводить в одной или больше дозах, вводимых последовательно с разницей в несколько часов или один день. Соединения изобретения могут быть введены любым обычным путем, особенно в форме геля, мази или местной инъекции.
Примерами интервалов дозировки для человека типичных NO-субстратов и NO-доноров являются:
L-Аргинин - 500 мг - 10 г/день
Нитропруссид натрия - интервал 500 - 2000 мкг/кг/день
Нитроглицерин - 0,5 - 10 мг/день
Изосорбидмононитрат - 10 - 100 мг/день
Изосорбиддинитрат - 10 - 100 мг/день
Другие доноры и субстраты NО используют в биоэквивалентных количествах.
Примерами интервалов дозировки типичных NО-ингибиторов являются:
L-NAME - 1 - 50 мг/кг/день
L-NIO - 1 - 50 мг/кг/день
L-NА - 1 - 50 мг/кг/день
L-MMA - 1 - 50 мг/кг/день
L-NG - 1 - 50 мг/кг/день
L-NMA - 1 - 50 мг/кг/день
Аминогуанидин - 0,1 - 100 мг/кг/день
Другие ПО-ингибиторы используются в биологически эквивалентных количествах.
Интервал дозировки Р 486: 25-600 мг/день на унцию. Другие антипрогрестины используются в биологически эквивалентных количествах.
Дозировочный интервал для сульпростона: 100-1000 мкг/день внутримышечно или внутривенно. Другие простагландины, такие как РСЕ2 используются в биологически эквивалентных количествах. Простагландины также можно использовать внутришеечно в виде геля внутривагинально в форме геля или таблеток.
Дозировочный интервал для ингибиторов СОХ-2: 0,1-100 мг/кг/день.
Дозировочный интервал для 1L - 8: 100 нг - 500 мкг/день;
дозировочный интервал для 1L - 1β: 100 нг - 500 мкг/день.
Биологически эквивалентные количества других соединений, отличных от указанных выше, могут быть определены методами, изложенными в примерах, как количества, которые приводят к аналогичным эффектам в шейке матки, что и раскрытые количества при аналогичных условиях.
Результаты изобретения отражены на чертежах, на которых:
Фиг. 1 показывает эффект нитропруссида натрия на созревание шейки матки у беременных морских свинок. Животных обрабатывают как описано в Примере 1. Верхняя панель показывает начальное расширение (в мм) во время измерения растяжения; нижняя панель демонстрирует влияние на растяжение (наклон кривой регрессии). Данные представлены в виде диаграмм.
Вертикальные линии представляют интервал от минимального до максимального количества. Высота столбца, горизонтальная линия и звездочка соответствуют межквартильному интервалу, серединному и среднему значению соответственно.
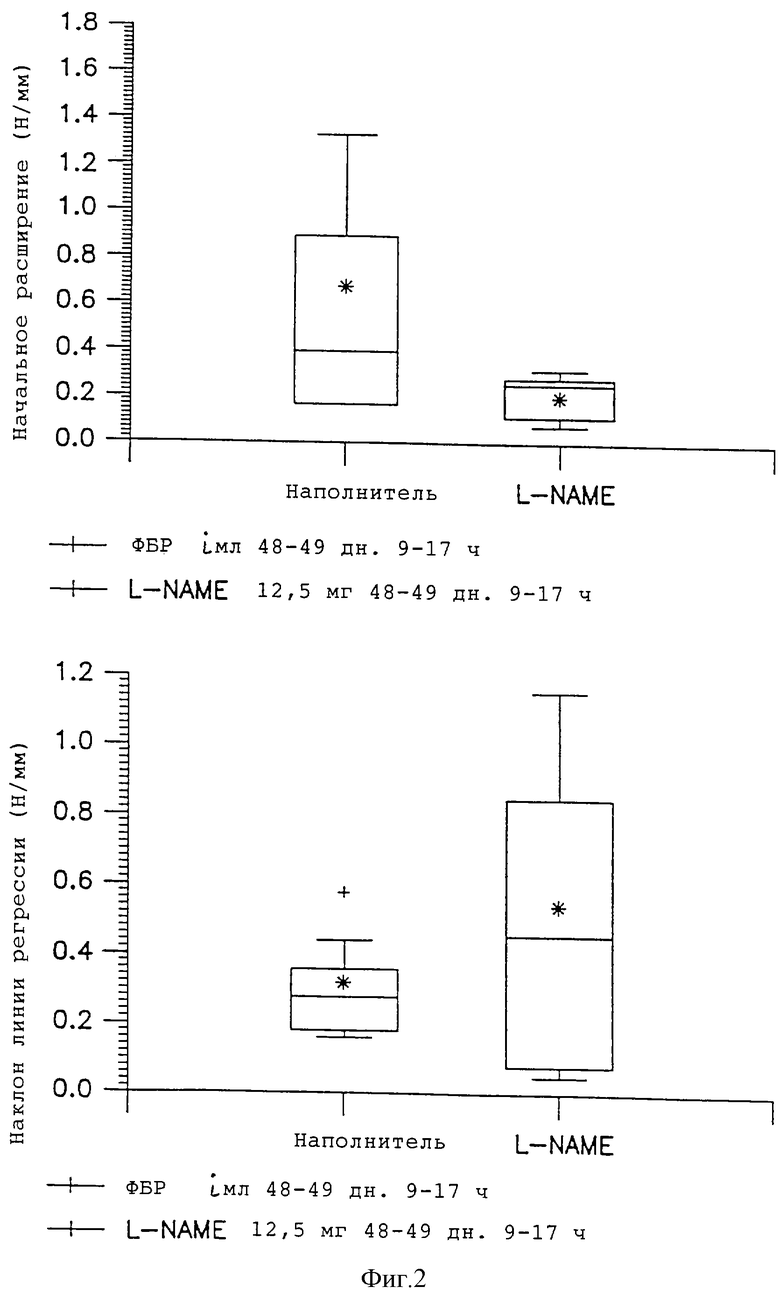
Фиг. 2 показывает влияние L-NАМЕ на шейку матки у беременных морских свинок. Верхняя панель показывает начальное расширение (в мм) во время измерения растяжения; нижняя панель демонстрирует влияние на растяжение (наклон кривой регрессии (N/мм)). Данные представлены в виде диаграммы, как описано для фиг. 1.
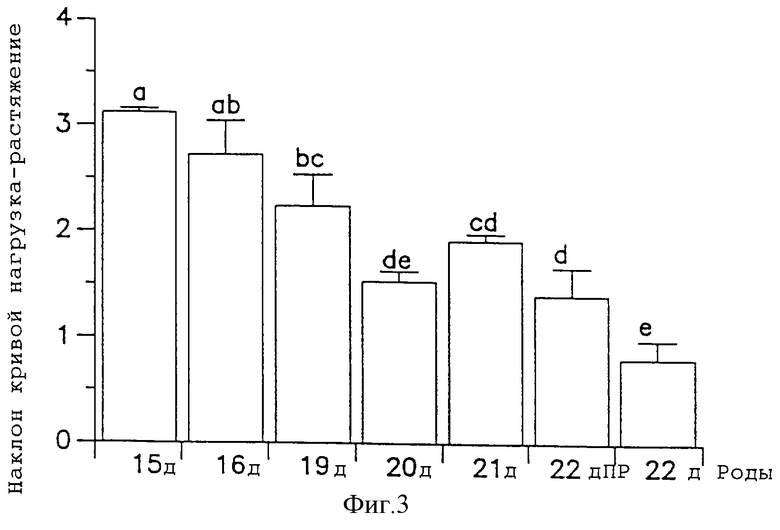
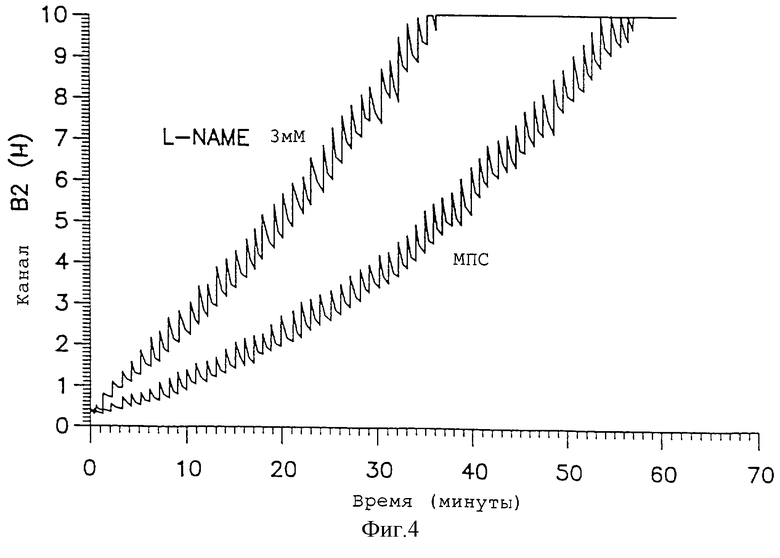
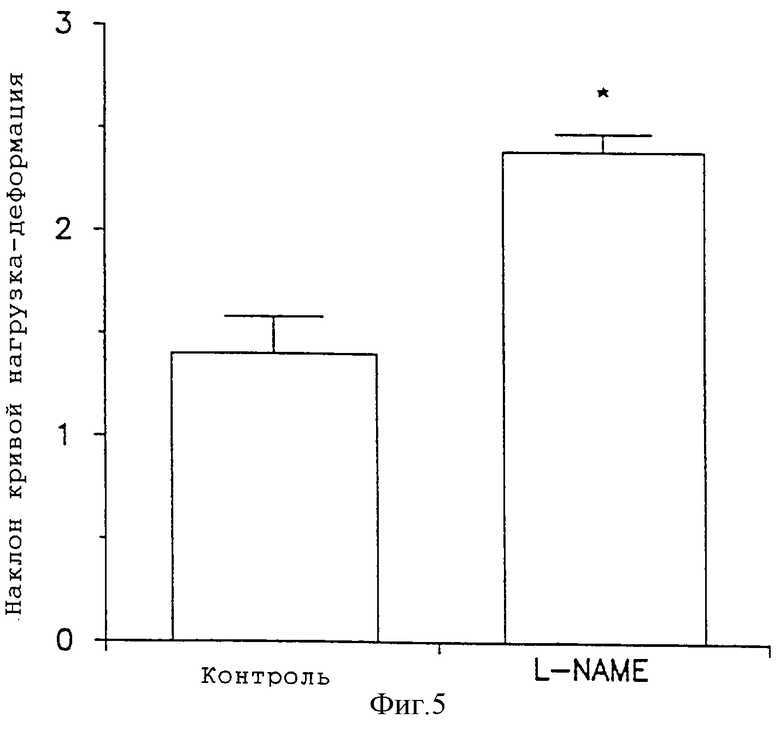
Фиг. 3-5 показывают растяжимость шейки матки крыс после обработки L-NAME (50 мг/крысу) и без обработки. Фиг. 3 показывает растяжимость шейки матки при беременности у крыс (значения с по меньшей мере одним общим верхним индексом не различаются при величине p<0,05 (n=4 в каждой группе), статистический анализ: повторный дисперсионный анализ ANOVA с последующими множественными сравнениями, использующими критерии наименьших значимых различий Фишера). Фиг. 4 показывает растяжимость матки (инкубация in vitro) с L-NAME 3 мМ). Фиг. 5 показывает растяжимость шейки матки после инкубации с L-NAME 3 мМ in vitro (значения различаются при величине p<0,005 (n=6 в каждой группе), статистический анализ: первый t-тест).
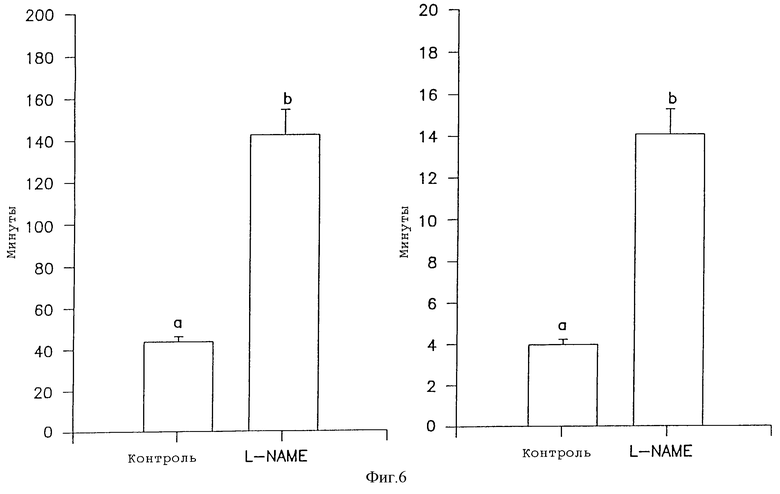
Фиг. 6 показывает эффекты L-NАМЕ (50 мг/день) на роды крыс (значения с различными верхними индексами различаются при величине p<0,01 (двусторонний Т-тест), n= 10 в каждой группе), то есть увеличение в длительности родов и интервале появления детенышей (время между рождением детенышей при обработке L-NAME).
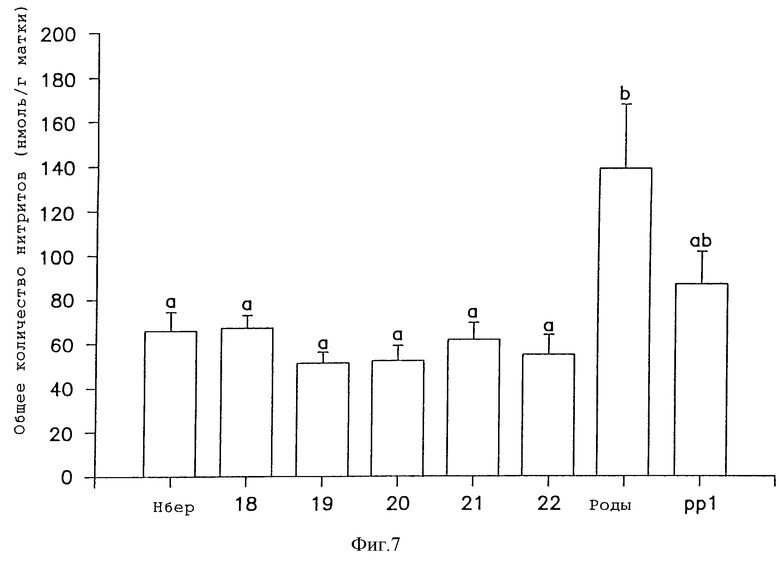
Фиг. 7-9 показывают выработку NО во время нормального расширения шейки матки после прогестерона
после прогестерона  антипрогестина
антипрогестина  и
и  Фиг. 7 показывает уровни нитрит + нитрат в шейке матки крыс в течение беременности (значения с по меньшей мере одним общим верхним индексом не различаются при величине p<0,05 (n=5-9), статистический анализ: повторный дисперсионный анализ ANOVA с последующими множественными сравнениями, использующими критерии наименьших значимых различий Фишера).
Фиг. 7 показывает уровни нитрит + нитрат в шейке матки крыс в течение беременности (значения с по меньшей мере одним общим верхним индексом не различаются при величине p<0,05 (n=5-9), статистический анализ: повторный дисперсионный анализ ANOVA с последующими множественными сравнениями, использующими критерии наименьших значимых различий Фишера).
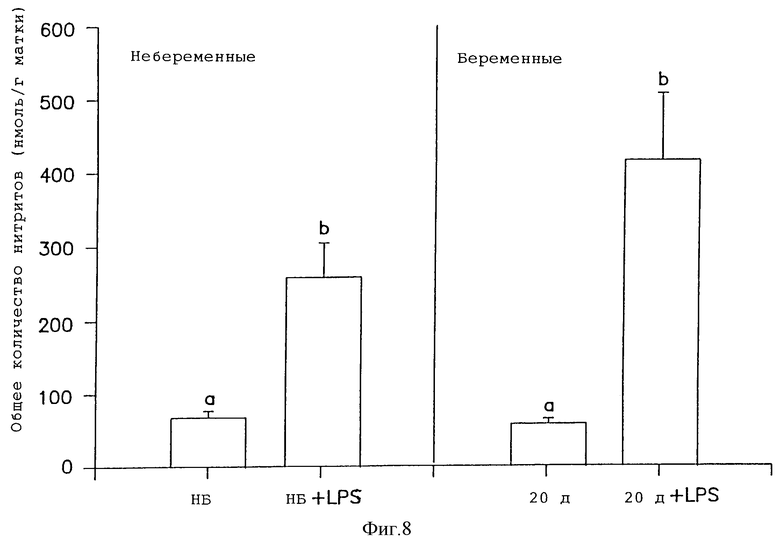
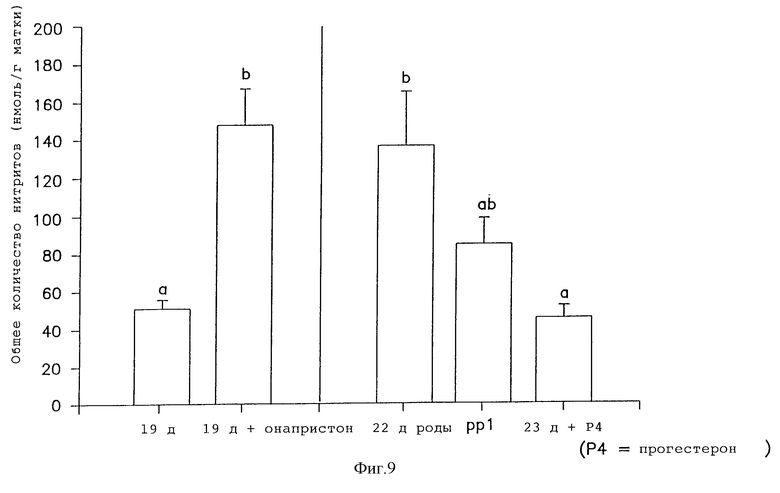
Фиг. 8 показывает уровни нитрит + нитрат в шейке матки крыс при обработке прогестероном или антипрогестином онаристом (значения с по меньшей мере одним общим верхним индексом не различаются при величине p<0,05 (n=5), статистический анализ: повторный дисперсионный анализ АNОVА с последующими множественными сравнениями, использующими критерии наименьших значимых различий Фишера).
Фиг. 9 показывает уровни нитрит + нитрат в шейке матки крыс при обработке LPS (значения с по меньшей мере одним общим верхним индексом не различаются при величине p<0,05 (n=5), статистический анализ: повторный дисперсионный анализ ANOVA с последующими множественными сравнениями, использующими критерии наименьших значимых различий Фишера).
ПРИМЕР 1
Влияние оксида азота на созревание шейки матки у беременных морских свинок
а) Общая часть
Измерение созревания
Целые шейки матки получали из морских свинок на 44 день после коитуса. Растяжимость изучали модифицированным методом, описанным в публикации Доунинга и Шервуда (1985) Endocrinology 116: 1215-1220. Отделение шейки матки растягивали между двумя крюками, продетыми через каждый канал шейки. Один крюк закоплялся, а другой двигался с частотой отбора проб 1 Гц вверх, в то время как измерялась сила и смещение. Первую шейку матки растягивали до достижения силы 50 нМ. Связанное с этим смещение записывалось и было названо начальным расширением. Следовательно, природная внутренняя окружность шейки матки есть удвоенное начальное расширение.
После чего шейку матки растягивали движением крюка на 0,1 мм, затем крюк фиксировали и шейке позволяли расслабляться 2 минуты. Эту процедуру повторяли до разрыва шейки или по меньшей мере до достижения точки выхода, то есть огибающая линия нагрузки в зависимости от времени становилась нелинейной (смотри публикацию Конрад и Уеланд (1979) Am. J. Obstet, Gynecol.).
б) Анализ
Для определения растяжимости шейки матки изучалась кривая зависимости силы от отношения удлинения. Эту кривую получали, исходя из максимальной силы на каждой стадии растяжения и связанного с ней отношения удлинения, которое определяли как смещение относительно начального расширения. Наклон линии регрессии по линейной части кривой принимался как количественный эффект обработки растяжимости шейки. Уменьшение наклона представляет увеличение растяжимости шейки (эффект созревания).
в) Специальная часть
Беременные морские свинки, которые имели 42 дня после коитуса (n=6 животных в группе) обрабатывались на 42 и 43 день внутришеечно дважды в день (в 9 утра и 17 вечера) 200 мкл геля (3% гидроксицеллюлоза), содержащего 0,03 мМ нитропруссида натрия. Измерение растяжимости матки (параметры: наклон линии регрессии, начальное расширение) проводились на 44 день после коитуса.
После введения зеркала во влагалище через 100 мм тупую иглу в канал матки инъецировали 200 мкл целлюлозного геля, содержащего или не содержащего нитропруссид натрия. Часть геля проходила по каналу, располагаясь вокруг унциевого интернума шейки матки. Состав геля: гель содержит соединения изобретения в фосфатном буферном физиологическом растворе (ФБР) (смотри Хадсон и Хэй (1980) Practical Immunology, Oxford, sec. edition) с 3% (масса/объем) гидроксиэтилцеллюлозы. Контрольная группа получила гель, содержащий 3% (масса/объем) гидроксиэтилцеллюлозы в ФБР.
Механические свойства шейки измеряли по методу, описанному выше, который позволил дать количественное представление о растяжении шейки и расширении шейки матки в изометрических условиях.
г) Результаты примера 1 показаны на фиг. 1. Верхняя панель показывает наклоны линии регрессии, которая является параметром растяжимости шейки матки. Нижняя панель показывает начальное расширение шейки матки в мм. Результаты показывают, что NO донор нитропруссид натрия (SNP) после локального введения значительно увеличивает созревание шейки матки у беременных морских свинок.
ПРИМЕР 2
Влияние нитропруссида натрия (SNP) на морфологию шейки матки у беременных морских свинок
SNP (0,1 М) вводили внутришеечно с 0,2 мл буфера ФБР, содержащего 3% гидроксицеллюлозы, дважды в день на 42-43 день после коитуса, а влияния были оценены на 44 день после коитуса морфологической оценкой. Контрольные животные были обработаны наполнителем. Все шейки матки, использованные для морфологической оценки, получали после фиксации in situ методом сосудистой перфузии. Процедуру перфузии выполняли на 50 день после коитуса между 9 и 10 часами утра под анестезией 1,5 мл пентабарбитала внутримышечно (60 мг/мл). Канюля была имплантирована в абдоминальную аорту ниже разветвления почечной артерии; перфузию животным выполняли какодилатным буфером, pH 7,4 в течение 60-90 секунд с последующей фиксацией 2,5% глутаральдегидом в какодилатном буфере pH 7,4 в течение 6-10 минут при давлении 80-100 см водного столба. Шейки матки иссекали и отделяли от соседних тканей, затем фиксировали при 4oС в том же фиксаторе. После буферной промывки материал фиксировали 2 часа в холодном какодилатном буфере, содержащем 1% OSO4, дегидратировали качественной серией этанола и погружали в эпоксидную смолу Аральдит. Отрезали от каждого образца поперечные тонкие исследовательские срезы 1-2 мкм толщиной и окрашивали 1% толуидина синего в борате натрия для изучения метода световой микроскопии. Это дало возможность изучить целую шейку матки, тем самым обеспечивая обзор распределения различных популяций клеток в шейке матки. После чего отрезали маленькие образцы (1-2 мм3) от поперечного блока шейки матки и готовят ультратонкие срезы стеклянным или бриллиантовым ножом на микротоме Райхерт Ом U3 и помещают на однощелевые медные опорные решетки, покрытые Формваром. Окрашивали ацетатом уранила и ацетатом свинца и изучали на электронном микроскопе Цейсс ЕМ при 60-80 кВ. Изучение электронной микроскопией показало явное созревание шейки матки, сопровождаемое растворением коллагеновых волокон, стромальными отеками, расширением артерий и инфильтрацией макрофагов, лимфоцитов и гранулоцитов. Присутствуют также многочисленные мастоциты. Морфологические эффекты SНР были похожи на эффекты, наблюдаемые в течение нормального созревания шейки матки перед родами или после обработки антипрогестином онапристон или цитокином IL-8.
ПРИМЕР 3
Влияние L-NAME на шейку матки у беременных морских свинок
Беременные морские свинки были обработаны L-NAME (12,5 мг/день/животное, подкожно) на 48 и 49 день после коитуса. Растяжение и расширение шейки матки измеряли на 50 день после коитуса, т.е. через два дня после начала обработки. Измерение проводили как описано в Примере 1. Результаты Примера 3 показаны на фиг. 2. Как начальное расширение, так и растяжимость шейки (увеличение наклона) уменьшались по сравнению с контрольной группой.
ПРИМЕР 4
Влияние L-NАМЕ на роды у беременных морских свинок
Осмотический мининасос, содержащий L-NAME (группа 1: 7 мг, группа 2: 12,5 мг и группа 3: 25 мг/животное/день), имплантировали подкожно на 50 день после коитуса (роды = 67+2 дня после коитуса). Контрольная группа была обработана наполнителем.
Все животные (5/5) из группы 3 и 3/5 из группы 2 рожали преждевременно (до 65 дня после коитуса) в пределах 8 дней после обработки. Исследования показали, что L-NAME вызывает преждевременные роды у морских свинок путем активации сокращений матки. Однако у животных, обработанных L-NAME, наблюдались продолжительные роды, длящиеся несколько часов. Это наблюдение является непрямым указанием на недостаточное созревание шейки матки, которое было показано в отдельном эксперименте, выполненном на 50 день после коитуса, с использованием измерения растяжимости шейки матки (фиг. 2).
ПРИМЕР 5
Влияние L-NAME на роды у крыс
Фиг. 6, которая базируется на эксперименте, подобном описанному в Примере 4, показывает, что в течение обработки L-NAME (50 мг/день) беременных крыс длительность родов и интервал появления детенышей, который является временем между рождением отдельных детенышей, заметно увеличиваются. Это ясно показывает, что ингибиторы оксида азота предотвращают созревание шейки матки у крыс.
ПРИМЕР 6
Выработка оксида азота у крыс в течение нормального расширения шейки матки, после обработки прогестероном, антипрогестином и LPS
а) Метод
Активность генерирования оксида азота, измеренную как общее количество накопленного нитрита в тканях шейки и матки, оценивали по методу, описанному в: Ялампалли, Гарфилд, Байэм-Смит (1993): Оксид азота ингибирует сократительную способность матки во время беременности, но не во время родов, Endocrinology 133: 1899-1902. Вкратце, маленькие кусочки тканей шейки или матки получали из рожающих крыс (22-23 день беременности), обрабатывали онапристоном (10 мг на 18 день после коитуса подкожно) и наполнителем на 18-21 день после коитуса (контроль) и инкубировали в минимальной поддерживающей среде (МПС) с L-аргинином с или без L-NAME 24 часа при 37oС. Среду анализировали на общее количество нитритов с помощью реактива Гриесса.
(б) Результаты
Выработка нитрита в маточной ткани (миомитрий): выработка значительно падает в образцах матки, полученных из рожающих животных по сравнению с 18 днем беременности (Яллампилли и др. ссылка цитирована). Выработка нитрита в ткани шейки матки (фиг. 7): имеется значительное увеличение выработки NO в шейке матки, полученной от рожающих животных, по сравнению с беременными крысами на 18-22 день после коитуса. Влияние онапристона на выработку NO в шейке матки (фиг. 8): имеется значительное увеличение выработки NO в шейке по сравнению с контрольной группой на 19 день после коитуса до уровней, отмеченных для самопроизвольно рожающих животных.
ПРИМЕР 7
Предварительное вызывание созревания шейки матки донором оксида азота
Беременной женщине (около 30 лет, 50-80 кг) на 38 неделе беременности, которой было назначено вызывание родов из-за преэклампсии, ввели нитропруссид натрия в концентрации 0,01-0,1 мМ в геле внутришеечно дважды в день, чтобы достичь созревания шейки матки. Вызывание родов было выполнено на следующий день, используя вливание окситоцина внутривенно.
ПРИМЕР 8
Лечение недостаточности шейки матки местным применением L-NАМЕ
Беременной женщине (около 30 лет, 50-80 кг) на 26 неделе беременности, показывающей признаки недостаточности шейки матки (расширение шейки матки, размягчение шейки матки) вводили L-NAME в геле внутришеечно или внутривагинально в концентрации 0,1-50 мг/мл по 2-3 дозы в день до улучшения симптомов недостаточности шейки матки.
Изобретение относится к медицине. Предложено новое средство для регуляции расширения и/или растяжения шейки матки. В качестве такого средства применяют доноры и/или субстраты окиси азота (ими могут служить, например, L-аргинин, нитропруссид натрия, нитроглицерин, глицерилтринитрат, изосорбидмононитрат, изосорбиддинитрат или SIN-1). Изобретение расширяет арсенал средств для снижения симптомов недостаточности шейки матки. 9 ил.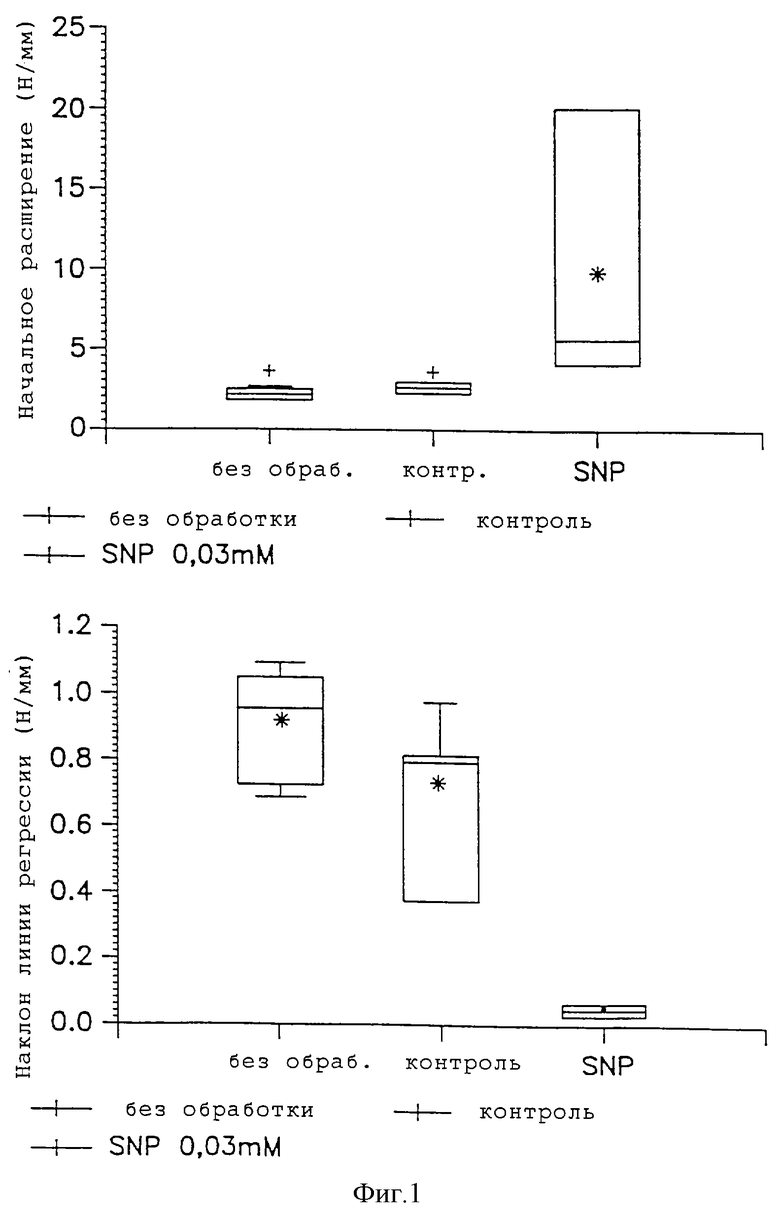
Применение доноров и/или субстратов окиси азота для производства фармацевтической композиции для регуляции расширения и/или растяжения шейки матки.
| ШУЕВ Б.В | |||
| и др | |||
| Аспирин как ингибитор циклоксигеназы при некоторых осложнениях гестационного периода | |||
| - Акушерство и гинекология, 1992, №3-7, с.10-14 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
Авторы
Даты
2003-02-27—Публикация
1996-03-14—Подача