Изобретение относится к области медицины, а именно к хирургии.
Острый холецистит за последние десятилетия приобрел характер социальной проблемы, причем 34 - 40% от общего числа больных, поступающих в лечебные учреждения с данной патологией, составляют люди пожилого и старческого возраста [1].
Согласно современным представлениям, в патогенезе острого холецистита у данной категории больных, кроме острой обтурации пузырного протока, приводящей к резкому повышению внутрипузырного давления и перерастяжению стенки желчного пузыря, большое значение придается сосудистому фактору [2].
Нарушение гемоциркуляции в стенке желчного пузыря в связи со склерозом и тромбозом сосудов является причиной быстрого (в течение нескольких часов с момента заболевания) развития деструктивных форм острого холецистита [3, 4].
Однако у больных старше 60 лет, несмотря на большой процент деструктивных форм, бурное течение заболевания с выраженной клинической картиной со стороны брюшной полости или отсутствует, или продолжается недолго, т.е. патоморфологические изменения не успевают реализоваться в симптомы. После чего на первый план в развитии острого холецистита выступают явления интоксикации на фоне имеющихся возрастных изменений и сопутствующей патологии [5, 1]. Таким образом, операция, предпринятая по "изменению клинической картины" со стороны брюшной полости, оказывается запоздалой. Вследствие этого послеоперационная летальность остается стабильно высокой, составляя более 20% [1].
В свете изложенного становится понятной значимость дополнительных инструментальных методов диагностики блока пузырного протока.
В настоящее время наибольшее распространение нашли следующие способы диагностики:
1. Ультразвуковое исследование (УЗИ). Принцип работы диагностических приборов заключается в следующем: объект подвергают воздействию направленного ультразвукового луча и регистрируют эхосигналы, отраженные от границы двух сред с различной акустической плотностью [6]. Простота, безопасность, возможность обследования больного неограниченное число раз, независимо от тяжести его состояния делает ультразвуковое исследование незаменимым в диагностике острого холецистита.
2. Дуоденальное зондирование [1, 7]. Предложено в 1919 году. Выделяют три порции желчи: "А" - содержимое двенадцатиперстной кишки (золотисто-желтая жидкость), "В" - пузырная желчь (темно-оливкового цвета, тягучая жидкость), "С" - печеночная желчь (менее тягучая, прозрачная, золотистая жидкость). Для стимуляции пузырного рефлюкса вводят через зонд в двенадцатиперстную кишку магния сульфат. Отсутствие порции "В" указывает на блок пузырного протока.
3. Проба D. Febres. Для более четкого определения пузырной желчи D. Febres (1942)[8] предложил пробу с метиленовой синью. Он установил, что метиленовая синь, введенная внутрь (в капсулах), выводится частично печенью, частично почками. При выделении из печени она превращается в бесцветное лейкооснование, которое в желчном пузыре вновь превращается в хромоген и окрашивает пузырную желчь в сине-зеленый цвет, в то время как желчь порций "А" и "С", содержащих лейкооснование, окрашена в обычный цвет. Интенсивность окраски зависит от концентрирующей способности слизистой желчного пузыря, а также от рН желчи, снижение последней способствует окислению красителя и окрашиванию желчи. Сдвиг рН желчи в кислую сторону свидетельствует о воспалительном процессе в желчном пузыре. У больных острым калькулезным холециститом рН пузырной желчи составляет в среднем 5,3 по сравнению с 6,9 в контрольной группе [9].
Таким образом, применяя пробу D. Febres при дуоденальном зондировании, легко отличить одну порцию от другой, так как только пузырная желчь бывает окрашена в сине-зеленый (малахитовый) цвет.
4. Ускоренное хроматическое дуоденальное зондирование [10]. Представляет собой сочетание дуоденального зондирования и пробы D. Febres. При выполнении данного исследования применяется 0,4% раствор индигокармина внутривенно вместо метиленовой сини, что дает аналогичный эффект. Больному вводят зонд в двенадцатиперстную кишку, а затем внутривенно 5 мл 0,4% раствора индигокармина. Для стимуляции пузырного рефлюкса используется 40-50 мл 25% раствора сернокислой магнезии. Окрашивание пузырной желчи, полученное при зондировании, исключало острый холецистит, поскольку указывало на проходимость пузырного протока.
Перечисленные виды исследований не лишены ряда недостатков.
При ультразвуковом исследовании информативность в диагностике острого холецистита достигает 92-98% [11, 12]. В некоторых случаях возможны как ложноположительные, так и ложноотрицательные результаты. Причина их очевидно в наличии загазованности кишечника (рефлекторный парез желудочно-кишечного тракта) и, в связи с этим, невозможность четкой визуализации желчного пузыря.
Различные виды дуоденальных исследований также не лишены недостатков. При дуоденальном зондировании трудно судить о проходимости пузырного протока, так как разница в цвете между пузырной и печеночной желчью - довольно субъективный критерий. Проба D. Febres позволяет более достоверно определить пузырную желчь, однако ввиду того, что метиленовая синь вводится per os, информативность метода снижается при наличии заболеваний желудочно-кишечного тракта.
Ускоренное хроматическое дуоденальное зондирование имеет свои отрицательные моменты. К ним следует отнести: 1. Трудности, а порой невозможность проведения дуоденального зондирования у больных острым холециститом в связи с частой рвотой, двигательным беспокойством, дуоденостазом, с забросом содержимого двенадцатиперстной кишки в желудок. Неудачи, по нашим данным, составляют 60%. 2. Продолжительность процедуры зондирования. 3. Отсутствие достоверных критериев нахождения зонда в двенадцатиперстной кишке. 4. Отсутствие окрашенной желчи при использовании данной методики не всегда указывает на блокаду пузырного протока - возможны случаи непроходимости холедоха.
Прототипом предлагаемого нами исследования является хромодуоденоскопия (ХДС) - визуальное наблюдение за выделением краски из большого соска двенадцатиперстной кишки (БСДК) при помощи дуоденоскопа [13]. ХДС, как и ускоренное хроматическое дуоденальное зондирование, основано на пробе D. Febres.
Методика заключается в следующем: 1) подготовка - натощак и при необходимости в случае экстренной ХДС промывание желудка; 2) премедикация - за 30 минут до исследования введение промедола, атропина сульфата, димедрола и при необходимости аэрон под язык; 3) внутривенное введение 5 мл 0,4% раствора индигокармина за 10-15 минут до исследования; 4) введение эндоскопа под местной анестезией 2% раствором дикаина; 5) осмотр пищевода, желудка, двенадцатиперстной кишки и БСДК. Авторы не вызывали пузырный рефлюкс с помощью магния сульфата. По интенсивности окраски выделенной желчи и красителя можно, по мнению авторов, с достоверностью судить о функции желчного пузыря, степени обструкции пузырного протока, наличии дилятации холедоха и нарушении моторики желчных путей. По длительности интервала между периодами сокращения сфинктера Одди судят о его функциональных и органических изменениях. При нарушении моторики желчных путей и дилятации холедоха функционального характера интервал между выбросами окрашенной желчи увеличивается по сравнению с нормой в 2-3 раза.
Описанный метод имеет ряд недостатков: 1. Препараты, применяемые для премедикации (промедол, атропина сульфат, димедрол), влияют на сократительную способность желчного пузыря и сфинктерного аппарата [14], что может привести к артефактам. 2. Не производится стимуляция пузырного рефлюкса, что не позволяет достоверно судить о проходимости пузырного протока. 3. О функции желчного пузыря, степени обструкции пузырного протока судят по интенсивности окраски желчи, что является субъективным критерием. 4. Не приводятся четкие временные критерии выделения окрашенной пузырной желчи, ибо не всегда окрашенная желчь является пузырной.
Наряду с проблемой диагностики острого холецистита у лиц с атипичной или бессимптомной клинической картиной, остается актуальной выбор способа хирургического лечения.
В случае отсутствия эффекта от консервативной терапии (сохранение блока пузырного протока более 24 часов, подтвержденное данными инструментальных методов) больным показано оперативное лечение. Холецистэктомия - наиболее эффективный способ лечения острого холецистита, поскольку она одновременно устраняет и желчную гипертензию и очаг воспаления. Однако у больных пожилого и старческого возраста, имеющих тяжелые сопутствующие заболевания, радикальная операция связана с чрезмерно большим риском, поэтому им выполняются минимальные по объему вмешательства, направленные только на снятие желчной гипертензии. В настоящее время применяются следующие виды декомпрессионных вмешательств:
- лапароскопическая пункция желчного пузыря [15, 16, 17];
- пункция желчного пузыря под ультрасонографическим контролем [18, 19];
- различные виды лапароскопических холецистостомий [2]:
а) кожная холецистостомия - желчный пузырь подшивают к небольшому разрезу на коже;
б) апоневротическая холецистостомия - желчный пузырь подтягивают и подшивают к апоневрозу брюшной стенки, что способствует выполнению операции при сравнительно малоподвижном пузыре и особенно у тучных больных;
в) пункционная чреспеченочная - дренаж проводят через иглу, введенную в желчный пузырь чрескожно, чреспеченочно [20, 21, 18];
г) пункционная чреспузырная - дренаж вводят с помощью иглы в желчный пузырь через его переднюю стенку [22, 23];
- чрескожная, чреспеченочная микрохолецистостомия под ультрасонографическим контролем [24, 25, 26, 27, 18];
- транспапиллярная эндоскопическая ретроградная холецистостомия [28].
Однако указанные методы имеют различные недостатки:
- наложение пневмоперитонеума и эндотрахеальный наркоз, необходимые при выполнении лапароскопических вмешательств, небезразличны для больных с явлениями сердечно-легочной недостаточности;
- иногда происходит повреждение обеих стенок желчного пузыря, преждевременное выпадение дренажа;
- для их выполнения требуется специальная аппаратура и высокая квалификация специалистов.
Еще одним недостатком указанных методов является невозможность полного удаления конкрементов из полости пузыря, особенно вклиненных в области шейки. С целью удаления в послеоперационном периоде предпринимались попытки их химического растворения, например, хенодезоксихолевой, уродезоксихолевой кислотами, спирт эфирной смесью, метил- тертбутиловым эфиром и т.д.; физического разрушения посредством экстракорпоральной волновой литотрипсии, электрогидравлической литотрипсии [29, 30]. Указанные способы не всегда эффективны, долгосрочны и дорогостоящи.
Поэтому классическая хирургическая холецистостомия, послужившая прототипом предлагаемого варианта, продолжает использоваться [31, 2]. Брюшная полость вскрывается небольшим разрезом в правом подреберье. На дно желчного пузыря накладывается два кисетных шва на расстоянии 1 см друг от друга. После пункции, в центре первого шва выполняется разрез длиной 1,5-2 см, через который удаляются оставшаяся желчь и камни. В желчный пузырь вводится трубка диаметром 0,5-0,7 см, вокруг нее затягиваются два ранее наложенных кисетных шва. Дно пузыря подшивается к брюшине в области разреза, после чего на рану накладываются послойные швы.
Классическая хирургическая холецистостомия также не лишена недостатков:
- при ее выполнении дренаж укрепляется двумя кисетными швами, что приводит к образованию "мертвого пространства" в зоне кисетных швов, малодоступного для санации, что опасно развитием гнойно-воспалительных послеоперационных осложнений;
- после декомпрессии желчного пузыря происходит его сокращение, что приводит к натяжению швов, фиксирующих пузырь к париетальной брюшине и препятствует формированию прочного фистульного хода;
- возможно также преждевременное выпадение дренажа, подтекание желчи в свободную брюшную полость, особенно при наложении холецистостомы "на протяжении".
Однако даже при полном удалении камней, все вышеперечисленные методы лечения не могут считаться достаточно эффективными. Перенесенные приступы острого холецистита приводят к грубым морфологическим изменениям стенки желчного пузыря, особенно ее мышечного слоя, с частичной или полной утратой сократительной функции. Несмотря на то, что в пожилом возрасте вероятность камнеобразования невелика [32], застой желчи способствует присоединению инфекции и рецидиву воспалительного процесса, с развитием различных осложнений - вторичных эмпием, водянок, гнойно-желчных свищей и др. [2, 31].
Для предотвращения указанных осложнений применяется облитерация просвета желчного пузыря, превращение его в рубцовый тяж, что равносильно удалению органа. Облитерация полого органа, имеющего слизистую оболочку, наступает лишь после полного уничтожения последней (мукоклазии). Достигается это различными способами.
Одни авторы применяли электрокоагуляцию с помощью моно- или биполярного электрода под контролем холедохо- или гистероскопов [33, 34]. В экспериментах на кроликах установлено, что наиболее эффективная и малотравматичная коагуляция возможна при силе тока 50 мA и экспозиции 10 с [35].
С целью мукоклазии применяются и иные агенты: растворы первомура [36], таннола, йодная настойка, нашатырный спирт, водные растворы нитрата серебра, препараты на основе фенола [37], 95% раствор этилового спирта самостоятельно [38] и в сочетании с 3% раствором содиум - тетрадецил сульфата [39, 40]. Из физических факторов кроме того опробованы УФ-излучение, СО2 и ИАГ-лазеры [41, 37].
Наибольшая эффективность отмечается при применении фенола.
Фенол (карболовая кислота ) С6Н5ОН - производное ароматических углеводородов. В медицинской практике применяется при консервировании вакцин, как антисептик, входит в состав ферезола (применяется в лечении бородавок, кондилом, кератом и т. д. ), клея БФ-6. В литературе встречается информация о применении препаратов фенола с целью демукозации желчного пузыря, для облитерации "слепого мешка" при затрудненной пластике пищевода, для облитерации маточных труб и бартолиниевых желез [37].
Фенол обладает общетоксическим действием, однако экспериментально установлено [37] , что повышения концентрации фенола в крови, после обработки слизистой оболочки желчного пузыря эмульсией фенола, не происходит.
Наиболее близким по технической сущности предлагаемому варианту лечения является способ "Облитерации просвета желчного пузыря у больных с высоким операционным риском" [34].
С целью декомпрессии желчного пузыря авторами выполняется эндоскопическая холецистостомия. После санации желчного пузыря проводится его "отключение" от внепеченочных желчных протоков. С этой целью выполняется электрокоагуляция пузырного протока на протяжении около 7 мм и прилежащей к нему части шейки желчного пузыря. Если желчеистечение по холецистостоме прекращалось, а при контрольной фистулографии внутри- и внепеченочные протоки не контрастировались, то выполняется химическая мукоклазия желчного пузыря 60% эмульсией фенола. После 6-минутной экспозиции фенол аспирируется, полость пузыря промывается 0,9% раствором хлорида натрия и дренируется латексным выпускником. С целью защиты от химического ожога кожу вокруг свищевого хода покрывают пленкообразующим клеем. В случае, если после электрокоагуляции пузырного протока возобновлялось стойкое желчеистечение из свищевого хода, проводится дуоденоскопия с эндоскопической папиллосфинктеротомией, чем устраняется желчная гипертензия во вне- и внутрипеченочных протоках.
Приведенный способ лечения имеет ряд недостатков: 1. Декомпрессия желчного пузыря осуществляется посредством лапароскопической холецистостомии (невозможность полного удаления конкрементов, возможность повреждения задней стенки желчного пузыря и других органов, недостаточно надежная фиксация дренажа, отрицательное воздействие пневмоперитонеума, эндотрахеального наркоза на организм). 2. Дренирование пузыря после выполнения мукоклазии производится латексным выпускником, что затрудняет отхождение некротизированной слизистой оболочки. 3. Не приводятся параметры (сила тока, время экспозиции) безопасной электрокоагуляции. 4. С целью уменьшения желчеистечения, не используются медикаментозные препараты, направленные на снятие спазма и воспаления сфинктера Одди. 5. Недостаточной является концентрация эмульсии фенола (60%), применяемая для химической мукоклазии.
Цель изобретения - своевременная диагностика острого холецистита, основанная на объективном критерии - информации о состоянии пузырного протока и применение малоинвазивного способа хирургического лечения, направленного на снижение послеоперационных осложнений и летальности у больных с высокой степенью операционно-анестезиологического риска.
Сущность изобретения состоит в использовании для диагностики острого холецистита двух взаимодополняющих видов исследования - УЗИ и ХДС, и хирургического лечения способом модифицированной холецистостомии в сочетании с химической мукоклазией желчного пузыря (70% эмульсией фенола с экспозицией 4 минуты), позволяющего достичь полной облитерации его просвета и превращения в рубцовый тяж, что равносильно холецистэктомии.
Описание изобретения: ультразвуковое исследование применяется как первичная скрининговая процедура у больных с подозрением на острый холецистит. В ультразвуковой семиотике острого обтурационного холецистита имеется сочетание следующих основных признаков: увеличение размеров желчного пузыря более чем 90/30 мм, утолщение стенки более 3 мм, наличие фиксированных гиперэхогенных структур с акустической тенью в проекции шейки желчного пузыря.
Второй этап диагностики - предлагаемый вариант ХДС. Исследование выполняется спустя 24 часа с момента поступления больного в стационар. Учитывая, что больные острым холециститом после поступления находятся на лечебном голоде, исследование проводится натощак, и необходимости в промывании желудка перед исследованием не возникает. Премедикация перед ХДС промедолом, атропина сульфатом, димедролом не проводится. У больных с повышенным эмоциональным настроем используется седуксен 40 мг внутривенно с хорошим эффектом. Введение эндоскопа осуществляется под местной анестезией 10% раствором лидокаина через 30 минут после того, как больному вводится внутривенно 5 мл 0,4% раствора индигокармина. Оценивается состояние желудка, двенадцатиперстной кишки, БСДК, наличие косвенных признаков панкреатита и холецистита. В двенадцатиперстную кишку вводится 40 мл 25% раствора сернокислой магнезии. Далее ожидается поступление окрашенной желчи из БСДК (фиг.1) Поступление мутной желчи до появления окрашенной порции является объективным критерием наличия холангита.
При проведении ХДС имели 4 варианта результатов у больных острым холециститом:
1) отсутствие окрашенной желчи свыше 15 минут после стимуляции пузырного рефлюкса сернокислой магнезией;
2) наличие окрашенной желчи в двенадцатиперстной кишке без предшествующей стимуляции пузырного рефлюкса;
3) появление окрашенной желчи после стимуляции пузырного рефлюкса сернокислой магнезией через 1-6 минут;
4) появление окрашенной желчи из БСДК через 6-15 минут после стимуляции.
При сопоставлении полученных данных с операционными находками, установлено, что во время операций имела место обтурация пузырного протока при первом, втором и третьем результатах ХДС. Наиболее вероятная причина раннего появления окрашенной желчи - воспаление стенки холедоха, инфицирование холедохеальной желчи и вследствие этого изменение ее рН в кислую сторону, что способствует окислению лейкооснования индигокармина и окрашиванию холедохеальной желчи.
Таким образом, в данной ситуации имеет значение время с момента введения сернокислой магнезии до появления окрашенной желчи из БСДК. Клинико-экспериментальными исследованиями установлено, что пузырная желчь в норме поступает в двенадцатиперстную кишку после стимуляции пузырного рефлюкса сернокислой магнезией через 6-15 минут. Окрашенная желчь, поступающая до 6 минут, является холедохеальной.
В случае сохранения блока пузырного протока (подтвержденного данными УЗИ и ХДС), несмотря на проведенную в течение 24 часов консервативную терапию, выполняется операция. Предлагается способ холецистостомии при помощи трубки с баллоном- обтуратором, который является модификацией классической хирургической холецистостомии.
Операция выполняется под местной анестезией с нейролептанальгезией из небольшого разреза в правом подреберье. Место разреза уточняется при помощи УЗИ. После пункции пузыря, в области дна вскрывается его просвет разрезом до 1,5-2 см, через который удаляются желчь и камни. Для дренирования пузыря применяется резиновая трубка с баллоном-обтуратором из латекса на конце. Реакция окружающих тканей на резиновую трубку более выраженная, чем на полихлорвиниловую, что ускоряет формирование свищевого хода.
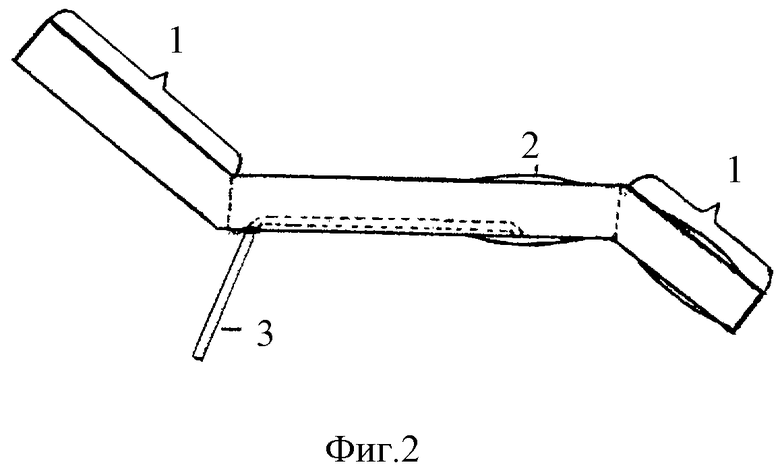
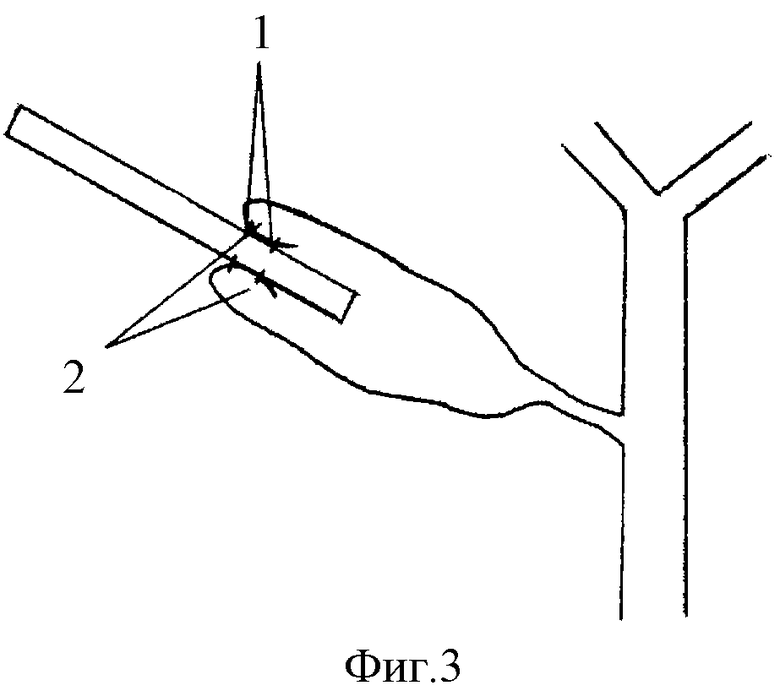
Для изготовления дренажа используются резиновые интубационные трубки отечественного производства - фиг. 2, где 1 - удаляемые части трубки, 2 - баллон-обтуратор, 3 - проводник для заполнения баллона. При фиксации подобной трубки можно ограничиться наложением одного кисетного шва, что исключает образование "мертвого пространства" - фиг. 3, где 1 - кисетные швы, 2 - "мертвое пространство" в полости желчного пузыря.
Заполняемый жидкостью баллон препятствует раннему выпадению холецистостомической трубки и, плотно прижимая дно пузыря к брюшной стенке, обеспечивает достаточный герметизм. Для заполнения баллона используется 0,9% раствор NaCl. Это позволяет в дальнейшем, зная первоначальное количество жидкости, с целью профилактики пролежней стенки желчного пузыря, периодически опорожнять баллон.
Завершается операция подведением в подпеченочное пространство страховочного дренажа через отдельный прокол в правой боковой области живота.
По ходу операции обязательно учитываются несколько моментов:
- с целью обеспечения герметизма, желчный пузырь подшивается к париетальной брюшине;
- если это выполнить невозможно, формируется холецистостома на протяжении, с обязательной фиксацией пряди большого сальника, окутывающей трубку, к париетальной брюшине и к желчному пузырю. В данном случае трубка с наполненным баллоном приобретает особую важность, являясь каркасом для формирования фистульного хода;
- трубка, вводимая в желчный пузырь, должна иметь широкий просвет (≥ 1 см) для возможного выполнения лечебной и диагностической эндоскопической холецистоскопии (контроль динамики воспалительного процесса в желчном пузыре, инструментальное удаление резидуальных конкрементов, электрокоагуляция устья пузырного протока).
В некоторых случаях возможно развитие несостоятельности холецистостомы, что чаще всего связано с чрезмерно активным поведением больного. Наличие страховочного дренажа в подпеченочном пространстве не всегда позволяет вовремя диагностировать подтекание желчи. Это связано с ограниченным временем функционирования дренажа (~24 часов).
Клинически также трудно заподозрить желчеистечение, т.к. раздражающий агент находится в непосредственной близости от операционной раны. Применение в послеоперационном периоде анальгетиков, в том числе наркотических, сглаживает перитонеальные явления. Ультрасонография на ранних стадиях желчеистечения также малоинформативна.
С целью контроля состоятельности холецистостомы применяется оригинальный способ, в основу которого положена трехкомпонентная теория цветного зрения [42] , предполагающая получать тот или иной заданный цвет трехзональным цветоделением, т.е. разделением излучения отражаемого объектом на синий, зеленый, красный диапазоны видимого спектра. При субстрактивном принципе синтеза цвета цветовоспроизведение осуществляется вычитанием (субстракцией) из белого цвета основных цветов. Последнее достигается обычно смешением на белой или прозрачной основе различных количеств красителей, цвета которых являются дополнительными к основным - соответственно желтого, пурпурного и голубого. Так смешением пурпурного и голубого красителей получают синий цвет (пурпурный цвет из белого цвета вычитает зеленый, а голубой - красный). Смешение желтого и пурпурного красителей дает красный цвет, а голубого и желтого - зеленый (за счет вычитания из белого цвета красного и синего диапазонов соответственно). Таким образом, при смешении дополнительных цветов голубого и желтого получается один из основных цветов видимого спектра - зеленый.
Имея всегда один из компонентов данной композиции - желтый цвет (желчь), в качестве второго мы остановили свой выбор на метиленовой сини. Разбавленные водные растворы последней имеют голубой цвет. Препарат относится к антисептическим средствам из группы органических тиозиновых красителей, нетоксичен, не обладает местным агрессивным действием. Применяется достаточно разбавленный раствор (до прозрачно-голубого цвета). Концентрация 0,05-0,025% достигается путем разбавления стандартного 1% водного раствора метиленовой сини физиологическим раствором под контролем зрения.
При подозрении на несостоятельность холецистостомы, желчеистечение в брюшную полость, 0,05-0,025% раствор метиленовой сини вводится в страховочный дренаж. Дренаж перекрывается на 5-10 мин. Если происходит окрашивание раствора в зеленый цвет (присутствие желчи), то в зависимости от ситуации используются дополнительные мероприятия.
Если проблем с состоятельностью холецистостомы нет, в течение 12-14 суток, до стихания воспаления желчный пузырь санируется антисептиками. При обильном желчеистечении из холецистостомы, обусловленном желчной гипертензией в результате спазма, воспалительных изменений сфинктера Одди, применяются спазмолитики, холинолитики внутримышечно, теплый 25% раствор сульфата магния или 0,5% раствор новокаина внутрь по 1 десертной ложке 10 раз в сутки.
На 12-14 сутки выполняется фистулохолеграфия. Если внутри- и внепеченочные протоки не контрастируются, при условии отсутствия камней в желчном пузыре, выполняется его химическая мукоклазия. В случае, когда блок пузырного протока обусловлен резидуальным камнем, проводится его неоперативное удаление путем химического растворения гепарином, спирт-эфирной смесью или с помощью различных инструментов. Манипуляции производятся не ранее 3-4 недель с момента операции. Этот срок необходим для формирования прочного фистульного хода, так как может возникнуть необходимость в манипулировании через свищевой ход.
В случае, когда при фистулографии контрастное вещество поступает во внутри- и внепеченочные протоки, для предупреждения попадания фенола в них, выполняется электрокоагуляция (сила тока 50 мA с экспозицией 10 с) слизистой оболочки устья пузырного протока и прилегающей к нему части шейки пузыря одно- или биполярным электродом под контролем эндоскопа. При наличии стабильного блока, подтвержденного контрольной фистулографией, выполняется мукоклазия.
После выполнения электрокоагуляции возможно возобновление желчеистечения, что обусловлено желчной гипертензией, связанной с нарушением проходимости терминального отдела холедоха (склерозирующий папиллит, аденоматоз БСДК, конкременты и др. ). В таких случаях показана эндоскопическая ретроградная панкреатохолангиография с эндоскопической папиллосфинктеротомией.
Химическая мукоклазия желчного пузыря осуществляется путем введения по трубке 70% эмульсии фенола с экспозицией 4 минуты. Установлено, что именно данная концентрация фенола позволяет добиться полной и безопасной мукоклазии. Применение как менее, так и более концентрированных препаратов фенола, с другой экспозицией приводит к частичной мукоклазии (60%) или некрозу всей стенки (95%). Эффективность воздействия определяется по оценке макроскопических изменений в желчном пузыре и при исследовании микропрепаратов, окрашенных гематоксилином и эозином и по Ван-Гизону.
После аспирации фенола полость пузыря многократно промывается 0,9% раствором хлорида натрия. С целью защиты от химического ожога, кожа вокруг холецистостомы покрывается пленкообразующим клеем или обклеивается лейкопластырем.
В дальнейшем в течение 2-3-х недель проводится санация полости желчного пузыря с введением в просвет пузыря мази "Левомеколь", ускоряющей развитие грануляционной ткани. Процесс облитерации контролируется эндоскопическим, сонографическим и рентгенологическим исследованием.
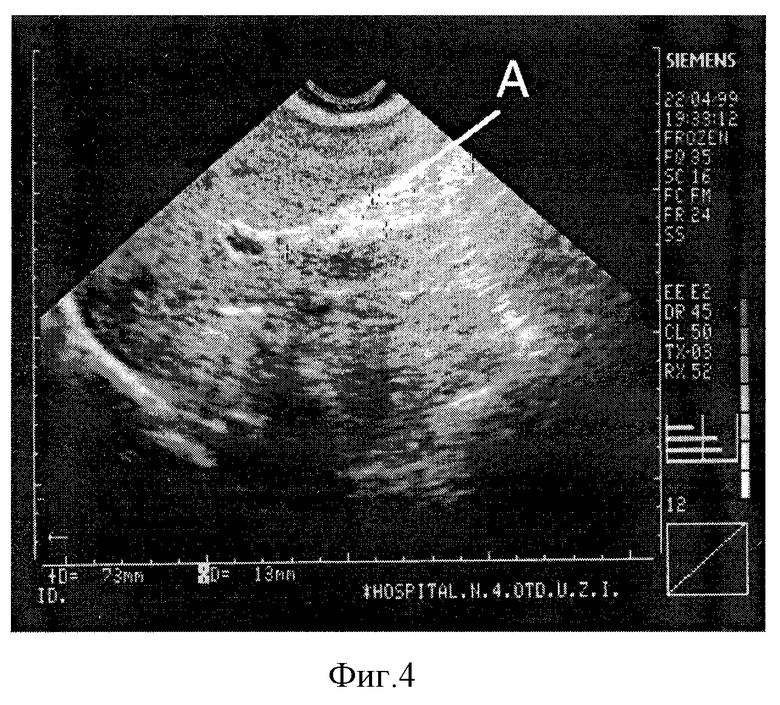
Предлагаемый комплексный способ диагностики и хирургического лечения острого холецистита у больных с высоким операционно-анестезиологическим риском, см. предлагаемую схему, был применен у 19 пациентов. Осложнений не наблюдалось. Больные подвергались плановому обследованию через 6, 12 месяцев после выписки из стационара. У всех результаты лечения расценены как хорошие: больные не испытывали болей и неприятных ощущений в правом подреберье и в подложечной области, по данным УЗИ просвет желчного пузыря не определялся, в его проекции имеется плотный эхопозитивный тяж - фиг.4, где А - облитерированный желчный пузырь.
Преимуществами предлагаемого комплексного способа диагностики и хирургического лечения являются:
- сочетание ХДС и УЗИ в диагностике блока пузырного протока позволяет достичь достоверности, равной 100%, своевременно выставить показания к хирургическому лечению;
- учет временных критериев появления окрашенной желчи при выполнении ХДС позволяет избежать ложноположительных результатов;
- отказ от премедикации промедолом, атропина сульфатом, димедролом исключает артефакты при проведении ХДС;
- применение резиновой трубки с наполняемым баллоном-обтуратором способствует формированию прочного свищевого хода, обеспечивает герметизм холецистостомы, предотвращает преждевременное выпадение дренажа, образование "мертвого пространства" в области дна желчного пузыря и связанные с этим осложнения;
- применение именно 70% эмульсии фенола с экспозицией 4 мин обеспечивает наиболее полную и безопасную мукоклазию желчного пузыря, с последующей полной облитерацией его просвета;
- при выполнении операции исключается отрицательное воздействие на организм пневмоперитонеума и наркоза;
- простота и доступность используемых материалов и самого способа позволяет широко применять его в хирургических стационарах общего профиля.
Источники информации
1. Галеев М.А., Тимербулатов В.М. Желчнокаменная болезнь и холецистит // Уфа,- 1997.-201с.
2. Королев Б.А., Пиковский Д.Л. Экстренная хирургия желчных путей // М., Медицина.- 1990.- 240с.
3. Кукош М. В. Особенности клинического течения острого холецистита у больных пожилого и старческого возраста с наличием сопутствующих заболеваний // В кн.: Острый холецистит. Пути совершенствования диагностики и хирургического лечения. Сб. науч. тр., Горький. - 1988.- С.50-52.
4. Кочнев О.С. Экстренная хирургия желудочно-кишечного тракта // Издательство Казанского университета. - 1984.-288с.
5. Падишина Л. Г., Набегаев А.И., Морозов И.С. Острый холецистит у лиц пожилого и старческого возраста // Новые технологии в хирургической гепатологии: Мат. 3 конф. хирургов-гепатол.- СПб.,-1995.-С.453-456.
6. Богер М.М., Мордвов С.А. Ультразвуковая диагностика в гастроэнтерологии // Новосибирск. Издательство "Наука". Сибирское отделение. - 1988.-160с.
7. Гришин И.Н. Холецистэктомия: Практ. пособие // Мн., Выш. шк.- 1989. -198с.
8. Febres D. - цит. по Л.В.Авдей. Клиника и хирургическое лечение холецистита // Мн.-1963.- 222с.
9. Дедерер М.Ю., Крылова Н.П., Устинов Г.Г. Желчнокаменная болезнь // М. , Медицина.-1983.-176с.
10. Дихтенко Г.И. Ускоренное хроматическое дуоденальное зондирование в экспресс-диагностике острого холецистита // Клин. хир.- 1971.- 3.-С.13-16.
11. Вахидов В.В., Ходжибеков М.Х., Цой К.В. Эхография и холецистография в диагностике калькулезного холецистита // Вест.хир.- 1984.- 11.-С.35-38.
12. Постолов П. М. , Быков А.В. Ультразвуковая семиотика и диагностика острого холецистита //Хирургия. -1990.- 2.-С.21-23.
13. Кочнев О. С. , Ким И.А., Валеев А.Г. Эндоскопическая диагностика и лечение острого холецистита // Хирургия.-1984. - 7.- С.25-30.
14. Машковский М.Д. Лекарственные средства: в 2-х томах.-10-е изд. стер. -М.- 1985.-624с.-Т.2.-576с.
15. Затевахин И. И., Кушнир В.К., Цициашвили М.Ш., Блинов В.Ю., Угольников С. Г. Эндоскопическая холецистостомия в лечении острого холецистита у лиц с высокой степенью операционного риска // Хирургия.- 1988.- 1.-С.11б-117.
16. Чадаев А.П., Любский А.С. Двухэтапное лечение острого холецистита у больных старческого возраста // Междунар. науч. конф.: "Актуальные вопросы диагностики и лечения заболеваний гепатобилиарной зоны. Эндоскопическая хирургия".Тез. докл.- СПб.-1996.- С. 162-163.
17. Braun В., Blank W. Gallbladder puncture and drainage as therapy of acute cholecystitis // Med. Klin.-1996.- Vol. 91, 6.- P.359-365.
18. Брискин Б.С., Минасян А.М., Васильева М.А., Барсуков М.Г. Чрескожная чреспеченочная микрохолецистостомия в лечении острого холецистита // Анналы хирургической гепатологии.- 1996.- 1.- С.98-107.
19. Verbanck J.J., Demol J.W., Ghillebert G.L. et al. Ultrasound quided puncture of the gallbladder for aqute cholecystitis // Lancet.- 1993.- 341.- P.1132.
20. Van Steenbergen W. , Ponette E., Marchal G. et al. Percutaneous transhepatic cholecystostomy for acute complicated cholecystitis in elderly patients //Am. J. Gastroenterol.- 1990.- 85.- P. 1363.
21. Van Overhagen H., Meyers H., Tilanus H.W., Jeekel J., Lamberis J.S. Percutaneous cholecystostomy for patient with acute cholecystitis and an increased surgical risk. // Cardiovasc. Intervent. Radiol.- 1996.- Vol.19, 2.- P.72-76.
22. England R.E., McDermott V.G., Smith T.P., Suhocki P.V., Payne C.S., Newman G. E. "Percutaneous cholecystostomy: who responds? // Am. J. Roentgenol.- 1997.- Vol.168, 5.- P. 1247-1251.
23. Bakke К. , Navjord D. , Nilsen B.H. Percutaneous drainage of the gallbladder in acute cholecystitis // Tidsskr/Laegeforen.- 1999,-Vol. 119, 22.-P. 3260-3262.
24. Охотников О. И. Чрескожная чреспеченочная микрохолецистостомия под эхоскопическим контролем в комплексной терапии острого холецистита у больных с высоким операционным риском // Морфогенез и регенерация: Мат. конф. морфол. , иммунол. и клиницистов Черноземья, посв. 60-летию Курс. гос. мед. ин-та.- Курск.- 1995.- С.62-63.
25. Шаповальянц С.П., Михайлусов С.В., Максимова В.В. Показания к микрохолецистостомии под контролем ультразвука // Хирургия.-1997.- 1,-С.68-71.
26. Famulari С., Macri A., Galipo S., Terranova M., Freni О., Guzzocrea D. The role of ultrasonographic percutaneous cholecystostomy in treatment of acute cholecystitis //Hepatogastroenterol.- 1996.- Vol.43, 9.- P. 538-541.
27. Sugiyama M., Tokuhara M., Atomi Y. Is percutaneous cholecystitis in the very elderly? //World J. Surg.-1998.-Vol. 22, 5.- P. 459-463.
28. Dumas R., Caroli-Bosc F.X., Demarquay J.F. Zanaldi H., Hastier P., Conio M. , Maes В., Delmont J.P. Acute inoperable cholecystitis treated by endoscopic naso- vesicular drainage. Study of 15 patients // Gastroenterol/Clin. Biol.-1997.-Vоl.21, 11.-P. 854-858.
29. Hu-hai, Xue-shou, Wang Xue-zhi, Zhang Sheng-dao. Extracorporeal shokwave lithotripsy and methyl tert-butyl ether for gallbladder stones // Chin. Med. J.- 1992.- Vol.105, 8.- P. 630-634.
30. Barton K.E., Picus D., Hicks M.E., Darcy M.D., Vesely T.M., Kleinhoffen M.A. Electrohydraulic lithotripcy as an a djunct to percutaneous and endoscopic removal of biliary calculi // 17th Annu. Sci. Meet., Washington. D. C. : Program / Soc. Cardiovasc. and Intervent. Radiot- Washington (D.C.). -1992.-P. 47.
31. Королев Б. А., Пиковский Д.Л., Грудинская И.Н. Холецистостомия при остром холецистите // М., Медицина.- 1973.-104 с.
32. Дзарасова Г.Ж. Отдаленные результаты двухэтапного эндоскопического метода лечения острого калькулезного холецистита у больных с высокой степенью операционного риска // Автореф. дис....канд. мед. наук. М.,-1993.
33. Емельянов С. И., Федоров А.В., Феденко В.В., Матвеев Н.Д., Евдокименко В.В., Александров К.Р. Технологические аспекты эндоскопической хирургии желчных путей // Анналы хирургической гепатологии.-1996.- 1.-С.115-119.
34. Гуляев А.А., Шаповальянц С.Г., Бурова В.А., Михайлусов С.В., Аввакумов А.Г. Облитерация просвета желчного пузыря у. больных с высоким операционным риском // Хирургия.-1998.- 9.- С.42-44.
35. Ji Z.L., Chen H.R., Lei R.Q., Yang J.Z., Huang M.H. Cystic duct occlusion by microwave tissue coagulator in rabbits // J/R Coil. Surg. Edinb.- 1991.-Vol. 36, 6.-P. 395-398.
36. Никуленков С.Ю., Бельков А.В., Ефимкин А.С. Эндоскопическая облитерация желчного пузыря у больных острым холециститом с высоким операционным риском // Эндоскопическая хирургия.-1998.- 1.-С.34.
37. Шуркалин Б.К., Ермолов А.С., Гуляев А.А., Удовский Е.Е., Юрченко С. В. , Каримов T.M., Пономарев В.Г., Елисеенко В.И., Лурье Б.Л. Химическая мукоклазия и облитерация просвета желчного пузыря у больных с высоким операционным риском (экспериментальное исследование) // Хирургия.- 1993.- 4.-С. 38-43.
38. Назаренко П.М., Тарасов О.Н., Должиков А.А. К морфологическому обоснованию метода облитерации желчного пузыря при лечении желчнокаменной болезни // Морфогенез и регенерация: Мат. конф. морфол., иммунол. и клиницистов Черноземья, посв. 60-летию Курс. гос. мед. ин-та.-Курск.- 1995.-С. 59-61.
39. Becker C. D., Fache J.S., Malone D.E., Stoller J.L., Burhenne H.J. Ablation of the cystic duct and gallbladder: clinical observations // Radiology.- 1990.-Vol. 176, 3.-P. 687-690.
40. Girard M.J., Saini S., Mueller P.R., Lee M.J., Ribeiro R.E., Fermcci J. T., Flotte T.J. Percutaneous chemical gallbladder sclerosis after laser - induced cystic duct obliteration: results in an experimental model // Am. J. Roentgenol.-1992.- Vol.159, 5.- P. 997-999.
41. Girard M.J., Saini S., Mueller P.R., Flotte T.J., Staritz M., Domankevitz Y. , Ferrucci J. T. , Nishioka N. Percutaneous obliteration of the cystic duct with a holmium: yttrium - aluminium - garnet laser: results of in vitro and animal experiments // Am. J. Roentgenol.- 1992.- Vol.159, 5.- P. 991-995.
42. Б.С.Э. Издательство: Советская энциклопедия.-1978.- т. 28.- С. 460.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТЕРМИЧЕСКОЙ МУКОКЛАЗИИ ЖЕЛЧНОГО ПУЗЫРЯ И ОДНОВРЕМЕННОЙ ОЦЕНКИ ЕЕ ЭФФЕКТИВНОСТИ | 2009 |
|
RU2396915C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ХОЛЕЦИСТИТА | 1993 |
|
RU2086186C1 |
| СПОСОБ ВЫСОКОЭНЕРГЕТИЧЕСКОЙ ЛАЗЕРНОЙ ДЕМУКОЗАЦИИ ЖЕЛЧНОГО ПУЗЫРЯ У БОЛЬНЫХ ОСТРЫМ ХОЛЕЦИСТИТОМ С ВЫСОКИМ ОПЕРАЦИОННО-АНЕСТЕЗИОЛОГИЧЕСКИМ РИСКОМ | 2019 |
|
RU2713967C1 |
| СПОСОБ ЛАПОРОСКОПИЧЕСКОЙ МУКОКЛАЗИИ | 1992 |
|
RU2045230C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОСТРОГО БЕСКАМЕННОГО ХОЛЕЦИСТИТА У БОЛЬНЫХ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА С ВЫСОКИМ ОПЕРАЦИОННО-АНЕСТЕЗИОЛОГИЧЕСКИМ РИСКОМ | 2019 |
|
RU2720105C1 |
| СПОСОБ БИПОЛЯРНОЙ МУКОКЛАЗИИ ДЛЯ РАДИКАЛЬНОГО ЛЕЧЕНИЯ ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНИ У ЛИЦ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА | 2004 |
|
RU2261683C1 |
| СПОСОБ ТЕРМИЧЕСКОЙ МУКОКЛАЗИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2207059C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ХОЛЕЦИСТИТА | 2003 |
|
RU2260453C2 |
| Способ чрескожной чреспеченочной холангиостомии у холецистостомированных больных | 2017 |
|
RU2649532C1 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТОДУОДЕНОСТОМИИ | 2002 |
|
RU2277389C2 |
Изобретение относится к медицине, хирургии, может быть использовано для диагностики и лечения острого холецистита у больных с высоким операционно-анестезиологическим риском. Выполняют ультразвуковые обследования, хромодуоденоскопию. Учитывают при хромодуоденоскопии временной фактор выделения окрашенной желчи из фатерова соска. Выполняют холецистостомию под местной анестезией при блоке пузырного протока с наложением одного кисетного шва. Контролируют состояние холецистостомы с использованием метиленовой сини. При получении зеленого отделяемого по страховочному дренажу после введения метиленовой сини выполняют химическую мукоклазию. Используют медикаментозные препараты для уменьшения отека и спазма фатерова соска. Способ позволяет снизить послеоперационные осложнения. 4 ил.
Комплексный способ диагностики и хирургического лечения острого холецистита у больных с высоким операционно-анестезиологическим риском, включающий ультразвуковое исследование, хромодуоденоскопию, хирургическую холецистостомию, химическую мукоклазию, отличающийся отсутствием премедикации при выполнении хромодуоденоскопии у больных с нормальным эмоциональным настроем и использованием внутривенно 40 мг седуксена у больных с повышенным эмоциональным настроем, применением магния сульфата для стимуляции пузырного рефлюкса, учетом временного фактора выделения окрашенной желчи из фатерова соска в двенадцатиперстную кишку при диагностике проходимости протока, с нормой ее поступления через 6-15 мин после стимуляции, использованием холецистостомии под местной анестезией в случае сохранения блока пузырного протока при помощи трубки с просветом более или равным 1 см, с баллоном-обтуратором, фиксируемой одним кисетным швом, исключающей отрицательное воздействие на организм наркоза, пневмоперитонеума и образование "мертвого пространства" в зоне кисетных швов, заполнением баллона жидкостью, введением в страховочный дренаж 0,05- 0,025% раствора метиленовой сини для ранней диагностики и контроля состоятельности холецистостомы, и при получении из дренажа отделяемого зеленого цвета, проведении мероприятий, устраняющих несостоятельность холецистостомы, проведением химической мукоклазии 70% эмульсией фенола, с экспозицией 4 мин, сохранением холецистостомической трубки до окончания отхождения некротизированной слизистой оболочки, использованием для уменьшения желчеистечения из холецистостомы медикаментозных препаратов, направленных на уменьшение отека и спазма фатерова соска.
| ВЫРОДОВ И.С | |||
| Место хромодуоденоскопии и сонографии в лечении острого холецистита методом химической мукоклазии/В кн.: "Современные медицинские технологии - здравоохранению", 1999, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| АРХИПОВ О.И | |||
| Облитерация просвета желчного пузыря путем химической мукоклазии./В кн | |||
| "Здоровье - системное качество человека", 1999, с.88-89 | |||
| СТОЛЯРОВА Л.Ф | |||
| Кислотопродуцирующая функция желудка после селективной проксимальной ваготомии | |||
| - Автореф | |||
| дисс | |||
| к.м.н., 1992, с.17. | |||
Авторы
Даты
2003-03-10—Публикация
2000-08-10—Подача