Изобретение относится к области медицины и может быть использовано в акушерстве, гинекологии, педиатрии, неонатологии, фармакологии, микробиологии, физиологии, гистологии, лабораторной диагностике.
В зарубежной и отечественной справочно-информационной литературе аналогов заявляемому способу моделирования гестационного пиелонефрита нет.
Задача изобретения - разработать модель гестационного пиелонефрита, развивающуюся на фоне инфекционно-воспалительного процесса мочевыводящих путей и максимально приближенную к аналогии подобного процесса в человеческом организме.
Выполнение поставленной задачи осуществляют путем трехразового введения взвеси микроорганизмов Escherichia coli штамма O6 в мочевой пузырь беременной крысы.
Способ осуществляют следующим образом.
В качестве подопытных животных используют белых беспородных крыс, потому что эти лабораторные животные крысы обладают непродолжительной беременностью - 21-22 дня. Кроме того, крысы способны вынашивать беременность независимо от времени года.
Для моделирования инфекционно-воспалительного процесса в качестве инфекционного агента используют кишечную палочку - Escherichia coli (Е. coli) на следующем основании. Во-первых, возникновение гестационного пиелонефрита происходит только на фоне урогенитальной инфекции. Известно, что ведущую этиологическую роль в его возникновении принадлежит Е. coli [8]. Во-вторых, она является наиболее частой этиологической причиной формирования осложненной инфекции мочевыводящих путей вообще [4]. Среди большой разновидности эшерихий по O-антигену выбор был остановлен на сероваре кишечной палочки O6, потому что этот серотип Е. coli наблюдается при обструктивных и необструктивных формах урогенитальной инфекции и занимает при этом второе место по высеваемости [5] . Занимающий первое место по высеваемости серотип кишечной палочки O9 использовать нецелесообразно в связи с тем, что Е. coli О9, как возбудитель урогенитальной инфекции, свои патогенные качества реализует только в условиях обструкции мочевыводящих путей [4]. Следовательно, использование кишечной палочки серотипа O6 с точки зрения вероятности воспроизведения инфекционно-воспалительного процесса в мочевыводящих путях представляется наиболее оправданным.
С этой целью штамм Е. coli О6, производимый Государственным НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А. Тарасовича, культивируют на питательных средах в условиях термостата. Стерильным физиологическим раствором готовят смыв колоний Е. coli О6, суточного возраста. Для заражения животных используют взвесь Е. coli O6, в концентрации микробных тел 1•107 КОЕ/мл, приготовленную методом последовательных серийных десятикратных разведений.
Соблюдая правила асептики и антисептики, катетер через уретру вводят в мочевой пузырь, затем через катетер с помощью шприца в мочевой пузырь вводят взвесь микроорганизмов. На каждые 100 г массы животного вводят 0,1 мл взвеси микроорганизмов в концентрации 1•107 КОЕ /1 мл.
Для осуществления катетеризации мочевого пузыря крысу под легким эфирным наркозом иммобилизируют на спине. Процесс иммобилизации крысы на спине с окончанием действия эфирного наркоза всегда сопровождался актом мочеиспускания. Этот факт свидетельствует о том, что мочевой пузырь опорожнен и позволяет ввести в него определенный объем жидкости. Во избежание инициации повторного рефлекторного мочеиспускания у крысы за счет раздражения терморецепторов стенки мочевого пузыря температура шприца, его содержимого и катетера с помощью термостата поддерживают на уровне температуры внутренних органов крысы - 37,0oС. Кроме того, во избежание раздражения механорецепторов стенки мочевого пузыря с инициацией повторного рефлекторного мочеиспускания используют малый объем жидкости - 0,1 мл на 100 г массы тела крысы. Это связано с тем, что объем внутрипузырной жидкости 0,1 мл и объем мочевого пузыря при массе тела крысы 100 г соотносятся между собой как 1/7-1/5. Следовательно, заполнение пустого мочевого пузыря на 1/7-1/5 его объема жидкостью, имеющей температуру, равную температуре внутренних органов крысы, не будет инициировать рефлекторное мочеиспускание. Это предположение было подтверждено собственными наблюдениями: катетеризация мочевого пузыря у иммобилизованного на спине животного с введением жидкости в мочевой пузырь при соблюдении вышеописанных условий ни разу не сопровождалась рефлекторным актом мочеиспускания.
Сразу после введения через катетер стерильного физиологического раствора или взвеси микроорганизмов в полость мочевого пузыря катетер извлекают из уретры, а животное освобождают от иммобилизации.
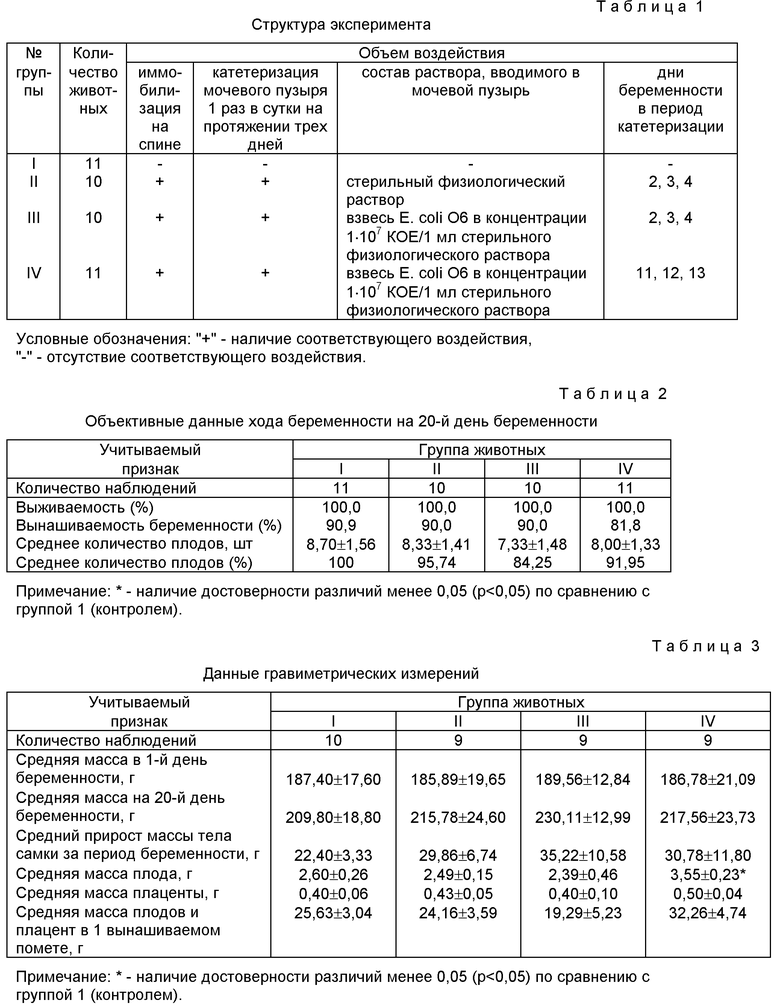
Все подопытные животные по объему воздействия были разделены на 4 группы (таблица 1).
I группа животных - это контрольная группа животных. Животным этой группы иммобилизацию и катетеризацию не проводят. II, III и IV группы животных - это опытные группы. Каждому животному из этих групп один раз в сутки и три дня подряд производят катетеризацию мочевого пузыря. Животным второй группы в мочевой пузырь вводят стерильный физиологический раствор в расчете 0,1 мл физиологического раствора/100 г массы животного. Животным третьей и четвертой групп вводят взвесь Е. coli O6 в концентрации 1•107 КОЕ/1 мл стерильного физиологического раствора в расчете 0,1 мл взвеси/100 г массы крысы. Катетеризацию мочевого пузыря с введением в его полость взвеси микроорганизмов осуществляют: для животных III группы - на 2-4-й день беременности, для животных IV группы - на 11-13-й день беременности.
Такая структура эксперимента позволяет: на примере второй группы выявить негативное влияние иммобилизации и катетеризации на процессы гестации; на примере третьей и четвертой групп животных установить возникновение гестационного пиелонефрита и наличие инфекционно-воспалительного процесса в мочевыводящих путях.
Для оценки условий течения и исхода беременности, длящейся у крыс в среднем 21-22 дня, животных всех четырех групп накануне родов - на 20-й день беременности - подвергают эвтаназии. При этом проводят ряд гравиметрических, гематологических, микробиологических и морфометрических исследований.
В таблице 2 приведены объективные данные хода беременности на 20-й день беременности.
Наличие одинаковых показателей выживаемости животных и вынашиваемости беременности в группах I и II свидетельствует об отсутствии негативного влияния наркотизации животного с целью иммобилизации и самой иммобилизации на гестационные процессы. Примерное совпадение среднего количества плодов в абсолютных и относительных цифрах у животных этих групп отражает отсутствие эмбриотоксического эффекта трехразовой эфирной наркотизации легкой степени и стрессового влияния трехразовой иммобилизации беременной самки на спине.
Выживаемость самок в группах III и IV по сравнению с группой I указывает, что введение взвеси Е. coli О6 не приводит к развитию септических состояний. Примерно одинаковый результат по сравнению с контролем наблюдается и по вынашиваемости беременности (90,9% и 8 1.8% против 90,9%). В то же время, при отсутствии статистической достоверности различий между абсолютными значениями среднего количества плодов в группах III и IV, отмечается тенденция к их снижению в относительных величинах. Так, если принять среднее значение плодов в группе I за 100%, то значение среднего числа плодов в группе III составит 84,25%, в группе IV - 91,95%.
Таким образом, по данным таблицы 2 можно утверждать, что использование инфекционного агента не оказывает решающего влияния на объективные параметры условий протекания беременности, то есть на выживаемость беременной крысы-самки и вынашиваемость беременности. В то же время, инфицирование мочевыводящих путей во время беременности имеет тенденцию негативного влияния инфекционного агента на гестационные процессы в виде снижения вынашиваемости беременности и снижения среднего количества плодов, определяемых в полости матки у крыс групп III и IV.
В таблице 3 приведены данные гравиметрических измерений. Значения учитываемых признаков между группами I и II практически совпадают. Следовательно, различия между группами I и III, I и IV будут связаны с введением инфекционного агента в мочевыводящие пути.
На первый день беременности средняя масса животных во всех группах практически совпадает. Средняя масса самок к 20-му дню беременности увеличивается, а средний прирост массы тела самки в группах III и IV имеют наибольшие значения (35,22 г и 30,78 г соответственно против 22,40 г в контроле). Следовательно, процесс протекания беременности в группах III и IV имеет особенности по сравнению с контрольной группой. В группе IV средние массы плода, плаценты, средняя масса плодов и плацент в вынашиваемом помете имеют тенденцию к росту выше контрольных значений, а в группе III - ниже контрольных. Это следует оценивать как срыв адаптационных процессов материнского организма в метаболическом обеспечении фетоплацентарного комплекса у животных группы III в декомпенсированной, а у животных группы IV и компенсированной форме.
Следовательно, по данным гравиметрических исследований можно утверждать, что создание у беременной крысы-самки инфекционно-воспалительного процесса в мочевыводящих путях в обе половины беременности приводит к нарушению нормального хода беременности.
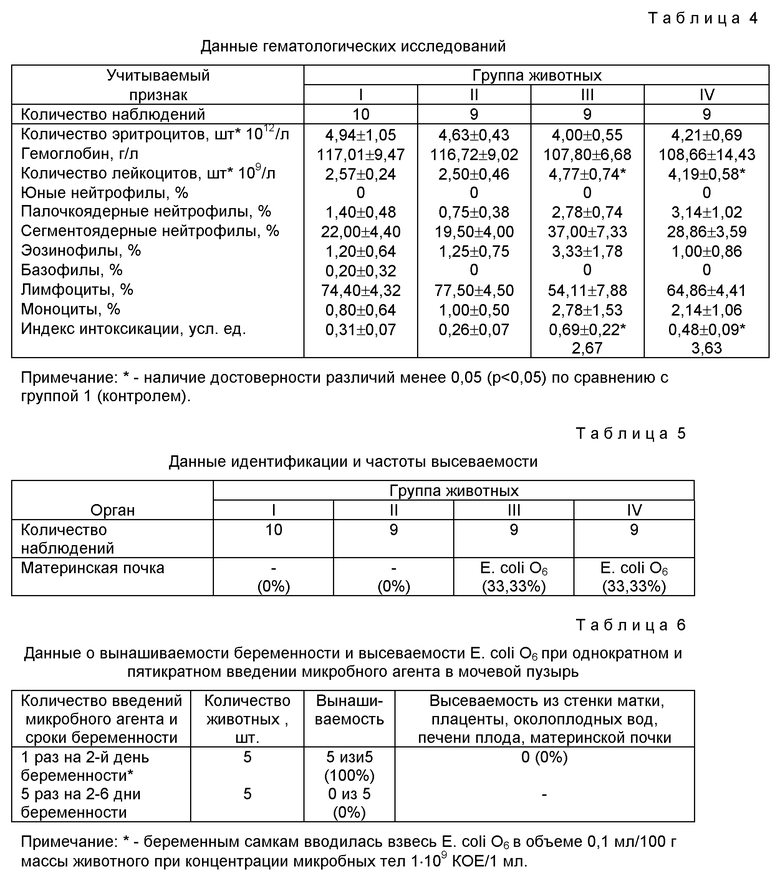
В таблице 4 приведены данные гематологических исследований.
Гематологические данные групп I и II практически совпадают. Характер изменения гематологических величин в группах III и IV по сравнению с контролем имеет особенности. Для этих экспериментальных групп характерна тенденция: снижения количества эритроцитов, уровня гемоглобина и увеличения числа лейкоцитов. Изменение лейкоцитарной формулы в этих группах характеризуется тенденцией к нейтрофилии, моноцитозу, лимфопении. Выявляемые изменения лейкоцитарной формулы отражают наличие воспалительной реакции у беременных крыс. Увеличение индекса интоксикации в группах III и IV также подтверждает проявление инфекционно-воспалительной реакции в организме беременных самок. Таким образом, введение инфекционного агента беременным крысам отражается в гематологических параметрах в виде воспалительной реакции с интоксикационным синдромом.
Для выявления гестационного пиелонефрита производили посев материнской почки. Процедуру забора биоматериала для микробиологического исследования осуществляли с соблюдением всех правил асептики в течение ближайших минут с момента эвтаназии животного. Культивирование, идентификацию выделенных культур осуществляли согласно приказу 535 М3 СССР от 22 апреля 1985 года [6].
С целью выявления любого возможного инфекционного агента посевы проводили на неселективные среды - отдельно для выделения аэробов, отдельно для анаэробов. Роста колоний на анаэробных средах не наблюдали ни в одном случае. На аэробных средах наблюдали рост колоний только одного вида микроорганизмов, которые были подвергнуты дальнейшей идентификации на питательных средах [6] . В таблице 5 приведены данные идентификации и частоты высеваемости.
Табличные данные свидетельствуют, что вводимая в мочевыводяшие пути во время беременности кишечная палочка высевалась к конце беременности из почки. С учетом способа инфицирования это свидетельствует о наличии нефрита инфекционно-воспалительной природы. Совпадение серотипа кишечной палочки, вводимой в мочевой пузырь, и серотипа кишечной палочки, высеваемой из почки, доказывает материальную взаимосвязь этих процессов. Таким образом, введение Е. coli O6, в мочевыводящие пути в различные сроки беременности приводит к возникновению нефрита с очевидной инфекционно-воспалительной причиной, то есть пиелонефриту.
Выбор концентрации микроорганизмов для введения в мочевой пузырь беременной крысы связан с тем, что истинная бактериурия при инфекции мочевыводящих путей составляет 1•105 КОЕ/1 мл мочи [1, 7]. Поэтому использование взвеси микробных тел в концентрации 1•107 КОЕ/1 мл с введением этой взвеси из расчета 0,1 мл взвеси на 100 г веса животного при массе животных в 150-200 г предполагает введение дозы микробов в количестве (1,5-2)•106 КОЕ. Таким образом, концентрация микробных тел 1•107 КОЕ/мл позволяет одновременно: 1) осуществить введение дозы микроорганизмов на один порядок выше истинной бактериурии, то есть дозы 1•106 КОЕ/100 г массы, с целью создания первичного инфекционно-воспалительного процесса в мочевыводящих путях, 2) осуществить количественное введение инфекционного агента пропорционально массе тела, а следовательно, и полостям мочевыводящей системы.
Выбор трехразового введения микроорганизмов сделан на основе экспериментального подбора (таблица 6) и объясняется тем, что одноразовое введение даже более высокой дозы микроорганизмов не приводит к развитию урогенитальной инфекции, а увеличение числа введений приводит к резкому снижению вынашиваемости беременности.
Это подтверждает известные данные о том, что вероятность развития инфекции мочевыводящих путей определяется гормональным фоном беременности и нарушением уродинамики во время беременности [5,8]. Поэтому использование трехразового введения взвеси микроорганизмов в мочевой пузырь является обязательным условием воспроизведения гестационного пиелонефрита.
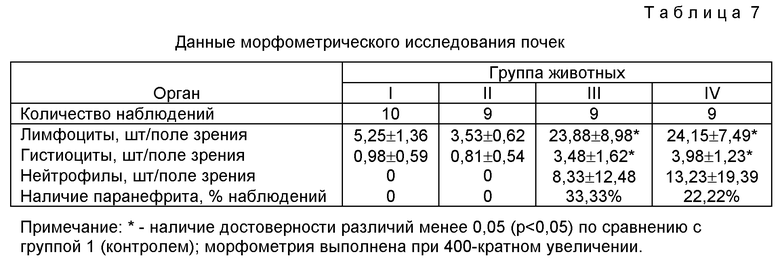
В таблице 7 приведены данные морфометрического исследования материнских почек по признакам, позволяющим судить о наличии нефрита.
В группах III и IV наблюдается рост числа лимфоцитов, гистиоцитов, нейтрофилов и случаев паранефрита. При этом увеличение количества лимфоцитов и гистиоцитов достигает достоверного уровня различий. Учитывая данные микробиологических исследований (таблица 5) и данные морфометрии (таблица 7), можно утверждать наличие нефрита.
На основании полученных результатов объективного наблюдения, гравиметрических, гематологических, микробиологических и морфометрических исследований можно утверждать, что введение в мочевыводящие пути беременной крысы взвеси микроорганизмов Eschenchia coil O6 в различные сроки беременности приводит к возникновению пиелонефрита во время беременности, то есть гестационному пиелонефриту.
Из достоинств предлагаемого способа моделирования гестационного пиелонефрита можно выделить следующие моменты: 1) протяженность беременности крыс в 21-22 дня позволяет проводить эксперименты в относительно непродолжительные сроки, 2) воспроизведение первичного источника инфекционно-воспалительного процесса в мочевыводящих путях материнского организма имеет реальную сопоставимость с проблемой гестационного пиелонефрита для человека, 3) возникновение и протекание пиелонефрита в эксперименте протекает без очевидных признаков нарушенного хода беременности, что характерно для протекания подобного процесса и у человека, 4) проведение эксперимента на крысах имеет низкую себестоимость исследований.
Таким образом, упоминаемые достоинства предлагаемого способа позволяют считать его адекватной моделью гестационного пиелонефрита, имеющего место у человека. Экспериментальное исследование патогенеза гестационного пиелонефрита по предлагаемому способу позволит определять направления коррекции и профилактики формирующейся патологии беременности с целью предупреждения рождения неполноценного потомства и охраны здоровья матери.
Источники информации
1. Арбулиев М.Г., Арбулиев К.М., Османов Г.М. К вопросу лечения гнойного пиелонефрита // Урология и нефрология. - 1997. - 6. - С. 14-17.
2. Говорка Э. Плацента человека. - Варшава: Пол. гос. мед. изд-во, 1970. - 471 с.
3. Брусиловский А. И. Функциональная морфология плацентарного барьера человека. - Киев: Здоров'я, 1976. - 136 с.
4. Идентификация возбудителей инфекций мочевыводящих путей у детей / В. И. Кириллов, Л.Т. Теблоева, Е.Б. Алексеев и соавт. // Педиатрия. -1997. - 6. - С. 8-13.
5. Лопаткин Н. А., Деревянко И.И. Неосложненные и осложненные инфекции мочеполовых путей. Принципы антибактериальной терапии // Русский медицинский журнал. - 1997, Т.5. - 24. - С. 1579-1588.
6. Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностических лабораториях, лечебно-профилактических учреждениях / Приказ 535 М3 СССР от 22 апреля 1985 г. - М., 1985. - 127 с.
7. Особенности сочетанного течения беременности и пиелонефрита в современных условиях / С. С. Заяц, И.А. Логинов, Г.М. Перцева, И.В. Смирнова / Мат. 4-й межобластной научно-практ. конф. "Актуальные проблемы акушерства и гинекологии", 8-9 октября 1998 г. Волгоград. - Волгоград, 1998. - С. 125-127.
8. Шехтман М. М. Экстрагенитальная патология и беременность. - Л.: Медицина, 1987. - С. 174-181.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ НА ФОНЕ ИНФЕКЦИИ МОЧЕВЫВОДЯЩИХ ПУТЕЙ | 1999 |
|
RU2197750C2 |
| СПОСОБ ВОСПРОИЗВЕДЕНИЯ ВОСПАЛИТЕЛЬНО-ИНФЕКЦИОННОГО ПРОЦЕССА НА КРЫСАХ | 2000 |
|
RU2196990C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГЕСТАЦИОННОГО ПИЕЛОНЕФРИТА | 2013 |
|
RU2532402C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ИНФЕКЦИИ МОЧЕВОЙ СИСТЕМЫ | 2004 |
|
RU2282899C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ МОЧЕВЫВОДЯЩИХ ПУТЕЙ У ДЕТЕЙ | 2001 |
|
RU2199358C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИИ РОДОВЫХ ПУТЕЙ БЕРЕМЕННЫХ И ПРОФИЛАКТИКИ ВНУТРИУТРОБНОГО ИНФИЦИРОВАНИЯ ПЛОДА | 1998 |
|
RU2141265C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ АППЕНДИКУЛЯРНОГО ИНФИЛЬТРАТА | 2001 |
|
RU2204866C2 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ФЕТОПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ | 2001 |
|
RU2198701C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ОСТРОГО ГНОЙНОГО ПИЕЛОНЕФРИТА | 2000 |
|
RU2188456C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ОСТРОГО ПИЕЛОНЕФРИТА | 2007 |
|
RU2349965C1 |
Способ может быть использован в медицине, в частности в акушерстве, гинекологии, педиатрии, неонатологии, фармакологии, микробиологии, физиологии, гистологии, лабораторной диагностике. Способ моделирования гестационного пиелонефрита на фоне инфекционно-воспалительного процесса мочевыводящих путей осуществляют путем трехразового введения взвеси микроорганизмов Escherichia coli штамма O6 в мочевой пузырь беременной крысы. Способ позволяет разработать модель гестационного пиелонефрита, максимально приближенную к аналогии подобного процесса в человеческом организме. 7 табл.
Способ моделирования гестационного пиелонефрита на фоне инфекционно-воспалительного процесса мочевыводящих путей осуществляют путем трехразового введения взвеси микроорганизмов Escherichia coli штамма O6 в мочевой пузырь беременной крысы.
| Способ моделирования пиелонефрита | 1986 |
|
SU1422239A1 |
| ПУЛЯ ОХОТНИЧЬЕГО ПАТРОНА ДЛЯ НАРЕЗНОГО ОРУЖИЯ | 1998 |
|
RU2138008C1 |
| ЛОПАТКИН Н.А | |||
| и др | |||
| Пиелонефрит у детей | |||
| - М.: Медицина, 1979, с | |||
| Ножевой прибор к валичной кардочесальной машине | 1923 |
|
SU256A1 |
Авторы
Даты
2003-04-20—Публикация
2000-04-24—Подача