Изобретение относится к медицине, а именно к экспериментальной вертебрологии, и может быть использовано в ходе экспериментальных исследований биологических свойств костных и искусственных имплантатов, а также репаративных свойств костной ткани, в частности для оценки пригодности имплантатов к использованию при переднем и заднем спондилодезе.
Известен способ моделирования переднего спондилодеза на собаках с использованием в качестве пластического материала компактно-спонгиозных (губчатых) аутотрансплантатов из метаэпифиза левой большой берцовой кости собаки [1]. Согласно методике указанного способа-аналога осуществляли передненаружный левосторонний внебрюшинный доступ к телам позвонков экспериментального животного. Формировали костное ложе для трансплантата в теле пятого и торцевых отделах четвертого и шестого поясничных позвонков. При этом удаляли механическим путем (с помощью долота и костной ложечки) фиброзные кольца четвертого и пятого межпозвопковых дисков в средних и задних отделах и их пульпозные ядра до задней продольной связки по ходу трансплантата, а также компактно-спонгиозную кость в каждом из указанных позвонков, формируя прямоугольный костный паз (ложе) в теле пятого, каудальном отделе четвертого и краниальном отделе шестого поясничных позвонков. Затем трансплантат укладывали в сформированное материнское ложе таким образом, чтобы он своей спонгиозной поверхностью плотно соприкасался с ложем, а кортикальная поверхность трансплантата была расположена на 0,2-0,3 см ниже от передней поверхности тел смежных позвонков. Фиксацию трансплантата осуществляли путем перевода собаки из операционного положения искусственного поясничного гиперлордоза в физиологически нормальное положение, тем самым заклинивая трансплантат между телами смежных позвонков в костном ложе (состояние реклинации). Послеоперационные раны ушивали послойно наглухо. Срок наблюдения за подопытными животными до 1,5 лет.
Наиболее близким к заявленному решению по совокупности существенных признаков является способ моделирования переднего спондилодеза на собаках [2] . В качестве пластического материала использовали аллотрансплантаты компактно-губчатого характера из тел позвонков взрослой особи, консервированные в 0,5% растворе формалина при разных сроках консервации (3 варианта аллотрансплантатов). Согласно способу-прототипу осуществляли левостороннюю люмботомию, внебрюшинный доступ к телам позвонков экспериментального животного. Формировали костное ложе для трансплантата в телах четвертого и пятого поясничных позвонков. При этом полностью удаляли межпозвонковый диск и создавали прямоугольной дефект (паз) в телах указанных позвонков с помощью циркулярной фрезы от бормашины. Плотно внедряли трансплантат в образованный дефект (материнское ложе). Затем осуществляли фиксацию трансплантата в передних отделах позвоночника. При этом впереди трансплантата накладывали лавсановый шов в виде "восьмерки" на переднюю продольную связку позвоночника и поверхностный слой хрящевых дисков у места сращения последних с телами позвонков материнского ложа. Послойно ушивали операционную рану. Передний спондилодез, осуществляемый по методике способа-прототипа, при использовании формализированных аллотрансплантатов из тел позвонков обеспечивает, как указано в работе [2], формирование костного блока между телами позвонков через 3-4 месяца после операции.
Однако как способ-аналог [1], так и способ-прототип [2] не обеспечивают достигаемого при использовании заявленного решения технического результата. Это обусловлено следующими причинами. Предусмотренные методиками известных способов [1, 2] зоны трансплантации обеспечивают возможность формирования костного блока между телами позвонков в передних отделах позвоночника, т.е. возможность моделирования переднего спондилодеза. Это не позволяет одновременно оценивать пригодность имплантатов к использованию и при переднем и при заднем спондилодезе. В рассматриваемых способах особенности формирования материнского ложа (паз в телах позвонков) в сочетании с особенностями фиксации трансплантата (внутренняя фиксация) обусловливают то, что наряду с остеопластической функцией трансплантат выполняет также функцию фиксатора позвоночника. Для выполнения указанной функции необходимо плотное внедрение трансплантата в паз, что накладывает определенные требования на прочностные характеристики применяемого трансплантата. В этой связи в известных способах [1, 2] моделирование спондилодеза возможно только при использовании имплантатов, прочностные характеристики которых сопоставимы с прочностью позвонков (в частности, губчатых и кортикальных костных трансплантатов от взрослых доноров). Применение имплантатов с относительно низкой механической прочностью (фетальных костных трансплантатов, деминерализованных костных трансплантатов, некоторых комбинированных трансплантатов, таких как коллапол, и т.п.) в способах [1, 2] технически невозможно (костный блок не будет формироваться, т. к. имплантаты будут "раздавливаться"). Однако, даже при использовании имплантатов с относительно высокой механической прочностью, применяемая фиксация не позволяет исключить возможность смещения трансплантата, которое, в ряде случаев (особенно при выпадении последнего из материнского ложа), будет препятствовать формированию костного блока, что, в свою очередь, приведет к развитию деформации позвоночника (в виде кифоза в поясничном отделе). Так, в способе-аналоге [1] это вызвано тем, что функция трансплантата как фиксатора сводится к функции расклинивания смежных позвонков. Подобная фиксация не позволяет обеспечить стабильность расположения позвонков при разгибательных нагрузках на позвоночник, т.к. при этом увеличивается лордозирование поясничного отдела позвоночника и исчезает эффект расклинивания. В способе-прототипе [2] при осуществлении фиксации трансплантата путем пластики передней продольной связки в виде шва "восьмерки" прочность указанной структуры будет недостаточна для удержания трансплантата при увеличении размеров паза в результате лордозирования поясничного отдела позвоночника, что, в ряде случаев, приведет к дестабилизации позвоночника. Моделирование спондилодеза с помощью рассматриваемых способов [1, 2] не позволяет исключить возможность повреждения мышц в зоне фиксации, в частности передней продольной связки и мышц-сгибателей позвоночника (подвздошно-поясничных мышц), являющихся источниками кровоснабжения зоны трансплантации. Относительно высокий риск кровотечения из сегментарных сосудов позвоночника обусловливает необходимость перевязки последних в ходе оперативного доступа, что также способствует ухудшению кровоснабжения зоны трансплантации. Предусмотренные методиками способа-аналога [1] и способа-прототипа [2] зоны трансплантации (передние отделы позвоночника) и левосторонний люмботомический доступ к телам позвонков обусловливают относительно высокую вероятность повреждения брюшины и органов забрюшинного пространства (аорта, почки, мочеточники), что может приводить к смертельному исходу операции. Не исключается также возможность повреждения мышц передней брюшной стенки, что увеличивает объем кровотечения в зоне операции. Формирование материнского ложа путем создания паза в телах поясничных позвонков приводит к усилению кровотечения из спонгиозной костной ткани и увеличивает длительность операции. И наконец, известные способы моделирования [1, 2] требуют применения длительного интубационного наркоза, миорелаксантов и парентерального введения кровезаменителей в интраоперационном и послеоперационном периодах, что значительно усложняет постановку эксперимента и увеличивает его продолжительность. Кроме того, как следствие глубокого наркоза и тяжести операции (массивная травма), у подопытных животных, как правило, наступает послеоперационное возбуждение, которое, в ряде случаев, может приводить к нарушению фиксации и смешению трансплантата (вплоть до его выпадения из материнского ложа). Не исключается также возможность развития неврологических нарушений (парезы нижних конечностей, расстройства тазовых органов).
Задачей изобретения является создание способа моделирования снондилодеза, обеспечивающего возможность одновременной оценки пригодности имплантатов с различными биологическими свойствами к использованию при переднем и заднем спондилодезе, при исключении возможности повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации, повреждения жизненно важных анатомических органов и структур позвоночника в зоне фиксации, а также повреждения жизненно важных анатомических органов и структур по ходу доступа, за счет создания условий для формирования блока между телами позвонков и задними структурами позвоночника и стабильности расположения фиксируемых позвонков в процессе формирования костного блока как друг относительно друга, так и относительно имплантата, при минимизации значений характеристических параметров фиксации.
Поставленная задача решается тем, что в способе моделирования спондилодеза, включающем осуществление доступа к позвоночнику экспериментального животного, формирование материнского ложа для имплантата, постановку в него имплантата и фиксацию имплантата с последующим ушиванием операционной раны, согласно изобретению доступ к позвоночнику экспериментального животного осуществляют с дорсальной поверхности его хвоста, а формирование материнского ложа для имплантата и постановку имплантата производят между третьим и четвертым хвостовыми позвонками. Фиксацию имплантата осуществляют путем фиксации смежных с имплантатом позвонков двумя фиксаторами позвонков, которые перекрестно проводят через центры тел указанных позвонков под углом 40-50o к фронтальной оси, проходящей через центр тела позвонка. Фиксацию производят с помощью приспособления для фиксации, выполненного в виде прямой правильной полой шестиугольной призмы, на четырех попарно параллельных боковых гранях которой размещено не менее двух пар сквозных попарно соосных каналов под фиксаторы позвонков, причем ось каждой пары каналов пересекает центральную ось призмы и продольную ось симметрии каждой из двух взаимно параллельных боковых граней призмы, на которых размещены каналы данной пары. При этом в ходе фиксации один из фиксаторов позвонков проводят через соосные каналы, размещенные на одной из пар взаимно параллельных боковых граней призмы, и через центр тела позвонка, расположенного краниально относительно имплантата, а другой фиксатор - через соосные каналы, размещенные на другой из пар взаимно параллельных боковых граней призмы, и через центр тела позвонка, распложенного каудально относительно имплантата. После этого производят наружную жесткую фиксацию свободного конца каждого из фиксаторов позвонков. Оптимальным является использование в качестве экспериментального животного крысы. Наиболее эффективно непосредственно перед осуществлением доступа к позвоночнику экспериментального животного дополнительно определять область локализации третьего и четвертого хвостовых позвонков, например с помощью линии окончания роста шерсти на хвосте крысы, а непосредственно перед формированием материнского ложа для имплантата дополнительно определять место локализации диска между указанными позвонками. Оптимальным приемом для определения места локализации указанного межпозвоночного диска является осуществление принудительных качательных движений хвоста экспериментального животного в горизонтальной плоскости, в процессе которых выявляют зону неподвижности между телами третьего и четвертого хвостовых позвонков, которую считают соответствующей месту локализации межпозвонкового диска. Наиболее эффективным является формирование ложа для имплантата путем удаления вещества диска между третьим и четвертым хвостовыми позвонками и эпифизарных пластинок тел указанных позвонков. Оптимальным является использование в качестве фиксатора позвонка инъекционной иглы. Наиболее эффективно, когда в ходе фиксации позвонков каждый из фиксаторов позвонков вводят через входное отверстие сквозного канала под фиксатор позвонка на одной из боковых граней призмы, размещенной с дорсолатеральной стороны хвоста, проводят через указанный канал, вводят чрезкожно с дорсолатеральной стороны хвоста и, после проведения через тело позвонка, выводят на противоположную вентролатеральную сторону хвоста, затем проводят через соосный с указанным каналом сквозной канал на боковой грани призмы, параллельной первой и размещенной с противоположной вентролатеральной стороны хвоста, после чего свободный конец фиксатора выводят наружу через выходное отверстие второго из указанных каналов. Наиболее эффективным также является осуществление наружной жесткой фиксации каждого из фиксаторов позвонков путем загибания выведенного наружу свободного конца фиксатора за боковое ребро между смежными боковыми гранями призмы, одна из которых размещена с вентролатеральной, а другая - с дорсолатеральной стороны хвоста, с последующим поворотом указанного конца фиксатора на угол 90o на боковую грань призмы, размещенную с вентролатеральной стороны хвоста.
Выбор оптимальных условий осуществления действий заявленного способа производили следующим образом. Экспериментальные исследования выполняли на половозрелых лабораторных крысах. Предварительно были выполнены макроскопические исследования хвоста у 5 крыс, в ходе которых производили поперечные разрезы хвоста на уровнях третьего и четвертого хвостовых позвонков. При этом было установлено, что зоны межмышечного пространства между дорсальными, латеральными и вентральными мышцами и сухожилиями сгибателей хвоста (две дорсолатеральные и две вентролатеральные пространственные зоны) на уровне третьего и на уровне четвертого позвонков размещаются в секторе, ограниченном радиусами, один из которых расположен под углом (35±3)o, а другой - под углом (55±3)o относительно фронтальной оси, проходящей через центр тела, соответственно, третьего или четвертого позвонка.
После этого в условиях эксперимента производили переднезадний спондилодез кортикальными аллотрансплантатами от взрослых особей (производства Российского научно-исследовательского института травматологии и ортопедии им. Р. Вредена, лаборатории заготовки и консервации тканей) по методике предложенного способа. Оптимальные условия осуществления каждого из анализируемых действий способа подбирали путем варьирования значений причинно-значимых параметров, отражающих эти условия (т.е. параметров, влияющих на достижение технического результата). В качестве причинно-значимых параметров рассматривали:
- место постановки трансплантата;
- количество фиксаторов позвонка, проводимых через тело каждого из позвонков, смежных с трансплантатом;
- угол проведения (постановки) фиксатора позвонка относительно фронтальной оси, проходящей через центр тела позвонка;
- плоскости проведения фиксаторов позвонков.
Было проведено 4 серии опытов. В каждой из серий осуществляли варьирование одного из причинно-значимых параметров на фоне постоянных (оптимальных) значений прочих параметров рассматриваемой совокупности. Каждое значение варьируемого параметра испытывали на группе животных, состоящей из 5 особей. Во всех сериях в качестве фиксатора позвонка использовали инъекционную иглу с диаметром поперечного сечения 1 мм. Срок наблюдения за подопытными животными 14 дней. Распределение животных по сериям и группам при указанном варьировании условий эксперимента выглядело следующим образом:
I серия опытов: постановка трансплантата:
в группе 1 - между вторым и третьим хвостовыми позвонками крысы;
в группе 2 - между третьим и четвертым хвостовыми позвонками;
в группе 3 - между четвертым и пятым хвостовыми позвонками;
II серия опытов: через центры тел третьего и четвертого хвостовых позвонков крысы перекрестно проведено в плоскостях, параллельных фронтальной плоскости проекций, под углом (45±1)o к фронтальной оси, проходящей через центр тела позвонка:
в группе 4 - по два фиксатора позвонка;
в группе 5 - по одному фиксатору позвонка;
III серия опытов: два фиксатора позвонка перекрестно проведены через центры тел третьего и четвертого хвостовых позвонков (в каждом позвонке - один фиксатор) в плоскостях, параллельных фронтальной плоскости проекций, под углом к фронтальной оси, проходящей через центр тела соответствующего позвонка, составляющим;
в группе 6 - (20±3)o;
в группе 7 - (30±3)o;
в группе 8 - (40±3)o;
в группе 9 - (50±3)o;
в группе 10 - (60±3)o;
в группе 11 - (70±3)(;
IV серия опытов: два фиксатора позвонка перекрестно проведены через центры тел третьего и четвертого хвостовых позвонков (в каждом позвонке - один фиксатор):
в группе 12 - в плоскостях, параллельных фронтальной плоскости проекций, под углом (45±1)o к фронтальной оси, проходящей через центр тела соответствующего позвонка;
в группе 13 - в сагиттальной плоскости под углом (45±1)o к сагиттальной оси, проходящей через центр тела соответствующего позвонка;
в группе 14 - в горизонтальной плоскости под углом (45±1)o к горизонтальной оси, проходящей через центр тела соответствующего позвонка.
Фиксацию позвонков в указанных экспериментах осуществляли с помощью разработанного авторами изобретения специального приспособления для фиксации позвоночных двигательных сегментов экспериментального животного (далее - "приспособление") в различных вариантах его конструктивного исполнения. Так, в I и II сериях опытов (группы 1-3, 4-5), а также в IV серии опытов (группа 12) было использовано приспособление, выполненное в виде прямой правильной полой шестиугольной призмы, на каждой из четырех попарно параллельных боковых граней которой имелось по 3 сквозных канала под фиксаторы позвонков, центры входных отверстий которых размещались на продольной оси симметрии данной грани. При этом на каждой из двух взаимно параллельных граней указанные каналы были выполнены соосными и идентичными по диаметрам поперечного сечения соответствующим каналам, размещенным на другой грани, а оси каждой пары каналов пересекали центральную ось призмы. На грани, не содержащей каналов под фиксаторы позвонков, находилось сквозное смотровое отверстие (оптимальный вариант исполнения приспособления). Приспособление устанавливали на хвосте крысы таким образом, чтобы две несмежные боковые грани призмы, содержащие каналы под фиксаторы позвонков, разместились с дорсолатеральных сторон хвоста, а две другие несмежные боковые грани со сквозными каналами, попарно параллельные указанным граням, - с вентролатеральных сторон хвоста, причем сквозное смотровое отверстие находилось над операционной раной (рабочее положение).
В группе 13 IV серии опытов был применен вариант приспособления, отличием которого от описанного выше являлось выполнение сквозных соосных каналов под фиксаторы позвонков на двух взаимно параллельных боковых гранях призмы (на каждой грани - по 2 канала), при этом сквозное смотровое отверстие размещалось на одной из граней, содержащей каналы под фиксаторы позвонков. Приспособление устанавливали на хвосте крысы таким образом, чтобы боковые грани, содержащие каналы под фиксаторы позвонков, разместились параллельно плоскости операционного стола (в горизонтальной плоскости), причем сквозное смотровое отверстие находилось непосредственно над операционной раной (рабочее положение). В группе 14 IV серии опытов был применен вариант приспособления, отличием которого от варианта, описанного выше для I серии опытов, являлось выполнение сквозных соосных каналов под фиксаторы позвонков на двух боковых ребрах смежных попарно параллельных боковых граней призмы (по 6 каналов на каждом ребре), а сквозное смотровое отверстие находилось на одной из боковых граней, ребра которой не содержали каналов. Приспособление устанавливали на хвосте крысы таким образом, чтобы в каждой паре смежных боковых граней, на общем ребре которых имелись каналы под фиксаторы позвонков, одна из граней разместилась с дорсолатеральной стороны хвоста, а другая - с вентролатеральной стороны хвоста, причем сквозное смотровое отверстие находилось непосредственно над операционной раной (рабочее положение). В III серии опытов (группы 6-11) фиксацию позвонков осуществляли с помощью приспособления, выполненного в виде прямого кругового полого цилиндра, на боковой поверхности которого имелись пары сквозных соосных каналов под фиксаторы позвонков, а также сквозное смотровое отверстие. При этом в указанной серии опытов в зависимости от условий постановки эксперимента использовали различные варианты приспособления, предусматривающие размещение пар соосных каналов таким образом, чтобы их оси располагались в заданных плоскостях под различными углами в соответствии с условиями эксперимента, причем ось каждой из пар каналов пересекала центральную ось цилиндра. Во всех опытах III серии приспособление устанавливали на хвосте крысы таким образом, чтобы обеспечить заданную плоскость и угол фиксации при размещении сквозного смотрового отверстия непосредственно над операционной раной (рабочее положение).
Авторами изобретения было экспериментально установлено, что стабильная фиксация смежных с трансплантатом позвонков, и, следовательно, стабильная фиксация трансплантата, может быть достигнута при помощи специального наружного приспособления для фиксации. Приспособление в общем случае представляло собой продолговатое геометрическое тело (блок фиксации), имеющее внутреннюю сквозную плоскость, расположенную вдоль его центральной оси, и элементы крепления фиксаторов позвонков, выполненные в виде не менее двух пар сквозных соосных каналов под фиксаторы позвонков, размещенных на боковой поверхности геометрического тела, причем каналы в каждой из пар были идентичны друг другу по диаметрам поперечного сечения. Оптимальную конструкцию приспособления, включая оптимальные значения параметров блока фиксации, подбирали экспериментальным путем с тем, чтобы одновременно обеспечить оптимальные условия фиксации трансплантата при соблюдении оптимальных условий осуществления действий заявленного способа и исключить возможность возникновения побочных эффектов и осложнений, обусловленных конструктивными особенностями приспособления. Так, было установлено, что оптимальные условия фиксации (угол и плоскость проведения фиксаторов позвонков, расположение оси фиксации в теле позвонка) принципиально могут быть достигнуты при размещении каналов под фиксаторы позвонков на боковой поверхности блока фиксации таким образом, чтобы ось каждой пары каналов располагалась в плоскости, параллельной фронтальной плоскости проекций, под углом 40-50o к фронтальной оси и пересекала центральную ось геометрического тела, а входные отверстия каналов разных пар размещались на боковой поверхности геометрического тела продольно относительно его центральной оси. При испытании различных вариантов конструктивного исполнения приспособления, в частности, описанных выше вариантов приспособления в виде прямого кругового полого цилиндра, в котором оси пар сквозных соосных каналов под фиксаторы позвонков располагались в заданных плоскостях под различными углами (III серия опытов, группы 6-11), а также вариантов приспособления в виде правильной полой шестиугольной призмы, в которой оси пар сквозных каналов располагались в различных плоскостях (I и II серии опытов, группы 1-5; IV серия опытов, группы 12-14), было выявлено, что оптимальным является выполнение приспособления в виде прямой правильной полой шестиугольной призмы с размещением сквозных соосных каналов на четырех попарно параллельных гранях (I и II серия опытов, группы 1-5; IV серия опытов, группа 12). Именно указанная форма приспособления в совокупности с особенностями выполнения и размещения каналов под фиксаторы позвонков позволила обеспечить соблюдение оптимальных условий фиксации с наибольшей точностью, а именно: проведение каждого из фиксаторов позвонков через центр тела соответствующего позвонка в плоскости, параллельной фронтальной плоскости проекций (оптимальная плоскость фиксации), под углом к фронтальной оси, проходящей через центр тела данного позвонка, значение которого (45o) находилось в середине интервала оптимальных значений указанного параметра (40-50o), при относительно высоком соответствии задаваемых конструкцией приспособления и фактически полученных значений данного угла (отклонение в пределах ±1o).
Выбор оптимальной длины приспособления и диаметра окружности, вписанной в шестиугольник, который представляет собой поперечное сечение внутренней полости призмы (далее - "диаметр вписанной окружности"), производили экспериментально путем их варьирования. При этом было испытано 12 вариантов приспособления, в 5-ти из которых осуществляли варьирование длины приспособления при постоянном (оптимальном) значении диаметра вписанной окружности (V серия опытов), а в 7-ми других вариантах - варьирование диаметра вписанной окружности при постоянном (оптимальном) значении длины приспособления (VI серия опытов). Длину приспособления определяли как зависимую величину от длины хвоста крысы, измеряемой от кончика хвоста до крестца (далее - "длина хвоста"). Диаметр вписанной окружности определяли как зависимую величину от наружного диаметра хвоста крысы в области третьего хвостового позвонка (далее - "диаметр хвоста"). Длину хвоста измеряли с помощью сантиметровой линейки, а диаметр хвоста - с помощью сантиметровой ленты. Каждое значение варьируемого параметра испытывали на группе животных из 5 особей. Срок наблюдения - 14 дней. Распределение животных по сериям и группам при испытании вариантов приспособления с различной длиной и различным диаметром вписанной окружности выглядело следующим образом:
V серия опытов: длина приспособления в группах 15-19 составляла, соответственно: 1/6 (0,17); 1/5 (0,20); 1/4 (0,25); 1/3 (0,33); 1/2 (0,50) длины хвоста;
VI серия опытов: диаметр вписанной окружности в группах 20-26 составлял, соответственно: 1,4; 1,6; 1,8; 2,0; 2,2; 2,4; 2,6 диаметра хвоста,
Результаты испытаний в I-VI сериях опытов оценивали с помощью клинических и рентгенологических исследований.
В ходе клинических исследований у оперированных животных определяли в пределах срока наблюдения наличие или отсутствие нарушений поведения, состояние раны и хвоста в целом (подвижность, чувствительность, наличие некротических изменений), наличие или отсутствие деформации позвоночника, а также целостность приспособления и наличие либо отсутствие его смещения из рабочего положения. Кроме того, во всех сериях опытов непосредственно после завершения проведения каждого из фиксаторов позвонков измеряли (визуально с помощью транспортира) угол постановки данного фиксатора (фактически полученное значение).
Рентгенологические исследования производили на аппарате "Арман 10Л6-01" (производства Казахстанского приборостроительного завода) в двух стандартных проекциях (прямой и боковой). Рентгенограммы выполняли с прямым увеличением в 4 раза на 7-е и 14-е сутки после операции. По рентгенограммам оценивали наличие или отсутствие разрушения тел фиксируемых позвонков; правильность соотношения фиксируемых позвонков и положение трансплантата относительно материнского ложа.
По результатам проведенных испытаний 1 серии опытов было установлено, что оптимальной является постановка трансплантата между третьим и четвертым хвостовыми позвонками крысы (группа 2). Клинические исследования показали отсутствие каких-либо нарушений поведения экспериментальных животных в пределах срока наблюдения, отсутствие несостоятельности швов и нагноения в области швов, сохранение подвижности и чувствительности дистальных отделов хвоста, отсутствие смещения приспособления из рабочего положения и отсутствие либо незначительные повреждения (в 20% случаев) его дистального конца без нарушения стояния фиксаторов позвонков. При анализе рентгенограмм выявлено: отсутствие разрушения тел фиксируемых позвонков; правильное соотношение позвонков в зоне трансплантации (в зоне костной пластики); четкое стояние трансплантата в материнском ложе (на 7-е и на 14-е сутки после операции).
При постановке трансплантата между вторым и третьим хвостовыми позвонками крысы (группа 1) у всех 5 особей на 3-4 сутки после операции наблюдалось нагноение в области швов, обусловленное близостью анального отверстия. Результаты рентгенологического исследования: на 7-е сутки после операции - в зоне костной пластики определяется полость, заполненная слаборентгеноконтрастным содержимым; на 14-е сутки после операции - дефрагментация трансплантата; "изъеденность" тел позвонков.
При постановке трансплантата между четвертым и пятым хвостовыми позвонками крысы (группа 3) на 3-7 сутки после операции отмечалось (в 100% случаев) разрушение дистальной части приспособления (вследствие сгрызания его крысой) с разъединением фиксатора позвонка и блока фиксации (корпуса) приспособления. На рентгенограммах: на 7-е сутки после операции - нарушение соотношения между фиксируемыми позвонками; смещение трансплантата относительно материнского ложа; на 14-е сутки после операции - усиление смещения фиксируемых позвонков друг относительно друга; выпадение трансплантата из материнского ложа.
Испытания, проведенные в рамках II серии опытов, показали, что оптимальным является проведение через тело каждого позвонка по одному фиксатору позвонка (группа 5). В этом случае результаты клинических и рентгенологических исследований аналогичны результатам группы 2 I серии опытов (незначительные повреждения дистального конца приспособления без нарушения стояния фиксаторов отмечены в 40% случаев).
Проведение через тело каждого из позвонков по два фиксатора позвонка (группа 4) приводило к разрушению тел позвонков в 100% случаев. Рентгенологические исследования показали: на 7-е сутки после операции - фрагментация тел фиксируемых позвонков; нарушение соотношения между фиксируемыми позвонками; на 14-е сутки после операции - фрагментация тел фиксируемых позвонков; усиление смещения фиксируемых позвонков друг относительно друга.
Данные III серии опытов свидетельствовали о том, что оптимальным является проведение фиксатора позвонка через центр тела позвонка под углом 40-50o к фронтальной оси, проходящей через центр тела позвонка (группы 8, 9). В указанных группах результаты клинических и рентгенологических исследований были аналогичны результатам группы 2 I серии опытов (незначительные повреждения дистального конца приспособления наблюдались в 20-60% случаев).
При проведении фиксатора позвонка через тела позвонков под углами 20 и 30o (группы 6, 7) на 1-2 сутки после операции наблюдалось отсутствие подвижности и чувствительности хвоста, а на 3-4 сутки после операции - некротические изменения дистальных отделов хвоста (соответственно, в 100 и 80% случаев), что свидетельствовало о повреждении сосудов хвоста.
В группах 10, 11, где углы постановки фиксатора позвонка составляли 60 и 70o относительно фронтальной оси, проходящей через центр тела соответствующего позвонка, на 5-7 сутки после операции отмечено смещение приспособления латерально относительно оси хвоста и искривление хвоста в горизонтальной плоскости в 80-100% случаев. Результаты рентгенологических исследований: на 7-е сутки после операции - нарушение соотношения между позвонками; смещение трансплантата относительно материнского ложа (в 40-60% случаев); на 14-е сутки после операции - усиление смещения позвонков друг относительно друга; выпадение трансплантата из материнского ложа (в 80-100% случаев).
В ходе испытаний в IV серии опытов было установлено, что оптимальной плоскостью фиксации является фронтальная плоскость. В группе 12 при перекрестном проведении фиксаторов позвонков в плоскостях, параллельных фронтальной плоскости проекций, под углом (45±1)o к фронтальной оси, проходящей через центр тела соответствующего позвонка, результаты клинических и рентгенологических исследований были аналогичны результатам группы 2 I серии опытов.
При перекрестном проведении фиксаторов позвонков в сагиттальной плоскости (группа 13) полученные результаты клинических и рентгенологических исследований были аналогичны результатам групп 6, 7 III серии опытов (отсутствие подвижности и чувствительности хвоста с последующим развитием некротических изменений дистальных отделов хвоста в 100% случаев).
При фиксации в горизонтальной плоскости (группа 14) сразу после операции наблюдалось отсутствие движений хвоста в 100% случаев (что свидетельствовало о повреждении латеральных мышечных групп), а также в 40% случаев кровотечение из мест вкола фиксаторов (что свидетельствовало о повреждении больших мышечных масс).
Результаты испытаний в V серии опытов показали, что оптимальная длина приспособления составляет 0,25-0,33 (1/4-1/3) длины хвоста (группы 17, 18). В указанных группах результаты клинических и рентгенологических исследований были аналогичны результатам группы 2 I серии опытов.
При использовании вариантов приспособления длиной 0,17 и 0,20 (1/6 и 1/5) длины хвоста (группы 15, 16) полное ушивание операционной раны оказалось технически неосуществимым, вследствие чего в 100% случаев наблюдалось длительное кровотечение из операционной раны, а также в 60% случаев - нагноение в области швов на 3-4 сутки после операции. Результаты рентгенологических исследований: на 7-е сутки после операции - в зоне костной пластики в 40% случаев определялась полость, заполненная слаборентгеноконтрастным содержимым; в 40% случаев - смещение трансплантата относительно материнского ложа и в 10% случаев - наличие полости и смещение трансплантата; на 14-е сутки после операции - в 60% случаев - дефрагментация трансплантата, "изъеденность" тел позвонков; в 20% случаев - усиление смещения позвонков друг относительно друга.
Применение приспособления, длина которого составляла 0,5 (1/2) длины хвоста (группа 19), обусловило нарушение поведенческих реакций подопытных животных (затруднения в питании, перемещении), которые наблюдались, начиная с первых суток после операции, в течение всего срока наблюдения, что свидетельствовало о неоправданном утяжелении конструкции.
На основании результатов VI серии опытов было выявлено, что оптимальным является диаметр вписанной окружности, составляющий 1,8-2,2 диаметра хвоста (группы 22-24). В указанных группах результаты клинических и рентгенологических исследований были аналогичны результатам группы 2 I серии опытов.
В группах 20, 21, где испытывались варианты приспособления с диаметрами вписанной окружности 1,4 и 1,6 диаметра хвоста, на 1-2 сутки после операции отмечалось отсутствие подвижности и чувствительности хвоста (соответственно, в 100 и в 80% случаев); на 3-4 сутки после операции - некротические изменения дистальных отделов хвоста (в 100% случаев), что свидетельствовало о нарушении кровообращения вследствие избыточного сдавливания хвоста.
При использовании приспособлений, диаметры вписанной окружности которых составляли 2,4 и 2,6 диаметра хвоста (группы 25, 26), на 1-2 сутки после операции наблюдалось смещение приспособления вверх или вниз относительно продольной оси хвоста, что приводило к искривлению хвоста в горизонтальной плоскости (соответственно, в 60 и 100% случаев). На рентгенограммах: на 7-е сутки после операции - нарушение соотношения между фиксируемыми позвонками; смещение трансплантата относительно материнского ложа; на 14-е сутки после операции - усиление смещения фиксируемых позвонков друг относительно друга и трансплантата относительно материнского ложа (соответственно, в 60 и 100% случаев).
Достижение обеспечиваемого изобретением технического результата обусловлено следующим. В современной вертебрологии наблюдается большой спрос на костно-пластические и искусственные материалы, обеспечивающие формирование надежного блока между телами позвонков. По данным мировой литературы [3], частота возникновения псевдоартроза при спондилодезе в клинике составляет от 4 до 60%. Известно, что изолированный задний спондилодез не может обеспечить стабильность позвоночника. Поэтому в клинике при нестабильности позвоночника, как правило, применяют передний спондилодез или сочетание переднего и заднего спондилодеза. Последний вариант обеспечивает высокую стабильность в позвоночном двигательном сегменте за счет формирования костного блока между телами позвонков и задними структурами позвоночника [4]. Указанный блок обеспечивает абсолютную стабильность во всех трех колоннах позвоночника (в отличие от блока между телами позвонков, который обеспечивает стабильность только в передней и средней колоннах позвоночника) [5]. Учитывая, что на передние отделы позвоночника приходится до 75% от веса тела человека [5], для проведения операций переднего спондилодеза требуются имплантаты с повышенной механической прочностью. При заднем спондилодезе стабильность в зоне оперированного позвоночно-двигательного сегмента, как правило, обеспечивается специальными металлоконструкциями [4]. Поэтому при заднем спондилодезе основное значение имеют не механические, а остеоиндуктивные и остеопластические свойства имплантатов. Вместе с тем, в современной хирургии позвоночника использование ряда новых металлоконструкций для фиксации [6, 7, 8] позволяет, в ряде случаев, применять при переднем спондилодезе имплантаты с высокими остеоиндуктивным и остеопластическими свойствами, даже если они обладают относительно низкой механической прочностью. В этой связи в настоящее время важную роль играют экспериментальные методы, позволяющие изучать биологические свойства различных имплантатов при спондилодезе. При этом методы экспериментального спондилодеза должны обеспечивать возможность сравнительной проверки имплантатов с различными свойствами для оценки целесообразности использования того или иного имплантата при различных вариантах проведения спондилодеза у людей при максимально возможной простоте и надежности эксперимента и минимальных сроках получения показательных результатов.
Заявленная зона имплантации (между третьим и четвертым хвостовыми позвонками экспериментального животного) обеспечивает возможность формирования костного блока между телами позвонков и задними структурами позвоночника, т. е. возможность моделирования переднезаднего спондилодеза. Это, в свою очередь, позволяет в ходе одного эксперимента одновременно проверять пригодность имплантатов как для переднего, так и для заднего спондилодеза. Подход к позвоночнику животного через верхнюю полуокружность хвоста - дорсальный доступ - позволяет осуществить переднезадний спондилодез с одного разреза. При этом дорсальный доступ наиболее удобен технически, т.к. подопытное животное находится в физиологичном для него положении, и практически полностью исключает возможность повреждения сосудов хвоста, расположенных вентрально. Кроме того, предложенные зона имплантации и дорсальный доступ к позвоночнику позволяют практически полностью исключить возможность повреждения жизненно важных анатомических органов и структур по ходу доступа, в частности органов забрюшинного пространства (аорта, почки, мочеточники), мышц передней брюшной стенки, что сводит к минимуму интраоперационную летальность и уменьшает объем кровотечения в зоне операции. И наконец, заявленные зона имплантации и доступ к позвоночнику позволяют использовать кратковременный масочный или внутримышечный (внутривенный) наркоз без применения интубации и парентерального введения кровезаменителей в интраоперационном и послеоперационном периоде. Это дает возможность избежать послеоперационного возбуждения у подопытных животных, что дополнительно способствует стабильности фиксации, а также позволяет практически полностью исключить возможность развития неврологических нарушений в виде парезов нижних конечностей, расстройств тазовых органов. Кроме того, применение указанного наркоза существенно упрощает постановку эксперимента и сокращает его продолжительность.
Заявленные особенности проведения фиксатора позвонка (через центр тела позвонка в плоскости, параллельной фронтальной плоскости проекций, под углом 40-50o к фронтальной оси, проходящей через центр тела данного позвонка) обусловливают то, что в рабочем положении фиксатор располагается перпендикулярно всем плоскостям, в которых могут происходить движения хвоста при работе различных групп мышц-сгибателей хвоста (латеральной-латеральной и вентральной-дорсальной). Подобное размещение фиксатора обеспечивает блокировку всех возможных видов движений хвоста, что сводит к минимуму вероятность децентрации хвоста (искривления хвоста в горизонтальной плоскости). Это, в свою очередь, способствует сохранению формы материнского ложа для имплантата и практически полностью исключает возможность смещения имплантата (при его относительно высокой механической прочности) или раздавливания имплантата (при его относительно низкой механической прочности).
Известно, что кровоснабжение регенерата (костного блока) обеспечивается как за счет материнского ложа, так и за счет мягких тканей, прилегающих к зоне костной пластики, особенно за счет хорошо кровоснабжаемых мышц [9]. В заявленной зоне имплантации основными источниками кровоснабжения являются костное ложе и латеральные группы мышц, которые, в свою очередь, кровоснабжаются за счет сосудистого пучка хвоста. При выполнении заявленных условий проведения фиксатора позвонка последний проходит в межмышечном пространстве между дорсальными, латеральными и вентральными мышцами и сухожилиями сгибателей хвоста (в дорсолатеральном и вентролатеральном пространстве), не повреждая сосудистого пучка хвоста (артерий и вен). Таким образом, заявленные условия проведения фиксатора позвонка позволяют исключить возможность повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации.
Заявленные условия фиксации (оптимальная плоскость и оптимальный угол фиксации, прохождение оси фиксации через центр тела фиксируемого позвонка, оптимальное количество фиксируемых позвонков и фиксаторов в каждом позвонке, наружная жесткая фиксация свободного конца каждого из фиксаторов) могут быть реализованы, по мнению авторов изобретения, только при использовании предложенного приспособления. Именно основные конструктивные особенности этого приспособления (форма блока фиксации, особенности выполнения и размещения каналов под фиксаторы позвонков) фактически обеспечивают возможность осуществления фиксации так называемым "стержневым" методом (по соотношению размеров фиксатора и фиксируемого позвонка), позволяющим захватывать меньшее количество сегментов и меньшие по размерам сегменты. Авторами изобретения экспериментально установлено, что в заявленном способе при использовании приспособления стабильность расположения фиксируемых позвонков как друг относительно друга, так и относительно имплантата достигается при фиксации двух позвонков (один из которых расположен краниально, а другой - каудально относительно имплантата), причем каждого из них - только одним фиксатором. При этом авторами изобретения экспериментально доказано, что подобная минимизация характеристических параметров фиксации позволяет практически полностью исключить возможность разрушения структур фиксируемых позвонков (даже при их небольших размерах), а также вероятность повреждения спинного мозга. Появляется также принципиальная возможность моделирования спондилодеза на мелких лабораторных животных, в частности на крысах. Наружная жесткая фиксация свободного конца каждого из фиксаторов позвонков, осуществляемая с помощью приспособления, обеспечивает стабильность положения фиксаторов в процессе формирования костного блока. Таким образом, указанные конструктивные особенности приспособления не только обеспечивают соблюдение оптимальных качественных и количественных характеристик условий фиксации в ходе операции спондилодеза, но и позволяют сохранять оптимальный уровень указанных характеристик в динамике эксперимента. Именно указанный комплекс (метод и реализующее его средство) является основой для создания и функционирования в ходе эксперимента системы жесткой внеочаговой наружной фиксации, которая обеспечивает стабильность расположения фиксируемых позвонков в процессе формирования костного блока, при исключении возможности повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации, повреждения жизненно важных анатомических органов и структур позвоночника в зоне фиксации, а также жизненно важных анатомических органов и структур по ходу доступа. В условиях функционирования указанной системы фиксации имплантат играет чисто биологическую роль, выполняя только остеоиндуктивную и остеопластическую функции; функцию фиксатора позвоночника берет на себя приспособление, как неотъемлемый элемент системы. Это, в свою очередь, обеспечивает высокую вероятность формирования у всех подопытных животных полноценного костного блока при постановке имплантатов как с относительно высокой механической прочностью (сопоставимой с прочностью позвонков), так и с относительно низкой механической прочностью.
Кроме того, заявленная последовательность действий и условия их осуществления, в т.ч. использование специального приспособления для фиксации в предложенной конкретной форме его выполнения (с оптимальными параметрами блока фиксации), обеспечивают дополнительное усиление заявленного технического результата, либо достижение дополнительных преимуществ в частных конкретных случаях реализации изобретения. Так, использование в качестве экспериментального животного крысы позволяет дополнительно сократить сроки постановки эксперимента и повысить его надежность. Это обусловлено тем, что крысы обладают высокой выживаемостью, устойчивостью к инфекции и высокой скоростью репарационных процессов. Использование в качестве фиксатора позвонка инъекционной иглы способствует упрощению процедуры фиксации в связи с наличием мандрена. который повышает удобство манипулирования фиксатором.
Предварительное определение области локализации третьего и четвертого хвостовых позвонков обеспечивает повышение точности осуществления доступа к заявленной зоне имплантации, что дополнительно повышает вероятность осуществления переднезаднего спондилодеза с одного разреза, что, в свою очередь, способствует упрощению операции и снижению ее травматичности. При этом линия окончания роста шерсти на хвосте крысы является удобным клиническим ориентиром, который дополнительно увеличивает точность определения области локализации третьего и четвертого хвостовых позвонков.
Формирование ложа для имплантата предложенным методом (удаление вещества диска между третьим и четвертым хвостовыми позвонками экспериментального животного и эпифизарных пластинок тел указанных дисков) при наличии системы жесткой внеочаговой наружной фиксации позволяет исключить необходимость создания паза в телах позвонков, что снижает объем кровотечения из тел позвонков. Кроме того, при формировании ложа заявленным методом не требуется обязательного использования специальной аппаратуры (например, бормашины), что упрощает выполнение указанной процедуры и, следовательно, операции спондилодеза в целом. Предварительное (перед формированием ложа) определение места локализации диска между третьим и четвертым хвостовыми позвонками позволяет упростить процедуру формирования костного ложа и снизить ее травматичность. При этом использование для выполнения указанной процедуры клинического приема, заключающегося в осуществлении принудительных качательных движений хвоста крысы с последующим выявлением зоны неподвижности между телами третьего и четвертого позвонков, позволяет исключить необходимость рентгеновского обследования и скелетизации позвоночника (хирургическая процедура), что дополнительно способствует упрощению рассматриваемой процедуры и снижению ее травматичности.
Заявленное направление проведения фиксатора позвонка, которое выдерживают с помощью приспособления для фиксации (фиксатор вводят с дорсолатеральной стороны хвоста, проводят через соответствующие сквозные каналы под фиксатор позвонка и через тело позвонка и выводят на вентролатеральную сторону хвоста), обеспечивает техническое удобство в ходе осуществления процедуры фиксации, т. к. имеется свободное пространство для манипулирования фиксатором (повышается свобода манипулирования). Кроме того, указанные особенности проведения фиксатора дополнительно способствуют исключению возможности повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации.
Предложенный конкретный прием осуществления наружной фиксации фиксатора позвонка (выполняемое определенным образом и в определенном направлении загибание свободного конца фиксатора) позволяет исключить возможность вращения фиксатора, что дополнительно повышает стабильность фиксации. Кроме того, указанный прием позволяет дополнительно упростить процедуру фиксации, т.к. в этом случае для фиксации свободного конца фиксатора не требуется дополнительных приспособлений или действий (например, наплавления фиксатора).
Конкретная оптимальная форма выполнения блока фиксации приспособления (в виде правильной полой шестиугольной призмы) в сочетании с особенностями выполнения каналов под фиксаторы
позвонков (в частности, их попарная соосность) и их размещения на боковых гранях призмы (в частности, относительно центральной оси призмы и продольных осей симметрии боковых граней) способствует дополнительному повышению точности соблюдения оптимальных условий фиксации. В частности, указанные конструктивные особенности повышают точность установки фиксаторов, что дополнительно увеличивает вероятность проведения каждого из фиксаторов через центр тела фиксируемого позвонка, а также обеспечивает конкретное значение (45o) угла проведения каждого фиксатора (относительно фронтальной оси, проходящей через центр тела данного позвонка), которое находится в середине интервала оптимальных значений указанного параметра (40-50o).
Оптимальная длина приспособления дополнительно повышает стабильность фиксации и упрощает постановку эксперимента. Это обусловлено тем, что, с одной стороны, исключается вероятность нагноения в области швов, что, в свою очередь, дополнительно способствует устранению возможности смещения имплантата относительно материнского ложа и его дефрагментации. С другой стороны, применение приспособления оптимальной длины способствует уменьшению болевого синдрома у экспериментального животного и позволяет обеспечить свободу передвижения последнего по клетке, что обусловливает конкурентоспособность животного в ходе кормления. В результате этого устраняется необходимость изолированного содержания каждого отдельно взятого подопытного животного. Оптимальный диаметр вписанной окружности, с одной стороны, позволяет исключить вероятность тяжелых инфекционных осложнений (некроз дистальных отделов хвоста), которые в ряде случаев могут привести к гибели экспериментального животного. С другой стороны, оптимальные значения указанного параметра способствуют дополнительному повышению стабильности фиксации за счет исключения возможности смещения имплантата относительно материнского ложа, обусловленного искривлением хвоста подопытного животного в горизонтальной плоскости вследствие смещения приспособления из рабочего положения. Наличие смотрового отверстия, размещенного на боковой грани призмы, не содержащей каналов под фиксаторы позвонков, с одной стороны, повышает удобство зашивания операционной раны, что способствует устранению вероятности кровотечения из раны в послеоперационном периоде. С другой стороны, наличие смотрового отверстия в сочетании с особенностями его размещения исключают необходимость проведения рентгенологического контроля в ходе операции и непосредственно после нее, что упрощает операцию спондилодеза и постановку эксперимента в целом. Кроме того, смотровое отверстие дополнительно способствует устранению вероятности повреждения спинного мозга.
Таким образом, именно заявленная совокупность действий (включающая в т. ч. и использование специально сконструированного приспособления для фиксации позвоночных двигательных сегментов экспериментального животного) обеспечивает возможность одновременной оценки пригодности имплантатов с различными биологическими свойствами (в частности, с различными остеоиндуктивными, остеопластическими свойствами, с различной механической прочностью) к использованию как при переднем, так и при заднем спондилодезе, при исключении возможности повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации, повреждения жизненно важных анатомических органов и структур позвоночника в зоне фиксации, а также повреждения жизненно важных анатомических органов и структур по ходу доступа. Это достигается за счет создания условий для формирования блока между телами позвонков и задними структурами позвоночника, а также обеспечения стабильности расположения фиксируемых позвонков в процессе формирования костного блока как друг относительно друга, так и относительно имплантата, при минимизации значений характеристических параметров фиксации. При этом из известного уровня техники не выявляется, по мнению заявителя, влияния предписываемых изобретением преобразований, характеризуемых отличительными от прототипа существенными признаками, на достижение технического результата.
Способ осуществляют следующим образом. В качестве экспериментальных животных используют крыс. В качестве имплантатов могут быть использованы имплантаты с различными биологическими свойствами (в т.ч. с различной механической прочностью), в частности костные трансплантаты (например, приготовленные по стандартным методикам фетальные костные аллотраисплантаты, губчатые отмытые аллотрансплантаты, кортикальные аллотрансплантаты), а также имплантаты из синтетических материалов (например, гидроксиапатитная или корундовая керамика).
Непосредственно перед началом экспериментальной операции по моделированию спондилодеза крысу размещают на операционном столе на животе, фиксируя ее лапы и тело, например с помощью капроновых лент. Крысе дается наркоз, например, эфирный. Производят антисептическую обработку хвоста и задней трети туловища животного, например 96%-ным раствором этилового спирта. Затем определяют область локализации третьего и четвертого хвостовых позвонков, например по линии окончания роста шерсти на хвосте. Выполняют продольный разрез в проекции третьего, четвертого хвостовых позвонков с дорсальной поверхности хвоста животного. Ткани остро и тупо разъединяют до костных структур позвоночника, например с помощью скальпеля и тупфера. После этого дополнительно уточняют место локализации диска между третьим и четвертым хвостовыми позвонками. При этом осуществляют принудительные качательные движения хвоста крысы в горизонтальной плоскости и выявляют подвижные и неподвижные зоны между телами третьего и четвертого позвонков. Зона неподвижности между телами указанных позвонков соответствует месту локализации межпозвонкового диска. Затем формируют ложе для имплантата между третьим и четвертым хвостовыми позвонками. При этом удаляют вещество межпозвонкового диска и эпифизарные пластинки тел третьего и четвертого позвонков механическим путем, например с помощью бормашины при скорости вращения бора 1500 оборотов/мин или с помощью ложечки Фолькмана и маленьких кусачек Листона. В сформированное ложе (паз между позвонками) устанавливают имплантат. После этого осуществляют фиксацию смежных с имплантатом позвонков (третьего и четвертого), например с помощью разработанного авторами изобретения специального приспособления для фиксации позвоночных двигательных сегментов экспериментального животного.
Изобретение поясняется чертежами, где на фиг.1 представлен общий вид используемого в ходе заявляемого способа приспособления (аксонометрическая проекция); на фиг.2 - приспособление в 3-х видах (фронтальный разрез А-А); на фиг.3 - изображение приспособления, установленного в рабочем положении на хвосте крысы (фронтальный разрез Б-Б).
Приспособление, выполненное в виде прямой правильной полой шестиугольной призмы, состоит из стенок (боковых граней призмы) 1, 2, 3, 4, 5, 6; внутренней сквозной полости 7, которая расположена вдоль центральной оси призмы, а ее профиль соответствует профилю наружной поверхности призмы, и шести пар сквозных соосных каналов 8 и 9, 10 и 11, 12 и 13, 14 и 15, 16 и 17, 18 и 19. Сквозные каналы 8, 10, 12 и 9, 11, 13 выполнены на параллельных боковых гранях призмы (стенках), соответственно, 2 и 5, а сквозные каналы 14, 16, 18 и 15, 17, 19 - на параллельных боковых гранях, соответственно, 6 и 3 таким образом, что ось каждой пары каналов, соответственно, 8 и 9, 10 и 11, 12 и 13, 14 и 15, 16 и 17, 18 и 19 пересекает центральную (горизонтальную) ось призмы и продольную ось симметрии каждой из двух взаимно параллельных боковых граней, на которых размещены каналы данной пары. Так, ось KK1 пары каналов 14 и 15 пересекает центральную (горизонтальную) ось призмы в точке О, а также продольную ось симметрии LL1 боковой грани 6 и продольную ось симметрии MM1 боковой грани 3, соответственно, в точках К2 и К3 (фиг.2 вид спереди, вид сверху, вид сбоку). При этом угол между осью KK1 и фронтальной осью O1O2 - угол КОО2 - составляет 45o (фиг.2 вид спереди). Центры входных отверстий сквозных каналов, размещенных на каждой из боковых граней, расположены на продольной оси симметрии соответствующей грани. Так, например, центры входных отверстий каналов 8, 10, 12 размещены на продольной оси NN1 боковой грани 2 (фиг.2 вид сверху, вид сбоку); центры входных отверстий каналов 14, 16, 18 - на продольной оси LL1 боковой грани 6 (фиг.2 вид сверху); центры входных отверстий каналов 15, 17, 19 - на продольной оси MM1 боковой грани 3 (фиг. 2 вид сбоку). При этом центры ближайших от торцов приспособления входных отверстий каналов, например 8, 14, 15, расположены на расстоянии 5-7 мм от соответствующих оснований призмы, а расстояния между центрами входных отверстий каналов, размещенных на одной боковой грани, например каналов 8, 10, 12 на грани 2, каналов 14, 16, 18 на грани 6, каналов 15, 17, 19 на грани 3, равны между собой и составляют 1,5-2 мм. Диаметры поперечного сечения каналов в каждой из пар равны друг другу и соответствуют диаметру поперечного сечения фиксатора позвонка, проводимого через каналы, составляющие данную пару (рабочие каналы). В качестве фиксатора позвонка используют, например, инъекционную иглу (далее - "игла"), спицу и т.п. При использовании иглы с диаметром поперечного сечения 1 мм рабочие каналы, например 8 и 9, 14 и 15, были выполнены с диаметром поперечного сечения, равным 1 мм. Оптимальная длина приспособления (длина каждой из боковых граней призмы) составляет 0,25-0,33 длины хвоста крысы. Например, при длине хвоста 10 см приспособление было выполнено длиной 3,0 см. Оптимальный диаметр окружности, вписанной в шестиугольник, который представляет собой поперечное сечение внутренней полости 7 призмы, составляет 1,8-2,2 наружного диаметра хвоста крысы в области третьего позвонка. Например, при диаметре хвоста 0,5 см приспособление было выполнено с диаметром указанной окружности, равным 1,0 см. Соответственно, ширина боковой грани призмы (сторона шестиугольника в основании призмы) составляла 0,6 см. Приспособление может быть выполнено, например, из полиэтилена. Толщина стенок не менее 1-2 мм. Приспособление дополнительно оборудовано сквозным смотровым отверстием 20, предназначенным для контроля за ходом операции. Смотровое отверстие 20 выполнено на боковой грани призмы, не содержащей каналов под фиксатор позвонка, например на боковой грани 1 призмы. Длина смотрового отверстия составляет 0,8-1,0 длины боковой грани призмы, а его ширина, как правило, соответствует ширине боковой грани. Например, при длине боковой грани 3,0 см и ширине грани 0,6 см размеры смотрового отверстия составили 2,4х0,6 см.
Для осуществления фиксации позвоночных двигательных сегментов экспериментального животного приспособление устанавливают в рабочее положение. При этом хвост 21 крысы вводят во внутреннюю сквозную полость 7 призмы и устанавливают приспособление таким образом, чтобы центральная ось приспособления совместилась с продольной осью хвоста; операционная рана разместилась непосредственно под смотровым отверстием 20; один из торцов приспособления (одно из оснований призмы) расположился у основания хвоста, а второй торец - за пределами операционной раны каудально; две несмежные боковые грани призмы, на которых выполнены сквозные каналы под фиксаторы позвонков, например грани 2 и 6, располагались с дорсолатеральных сторон хвоста, а две другие несмежные боковые грани со сквозными каналами, попарно параллельные указанным граням, например боковые грани 5 и 3, - с вентролатеральных сторон хвоста. Фиксатор позвонка - иглу 22 вводят во входное отверстие сквозного канала 8 под фиксатор позвонка на боковой грани 2 призмы, проводят через указанный канал и выводят через выходное отверстие канала 8 во внутреннюю полость 7 приспособления. Затем вводят иглу 22 через кожу с дорсолатеральной стороны хвоста под углом 40-50o к фронтальной оси, проходящей через центр тела третьего хвостового позвонка (измеряют угол, например, с помощью транспортира). Проводят иглу 22 через центр тела третьего хвостового позвонка 23, выводят на противоположную вентролатеральную сторону хвоста, проводят через сквозной канал 9 на боковой грани 5 призмы и выводят через выходное отверстие указанного канала. Затем выполняют наружную фиксацию иглы 22: загибают иглу, например, с помощью иглодержателя, при этом свободный конец иглы загибают за боковое ребро между боковыми гранями 5 и 4 призмы, а затем поворачивают его на угол 90o на боковую грань 5 призмы (что создает натяжение фиксатора позвонка). Аналогичным образом второй фиксатор позвонка - иглу 24 проводят через сквозной канал 14 на боковой грани 6 призмы, через центр тела четвертого хвостового позвонка, через сквозной канал 15 боковой грани 3 призмы, выводят из приспособления и осуществляют наружную фиксацию иглы. После установки приспособления в рабочее положение (оба фиксатора позвонка проведены через тела хвостовых позвонков под углом 40-50o к фронтальной оси, проходящей через центр тела соответствующего позвонка, и зафиксированы) через смотровое отверстие 20 проверяют визуально правильность положения имплантата в ложе. Затем ушивают операционную рану 2-3 узловыми швами. Через 1,5-2 месяца после операции иглы-фиксаторы извлекают из тел позвонков крысы и из соответствующих сквозных каналов на боковых гранях призмы и приспособление снимают.
Заявленный способ был применен в ходе экспериментальных исследований биологических свойств костных трансплантатов с различной механической прочностью. Производили передне-задний спондилодез у экспериментальных животных согласно заявленному способу с использованием трех видов трансплантатов (производства Российского научно-исследовательского института травматологии и ортопедии им. Р. Вредена /РосНИИТО/, лаборатории заготовки и консервации тканей):
- фетальных костных аллотрансплантатов;
- губчатых отмытых аллотрансплантатов от взрослых особей;
- кортикальных аллотрансплантатов от взрослых особей.
Все виды трансплантатов заготавливались, консервировались и стерилизовались (в модифицированном растворе 31 Е) по стандартным методикам и хранились в холодильнике от 2-х недель до 3-х месяцев при температуре (-8)-(-10)oС.
Было проведено 3 серии опытов на 60 половозрелых лабораторных крысах в стандартных условиях (в каждой серии - по 20 животных). Срок наблюдения за экспериментальными животными - 2 месяца.
Для сравнения все указанные виды трансплантатов были испытаны также в условиях моделирования спондилодеза согласно методике способа-прототипа [2]. Было проведено 3 серии опытов на 30 взрослых беспородных собаках (в каждой серии - по 10 животных). Срок наблюдения за подопытными животными - 4 месяца.
Распределение экспериментальных животных в серии опытов осуществлялось следующим образом:
I серия (крысы) - фетальные костные аллотрансплантаты (от плодов крыс);
II серия (крысы) - губчатые отмытые аллотрансплантаты от взрослых особей (из метафиза бедра крыс);
III серия (крысы) - кортикальные аллотрансплантаты от взрослых особей (из диафиза бедренных костей крыс);
IV серия опытов (собаки) - фетальные костные аллотрансплантаты (от плодов собак);
V серия (собаки) - губчатые отмытые аллотрансплантаты от взрослых особей (из метафиза бедра собак);
VI серия (собаки) - кортикальные аллотрансплантаты от взрослых особей (из диафиза бедренных костей собак).
Результаты испытаний в I-VI сериях опытов оценивали с помощью клинических, рентгенологических, гистологических и патологоанатомических исследований.
В ходе клинических исследований у оперированных животных определяли в пределах срока наблюдения наличие или отсутствие нарушений поведения, неврологических нарушений, состояние раны и хвоста в целом (подвижность, чувствительность, наличие некротических изменений), наличие или отсутствие деформации позвоночника. Оценивали также интраоперационную летальность (количество случаев смерти подопытных животных на операционном столе от кровопотери). При этом умершие во время операции животные были заменены новыми с тем, чтобы численность особей в группе сохранялась постоянной.
Рентгенологические исследования производили на аппарате "Арман 10Л6-01" (производства Казахстанского приборостроительного завода) в двух стандартных проекциях (прямой и боковой). Рентгенограммы выполняли с прямым увеличением в 4 раза на 14-е сутки, на 30-е сутки (через 1 месяц), на 45-е сутки (через 1,5 месяца), на 60-е сутки (через 2 месяца) после операции - у крыс и собак; через 3 и 4 месяца после операции - у собак. По рентгенограммам оценивали в динамике наличие или отсутствие разрушения тел фиксируемых позвонков; правильность соотношения фиксируемых позвонков и положение трансплантата (трансплантатов) относительно ложа; рентгенологические изменения, происходящие в применяемом трансплантате (трансплантатах) и ложе (наличие и ход процесса формирования костного блока и сроки его завершения, либо отсутствие указанного процесса); наличие или отсутствие деформации позвоночника.
Для проведения гистологических исследований животные в каждой серии выводились из опыта в следующие сроки после операции: крысы - через 1,5 месяца (10 животных) и через 2 месяца (10 животных); собаки - через 3 месяца (2 животных) и через 4 месяца (8 животных). При заборе экспериментального материала у крыс извлекали третий и четвертый хвостовые позвонки, у собак - четвертый и пятый поясничные позвонки. Препараты фиксировали в 10%-ном растворе формалина в течение 3-4 недель. Участки, взятые для гистологического исследования, подвергались декальцинации в 10-15%-ном растворе азотной кислоты. После промывки препараты обезжиривали с помощью спирта, после чего заливали в жидкий, а затем - в густой целлоидин. Срезы окрашивали гематоксилин-эозином и по Ван-Гизону по стандартным методикам [10]. Оценивали морфологические изменения, происходящие в применяемом трансплантате (трансплантатах) и материнском ложе (наличие и ход процесса формирования костного блока и сроки его завершения, либо отсутствие указанного процесса).
Патологоанатомические исследования осуществляли следующим образом. После выведения из опыта у каждого животного производили вскрытие зоны операции и выделение места, где была произведена костная пластика. Определяли наличие или отсутствие разрушения тел фиксируемых позвонков, наличие или отсутствие рубцовых изменений мышц в зоне фиксации, а также наличие или отсутствие повреждений органов забрюшинного пространства и мышц передней брюшной стенки. Кроме того, при патологоанатомическом исследовании у каждого животного производили забор ткани из костного блока на гистологию.
Сводные результаты клинических, рентгенологических, гистологических и патологоанатомических исследований представлены в табл.1, 2.
Из данных табл.1 видно, что при моделировании спондилодеза по методике заявленного способа при постановке всех видов испытываемых трансплантатов у всех подопытных животных (в 100% случаев) происходило формирование костного блока между телами позвонков и задними структурами позвоночника, которое завершалось, как правило, в следующие сроки после операции: при использовании фетальных костных аллотрансплантатов (I серия опытов) - через 1,5 месяца; губчатых отмытых аллотрансплантатов от взрослых особей (II серия опытов) - через 1,5-2 месяца; кортикальных аллотрансплантатов от взрослых особей (III серия опытов) - через 2 месяца. При этом, как следует из данных табл.2, не было отмечено также случаев смещения трансплантата (трансплантатов) и деформации позвоночника. Это подтверждалось результатами рентгенологических, гистологических и клинических исследований.
Так, в I-III сериях опытов рентгенологические исследования показали следующее:
на 14-е сутки после операции:
- исчезновение четких контуров трансплантатов; визуализация задних структур позвоночника; правильное соотношение позвонков в зоне костной пластики; четкое стояние трансплантатов в ложе (I-III серии опытов - в 100% случаев);
на 30-е сутки (через 1 месяц) после операции:
- наличие сращения трансплантатов с ложем (с телами смежных позвонков); исчезновение четких очертаний задних структур позвоночника, слияние их в один блок; контуры трансплантатов на прослеживаются; правильное соотношение позвонков в зоне костной пластики (I серия - в 100% случаев; II серия - в 30% случаев);
- наличие сращения трансплантатов с материнским ложем (с телами смежных позвонков); визуализация задних структур позвоночника, контуры трансплантатов прослеживаются; правильное соотношение позвонков в зоне костной пластики (II серия - в 70% случаев; III серия - в 100% случаев);
на 45-е сутки (через 1,5 месяца) после операции:
- между телами позвонков и задними структурами позвоночника сформирован блок; контуры трансплантатов не прослеживаются; правильное соотношение позвонков в зоне костной пластики (I серия - в 100% случаев; II серия - в 30% случаев);
- идет формирование блока между телами позвонков и задними структурами позвоночника; контуры трансплантатов прослеживаются нечетко; правильное соотношение позвонков в зоне костной пластики (II серия - в 70% случаев; III серия - в 100% случаев);
на 60-е сутки (через 2 месяца) после операции:
- результаты аналогичны результатам, полученным на 45-е сутки в I серии опытов (I-III серии - в 100% случаев).
Результаты гистологических исследований:
через 1,5 месяца после операции:
- наличие костно-хрящевых элементов между телами и дугами позвонков, составляющих блок; отсутствие границы между телом позвонка и новообразованной костной тканью (в I серии опытов - у 10 животных; во II серии - у 3 животных);
- преобладание фиброзно-хрящевых элементов между телами и дугами позвонков, составляющих блок, с отдельными костными элементами (во II серии - у 7 животных; в III серии - у 10 животных);
через 2 месяца после операции:
- результаты аналогичны результатам, полученным чрез 1,5 месяца в I серии опытов (I серия - 10 животных; II серия - 10 животных; III серия - 10 животных).
Данные табл. 1 свидетельствуют также о том, что при моделировании спондилодеза у собак по методике способа-прототипа [2] формирование костного блока между телами позвонков имело место только при использовании губчатых (в 60% случаев) и кортикальных (в 40% случаев) аллотрансплантатов (V и VI серии опытов). При этом сроки формирования указанного блока составляли, соответственно, 3-4 и 4 месяца после операции. При спондилодезе фетальными аллотрансплантатами (IV серия опытов) костный блок не формировался. Результаты рентгенологических, гистологических и клинических исследований, представленные в табл. 1, 2, показали, что при постановке фетальных аллотрансплантатов (IV серия опытов) у всех собак происходило раздавливание трансплантатов, что являлось причиной отсутствия формирования костного блока в 100% случаев и обусловливало развитие деформации позвоночника в виде кифоза в поясничном отделе. При использовании губчатых и кортикальных аллотрансплантатов (V и VI серии опытов) имело место смещение трансплантатов, соответственно, в 40 и 60% случаев. Авторами изобретения было установлено, что формирование костного блока происходило, как правило, при отсутствии смещения трансплантата. Смещение трансплантата (с последующим выпадением его из материнского ложа), как правило, коррелировало с отсутствием формирования костного блока, что приводило (как и в IV серии опытов) к развитию деформации позвоночника в виде кифоза в поясничном отделе (в V серии опытов - в 40% случаев, в VI серии опытов - в 60% случаев).
Так, в IV серии опытов рентгенологические исследования показали:
на 14-е сутки после операции:
- трансплантаты прослеживаются как в, так и вне ложа; наличие кифотической деформации в поясничном отделе позвоночника (в 100% случаев);
на 30-е сутки (через 1 месяц) после операции:
- трансплантаты прослеживаются в виде однородной массы как в, так и вне ложа; усугубление кифотической деформации в поясничном отделе позвоночника (в 100% случаев);
на 45-е сутки (через 1,5 месяца) после операции:
- трансплантаты не прослеживаются; усугубление кифотической деформации в поясничном отделе позвоночника; начало формирования псевдоартроза между телами позвонков (в 100% случаев);
на 60-е сутки (через 2 месяца) после операции:
- сохранение кифотической деформации в поясничном отделе позвоночника; наличие псевдоартроза между телами позвонков (в 100% случаев);
через 3 месяца после операции:
- стабилизация кифоза в поясничном отделе позвоночника; наличие псевдоартроза между телами позвонков (в 100% случаев);
через 4 месяца после операции:
- стабилизация кифоза в поясничном отделе позвоночника; сохранение псевдоартроза между телами позвонков (в 100% случаев).
Результаты гистологических исследований:
через 3 месяца после операции:
- наличие фиброзной ткани; единичные элементы костной ткани (в 100% случаев);
через 4 месяца после операции:
- наличие фиброзной ткани; элементы костной ткани отсутствуют (в 100% случаев).
В V и VI сериях опытов получены следующие результаты рентгенологических исследований:
на 14-е сутки после операции:
- четкая визуализация контуров трансплантата; правильное соотношение позвонков в зоне костной пластики; четкое стояние трансплантата в ложе (V серия - в 60% случаев; VI серия - в 40% случаев);
- четкая визуализация контуров трансплантата; нарушение соотношения между фиксируемыми позвонками; смещение трансплантата относительно ложа; наличие кифотической деформации в поясничном отделе позвоночника (V серия - в 40% случаев; VI серия - в 60% случаев);
на 30-е сутки после операции:
- результаты аналогичны результатам, полученным на 14-е сутки (V серия - в 60% случаев; VI серия - в 40% случаев);
- четкая визуализация контуров трансплантата; усиление смещения фиксируемых позвонков друг относительно друга; выпадение трансплантата из ложа; усугубление кифотической деформации в поясничном отделе позвоночника (V серия - в 40% случаев; VI серия - в 60% случаев);
на 45-е сутки после операции:
- результаты аналогичны результатам, полученным на 14-е сутки (V серия - в 60% случаев; VI серия - в 40% случаев);
- четкая визуализация контуров трансплантата вне ложа; усугубление кифотической деформации в поясничном отделе позвоночника (V серия - в 40% случаев; VI серия - в 60% случаев);
на 60-е сутки (через 2 месяца) после операции:
- исчезновение четких контуров трансплантата; правильное соотношение позвонков в зоне костной пластики (V серия - в 60% случаев; VI серия - в 40% случаев);
- исчезновение четких контуров трансплантата; сохранение кифотической деформации в поясничном отделе позвоночника; начало формирования псевдоартроза между телами позвонков (V серия - в 40% случаев; VI серия опытов - в 60% случаев);
через 3 месяца после операции:
- между телами позвонков сформирован костный блок; контуры трансплантата не прослеживаются; правильное соотношение позвонков в зоне костной пластики (V серия - в 20% случаев);
- идет формирование блока между телами позвонков; контуры трансплантата прослеживаются нечетко; правильное соотношение позвонков в зоне костной пластики (V серия - в 40% случаев; VI серия - в 40% случаев);
- контуры трансплантата прослеживаются нечетко; стабилизация кифоза в поясничном отделе позвоночника; наличие псевдоартроза между телами позвонков (V серия - в 40% случаев; VI серия - в 60% случаев);
через 4 месяца после операции:
- между телами позвонков сформирован костный блок; контуры трансплантата не прослеживаются; правильное соотношение позвонков в зоне костной пластики (V серия - в 60% случаев; VI серия - в 40% случаев);
- контуры трансплантата не прослеживаются; стабилизация кифоза в поясничном отделе позвоночника; сохранение псевдоартроза между телами позвонков (V серия - в 40% случаев; VI серия - в 60% случаев).
Результаты гистологических исследований:
через 3 месяца после операции:
- наличие костно-хрящевых элементов между телами позвонков; отсутствие границы между телами позвонков и новообразованной костной тканью (V серия - в 20% случаев);
- преобладание фиброзно-хрящевых элементов между телами позвонков, составляющих блок, с небольшим количеством костных элементов (V серия - в 40% случаев; VI серия - в 40% случаев);
- наличие фиброзной ткани между телами позвонков (V серия - в 40% случаев; VI серия - в 60% случаев);
через 4 месяца после операции:
- наличие костно-хрящевых элементов между телами позвонков; отсутствие границы между телами позвонков и новообразованной костной тканью (V серия - в 60% случаев; VI серия - в 40% случаев);
- наличие фиброзной ткани между телами позвонков (V серия - в 40% случаев; VI серия - в 60% случаев);
Данные, представленные в табл.2, показывают, что применение заявленного способа моделирования обеспечивало во всех сериях опытов (I-III) отсутствие случаев со смертельным исходом во время операции, а также практически полное отсутствие нарушений поведения и неврологических нарушений. У всех подопытных животных после операции сохранялась подвижность и чувствительность хвоста (клинические наблюдения). Результаты патологоанатомических исследований показали практически полное отсутствие рубцовых изменений всех групп мышц (вентральной, латеральной, дорсальной) в зоне фиксации, а также отсутствие каких-либо повреждений органов забрюшинного пространства и мышц передней брюшной стенки у всех крыс во всех сериях опытов (I-III).
При осуществлении спондилодеза по методике способа-прототипа (как это видно из табл.2) у всех собак (в 100% случаев) во всех сериях опытов (IV-VI) наблюдались нарушения поведения в виде длительного послеоперационного возбуждения (в течение 1-2 суток после операции). По результатам клинических исследований были отмечены неврологические нарушения в виде парезов нижних конечностей различной степени выраженности и расстройств тазовых органов (в первые сутки после операции):
- при использовании фетальных аллотрансплантатов - в 100% случаев (у 10 собак - парезы нижних конечностей, в т.ч. у 5-ти из них - в сочетании с расстройствами тазовых органов);
- при использовании губчатых аллотрансплантатов - в 40% случаев (у 4 собак - парезы нижних конечностей, в т.ч. у одной из них - в сочетании с расстройствами тазовых органов);
- при использовании кортикальных аллотрансплантатов - в 30% случаев (у 3 собак - парезы нижних конечностей, в т.ч. у одной из них - в сочетании с расстройствами тазовых органов).
Патологоанатомические исследования показали наличие рубцовых изменений в области передней продольной связки и мышц-сгибателей позвоночника (подвздошно-поясничных мышц) у всех собак IV-VI серий опытов (в 100% случаев), а также наличие рубцовых изменений в области мышц передней брюшной стенки (в IV-VI сериях в 100% случаев), и, в ряде случаев, повреждения мочеточников (в IV серии - у 3 собак; в V серии - у 4 собак; в VI серии - у 2 собак). Кроме того, были зафиксированы случаи повреждения аорты с кровоизлиянием в забрюшинное пространство (смерть на операционном столе от кровопотери): при применении фетальных и губчатых отмытых аллотрансплантатов (IV и V серии опытов) - у 2 собак (в каждой серии); кортикальных аллотрансплантатов (VI серия опытов) - у 1 собаки.
Данные табл.1, 2 свидетельствуют также о том, что с помощью заявленного способа оценка свойств трансплантатов во всех сериях опытов (I-III) могла быть произведена на всех животных каждой из подопытных групп (за счет формирования костного блока у 100% животных и исключения интраоперационной летальности). С помощью способа-прототипа подобная оценка могла быть произведена только у 50% подопытных животных при постановке губчатых аллотрансплантатов (V серия опытов) и у 30% подопытных животных при постановке кортикальных аллотрансплантатов (VI серия опытов).
Таким образом, проведенные сравнительные испытания показали, что заявленный способ обеспечивает возможность оценки пригодности имплантатов (в частности, костных трансплантатов) к использованию как при переднем, так и при заднем спондилодезе, тогда как способ-прототип - только при переднем спондилодезе. Заявленный способ позволяет также оценивать имплантаты с различной механической прочностью, в т.ч. имплантаты с относительно низкими прочностными характеристиками (в частности, фетальные костные аллотрансплантаты). Способ-прототип пригоден только для оценки имплантатов, прочностные характеристики которых сопоставимы с прочностью позвонков (в частности, губчатые и кортикальные аллотрансплантаты от взрослых особей). При этом при использовании заявленного способа сроки постановки эксперимента сокращаются на 1,5-2 месяца, а достоверность оценки свойств имплантата увеличивается (по сравнению со способом-прототипом). Кроме того, заявленный способ позволяет практически полностью исключить возможность повреждения анатомических органов и структур, являющихся источниками кровоснабжения зоны имплантации, повреждения жизненно важных анатомических органов и структур позвоночника в зоне фиксации, а также повреждения жизненно важных анатомических органов и структур по ходу доступа. И наконец, заявленный способ, в отличие от способа-прототипа, является технически простым в выполнении и обеспечивает относительно высокую надежность эксперимента.
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Султангазин Б.И.
Сравнительная оценка некоторых видов переднего спондилодеза в эксперименте: Автореф. дис. на соиск. учен. степ. канд. мед. наук / Карагандинский госуд. мед. ин-т. - Караганда, 1972. - 20 с.
2. Брус И.Г.
Пластические операции на позвоночнике формализованными гомотрансплантатами (экспериментальное исследование): Автореф. дис. на соиск. учен. степ. канд. мед. наук / Кишиневский госуд. мед. ин-т. - Кишинев: Изд-во ЦК КП Молдавии, 1972. - 17 с. (прототип).
3. Bradford D.S.
Instrumentation of the Lumbar Spine. // Clinical Orthopedics and Related Research. - 1986 (203). - P. 209-218.
4. Ульрих Э.В.
Аномалии позвоночника у детей. - СПб.: Сотис, 1995. - С.226-252.
5. Denis F.
The three column spine and its significance in the classification of acute thoracolumbar spinal injures // Spine. - 1983. - 8. - Р. 817-831
6. Gurr K.R, McAfee P.C, Shih C.M.
Biomechanical analysis of anterior and posterior instrumentation systems after corpectomy // J.-Bone and Joint Surgery. - Am. vol. 70 (8)1988. - P. 1182-1191.
7. Hopf C.
Indikation und Ergebnisse des CD-Verfahrens in der operativen Skoliosetherapie // Beitr. Orthopad Traumatol - 1990 - 37, 7 - S.401-403.
8. Ryan.
Bolt-Plate Fixation for Anterior Fusion // Clinical Orthopedics and Related Research. - (203) 1986. - Р.196.
9. Торгашева Г.Я.
Частичное замещение тел позвонков в эксперименте: Автореф. дис. на соиск. учен. степ. канд. мед. наук - Новосибирск, 1969. - 15 с.
10. Учебник гистологии. / Под ред. Ю.И. Афанасьева и Н.А. Юриной. Изд. 4-е. - М.: Медицина, 1989. - С.9-18.
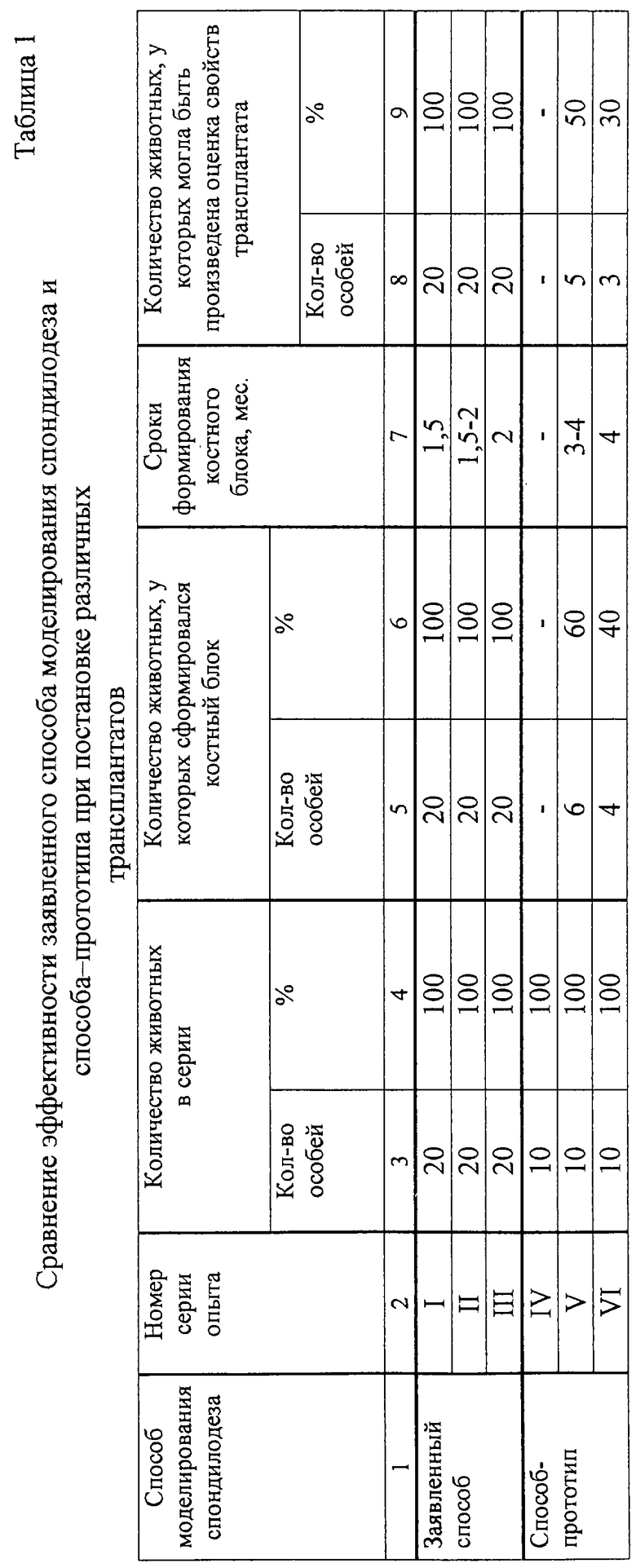
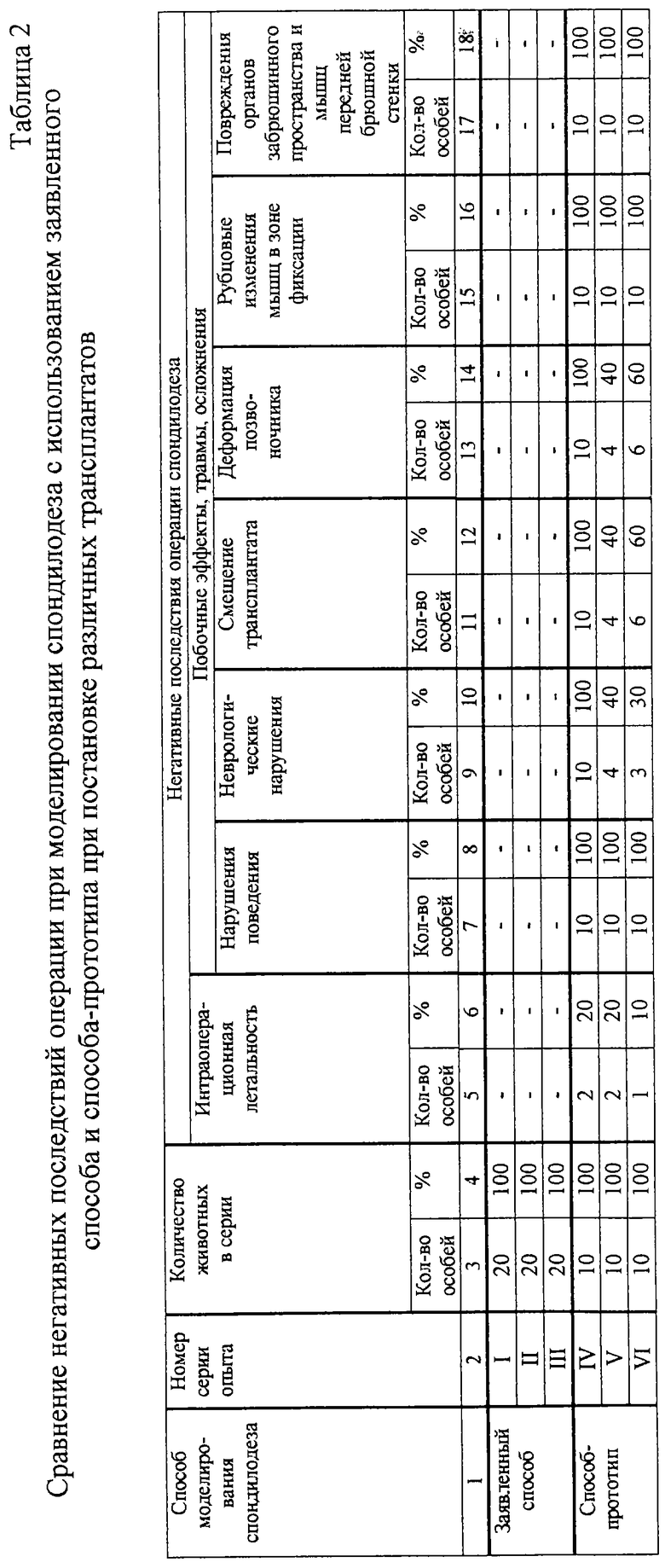
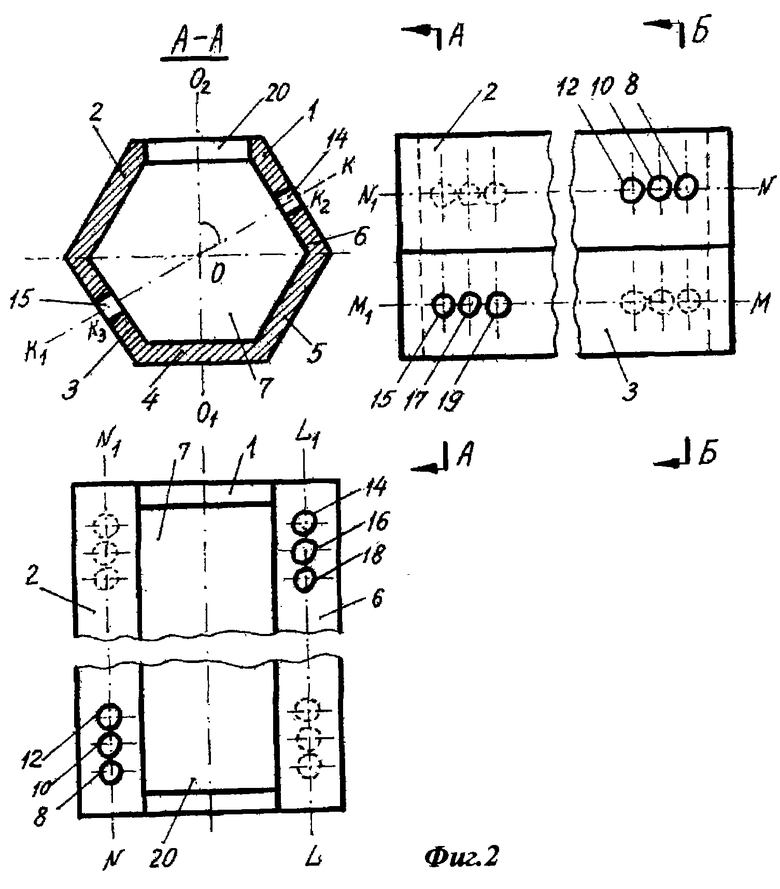
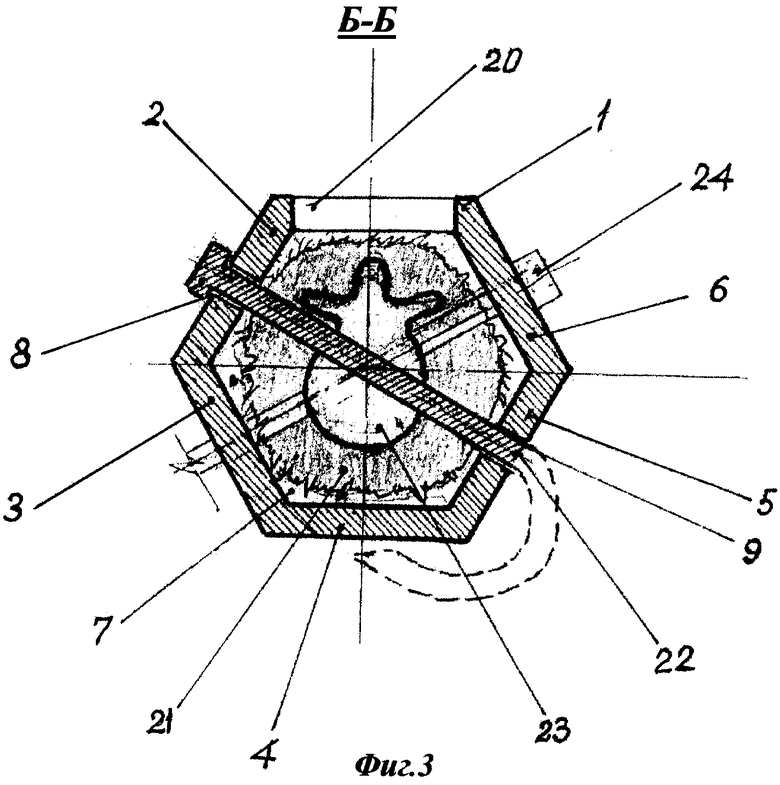
Изобретение относится к моделированию в медицине и может быть применимо для моделирования спондилодеза. Осуществляют доступ к позвоночнику экспериментального животного с дорсальной поверхности его хвоста. Формируют ложе для имплантата и устанавливают имплантат между третьим и четвертым хвостовыми позвонками. Фиксируют имплантат путем фиксации смежных с имплантатом позвонков двумя фиксаторами позвонков. Проводят фиксаторы перекрестно через центры тел указанных позвонков под углом 40-50o к фронтальной оси, проходящей через центр тела позвонка. Производят наружную жесткую фиксацию свободного конца каждого из фиксаторов позвонков с помощью приспособления для фиксации. Приспособление для фиксации выполнено в виде прямой правильной полой шестиугольной призмы, на четырех попарно параллельных боковых гранях которой размещено не менее двух пар сквозных попарно соосных каналов под фиксаторы позвонков, оси каждой из которых пересекают центральную ось призмы и продольную ось симметрии каждой из двух взаимно параллельных боковых граней призмы, на которых размещены каналы данной пары. Способ позволяет повысить достоверность оценки свойств имплантата, исключить возможность повреждения источников кровоснабжения зоны имплантации, упростить технику вмешательства. 9 з.п.ф-лы, 2 табл., 3 ил.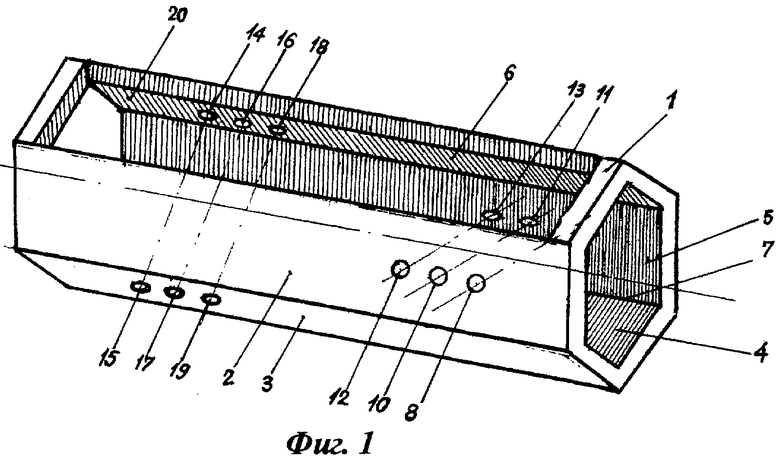
| WHITEHILL R | |||
| Posterior cervisal fusions using cerclage wires, methylmethacrylate cement and autogenous bone graft | |||
| An experimental studu of a canine model | |||
| Реферат из АДБ "Medline": - Spine, 1987, Jun-Feb; 12(1):12-22 | |||
| СПОСОБ МОДЕЛИРОВАНИЯ ПЕРЕДНЕГО СПОНДИЛОДЕЗА ПОЯСНИЧНЫХ ПОЗВОНКОВ | 1991 |
|
SU1823674A1 |
| ОСТРОВЕРХОВ Г.Е | |||
| и др | |||
| Оперативная хирургия и топографическая анатомия | |||
| - Курск, 1995, с.499 и 500. | |||
Авторы
Даты
2003-09-10—Публикация
2001-09-28—Подача