Это - частичное продолжение заявки на патент США 08/232502, поданной 25 апреля 1994 г., которая является продолжением частичного продолжения заявки на патент США 07/986189, отклоненной в настоящее время заявки на патент США 07/802963, называемой "Усовершенствованный способ и устройство для приготовления и введения инфузионных растворов для анестезии", автором которой является д-р Edward Teeple.
Настоящее изобретение относится к способу и устройству для приготовления растворов препаратов для постоянного вливания пациенту и особенно к усовершенствованному, экономичному и надежному способу и устройству для использования квалифицированными врачами и другими специалистами, при котором количество препарата определяется на основании стандартизированной скорости вливания.
При лечении больных могут применяться многие классы средств для внутривенного введения, такие как средства для общей анестезии или добавки ингаляционных анестетиков; препараты, вызывающие нервно-мышечную блокаду; кардиореанимационные препараты для применения в неотложной терапии и многие другие. Часто анестезиологи применяют один или более препаратов для методик постоянного вливания. Однако существующие в настоящее время способы и устройства для внутривенного вливания различных препаратов, в частности анестезирующих препаратов, имеют множество описанных здесь недостатков.
Предшествующие способы введения анестезирующих препаратов
Практика вливания множества препаратов может быть обременительной и трудной ввиду наличия большого числа переменных величин и трудности запоминания каждого важного фактора, задействованного при введении одного препарата или комбинации препаратов. В прошлом при попытке определить соответствующий диапазон доз анестезирующих препаратов в различных медицинских условиях анестезиологи полагались на память. Многие анестезиологи выбирали лишь одно или два средства для упрощения сложных композиций, которые иначе следует применять, и запоминания требований введения, относящихся к этим одному или двум конкретным средствам. К сожалению, ограничение числа препаратов в арсенале анестезиолога может резко ограничить возможность анестезиолога подбирать анестезию в соответствии с определенными нуждами пациента.
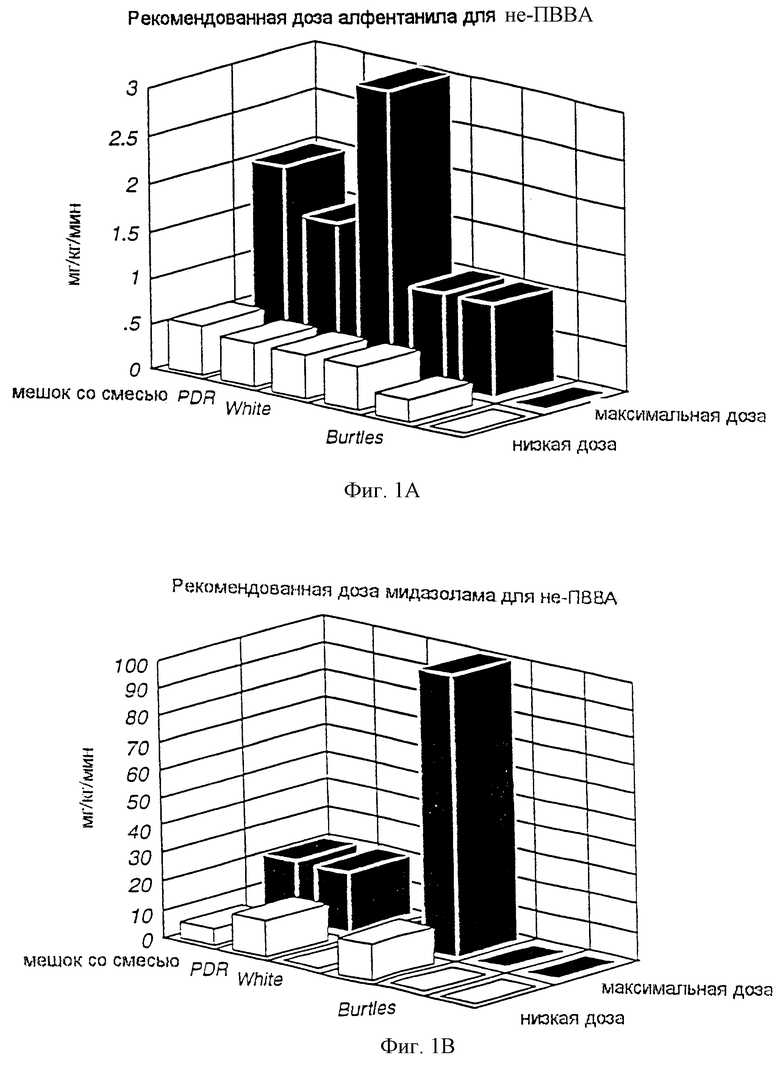
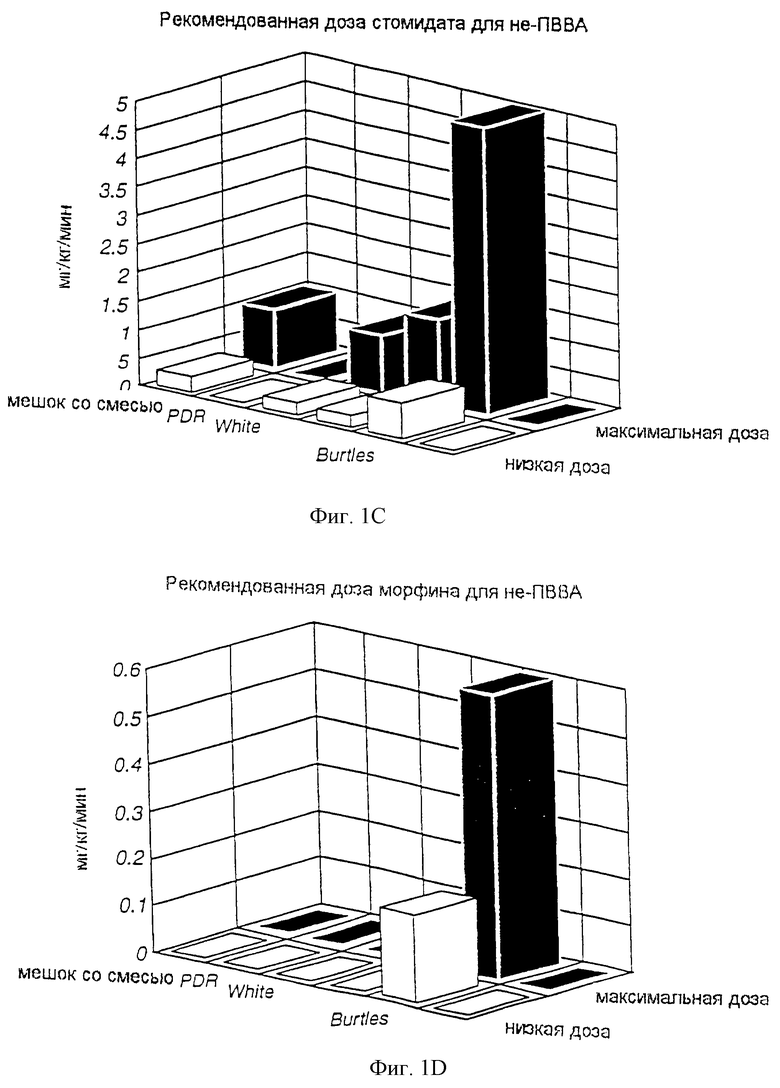
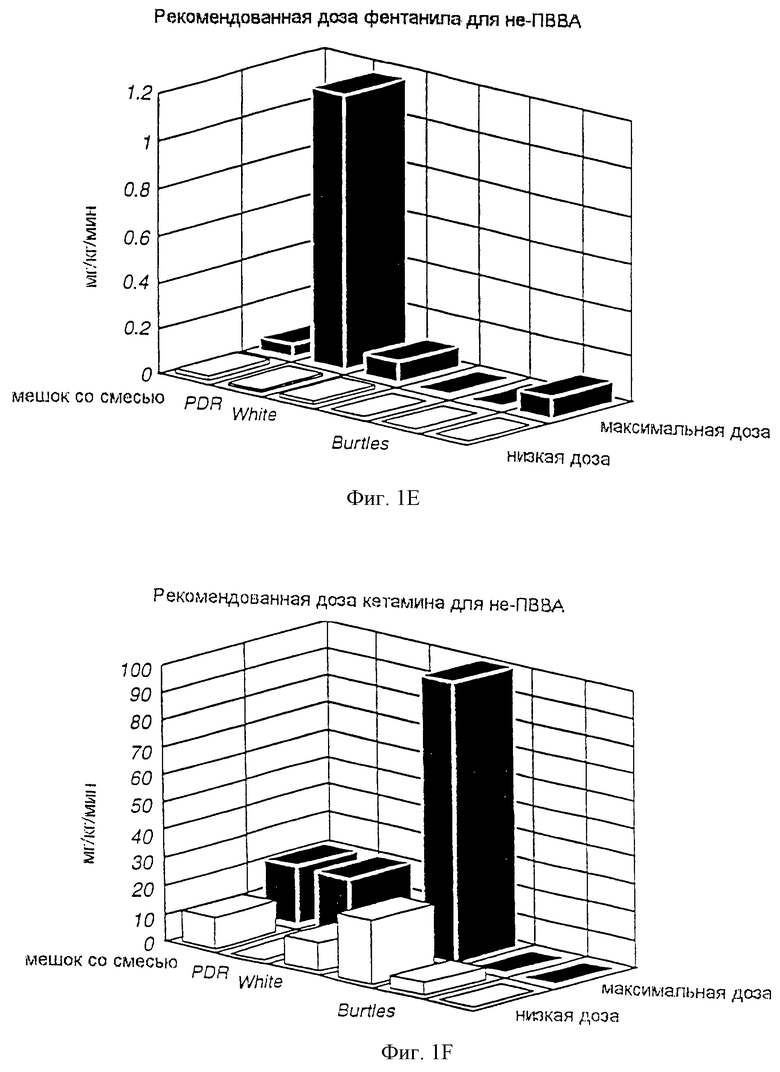
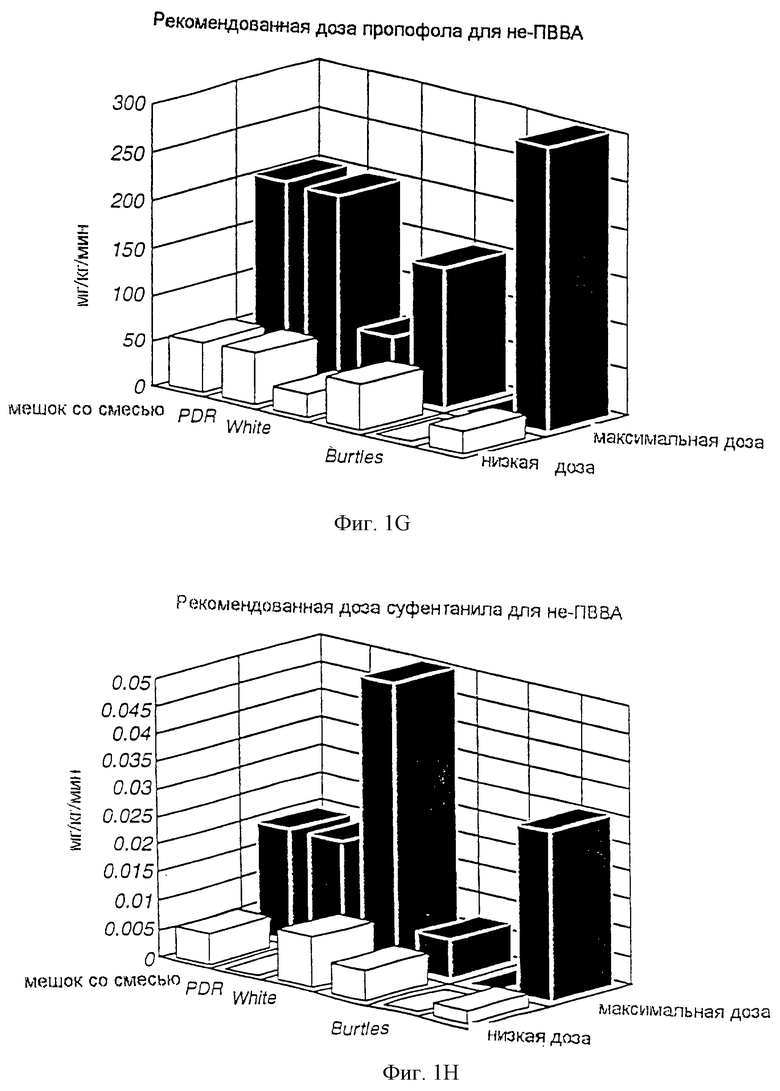
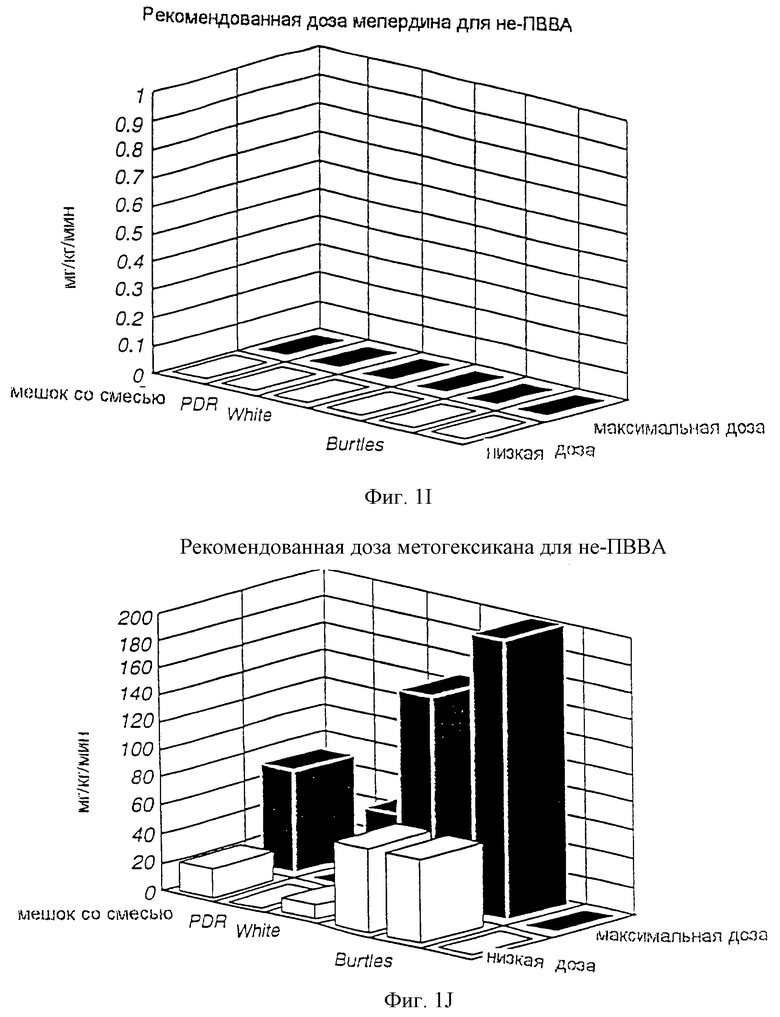
Кроме того, память анестезиолога основывается на опыте, чтении о рекомендуемых диапазонах доз в Physician Desk Reference ("PDR"), чтении о рекомендуемых диапазонах доз в литературе и взаимодействиях с представителями фармацевтических компаний. К сожалению, рекомендуемые этими источниками безопасные диапазоны лекарственных доз не согласованы и по рекомендуемым диапазонам доз существуют большие расхождения. На фиг.1 схематически представлены диапазоны доз, рекомендуемые в различных литературных источниках. Предлагаемые диапазоны также не отражают принятие во внимание конкретных случаев применения, требующих существенного подбора дозы и скорости введения, например при операциях на сердце. Кроме того, безопасные диапазоны анестезирующих препаратов варьируют в зависимости от способа ведения анестезии. Тем не менее безопасные диапазоны доз, описанные в обычных источниках по анестезирующим препаратам, не отражают учет способа проведения анестезии.
Например, с точки зрения определенных препаратов, в PDR не производится поправка рекомендуемых диапазонов доз при использовании полной внутривенной анестезии (ПВВА) в сравнении с использованием не-ПВВА. В предшествующем уровне техники также не описан способ анестезии, который в достаточной степени исключает накопление препаратов и предотвращает замедленный выход пациента из анестезии. Многие из предложенных в предшествующем уровне техники диапазонов доз слишком агрессивны и часто приводят к их передозировке у пациентов вследствие синергического эффекта при комбинировании множества препаратов. Подводя итог можно сказать, что данные литературы и имеющиеся ресурсы в значительной степени не соответствуют потребностям с точки зрения предоставления анестезиологам безопасных диапазонов доз для препаратов или способа внутривенного введения.
Были предложены уравнения, которые якобы позволяют анестезиологу рассчитать соответствующие дозы в каждом конкретном случае, причем эти уравнения настолько сложны, что их использование ограничено и приводит к множеству ошибок расчета. Многие анестезиологи понимают фармакокинетические принципы анестезии посредством классической трехкомпартментальной модели. Трехкомпартментальная модель используется для описания нескольких способов введения анестезирующих средств. В соответствии с трехкомпартментальной моделью препарат, помещенный в компартмент 1, возвратно перемещается между компартментами 1 и 2 с постоянными скоростями k12 и k21, a между компартментами 1 и 3 - с постоянными скоростями k13 и k31 до тех пор, пока препарат не будет необратимо удален из компартмента 1 с постоянной скоростью k10. Объем компартментов 1, 2 и 3 известен соответственно как V1, V2 и V3. Движение препарата между компартментом 1 и компартментами 2 и 3 известно как "распределение", а необратимое движение препарата из компартмента 1 известно как "выделение". Выделение препарата отражает метаболизм или выведение препарата. Предполагается, что при бесконечном продолжительном вливании стационарная концентрация препарата в каждом компартменте равна и, следовательно, общий объем распределения составляет Vτ, где Vτ=V1+V2+V3. Скорость, с которой препарат удаляется из центрального компартмента, прямо пропорциональна объему препарата в центральном компартменте. Таким образом, клиренс центрального компартмента, т. е. скорость выделения из центрального компартмента, составляет Cl1, которая определяется выражением V1k10. Было предложено много уравнений для попытки количественного определения движения анестетических препаратов у пациентов в соответствии с этой моделью. См., например, White и табл. 1, в которой Vc представляет собой объем клиренса, который равен определяемому уровню концентрации препарата в крови. Vc обратно пропорционален концентрации препарата в клетках. Vdss представляет собой стационарный объем распределения. К сожалению, у этой модели есть несколько существенных ограничений. Например, концентрация в плазме крови часто ведет к воздействию концентрации на конечный орган при вводном наркозе и отставанию при выходе из наркоза. Величины Vdss представлены здесь для обеспечения возможности сравнения методики White и настоящего изобретения.
Самый обычный существующий способ вливания множества препаратов требует от анестезиологов определения доз, которые они предполагают ввести пациенту, в соответствии со следующим громоздким уравнением 1:
D•BW•60=C•R
Переменные величины для уравнения 1 определяются следующим образом:
D = скорость введения дозы, выраженная в мкг/кг/мин;
BW = вес тела, выраженный в кг;
С = концентрация вливаемого препарата, выраженная в мкг/мл;
R = скорость вливания, выраженная в мл/ч.
(Константа = 60 мин/ч)
Уравнение 1 включает в себя пять "неизвестных" ("С", включающее в себя две переменные величины: числитель (вес в мг) и знаменатель (объем в мл), требующие, чтобы каждый раз при приготовлении и использовании лекарственной смеси производилась серия расчетов). Эти сложные расчеты делают применение методик инфузии трудоемким и увеличивают риск ошибки человека. Необходимость обеспечения интенсивной терапии в сочетании с необходимостью длительной работы медицинского персонала допоздна делает желательным любой способ, который снижает возможность ошибки.
Ввиду варьирующего веса пациентов желаемая скорость потока препарата варьирует в каждом случае. Соответственно при использовании методики, описанной уравнением 1, становится очень трудно во время клинических процедур проводить повторную переоценку дозы препарата, которую получает пациент. Одним способом решения этой проблемы была стандартизация концентраций препаратов. Однако при использовании этого способа остается существенная проблема: еще меняется скорость доставки. Кроме того, уравнение не учитывает синергический эффект при использовании множества анестетических средств, что является обычным способом анестезии или потребности определенного вида операций, например операций на сердце.
Таким образом, в условиях способа предшествующего уровня техники, когда анестезиолога внезапно вызывают для введения препарата пациенту, анестезиолог вынужден полагаться на свою память о противоречивых и неточных безопасных диапазонах доз препаратов, которые он предполагает использовать в схеме, которую он предполагает назначить пациентам, или анестезиолог должен пытаться манипулировать с громоздкой формулой, которая включает в себя слишком много переменных величин.
Устройства предшествующего уровня техники для введения анестетических средств
Устройства, которые были разработаны для внутривенного введения препаратов, включая анестетические препараты, имели множество недостатков, которые мешали анестезиологам. Например, несколько способов внутривенного вливания основаны на устройстве в виде насоса и шприца для доставки анестетических препаратов. К сожалению, шприцевые насосы, использованные в таких устройствах и не точны, и не обеспечивают эффективную доставку препаратов в систему, требуются низкие объемы. При низких объемах препараты, доставка которых предполагается, часто теряют активность в трубчатых магистралях таких устройств. Во многих таких устройствах по меньшей мере 1 см3 препарата, доставка которого предполагается, остается в трубчатых магистралях устройства, в других в трубках остается до 5 см3. Во-вторых, у различных компаний варьируют объемы шприцев, используемых с насосом, и шприцевых устройств. Такое различие вызывает доставку насосами и шприцевыми устройствами различных доз препаратов даже при выборе одинаковой скорости титрования. В-третьих, известно, что используемые в шприцах поршни подвержены сопротивлению в цилиндре шприца. Сопротивление вызывает неравномерное продвижение поршня в полости шприца. Неравномерное движение поршня в полости шприца вызывает неравномерную доставку препарата, т.е. при преодолении сопротивления препарат (препараты) подается небольшими порциями, а не продолжительно в постоянном количестве. Другая проблема, мешающая реализации способов, основанных на шприцах, состоит в том, что такие способы часто требуют перезарядки шприца во время процедуры.
Другие способы основаны на компьютеризированных устройствах доставки, которые автоматически подбирают скорость в зависимости от потребностей анестезии. Однако такие устройства крайне дороги, что делает их экономически нерентабельными для многих операционных. Кроме того, ведение анестезии является искусством, а также наукой, и полностью компьютеризированная система не может полностью заменить необходимость в проводящем анестезию враче для оценки, понимания и манипуляции с факторами, связанными с применением каждого препарата, для облегчения соответствующих корригирующих мероприятий на основании клинической реакции пациента на введенные препараты, т.е. даже устройства "замкнутого цикла" требуют тщательного контроля. Например, модели полностью замкнутого цикла не могут учитывать изменение стимула, что часто встречается в хирургии. Кроме того, ввиду отсутствия способа, гарантирующего определение того, спит ли пациент или находится в бессознательном состоянии, устройства замкнутого цикла противопоказаны. Наконец, оказалось, что при использовании множества анестетических средств работа устройств полностью замкнутого цикла невозможна.
Инфузионные насосы также хорошо известны, хотя во многих клинических учреждениях дороговизна этих устройств может препятствовать их использованию. См. "Infusion Pumps", Milestones in Anesthesia, pp.2-3.
См. также Burtles, Richard; "Continuous Infusion of Drugs: A Simple and Rational System", Journal of Cardiothoracic and Vascular Anesthesia, 1991; 5(4):362-364; Tilden, Samuel and Hopkins, Robert L.; "Calculation of Infusion Rates of Vasoactive Substances", Annals of Emergency Medicine, 1983; 12: б97-99. Наконец, многие устройства и способы внутривенной подачи требуют длительных и дорогостоящих мероприятий по наладке. Например, если используется множество анестетических средств, необходимо множество инфузионных насосов.
Различные патенты и другие ссылки раскрывают способы и устройства для приготовления и внутривенного введения анестетических препаратов.
В патенте США 4853521 раскрыто устройство для верификации и регистрации введения препарата пациенту, включающее в себя компьютеризированную систему для проведения подачи.
В патенте США 4898578 раскрыто устройство для инфузии препаратов, которое обеспечивает возможность дискретного определения различных переменных величин обычно используемых способов инфузии.
В патенте США 4058120 раскрыт поворотный магазин испарителя для наркозного аппарата.
В патентах США 4246894 и 4334526 раскрыты способ и устройство для проведения общей анестезии диссоциативного типа.
В патенте США 5015781 раскрыты анестетическое соединение и способ его получения.
В патенте США 4917670 раскрыты устройство и способ проведения продолжительной спинальной анестезии.
В патенте США 4873076 и в аналогичных ссылках раскрыт способ безопасного обеспечения анестезии или седативного эффекта с сохранением сознания.
В патенте США 4825860 раскрыто устройство для доставки систем подачи анестетиков.
В патенте США 4053604 раскрыт способ усовершенствования смесей и композиций для анестезии.
Paul F. White в своей статье "Clinical Uses of Intravenous Anesthetic and Analgetic Infusions". Anesthesia and Analgesia, 1989; 68:161-71 (далее именуемой "статья White") описывает возможности клинического применения продолжительной инфузионной анестезии, но не рассматривает усовершенствованные способы настоящего изобретения.
Поэтому стало желательно разработать способ приготовления растворов препаратов для постоянной инфузии, который лишен недостатков предшествующих способов.
В целом, настоящее изобретение представляет собой способ приготовления раствора препарата для постоянной инфузии, который обеспечивает следующие этапы: установление стандартизированного диапазона дозировки; установление стандартизированного диапазона скорости инфузии и определение требуемой концентрации препарата на основании веса пациента, стандартизированного диапазона дозировки и стандартизированного диапазона скорости инфузии. Предпочтительно эти этапы повторяются для ряда препаратов с нарастанием веса для установления эталонной таблицы требуемых концентраций. Концентрации предпочтительно определяются на стандартной миллилитровой основе для обеспечения возможности легкого определения количества препарата (препаратов), который нужно добавить в растворитель в инфузионном мешке. Кроме того, стандартизированная скорость дозирования предпочтительно основана на максимальной поддерживающей скорости инфузии, установленной для препарата.
Анестезия, проводимая в соответствии с настоящим изобретением, индуцируется в соответствии со стандартными методиками анестезии с использованием соответствующей дозы насыщения. Препарат, используемый для поддерживающей анестезии, может также вводиться в виде непосредственной внутривенной премедикации, т.е. в качестве праймера или для индукции анестезии. Умелые, опытные анестезиологи понимают, что "примирование" пациента к анестетику повышает реактивность пациента на анестезию и позволяет анестезиологу избежать подачу большого начального болюса для начала анестезии. Подача меньшего болюсного количества для индукции анестезии позволяет анестезиологам снизить вероятность подачи токсических количеств анестетика и уменьшает общее количество анестетика, используемого для индуцирования анестезии у пациента. Уменьшенное количество требуемого анестетика может снизить стоимость анестезии. Таким образом, методология проведения анестезии может обеспечить введение дозы насыщения, которая направлена на удовлетворение конкретных потребностей пациента и учитывает способ, который предполагается использовать для поддержания анестезии. Как при большинстве анестетических процедур, доза насыщения быстро повышает концентрацию препарата в плазме до желаемого уровня, а поддерживающая скорость введения возмещает потерю препарата на метаболизм и выведение.
Таким образом, после индукции начинается и продолжается поддерживающая инфузия. Потребности в анестетике варьируют в соответствии с предполагаемой оперативной процедурой, здоровьем и состоянием пациента, продолжительностью процедуры и многими другими факторами. Частичный перечень таких факторов представлен в табл. 1. Эти факторы учитываются при установлении диапазона концентрации препарата (препаратов), который предполагается ввести пациенту во время процедуры.
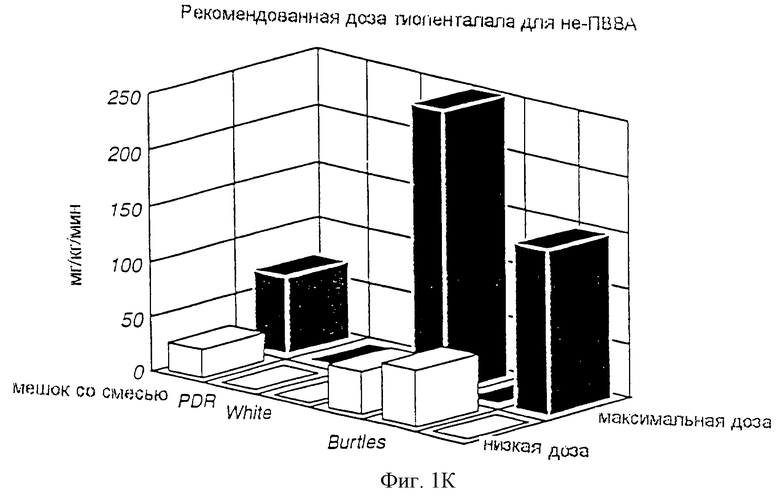
В соответствии с настоящим изобретением в качестве стандарта для подачи высокой (или "максимальной") дозировки инфузии используется стандартизированная скорость инфузии, предпочтительно 30 мл/ч. Однако если предполагается в качестве препарата для продолжительной инфузии использование дополнительного анестезирующего средства, скорость инфузии соответственно уменьшается. На фиг.2 показана стандартизированная кривая титрования со снижением концентрации, которая используется с целью избежания накопления препарата во время анестезии. На ней также показано время отключения для предоставления возможности человеку насколько возможно быстро выйти из наркоза в конце операции. Кроме того, часто необходимо подобрать скорость, а следовательно, количество подаваемого препарата на основании клинической реакции пациента на препарат (препараты). Настоящее изобретение позволяет анестезиологу делать поправку на эти факторы. На фиг.3 представлен эталон для интерпретации диапазонов скорости от низкого до высокого для десяти соответствующих препаратов для анестезии.
Настоящее изобретение может также использовать устройство для определения и/или приготовления раствора препарата для постоянной инфузии, которое может включать в себя:
1) средство для ввода данных;
2) запоминающее средство для хранения данных, причем запоминающее средство имеет хранящиеся в нем заранее установленную скорость дозирования препарата и стандартизированную скорость инфузии, зависящую от применения препарата;
3) средство, запускаемое для определения требуемой концентрации препарата на основе заданной скорости дозирования, стандартизированной скорости инфузии и веса пациента, подаваемые через средство ввода;
4) средство для высвечивания на дисплее требуемой концентрации и/или приготовления помещаемой в мешок окончательной смеси инфузионного раствора препаратов и растворителя, введение которых предполагается;
5) средство для смешивания растворителя и концентрата (концентратов) препаратов в помещаемый в мешок окончательный смешанный инфузионный раствор, готовый для введения;
6) средство для маркировки ингредиентов на наружной стенке каждого мешка с окончательной смесью для вливания.
Настоящий способ может использоваться для введения широкого разнообразия видов препаратов, включая, но не ограничиваясь ими, анестетики, мышечные релаксанты, седативные средства, анальгетики и препараты для кардиореанимации. Этот способ инфузии может также использоваться в различных клинических учреждениях, включая операционную, отделение интенсивной терапии, аптеку, поликлинику и стоматологическую клинику. Здесь преимущественно описано применение изобретения в качестве способа подачи анестетиков, но специалистам в этой области будет понятно, что оно может использоваться в описанных выше других видах применения.
Предпочтительный вариант реализации изобретения обеспечивает, чтобы анестетики и другие препараты, введение которых предполагается, готовились из флаконов с предварительно отмеренными дозами для пациентов в пределах определенного диапазона веса для исключения этапов расчета и смешивания, которые в противном случае были бы необходимы, дополнительно снижая риск связанной с человеческим фактором ошибки и, таким образом, дополнительно повышая безопасность вливания. Флакончики с заранее отмеренным количеством концентрата могут иметь штрих-коды или закодированы другим образом набором данных, которые могут считываться компьютером (например, тип препарата, дата приготовления, концентрация, объем) для гарантии того, что получена соответствующая лекарственная смесь, что, если не устраняет, то снижает возможность ошибки, связанной с человеческим фактором. В отличие от других изобретений, которые предписывают доставку определенных количеств препарата, независимо от клинических обстоятельств, описанное здесь изобретение предоставляет практикующему врачу диапазон для подбора подаваемого количества препарата и позволяет практикующему врачу подобрать скорость введения на основании реакции пациента в пределах рассчитанного компьютером безопасного диапазона для используемой анестезии.
Описанное здесь изобретение предоставляет практикующему врачу две возможности подбора расчета количества препарата, доставляемого пациенту. Во-первых, после оценки максимального количества препарата, которое может потребовать и перенести пациент, практикующий врач подбирает концентрацию препарата (препаратов), добавляемых в растворитель в инфузионном мешке. Подбор концентрации препарата, помещенного в мешок с растворителем, означает подбор количества препарата по умолчанию, которое будет введено пациенту. Таким образом, клиническое состояние пациента и прогнозируемая потребность в анестетике и прогнозируемая реакция играют существенную роль в определении дозы, которую предстоит добавить в мешок с растворителем. Во-вторых, после определения и добавления в мешок с растворителем соответствующей поддерживающей дозы на основании развития заболевания и действительной реакции пациента на анестезию практикующий врач может подобрать количество доставляемого пациенту препарата с помощью подбора скорости титрования доставляемого препарата в пределах определенного с помощью компьютера безопасного диапазона доставки препарата. Это экономит время ввиду отсутствия необходимости в дальнейших расчетах. Высокий низкий предел диапазона, предоставленный настоящим изобретением, насколько возможно близко имитирует клиническую практику, в то же самое время стандартизируя ее. (Такая стандартизация облегчает достижение дозы синергизма, например можно разделить пополам недостающий объем дозы, предусмотренной программой.)
Далее, описанный здесь способ легко приспособляем для следующих видов анестезиологического применения, которые представляют собой необычные проблемы практикующего анестезиолога: (1) у кардиологических больных, (2) в педиатрии, (3) в случаях применения пропофола, (4) в случаях использования смесей различных анестетических препаратов, (5) при использовании ПВВА у кардиологических больных и (6) в случаях анестезии у очень тяжелых больных.
Многим анестезиологам концептуально настоящее изобретение будет понятно по аналогии с моделью испарителя/процентной подачи.
Суммируя, способ настоящего изобретения предоставляет ряд преимуществ в сравнении с предшествующими способами смешивания и введения таких препаратов. Стандартизация скорости дозирования настоящего способа намного облегчает интерпретацию и применение для врача и гораздо безопаснее для пациента. Настоящий способ также обеспечивает возможность использования более простых и гораздо менее дорогих инфузионных насосов, которые уже широко доступны в клинических учреждениях. Ввиду того что способ обеспечивает смешивание соответствующего и большого количества препарата, способ позволяет избежать проблем, обусловленных повторным заполнением шприца, которые порочат другие способы. Способ можно в равной степени использовать в операционной, отделении интенсивной терапии или в других отделениях больницы. Наконец, настоящий способ также обеспечивает возможность большей гибкости в выборе средства для использования при постоянной инфузии растворов препаратов, включая анестетические или анальгетические препараты. Врачи, избавленные от сложностей предшествующих способов приготовления и введения растворов препаратов, включая анестетики, получат стимул расширить количество и типы препаратов, которые они применяют для постоянных вливаний. Таким образом, врачи могут применять лучшие комбинации препаратов со сниженным риском неправильной дозировки.
Задачей изобретения является предоставление способа упрощения расчетов, которые предполагается использовать в системах постоянной инфузии, способа, который не требует от анестезиолога запоминания множества параметров для используемых вводимых внутривенно препаратов.
Еще одной задачей изобретения является исключение накопления вливаемых препаратов. Ввиду использования упрощенного расчета можно легко провести подбор вливаемых препаратов во избежание такого накопления.
Еще одной задачей изобретения является предоставление способа установления правильных диапазонов дозировки препаратов, вливание которых предполагается, причем диапазоны учитывают способ доставки анестетического препарата, синергический эффект множества препаратов и специфические потребности в анестетиках, такие, которые возникают в педиатрии и кардиологии.
Другой задачей изобретения является предоставление способа вливания препарата с большей эффективностью затрат, который преодолевает некоторые недостатки существующих механизмов, например отсутствие механизма поправки на клиническую реакцию, нерегулярную подачу препарата и множество устройств и наладок при использовании множества препаратов.
Краткое описание чертежей
Изобретение будет легче понять из следующего описания его предпочтительных методов реализации, показанных только в качестве примера, в сопровождающих чертежах, в которых:
на фиг.1 схематически представлены диапазоны доз, рекомендуемых различными литературными источниками;
на фиг.2 представлен график, показывающий стандартную кривую и титрование препаратов, доставляемых с использованием настоящего изобретения;
на фиг. 3 представлен эталон для интерпретации диапазонов скорости от низкого до высокого для десяти соответствующих препаратов для анестезии;
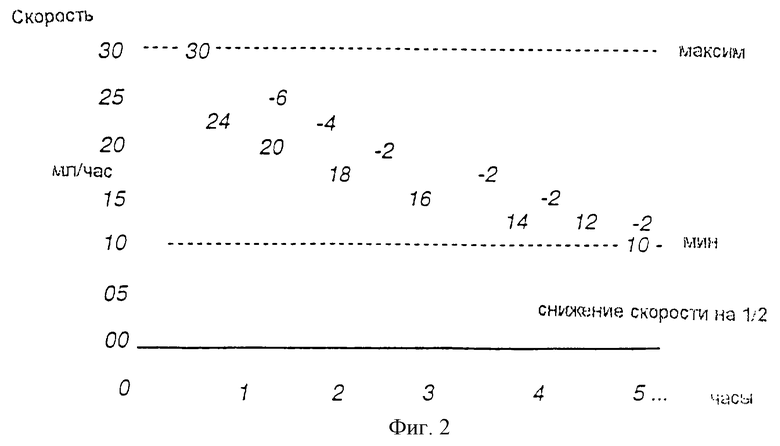
на фиг. 4А представлен график, показывающий кривую титрования доставки препарата в соответствии с настоящим изобретением;
на фиг.4В представлен график, показывающий доставку препарата в соответствии со способами предшествующего уровня техники;
на фиг. 5 показан образец высвечиваемого на экране выходного сигнала компьютера и/или этикетку на мешке с конечной смесью для вливания, на которой приведен перечень определения смешивания;
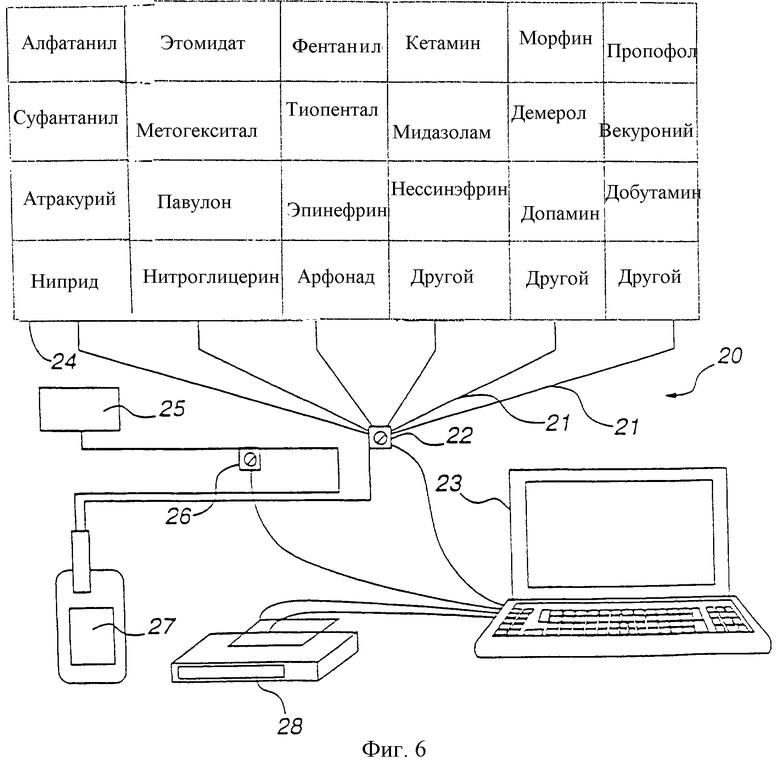
на фиг. 6 показана компоновка компьютерного контролирующего устройства смеси для приготовления смесей препаратов;
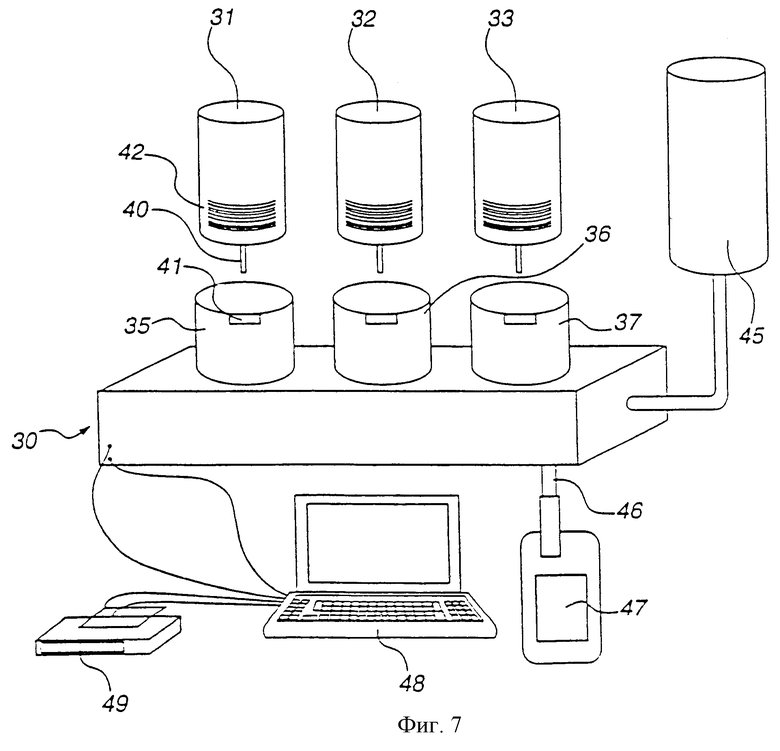
на фиг.7 показано устройство для приготовления смесей препаратов.
Способ настоящего изобретения
Описанный здесь способ обеспечивает (1) генерирование величин концентрации после фиксации определенных переменных величин как описано в настоящем изобретении, (2) подсчет величин для установления диапазона титрования вливания, (3) определение требуемой концентрации по меньшей мере одного препарата на основании массы пациента, указанной скорости дозирования количества указанного раствора и стандартизированной скорости вливания и (4) смешивание по меньшей мере одного препарата в контейнер для растворителя для введения препарата пациенту.
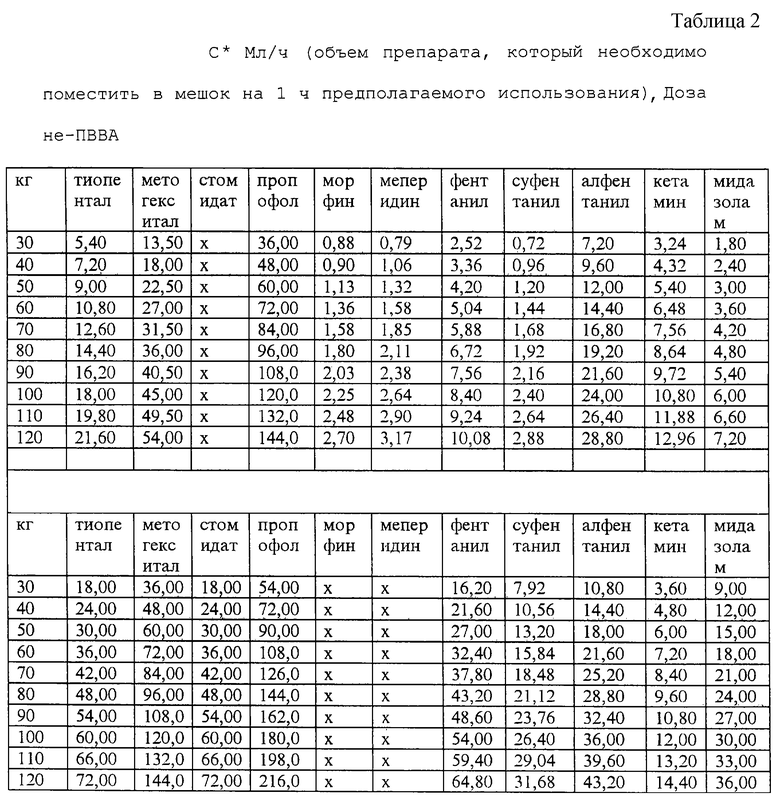
Одним из отличительных признаков настоящего изобретения является использование таблицы, которая содержит заданные величины концентрации при различной массе тела, которые могут исключить многие этапы при приготовлении вливаний, включая анестетики, введение которых предполагается. В качестве полученного примера см. табл. 2, применявшуюся и использовавшую описанные здесь способы. Каждая переменная величина определена и объяснена ниже.
1.Дозировка (Р)
"The White Paper" предлагает использование клинически определенных больших и малых величин в методиках постоянного вливания. В связи с описанной здесь ранее трехкомпартментальной моделью клинические диапазоны различных препаратов представлены в табл. 1 в колонке, отмеченной Ср. Эти клинические величины получены с помощью применения соответствующих принятых величин, описанных в литературе по анестезиологии и фармакокинетике. В соответствии с "The White Paper" величина поддерживающей скорости инфузии (ПСВ) определяется с помощью умножения концентрации препарата в плазме пациента (Ср) на клиренс (КЛ), т.е. выведения или скорости метаболизма. Столбец Ср табл. 1 показывает высокий и низкий диапазоны величин каждого средства.
В соответствии с настоящим способом для получения величин дозировки, используемых для определения величин концентрации препаратов для ПВВА, которые в свою очередь используются для стандартизации препаратов, вливание которых предполагается, например величин, представленных в табл. 2, высокая величина Ср выбирается из диапазона, представленного в колонке Ср табл. 1. В соответствии с описанным здесь способом высокая величина всегда отбирается так, чтобы вливание обеспечило концентрацию и объем, требуемые для подачи самой высокой ожидаемой потребности препаратов, вливание которых предполагается. Таким образом, дозировка D, используемая для расчета величин табл.2, основана на максимальной скорости поддерживающего вливания (MaxIR) для каждого препарата. При использовании в качестве примера тиопентала и беря величины из табл. 1, высокая величина Ср, равная 20 мкг/мл, умножается на клиренс, составляющий 3 мл/кг, что равно 60 мг/кг/мин. Таким образом, дозировка тиопентала, которая используется для расчета величин для табл.2, составляет 60 мг/кг/мин.
С точки зрения дозировок не-ПВВА, которые также представлены в табл. 2, в результате клинического наблюдения был определен средний диапазон величин, описанный "White Paper" и подтвержденный клиническим наблюдением. Соответственно величины С* для не-ПВВА отражают более низкие дозировки.
2. Масса тела (B.W.)
Масса тела представляет собой фиксированную величину для каждого отдельного пациента. В табл.2 создана колонка для каждого приращения тела пациента на 10 кг.
3. Константа
Константа 0,06 корректирует на единицу различия измерения между дозировкой и скоростью вливания (мл/ч).
4. Скорость вливания (R)
Номинально скорость вливания может быть любой выбранной величиной. Однако для упрощения и стандартизации скоростей вливания для всех внутривенных средств настоящее изобретение в предпочтительном варианте реализации, когда способ используется для расчета поддерживающей скорости у взрослого человека, устанавливает скорость на 30 мл/ч. Эта скорость была выбрана потому, что большинству пациентов, которым необходима анестезия, необходим этот объем жидкости в случаях вмешательства, требующего анестезии. Кроме того, эта скорость вливания позволяет преодолевать проблемы доставки низкого объема, которые возникают при использовании способов и устройств предшествующего уровня техники. Стандартизация дозировки MaxIR скоростью подачи обеспечивает постоянство применения анестетиков для внутривенного вливания. Эта стандартизация скорости вливания является определяющим признаком описанного здесь способа, которая отличает его от способов предшествующего уровня техники. Следует отметить, что в других вариантах реализации изобретения скорость вливания устанавливается при других скоростях. Например, в педиатрических случаях MaxIR составляет 10 мл/ч, в случаях вмешательств у взрослых людей с использованием пропофола - 12 мл/ч, в педиатрических случаях с использованием пропофола - 40 мл/ч, при кардиохирургических вмешательствах - 45 мл/ч и в случаях, когда предполагается использование препаратов только для седативного эффекта или анальгезии, - 9 мл/ч.
5. Концентрация вливания (С)
Концентрация смеси для вливания дана в мг/мл.
6. Объем препарата, который предполагается доставить за 1 ч (С*)
Объем препарата, который предполагается доставить за 1 ч. С*, представляет собой С, деленное на стандартную концентрацию, при которой препарат имеется в продаже, и дана в мл/ч. Величины, представленные в табл.2, равны С*.
Получение величин концентрации: определение табл. 2
В целях демонстрации и в согласовании с предшествующим описанием были сделаны следующие предположения:
D = MaxIR, выраженная в мкг/кг/мин 20 BW = фиксированная масса на колонку, выраженная в кг
R = 30 мл/ч
С = концентрация вливания, выраженная в мкг/мл.
Для определения объема препарата, который предполагается доставить в его стандартной доступной концентрации, С*, С просто делится на стандартную концентрацию, в которой представлен препарат.
Используя уравнение, т. е. D•BW•60=C•R и производя решение для С* (для каждого препарата на каждый кг массы), получают таблицу, подобную табл. 2. Например, используя приведенный выше расчет (в целом Ср умноженное на С1) для D, которую предполагается использовать при выведении величин для тиопентала, и выбрав BW = 50 кг, рассчитывается С* как: (60 мг/кг/мин)•(50 кг)•(60 мин/ч)/30 мл/ч = 6000 мг/ч, и поскольку тиопентал имеется в концентрации 200 мг/мл С* равен 30 мл/ч, что отражено в колонке массы 50 кг табл. 2. Отбор (1) желаемого средства для внутривенного введения и (2) массы в кг пациента по колонке позволяет практикующему врачу выбрать С*. С* равен объему (выраженному в мл) соответствующего препарата, который предполагается добавить в инфузионный мешок и должен доставляться в 1 ч. Эта смесь доставит MaxIR, если инфузионный насос установлен на доставку MaxIR, т.е. в предпочтительном варианте реализации 30 мл/ч.
MaxIR, используемая для получения величины С* в соответствии с описанным здесь способом, отражает описанные выше особые случаи. Например, ввиду свойств пропофола для получения величин для табл. 2 для препарата пропофол MaxIR для пропофола должна быть увеличена до 120 мл/ч. Аналогичным образом, ввиду относительной простоты расчета дозы препарата для введения пациентам у педиатрических больных для получения величины для табл. 2 используется MaxIR, равная 10 мл/ч. MaxIR для других таких случаев обсуждена выше.
После выведения величин С* способ обеспечивает многоэтапное приготовление инфузионного мешка. Из следующего описания будет ясно, что хотя величины скорости и дозировки устанавливаются как описано выше для получения величин С*, величины скорости и дозировки варьируют на других этапах настоящего изобретения для соответствия различным клиническим обстоятельствам, например при плохом состоянии здоровья пациента и при доставке не-ПВВА
Процедура 1: Определение дозы насыщения
A) Выбрать BW - [ ] кг
B) Выбрать дозу насыщения средства для внутривенного введения из табл.3.
- Доза насыщения
Высокая доза - [ ] • [ ] кг = [ ] мг
Средняя доза - [ ] • [ ] кг = [ ] мг
Низкая доза - [ ] • [ ] кг = [ ] мг
В табл. 3 представлены диапазоны высоких и низких доз для средства. Диапазон доз предназначен для применения препарата в качестве первичного анестетика. Если предполагается использование препарата в качестве дополнительного средства, следует применять более низкие дозы. Истинная доза насыщения будет определяться клиницистом на основании клинического состояния отдельного пациента с предпочтением самой высокой дозы насыщения, которую может перенести пациент.
Некоторые факторы, которые следует учитывать при отборе соответствующей дозы насыщения, включают в себя возраст пациента, другие препараты, вводимые пациенту, заболевание основных систем органов и вид вмешательства, которое предполагается выполнить у пациента, например вид операции, которую предполагается провести. Таким образом, если состояние здоровья пациента плохое или он особенно чувствителен к анестетическим препаратам, клиницист выберет низкую дозу насыщения. Если состояние здоровья пациента хорошее и он проявляет обычную реакцию на анестезию, выбирается высокая доза насыщения. Общая анестезия вызывается "болюсным введением" соответствующей дозы насыщения.
Процедура 2: Смешивание раствора для инфузионного мешка
Раствор в инфузионном мешке следует готовить в соответствии со следующими этапами:
A) Масса пациента, кг
B) Выбрать средство (средства) для внутривенного введения
C) Выбрать соответствующую колонку и С* ряд из табл. 2 для выбора С* для каждого средства
D) Требуемый объем инфузионного мешка, необходимое количество в мл
Ожидаемая продолжительность вмешательства
Е) Требуемый объем средства (средств), мл*
длительность вмешательства • С*
F) Удалить количество мл* из инфузионного мешка
G) Добавить количество мл* из инфузионного мешка
Н) Маркировать мешок и смешать растворитель и препарат (препараты)
I) Подвесить мешок на крючок инфузионного устройства, которое подает от 1 до 150 мл/ ч.
(Примечание: Если используется множество препаратов, клинический опыт показал, что для поправки на синергическое преимущество доставки множества анестетических препаратов каждый раз при использовании наркотика анестезиолог, применяющий описанное здесь изобретение, уменьшает наполовину количество второго препарата, который в противном случае был бы рассчитан компьютером на этапе С. Следует также отметить, что большинство препаратов продается в стандартных концентрациях. Тем не менее, предоставленный здесь способ позволяет анестезиологу на этапе F завершить расчеты при использовании различных концентраций препаратов).
Важно, что в отличие от способов, предложенных предшествующим уровнем техники, в настоящем изобретении используется только один мешок для смешивания и доставки анестетических препаратов для внутривенного введения. Таким образом, в дополнение к эффективности такой способ обеспечивает титрование препаратов для внутривенного введения и в настоящем изобретении более эффективно, чем в предшествующих способах, используются ресурсы времени и оборудования, например насосы, шприцы и мешки. Ввиду того что в одном и том же мешке может использоваться множество препаратов, описанный здесь способ (а) экономит время наладки, включая расчет, смешивание и время настройки оборудования; b) использует одну в/в настройку; с) использует одну наладку насоса и d) экономит средства путем использования меньшего количества оборудования. Например, ввиду того что шприцевые насосы не позволяют доставку более чем одного препарата, при необходимости использования множества препаратов способ вливания, требующий использования шприцевых насосов, потребует множества шприцевых насосов, что было бы дорогостоящим и обременительным. Кроме того, описанный здесь способ безопаснее, чем способы с использованием шприцевых насосов, потому что, по данным исследователей, при использовании анестезиологом шприцев различного размера и разных производителей шприцевые насосы подают неточные и неравномерные объемы ввиду меняющегося размера просвета и сопротивления движению. Далее, при использовании таких устройств и необходимости в низком объеме вливания препарат часто не прокачивается через трубки устройства постоянным образом. При доставке больших объемов, как это происходит в предоставляемом здесь способе, возможность такой неточной и неравномерной доставки препаратов снижается. В дополнение к преимуществам, определяемым применением одной наладки для доставки множества препаратов, описанный здесь способ преодолевает несколько недостатков предшествующего уровня техники: способ может применяться с более простыми и менее дорогими насосами, способ осуществляется со всеми насосами и при нем приходится меньше проводить повторное заполнение шприца, что является обычной проблемой при использовании способов инфузии, которые включают шприцевые насосы. Далее, снижаются затраты на оборудование и неудобства: как более полно обсуждено ниже, для инфузии не требуется компьютер, для этапа в/в введения не требуется инфузор, способ реализуется с помощью компьютера "laptop" или "palmtop", которые могут производить расчеты, для проведения титрования не требуется компьютер, контролирующий инфузию (таким образом, в изобретении возможно проведение ручного титрования), способ совместим со всеми компьютерными инфузионными устройствами в качестве информационной базы для инфузии. Таким образом, использование описанного здесь способа снижает затраты, связанные с предшествующим способом: перерасчеты, больничное обслуживание, когда совершаются ошибки, которые оставляют пациента спящим после завершения операции, большее количество и более сложное оборудование и неиспользованные большие объемы стандартной смеси препарата.
Вводный наркоз и поддерживающая анестезия/титрование
Вводный наркоз проводится в соответствии со стандартной анестезиологической методикой. Для вводного наркоза вводится соответствующая доза насыщения, рассчитанная в соответствии с описанной выше процедурой. После вводного наркоза начинают поддерживающую инфузию. Для инфузии может использоваться множество препаратов. Количество препарата (препаратов), которое предполагается добавить в растворитель, готовится в соответствии со второй процедурой. После добавления препаратов в растворитель для смешивания препаратов может использоваться несколько способов. Например, (1) можно производить встряхивание контейнера, содержащего все препараты и растворитель, введение которых предполагается; (2) контейнер можно массировать; или (3) может применяться устройство, образующее воздушные пузырьки. Предпочтительно контейнер следует встряхивать непосредственно перед тем, как он подвешивается на стойке для вливания пациенту. Для точной доставки препарата может использоваться почти любое устройство, способное доставить хорошо контролируемый объем препарата от 1 до 150 мл/ч. Следует также отметить, что многие анестетические препараты прилипают к трубкам, используемым в устройствах для доставки препаратов, и поэтому следует использовать трубки, которые препятствуют поглощению.
При использовании описанного здесь способа все препараты могут доставляться при одной наладке и одном устройстве доставки, экономя таким образом время наладки, время расчета и стоимость оборудования. В начале инфузии скорость инфузии выбирается для доставки MaxIR. В предпочтительном варианте реализации настоящего изобретения MaxIR составляет 30 мл/ч. Однако если препарат предполагается постоянно вливать в качестве дополнительного анестезирующего средства, или ввиду вливания множества препаратов, или если используется применение не-ПВВА, например препарат для внутривенного введения вводится в комбинации с закисью азота или летучими анестетиками, соответственно следует снизить скорость инфузии. Например, при использовании фентанила можно снизить количество вливаемых анестетиков.
Потребности в введении желаемого отдельного анестетика значительно варьируют. На фиг.3 показаны от высоких до низких скоростей подачи, которые отражают величины, представленные в табл.4 "White Paper". Поддержание скорости потока инфузии в пределах клетчатой зоны обеспечивает доставку рекомендуемых уровней дозировки соответствующего препарата (препаратов). Фиг.3 позволяет анестезиологу визуально оценить, когда инфузия укладывается в диапазон выбранных от высоких до низких скоростей поддерживающей инфузии.
Во время введения анестетиков следует серийно снижать MIR для поддержания самой низкой переносимой скорости инфузии, которая обеспечивает адекватную анестезию, анальгезию и отсутствие сознания. Это позволяет ускорить пробуждение пациента в конце вмешательства. Таким образом, если жизненные показатели пациента остаются неизменными и стабильными, количество инфузии можно снизить, как описано здесь. Напротив, если артериальное давление или частота сердечных сокращений пациента возрастает, количество вливаемого препарата можно увеличить.
Принципиальное преимущество настоящего изобретения состоит в том, что оно упрощает титрование всех анестезирующих препаратов. Все препараты комбинировались для доставки с одинаковой скоростью, и их концентрация была установлена для обеспечения возможности одновременной инфузии при одном и том же виде анестезии, причем единственное исключение составляют случаи использования пропофола. Вспомните, что при использовании пропофола MaxIR составляет 120 мл/ч, a MinIR составляет 40 мл/ч. Опять же, после первоначального расчета ударной и поддерживающей доз в настоящем изобретении используется фиксированная концентрация всех препаратов и меняющаяся скорость доставки. В начале инфузионной терапии концентрация препаратов основывается на концентрации, необходимой для доставки максимальной дозы по умолчанию при максимальной стандартной скорости (в предпочтительном варианте реализации 30 мл/ч). Изменение доставляемой дозы создается изменением скорости вливания (в мл/ч) в пределах диапазона титрования.
Кривая диапазона скорости титрования отражает быстрое снижение скорости титрования вначале и имеет заострение в последующем, где исходное количество первоначально доставляемого препарата составляет х, причем MaxIR и нижний диапазон доставляемого препарата составляет приблизительно х/3, MinIR. В предпочтительном варианте реализации скорость х, MaxIR, составляет 30 мл/ч, создавая таким образом диапазон для доставки препарата, при котором 30 мл/ч является максимальной скоростью, а 10 мл/ч является минимальной скоростью, MinIR. Хотя диапазон от 30 до 10 мл/ч является наиболее распространенным, ясно, что описанный здесь способ можно приспособить для других режимов применения. Например, в педиатрических случаях или в других случаях, при которых масса пациента составляет от 4 до 27 кг, и он таким образом имеет значительно меньшие потребности в жидкости, чем взрослый человек со средней массой тела, и у него ранее не применялись препараты, скорость титрования составляет от 10 до 3 мл в 1 ч. В кардиохирургических случаях диапазон составляет от 45 до 15 мл/ч, при операциях у взрослых людей с использованием пропофола диапазон составляет от 120 до 40 мл/ч, в педиатрических случаях с использованием пропофола диапазон составляет от 40 до 13 мл/ч и если препарат используется в качестве седативного средства диапазон составляет от 9 до 3 мл/ч.
С точки зрения наклона гиперболической кривой титрования, опыт показал, что если перед окончанием операции скорость х снижается приблизительно наполовину и подача препарата прекращается в пределах 30 мин до конца вмешательства, то пациент выходит из операции, т.е. начинает спонтанно дышать и возвращается в бодрствующее состояние в пределах короткого периода после завершения вмешательства, но выходит не столь быстро, чтобы выйти из наркоза до окончания операции. Быстрый выход из наркоза позволяет избежать самых распространенных осложнений при внутривенном вливании анестетиков: длительное угнетение дыхания и пробуждения. Таким образом, эта методика инфузии лучше методики, описанной в предшествующем уровне техники, потому что она позволяет избегать массивного введения насыщающих доз опиоидов, имеющего место при использовании таких способов, и обеспечивает более прогнозируемое пробуждение.
В других моделях для описания процедуры титрования не используется гиперболическая кривая, а используется прямолинейная доставка препарата. Кроме того, другие модели обеспечивают периодическую доставку препарата, т.е. периодическое прекращение и возобновление доставки препарата. К сожалению, прямолинейный способ не может отражать чувствительный ко времени контекст периода полувыведения из плазмы (т.е. накопление препарата). Кривая титрования настоящего изобретения соответствует клинической реакции пациента на препарат и в целом имитирует гиперболическую кривую. В отличие от других методологий кривая титрования не основана на уровне доставляемого препарата в крови, а основана на клинической реакции пациента. Настоящее изобретение показывает, что нет необходимости в способе обеспечения анестезии, который основан на концентрации препарата в крови.
Таким образом, в предпочтительном варианте реализации изобретения для процедуры анестезии титрование препарата (препаратов) происходит по схематической кривой, представленной на фиг.4А.
При использовании способа для анестезии и анестезия, обеспечиваемая в соответствии со способом, является первичным средством, подходит использование более высокого диапазона инфузии (20-30 мл/ч). Для применения в качестве дополнительного или седативного средства более соответствующим было бы использование скоростей 10-20 мл/ч. Для мягкого анальгетического эффекта соответствовали бы скорости <10 мл/ч. Анестезиолог может просто подобрать дозу в соответствии с клиническими потребностями. Например, если оказывается, что пациент подвергнут слишком глубокому седативному воздействию, анестезиолог может сдвинуть кривую вниз быстрее, чем это предусмотрено обычной скоростью. Напротив, если оказывается, что пациент подвергнут слишком легкой анестезии, анестезиолог может просто сдвинуться назад вверх по кривой титрования. Опять же, этот способ обеспечивает возможность реагировать на реакцию конкретного пациента на введение препаратов и на свойства используемых препаратов. Например, хотя кривая обеспечивает общее направление титрования анестетических препаратов, существуют изменения в зависимости от того, имеют ли анестетики быструю кинетику или они имеют медленную кинетику. Анестетические препараты, имеющие быструю кинетику, требовали в пределах первого часа от 2 до 3 титрований. Напротив, анестетические препараты, имеющие медленную кинетику, в течение первого часа титруются лишь однократно вниз на один этап. Когда препараты, имеющие быструю кинетику, смешиваются с препаратами, имеющими медленную кинетику, смесь титруется по требованиям к препаратам, имеющим быструю кинетику.
С помощью создания стандартного диапазона титрования упрощается использование внутривенных вливаний. Все используемые препараты вводятся в одном и том же диапазоне титрования. Доза всех препаратов одинаковым образом сужается к концу титрования. См. фиг.4А. Например, если препарат А представляет собой первичный анестетик, то в начале вмешательства препарат А вводится в виде болюса и вливание начинается со скоростью 30 мл/ч. Через 30 мин скорость снижается по 6 мл/ч и доводится до 24 мл/ч. Еще через 30 мин скорость снижается по 4 мл/ч до 20 мл/ч и т.д. Это продолжается до момента за 1 ч до конца вмешательства, когда скорость снижена наполовину. За 30 мин до конца вмешательства вливание прекращается и пациент пробуждается. Ни один из способов предшествующего уровня техники не предлагает и этого и дает гораздо меньше информации, чем этот заявляемый способ.
Заявляемый способ стандартизирует способ для всех препаратов. Способ упрощает задействованный математический аппарат. Когда диапазон титрования составляет от 30 до 10 мл в 1 ч, кривая титрования на фиг.4А в целом эквивалентна следующей формуле: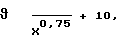
где х = число часов вмешательства;
y = мл/ч.
Пример 1: х=1 ч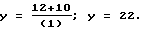
Пример 2: х=4 ч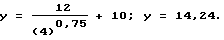
Следует отметить, что приведенная выше математическая модель для гиперболической кривой не предназначена для того, чтобы служить в качестве точной модели доставки препарата, а является схематическим представлением концептуального снижения и титрования скорости доставки препарата. Фиг.2 более точно отражает скорость титрования препарата. Упомянутая выше математическая модель просто показывает кривую предпочтительного варианта реализации, когда не следует производить других поправок доставки.
Без стандартной кривой и стандартного титрования заявленного способа каждый раз при необходимости изменения дозы необходимо было бы независимо рассчитывать каждую скорость с использованием первоначального уравнения. Многие анестезиологи утверждают, что пересчет скорости вливания каждый раз, когда необходимо изменение дозы, очень труден и проблематичен и поэтому они предпочитают доставлять препарат с использованием способа, показанного на фиг. 4В. На фиг. 4В показан способ вливания по принципу "все или ничего". Когда производится вливание препарата, он вводится со скоростью, имеющей величину по умолчанию. Если при использовании слишком большого количества препарата развиваются побочные эффекты, вливание прекращается. Затем анестезиолог вновь включает инфузию, когда глубина анестезии представляется слишком поверхностной. Такой способ доставки, изображенный на фиг.4В и используемый в предшествующем уровне техники, не считается идеальным, частично ввиду того, что такая болюсная дозировка может потребовать больших общих доз препарата вследствие необходимости поддержания периодически более высоких концентраций препарата в плазме. Титрование, обеспечиваемое с помощью описанного здесь способа, имеет преимущество перед способом доставки, изображенном на фиг.4В, потому что оно приводит к более низким пикам и к меньшему количеству пиков, имеет меньше субтерапевтических углублений и может обеспечить действие длительно действующих препаратов, подобное действию препаратов короткого действия. Кроме того, представленный здесь способ многоэтапного титрования более близко соответствует точной потребности пациента в препаратах, т.е. он приближается к идеализированной фармакокинетической доставке таких препаратов.
Заявляемый в настоящее время способ, устанавливающий стандартный диапазон титрования для всех препаратов, предоставляет множество преимуществ. Во время вмешательства нет необходимости в перерасчете концентрации препарата по скорости титрования.
Пример проведения анестезии
Теперь будет представлен пример с использованием табл.2 и 3. Необходимо провести анестезию у женщины с массой тела 70 кг. Планируется вводный наркоз тиопенталомсукцинилхолином. Этот вводный наркоз проводится с использованием стандартных методик анестезии. Для поддерживающей анестезии будет использоваться дополнительное вливание фентанила. Ожидаемая продолжительность операции 3 ч. Для определения дозы насыщения выбранного препарата (фентанила) используется табл.3.
Процедура 1. Определение дозы насыщения производится следующим образом:
Средняя доза насыщения: 0,0111 мг/кг • 70 кг = 0,777 мг = 777 мкг.
Высокая доза насыщения: 0,021 мг/кг • 70 кг = 1,47 мг = 1470 мкг.
Низкая доза насыщения: 0,0012 мг/кг • 70 кг = 0,08 мг = 84 мкг.
Выполняется процедура 2. Смешивание раствора в мешке для капельного вливания:
A) BW = 70 кг.
B) Средство = фентанил.
C) С* = 5,88 мл/ч.
D) Ч [3] • 30 мл/ч = 90 мл - > будут смешаны в инфузионном мешке емкостью 100 мл.
Е) Требуемый объем средств = 3 ч • 5,88 = 17,64 мл.
F) Удалить 17,64 мл жидкости из инфузионного мешка, содержащего 100 мл растворителя.
G) Добавить 17,64 мл фентанила в концентрации 50 мкг/мл в инфузионный мешок, содержащий растворитель.
I) Маркировать мешок и смешать.
J) Подвесить инфузионное устройство. Установить устройство для начала на 30 мл/ч.
Для вводной фазы действительной доставки анестетика выбранная доза насыщения фентанила будет вводиться в качестве непосредственной внутривенной премедикации или как часть вводного наркоза. После вводной фазы будет начато постоянное вливание фентанила со скоростью 30 мл/ч (см. фиг.3). Скорость вливания будет подбираться в зависимости от эффекта с использованием инструкций, предложенных на фиг.4 статьи White.
После получения уровня анестезии скорость постоянной инфузии фентанила серийно снижается в соответствии с гиперболической кривой, изображенной на фиг.4А, для поддержания эффективной анальгезии, в то же время, сводя к минимуму накопление препарата. За 1 ч до окончания операции вливание должно уменьшиться наполовину и по мере толерантности прекращено за 30 мин до конца операции для обеспечения возможности быстрого пробуждения. Более подробное описание способа постоянной инфузионной анестезии дано в "White Paper".
Компьютерная программа для определения смесей препаратов
На фиг. 5 показан образец выходного сигнала на дисплее компьютера и/или этикетка окончательной смеси раствора в инфузионном мешке, приводящая перечень действий определения смешивания. Компьютер запрограммирован в соответствии с описанным выше способом таким образом, что при введении пользователем необходимых данных, предусмотренных способом, программа выполняет этапы определения дозировки для оператора. Компьютерная программа с использованием описанного здесь способа имеет преимущество перед сложными запускаемыми компьютером устройствами, которые производят вливание одиночных препаратов с замкнутой системой контроля. Такие замкнутые системы предполагают, что ручное титрование инфузионных систем для внутривенного вливания слишком трудное. Однако компьютерная система, использующая способ настоящего изобретения, проста, характеризуется эффективностью затрат и дает возможность ручного титрования, позволяя таким образом анестезиологу обеспечить больший контроль. Компьютерная программа автора изобретения для описанного выше способа получила одобрение Администрации по продуктам питания и лекарственным препаратам США.
Результаты определения дозировки (включая информацию, показанную на фиг. 1) могут предпочтительно распечатываться на этикетке с клеевой подложкой для ручного или автоматического прикрепления к инфузионному мешку с окончательной смесью для вливания.
Пользователи компьютерной программы могут легко изменять смеси растворителя и концентрацию препарата для отбора любой стандартной или нестандартной скорости потока в соответствии с наиболее желаемым применением препаратов. Такие изготовленные на заказ смеси приводят к важным преимуществам безопасности для пациента во многих особых ситуациях, таких как анестезия у новорожденных или другие, где могут потребоваться специализированные скорости потока.
Компьютеризированное контролирующее устройство для приготовления смесей препаратов
На фиг.6 показана схема компоновки компьютеризированного контролирующего устройства 20 для приготовления смесей препаратов. Компьютеризированное контролирующее устройство для приготовления смесей препаратов способно выполнять определение смешивания и смешивать препараты из матрикса 24 препаратов через линии подачи 21 (контролируемые многопутевым клапаном 22 концентрации препаратов) и растворителя из сосуда 25 (контролируемый клапаном 26 растворителя) для смешивания раствора в инфузионном мешке 27 для анестезиолога. Компьютер 23 предварительно запрограммирован в соответствии со способом настоящего изобретения таким образом, что при вводе пользователем необходимых параметров и подачи соответствующей команды устройство завершает этапы определения дозировки, смешивания раствора в инфузионном мешке и маркировки (в виде выходного сигнала автоматического изготовителя этикеток 28) для оператора. Компьютер 23 может также быть оборудован сигнальным устройством, способным подать сигнал оператору о неполадках в работе устройства, недостаточном количестве растворителя или концентрата препарата, ошибке программы и/или неправильном вводе данных. Результаты определения дозировки (включая всю информацию, высвечиваемую на экране дисплея, показанном на фиг.1) распечатываются изготовителем этикеток 28 для прикрепления на мешок с окончательной смесью.
Компьютеризированное контролирующее устройство смеси оборудовано устройством расходомера-клапана, так что при вводе соответствующей команды необходимый растворитель подается в инфузионный мешок для подачи. Затем из отдельных сосудов, снова с использованием клапана, расходомера или карусельной и клапанной установки, в инфузионный мешок для подачи подаются необходимые концентраты препаратов. После того как компьютеризированное контролирующее устройство смеси подает окончательные количества препарата и растворителя в инфузионный мешок для подачи, инфузионный мешок может быть герметично закрыт вручную или автоматически и к инфузионному мешку может вручную или автоматически прикрепляться этикетка с клеевой подложкой, содержащая информацию о конечной смеси.
Вместо использования устройства предшествующего уровня техники, которое требует применения у каждого пациента в течение операции сложного электронного обеспечения, нагнетательных или других инфузионных насосных средств, устройство настоящего изобретения обеспечивает возможность использования одного устройства для быстрого приготовления растворов в инфузионных мешках для всего медицинского комплекса или множества учреждений. Анестезиолог может использовать ручной, удерживаемый на коленях и настольный компьютер в каждом участке вливания пациенту или в централизованном месте.
Ввиду того что анестетики имеют тенденцию к распаду с течением времени, флаконы, содержащие концентраты анестетических препаратов, наиболее желательно перед использованием хранить в среде с контролируемой температурой; аналогичным образом, после смешивания инфузионный мешок может храниться в этой контролируемой среде. Желательно также, чтобы компьютерная программа была снабжена функцией контроля за сроком годности препаратов; когда срок годности препарата истекает, оператор может оповещаться об этом или на место может автоматически перемещаться свежий концентрат препарата, а флакон с истекшим сроком годности автоматически удален. Для контроля даты истечения срока годности могут использоваться устройство считывания штрих-кода и монитор того, что в автоматическое устройство контроля смеси был загружен правильный концентрат препарата.
На фиг. 7 показано устройство 30 для приготовления смесей препаратов. Флаконы 31, 32 и 33 с концентратом препаратов вставляются в держатели 35, 36 и 37. Терминал 38 компьютера предварительно программируется в соответствии со способом настоящего изобретения так, что при вводе пользователем необходимых параметров и подачи соответствующей команды устройство завершает для оператора этапы определения дозировки и смешивания раствора в инфузионном мешке. Результаты определения дозировки могут снова распечатываться для прикрепления к мешку с окончательной смесью.
Соединитель 40 для жидкости на каждом сосуде с концентратом препарата обеспечивает возможность дозирования препарата из каждого флакона с помощью клапана или расходомера, а затем перекачки или дренирования через линию подачи 46 в инфузионный мешок 47. Считывающее устройство 41 штрих-кода контролирует тип препарата и дату истечения срока годности в каждом флаконе с концентратом препарата в соответствии с показаниями штрих-кода 42. Если в автоматическое контролирующее устройство 48 смеси был загружен неправильный концентрат препарата или если истек срок годности препарата, может раздаваться звуковой сигнал и/или устройство может автоматически производить блокировку для предотвращения подачи неправильного или несвежего препарата. Средство подачи 45 растворителя обеспечивает доставку требуемого растворителя в мешок 47 с окончательной смесью. Изготовитель этикеток 49 может вручную или автоматически наносить содержащую данные этикетку с клеевой подложкой на мешок с окончательной смесью. В соответствии со способом настоящего изобретения компьютер предварительно запрограммирован так, что при вводе пользователем необходимых параметров и подачи соответствующей команды устройство завершает этапы определения дозировки и смешивания раствора в инфузионном мешке для оператора. Результаты определения дозировки (включая информацию, высвечиваемую на экране дисплея, показанную на фиг.5) снова могут распечатываться для прикрепления на инфузионный мешок с окончательной смесью.
Резюме
Способ и устройство настоящего изобретения стандартизируют и упрощают применение препаратов для постоянного внутривенного вливания, включая препараты для анестезии и анальгезии. Учреждениям, в которых активно применяются предложенные смеси, следует стандартизировать скорость вливания всех перечисленных препаратов.
При упрощении определений дозировки и при использовании компьютера и/или компьютеризированного устройства контроля смеси анестезиологи смогут активнее применять имеющиеся средства. Процедура позволяет легко смешивать любой требуемый объем препарата для операции определенной длительности. Это ведет к уменьшению расхода препарата. Настоящий способ особенно эффективен для первичных или дополнительных анестетических средств, анальгетических средств и седативных средств. Описание видов клинического применения анестезии с постоянным вливанием изложены в "White Paper", здесь не повторяются.
Большинству практикующих анестезиологов удобнее оценивать применение препарата в концепции "общей дозы". При использовании этой концепции выбранный С* (см. табл. 2) (мл/ч), умноженный на общее количество часов введения, будет равен общей дозе. Это лучше всего демонстрируется с помощью аналогичной концепции испарителя/процентной доставки.
Желаемый способ и важное усовершенствование практики доставки фармацевтических препаратов, включенные в настоящее изобретение, заключаются в применении предварительно отмеренных (и стандартизированных) флаконов анестетических препаратов с этикетками данных в виде штрих-кодов. Желательно, чтобы эти флаконы совпадали с показателями, представленными в табл. 1. Это обеспечивает возможность стандартизированного и более легкого смешивания препаратов анестезиологом. Это опять же повысило бы безопасность ввиду того, что производитель определял бы количества препаратов.
При использовании устройства (такого как компьютер или ему подобное) для завершения определения требуемых смесей различных препаратов, которые предполагается использовать в способе настоящего изобретения, это устройство может быть соединено с принтером для вывода на печать этикетки, которую предстоит прикрепить к инфузионному мешку. Для автоматизированного устройства смешивания может также быть предусмотрена возможность приготовления растворов препаратов с использованием флаконов с предварительно смешанным раствором или аналогичный способ калибровки требуемых объемов/масс препаратов и растворителя, которые предполагается использовать в мешке для вливания препаратов.
Способ настоящего изобретения может изменяться в соответствии с описанными формулировками для удовлетворения специфических функциональных характеристик в целях широкого разнообразия видов применения препаратов для внутривенного введения. Хотя способ введения препаратов для анестезии, предложенный настоящим изобретением, был подробно описан в предшествующем описании в целях иллюстрации, следует понимать, что эти подробности приведены исключительно с этой целью, и специалисты в этой области могут вносить в него изменения, не отходя от сущности и диапазона притязаний изобретения, описанного в следующей формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ анестезиологической защиты при выполнении оперативных вмешательств на позвоночнике у взрослых пациентов | 2020 |
|
RU2754837C1 |
| СПОСОБ ИНФУЗИОННОЙ ПОДДЕРЖКИ ПРИ КЕСАРЕВОМ СЕЧЕНИИ ПОД СПИНАЛЬНОЙ АНЕСТЕЗИЕЙ | 2015 |
|
RU2600668C1 |
| СПОСОБ АНЕСТЕЗИИ В АМБУЛАТОРНЫХ УСЛОВИЯХ У ПАЦИЕНТОВ СТОМАТОЛОГИЧЕСКОГО ПРОФИЛЯ | 2014 |
|
RU2591638C1 |
| АНЕСТЕТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ АНТАГОНИСТ NMDA И АЛЬФА-2 АДРЕНЕРГИЧЕСКИЙ АГОНИСТ | 2000 |
|
RU2244558C2 |
| СПОСОБ КАРДИОПРОТЕКЦИИ И НЕЙРОПРОТЕКЦИИ ВНУТРИВЕННЫМ ВВЕДЕНИЕМ ГАЛОГЕНСОДЕРЖАЩЕГО ЛЕТУЧЕГО АНЕСТЕЗИРУЮЩЕГО СРЕДСТВА | 2003 |
|
RU2350323C2 |
| СПОСОБ УПРАВЛЕНИЯ МНОГОКОМПОНЕНТНОЙ АНЕСТЕЗИЕЙ ПРИ ОБЩЕХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ | 2011 |
|
RU2499546C2 |
| СПОСОБ АНЕСТЕЗИОЛОГИЧЕСКОГО ОБЕСПЕЧЕНИЯ ОТКРЫТЫХ ОПЕРАЦИЙ НА ПЛОДЕ ПО КОРРЕКЦИИ SPINA BIFIDA | 2022 |
|
RU2789590C1 |
| Способ анестезиологического обеспечения радикальных операций у онкологических больных | 2016 |
|
RU2627289C1 |
| СОСТАВЫ ВНУТРИВЕННЫХ РАСТВОРОВ ПОЗАКОНАЗОЛА, СТАБИЛИЗИРОВАННЫЕ ПОСРЕДСТВОМ ЗАМЕЩЕННОГО БЕТА-ЦИКЛОДЕКСТРИНА | 2011 |
|
RU2575768C2 |
| АНЕСТЕЗИРУЮЩИЙ СОСТАВ | 2011 |
|
RU2574022C2 |





Изобретение относится к медицине, в частности к анестозиологии, и касается подготовки и введения одного или более растворов препаратов для постоянного вливания. Согласно изобретению, скорости потока стандартизируются с помощью изменения концентраций препаратов в соответствии с предварительно установленным набором таблиц. Способ значительно упрощает клиническое применение анестезии путем постоянного вливания и обеспечивает возможность легкого приготовления различных объемов, которые сводятся к минимальному расходу препаратов. Стандартизация скорости, предусмотренная настоящим способом, облегчает интерпретацию и смешивание, приводит к облегчению применения препаратов и повышает безопасность пациента. Устройство облегчает точный и эффективный перевод в нестандартные скорости потока, требуемые для особых видов применения. Компьютеризированное устройство выполняет смешивание и подачу конечного раствора препарата в готовый к применению инфузионный мешок. Способ и устройство позволяют вводить лекарственные средства при нестандартных скоростях потока, требуемых в особых ситуациях, таких как анестезия у новорожденных, когда требуются низкие скорости потока. Предварительно отмеренные количества анестетических препаратов вручную или с использованием компьютеризированного устройства подаются для проведения контроля полученной смеси. Изобретение обеспечивает повышение безопасности пациентов ввиду стандартизированных количеств препаратов, приготовленных производителем. 4 с. и 26 з.п. ф-лы, 7 ил., 3 табл.
| WO 9310851 А1, 10.06.1993 | |||
| US 5040699 А, 20.08.1991 | |||
| US 4898578 А, 06.02.1990 | |||
| WHITE "Clinical uses of intravenous Anesthetic and Analgetic infusions", Anesthesia and Analgesia, 1989, p.161-171 | |||
| УСТРОЙСТВО ДЛЯ ДОЗИРОВАННОЙ ИНФУЗИИ | 1992 |
|
RU2063247C1 |
Авторы
Даты
2003-09-20—Публикация
1998-01-15—Подача