Изобретение относится к твердым галеновым формам типа таблеток с контролируемым высвобождением, предназначенным для очень быстрого, а затем пролонгированного высвобождения одного или нескольких действующих веществ.
Важность таких галеновых форм является несомненной. Очень быстрое высвобождение действующего вещества должно обеспечивать его практически мгновенную биологическую доступность, что особенно важно в том случае, когда пациент страдает острыми состояниями.
Однако в тех случаях, когда действующие вещества имеют короткую продолжительность полужизни, терапевтическая активность является весьма непродолжительной. В настоящее время для эффективного лечения часто требуется непрерывное и регулярное введение действующего вещества. Для этой цели разработаны многочисленные системы с очень быстрым и с пролонгированным высвобождением.
В качестве ссылки можно назвать, например, следующие патенты и заявки на патент, характеризующие уровень техники: WO 96/03111, US 4990335, ЕР 352190, BE 905282, ЕР 106443, ЕР 36350, ЕР 615444 и ЕР 220670.
Однако в известных из уровня техники системах кинетические характеристики высвобождения действующего вещества зависят от многих факторов, таких как ферментативная активность и значение рН, которые в значительной степени варьируются не только от особи к особи, но и для одного и того же индивидуума в зависимости от того, попадают они в пустой желудок или нет. Кроме того, значения рН изменяются на протяжении всего желудочно-кишечного тракта. Таким образом, для известных в качестве прототипов систем с очень быстрым и с пролонгированным высвобождением трудно с точностью предсказать профиль высвобождения in vivo данного вещества после его введения.
В основу настоящего изобретения была положена задача решить эту проблему с помощью таблеток, которые сохраняли бы свои характеристики высвобождения действующих веществ вне зависимости от условий применения in vivo.
При применении таблеток по изобретению получены достаточно хорошо воспроизводимые результаты, свидетельствующие о том, что контроль за скоростью высвобождения можно в значительной степени усиличить во время фазы пролонгированного высвобождения действующего вещества. При использовании таблеток по изобретению становится возможным оптимизировать введение действующего вещества в организм, принимая при этом во внимание как переносимость действующего вещества пациентом, так и фармакокинетические и метаболические профили действующего вещества.
Кроме того, таблетки по изобретению имеют преимущество с точки зрения композиции действующего вещества, поскольку научно обоснованный выбор эксципиентов позволяет приготовить таблетки с более высокими концентрациями действующих веществ.
Так, в частности, можно получать таблетки с очень высоким дозами, имеющие размер, приемлемый для орального введения.
Более конкретно изобретение относится к многослойным таблеткам для очень быстрого, а затем пролонгированного высвобождения действующих веществ, включающим по меньшей мере два наложенных друг на друга слоя, отличающимся тем, что:
- первый наружный слой состоит из смеси эксципиентов и первого действующего вещества, и этот первый слой позволяет осуществлять очень быстрое высвобождение первого действующего вещества,
- второй слой, который контактирует с первым слоем и состоит из биологически неразложимой инертной пористой полимерной матрицы, в которой диспергировано второе действующее вещество.
Второй слой, контактирующий с первым слоем, либо полностью, либо только частично покрывается первым слоем.
В первом случае два слоя являются концентрическими.
Во втором случае только одна из поверхностей второго слоя контактирует с первым слоем: далее в контексте настоящего описания этот тип таблетки обозначен как "содержащий параллельные слои", причем форма таблетки не имеет решающего значения, в частности, она является яйцевидной. В этом случае очевидно, что два слоя имеют одну наружную поверхность, а их вторые поверхности находятся в контакте друг с другом.
Таблетки по изобретению предпочтительно являются двухслойными. Однако под объем изобретения также подпадают многослойные таблетки, если они включают комбинацию указанных выше первого и второго слоев.
Для некоторых действующих веществ при их включении в матрицу с пролонгированным высвобождением могут возникнуть проблемы, связанные со стабильностью. В этом случае целесообразно останавливать выбор на изготовлении таблеток, содержащих концентрические слои.
Кинетические характеристики высвобождения действующего вещества во всех случаях зависят от точного состава рассматриваемого слоя. Кинетические характеристики высвобождения можно изменять путем соответствующего подбора природы и количества эксципиентов, входящих в состав обоих слоев.
Одной из основных характеристик первого слоя является его быстрый распад в месте введения. В отличие от этого второй слой является биологически неразложимым. Его матрица является инертной в том отношении, что она не вступает во взаимодействие с окружающей средой. Матрица второго слоя сохраняет свою физическую и химическую целостность в течение всего времени пролонгированного высвобождения действующего вещества вне зависимости от изменения значений рН.
Поскольку первый слой очень быстро распадается при контакте с водной средой, такой как физиологическая среда, легко понять, почему высвобождение первого действующего вещества является практически мгновенным.
В случае второго слоя, поскольку составляющая его матрица является инертной (она не распадается и не разбухает в водной среде), высвобождение второго действующего вещества происходит вследствие выщелачивания и диффузии. Окружающая водная среда постепенно проникает в инертную пористую матрицу, и затем постепенно эта водная среда растворяет действующее вещество, диспергированное в инертной матрице. Поскольку механизм диффузии является медленным по своей природе, можно понять, почему в этом случае высвобождение действующего вещества является пролонгированным.
Так как механизм разложения первого слоя не зависит вообще или зависит лишь в незначительной степени от природы действующего вещества, ясно, что большая или меньшая степень гидрофильности действующего вещества второго слоя может влиять на кинетические характеристики выщелачивания/диффузии.
Однако изобретение не ограничено природой действующих веществ. Каждый слой может содержать различные действующие вещества.
Однако согласно одному из конкретных вариантов осуществления изобретения первый и второй слои включают одно и то же действующее вещество.
В частности, действующие вещества могут быть выбраны из любого вещества из следующих групп (для обозначения действующих веществ использованы международные названия, не являющиеся товарными знаками):
- лекарственные средства, активные в отношении астмы, такие как 2-этоксиметил-4-(3Н)-птеридинон, и бронхолитические средства, такие как теофиллин, и/или некоторые противовоспалительные агенты или антигистаминные препараты типа кетотифена;
- лекарственные средства, активные в отношении лечения диабета и связанных с ним показаний неврологического, нефрологического, глазного или васкулярного типа. В качестве примера можно назвать метформин, гиполипидемические агенты, такие как фенофибрат или правастатин и антиатеросклеротические агенты в целом;
- лекарственные средства, активные в отношении лечения алкоголизма, такие как акампросат;
- периферические аналгетики, например производные пара-аминофенола, такие как парацетомол, салицилированные производные, такие как аспирин, дифлунизал, производные пропионовой кислоты, такие как ибупрофен, фенопрофен, кетопрофен, производные аминохинолина, такие как флоктафенин, производные пиразолона, такие как норамидопирин;
- центральные аналгетики, такие как декстропоксифен, кодеин, морфин, петидин, декстроморамид, бупренорфин, налбуфин, пентазоцин;
- антиспазматические средства, такие как тиемониум, дифемерин, флороглуцинол, тримебутин, пинавериум, прифиниум;
- нестероидные противовоспалительные средства, такие как, например:
- производные арилпропионовой кислоты, такие как кетопрофен, ибупрофен, напроксен, флурбипрофен, алминопрофен, тиапрофеновая кислота,
- производные арилуксусной кислоты, такие как диклофенак, фентиазак,
- производные арилкарбоновой кислоты, такие как фенбуфен и этодолак,
- производные антраниловой кислоты или фенаматы, такие как нифлуминовая кислота и мефенамовая кислота,
- индольные производные, такие как индометацин и оксаметацин,
- оксикамы, такие как пироксикам, теноксикам,
- пиразолсодержащие производные, такие как фенилбутазон,
- производные индена, такие как сулиндак;
- стероидные противовоспалительные средства, такие как кортикоиды преднизонового, преднизолонового и метилпреднизолонового типа;
- антибиотики
β-лактамового типа, такие как пенициллины,
цефалоспоринового типа, такие как цефуроксимаксетил,
типа ингибиторов β-лактамазы, такие как клавулановая кислота,
аминогликозидного типа, такие как неомицин,
макролидного типа, такие как спирамицин, эритромицин,
тетрациклинового типа, такие как миноциклин и доксициклин,
сульфамидного типа, такие как сульфадиазин,
хинолонового типа, такие как пефлоксацин;
- противотуберкулезные средства, такие как изониазид, рифампицин, этамбутол, пиразинамид;
- полиеновые противогрибковые агенты, такие как амфотерицин В, нистатин,
- имидазолсодержащие противогрибковые агенты, такие как миконазол, кетоконазол, флуконазол, флуцитозин, гризеофулвин;
- антивирусные агенты типа зидовудина, ацикловира, адамантана, такие как римантадин, амантадин и мороксидин;
- β-адреноблокирующие средства, такие как ацебутолол, целипролол, атенолол, бетаксолол, метопролол, бизопролол, пропанолол, надолол, тимолол, тертатолол, соталол, пиндолол, пенбутолол, картеолол, оксипренолол, лабеталол;
- нитрованные производные, такие как динитрат изосорбида, мононитрат изосорбида, тетранитрат пентаэритритила, тетранитрат эритритила;
- противоангинозные средства типа сиднонимина, такие как молсидомин и линсидомин;
- кардиотонические средства, такие как орципреналин, или в альтернативном варианте типа дигиталина, такие как дигоксин, дигитоксин;
- мочегонные средства, такие как фуросемид, буметанид, клопамид, типа тиазида, такие как гидрохлортиазид, ксипамид, типа тиенилиновой кислоты, такие как индапамид, циклетанин, спиронолактон, канренон, амилорид, триамтерон;
- ингибиторы участвующих в превращении ферментов, такие как каптоприл, эналаприл, лизиноприл, периндоприл, хиналаприл, рамиприл, беназеприл;
- ингибиторы кальция, такие как нифедипин, никардипин, нитрендипин, дилтиазем, верапамил, бепридил;
- антигипертензивные средства, такие как рилменидин, клонидин, метилдопа, дигидралазин, празозин, урадипил, миноксидил;
- антиаритмические средства, такие как хинидин, дизопирамид, цибензолин, пропафенон, флекаинид, априндин, надоксолол, мексилетин, бретилиум, амиодарон;
- антиишемические средства, такие как нафтидрофурил, триметазидин, пентоксифиллин, ницерголин, буфломедил, дигидроэрготоксин, дигидроэргокристин, дигидроэргокриптин, моксисилит, раубазин, винкамин, папаверин, никотиновая кислота;
- венотомические средства, такие как витамин Р;
- корректоры гипотензии, такие как гептаминол;
- гормоны, такие как тиреоидные гормоны типа левотироксина натрия;
- лекарственные средства, стимулирующие гастродуоденальную моторную функцию, такие как цисаприд, домперидон;
- противорвотные средства, такие как метоклопрамид, метопимазин, алипразид, одансетрон, скополамин;
- противоязвенные агенты, такие как ранитидин, фамотидин, низатидин, циметидин, омепразол, противоязвенные средства простагландинового типа, такие как мизопростол, сукралфат, гидроксид алюминия;
- антидиарейные средства, такие как лоперамид, дифеноксилат, лекарственные средства, усиливающие рост бактериальной флоры и усиливающие рост дрожжевой флоры;
- кишечные антисептики, такие как нитрофуран;
- контрацептивы, такие как остропрогестогены;
- антианемичные средства, такие как железо;
- антигистаминные препараты, такие как фенотиазин;
- витамины, такие как тиамин, никотинамид, пиридоксин, биотин, аскорбиновая кислота, цианкобаламин, ретинол, холекальциферол;
- антиэпилептические средства, такие как валпроновая кислота, фенитоин, карбамазепин, этосукцимид, прогабид, вигабатрин;
- средства от мигрени, такие как оксеторон, индорамин, эрготамин, производные спорынии ржи, такие как дигидроэрготамин, метисергид, трициклические производные, такие как пизотифен;
- антикоагулянты, такие как агенты, препятствующие проявлению биологической активности витамина К;
- средства против болезни Паркинсона, такие как леводопа, селегилин, лисурид, бромкриптин, бипериден, орфенадрин, проциклидин, тропатепин, скополамин;
- анксиолитические средства, являющиеся производными бензодиазепинов, такие как клотиазепам, тофисопам, оксазепам, алпразолам, лоразепам, бромазепам, празепам, буспирон, алпидем, гидроксизин, мепробамат, фебарбамат;
- антидепрессанты, такие как хинупрамин, десипрамин, имипрамин, кломипрамин, амитриптилин, вилоксазин, аминептин, флувоксамин, флуоксетин, тианептин, оксафлозан, мапротилин, миансерин, тразодон, медифоксамин, толоксатон, IMAOs;
- гипнотические средства, такие как зопиклон, золпидем и производные бензодиазепина, такие как флунитразепам, нитразепам, триазолам, производные фенотиазина, такие как ниапразин, доксиламин, производные барбитурата, такие как бутобарбитал, амобарбитал, фенобарбитал;
- средства, нормализующие функцию тимуса, такие как литий, вальпромид;
- нейролептики, такие как тиоксантен, пимозид, локсапин, карпипрамин, производные фенотиазина, такие как хлорпромазин, тиоридазин, флуфеназин, производные бутирофенона, такие как галоперидол, пенфлуридол, пипамперон, бенперидол, производные бензамида, такие как сульпирид, амисульпирид, тиаприд, сультоприд;
- антиметаболиты, такие как метотрексат, меркаптопурин, флуороурацил, цитарабин, гидроксомочевина, аспарагиназа;
- алкилирующие агенты, такие как бусулфан, пипоброман, прокарбазин, азотсодержащие производные горчицы, такие как хлорамбуцил, циклофосфамид, эстрамустин, мелфалан, ломустин, фотемустин;
- противораковые стероиды, такие как метоксипрогестерон, гестонорон, норэтистерон, диэтилстилбестрол, диенэстрол;
- и более общий класс пептидов, обладающих терапевтической активностью.
В качестве действующего вещества может также быть выбрана фармацевтически приемлемая соль любого из перечисленных выше действующих веществ, способного образовывать соли.
Содержание действующего вещества в первом слое должно определяться в зависимости от подлежащей лечению патологии.
Это содержание может быть высоким, при этом содержание действующего вещества может составлять до 99% в пересчете на общую массу первого слоя, например от 1 до 99,0 мас.%, предпочтительно от 85 до 95 мас.% в пересчете на общую массу первого слоя.
Второй слой может содержать до 98,5 мас.% действующего вещества, например от 1 до 95 мас.%, более предпочтительно от 60 до 80%.
Многочисленные композиции с очень быстрым высвобождением известны в данной области, и поэтому специалистам в данной области техники известны технологии, позволяющие легко изготовить первый слой.
Так, в частности, составляющие первого слоя можно выбрать таким образом, чтобы обеспечить быстрый его распад при контакте с водой или физиологическими средами.
Известно, например, что в этот тип слоя можно включать разрыхлитель, роль которого состоит в способности вызывать разрушение таблетки в присутствии воды или физиологических сред.
Эти разрыхлители, как правило, включают в этот слой в количестве от 0 до 15 мас. %, предпочтительно от 2 до 5 мас.%. Примерами таких разрыхлителей являются альгиновая кислота, карбоксиметилцеллюлоза кальция, карбоксиметилцеллюлоза натрия, безводная коллоидная двуокись кремния, кроскармеллоза натрия, кросповидон, гуаровая камедь, силикат магния и алюминия, метилцеллюлоза, микрокристаллическая целлюлоза, полакрилин калия, целлюлоза, предварительно оклейстеризованный крахмал, альгинат натрия, натрийгликолят крахмала, крахмал и шипучие смеси, разрыхляющее действие которых известно в данной области.
Шипучие смеси представляют собой часть соединений, способных быстро вызывать разрушение первого слоя, особенно когда последний приходит в контакт с кислотами желудочного сока. Эти смеси, как правило, содержат карбонаты или бикарбонаты щелочного металла или щелочноземельного металла или глицинкарбонат натрия.
В слой с очень быстрым высвобождением могут быть включены другие добавки, такие как разбавители, связующие агенты, замасливатели, антиоксиданты, красители, подслащивающие вещества, корригенты и подкислители, смачивающие агенты, гидрофилизирующие агенты, такие как сорбит и циклодекстрины, агенты для регулирования осмотического давления, такие как маннит, вещества для коррекции значения рН, стабилизирующие агенты, такие как трегалоза и маннит, адсорбирующие вещества, хелатирующие агенты и пассиваторы и устойчивые к действию желудочных соков эксципиенты для образования пленочного покрытия типа ацетилфталата целлюлозы и полиметакрилатов.
В качестве примера может быть выбран любой один из следующих разбавителей: карбонат кальция, сульфат кальция, сахароза, декстраты, декстрин, декстроза, дигидрат дикальцийфосфата, каолин, карбонат магния, оксид магния, мальтодекстрин, целлюлоза, микрокристаллическая целлюлоза, сорбит, крахмалы, предварительно оклейстеризованный крахмал, тальк, трикальцийфосфат и лактоза или же комбинация этих веществ.
Из связующих веществ следует назвать гуммиарабик, трагакантовую камедь, гуаровую камедь, альгиновую кислоту, альгинат натрия, карбоксиметилцеллюлозу натрия, декстрин, желатин, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, жидкую глюкозу, силикат магния и алюминия, мальтодекстрин, повидон, предварительно оклейстеризованный крахмал, крахмал и зеин.
Замасливатели представляют собой способствующие скольжению вещества (такие как безводная коллоидная двуокись кремния, трисиликат магния, силикат магния, целлюлоза, крахмал, тальк или трикальцийфосфат) или в другом варианте представляют собой агенты, способствующие приданию антифрикционных свойств (такие как стеарат кальция, глицерилмоностеарат, глицерилпальмитостеарат, гидрогенизированные растительные масла, парафин, стеарат магния, полиэтиленгликоль, бензоат натрия, лаурилсульфат натрия, фумаровая кислота, стеариновая кислота или стеарат цинка и тальк).
В качестве примера антиоксидантов можно назвать следующие соединения: аскорбиновую кислоту, аскорбилпальмитат, фумаровую кислоту, пропилгаллат, аскорбат натрия и метабисульфит натрия, альфа-токоферол, яблочную кислоту, трет-бутил-4-метоксифенол (ВНА) и ВТН.
Предпочтительными смачивающими веществами являются следующие:
- докусат натрия и лаурилсульфат натрия, которые представляют собой анионогенные поверхностно-активные вещества;
- бензалконийлорид, бензетоний хлорид и цетримид, которые представляют собой катионогенные поверхностно-активные вещества;
- глицерилмоноолеат, эфиры жирных кислот и полиоксиэтиленсорбитана, поли (виниловых спиртов) и сорбитанов, которые представляют собой неионогенные поверхностно-активные вещества.
Из регуляторов рН известны подкисляющие агенты типа, например, лимонной кислоты, соляной кислоты, молочной кислоты, винной кислоты, а также подщелачивающие агенты типа, например, моноэтаноламина, диэтаноламина и триэтаноламина, цитрата натрия, бикарбоната натрия, дигидрата цитрата натрия.
Примерами адсорбирующих веществ являются бентонит, безводная коллоидная двуокись кремния, каолин, силикат магния и алюминия, микрокристаллическая целлюлоза и целлюлоза.
В качестве хелатирующих агентов и пассиваторов могут применяться моногидрат лимонной кислоты, эдетовая кислота, динатрийфосфат, первичный кислый фосфат натрия, цитрат калия, винная кислота и дигидрат цитрата натрия.
Количества этих добавок соответствуют таковым, обычно применяемым в данной области. Как правило, связующее вещество может составлять от 0,5 до 25 мас. %, более предпочтительно от 2 до 5 мас.% в пересчете на массу первого слоя.
Замасливатели предпочтительно входят в состав первого слоя в количестве от 0,01 до 10 мас.%.
Как правило, количество устойчивых к действию желудочных соков эксципиентов, предназначенных для образования пленочного покрытия, варьируется от 0,5 до 9 мас.%.
Следует отметить, что все вышеперечисленные добавки, за исключением разрыхлителей, также могут входить в аналогичных пропорциях в состав слоя с пролонгированным высвобождением. Кроме того, слой с пролонгированным высвобождением может включать разбавители, выбранные из группы, включающей глицерилпальмитостеарат, гидрогенизированные растительные масла, полиметакрилаты, хлорид калия и хлорид натрия.
Кроме того, в слой с пролонгированным высвобождением могут входить связующие вещества, такие как карбомер, этилцеллюлоза, гидрогенизированные растительные масла, гидроксипропилметилцеллюлоза, метилцеллюлоза и полиметакрилаты.
Однако основными компонентами второго слоя с пролонгированным высвобождением являются полимерные материалы, которые обусловливают его инертные и биологически неразложимые свойства. Согласно изобретению рассматриваемыми полимерными материалами являются нерастворимые в воде (но не образующие геля при погружении в водную среду) полимеры или сополимеры, которые выводятся организмом в интактной форме.
Эти полимеры могут играть роль связующего вещества в композиции второго слоя.
Такие материалы, в частности, представлены поливинилхлоридами, сополимерами винилацетата и винилхлорида, сополимерами акрилонитрила и винилиденхлорида, полидиметилсилоксанами и сополимерами, дериватизированными из (мет)акриловых кислот.
Сополимеры, дериватизированные из (мет)акриловых кислот, включают сополимеры производных метакриловой кислоты и сополимеры производных акриловой кислоты и производных метакриловой кислоты. В качестве производных (мет)акриловых кислот предпочтительными являются эфиры.
Согласно предпочтительному варианту осуществления изобретения биологически неразложимый инертный полимерный материал выбирают из группы, включающей сополимеры этилакрилата и метилметакрилата, сополимеры метакрилата этиламмония и метилакрилата, сополимеры метакрилата этиламмония и этилакрилата, сополимеры метакрилата этиламмония и метилметакрилата, сополимеры метакрилата этиламмония и этилметакрилата, сополимеры метакриловой кислоты и этилакрилата, сополимеры метакриловой кислоты и метилметакрилата.
Согласно изобретению "этиламмоний" обозначает радикал, выбранный из группы, включающей аммониоэтил, С1-С4-алкиламмониоэтил, ди-С1-С4-алкиламмониоэтил и три-С1-С4-алкиламмониоэтил. Предпочтительно этиламмоний обозначает триметиламмониоэтильный радикал.
Такие продукты поставляются на рынок, например, компанией Rohm.
Исключительно в качестве справки следует также упомянуть следующие вещества:
- сополимеры Eudragit RL 30 D®, Eudragit RS 30 D®, Eudragit RL PO D®, Eudragit RS PO D®, Eudragit RL 12.5 D®, Eudragit RS 12.5 D®, Eudragit RL 100 D® и Eudragit RS 100®, которые представляют собой сополимеры эфиров акриловой кислоты и эфиров метакриловой кислоты с низким содержанием аммонийных групп. Эти полимеры несут в качестве повторяющегося звена группу: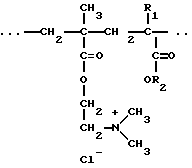
где R1 обозначает атом водорода или метальную группу, a R2 обозначает метильную или этильную группу;
- сополимер Eudragit NE 30 D®, который представляет собой нейтральный сополимер этилакрилата и метилметакрилата, в котором повторяющееся звено имеет формулу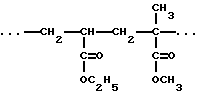
- сополимеры Eudragit L 30 D-55® и Eudragit L100-55®, которые представляют собой сополимеры метакриловой кислоты и этилакрилата, в которых повторяющееся звено имеет формулу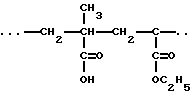
- сополимеры Eudragit L 100®, Eudragit S 12.5®, Eudragit S 100® и Eudragit S 12.5®, которые представляют собой сополимеры метакриловой кислоты и метилметакрилата, в которых повторяющееся звено имеет формулу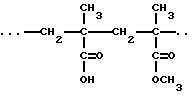
Из этих сополимеров особенно предпочтительным оказался сополимер NE 30 D®. В целом, применение сополимеров эфиров метакриловой кислоты и эфиров акриловой кислоты является предпочтительным для любого типа инертной матрицы.
Молекулярная масса применяемого полимерного материала может варьироваться в широких пределах в зависимости от природы мономеров, входящих в этот материал.
В том случае, когда сополимеры получают из указанных выше акриловой и/или метакриловой кислоты, средняя молекулярная масса составляет от 100000 до 1000000, предпочтительно от 130000 до 800000.
Предпочтительно, чтобы количество инертных полимерных материалов не превышало 25% от общей массы второго слоя, но не составляло менее 1% от общей массы этого слоя. Предпочтительно, чтобы количество полимерных материалов составляло от 2,5% до 12% от общей массы второго слоя.
На всю таблетку может быть нанесено покрытие из устойчивой к действию желудочных соков или из энтеросолюбильной полимерной пленки, в результате чего действующее вещество высвобождается только в двенадцатиперстной кишке.
Как правило, полимерные вещества, применяемые для получения устойчивой к действию желудочных соков системы, представляют собой ацетофталат целлюлозы, ацетопропионат целлюлозы, тримеллитат целлюлозы или полимеры или сополимеры (мет)акриловых кислот.
Таблетки по изобретению, как правило, получают способом, предусматривающим грануляцию с последующим прессованием.
Более конкретно способ получения, который является объектом изобретения, включает следующие стадии:
а) получение гранулята первого действующего вещества из порошкообразной смеси этого первого действующего вещества, разрыхлителя и одной или нескольких добавок, пригодных для получения слоя для очень быстрого высвобождения этого действующего вещества,
б) получение гранулята второго действующего вещества из порошкообразной смеси этого второго действующего вещества, из одного или нескольких биологически неразложимых инертных полимерных материалов и из одной или нескольких добавок, пригодных для получения слоя для пролонгированного высвобождения этого действующего вещества,
в) объединение путем прессования хорошо известным методом двух типов гранулятов, полученных на описанных выше стадиях а) и б), с получением таблеток, в которых первый слой, позволяющий осуществлять очень быстрое высвобождение, получают прессованием гранулята, полученного на стадии а), и в которых имеется второй слой, находящийся в контакте с первым слоем, причем этот второй слой получают прессованием гранулята с пролонгированным высвобождением, полученного на стадии б).
Первая стадия (стадия а)) служит для получения гранулята, основой которого является первое действующее вещество, и эта стадия после прессования позволяет получить первый слой, обозначенный как слой с очень быстрым высвобождением.
Вторая стадия (стадия б)) служит для получения гранулята, основой которого является это же действующее вещество или другое действующее вещество, и эта стадия после прессования позволяет получить второй слой, обозначенный как слой с пролонгированным высвобождением. Составляющими этого слоя являются продукты, входящие в состав описанной выше биологически неразложимой инертной полимерной матрицы.
Стадия в) служит для получения таблетки путем последовательного прессования гранулятов, полученных на описанных выше стадиях а) и б).
Стадии а) и б) включают грануляцию порошкообразных форм аморфных или кристалличесикх частиц. Эту грануляцию проводят хорошо известным методом, например методом мокрой грануляции.
Метод грануляции включает пять основных стадий: (I) смешение различных составляющих в сухом виде, (II) смачивание, (III) соответствующая грануляция, (IV) сушка и затем (V) классификация, т.е. разделение по размерам.
Смешение в сухом виде представляет собой смешение порошкообразных эксципиентов, входящих в состав гранулята.
Увлажнение состоит в добавлении к порошкообразной смеси различных составляющих, смачивающей жидкости, которая может представлять собой воду, С1-С4-алканол, водный раствор связующего вещества или спиртовой раствор связующего вещества. Согласно изобретению понятие "спиртовой раствор связующего вещества" включает как спиртовые, так и водно-спиртовые растворы, в которых растворитель представляет собой смесь одного или нескольких С1-С4-алканолов или смесь воды и одного или нескольких С1-С4-алканолов. Предпочтительным С1-С4-алканолом является изопропанол. Процесс осуществляют в месильной машине, в смесителе планетарного типа, в чане для смешения, в миксере выдавливающего или вихревого типа или в смесителе-грануляторе быстрого типа.
На стадии а) приемлемой смачивающей жидкостью является вода, C1-С4-алканол, водный раствор связующего вещества или спиртовой раствор связующего вещества, как он определен выше, который обычно рекомендуется для применения в данной области.
На стадии б) в качестве смачивающей жидкости можно использовать водную дисперсию или органический раствор биологически не разложимого (ых) полимерного (ых) материала (ов). При этом достигается более гомогенное распределение матрицы. Под понятием "органический растворитель" в контексте изобретения следует понимать раствор биологически не разложимого (ых) полимерного (ых) материала (ов) в органическом растворителе, который представляет собой либо смесь одного или нескольких С1-С4-алканолов, либо смесь одного или нескольких (С1-С4-алкил)(С1-С4-алкил)кетонов и одного или нескольких С1-С4-алканолов. Согласно изобретению предпочтительным С1-С4-алканолом является изопропанол. Аналогично этому, когда используют смесь кетона(ов) и спирта (ов), предпочтительными являются изопропанол и ацетон.
Когда полимерный материал представляет собой сополимер, полученный на основе акриловой и/или метакриловой кислоты, дисперсия или раствор предпочтительно должны иметь вязкость от 10 до 300 мПа•с, более предпочтительно от 15 до 200 мПа•с.
Согласно предпочтительному варианту осуществления изобретения классификацию осуществляют просеиванием продукта через сито с размером ячеек от 0,5 до 1,5 мм, предпочтительно от 0,8 до 1,5 мм.
Предпочтительный размер ячеек, который используется на каждой из стадий а) и б), составляет 1,25 мм.
Однако изобретение не ограничено использованием метода мокрой грануляции. Так, в частности, можно применять также другие существующие методы грануляции, такие как метод сухой грануляции.
Последняя стадия (стадия в)) служит для получения таблетки. Объединение гранулятов проводят общепринятым методом, используя грануляты, полученные на стадиях а) и б).
В случае двухслойных таблеток, содержащих концентрические слои, эта стадия включает (I) прессование в первой камере для прессования всего гранулята с пролонгированным высвобождением, полученного на стадии б), с получением ядра таблетки, (II) прессование во второй камере для прессования части, предпочтительно 50 мас.% гранулята с очень быстрым высвобождением, полученного выше на стадии а), (III) введение во вторую камеру для прессования и регулировку положения ядер таблеток, полученных выше на стадии (I), (IV) осторожное прессование с центрированием ядра в этой второй камере для прессования, (V) добавление оставшейся части гранулята с очень быстрым высвобождением во вторую камеру для грануляции и (VI) совместное спрессовывание гранулята с очень быстрым высвобождением с таблеткой, полученной выше на стадии (IV).
В случае двухслойных таблеток, содержащих параллельные слои, стадия в) включает (I) острожное прессование всего гранулята с пролонгированным высвобождением в камере для прессования, а затем (II) добавление всего гранулята с очень быстрым высвобождением в эту камеру для прессования и регулировку его положения на таблетке, полученной выше на стадии (I), и (III) конечную стадию прессования таблетки.
Относительные пропорции гранулята с очень быстрым высвобождением и с пролонгированным высвобождением не имеют решающего значения согласно изобретению.
Таблетки по изобретению могут вводиться оральным или вагинальным путем. Они дают возможность очень быстро высвобождаться первому действующему веществу, а затем высвобождение второго действующего вещества, которое необязательно идентично первому, происходит в течение 2-12 ч.
Многослойные таблетки по изобретению являются особенно предпочтительными, поскольку способ их получения является простым, а входящие в их состав эксципиенты имеются в продаже. Кроме того, при их изготовлении возможно путем соответствующего подбора биологически неразлагаемых инертных полимерных материалов изменять профили растворения в очень большом диапазоне и с высокой точностью в зависимости от конкретных требований.
Согласно предпочтительному варианту осуществления изобретения применяют полимерные материалы, относящиеся к продуктам из серии Eudragit, которые поставляются на рынок компанией Röhm. Эти материалы представляют собой сополимеры, полученные из метакриловой и/или акриловой кислоты. Благодаря разнообразию свойств этих сополимеров можно изменять профиль высвобождения действующих веществ.
Кроме того, эти сополимеры придают получаемым таблеткам очень высокую емкость в отношении композиции (возможность включать высокие уровни действующих веществ) и способность к прессованию.
Выбор таких сополимеров, кроме того, определят возможность осуществлять нанесение пленочного покрытия на таблетки, изготовленные с использованием в качестве эксципиентов материалов типа Eudragit, для получения устойчивого с действию желудочных соков покрытия.
С другой стороны, эти сополимеры абсолютно инертны в отношении организма, что обеспечивает высвобождение действующего вещества независимо от воздействия на этот процесс организма (в частности, изменения значений рН), в результате чего достигается надежность, безопасность, высокое качество, воспроизводимость и лучшая переносимость воздействий при введении таблеток по изобретению.
Ниже изобретение проиллюстрировано на примерах. При этом используются ссылки на приложенные к описанию фиг.1-6.
Пример 1
а) Получение и композиция гранулята с очень быстрым высвобождением
Действующее вещество представляет собой 2-этоксиметил-4(3Н)-птеридинон, который ниже обозначен как ЭМП.
Для получения гранулята с очень быстрым высвобождением, обозначенного ниже как GLI-1, используют следующие ингредиенты, взятые в указанных ниже соотношениях в пересчете на массу,%:
ЭМП - 94,12
Поливинилпирролидон 30 - 2,94
Сшитая карбоксиметилцеллюлоза - 2,94
Всего - 100,00
Действующее вещество, поливинилпирролидон 30 и карбоксиметилцеллюлозу вводят в смеситель-гранулятор для смешения в течение 3 мин.
Затем в смеситель-гранулятор вводят смачивающую жидкость, т.е. воду с установленным осмотическим давлением, до тех пор, пока не получат правильно оформленные гранулы и агломераты. Затем весь продукт сушат (сушильная печь или в псевдоожиженном воздушном слое) и классифицируют с помощью сита с размером ячеек 1,25 мм.
б) Получение и композиция гранулята с пролонгированным высвобождением
Используют такое же действующее вещество, что и в примере 1.
Используемый биологически неразлагаемый полимерный материал представляет собой Eudragit NE 30 D®, поставляемый компанией 
Для получения гранулята с пролонгированным высвобождением, обозначенного ниже как GLP-1, используют следующие ингредиенты, взятые в указанных ниже соотношениях в пересчете на массу, %:
ЭМП - 71,70
Тонкоизмельченная порошкообразная лактоза - 17,20
Eudragit NE 30 D® - 8,80
Тальк - 1,10
Стеарат магния - 1,20
Всего - 100,00
Действующее вещество и лактозу вводят в смеситель-гранулятор для смешения в течение 3 мин. Затем в смесь постепенно вводят в качестве смачивающей жидкости Eudragit NE 30 D®, который представляет собой водную дисперсию нейтрального сополимера этилакрилата и метилметакрилата. При необходимости добавляют очищенную воду с целью получения правильно оформленных гранул, включающих агломераты. Затем гранулят сушат в псевдоожиженном воздушном слое и классифицируют с помощью сита с размером ячеек 1,25 мм. Затем с полученным выше гранулятом в течение 40 с перемешивают замасливатели (тальк и стеарат магния).
в) Получение таблеток, содержащих концентрические слои, и так называемых таблеток с параллельными слоями
Описанные ниже содержащие параллельные слои таблетки А-Г получают осуществлением следующих стадий с использованием таблетирующей машины, снабженной яйцевидными пресс-формами:
(I) осторожное прессование в камере для прессования всего гранулята с пролонгированным высвобождением из примера 1б),
(II) добавление в эту же камеру для прессования всего гранулята с очень быстрым высвобождением из примера 1а) на таблетку, полученную на стадии (1),
(III) последующее прессование всей смеси, состоящей из гранулята с очень быстрым высвобождением из примера 1а) и таблетки, полученной выше на стадии (I).
Описанные ниже содержащие концентрические слои таблетки Д получают осуществлением следующих стадий:
(а) прессование в первой камере для прессования всего гранулята с пролонгированным высвобождением из примера 1б) с получением ядра таблетки,
(б) прессование во второй камере для прессования части (примерно половины) гранулята с очень быстрым высвобождением из примера 1а),
(в) перенос таблетки, полученной на стадии (а), во вторую камеру для прессования,
(г) осторожное прессование с центрированием таблетки, полученной на стадии (а), во второй камере для прессования,
(д) добавление оставшейся части гранулята с очень быстрым высвобождением из примера 1а) во вторую камеру для прессования и
(е) совместное спрессовывание гранулята с очень быстрым высвобождением из примера 1а) и таблетки, полученной выше на стадии (г).
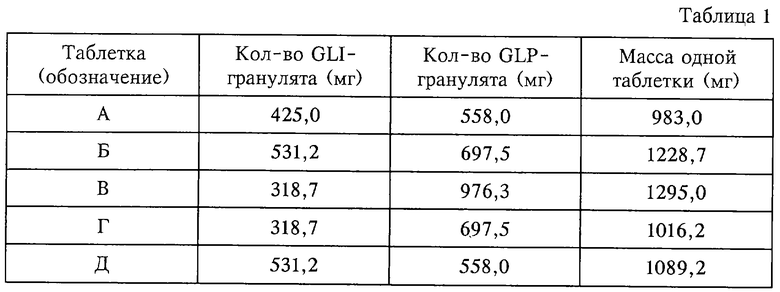
В приведенной ниже таблице 1 приведены данные об относительных количествах используемых гранулятов для каждой таблетки.
Пример 2
Профили растворения таблеток, изготовленных согласно примеру 1
Профили растворения таблеток, изготовленных согласно предыдущему примеру, определяют с помощью УФ-спектрометрии.
Тестируемые таблетки при 37oС вносят в реактор, который снабжен системой для регулирования температуры и эффективной системой для перемешивания и в который предварительно загружен 1 л воды с установленным осмотическим давлением. Во время всего эксперимента температуру в реакторе поддерживают на уровне 37oС.
Через определенные промежутки времени t берут образцы среды, содержащейся в реакторе, их фильтруют через фильтр с размером пор 0,48 мкм и анализируют с помощью УФ-спектрометрии.
Условия проведения анализа с помощью УФ-спектрометрии
Оптическую плотность собранных образцов, которые разбавлены известным объемом воды с установленным осмотическим давлением, измеряют при 313 нм.
Количество q присутствующего в образце действующего вещества определяют путем сравнения с оптической плотностью контрольного раствора действующего вещества, т.е. ЭМП, с известной концентрацией. Путем простого расчета можно определить общее количество действующего вещества, высвободившегося в реакторе к моменту времени t.
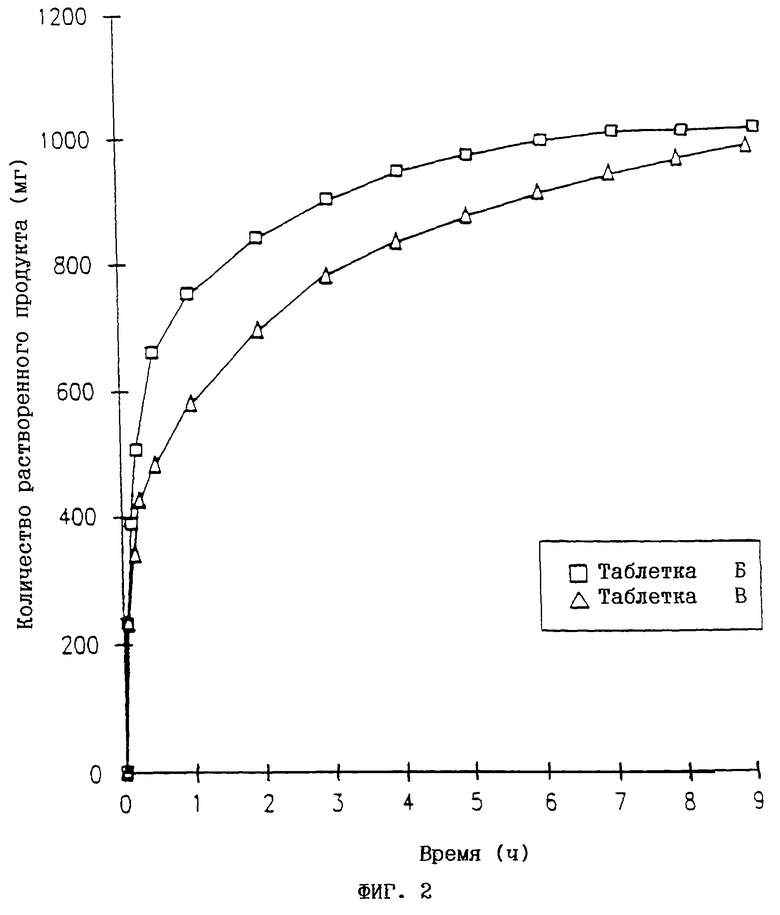
Профиль растворения для тестируемой таблетки получают, строя график зависимости рассчитанных количеств действующего вещества в функции от времени сбора.
На фиг.1 и 2 показаны профили растворения, полученные для описанных выше таблеток А-Д.
Пример 3
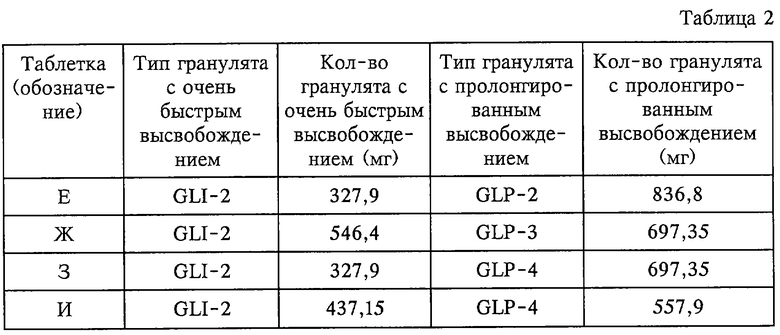
Работая по методике, описанной в примере 1, получают содержащие параллельные слои таблетки Е-И, состав которых приведен в таблице 2.
Состав гранулятов с очень быстрым высвобождением, т.е. GLI-2, приведен ниже, %:
ЭМП - 91,5
Поливинилпирролидон 30 - 4,0
Сшитая карбоксиметилцеллюлоза - 4,0
Стеарат магния - 0,5
Всего - 100,0
Эти грануляты получают согласно примеру la).
Составы гранулятов с пролонгированным высвобождением приведены ниже, %:
GLP-2
ЭМП - 71,7
Тонкоизмельченная порошкообразная лактоза - 16,0
Eudragit RSPO - 10,0
Тальк - 1,1
Стеарат магния - 1,2
Всего - 100,0
GLP-3
ЭМП - 71,7
Тонкоизмельченная порошкообразная лактоза - 17,2
Eudragit RS30D - 8,8
Тальк - 1,1
Стеарат магния - 1,2
Всего - 100,0
GLP-4
ЭМП - 71,7
Тонкоизмельченная порошкообразная лактоза - 17,2
Eudragit RS30D - 8,8
Тальк - 1,1
Стеарат магния - 1,2
Всего - 100,0
Эти грануляты получают согласно примеру 1б).
Пример 4
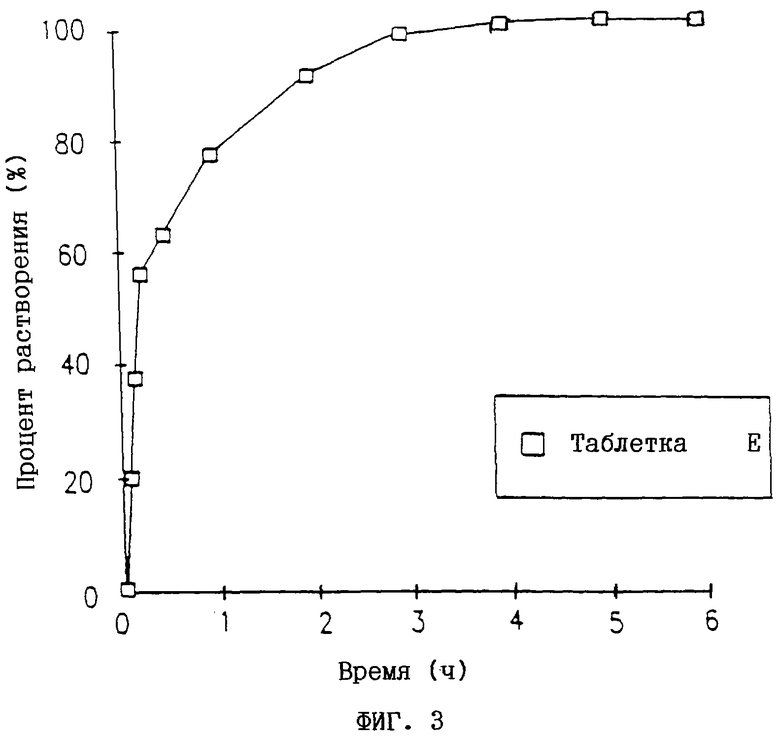
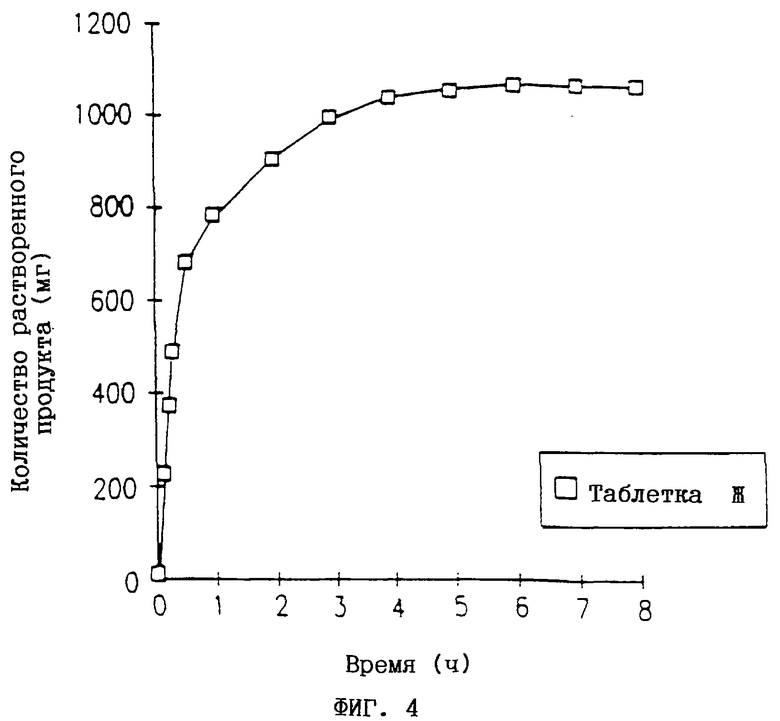
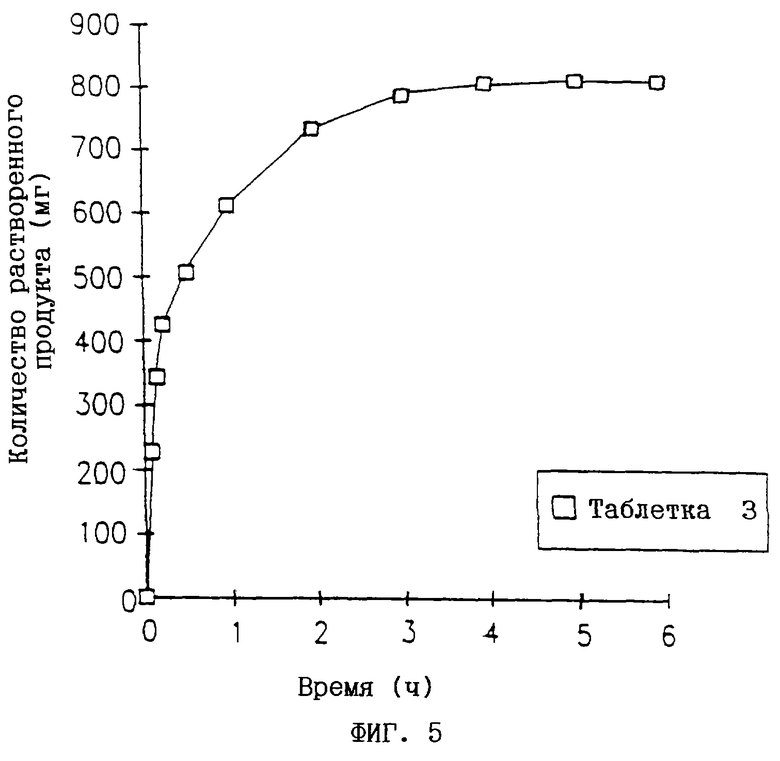
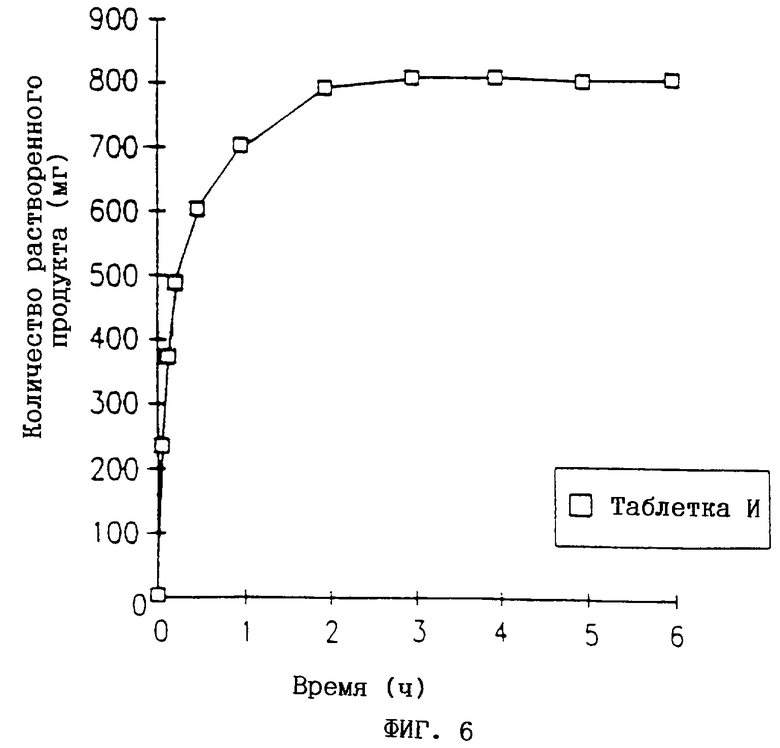
Кривые растворения для таблеток Е-И получают из графиков по методике, описанной в примере 2. Эти кривые представлены на фиг.3-6.
Описана двухслойная таблетка для очень быстрого, а затем пролонгированного высвобождения действующих веществ. Таблетка включает два наложенных друг на друга слоя. Первый наружный слой состоит из смеси эксципиентов, одного или нескольких разрыхлителей и действующего вещества. Первый слой позволяет осуществлять очень быстрое высвобождение действующего вещества. Второй слой контактирует с первым слоем и состоит из биологически неразлагаемой инертной пористой полимерной матрицы, в которой диспергировано действующее вещество. Таблетки по изобретению получают способом грануляции с последующим прессованием. Предпочтительно, действующим веществом является 2-этоксиметил-4(3Н)-птеридинон. Двухслойные таблетки по изобретению сохраняют свои кинетические характеристики высвобождения действующего вещества вне зависимости от условий применения in vivo. 2 с. и 9 з.п. ф-лы, 6 ил., 2 табл.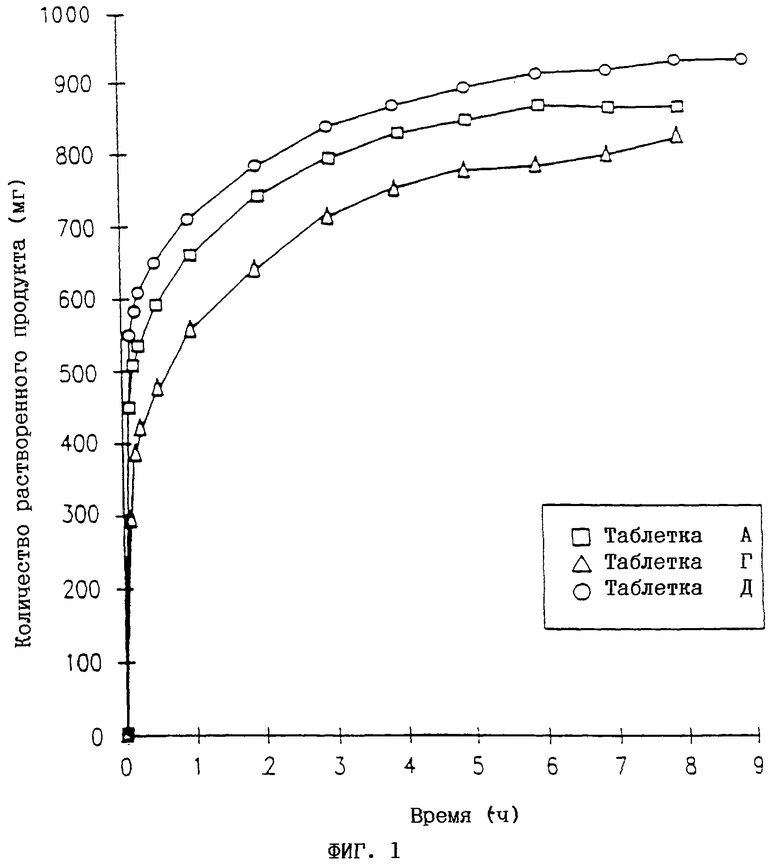
| US 4359483 A, 16.11.1982 | |||
| УСТРОЙСТВО ЛЕНТОПРОТЯЖНОГО МЕХАНИЗМА ДИКТОФОННОЙ ПРИСТАВКИ | 0 |
|
SU169821A1 |
| Блок конденсаторов и способ контроля его исправности (2 варианта) | 2016 |
|
RU2645152C2 |
| RU 94043798 A1, 10.11.1996. | |||
Авторы
Даты
2003-09-27—Публикация
1998-12-11—Подача