Изобретение относится к способу оценки риска развития пептической язвы путем определения наличия топографического фенотипа гастрита у индивидуума.
Хронический гастрит является крайне распространенным расстройством. По оценкам, почти у половины мирового населения в течение жизни разовьется гастрит. Чаще всего хронический гастрит вызван инфекцией Helicobacter pylori и в подавляющем большинстве случаев может считаться иммунологической реакцией против этой бактерии [1-6].
Хронический гастрит представляет собой достаточно уникальную бактериальную инфекцию с характерным хроническим течением и продолжительностью в течение всей жизни. Спонтанное излечение гастрита, нормализация слизистой оболочки желудка и в антральной части, и в теле желудка, является редким событием. Обычно естественное течение хронического гастрита представляет собой последовательность изменений от воспаления до атрофии, которая значительно меняет структуру и функцию слизистой оболочки желудка. Исход хронического гастрита представлен несколькими важными расстройствами, все из которых, как представляется, проявляют связь со специфическим изменением и с некоторым определенным состоянием в процессе течения гастрита.
Бактериальная инфекция приводит к простому воспалению в слизистой оболочке желудка, которое состоит из иммунокомпетентных лимфоцитов и плазматических клеток, а часто гранулоцитов [7-11]. Исследования, проведенные у детей и людей молодого возраста, свидетельствуют о том, что это хроническое воспаление представляет собой преобладающий начальный фенотип гастрита в раннем возрасте. У пожилых лиц часто встречающимися феноменами являются атрофия и кишечная метаплазия подлежащей слизистой оболочки, распространенность которых с возрастом возрастает [12-18].
Исследования свидетельствуют о медленном прогрессировании хронического гастрита до развития атрофии. Гастрит и последующая атрофия являются важными причинами нескольких функциональных и гомеостатических нарушений слизистой оболочки желудка. Атрофия приводит к недостаточности секреции кислоты, пепсиногенов и гастрина из слизистой оболочки тела и антрального отдела желудка наряду с развитием атрофии (утрата нормальных желез слизистой оболочки).
Инфекция Helicobacter pylori и гастрит являются важными факторами риска пептической язвы и 12-перстной кишки, и желудка. Гастрит предшествует и язвенной болезни 12-перстной кишки, и желудка, свидетельствуя о причинной связи между инфекцией Н. Pylori, гастритом и образованием язвы [19, 20]. Антральный гастрит (воспаление, ограниченное антральным отделом желудка) или пангастрит (воспаление и антрального отдела, и тела желудка) увеличивают риск развития язвенной болезни 12-перстной кишки приблизительно в 10 раз [19] . Антральный или пангастрит с одновременным наличием атрофии слизистой оболочки антрального отдела может и с кумулятивной, и с относительной точек зрения в десятки раз увеличить риск, в частности, язвенной болезни желудка, в сравнении с риском ее развития у людей со здоровым желудком [21, 22].
Гастрит может также снизить риск образования язв. Это, в частности, наблюдается в случае, когда гастрит развивается в теле желудка и прогрессирует в выраженную атрофию. Независимо от наличия и степени поражений в антральном отделе риск пептической язвы снижен до уровня, который даже ниже, чем у людей со здоровым желудком.
В целом, риск пептической язвы возрастает экспоненциально с возрастанием степени поражений антрального отдела (гастрит и атрофия), но экспоненциально снижается с увеличением степени поражений в теле желудка.
Электрофоретически можно дифференцировать 7 различных пепсиногенов из слизистой оболочки желудка у людей. Пять самых быстрых из них образуют иммунологически однородную группу пепсиногена I. Два других образуют группу пепсиногена II. Пепсиногены I группы синтезируются только в основных клетках и секретирующих слизь клетках области тела желудка. В отличие от них пепсиногены II группы образуются в железах по всему желудку и в некоторой степени также в верхней части 12-перстной кишки в железах Brunner. В сыворотке здорового человека концентрация пепсиногена I приблизительно в 6 раз превышает концентрацию пепсиногена II. При атрофическом гастрите области тела желудка сывороточная концентрация пепсиногена I снижается, тогда как сывороточная концентрация пепсиногена II остается на прежнем уровне. Таким образом, сывороточная концентрация пепсиногена I достаточно хорошо отражает количество клеток, секретирующих пепсиноген в области тела желудка, и их состояние. Чем тяжелее атрофический гастрит области тела желудка, тем ниже сывороточная концентрация пепсиногена I. Низкая концентрация пепсиногена I в сыворотке с чувствительностью 90% и специфичностью почти 100% указывает на наличие тяжелого атрофического гастрита в области тела желудка [23].
Гастрин секретируется в желудочно-кишечном тракте по меньшей мере в трех различных формах, причем иммунореактивная активность всех этих форм измеряется при определении содержания гастрина в сыворотке (общий сывороточный гастрин). Подтипами гастрина являются так называемые минигастрин (G-14), маленький гастрин (G-17) и большой гастрин (G-34). Физиологически наиболее важными являются гастрин-17 и гастрин-34. Влияние гастрина-17 на секрецию соляной кислоты в 6 раз превышает влияние гастрина-34. Гастрин секретируется из так называемых G-клеток, которые имеются и в антральном отделе желудка, и в 12-перстной кишке. Самыми важными ускорителями секреции гастрина являются тонус блуждающего нерва и продукты белкового распада. Секреция гастрина замедляется снижением рН ниже 2,5. Гастрин, секретируемый из антрального отдела, более чем на 90% представляет собой гастрин типа 17, в то время как гастрин 12-перстной кишки представляет в первую очередь гастрин типа 34 [24]. В ситуации голодания в сыворотке обнаруживается преимущественно гастрин-34, тогда как после приема пищи сывороточный гастрин состоит из гастрина типа 17 [25] . Секрецию гастрина-17 можно также изучать с использованием так называемого теста белковой стимуляции. При таком тесте после голодания утром берут образец крови, после чего пациент съедает богатое белком стандартное блюдо и в течение двух часов через 15-минутные интервалы берут образцы крови. Максимальное нарастание очевидно приблизительно через 20 мин.
При атрофическом антральном гастрите слизистая оболочка антрального отдела атрофирована и, следовательно, секреция в ней гастрина-17 снижается, и его концентрация в сыворотке падает. Таким образом, сниженная концентрация гастрина-17 в сыворотке могла бы быть показателем атрофии слизистой антрального отдела и повышенного риска развития рака в этой области. В случае атрофии слизистой оболочки антрального отдела также имеется сниженная реакция при тесте белковой стимуляции, который представляется более чувствительным индикатором атрофии, чем просто определение концентрации. В публикации WO 96/15456 описан способ скрининга для выявления риска рака путем определения наличия атрофии в различных частях желудка.
Вследствие высокой распространенности хронического гастрита, особенно у популяции пожилого возраста, было бы, однако, важно разработать также способ для оценки наличия топографических фенотипов хронического гастрита для оценки связанного с ними риска пептической язвы. Особенно благоприятно было бы разработать способ, который бы позволил проводить указанную оценку неинвазивным образом, то есть без необходимости прибегать к взятию образцов биопсии слизистой во время диагностической гастроскопии. Имела бы также преимущества разработка способа, который бы позволил не только оценить риск развития пептической язвы, но и способ, который позволил бы дифференцировать риск развития язвы желудка и риск развития язвы 12-перстной кишки.
Указанные выше цели достигаются с помощью способа в соответствии с изобретением, который относится к способу оценки риска пептической язвы у индивидуума, причем способ включает в себя этапы
- количественного определения концентрации пепсиногена I и гастрина-17 в образце сыворотки указанного индивидуума,
- выбора специфической для способа эталонной величины и величины отсечки для соответствующих анализируемых веществ,
- сравнения определяемой таким образом концентрации пепсиногена I и гастрина-17 со специфической для способа эталонной величиной и величиной отсечки, посредством чего сывороточная концентрация пепсиногена I и гастрина-17 выше верхнего предела соответствующей эталонной величины или сывороточная концентрация пепсиногена I выше верхнего предела ее эталонной величины в комбинации с концентрацией гастрина-17 в пределах эталонного диапазона или ниже ее величины отсечки, указывает на возросший риск пептической язвы у указанного индивидуума.
Таким образом, настоящее изобретение включает в себя этап выявления индивидуума, имеющего либо сывороточную концентрацию пепсиногена I и гастрина-17 выше верхнего предела соответствующей эталонной величины, либо сывороточную концентрацию пепсиногена I выше верхнего предела ее эталонной величины в комбинации с концентрацией гастрина-17 в пределах эталонного диапазона или ниже ее величины отсечки, как индивидуума с повышенным риском развития пептической язвы или имеющего предрасположенность к ней.
В соответствии с предпочтительным вариантом реализации изобретения способ включает в себя также этап диагностики у указанного индивидуума инфекции Helicobacter pylori путем определения антител против Helicobacter pylori в образце сыворотки.
Таким образом, в способе в соответствии с изобретением используются в комбинации два или предпочтительно три определения по образцу сыворотки пациента, у которого предполагается скрининг для выявления риска пептической язвы, а именно определение сывороточного пепсиногена I (PGI), гастрина-17 (G-17) и, необязательно, антител против Helicobacter pylori.
Различные способы определения PGI, G-17 и антител против Helicobacter pylori как таковые хорошо известны специалисту в данной области, и в продаже также имеются наборы для проведения этих определений. Такие способы представляют собой обычно иммунологические способы с использованием моно- или поликлональных антител к анализируемому соединению. Способы выявления, пригодные для использования, включают в себя, например, измерение оптического поглощения, флуоресценции или люминесценции. Возможно также проведение всех трех измерений одновременно, например, на одном и том же микропланшете, в различных его ячейках, причем комбинированная аналитическая система обеспечивает особенно удобный способ диагностики.
Изобретение включает в себя этап сравнения измеряемых концентраций анализируемых веществ со специфическими для способа величиной отсечки и эталонной величиной для указанных анализируемых веществ. Отбор таких величин хорошо известен специалисту в данной области и зависит от специфичности и чувствительности, выбранных для способа испытания, используемого для определения концентраций анализируемых веществ (см., например, William J Marshall, Clinical Chemistry, Third Edition, 1995, Mosby).
Для определения антител против Helicobacter pylori имеется ряд коммерческих "наборов" (например, Orion Pyloriset EIA-G, Pyloriset EIA-A, EIA 2G, выпускаемые Roche, Pyloristat, выпускаемый Whittaker Bioproducts). Антигены могут быть получены из бактерий Helicobacter pylori различными путями [26], и они также имеются в продаже.
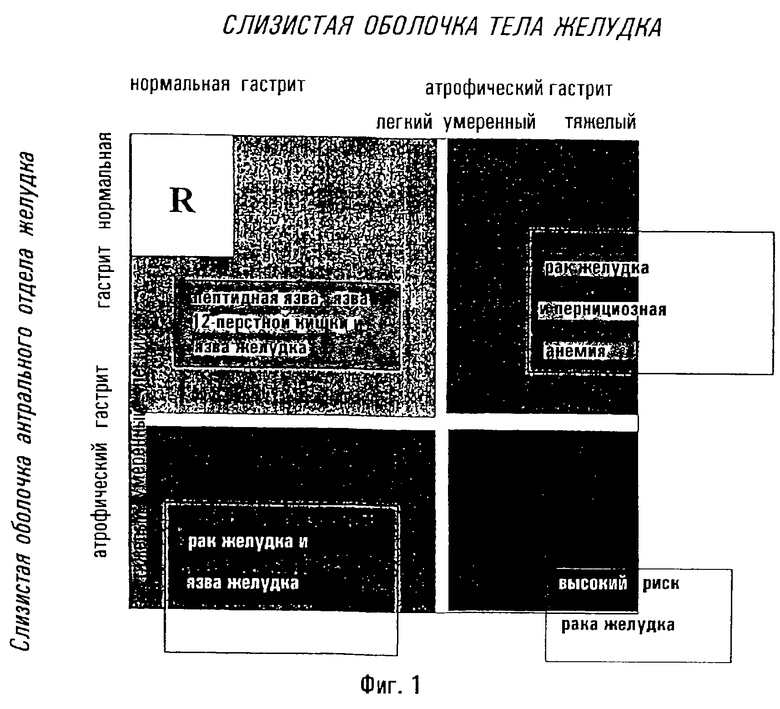
Фиг. 1 иллюстрирует фенотипы хронического гастрита и связанный с ними риск развития заболевания желудка.
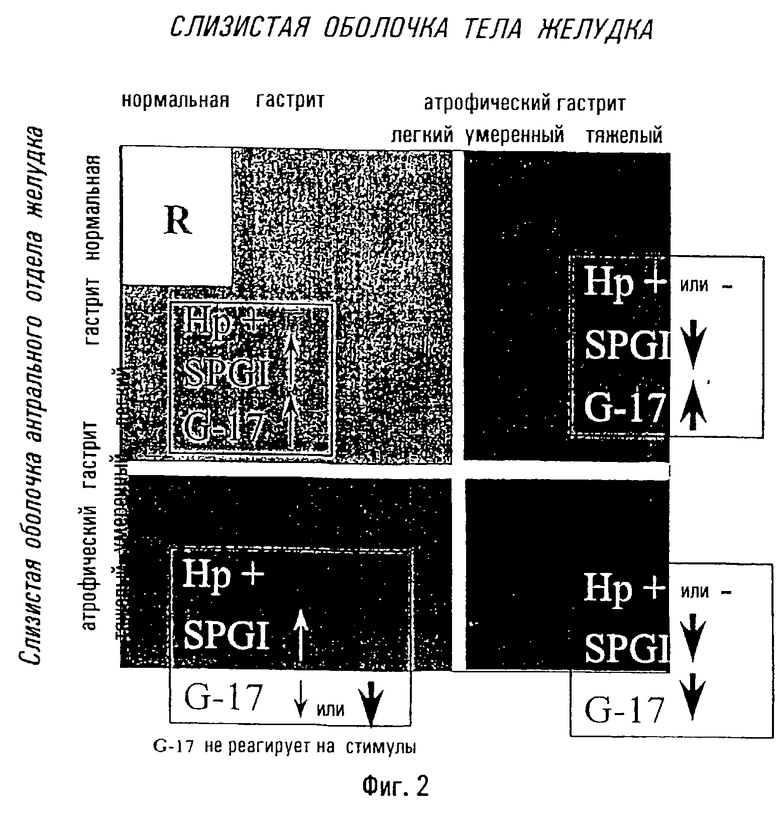
Фиг. 2 иллюстрирует связь между серологическими тестами для выявления SPGI, G-17 и инфекции Helicobacter pylori и топографическими фенотипами хронического гастрита.
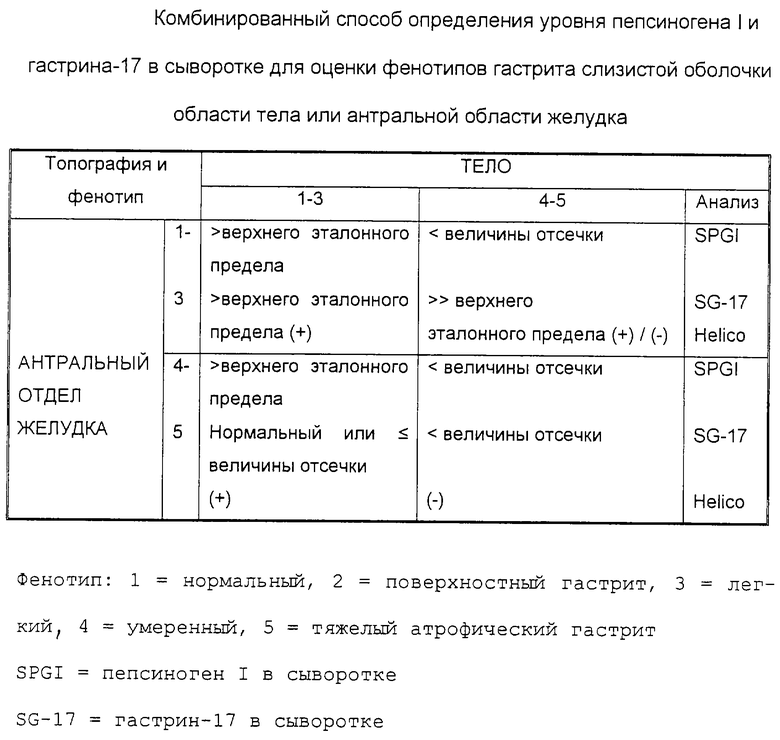
Используемый в изобретении термин "топография" или "топографический" относится к локализации гастрита в желудке. И в слизистой оболочке тела желудка, и антрального отдела проводят дифференциальную диагностику между фенотипами: нормальный, гастрит (поверхностный гастрит) и атрофический гастрит, причем атрофический гастрит, в свою очередь, классифицируется, в порядке возрастания тяжести, на легкий, умеренный и тяжелый атрофический гастрит.
Как очевидно из фиг.1, имеется возросший риск (по сравнению с индивидуумами со здоровым желудком) гастрита и, особенно, язвы 12-перстной кишки, когда гастрит и в слизистой оболочке тела желудка, и антрального отдела представляет собой поверхностный или легкий атрофический фенотип, причем риск особенно возрастает с возрастанием тяжести антрального гастрита. В этом случае и концентрация пепсиногена I, и концентрация гастрина-17 в сыворотке превышает соответствующие эталонные величины, причем, в зависимости от согласованной для рассматриваемого способа чувствительности и специфичности, верхний эталонный предел составляет от 25 до 120 мкг/л. Гастрин-17 будет также выше его нормальных или эталонных величин, которые находятся в диапазоне от 2 до 25 пмоль/л. Для положительного результата по Helicobacter pylori величина титра отсечки составляет от 200 до 500.
В ситуации, когда слизистая тела желудка нормальная или гастрит в теле желудка имеет поверхностный фенотип, а гастрит в антральном отделе имеет атрофический фенотип от умеренного до тяжелого, имеется повышенный риск, особенно язвы желудка (а также рака желудка). В этой ситуации концентрация пепсиногена I еще выше верхнего предела его эталонной величины, как указано выше, но величина гастрина-17 находится в нормальном диапазоне, на ее нижней эталонной величине или ниже ее величины отсечки для тяжелой атрофии, которая, в зависимости от специфичности и чувствительности способа, составляет 0,1-2 пмоль/л. Этот способ можно комбинировать с тестом белковой стимуляции путем измерения концентрации гастрина-17 в сыворотке в исходной ситуации, а затем, после белковой стимуляции, например, после съедания стандартного блюда, богатого белком. Отсутствие реакции при этом тесте подтверждает риск язвы желудка.
Из фигур также видно, что при возрастающей тяжести атрофического гастрита тела желудка при отсутствии или лишь поверхностном антральном гастрите концентрация пепсиногена I в сыворотке падает ниже величины отсечки, указывая на возросший риск рака и пернициозной анемии, причем эта величина отсечки, в зависимости от специфичности и чувствительности способа, составляет от 20 до 30 мкг/л. Как указано выше, концентрация гастрина-17 еще превышает ее эталонную величину.
При возрастающей тяжести атрофического гастрита и антрального отдела, и тела желудка концентрация пепсиногена I ниже ее величины отсечки, что указывает на возросший риск возникновения рака, а концентрация гастрина-17 в сыворотке находится на ее нижнем эталонном пределе или ниже величины отсечки, указывая на возросший риск рака. Эти фенотипы гастрита связаны с очень высоким риском рака желудка.
Описанное выше применение комбинированного способа для оценки фенотипов гастрита слизистой оболочки в различных частях желудка показано в таблице.
ССЫЛКИ
1. MARSHALL BJ, WARREN JR: Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration. Lancet 1984, i:1311-1314.
2. GOODWIN CS: The Sydney System: microbial gastritis. J. Gastroenterol Heparol 1991, 6:235-237.
3. DIXON MF: Helicobacter pylori and peptic ulceration; histopathological aspects. J. Gastroenterol Hepatol 1991, 6:125-130.
4. RAUWS EAJ, LANGENBERG W, HOUTHOFF HJ, ZANEN HC, TYTGAT GNJ: Campylobacter pyloridis-associated chronic active antral gastritis, Gastroenterology 1988, 94:33-40.
5. SIURALA M, SIPPONEN P, KEKKI M: Campylobacter pylori in a sample of Finnish population: relation to morphology and functions of the gastric mucosa. Gut 1988, 29:909-916.
6. PRICE AB, LEVI J, DOLBY JM, DUNSCOMBE PL, SMITH A, CLARK J, ET AL: Campylobacter pyloridis in peptic ulcer disease; microbiology, pathology and scanning electron microscopy. Gut 1985, 26:1183-1188.
7. MISIEWICZ JJ: The Sydney System: a new classification of gastritis. Introduction. J. Gastroenterol Hepatol 1991, 6:207-208.
8. PRICE Ab: The Sydney System: histological division. J Gastroenterol Hepatol 1991, 6:209-222.
9. WHITEHEAD R, TRUELOVE SC, GEAR MWL: The histological diagnosis of chronic gastritis in fiberoptic gastroscope biopsy specimens. J Clin Pathol 1972, 25:1-11.
10. CORREA P: Chronic gastritis: a clinico-pathological classification Am J Gastroenterol 1988, 83:504-509.
11. YARDLEY JH. Pathology of chronic gastritis and duodenitis. In Gastroeiniestinal Pathology edited by Goldman H, Appelman HD, Kauffman N Baltimore: Williams and Wilkins, 1990, pp. 69-143.
12. SIURALA M, SIPPONEN P, KEKKI M: Chronic gastritis: dynamic and clinical aspects. Scand J Gastroenterol 1985, 20 (suppl 109):69-76.
13. SIURALA M, VARIS K, KEKKI M: New aspects on epidemiology, genetics and dynamics of chronic gastritis. Front Gastrointest Res 1980, 6:148-165.
14. CHELI R, SANTI I, CIANCAMERA G, CANCIANI G: A clinical and statistical follow-up of atrophic gastritis. Am J Dig Dis 1973, 18:1061-1066.
15. CHELI R, PERASSO A, GIACOSA A: Gastritis, Berlin: Springer Verlag, 1987.
16. SIPPONEN P, KEKKI M, SIURALA M: Age-related trends of gastritis and intestinal metaplasia in gastric carcinoma patients and in controls representing the population at large. Br J Cancer 1984, 49:521-530.
17. VILLAKO К, SIURALA M: The behaviour of gastritis and related conditions in different population samples. Ann Clin Res 1981, 13:114-118.
18. CHELI R, SIMON L, ASTE H, FIGUS IA, NIGOLD G, BAJTAI A, ET AL: Atrophic gastritis and intestinal metaplasia in asymptomatic Hungarian and Italian population. Endoscopy 1980, 12:105-108.
19. SIPPONEN P: Chronic gastritis and ulcer risk. Scand J Gastroenterol 1990, 25:193-196.
20. SIPPONEN P, AARYNEN M, KAARIAINEN I, KETTUNEN P, HELSKE T, SEPPALA K: Chronic antral gastritis, Lewis a+ phenotype and male sex in predicting coexisting duodenal ulcer. Scand J Gastroenterol 1989, 24:581-588.
21. SIPPONEN P, SEPPALA K, AARYNEN M, HELSKE T, KETTUNEN P: Chronic gastritis and gastroduodenal ulcer: a case control study on risk of coexisting duodenal and gastric ulcer in patients with gastritis. Gut 1989, 30:922-929.
22. SIPPONEN P, VARIS K, FRAKI O, KORRI U-M, SEPPALA K, SIURALA M: Cumulative 10-year risk of symptomatic duodenal and gastric ulcer in patients with or without gastritis. A clinical follow-up of 454 patients. Scand J Gastroenterol 1990, 25:966-973.
23. VARIS K, KEKKI M, HÄRKÖNEN M, SIPPONEN P & SAMLOFF IM 1991: Serum pepsinogen I and serum gastrin in the screening of atrophic pangastritis with high risk of gastric cancer. Scand J Gastroenterology 26 (suppl 186): 117-123.
24. BERSON SA & YALOW RS, (1971): Nature of immunoreactive gastrin extracted from tissues of gastrointestinal tract. Gastroenterology 60:215-222.
25. LAMERS С, HARRISON A, IPPOLITI A & WALSH J (1979): Molecular forms of circulating gastrin in normal subjects and duodenal ulcer patients. Gastroenterology 76: 1179.
26. LELWALA-GURUGE J, NILSSON I, JUNGH À & WADSTRÖM T (1992): Cell surface proteins of Helicobacter pylori as antigens in an ELISA and a comparison with three commercial ELISA. Scand J Infect Dis 24:457-465.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И ПРОДУКТЫ ДЛЯ ДИАГНОСТИКИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ И РАКА ЖЕЛУДКА, СВЯЗАННОГО С АТРОФИЧЕСКИМ ГАСТРИТОМ | 2008 |
|
RU2519646C2 |
| СПОСОБ ДЛЯ ДИАГНОСТИКИ АТРОФИЧЕСКИХ ГАСТРИТОВ | 2002 |
|
RU2262706C2 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ АКТИВНОСТИ АНТРАЛЬНОГО ХЕЛИКОБАКТЕР-АССОЦИИРОВАННОГО ГАСТРИТА У БОЛЬНЫХ БРОНХИАЛЬНОЙ АСТМОЙ | 2009 |
|
RU2394499C1 |
| СПОСОБ ДИАГНОСТИКИ АТРОФИЧЕСКОГО ГАСТРИТА | 2011 |
|
RU2474824C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ HELICOBACTER PYLORI-АССОЦИИРОВАННОГО ХРОНИЧЕСКОГО ГАСТРИТА, ОСНОВАННЫЙ НА ОПРЕДЕЛЕНИИ ИММУНОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ У ЕВРОПЕОИДОВ ХАКАСИИ | 2015 |
|
RU2614851C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ИНДИВИДУУМА, У КОТОРОГО СУЩЕСТВУЕТ РИСК НЕОБРАТИМЫХ НЕВРОЛОГИЧЕСКИХ ПОВРЕЖДЕНИЙ, ВКЛЮЧАЮЩИЙ В СЕБЯ ЭТАПЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ПЕПСИНОГЕНА I (PGI) И ВИТАМИНА В12 | 2000 |
|
RU2224258C2 |
| СПОСОБ ИММУНОДИАГНОСТИКИ РАКА ЖЕЛУДКА | 2014 |
|
RU2580309C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ДЕСТРУКТИВНЫХ ИЗМЕНЕНИЙ СЛИЗИСТОЙ ОБОЛОЧКИ ГАСТРОДУОДЕНАЛЬНОЙ ЗОНЫ | 2008 |
|
RU2391915C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ЭКЗЕМЫ У БОЛЬНЫХ С СОПУТСТВУЮЩИМ ХРОНИЧЕСКИМ ГАСТРОДУОДЕНИТОМ | 2011 |
|
RU2461836C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО АТРОФИЧЕСКОГО ГАСТРИТА | 2002 |
|
RU2219940C1 |
Изобретение относится к области медицины, в частности к способу дифференциации между наличием риска образования язвы желудка и язвы двенадцатиперстной кишки. Сущность изобретения состоит в количественном определении концентраций пепсиногена I и гастрина-17 в образце сыворотки, сравнении концентраций пепсиногена I и гастрина-17 со специфической для способа эталонной величиной и величиной отсечки, при этом концентрация пепсиногена I и гастрина-17 в сыворотке выше верхнего предела соответствующей эталонной величины указывает на повышенный риск образования язвы двенадцатиперстной кишки, а сывороточная концентрация пепсиногена I выше верхнего предела ее эталонной величины в комбинации с концентрацией гастрина-17 в пределах эталонного диапазона или ниже ее величины отсечки указывает на повышенный риск образования язвы желудка у указанного индивидуума. Техническим результатом является разработка неинвазивного способа, позволяющего определить локализацию пептической язвы при наличии риска ее образования. 8 з.п. ф-лы, 2 ил., 1 табл.
| ЕЛИЗАВЕТИНА Г.А | |||
| и др | |||
| Комплексная оценка диагностических показателей агрессивных и защитных факторов у больных пилородуоденитом | |||
| Эффективность внедрения новых методов профилактики, диагностики и лечения в клинической медицине | |||
| Сб | |||
| науч | |||
| тр | |||
| - М., 1990, с.50-54 | |||
| ВАЛЕНКЕВИЧ Л.Н | |||
| Содержание гастрина и пепсиногена у больных хроническим атрофическим гастритом и язвой двенадцатиперстной кишки | |||
| Врачебное дело, 1993, № 2 и 3, с.56-58 | |||
| Клиническая оценка лабораторных тестов | |||
| - М.: Медицина, 1986, с.119 и 120 | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
Авторы
Даты
2004-03-10—Публикация
2000-04-28—Подача