Область техники
Настоящее изобретение относится к способу оценки состояния или условий слизистой оболочки желудка, в частности к способу диагностики изменений, связанных с высоким риском возникновения на слизистой оболочке желудка, в частности, атрофического гастрита, у пациента. В этом способе у пациента определяется концентрация конкретных анализируемых соединений, а именно концентрация пепсиногена I, концентрация гастрина (предпочтительно, гастрина-17), а также концентрация или присутствие маркера Helicobacter pylori, и необязательно, также концентрация пепсиногена II, и средства обработки данных используются для обработки полученных данных и для получения информации, например, в форме диагноза или предложений для дальнейшего лечения или исследований.
Предпосылки изобретения
Хотя частота появления новых случаев рака желудка и уменьшилась в последние годы, рак желудка все еще представляет собой одно из наиболее распространенных злокачественных заболеваний. В Финляндии регистрируются приблизительно от 250 до 300 новых случаев рака на один миллион человек в год. В возрастной группе людей старше 50 лет, согласно оценкам, встречается 2350 случаев рака желудка, что составляет около 3 средних значений для этой возрастной группы населения (Finnish Cancer Registry - The Institute for Statistical and Epidemiological Cancer Research 1993). Кроме Финляндии, высокая заболеваемость раком желудка существует в Исландии, Южной Америке и, в особенности, в Японии и Китае.
Прогноз рака желудка обычно является ненадежным, и специфичного лечения не существует. В настоящее время единственная возможность успешного лечения рака желудка представляет собой его ранее обнаружение и полное хирургическое удаление.
Рак желудка необязательно дает какие-либо симптомы на его ранних стадиях. Позднее появление симптомов естественным образом задерживает этап лечения пациента. С другой стороны, клинические данные на ранней стадии рака желудка часто являются неспецифичными. Основным методом диагностики для рака желудка в настоящее время является гастроскопия и биопсия, клеточное и аспирационное цитологическое исследование, ассоциируемое с ними. Поскольку рутинная гастроскопия осуществляется в порядке проверки симптомов, таких как боль, в верхней части живота, или кровотечение желудочно-кишечного тракта, симптоматически рак желудка, обнаруженный таким способом, часто находится на поздней стадии и поэтому является неоперабельным. Делаются также попытки усовершенствования первичной диагностики с помощью различных иммунологических методов, но достаточно специфичных иммунологических методов не было разработано.
Основной целью является нахождение средств, с помощью которых было бы возможным идентифицировать среди населения в целом просто и с умеренными затратами тех лиц, которые могут страдать раком желудка на его начальных стадиях. После идентификации эти лица должны непосредственно исследоваться с помощью гастроскопии. В то же время могут идентифицироваться те лица, которые демонстрируют предраковые изменения желудка, которые должны отслеживаться.
Раку желудка может предшествовать ряд различных заболеваний или состояний желудка (так называемые предраковые состояния), которые представляют собой хронический атрофический гастрит, пернициозную анемию, язву желудка, полипоз желудка и болезнь Менетрье (гигантский гипертрофический гастрит). Четко идентифицируемые изменения слизистой оболочки представляют собой дисплазию и аденому. Указанные состояния ассоциируются примерно с 4-5-кратным увеличением риска возникновения рака по сравнению с населением в целом. Установлено, что почти во всех случаях заболеваний риск опосредуется через хронический атрофический гастрит.
Хронический гастрит означает длительное воспалительное состояние слизистой оболочки желудка. Заболевание грубо может подразделяться на так называемую поверхностную и атрофическую форму. При поверхностном гастрите инфильтрация воспалительных клеток концентрируется под поверхностью эпителия. Случай, когда воспаление прогрессирует и диффундирует между конкретными секреторными железами желудка, определяется как хронический атрофический гастрит. В этом случае нормальные структуры желез слизистой оболочки желудка, по меньшей мере, частично замещаются метапластическими изменениями. Относительный риск возникновения рака желудка у пациентов, страдающих от атрофического гастрита в области главной части желудка, согласно оценкам, которые получаются из статистики рака в Финляндии, примерно в 4-5-раз больше по сравнению с лицами, имеющими здоровую слизистую оболочку. В дополнение к этому, существует риск заболевания пернициозной анемией из-за дефицита внутренних факторов и нарушений усвоения витамина B12. При острой атрофии антрального отдела желудка, риск возрастает даже в 18 раз. Если атрофические изменения появляются как в антральном отделе, так и в области главной части (пангастрит), риск может возрасти даже до 90 раз (Sipponen, P, Kekki, M, Haapakoski, J. Ihamuki, T & Siurala, M (1985) Gastric cancer risk in chronic atrophic gastritis: statistical calculations of crosssectional data. Int. J. Cancer 35:173-77).
Helicobacter pylori представляет собой грам-отрицательную бактерию спиральной формы, которая развивается в слизистой оболочке в непосредственной близости от поверхностных эпителиальных клеток слизистой оболочки желудка и в промежутках между клетками. Видимо, бактерия передается от одного лица к другому пероральным путем. Воздействие бактерии на слизистую оболочку желудка представляет собой воспалительную реакцию, которая опосредуется, дополнительно, путем высвобождения веществ - сильных медиаторов воспаления. После острой стадии воспаление трансформируется в хронический гастрит. У пациентов, страдающих хроническим гастритом, в 70-90% случаев устанавливается инфекция Helicobacter pylori (Calam, J (1994) Helicobacter pylori (Review) Eur. J. Clin. Invest 24: 501-510). Поскольку инфекция Helicobacter pylori и хронический гастрит в желудке тесно взаимосвязаны, предполагается, что это бактериальная инфекция может быть одним из этиологических факторов при развитии рака желудка. По этой причине является возможным, что уничтожение бактерии Helicobacter pylori на ранних стадиях инфекции может предотвратить развитие атрофии, связанной с хроническим гастритом, и таким образом, уменьшить риск возникновения рака и риск возникновения язв желудка и двенадцатиперстной кишки.
Публикация WO 96/15456, которая включена в настоящее описание посредством ссылки, описывает способ скрининга риска возникновения рака путем определения концентрации анализируемых соединений пепсиногена I и гастрина-17 из образца сыворотки пациента. В соответствии с указанной публикацией значения концентрации, определенные таким образом, затем сравниваются с пороговым значением и с эталонным значением для каждого анализируемого соединения. Значение концентрации пепсиногена I в сыворотке ниже порогового значения для уровня пепсиногена I в сочетании со значением концентрации гастрина-17 выше верхнего эталонного предела указывает на острую атрофию в области главной части желудка. Уровень гастрина-17 в сыворотке ниже порогового значения для гастрина-17 в сочетании со значением уровня пепсиногена I выше порогового значения для уровня пепсиногена I, с другой стороны, указывает на атрофию антрального отдела желудка. В случае когда уровень пепсиногена I в сыворотке находится ниже порогового значения для уровня пепсиногена I и уровень гастрина-17 находится на нижнем пределе его эталонного значения, это представляет собой указание на острую атрофию желудка в целом, то есть на атрофический пангастрит.В соответствии с возможным описанным вариантом осуществления указанные исследования могут быть объединены с исследованием антител к Helicobacter pylori.
В соответствии с указанной публикацией WO, способ может быть дополнен с помощью так называемого исследования с белковой стимуляцией, согласно которому образец крови отбирается натощак утром, после чего пациент ест обогащенную белками стандартную пищу, и образцы крови отбираются через 15 минутные интервалы в течение двух часов. Максимальное увеличение становится заметным примерно через 20 минут. В случае когда атрофия локализуется в антральном отделе, в этом исследовании будет осуществляться сильно пониженная реакция. Когда атрофия локализована в главной части желудка, реакция будет нормальной или повышенной, в то время как атрофия слизистой оболочки в целом приводит к пониженной реакции.
Публикация WO 00/67035, которая включена в настоящее описание посредством ссылки, описывает способ для оценки риска возникновения язвы желудка и двенадцатиперстной кишки путем количественного определения концентрации пепсиногена I в сыворотке и гастрина-17 в сыворотке. В соответствии с этим способом, если оба измеренных значения в сыворотке для уровней пепсиногена I и гастрина-17 являются высокими, выше верхнего предела их соответствующих эталонных значений, или значение уровня пепсиногена I в сыворотке превышает верхний предел его эталонного значения, в сочетании со значением гастрина-17 в пределах эталонного диапазона или ниже его порогового значения, это представляет собой указание на повышенный риск возникновения язвы желудка и двенадцатиперстной кишки. В данной области известны способы для измерения концентраций различных анализируемых соединений и существуют также коммерчески доступные наборы для этой цели. Некоторые примеры способов для осуществления указанных определений описаны также в публикации WO 96/15456.
Сущность изобретения
Задачей настоящего изобретения является создание способа для оценки состояния слизистой оболочки желудка, в частности, для диагностики изменений слизистой оболочки желудка, таких как атрофический гастрит, у пациента, путем анализа уровня анализируемых соединений пепсиногена I (PGI), гастрина и маркера для инфекции Helicobacter pylori, причем способ включает в себя
- измерение в образце от указанного пациента концентрации пепсиногена I и гастрина, и, в дополнение к этому, определение концентрации или присутствия маркера для Helicobacter pylori (Hp-маркер);
- введение данных, полученных таким образом, для указанных анализируемых соединений, в средства обработки данных, включающие в себя операционную систему, средство для приема и передачи и обработки данных, причем упомянутые средства для обработки данных выполнены с возможностью осуществления этапов;
- сравнения измеренного значения концентраций для анализируемого соединения с заранее определенным пороговым значением для указанного анализируемого соединения для получения комбинации результатов сравнения, которая является специфичной для исследуемого пациента, и генерирование информации в ответ на указанное сочетание результатов сравнения и дополнительно на другие введенные данные.
Средство для обработки данных может включать в себя дисплей, на котором отображается генерируемая информация. Генерируемая информация относится преимущественно к диагнозу или предложению относительно лечения или дополнительных исследований и/или тестов на основе полученных результатов сравнения.
Настоящее изобретение также направлено на набор и на программный продукт для компьютера, в особенности, для использования в способе согласно настоящему изобретению.
Настоящее изобретение также направлено на набор, содержащий средство для измерения в образце концентрации пепсиногена I и/или гастрина и/или средство для определения концентрации или присутствия маркера Helicobacter pylori, а также на программный продукт для компьютера, воплощенный в носителе информации, считываемом компьютером и содержащий средство компьютерного кода, предназначенное для осуществления этапов сравнения измеренного значения концентрации анализируемого соединения с заранее определенным пороговым значением для анализируемого соединения, объединения результатов сравнения в комбинацию результатов сравнения и получения информации в ответ на упомянутую комбинацию и дополнительно на другие введенные данные при выполнении упомянутого кода на компьютере.
Также задачей настоящего изобретения является создание программного продукта для компьютера, воплощенного в носителе информации, считываемом компьютером, и содержащего средство компьютерного кода, предназначенное для осуществления этапов сравнения измеренных концентраций анализируемого соединения с соответствующим пороговым значением для упомянутого анализируемого соединения, объединения результатов сравнения в комбинацию результатов сравнения и получения информации в ответ на упомянутую комбинацию и дополнительно на другие введенные данные при выполнении упомянутого кода на компьютере.
Подробное описание изобретения
Способ сравнения измеренного значения с пороговым значением для анализируемого соединения предназначен для установления того, является ли измеренное значение для уровня анализируемого соединения большим, равным или меньшим, чем соответствующее пороговое значение, и таким образом, для генерации конкретных комбинаций результатов сравнения для анализируемых соединений, причем на основе этой комбинации будет генерироваться конкретная информация и, например, отображаться на дисплее.
Таким образом, в соответствии с настоящим изобретением, для каждого пациента, который исследуется, средство для обработки данных генерирует конкретное множество результатов сравнения, это множество получается путем сравнения измеренного значения с заранее определенным пороговым значением для анализируемых соединений в любом заданном порядке или одновременно. В контексте настоящего изобретения под пациентом понимается млекопитающее, например человек или животное, в частности домашнее животное, например собака.
Настоящее изобретение, таким образом, включает в себя на первой стадии, способ для определения по меньшей мере маркера Helicobacter pylori, уровня пепсиногена I (PGI) и гастрина. Маркер или индикатор инфекции Helicobacter pylori может, таким образом, в соответствии с настоящим изобретением, представлять собой, например, антитело к Helicobacter pylori, значение уровня которого может измеряться в образце телесной жидкости. Такой образец предпочтительно представляет собой образец сыворотки, но может представлять собой также образец слюны, мочи или слезной жидкости, при этом для измерения, например, значений антител, могут использоваться коммерчески доступные наборы. Пороговое значение для уровня антител к Helicobacter pylori легко может быть определено специалистом в данной области. В одном из воплощений настоящего изобретения, авторы используют значение 30 Э.М.Е. в качестве порога для указания на присутствие или отсутствие инфекции Helicobacter pylori. Специфичные антитела к Helicobacter pylori также могут быть измерены с использованием вестерн-блоттинга.
Другая альтернатива представляет собой оценку присутствия инфекции Helicobacter pylori путем определения присутствия самого антигена. Такое измерение может осуществляться, например, на образце стула пациента, и для этой цели коммерчески доступными являются такие анализы, как иммуноферментные анализы, (смотри, например, Lancet 1999; 354, 30-33). Также возможно определение присутствия антигена по дыханию пациента с использованием хорошо известных методик измерения содержания двуокиси углерода, образование которого из меченой мочевины катализируется бактериями Helicobacter pylori, и системы для такого анализа также являются коммерчески доступными (например, Heliprobe™ от компании Noster AB, Швеция). Другая альтернатива представляет собой определение присутствия антигена в образце биопсии, взятом во время эндоскопии из желудка пациента. При этой альтернативе исследования являются либо положительными, либо отрицательными по отношению к антигену и присутствие антигена воспринимается как являющееся указанием на инфекцию Helicobacter pylori. Результат исследования соответствующим образом вводится в систему обработки данных в виде параметра булевой логики.
Пепсиноген и гастрин предпочтительно определяются из образца телесной жидкости, в частности из образца сыворотки или из образца мочи, слюны или слезной жидкости.
Настоящий способ включает в себя измерение уровня анализируемого соединения пепсиногена I, но в соответствии с одним из воплощений настоящего изобретения, также возможно измерение, в дополнение к этому, концентрации анализируемого соединения пепсиногена II (PGII) и использование отношения PGI к PGII, вместо уровня PGI или в дополнение к нему, в качестве значения, которое должно сравниваться с заранее определенным пороговым значением. Пепсиноген I, а также отношение уровня пепсиногена I к II, имеют тенденцию к линейному уменьшению при ухудшении атрофии слизистой оболочки главной части желудка.
В способе по настоящему изобретению, как правило, сначала используется нижнее пороговое значение для уровня пепсиногена I, которое представляет собой «нормальное» пороговое значение для дифференцирования нормальной и атрофической слизистой оболочки главной части желудка. В дополнение к этому может быть использовано второе, более высокое, пороговое значение для уровня пепсиногена I, такое более высокое значение, когда концентрация гастрина находится в ее пороговых пределах, указывает на только слегка стимулированную активность гастрина, определяя порог между неатрофическим (включая тело желудка) гастритом (пепсиноген I выше второго порога), и только слегка атрофической слизистой оболочкой главной части желудка (уровень пепсиногена I ниже второго порога) в сочетании с атрофией антрального отдела. Указанное второе пороговое значение легко может быть определено специалистом в данной области.
Концентрация гастрина, и в частности гастрина-17, подобным же образом уменьшается при ухудшении атрофии слизистой оболочки антрального отдела. Для гастрина может быть использован пороговый диапазон. Этот диапазон имеет нижний пороговый предел, значения ниже которого указывают на атрофию, по меньшей мере, антрального отдела, а также верхний пороговый предел, значения выше которого могут указывать на нормальный неатрофический гастрит или на атрофическую слизистую оболочку главной части желудка. Значения в пределах между нижним и верхним значением могут указывать на атрофию, по меньшей мере, области антрального отдела или в сочетании с высоким значением уровня пепсиногена (выше второго, более высокого порогового значения) также и на неатрофический гастрит, как обсуждалось выше. В дополнение к этому, третье пороговое значение, самое нижнее пороговое значение для уровня гастрина, может применяться для указания на нормальную слизистую оболочку, когда уровень пепсиногена I является равным или превышает его первое пороговое значение.
Анализируемое соединение гастрина может представлять собой гастрин в целом, то есть, по существу, сумму гастрина-34 и гастрина-17, но в соответствии с предпочтительным воплощением настоящего изобретения, измеряется уровень гастрина-17.
Как описано выше, способы для измерения уровня пепсиногена I, уровня пепсиногена II и гастрина хорошо известны в данной области. Эти измерения, как правило, представляют собой иммунологические методы с использованием моно- или поликлональных антител к указанным анализируемым соединениям. Пригодные для использования способы для детектирования включают в себя, например, измерение коэффициента поглощения, флуоресценции или люминесценции. Также возможно осуществление одновременных измерений всех трех анализируемых соединений, например, на одном и том же микропланшете, в различных лунках или в одной и той же лунке, что обеспечивает особенно удобный способ.
Значения для анализируемых соединений, полученные таким образом, затем вводятся в средства для обработки данных, такие как терминал для обработки данных, который имеет необходимую операционную систему, который может быть снабжен средствами для ввода данных и вывода данных и который содержит средства для сравнения измеренной концентрации анализируемых соединений с заранее определенным пороговым значением для этого анализируемого соединения. Данные могут быть введены с использованием любого оборудования терминала для обработки данных, снабженного соответствующим интерфейсом пользователя, или путем считывания данных с устройства-носителя для переноса и хранения данных, или путем приема данных из системы обеспечения данных с помощью средства передачи данных и сетей передачи данных, таких как Интернет.
Таким образом, интерфейс пользователя представляет собой средство, посредством которого пользователь может связываться с системой, снабжающей информацией, и посредством которого осуществляется ввод и проверка данных, и генерируемая информация сообщается или отображается или передается далее, для хранения или для распечатки на принтере.
Концепция пороговых значений при анализах, включающих в себя определение концентраций анализируемых соединений, хорошо известна специалистам в данной области и, как правило, обозначает некоторое значение или множество значений, выбранных в качестве предела между эталонными значениями (нормальные значения) и аномальными значениями для рассматриваемого исследования. Такие пороговые значения являются специфичными для каждого способа и зависят от специфичности и чувствительности, выбранной для способа исследования, используемого для определения концентраций анализируемых соединений (см., например, William J Marshall, Clinical Chemistry, Third Edition, 1995, Mosby).
Пороговые значения могут вводиться в систему обработки данных перед вводом измеренных значений для анализируемых соединений, или они могут предварительно сохраняться в системе обработки данных. В соответствии с настоящим изобретением, также предусматривается применение пороговых значений при осуществлении способа, когда желательно изменить чувствительность или специфику способа.В соответствии с настоящим изобретением, средство для обработки данных осуществляет операцию сравнения, в соответствии с которой различные измеренные концентрации анализируемых соединений сравниваются с соответствующим пороговым значением или пороговым диапазоном для указанного анализируемого соединения, полученные результаты сравнения объединяются, и в ответ на комбинацию результатов сравнения и, дополнительно, на другие или дополнительные данные или параметры, введенные в средства для обработки данных, генерируется информация, причем эта информация может быть отображена, например, на дисплее на интерфейсе пользователя.
Информация, создаваемая средством для обработки данных, может принимать форму диагноза, отображаемого в окне на дисплее, или она может принимать форму предложений для лечения или предложений для дополнительных исследований или тестов, отображаемых в том же или в ином окне дисплея.
Таким образом, в соответствии с настоящим изобретением, в зависимости от конкретной комбинации полученных результатов сравнения главный диагноз может определяться как «нормальная (слизистая оболочка)», «атрофический гастрит главной части желудка» (дополнительно, аутоиммунного типа), «атрофический гастрит антрального отдела и главной части желудка» (пангастрит), «атрофический гастрит антрального отдела желудка», или «неатрофический гастрит», и дополняться информацией, относящейся к присутствию или отсутствию инфекции Helicobacter pylori.
Приведенная ниже таблица включает в себя конкретные комбинации результатов сравнения, ассоциируемые с различными диагнозами, когда анализируемые соединения представляют собой Hp-маркер, такой как Hp-антитело, пепсиноген I и гастрин.
В таблице,
Hp-co означает пороговое значение для маркера Hp
P-coI означает первый порог для уровня пепсиногена I
P-coII означает второе пороговое значение для уровня пепсиногена I
G-coI означает значение нижнего порога для гастрина
G-coII означает значение верхнего порога для гастрина.
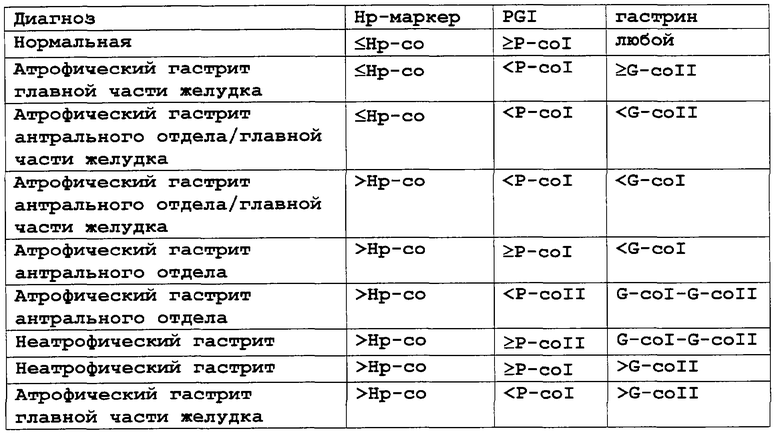
Из таблицы видно, что уровень маркера Helicobacter pylori разделяет множество конкретных комбинаций на две группы, где измеренные анализируемые соединения Hp маркера находятся либо выше, либо ниже порогового значения для уровня маркера Hp (Hp-co). Когда значение уровня Hp-маркера равно или меньше, чем порог, значение уровня PGI, равное или более высокое, чем значение первого порога PG (P-coI), указывает на нормальную слизистую оболочку, в то время как, если значение уровня PGI находится ниже указанного порога, значение уровня гастрина, равное или более высокое, чем верхний предел порога для гастрина (G-coII), указывает на атрофический гастрит главной части желудка, а если это значение находится ниже указанного порога, это указывает на атрофический гастрит антрального отдела/главной части желудка, то есть пангастрит. Вместо условия «любое значение» для гастрина при диагнозе «нормальная слизистая оболочка» можно также применить третье, самое низкое пороговое значение для уровня гастрина (G-coIII), выше которого концентрация гастрина должна указывать на нормальную слизистую оболочку.
С другой стороны, когда значение уровня Hp находится выше его порогового значения и значение уровня гастрина находится ниже его нижнего порогового предела (G-coI), это указывает на пангастрит, если также и уровень пепсиногена I находится ниже его первого порогового значения, и указывает на атрофический гастрит антрального отдела, если уровень пепсиногена I равен первому пороговому значению или превышает его. Если значение уровня гастрина находится в пороговом диапазоне (G-coI - G-coII) и уровень пепсиногена I находится ниже его второго порогового значения (P-coII), это также указывает на атрофический гастрит антрального отдела, но когда уровень пепсиногена I равен его второму пороговому значению или превышает, это указывает на неатрофический гастрит. Наконец, когда уровень гастрина находится выше верхнего порогового предела (G-coII) и уровень пепсиногена I равен первому пороговому значению или превышает его, это указывает на неатрофический гастрит, но когда уровень пепсиногена находится ниже первого порога, это указывает на атрофический гастрит главной части желудка. В приведенной выше таблице, когда определяется скорее присутствие маркера Hp, такого как антиген, чем концентрация антител, таблица включает в себя только опцию присутствия или отсутствия антигена в образце.
Рассмотренные выше диагнозы могут, кроме того, дополняться информацией, относящейся к риску развития язвы желудка и двенадцатиперстной кишки (желудочной и/или кишечной), а также к связанному с ней фактору риска, а также с возможным риском возникновения рака, со связанным с ним фактором риска. Критерии для установления риска язвы или рака желудка и двенадцатиперстной кишки, основывающиеся на измерениях значений уровней PGI и G-17 по сравнению с их пороговыми и эталонными значениями были описаны в WO 00/67035 и WO 96/15456 соответственно. Различные факторы риска, ассоциируемые с язвой и раком желудка и двенадцатиперстной кишки, описаны подробно, например, в Gastroenterology Clinics of North America, Volume 29, No. 3 (2000), в частности на странице 586, где различные факторы риска, ассоциируемые с нормальной, неатрофической, слегка, умеренно и остро атрофичной слизистой оболочкой антрального отдела и главной части желудка, описаны как для язвы, так и для рака желудка и двенадцатиперстной кишки, в форме диаграммы.
Другие дополнительные параметры, которые могут быть приняты во внимание при формировании информации для отображения, например, в форме диагноза, могут представлять собой возраст пациента, состояние, например, симптомы рефлюкса, диспепсии, и/или анемии, или также и другие симптомы и болезненные состояния, при этом в соответствии с одним из воплощений настоящего изобретения, рассмотренные симптомы или заболевания могут быть введены в средства для обработки данных в виде параметров булевой логики.
Таблица, приведенная выше, может быть дополнена, например, пороговым значением для возраста, при этом, например, возраст выше 45 лет, в сочетании с диспепсией, у пациентов с инфекцией Helicobacter pylori и неатрофическим гастритом или атрофическим гастритом главной части желудка, в дополнение к диагнозу, относящемуся к состоянию слизистой оболочки желудка, может обуславливать предложение относительно лечения пациента от инфекции Helicobacter pylori.
В дополнение к этому, например, диагноз атрофический гастрит главной части желудка, дополнительно в сочетании с пернициозной анемией, независимо от возраста, может обуславливать предложение об исследовании сыворотки на витамин B12 и гомоцистеин, и возможно, также и предложение о поддерживающем лечении витамином B12.
Настоящее изобретение также направлено на набор, содержащий средство для измерения, в образце, концентрации уровня пепсиногена I и/или гастрина, и/или средство для определения концентрации или присутствия маркера Helicobacter pylori. Этот набор также содержит различные средства, такие как реагенты, необходимые для измерения концентрации или присутствия рассматриваемого анализируемого соединения, упакованные в различные контейнеры, но содержащиеся в одной и той же упаковке. Этот набор также может содержать инструкции для использования. В дополнение к этому набор содержит программный продукт для компьютера, воплощенный на носителе информации, считываемом компьютером, и содержащий средство компьютерного кода, которое при исполнении упомянутого кода на компьютере обеспечивает осуществление этапов сравнения измеренных значений концентрации анализируемого соединения с заранее определенным пороговым значением для получения комбинации результатов сравнения, которые вместе с дополнительно введенными другими данными образуют основу для информации, которая должна в результате генерироваться. Программный продукт для компьютера может содержать заранее сохраненные пороговые значения для одного или нескольких анализируемых соединений, которые должны измеряться, или такие значения должны вводиться во время использования. При использовании набора концентрация, по меньшей мере, одного анализируемого соединения, а также концентрации любых других анализируемых соединений, если это требуется, измеренные с помощью одного и того же набора, или с использованием других средств или наборов, вводятся при использовании этой программы на компьютере.
Настоящее изобретение также относится к программному продукту для компьютера, воплощенному в носителе информации, считываемом компьютером, и содержащему средство компьютерного кода, предназначенное для осуществления этапов сравнения измеренных значений концентрации анализируемого соединения, таких как анализируемые соединения Hp-маркер, PGI и гастрин, с его заранее определенным пороговым значением, для получения комбинаций результатов сравнения для генерации вместе с другими дополнительно введенными данными информации при исполнении упомянутого кода на компьютере.
На чертеже представлена диаграмма, относящаяся к панели исследования или к «дереву решений» в соответствии с одним из воплощений настоящего изобретения. Пороговые значения для каждого из анализируемых соединений являются такими, как указано в диаграмме и описано ниже. Они, как показано, дают точные диагнозы для популяции в среднем. Разумеется, можно также использовать другие более или менее модифицированные пороговые значения, если это требуется в способах, используемых для определения концентраций анализируемых соединений, и/или при необходимости изменения чувствительности и специфики измерений.
Используемый образец представляет собой образец сыворотки крови, и гастрин представляет собой гастрин-17 (G-17). При определении уровня пепсиногена I в сыворотке пороговое значение для атрофического гастрита составляет, в соответствии с предварительными исследованиями авторов, 20-30 мкг/л в зависимости от специфики и чувствительности, соответствующей рассматриваемому способу, что соответствует примерно 450-690 пмоль/л. В этом примере авторы использовали значение 25 мкг/л в качестве первого порогового значения для атрофического гастрита в области главной части желудка или атрофического пангастрита. Тем не менее, в соответствии с настоящим изобретением, также можно использовать и второе значение для PGI в качестве порогового значения для установления различия между атрофическим гастритом в антральном отделе (с небольшим только атрофическим гастритом главной части желудка) и неатрофическим гастритом, соответственно когда уровень G-17 находится в пределах порогового диапазона для G-17. В контексте настоящего изобретения это второе значение определяется как второе пороговое значение. В этом примере авторы используют значения 50 мкг/л для этого второго порогового значения, это значение примерно в два раза превышает первое пороговое значение. Если в дополнение к этому измеряется концентрация анализируемого соединения пепсиногена II, первое пороговое значение для отношения PGI к PGII может составлять, например 2,5, а для второго порога, например, примерно 5.
В этом примере авторы используют концентрацию гастрина-17 в сыворотке крови, полученную после белковой стимуляции, то есть гастрина-17 после приема пищи. Пороговый диапазон для «стимулированного» уровня гастрина-17 (G-17st), как правило, находится в пределах от 5 до 10 пмоль/л, при этом нижний предел в 5 пмоль/л образует нижнее пороговое значение, верхний предел в 10 пмоль/л - верхнее пороговое значение, а диапазон в промежутке между ними - третий пороговый диапазон. В дополнение к этому существует самый нижний порог для уровня гастрина-17, 0,5 пмоль/л, который применяется для указания на нормальную слизистую оболочку при нормальных значениях уровня PGI (PGI ≥ 25 мкг/л). Соответствующие значения и диапазоны для нестимулированного уровня G-17 должны составлять примерно половину от значений, приведенных для стимулированных значений уровня. В этом примере авторы используют антитела к Helicobacter pylori в качестве Hp-маркера, причем авторы обнаружили, что соответствующие пороговые значения для значения антител к Helicobacter pylori составляет примерно 30 Э.М.Е.
В соответствии с описываемым вариантом осуществления, средство для обработки данных осуществляет сравнение измеренного значения уровня Hp-Ab с пороговым значением для уровня Hp-Ab, которое указывается как равное 30 Э.М.Е. В зависимости от измеренного значения уровня, которое может быть более высоким, или равным, или более низким, чем заранее определенное пороговое значение, средство для обработки данных осуществляет в первом случае сравнение измеренного уровня G-17st с его пороговым диапазоном, а в последнем случае средство для обработки данных осуществляет сравнение уровня PGI с его первым пороговым значением.
Если в первом случае уровень G-17st находится либо ниже нижнего порогового значения, либо выше его верхнего порогового значения, средство для обработки данных осуществляет сравнение уровня PGI с его указанным первым пороговым значением. Когда уровень G-17st находится ниже его нижнего порога и уровень PGI находится ниже его значения первого порога, система для обработки данных будет генерировать информацию, относящуюся к диагнозу атрофический гастрит антрального отдела и главной части желудка (пангастрит), но если уровень PGI является равным или более высоким, чем первое пороговое значение, информация будет связана с атрофическим гастритом антрального отдела.
Когда уровень G-17st находится выше его верхнего порога и уровень PGI находится ниже значения первого порога для уровня PGI, генерируемая информация будет связана с атрофическим гастритом главной части желудка, но если измеренный уровень PGI является равным или более высоким, чем первое пороговое значение уровня для PGI, генерируемая информация будет связана с неатрофическим гастритом. Такой же диагноз будет отображен, если измеренный уровень PGI является высоким и равным или более высоким, чем второе пороговое значение уровня для PGI, в сочетании с уровнем G-17st, находящимся в пороговом диапазоне. Если, в свою очередь, измеренный уровень PGI находится ниже второго порогового значения для уровня PGI, при этом уровень G-17st находится в пороговом диапазоне, отображаемый диагноз будет представлять собой атрофический гастрит области антрального отдела желудка.
С другой стороны, если значение уровня Hp-Ab является более низким или равным его пороговому значению, средство для обработки данных осуществляет сравнение измеренного значения уровня PGI с первым пороговым значением для уровня PGI. В случае когда измеренное значение уровня PGI является равным или более высоким, чем указанное пороговое значение, генерируемая информация будет связана с диагнозом нормальная слизистая оболочка при значении уровня гастрина-17st, более высоком, чем третий, самый нижний порог, который в этом примере составляет 0,5 пмоль/л. Однако если указанное измеренное значение уровня PGI находится ниже первого порогового значения, отображаемая информация будет связана с диагнозом атрофический гастрит главной части желудка, когда измеренный уровень G-17st является равным или более высоким, чем верхнее пороговое значение, и с диагнозом пангастрит, когда уровень G-17st также является низким, а именно ниже чем верхний пороговый предел. В этом случае атрофический гастрит главной части желудка будет представлять собой заболевание аутоиммунного типа.
Как указано ранее, путем введения дополнительных параметров в систему обработки данных и объединения их с генерируемой информацией может быть получена дополнительная информация, например, в форме предложений для дальнейшего лечения и/или дополнительных исследований, таких как предложение провести эндоскопию для определения уровней витамина B12 и гомоцистеина, и лечение, направленное на уничтожение инфекции Helicobacter pylori.
Приведенные ниже примеры иллюстрируют настоящее изобретение без ограничения его каким-либо образом. Измеренные анализируемые соединения представляют собой пепсиноген I в сыворотке, гастрин-17 в сыворотке и антитела к Helicobacter pylori; пороговые значения являются такими, которые указаны на фиг.1. Также возраст пациента включается в качестве параметра, при этом порог составляет 45 лет. Соответствующий диагноз приведен в каждом примере вместе с дополнительными предложениями для исследований и лечения, когда они могут применяться.
Предлагаемый диагноз: НОРМАЛЬНАЯ
1) Атрофического гастрита нет
2) Инфекции H.pylori нет
3) Нет риска возникновения заболеваний рака желудка и язвы желудка и двенадцатиперстной кишки (кишечных и желудочных); фактор риска IX.
Предлагаемое дальнейшее исследование и лечение:
Не рекомендуется никаких дополнительных исследований (например, эндоскопии).
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ ГЛАВНОЙ ЧАСТИ ЖЕЛУДКА
1) Заболевание язва желудка и двенадцатиперстной кишки (язва кишечника и желудка) маловероятно.
2) Атрофический гастрит главной части желудка аутоиммунного типа.
3) Повышенный риск возникновения рака желудка (фактор риска 3-5X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Рекомендуется определение уровней витамина B12 и гомоцистеина.
Заместительная терапия витамином B12, если уровень B12 ниже 170 пмоль/л.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ АНТРАЛЬНОГО ОТДЕЛА/ГЛАВНОЙ ЧАСТИ ЖЕЛУДКА.
1) Заболевание язва желудка и двенадцатиперстной кишки (кишечника и желудка) маловероятно.
2) Повышенный риск возникновения рака желудка (фактор риска 3-90X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Рекомендуется определение уровней витамина B12 и гомоцистеина.
Заместительная терапия витамином B12, если уровень B12 ниже 170 пмоль/л.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ АНТРАЛЬНОГО ОТДЕЛА/ГЛАВНОЙ ЧАСТИ ЖЕЛУДКА.
1) Заболевание язва желудка и двенадцатиперстной кишки (кишечника и желудка) маловероятно.
2) Повышенный риск возникновения рака желудка (фактор риска 3-90X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Рекомендуется определение уровней витамина B12 и гомоцистеина.
Заместительная терапия витамином B12, если уровень B12 ниже 170 пмоль/л. Необходимо лечение инфекции H.pylori.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ АНТРАЛЬНОГО ОТДЕЛА.
1) Высокий риск заболевания язвой желудка и двенадцатиперстной кишки (кишечника и желудка) (фактор риска 10-20X).
2) Повышенный риск рака желудка (фактор риска 18X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Необходимо лечение инфекции H.pylori.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ АНТРАЛЬНОГО ОТДЕЛА.
1) Высокий риск заболевания язвой желудка и двенадцатиперстной кишки (кишечника и желудка) (фактор риска 10-20X).
2) Повышенный риск рака желудка (фактор риска 18X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Необходимо лечение инфекции H.pylori.
Предлагаемый диагноз: НЕАТРОФИЧЕСКИЙ ГАСТРИТ.
1) Повышенный риск заболевания язвой желудка и двенадцатиперстной кишки (кишечника и желудка) (фактор риска 10X).
2) Низкий риск рака желудка (фактор риска 1-2X).
Предлагаемое дальнейшее исследование и лечение:
Эндоскопия не является необходимой. Необходимо лечение инфекции H.pylori.
Предлагаемый диагноз: НЕАТРОФИЧЕСКИЙ ГАСТРИТ.
1) Повышенный риск заболевания язвой желудка и двенадцатиперстной кишки (кишечника и желудка) (фактор риска 10X).
2) Низкий риск рака желудка (фактор риска 1-2X).
Предлагаемое дальнейшее исследование и лечение:
Эндоскопия не является необходимой. Необходимо лечение инфекции H.pylori.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ ГЛАВНОЙ ЧАСТИ ЖЕЛУДКА.
1) Повышенный риск рака желудка (фактор риска 3-5X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Рекомендуется определение витамина уровней B12 и гомоцистеина. Заместительная терапия витамином B12, если уровень B12 ниже 170 пмоль/л. Лечение инфекции H.pylori.
Предлагаемый диагноз: НЕАТРОФИЧЕСКИЙ ГАСТРИТ.
1) Повышенный риск заболевания язвой желудка и двенадцатиперстной кишки (кишечника и желудка) (фактор риска 10X).
2) Низкий риск рака желудка (фактор риска 1-2X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Лечение инфекции H.pylori, если есть симптомы диспепсии.
Предлагаемый диагноз: АТРОФИЧЕСКИЙ ГАСТРИТ ГЛАВНОЙ ЧАСТИ ЖЕЛУДКА.
1) Повышенный риск рака желудка (фактор риска 3-5X).
Предлагаемое дальнейшее исследование и лечение:
Желательна эндоскопия. Рекомендуется определение уровней витамина B12 и гомоцистеина. Заместительная терапия витамином B12, если уровень B12 ниже 170 пмоль/л. Необходимо лечение инфекции H.pylori, если есть симптомы диспепсии.
Изобретение относится к биохимии и медицине и касается способа оценки состояния слизистой оболочки желудка, в частности атрофического гастрита, путем анализа соединений пепсиногена 1, гастрина и маркера инфекции Helicobacter pylori (HP), и введение полученных результатов в средство обработки данных, включающее в себя операционную систему, средство для передачи и приема и обработки данных, причем упомянутое средство обработки данных предназначено для осуществления сравнения измеренного значения концентрации анализируемого соединения с пороговым значением для анализируемого соединения, и генерирования информации, в ответ на комбинацию результатов сравнения и дополнительно, на другие введенные данные. Изобретение касается также набора и программного продукта для компьютера, в частности для использования в способе по настоящему изобретению. Изобретение обеспечивает возможность идентифицирования лиц, страдающих раком на начальных стадиях заболевания. 3 н. и 13 з.п. 1 ил.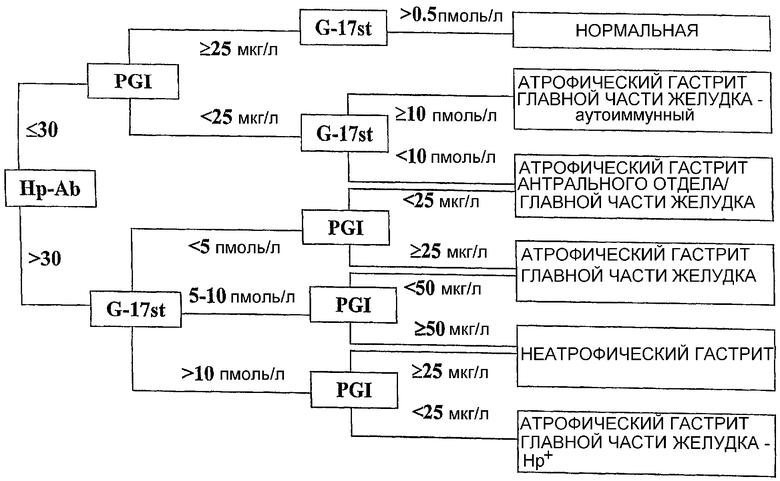
| WO 9615456 A, 23.05.1996 | |||
| Многобарабанная лебедка | 1945 |
|
SU67035A1 |
| KUIPPERS E.J | |||
| et al | |||
| Eur.J.Gastroenterol | |||
| Hepatol | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| abst | |||
| Способ определения состояния слизистой оболочки гастродуоденальной зоны при язвенной болезни | 1989 |
|
SU1789926A1 |
| Способ диагностики атрофического антрального гастрита | 1988 |
|
SU1704013A1 |
| RU 94034020 A1, 20.08.1996. | |||
Авторы
Даты
2005-10-20—Публикация
2002-01-04—Подача