Изобретение относится к электролитическому получению хлоркислородных соединений, в частности к способу получения гипохлоритов из растворов щелочных и щелочноземельных металлов, и может быть использовано для получения окислителей, применяемых качестве дезинфицирующих растворов в лечебно-профилактических учреждениях, домах отдыха, санаториях, предприятиях общественного питания и коммунального хозяйства, школах, детских садах, плавательных бассейнах, станциях водоснабжения и т. п.
Известны методы получения гипохлорита путем электролиза растворов хлоридов, где в качестве исходного рассола используются растворы хлористого натрия или природные электролиты.
Наиболее близким по технической сущности и достигаемому техническому результату является способ получения гипохлорита натрия путем электролиза раствора хлористого натрия на безнапорной электролизной установке непроточного типа ЭН-1 [Технические указания по эксплуатации электролизных установок непроточного типа производительностью 1, 5, 25 и 100 кг в сутки активного хлора. Отдел научно-технической информации АКХ, М., 1975, - прототип].
Недостатком данного способа является то, что процесс получения гипохлорита путем электролиза раствора хлористого натрия осуществляется с низким выходом по току, а сам гипохлорит имеет невысокую биологическую активность.
Техническая задача - повышение выхода по току гипохлорита при одновременном увеличении его биологической активности за счет увеличения концентрации хлоридов в растворе электролита.
Решение технической задачи достигается тем, что при получении гипохлорита, включающем электролиз растворов хлоридов, процесс электролиза ведут при плотности тока 0,1-1,5 А/дм2, и в качестве электролита используют раствор природного бишофита плотностью 1,3 г/см3, с содержанием ионов хлора 340,8 г/л, ионов брома 5,6 г/л.
При электролизе раствора природного бишофита (MgCl2·6H2O) на аноде происходит разряд ионов хлора и брома:
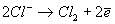
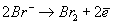
Выделяющийся хлор растворяется в электролите с образованием хлорноватистой, бромноватистой, хлористо- и бромистоводородных кислот:
Сl2+Н2O-НСlO+НСl
Вr2+Н2O=НВrO+НВr
На катоде происходит восстановление молекул воды с выделением водорода:
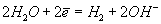
Атомы водорода после восстановления на катоде выделяются из раствора в виде газа, оставшиеся ионы ОН- образуют возле катода с ионами Mg2+ щелочь.
Вследствие перемешивания анолита с католитом происходит взаимодействие хлорноватистой и бромноватистой кислот со щелочью с образованием гипохлорита и гипобромита магния:
2HClO+Mg(OH)2=Mg(ClO)2+2H2O
2HBrO+Mg(OH)2=Mg(BrO)2+2H2O
Увеличение выхода по току гипохлорита обеспечивается за счет наличия высокой концентрации хлоридов в растворе природного бишофита. Это объясняется тем, что с повышением концентрации хлоридов улучшается соотношение потенциалов выделения хлора и кислорода, благоприятствующее разряду ионов хлора и подавлению разряда ионов кислорода, что приводит к увеличению концентрации гипохлорита в готовом продукте, а следовательно, и увеличению выхода его по току, одновременно за счет присутствия в составе ионов брома, при электролитическом окислении раствора природного бишофита, образуются гипохлорит и гипобромит магния, взаимное действие этих окислителей усиливает биологическую активность конечного дезинфицирующего продукта, что и является новым техническим эффектом заявляемого способа.
По предварительной оценке ВНИИгалургии общие запасы бишофита только Волгоградского месторождения составляют 250 млрд. тонн. Залежи природного бишофита в Нижнем Поволжье практически целиком (до 98%) сложены мономинералом - бишофитом (MgCl2·6H2O). Природным хлоридам магния, как правило, сопутствуют его бромиды. Содержание брома в бишофите даже при добыче в виде рассола в десятки и сотни раз превышает такое традиционное сырье.
Способ получения гипохлорита осуществлялся следующим образом: из раствора природного бишофита плотностью 1,3 г/см3, с содержанием ионов хлора 340,8 г/л, ионов брома 5,6 г/л готовят растворы различных концентраций. Далее раствор заливается в непроточный электролизер. В качестве катода используется стальной электрод. В качестве анода применяется угольный графитовый электрод. Процесс ведется на постоянном токе при заданных параметрах плотностей тока 0,1-1,5 А/дм2, источником тока служит лабораторный источник постоянного тока (ЛИПС-35). Процесс электролиза раствора природного бишофита осуществляется в течение 0,5 ч. По окончании электролиза по известной методике определяется концентрация активного хлора. Величина водородного показателя среды (рН) исходного и полученного растворов контролируется по рН-метру - милливольтметру рН-121.
По известным формулам расчета показателей электрохимического процесса рассчитывается выход по току, удельный расход электроэнергии.
Для проверки заявляемого способа были проведены серии стендовых испытаний с использованием растворов природного бишофита различных концентраций.
Примеры конкретного исполнения:
ПРИМЕР 1
Брали раствор природного бишофита концентрацией 75,4 г/л (0,5 н.) и проводили процесс электролиза на угольном графитовом электроде при плотностях тока от 0,1 до 1,5 А/дм2, при температуре 20° С (см. табл. 1).
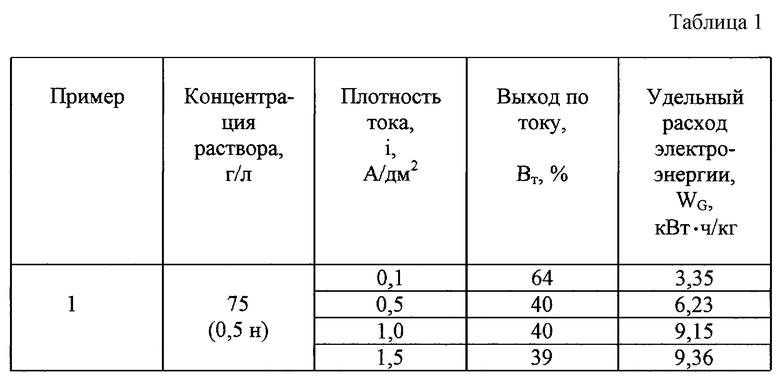
ПРИМЕР 2
Брали раствор природного бишофита концентрацией 151 г/л (1,0 н) и проводили процесс электролиза на угольном графитовом электроде при плотностях тока от 0,1 до 1,5 А/дм2, при температуре 20° С (см. табл. 2).
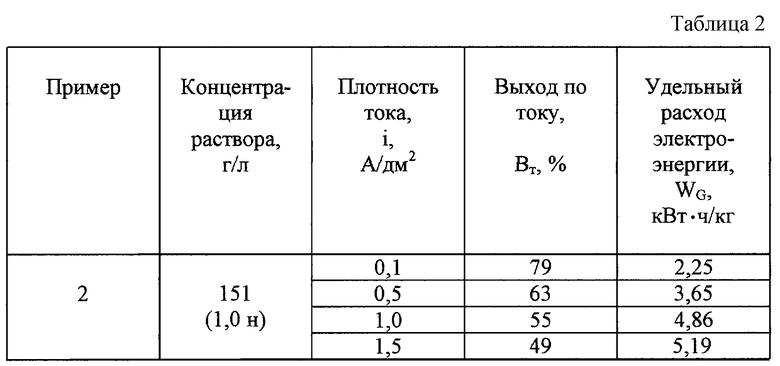
ПРИМЕР 3
Брали раствор природного бишофита концентрацией 226 г/л (1,5 н) и проводили процесс электролиза на угольном графитовом электроде при плотностях тока от 0,1 до 1,5 А/дм2, при температуре 20° С (см. табл. 3).
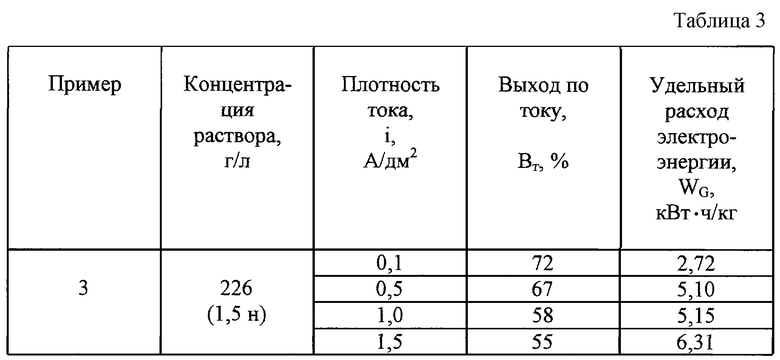
ПРИМЕР 4
Брали раствор природного бишофита, концентрацией 302 г/л (2 н) и проводили процесс электролиза на угольном графитовом электроде при плотностях тока от 0,1 до 1,5 А/дм2, при температуре 20° С (см. табл. 4).
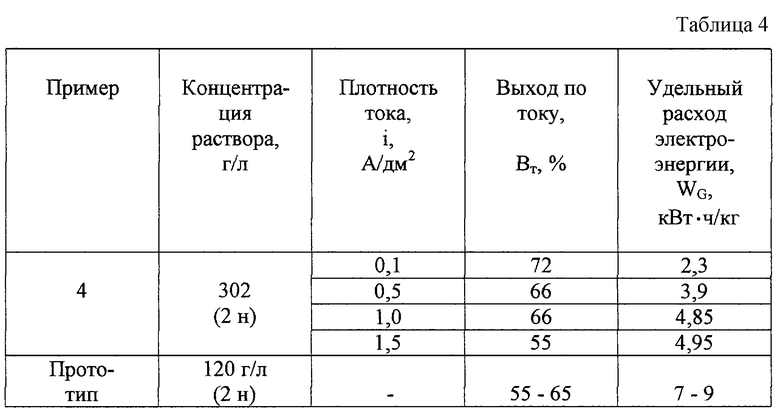
По приведенным результатам экспериментов видно, что оптимальным режимом, при котором отмечается наибольший выход по току при наименьших энергетических затратах, является электролиз раствора природного бишофита концентрацией 302 г/л и катодной плотности тока 0,1-0,5 А/дм2. Полученный при данных условиях гипохлорит имеет выход по току (в пересчете на активный хлор) 72-66%.
Таким образом, получение гипохлорита электролизом раствора природного бишофита по сравнению с гипохлоритом, полученным по прототипу из раствора хлористого натрия, обеспечивает увеличение выхода по току на 12%, а проведенный бактериологический анализ показал, что при обеззараживании гипохлоритом, приготовленным из раствора природного бишофита, требуется меньшая доза по активному хлору, чем при обеззараживании гипохлоритом, полученным из раствора хлористого натрия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ РАСТВОРА ГИПОХЛОРИТОВ МАГНИЯ И МЕДИ | 2011 |
|
RU2466214C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУНГИЦИДОВ МЕДИ | 2008 |
|
RU2361016C1 |
| АНТИСЕПТИЧЕСКИЙ ОГНЕЗАЩИТНЫЙ СОСТАВ ДЛЯ ДРЕВЕСИНЫ | 2012 |
|
RU2497662C1 |
| СРЕДСТВО ДЛЯ ПРЕДПОСЕВНОЙ ОБРАБОТКИ СЕМЯН | 2009 |
|
RU2412575C1 |
| Средство для лечения некробактериоза крупного рогатого скота | 2019 |
|
RU2714322C1 |
| Способ получения хлоркислородной соли натрия | 1974 |
|
SU672222A1 |
| Способ электрохимического получения раствора гипохлоритов магния и меди | 2018 |
|
RU2713176C2 |
| Способ получения раствора смеси хлората и гипохлорита магния | 1987 |
|
SU1624057A1 |
| Способ удаления нитрит-ионов из водных растворов | 2016 |
|
RU2625466C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРАЛЮМИНИЙСОДЕРЖАЩЕГО КОАГУЛЯНТА | 1994 |
|
RU2081830C1 |
Изобретение относится к электролитическому получению хлоркислородных соединений, в частности к способу получения гипохлоритов из растворов щелочных и щелочноземельных металлов, и может быть использовано для получения окислителей, применяемых в качестве дезинфицирующих растворов. Гипохлорит получают электролизом растворов хлоридов. Процесс электролиза ведут при плотности тока 0,1-1,5 А/дм2, и в качестве электролита используют раствор природного бишофита плотностью 1,3 г/см3, с содержанием ионов хлора 340,8 г/л, ионов брома 5,6 г/л. Технический эффект - повышение выхода по току гипохлорита при одновременном увеличении его биологической активности за счет увеличения концентрации хлоридов в растворе электролита. 4 табл.
Способ получения гипохлорита, включающий электролиз растворов хлоридов, отличающийся тем, что процесс электролиза ведут при плотности тока 0,1-1,5 А/дм2 и в качестве электролита используют раствор природного бишофита плотностью 1,3 г/см3 с содержанием ионов хлора 340,8 г/л, ионов брома 5,6 г/л.
| Способ получения раствора смеси хлората и гипохлорита магния | 1987 |
|
SU1624057A1 |
| СПОСОБ ПРОВЕДЕНИЯ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА СОЛИ | 1997 |
|
RU2125120C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПУЛЬПЫ ИЗ ЦЕЛЛЮЛОЗОСОДЕРЖАЩЕГО МАТЕРИАЛА, ПРИМЕНЕНИЕ ЛИГНИНА | 1996 |
|
RU2139965C1 |
| US 4049531 А, 20.09.1977 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2004-10-20—Публикация
2003-07-30—Подача