6-Гидрокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофен гидрохлорид (арзоксифен) в самом общем виде был впервые описан в Патенте США №5510357 и подробно рассмотрен в Патенте США №5723474 (‘474) и в Заявке на Европейский Патент 0729956. Арзоксифен представляет собой нестероидный смешанный антагонист/агонист эстрогена, между прочим, используется для снижения холестерина сыворотки, ингибирования гиперлипедимии, остеопороза, эстроген-зависимых раков, включая рак молочной железы и матки, эндометриоза, расстройств ЦНС, включая болезнь Альцгеймера, пролиферации клеток гладких мышц аорты и рестеноза.
Точнее, арзоксифен является полезным и в настоящее время применяется в клиниках для лечения рецептор-позитивного метастатического рака молочной железы, адъювантного лечения рецептор-позитивных пациентов после соответствующей системной и местной терапии; снижения распространения инвазивного и неинвазивного рака молочной железы и протоковой карциномы in situ (DCIS). Арзоксифен также используется в комбинации с лучевой терапией, ингибиторами ароматазы, аналогами LHRH (лютеинизирующий гормон – релизинг - гормон) и ингибиторами ацетилхолинэстеразы (AchE).
Исследования с помощью методов рентгеновской порошковой дифракции (XRD), термогравиметрического анализа (TGA), метода протонного ядерного магнитного резонанса (1Н ЯМР) и метода Карла Фишера (Karl Fischer; KF) основной массы арзоксифена, выделенного согласно способам, изложенным в ‘474, указывают, что названный материал является гидратированным, слабо кристаллизующимся и содержит в своей кристаллической решетке различные количества органического летучего компонента (этилацетата).
Обычно для приготовления лекарственных средств слабо кристаллизующиеся вещества менее желательны, чем высоко кристаллизующиеся вещества. Кроме того, вообще нежелательно получение фармацевтических средств, содержащих значительные количества органического растворителя (например, этилацетата), вследствие возможной токсичности растворителя для реципиента и изменения эффективности фармацевтического средства в результате действия растворителя.
Хотя арзоксифен, полученный согласно способам, предложенным в ‘474, можно использовать как фармацевтическое средство, крайне желательны и полезны поиски еще и кристаллической формы арзоксифена, которая не содержала бы органический растворитель в кристаллической решетке и которую можно воспроизводить и эффективно получать в коммерческом масштабе.
Данное изобретение относится к новой нестехиометрической гидратированной форме 6-гидрокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена гидрохлорида (F-III), имеющей рентгеновскую дифрактограмму, которая содержит следующие пики: 4,6±0,2; 7,8±0,2; 9,3±0,2; 14,0±0,2; 17,6±0,2; 20,8±0,2 и 24,3±0,2° при 2θ, полученные при 25±2°С и 35±10% относительной влажности (RH) из медного источника излучения.
Кроме того, данное изобретение относится к фармацевтической композиции, содержащей F-III; один или больше фармацевтических носителей, разбавителей или наполнителей; и необязательно эстроген, необязательно прогестин, необязательно ингибитор ароматазы, необязательно аналог LHRH и необязательно ингибитор ацетилхолинэстеразы (AChE).
К тому же данное изобретение относится к способам применения F-III для ингибирования патологических состояний, таких как фиброз матки, эндометриоз, пролиферация клеток гладких мышц аорты, рестеноз, рак молочной железы, рак матки, рак простаты, доброкачественная гиперплазия простаты, разрежение кости, остеопороз, сердечно-сосудистое заболевание, гиперлипидемия, расстройства ЦНС и болезнь Альцгеймера, а также применения F-III в производстве лекарственных средств для ингибирования таких заболеваний.
Данное изобретение также относится к способам применения F-III для активации холин-ацетилтрансферазы (ChAT) и применения F-III для производства лекарственного средства для активации этого фермента.
Краткое описание чертежей
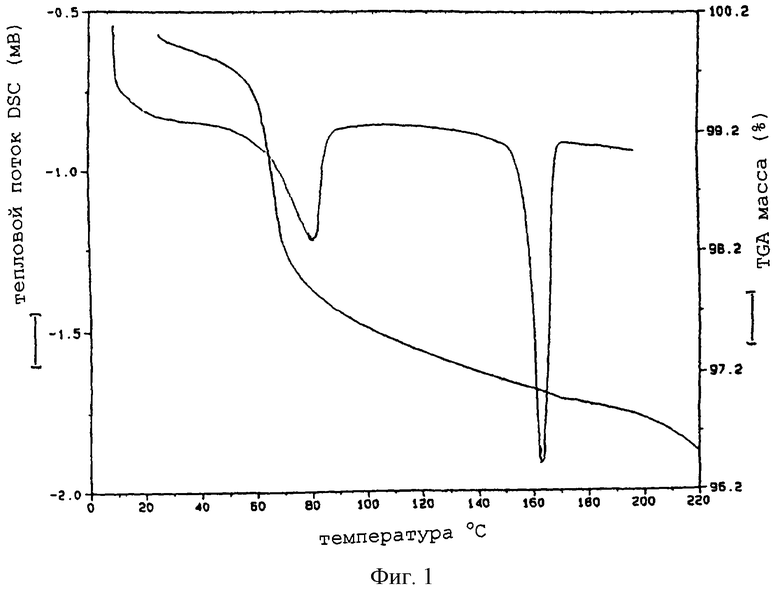
Фиг.1 является типичным изображением дифференциальной сканирующей калориметрии (DSC)/TGA S-II.
Фиг.2 является типичным изображением DSC/TGA F-I.
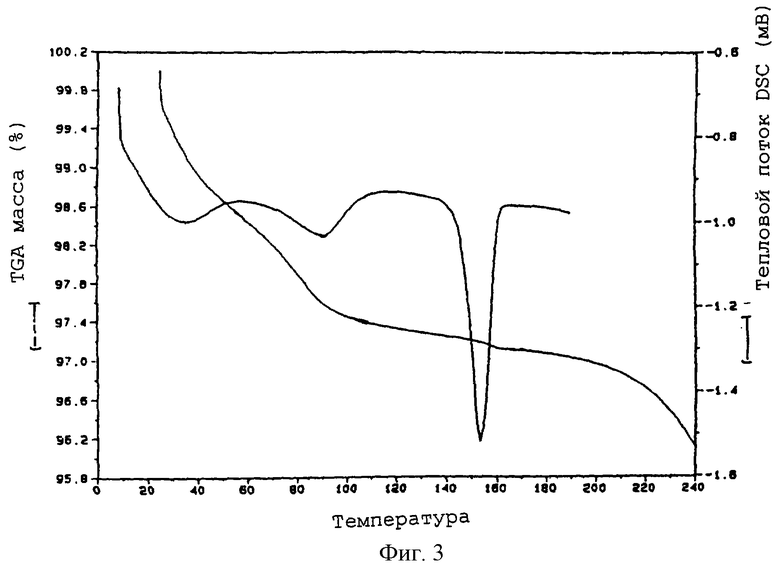
Фиг.3 является типичным изображением DSC/TGA F-III.
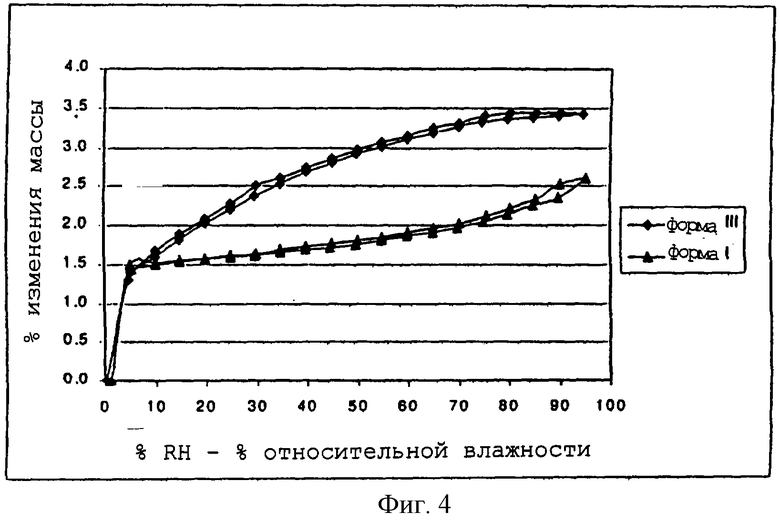
Фиг.4 изображает изотермы сорбции влаги для F-I и F-III.
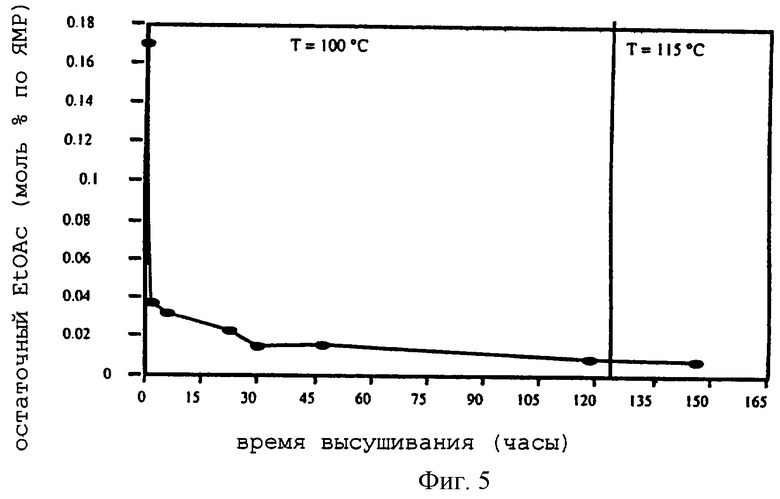
Фиг.5 изображает десольватацию S-II как функцию времени и температуры высушивания.
Детальное описание изобретения
Основная масса арзоксифена, полученного по методу, изложенному в ‘474 (пример 41, кристаллизация из смеси этанола и этилацетата, фильтрование и высушивание фильтровального осадка под вакуумом до постоянного веса при комнатной температуре), была охарактеризована методом XRD и, как было обнаружено, является слабо кристаллизующимся веществом. Методом 1Н ЯМР показали, что основная масса вещества содержит 6% этилацетата.
Предложенный в ‘474 способ кристаллизации впоследствии модифицировали с тем, чтобы этанол добавлять в суспензию неочищенного арзоксифена в кипящем этилацетате. После охлаждения и фильтрования под вакуумом, твердое вещество, полученное в результате этого модифицированного способа, представляет собой высоко кристаллический смешанный сольват арзоксифена в смеси этилацетат/вода (в дальнейшем упоминаемый как S-II), который, как было обнаружено позднее, является исходным материалом для F-I (другой нестехиометрической гидратированной кристаллической формы арзоксифена).
F-I может быть получен удалением этилацетата из кристаллической решетки S-II с помощью вакуумной сушки/отжигания S-II при повышенных температурах. Время и температура, необходимые для отжига S-II, чтобы получить F-I, изменяются от партии к партии, но обычно составляют порядка 5 дней приблизительно при 100°С. Для осуществления превращения S-II в F-I с помощью этого метода требуются высокие температуры, поскольку при суспендировании S-II в воде при температуре окружающей среды или хранении образца при 98% RH в течение 3 недель не происходит никакого превращения в F-I. Кроме того, высушивание S-II в конвекционной печи при высоких температурах не десольватирует никакой материал, позволяя предположить, что вакуум также необходим для вытягивания этилацетата из решетки S-II. Предпочтительно F-I быстро получают при температуре окружающей среды кристаллизацией арзоксифена (или его любой полиморфной модификации/сольвата) из тетрагидрофурана.
Согласно данному изобретению особенно предпочтительной формой арзоксифена является F-III. F-III легко получают и выделяют при температуре окружающей среды. При получении F-III для удаления низких уровней остаточного кристаллизационного растворителя требуются только умеренные условия сушки. Эти умеренные условия сушки соответственно приводят к получению твердого вещества с высокой степенью чистоты (то есть свободного от органического растворителя) и кристалличности и, таким образом, применение F-III устраняет появление токсичности, связанной с остаточным органическим растворителем и органическим растворителем кристаллической решетки. Кроме того, получение F-III оказывается простым и эффективным, то есть подходит для масштабного производства.
F-III легко получают и выделяют путем кристаллизации арзоксифена (или его любой полиморфной модификации/сольвата) из смеси изопропилового спирта (IPA) и воды при температуре окружающей среды. Обычно арзоксифен может быть суспендирован в смеси IPA и воды и нагрет с тем, чтобы растворить исходный материал арзоксифена. Как только достигается растворение, раствор оставляют для охлаждения до комнатной температуры, а затем далее до температуры между 0 и 5°С (с помощью ледяной бани или замораживания). После того как проходит достаточный для кристаллизации период времени, кристаллы можно собирать посредством вакуумного фильтрования и высушивания под вакуумом до постоянного веса, чтобы получить F-III с выходом более 80%.
Подходящий исходный материал для вышеупомянутой кристаллизации включает в себя S-II, F-I, арзоксифен, полученный способами, изложенными в ‘474, и его любую смесь, не ограничиваясь перечисленным. Неважно, какая форма арзоксифена окажется исходной, поскольку кристаллизация из IPA и воды, согласно описанным в заявке способам, дает в результате кристаллы F-III. Соотношение воды и IPA (объем:объем) обычно составляет приблизительно от 1:1 до 9:1. Более предпочтительно, соотношение оказывается между 2,5 и 5,6:1. Наиболее предпочтительно, когда соотношение оказывается между 3 и 5,6:1. После сбора кристаллов с помощью вакуумного фильтрования, перед высушиванием под вакуумом влажный осадок F-III может быть промыт охлажденной деионизированной водой. Кроме того, предпочтительно небольшое повышение температуры высушивания (около 50°С в течение от 12 до 24 часов). Для синтеза F-III в коммерческом масштабе может оказаться полезным внесение затравки кристаллизации F-III.
В предпочтительном способе F-III получают, выделяют и очищают одновременно с химическим удалением защитной группы 6-изопропилгидрокси из 6-изопропокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена гидрохлорида (предшественник А). Реакция освобождения от защиты контролируется до полного удаления изопропильной защитной группы, и как только устанавливают, что удаление по существу завершено, продолжение реакции предпочтительно будет включать в себя кристаллизацию при условиях, которые обеспечивают F-III, обсуждаемый выше и ниже.
Способы получения предшественника А и удаления изопропильной группы можно обнаружить в Патенте США №5723474, рекомендации которого приведены в описании.
В другом предпочтительном способе F-III получают, выделяют и очищают одновременно с химическим восстановлением
S-оксида и химическим удалением защитной бензильной группы от 6-гидрокси из 6-бензилокси-3-(4-[2-(пиперидин-1-ил)этокси]-2-(4-метоксифенил)-бенз[b]тиофена-(S-оксида) (предшественник В). Реакции восстановления и удаления защиты контролируются до полного восстановления сульфоксида до сульфида и полного удаления бензилгидроксизащитной группы. Как только устанавливают, что восстановление/удаление в основном завершено, продолжение реакции предпочтительно будет включать в себя кристаллизацию при условиях, которые обеспечивают F-III, описанный в заявке. Способы получения предшественника В, удаления бензильной группы и восстановления 1-сульфоксида до соответствующего сульфида также можно найти в уже цитированном Патенте США №5723474.
Независимо от химии, используемой на стадиях удаления защиты и восстановления, кристаллизация арзоксифена из растворов IPA/вода впоследствии дает кристаллы F-III с высокой степенью чистоты.
Характеристика и дифференциация S-II, F-I и F-III
Для характеристики S-II, F-I и F-III применяются методы DSC/TGA и XRD. TGA часто используется для выявления различий между разными твердыми формами вещества, так как температура(ы), при которой происходят физические изменения в веществе, обычно является характеристикой полиморфа или сольвата. DSC представляет собой способ, который часто используют для скрининга соединений для образования полиморфной модификации и сольвата. Наконец, XKD является способом определения дальнего порядка в кристаллическом веществе.
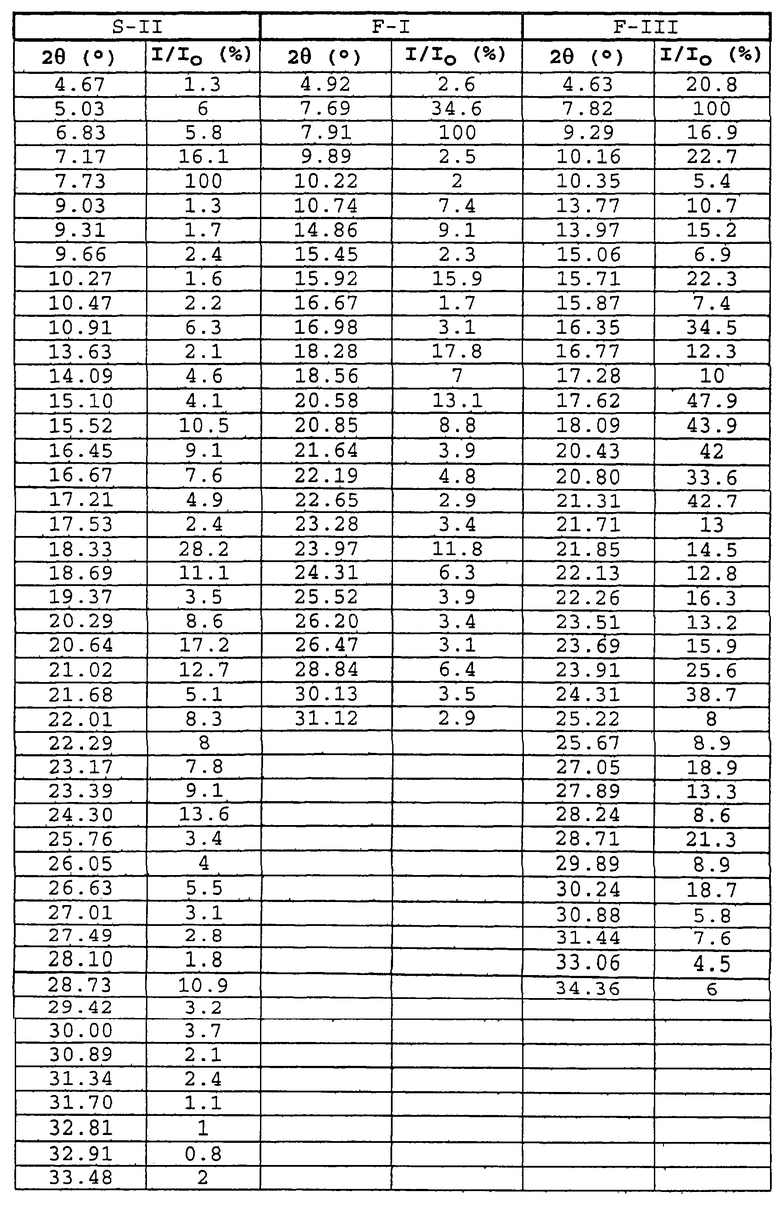
Арзоксифен, полученный способами, изложенными в ‘474, дает рентгенограмму с низким отношением сигнала к фону и повышенной базовой линией, что указывает на слабо кристаллизующееся вещество. Поэтому сравнивают F-I и F-III с веществом (S-II), полученным с помощью вышеописанного модифицированного способа кристаллизации арзоксифена (добавление этанола в суспензию арзоксифена в кипящем этилацетате).
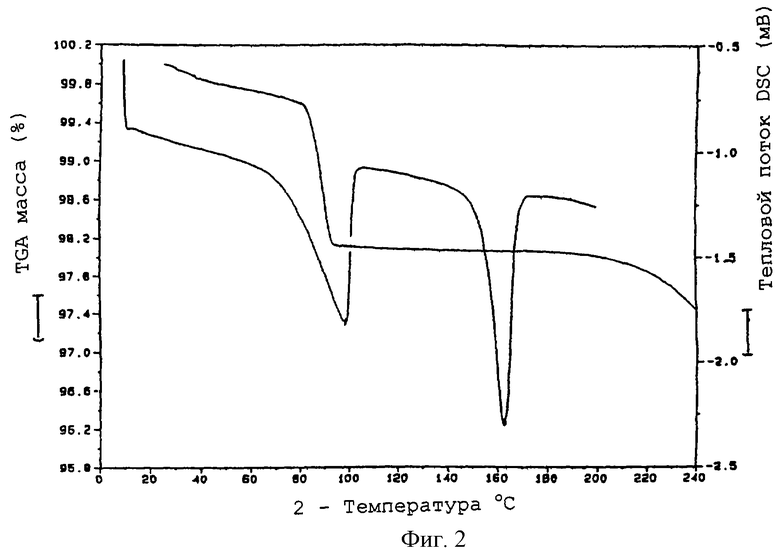
Типичные изображения DSC/TGA для S-II, F-I и F-III представлены на фиг.1, 2 и 3 соответственно. Изображение DSC для S-II показывает интенсивную эндотермическую реакцию, начинающуюся приблизительно при 62°С, соответствующую потере этилацетата и воды из решетки. Эндотермия, начинающаяся приблизительно при 152°С, представляет собой расплав. TGA-потеря массы приблизительно 2,5% происходит одновременно с первым превращением, тогда как оставшиеся 0,5% потери массы происходят вплоть до начала плавления, позволяя предположить, что некоторое количество молекул растворителя более прочно удерживается в решетке.
Изображение DSC для F-I демонстрирует интенсивную эндотермическую реакцию, начинающуюся приблизительно при 75°С, за которой следует вторая эндотермическая реакция, начинающаяся приблизительно при 155°С, соответствующая расплаву. Изображение TGA F-I показывает постоянную потерю 0,3% массы с последующей резкой потерей 1,5%, что вместе представляет собой дегидратацию решетки. Начало первого DSC превращения и соответствующая TGA потеря массы незначительно смещаются вследствие различий в скоростях нагревания. Первоначальная потеря массы представляет собой слабо удерживаемую воду гидратации, тогда как вторая потеря массы соответствует приблизительно 0,5 моля воды, присутствующей в решетке при очень низкой относительной влажности (ниже 5% - см. данные сорбции влаги).
Изображение DSC F-III представляет собой кривую интенсивной низкотемпературной эндотермической реакции приблизительно при 30°С с последующей второй полной, относительно слабой эндотермической реакцией, начинающейся приблизительно при 70°С, и конечное превращение, начинающееся приблизительно при 146°С, соответствующее расплаву. Резкая 1,5% потеря массы (~0,5 моля) в TGA, совпадающая с первой эндотермической реакцией, соответствует потере слабоудерживаемых молекул воды, тогда как дополнительная ~1,6% потеря массы при температуре выше 60°С представляет собой потерю более прочно удерживаемых молекул воды, то есть молекул, которые присутствуют при очень низкой относительной влажности. Потеря массы, наблюдаемая после 170°, соответствует разложению F-III.
Схемы XRD для F-I и F-III изображают острые пики и плоскую базовую линию, указывающие на высококристаллические вещества. Угловые положения пиков при 2θ и соответствующие данные I/I0 для типичных образцов F-I, F-III и S-II представлены в таблице 1. Хотя многие отражения интенсивности обычно находятся при подобных углах дифракции, каждая из форм дает особую порошковую рентгенограмму, указывая на четкие различия между S-II, F-I и F-III.
В области кристаллографии хорошо известно, что для любой данной полиморфной модификации относительные интенсивности дифракционных пиков могут изменяться вследствие предпочтительной ориентации, обусловленной такими факторами, как морфология кристаллов. Если имеется влияние предпочтительной ориентации, интенсивность пиков изменяется, однако характерные положения пиков полиморфной модификации не изменяются. См., например. The United States Pharmacopeia #23, National Formulary #18, pages 1843-1844, 1995. Таким образом, на основании интенсивности пиков, а также положения пиков, F-III может быть идентифицирован по присутствию пиков при 4,6±0,2; 7,8±0,2; 9,3±0,2; 14,0±0,2; 17,6±0,2; 20,8±0,2 и 24,3±0,2° при 2θ, когда изображения были получены при 25±2°С и 35±10% относительной влажности из медного источника излучения.
Дальнейшая характеристика F-I и F-III
Проведены исследования гигроскопичности F-I и F-III. На фиг.4 представлены изотермы сорбции влаги для F-I и F-III. После исходной экспозиции образцов приблизительно до 5% RH происходит немедленное увеличение массы влаги на 1,5 и 1,7% для F-I и F-III соответственно эквивалентное приблизительно 0,5 моля воды. Обе формы демонстрируют непрерывную сорбцию влаги по всей зоне влажности, что является следствием включения молекул воды в решетку.
Различия в поглощении влаги двумя формами, вероятно, отражает количество воды, которое может быть заключено в двух решетках (то есть, величину доступного пространства решетки, которое может вместить молекулы воды). Отсутствие гистерезиса в изотермах сорбция-десорбция для F-I и F-III указывает, что кристаллические формы быстро уравновешиваются при любой данной влажности.
Профили сорбции влаги для F-I и F-III показывают, что эти формы по существу являются нестехиометрическими гидратами. При относительной влажности окружающей среды (около 50% RH) F-I содержит приблизительно 1,7% воды, соответствующей 0,5 молям воды, тогда как F-III сорбирует около 3,0% воды, что соответствует приблизительно 0,85 молям воды. Основная масса форм F-I и F-III быстро уравновешивается с атмосферой, так что содержание воды, определяемое с помощью аналитических методов, является отражением относительной влажности во время сбора данных. По данным DSC, выявляемые различия от партии к партии, вероятно, обусловлены образцами, гидратированными в различной степени вследствие хранения при разных условиях окружающей среды.
Получены рентгенограммы для образцов F-I и F-III, хранившихся при различной относительной влажности (0; 22; 50 и 80%). Когда увеличивается относительная влажность, происходит постепенное смещение первоначальных (0% RH) пиков F-III приблизительно при 13,8; 17,6; 18,0; 20,5% и 24,0° на 2θ, так же, как и незначительное смещение менее интенсивных пиков. Эти наблюдаемые изменения в рентгенограммах F-III указывают, что меняются размеры элементарной ячейки, вероятно, чтобы вместить слабоудерживаемые молекулы воды, когда увеличивается относительная влажность. Непрерывное смещение пиков в зависимости от влажности хорошо коррелирует с данными по сорбции влаги, о чем свидетельствует постепенное увеличение массы в пределах этой области RH, доказывая вариабельность образования гидрата.
Аналогичный эксперимент проведен с F-I, чтобы установить, будет ли оказывать изменение относительной влажности подобное действие на его решетку (0; 25; 52; 73 и 95% RH). Наблюдается очень незначительное смещение пиков 0% RH приблизительно при 7,7; 18,3; 18,5; 20,5; 20,8° при 2θ, когда увеличивается относительная влажность. Также оказалось, что пики приблизительно при 7,7; 20,8 и 24,1 становятся несколько более расширенными и менее разделенными при более высокой относительной влажности, указывая на то, что вода оказывается сорбированной в аморфных компонентах (или пластифицирует твердое вещество), особенно при 73 и 95% RH. Смещение пиков на рентгенограммах F-I менее драматично, чем наблюдаемое смещение пиков в случае экспонирования F-III при различной относительной влажности. Это позволяет предположить, что решетка F-I не подвергается растяжению и/или уплотнению, как решетка F-III.
Обнаружено, что F-I и F-III стабильны в пределах всей области относительной влажности, несмотря на способность F-III сорбировать почти вдвое больше воды. Установлено, что две формы имеют сравнимые размеры кристаллов, морфологию, растворимость в воде и скорости растворения.
Проведено исследование высушивания, чтобы проследить десольватацию S-II как функцию времени и температуры высушивания (см. фиг.5). Во время эксперимента по десольватации получены рентгенограммы для различных временных точек. Большинство пиков дифракции, полученных при исследовании десольватации S-II, оказываются с углами, подобными F-I, подтверждая, что решетки S-II и F-I очень схожи. Исчезновение пиков дифракции приблизительно при 6,8; 7,2 и 14,0° при 2θ после только минимального высушивания позволяет предположить, что эти отражения могут быть отнесены к кристаллографическим плоскостям, вмещающим частичную плотность электронов молекул этилацетата.
Продолжительный отжиг под вакуумом сольватированного вещества при высоких температурах дает F-I. Полученный таким способом F-I показывает на рентгенограммах высокую степень кристалличности. Поэтому вещество, полученное кристаллизацией из раствора этанола и этилацетата с последующим высушиванием под вакуумом в течение только нескольких часов, как предложено в ‘474, проявляет очень низкую кристалличность, так как такой способ дает в результате частично десольватированный S-II.
F-I и F-III имеют некоторые преимущества перед вышеописанной формой арзоксифена предыдущего уровня техники. По сравнению с арзоксифеном, полученным с помощью способов, предложенных в ‘474, F-I и F-III являются более стабильными при температуре окружающей среды и поэтому оказываются более поддающимися фармацевтической обработке, то есть созданию дозированных композиций. Кроме того, F-I и F-III являются значительно более кристалличными, чем форма, описанная в ‘474. Кристаллические вещества обычно менее гигроскопичны и более стабильны (то есть менее склонны к химическому разрушению, сохраняют консистентные свойства), чем аморфные вещества, и поэтому являются более желательными для производства композиций. Кроме того, в отличие от формы арзоксифена, полученной способами, предложенными в ‘474, которая содержит в своей решетке этилацетат и воду, F-I и F-III содержат только воду.
Методы исследования
Измерения DSC проводили на приборах 2920 ТА, модулируемых DSC, присоединенных к тепловому анализатору 3100 и снабженных охлаждающей системой. Образцы (3-5 мг) нагревали в извитых алюминиевых резервуарах от 10 от 240°C при скорости нагревания 2°С/минуту.
Исследования TGA проводили на оборудовании 2050 ТА, термогравиметрическом анализаторе, присоединенном к тепловому анализатору 3100. Образцы (5-10 мг) нагревали в открытых резервуарах от 25 до 250°С при скорости нагревания 5°С/минуту.
Рентгенограммы получали на рентгеновском порошковом дифрактометре Siemens D5000, снабженном источником CuKα, (λ = 1,54056 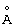 ), и Kervex-детектором твердого состояния, работающим при 50 кВ и 40 мА. Каждый образец сканировали между 4о и 35о при 2θ. Образцы оставляли для уравновешивания по крайней мере в течение 30 минут при требуемой температуре и/или относительной влажности до сбора данных.
), и Kervex-детектором твердого состояния, работающим при 50 кВ и 40 мА. Каждый образец сканировали между 4о и 35о при 2θ. Образцы оставляли для уравновешивания по крайней мере в течение 30 минут при требуемой температуре и/или относительной влажности до сбора данных.
Измерения гигроскопичности производили для F-I и F-III, используя метод VTI следующим образом. Каждый образец высушивали под вакуумом при 60°С до тех пор, пока не прекратилось выявление дальнейшей потери массы, за это время опытная камера была доведена до 0% относительной влажности. Изотермы сорбции влаги получены при 25°С с использованием вакуумных рычажных весов VTI со шкалой, проградуированной в процентах влажности, при следующих условиях: величина пробы 10-15 мг, область адсорбции/десорбции 0-95% относительной влажности, шаг интервала 5%, промежуток времени между отборами проб 10 минут.
Следующие примеры иллюстрируют способы получения гидрата согласно изобретению. Эти примеры никоим образом не являются ограничивающими объем защиты этих способов и не должны быть так истолкованы.
Примеры
Пример 1
F-III из 6-изопропокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена гидрохлорида
К раствору 6-изопропокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена гидрохлорида (10 г, 18 ммоль) в хлористом метилене (100 мл) в атмосфере азота при от -10 до -20°С добавлен ВСl3 (г) (4,23 г, 34 ммоль) со скоростью, которая поддерживает температуру реакции ниже -10°С. После окончания добавления реакционную смесь оставляли для перемешивания в течение дополнительных 2 часов. К реакционной смеси медленно был добавлен изопропиловый спирт (IPA, 12,35 мл, 167 ммоль) при температуре ниже -10°С, а перемешивание продолжали в течение 30 минут. Отдельную колбу заполняли 100 мл воды и охлаждали на ледяной бане приблизительно до 0°С. Раствор продукта переносили в воду с помощью канюли при энергичном перемешивании. Полученный белый шлам был оставлен для перемешивания при 0°С в течение 1 часа. Продукт извлекали фильтрованием и промывали 25 мл 40% СН2Сl2/вода, затем 25 мл холодной воды. Продукт суспендировали в 60 мл IPA и 60 мл воды и нагревали до 60°С. Раствор был получен при 48°С. Добавлена дополнительная вода (120 мл). Раствор оставляли для охлаждения до 35°С, и суспензию далее медленно охлаждали до 0-5°С и перемешивали в течение нескольких часов. Продукт изолировали фильтрованием и промывали холодной деионизованной водой (25 мл). Влажный осадок F-III высушивали до постоянного веса под вакуумом при 50°С в течение от 12 до 24 часов, чтобы получить F-III.
Пример 2
F-III из 6-бензилокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена-(S-оксида)
В 250 миллилитровую колбу Парра (Parr) вливали деионизованную воду (5,25 мл), 1М НСl (7,74 мл, 7,75 ммоль), 10% Pd/C (тип А32110, 1,37 г, 1,29 ммоль Pd), 6-бензилокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)-бенз[b]тиофен-(S-оксид) (3 г, 5,16 ммоль) и изопропиловый спирт (32 мл) при температуре окружающей среды. Колбу присоединяли к вибратору Парра, дважды последовательно откачивали газ и заполняли азотом и затем откачали газ и заполняли газообразным водородом до давления 30 фунтов на квадратный дюйм (1 фунт на кв.дюйм = 6,89476 кПа). Запускали вибратор, и реакционная смесь нагревалась до 60°С. Окончание реакции определяли с помощью ВЭЖХ-анализа приблизительно через 4 часа. Реакционную смесь отфильтровали через мягкую прокладку диатомной земли, и прокладку промывали 0,1 М НСl (2×10 мл). Растворитель удаляли под вакуумом приблизительно при 50°С. Полученный осадок был растворен в смеси 50% изопропиловый спирт/деионизованная вода (30 мл) и осторожно нагревался на паровой бане до тех пор, пока не был получен раствор. К раствору была добавлена деионизованная вода (22 мл), и раствор оставлен для охлаждения до температуры окружающей среды. Суспензия продукта далее охлаждалась до 0°С. Продукт был изолирован фильтрованием, промыт охлажденной деионизованной водой (2×15 мл) и высушен под вакуумом при 50°С до постоянного веса, чтобы получить F-III.
Пример 3
F-III из [6-изопропокси-3-[4-[2-(пиперидин-1-ил)этокси)фенокси]-2-(4-метоксифенил)]бенз[b]тиофена-(S-оксида)
Хлористый метилен (105 л) и [6-изопропокси-3-[4-[2-(пиперидин-1-ил)этокси)фенокси]-2-(4-метоксифенил)]-бенз[b]тиофен-(S-оксид) (10,5 кг) были смещены и охлаждены до от -15 до -20°С. Трихлорид бора (4,6 кг) добавлен для поддержания температуры реакции между -10° и -20°С. Перемешивание продолжали до тех пор, пока % площади пика исходного материала на ВЭЖХ не составил менее 1%. Система ВЭЖХ (4,6 мм внутренний диаметр × 25 см Zorbax SB-Phenyl колонка, 30°С, 70:30 метанол: 0,01 N серная кислота, скорость течения 1,5 мл/минуту; детектор 300 нм). Для поддержания температуры реакции между -10°С и -20°С был добавлен изопропанол (10,28 кг). Реакционная смесь перемешивалась в течение 30-45 минут. Неочищенный продукт реакции был выделен добавлением реакционной смеси к дополнительным 105 л воды, предварительно охлажденной до от 2 до 7°С для поддержания температуры реакции при 2 до 7°С. За добавлением следовала промывка хлористым метиленом (20 л), предварительно охлажденным до от 7 до 2°С. Кристаллический шлам перемешивали в течение от 2 до 3 часов и отфильтровывали и последовательно промывали хлористым метиленом (26 кг) и водой (53 л), предварительно охлажденными до от 7 до 2°С. Неочищенный влажный осадок смешивали с водой (42 л) и изопропанолом (40 л) и нагревали до от 65 до 70°С для достижения растворения. Горячий раствор фильтровали. Фильтрование проводили с промывкой, состоящей из смеси изопропанола (20 л) и воды (21 л), нагретых до 65-70°С, и промывкой, состоящей из воды (126 л), предварительно нагретой до 65-70°С. Раствор охлаждали до 40-45°С, вносили затравку кристаллизации и перемешивали при этой температуре в течение 2-3 часов, чтобы образовались кристаллы. Шлам осаждали до 0-5°С, перемешивали в течение 3-4 часов и фильтровали. Осадок на фильтре промывали водой (122,6 л), предварительно охлажденной до 2-7°С. Продукт высушивали под вакуумом при максимальной температуре 50°С до тех пор, пока изменение в весе осадка не составило менее 0,05 кг в течение 2-4 часов. Выход: 8,468 кг (87,3%). Эффективность ВЭЖХ: 98,5%. Вода по методу Карла Фишера: 3,0%. Всего вещества, связанного ВЭЖХ: 1,79%.
Пример 4
F-III из [6-бензилокси-3-[4-[2-(пиперидин-1-ил)этокси)фенокси]-2-(4-метоксифенил)]бенз[b]тиофена-(S-оксида)
Тетрагидрофуран (261 мл), воду (45 мл), концентрированную серную кислоту (6,14 г) и [6-бензилокси-3-[4-[2-(пиперидин-1-ил)этокси)фенокси]-2-(4-метоксифенил)]бенз[b]тиофена-(S-оксид) (емкость ВЭЖХ 99%, общий уровень вещества, связанного ВЭЖХ 0,35%), объединяли и перемешивали; до гомогенности. Добавляли 10% Pd/C (5,6 г суспендировали в 22 мл воды) с 5 мл водной промывки. Полученную суспензию отсасывали и оставляли под водородом при 60 фунтах на кв.дюйм (1 фунт на кв.дюйм = 6,89476 кПа). Температура реакции приведена к 30°С. Через 2 часа 10% Pd/C (5,6 г) дополнялся водой (30 мл). Гидрогенизация при 60 фунтах на кв. дюйм и 30°С продолжалась в течение дополнительных 22 часов. Добавляли дополнительные 4,40 г 10% Pd/C в 30 мл воды, а гидрогенизацию продолжали при 60 фунтах на кв.дюйм и 30°С в течение дополнительных 2,5 часов. Катализатор удаляли фильтрованием и рН фильтрата доводили до 7,24 50% гидроксидом натрия. Хлорид натрия (8,66 г), растворенный в воде (18 мл), был добавлен, и двухфазный раствор перемешивали в течение 30 минут. Фазы разделяли, и водную фазу снова экстрагировали 50 мл тетрагидрофурана. Органические фазы объединяли и концентрировали до объема 50 мл с помощью перегонки при атмосферном давлении. К концентрату при 24°С добавляли 180 мл метанола в течение 1-часового периода. Полученный кристаллический шлам перемешивали в течение 30 минут при 24°С, охлаждали до 0°С и перемешивали в течение 1 часа. Твердые вещества изолировали фильтрованием и промывали последовательно 39 мл воды и 39 мл метанола с последующей вакуумной сушкой в течение ночи при 50°С. Выход 15,52 г (67,8%).
Смешивали изопропанол (33 мл), воду (66 мл) и 10 г вышеописанного твердого вещества. К перемешиваемой смеси при 25°С добавили 1,8 М НСl (21 мл). Твердые вещества быстро растворяли с последующим переосаждением соли хлористоводородной кислоты. После перемешивания в течение 30 минут шлам нагревали до 70°С для растворения всех из твердых веществ. Раствор охлаждали до 60°С и добавляли 33 мл воды. Полученный раствор охлаждали до 25°С в течение 3-часового периода, во время которого осаждалась соль хлористоводородной кислоты. Шлам перемешивали приблизительно в течение 3 часов при 25°С, фильтровали, промывали водой (30 мл) и высушивали под вакуумом в течение ночи при 50°С, с выходом F-III 8,9 г (82,7%). Эффективность ВЭЖХ: 96,5%. Вода по методу Карла Фишера: 2,44%. Связанные ВЭЖХ вещества: 1,09%.
Использованная терминология
Используемый термин "эффективное количество" означает количество F-III, которое способно ингибировать заболевания или их пагубные воздействия, описанные в заявке. Когда F-III вводят одновременно с эстрогеном, прогестином, ингибитором ароматазы или ингибитором AChE, термин "эффективное количество" также означает количество такого агента, способное осуществить желаемое действие.
Термины "ингибирующий" и "ингибирует" подразумевают их общепринятые значения, то есть предупреждающий, препятствующий, ограничивающий, купирующий, уменьшающий интенсивность симптомов, замедляющий, останавливающий или реверсирующий прогрессирование или тяжесть патологического состояния или его осложнения, описанные в заявке.
Используемые термины "предупреждающий", "предупреждение", "профилактика", "профилактический" и "предотвращать" являются взаимозаменяемыми и подразумевают снижение вероятности, что у реципиента F-III останутся неизлечимыми или будут проявляться любые патологические состояния или их осложнения, описанные в заявке.
Термины "эстроген-дефицитный" и "недостаточность эстрогена" относятся к состоянию, или возникающему естественно или клинически индуцированному, когда женщина не может продуцировать достаточное количество эндогенных эстрогенных гормонов для поддержания эстроген-зависимых функций, например, менструальной функции, гомеостаза костной массы, нейронной функции, состояния сердечно-сосудистой системы и тому подобного. Такие эстроген-дефицитные состояния возникают во время менопаузы и в результате хирургической или химической овариэктомии, включая ее функциональный эквивалент, например, в результате лекарственной терапии ингибитором ароматазы, агонистами или антагонистами GnRH, ICI 182780 и тому подобным. Заболевания, связанные с недостаточностью эстрогена, включают в себя разрежение кости, остеопороз, сердечно-сосудистое заболевание и гиперлипидемию.
Используемый термин "эстроген" включает в себя стероидные соединения, характеризующиеся эстрогенной активностью, такие как 17β-эстрадиол, эстрон, конъюгированный эстроген (премарин; Premarin®), конский эстроген 17β-этинилэстрадиол и тому подобное. Предпочтительными соединениями на основе эстрогена являются премарин® и норэтилнодрел.
Используемый термин "прогестин" включает в себя соединения, проявляющие прогестероноподобную активность, такие, например, как прогестерон, норэтилнодрел, нонэстрел, мегестрол ацетат, норэтиндрон и тому подобные. Норэтиндрон является предпочтительным агентом на основе прогестерона.
Используемый термин "ингибитор ароматазы" включает в себя соединения, которые способны ингибировать ароматазу, например, такие коммерчески доступные ингибиторы, как аминоглутемид (цитандрен®; CYTANDREN®), анастразол (аримидекс®, ARIMIDEX®), летрозол (фемара®, FEMARA®)), форместан (ленатрон®, LENATRON®), эксеместан (аромасин®, AROMAS IN®), и тому подобное.
Используемый в описании термин "аналоги LHRH" относится к аналогам лютеинизирующего гормона рилизинг гормона, которые ингибируют продукцию эстрогена у женщин, находящихся в предклимактерическом периоде, и включают в себя, например, госерлин (золадекс®, ZOLADEX®), леупролид (лупрон®, LUPRON®) и тому подобное.
Используемый термин "ингибитор AChE" включает в себя соединения, которые ингибируют ацетилхолинэстеразу, например, физостигмина салицилат, такрина гидрохлорид, донепезила гидрохлорид и тому подобные.
Термин "активирует ChAT" подразумевает увеличение энзиматической активности ChAT, то есть ускорение превращения холина до ацетилхолина. Эта активация должна включать в себя увеличение эффективности и/или скорости реакции ChAT и холина и/или увеличение количества ChAT, присутствующего в районе действия. Это увеличение количества присутствующего фермента может быть обусловлено генной регуляцией или другой стадией синтеза при образовании фермента и/или уменьшением инактивации и метаболизма фермента.
Отдельные методы тестирования
Основной способ подготовки крыс: Самок крыс Sprague Dawley (диапазон от 200 до 255 г) в возрасте семидесяти пяти дней (если не указано особо) получали из лабораторий Charles River (Portage, MI). Животным проводили двустороннюю овариэктомию (OVX), или подвергали хирургической операции по Шаму (Sham) в лаборатории Charles River, а затем через одну неделю перевозили. По прибытии их размещали в металлические переносные клетки по группам из 3 или 4 животных на клетку и предоставляли свободный доступ к пище (содержание кальция приблизительно 0,5%) и воде в течение одной недели. Температура помещения поддерживалась при 22,2°С±1,7°С при минимальной относительной влажности 40%. Световой режим в помещении составлял 12-часовое освещение и 12-часовую темноту.
Схема дозирования и сбор ткани: После одной недели акклиматизации (поэтому две недели после OVX) начали ежедневное введение F-III. 17α-этинилэстрадиол или F-III давали перорально, если не указано особо, в виде суспензии в 1% карбоксиметилцеллюлозе или растворенными в 20% циклодекстрине. Животные получали дозы препарата ежедневно в течение 4 дней. После курса введения лекарственного средства животных взвешивали и анестезировали смесью кетамин: ксилазин (2:1, объем/объем) и в виде пунктата из сердца брали образцы крови. Животных затем умерщвляли асфиксией CO2, матку удаляли через срединный разрез и определяли влажный вес матки. 17α-этинилэстрадиол получали от Sigma Chemical Co., St. Louis, МО.
Сердечно-сосудистое заболевание/гиперлипидемия
Образцы крови, взятой у вышеупомянутых животных, оставляли для свертывания при комнатной температуре в течение 2 часов, и сыворотку получали после центрифугирования в течение 10 минут при 3000 оборотов в минуту. Холестерин сыворотки определяли, используя высокоэффективный анализ холестерина Boehringer Mannheim Diagnostics. Вкратце, холестерин окисляли до холест-4-ен-3-она и перекиси водорода. Затем перекись водорода взаимодействовала с фенолом и 4-аминофеназоном в присутствии пероксидазы с образованием п-хинониминового красителя, который определяли спектрофотометрически при 500 нм. Концентрацию холестерина затем рассчитывали по стандартной кривой. Все исследования автоматизировали, используя Biomek Automated Workstation.
Исследование пероксидазы эозинофилов матки
Матки от вышеупомянутых животных хранили при 4°С до момента исследования фермента. Матки гомогенизировали в 50 мМ трис-буфере (рН 8,0), содержащем 0,005% тритон Х-100. После добавления в трис-буфер 0,01% перекиси водорода и 10 мМ O-фенилендиамин (конечные концентрации) в течение одной минуты следили за увеличением поглощения при 450 нм. Присутствие эозинофилов в матке является показателем эстрогенной активности соединения. Определяли максимальную скорость 15-секундных интервалов в пределах начального, линейного отрезка реакционной кривой.
Способ тестирования ингибирования разрежения кости (остеопороза)
После проведения вышеописанной основной подготовки крыс обрабатывали ежедневно в течение тридцати пяти дней (6 крыс на группу и на 36-й день умерщвляли асфиксией двуокисью углерода. Тридцатипятидневного периода достаточно для достижения максимального снижения плотности кости, определяемого, как описано в заявке. Во время умерщвления матки удаляли, отслаивали инородные ткани, и жидкое содержимое выбрасывали перед определением влажного веса, для того чтобы подтвердить эстрогенную недостаточность, связанную с полной овариэктомией. Обычно в ответ на овариэктомию вес матки уменьшается приблизительно на 75%. Затем для проведения последующего гистологического анализа, матки помещали в 10% нейтральный забуференный формалин.
Правые бедренные кости иссекали и на периферическом метафизе получали дигитилизированную рентгенограмму и анализировали с помощью программы анализа изображения (NIH). Проксимальные части большеберцовых костей этих животных также сканировали с помощью количественной компьютерной томографии. В соответствии с вышеописанными способами, опытным животным перорально вводили F-III или этинилэстрадиол (ЕЕ2) в 20% гидроксипропил β-циклодекстрине. F-III также используется в комбинации с эстрогеном или прогестином.
Исследование пролиферации MCF-7
Клетки MCF-7 аденокарциномы молочной железы (АТСС НТВ 22) содержали в среде MEM (минимальная поддерживающая среда, без фенольного красного, Sigma, St. Louis, МО), дополненной 10% фетальной бычьей сывороткой (FBS) (объем/объем), L-глутамином (2 мМ), пируватом натрия (1 мМ), HEPES {(N-[2-гидроксиэтил]пиперазин-N’-[2-этансульфокислота] 10 мМ}, ненезаменимые аминокислоты и бычий инсулин (1 мкг/мл) (поддерживающая среда). За десять дней до исследования клетки MCF-7 переводили в поддерживающую среду, дополненную 10% покрытым декстрином древесным углем, захватывающим фетальную бычью сыворотку ((DCC-FBS) среда исследования) вместо 10% FBS, чтобы истощить внутренние накопления стероидов. Клетки MCF-7 удаляли из чашек с поддерживающей средой, используя клеточную диссоциирующую среду (Ca++/Mg++ без HBSS (без фенолового красного), дополненную 10 мМ HEPES и 2 мМ EDTA). Клетки дважды промывали аналитической средой и доводили до 80000 клеток/мл. Приблизительно 100 мл (8000 клеток) вносили в плоскодонные лунки микрокультуры (Costar 3596) и инкубировали при 37°С в 5% СО2 увлажненном инкубаторе в течение 48 часов, чтобы обеспечить клеточное сцепление и уравновешивание после переноса. Серии разведении лекарственных средств и DMSO, в качестве контроля, подготавливали в аналитической среде и 50 мл переносили в утроенные микрокультуры, с последующим добавлением 50 мл среды исследования до конечного объема 200 мл. После дополнительных 48 часов при 37°С в 5% СО2-инкубаторе, микрокультуры обрабатывали импульсной меткой тритированного тимидина (1 мкКи/лунка) в течение 4 часов. Культивирование завершали замораживанием при -70°С в течение 24 часов с последующим оттаиванием и сбором микрокультур, используя полуавтоматический коллектор клеток Skatron. Пробы считали в жидком сцинтилляторе, используя β-счетчик Wallac BetaPlace.
Ингибирование DМВА-индуцированной опухоли молочной железы
Эстроген-зависимые опухоли молочной железы получали у самок крыс Sprague-Dawley, которых покупали в Harlan Industries, Indianapolis, Indiana. Крысы в возрасте около 55 дней получали с однократным пероральным кормлением 20 мг 7,12-диметилбенз[а]антрацена (DMBA). Приблизительно через 6 недель после введения DMBA молочные железы пальпировали с недельными интервалами с целью выявления опухолей. Как только появлялась одна или больше опухолей, метрическим кронциркулем измеряли наибольший и наименьший диаметры каждой опухоли, регистрировали измерения, и таких животных отбирали для эксперимента. Предпринята попытка равномерно распределить опухоли различного размера между обрабатываемыми и контрольными группами так, чтобы опухоли среднего размера оказались равномерно распределенными между опытными группами. Контрольные и опытные группы для каждого эксперимента содержали от 5 до 9 животных.
F-III вводили или посредством внутрибрюшинной инъекции в 2% аравийской камеди, или перорально. Перорально вводимые соединения либо растворяли, либо суспендировали в 0,2 мл кукурузного масла. Каждую обработку, включая контрольные введения аравийской камеди и кукурузного масла, осуществляли один раз ежедневно каждому опытному животному. После первоначального измерения опухоли и отбора опытных животных опухоли измеряли каждую неделю с помощью вышеупомянутого способа. Обработку и обмер животных продолжали в течение от 3 до 5 недель, за время которых устанавливали конечные размеры опухолей. Для каждой обработки соединениями и для контрольных введений определяли изменение среднего размера опухоли.
Способы тестирования фиброза матки
Тест 1: Женщинам, в количестве между 3 и 20, страдающим фиброзом матки, вводили F-III. Количество вводимого соединения составляло от 0,1 до 1000 мг/день, а период введения составлял 3 месяца. Для выяснения влияния соединения на фиброз матки женщин наблюдали во время периода введения и вплоть до 3 месяцев после прекращения введения.
Тест 2: Использовали тот же способ, что в тесте 1, за исключением того, что период введения составлял 6 месяцев.
Тест 3: Использовали тот же способ, что и в тесте 1, за исключением того, что период введения составлял 1 год.
Тест 4: Для индукции лейомиомы у сексуально зрелых самок морских свинок применяли пролонгированную эстрогенную стимуляцию. Животным вводили эстрадиол в инъекциях 3-5 раз в неделю в течение 2-4 месяцев или до тех пор, пока не появлялись опухоли. Введения, состоящие из F-III или наполнителя, производили ежедневно в течение 3-16 недель, а затем животных умерщвляли, собирали матки и исследовали регрессию опухолей.
Тест 5: Ткань лейомиом человека имплантировали в брюшную полость и/или в миометрий матки половозрелой кастрированной самки бестимусной мыши. Экзогенный эстроген вводили, чтобы вызвать рост ткани эксплантата. В некоторых случаях собранные опухолевые клетки культивировали in vitro до имплантации. Обработку, состоящую из F-III или наполнителя, осуществляли промыванием желудка ежедневно в течение 3-16 недель, и имплантаты удаляли и оценивали рост или регрессию. Во время умерщвления крыс матки собирали, чтобы оценить состояние органа.
Тест 6: Получали ткань фиброзных опухолей и поддерживали in vitro в качестве первичных нетрансформированных культур. Операционные препараты пропускали через стерильную ячейку или сито или, альтернативно, с помощью иглы препарировали ткань от окружающих тканей, чтобы получить однородную клеточную суспензию. Клетки поддерживали в среде, содержащей 10% сыворотку и антибиотик. Определяли скорость роста в присутствии и в отсутствие эстрогена. Исследовали способность клеток продуцировать С3-компонент комплемента и их ответ на факторы роста и ростовые гормоны. In vitro оценивали пролиферативный ответ культур после обработок прогестинами, GnRH, F-III и наполнителями. Еженедельно определяли уровни рецепторов стероидных гормонов, чтобы выяснить, сохраняются ли in vitro важные клеточные свойства. Использовали ткань от 5-15 пациентов.
Тест 7: Определяли способность F-III ингибировать стимулируемую эстрогеном пролиферацию линий клеток ELT, полученных из лейомиомы, как описано Fuchs-Young, et al., "Inhibition of Estrogen-Stimulated Growth of Uterine Leiomyomas by Selective Estrogen Receptor Modulators" Mol. Car., 17(3):151-159 (1996), рекомендации которого включены в описание цитированием.
Способ тестирования эндометриоза
Тест 1: В качестве опытных животных использовали от двенадцати до тридцати взрослых самок крыс CD линии. Крыс разделили на три равные группы. У всех животных контролировали эстральный цикл. В день предтечки на каждой самке проводили операцию. У самок каждой группы удаляли левый рог матки, рог разрезали на небольшие квадратные кусочки, и эти квадраты произвольно пришивали в различных участках, прилегающих к мезентериальному кровотоку. Кроме того, самкам группы 2 удаляли яичники. Со дня после операции животным 1 и 2 производили внутрибрюшинные инъекции воды в течение 14 дней, тогда как животным группы 3 осуществляли внутрибрюшинные инъекции 1,0 мг F-III на килограмм веса тела в течение такого же периода времени. После 14 дней обработки каждую самку умерщвляли и удаляли эндометриальные эксплантаты, надпочечники, оставшуюся часть матки и яичники, что возможно, и подготавливали для гистологического исследования. Яичники и надпочечники взвешивали.
Тест 2: В качестве опытных животных использовали от двенадцати до тридцати взрослых самок крыс линии CD. Крыс делили на две одинаковые группы. Контролировали астральный цикл всех животных. В день предтечки каждой самке проводили операцию. У самок каждой группы удаляли левый рог матки, который разрезали на квадратные кусочки, и квадраты произвольно пришивали в различных участках, прилегающих к мезентериальному кровотоку. Приблизительно через 50 дней после операции животным группы 1 делали внутрибрюшинные инъекции воды в течение 21 дня, в то время как животным из группы 2 делали внутрибрюшинные инъекции 1,0 мг F-III на килограмм веса тела в течение такого же периода времени. После 21 дня обработки каждую самку умерщвляли, а эксплантаты эндометрия и надпочечники удаляли и взвешивали. Эксплантаты оценивали как показатель роста. Эстральные циклы контролировались.
Тест 3: Для индукции эндометриоза у крыс и/или кроликов использовали аутотрансплантат ткани эндометрия. Репродуктивно зрелых самок животных подвергали двусторонней овариэктомии, а эстроген возмещали экзогенно, обеспечивая таким образом определенный и постоянный уровень гормона. Аутогенную и обеспечивали эстрогеном, чтобы вызвать рост эксплантированной ткани. Обработку, состоящую из соединения данного изобретения, производили посредством промывания желудка ежедневно в течение 3-16 недель, имплантаты удаляли и оценивали рост или регрессию. Во время умерщвления брали интактный рог матки, чтобы оценить состояние эндометрия.
Тест 4: Ткань из патологических участков эндометрия человека имплантировали в брюшину половозрелых самок бестимусных мышей. Обеспечивали экзогенным эстрогеном, чтобы вызвать рост эксплантированной ткани. В некоторых случаях собранные клетки эндометрия культивировали in vitro до имплантации. Обработку, состоящую из F-III, производили с помощью промывания желудка ежедневно в течение 3-16 недель, имплантаты удаляли и определяли рост или регрессию. Во время умерщвления удаляли матку, чтобы оценить состояние интактного эндометрия.
Тест 5: Ткань из участков повреждения эндометрия человека собирали и содержали in vitro в качестве первичных нетрансформированных культур. Операционные препараты пропускали через стерильную ячейку или сито или, альтернативно, препарировали ткань от окружающих тканей, чтобы получить суспензию из клеток одного типа. Клетки поддерживали в среде, содержащей 10% сыворотку и антибиотик. Определяли скорость роста в присутствии и в отсутствие эстрогена. Исследовали способность клеток продуцировать С3 компонент комплемента, а также ответ клеток на факторы роста и ростовые гормоны. In vitro после обработки прогестинами, GnRH, F-III и наполнителем оценивали пролиферативный ответ GnRH, F-III и наполнителем оценивали пролиферативный ответ культур. Еженедельно определяли уровни рецепторов стероидных гормонов для выяснения того, сохраняются ли in vitro важные свойства клеток. Использовали ткань от 5-25 пациентов.
Расстройства ЦНС, включая болезнь Альцгеймера
Эстрогены такие, как 17β-эстрадиол регулируют генную транскрипцию посредством связывания с эстрогенными рецепторами (ER), которые находятся в цитоплазме определенных популяций клеток. Лигандная активация ER является предпосылкой для транспорта комплекса в ядро, где связывание с согласованной последовательностью 13 пар оснований палиндромной ДНК (элемент ответ эстрогена, или ERE) запускает процесс сборки транскрипционного аппарата, который достигает своей кульминации при активации соответствующих генов-мишеней. Идентифицировано множество генов, которые регулируются эстрогенами. Они включают в себя белки цитоскелета, ферменты биосинтеза нейротрансмиттеров и ферменты метаболизма и рецепторы, а также другие гормоны и нейропептиды. Элементы ERE идентифицированы во многих эстроген-позитивных генах, включая вителлогенин, c-fos, пролактин и лютеинизирующий гормон.
Имеющие большое значение для центральной нервной системы ERE-подобные последовательности были идентифицированы в p75ngr и trkA, обе из которых служат сигнальными молекулами для нейротрофинов: фактора роста нервов (NGF), произведенного из головного мозга нейротрофического фактора (BDNGF), и нейротрофин-3.
Показано, что BDNF, так же, как и NGF, повышают жизнеспособность холинэргических нейронов в культуре. Полагают, что взаимодействие между нейротрофинами и эстрогенами является важным для развития и выживаемости базальных нейронов переднего мозга (которые дегенерируют при болезни Альцгеймера) при тех клинических состояниях, при которых недостаточность эстрогена (постклимактерический период) может привести к потере этих нейронов.
Следующий эксперимент проводили на овариэктомированных крысах (подготовленных, как описано выше) для того, чтобы выявить сходство или различие во влиянии F-III и эстрогена на экспрессию гена в различных областях мозга. Крысам в возрасте шести недель ежедневно вводили с помощью подкожных инъекций эстрадиол бензоат (0,03 мг/кг), F-III или наполнитель (контроль). После пяти недель обработки животных умерщвляли, удаляли мозг и микродиссекцией собирали гиппокамп. Гиппокамп быстро замораживали в жидком азоте и хранили при -70°С. Общую ДНК получали из объединенной ткани животных из групп соответствующих обработок и контрольной группы и обратно транскрибировали, используя 3’-олигонуклеотидный праймер, который выбирали для популяций специфических РНК (поли-А+). Полимеразные цепьевые реакции (PCR) проводили в коктейле, состоящем из: произвольных 5’-олигонуклеотидов (длиной 10 пар оснований; всего 150), реакционного буфера. Tag полимеразы и 32PdTCP.
После 40 циклов амплификации продукты реакции фракционировали по размеру в 6% ТВЕ-мочевина геле, высушивали и экспонировали на рентгеновской пленке. Полученные картины распределения мРНК сравнивали между группами.
Применение F-III вместе с эстрогеном
Известно, что женщин в пери- и постклимактерическом периоде часто подвергают гормональной заместительной терапии (HRT), чтобы преодолеть негативные последствия, связанные со снижением в циркуляции эндогенного эстрогена, например, для лечения приступообразного ощущения жара. Однако HRT может быть связана с повышенным риском возникновения определенных раков, включая рак матки и молочной железы. F-III можно применять вместе с HRT для ингибирования этих процессов.
Применение F-III вместе с ингибитором ароматазы
По определению, у женщин в постклимактерическом периоде яичники не функционируют. Единственным источником эстрогенов у них является превращение андрогенов надпочечников до эстрогена с помощью ферментов ароматазы, который обнаружен в периферических тканях (включая жировую ткань, мышцы и саму опухоль молочной железы). Так, лекарственные средства, которые ингибируют ароматазу (ингибиторы ароматазы), истощают циркулирующий эстроген у женщин в постклимактерическом периоде. Истощение эстрогена путем ингибирования ароматазы является важной возможностью при лечении пациентов, страдающих метастатическим раком молочной железы. Во время лечения ингибитором ароматазы отсутствие циркулирующего эстрогена может оказывать негативные, не предполагаемые побочные воздействия, например, на уровень липидов в сыворотке. Для предупреждения этих негативных воздействий можно применять F-III.
Применение F-III вместе с аналогом LHRH
Длительное воздействие аналогом LHRH (лютеинизирующий гормон рилизинг гормон способствует ингибированию продукции эстрогена у женщин в преклимактерическом периоде, десенсибилизируя гипофизарную железу, которая потом больше не стимулирует яичники к продукции эстрогена. Клиническим эффектом является "лекарственная овариэктомия", которая является обратимой при отмене аналога LHRH. Во время лечения аналогом LHRH отсутствие циркулирующего эстрогена может быть причиной негативных, не предполагаемых побочных эффектов, например, влияние на уровни липидов сыворотки. F-III может применяться для ингибирования этих негативных эффектов.
Увеличение уровней ацетилхолина
Известно, что у пациентов с болезнью Альцгеймера. значительно ниже уровень холинэргических нейронов в гиппокампе, чем у их ровней, не страдающих этим заболеванием. Оказалось, что прогрессивная потеря этих холинэргических нейронов отражает потерю памяти и познавательной функции у таких пациентов. Полагают, что причиной снижения количества этих нейронов является утраченная или сниженная функция нейротрансмиттера ацетилхолина.
Уровень ацетилхолина в нейроне по существу определяют по тому, куда изменяется равновесие между биосинтезом и биодеградацией. Фермент холин-ацетилтрансфераза (ChAT) главным образом ответственен за синтез ацетилхолина, а ацетилхолинэстераза (AChE) - за его дегенерацию.
Для того, чтобы изучить влияние F-III на уровни ChAT проводили следующий эксперимент: после описанной выше обычной подготовки крыс, 40 крысам ежедневно вводили путем подкожной инъекции и перорального кормления через желудочный зонд 3 мг/кг/день F-III в наполнителе, содержащем 10% циклодекстрин, эстрадиол бензоат в количестве 0,03 или 0,3 мг/кг/день, или контроль наполнителя. Животных обрабатывали в течение 3 или 10 дней. Использовали двенадцать животных на каждую схему приема лекарственного средства. Через соответствующие интервалы времени животных умерщвляли и вскрывали их мозг. Определенные порции мозга гомогенизировали и анализировали.
Гомогенаты гиппокампа и лобной части коры мозга обрабатывали и проводили определение активности ChAT, путем анализа радиоактивности биосинтеза ацетилхолина. Этот метод может быть обнаружен в J. Neural Transmiss, 78:183-193, 1989, описание которого включено в виде ссылки.
Как предполагали, у OVX-животных уровни ChAT снижены на >50% (р<0,001) по сравнению с фиктивно оперированными контролями.
В другом аспекте данного изобретения F-III применяли в комбинации с ингибитором AChE. Применение ингибитора AChE приводило к повышению уровней ацетилхолина за счет блокирования его деградации через ингибирование AChE.
Доброкачественная гиперплазия простаты (ВРН)
Предыстория вопроса относительно связи между действием эстрогена и лечением ВРН и карциномы простаты изложена в международной заявке РСТ WO 98/07274, дата международной публикации: 15 октября, 1998.
В экспериментах, описанных ниже, оценивали способность F-III связывать рецепторы эстрогена на нескольких линиях клеток рака простаты человека.
Лизаты линий клеток LNCaP, DU-45 и РС-3 рака простаты человека готовили в среде TGE, содержащей 50 нМ трис-HCl, рН 7,4, 1,5 мМ этилендиаминтетрауксусную кислоту (EDTA), 0,4 М КСl, 10% глицерин, 0,5 мМ 2-МЕ и 10 мМ молибдата натрия, кроме того содержащей ингибиторы протеаз пепстатин (1 мг/мл), лейпептин (2 мг/мл) апротинин (5 мг/мл) и фенилметилсульфонилфторид (PMSF, 0,1 мМ) (TEGP).
Клеточные лизаты центрифугировали и осадок ресуспендировали в холодной TEGP (1 мл TEGP/100 мг осадка) и разрушали ультразвуком в течение 30 секунд (нагрузка цикла 70%, мощность 1,8) на ультразвуковой установке Branson, модель 450. Лизаты осаждали центрифугированием при 10000 × g в течение 15 минут при 4°С, после чего супернатант отделяли и либо использовали немедленно, либо хранили при -70°С.
Исследование конкурентного связывания: В качестве связывающего буфера использовали TEG, в котором 0,4 М КСl заменили 50 мМ NaCl и в который к тому же добавили 1 мг/мл овальбумина (TEGO). F-III разбавляли до 20 нМ в TEGO, из которого готовили 3-кратные серийные разведения. Исследования проводили в круглодонных полипропиленовых микропланшетах в утроенных микролунках. В каждую лунку помещают 35 мл меченного тритием 17β-эстрадиола (0,5 нМ, удельная активность 60,1 Ки/ммоль, DuPont-New England Nuclear, Boston, MA) и 35 мл охлажденного опытного соединения (0,1 нМ 5 мМ) или TEGO, после инкубации в течение 5 минут при 4°С при встряхивании добавляли 70 мл лизата линии MCF-7 клеток.
Планшеты инкубировались в течение 24 часов при 4°С, после этого в каждую лунку добавляли 70 мл покрытого декстраном древесного угля (DCC) с последующим энергичным встряхиванием в течение 8 минут при 4°С. Планшеты затем центрифугировали при 1500 × g в течение 10 минут при 4°С. Супернатант отбирали из каждой лунки в гибкий полистироловый микропланшет для сцинтилляционного подсчитывания в счетчике Wallac Micobeta Model 1450. Радиоактивность выражали как распад/минуту (DPM) после корректировки на эффективность счета (35-40%) и фон. Дополнительными контролями служили общий счет и общий счет + DCC, чтобы определить нижний предел DCC-экстрагируемого счета. Результаты этого конкурентного связывания выражали как средний процент связывания (% связывания) +\- стандартное отклонение, используя формулу:

Предупреждение рака молочной железы
Данное изобретение также относится к введению F-III реципиенту, который принадлежит к группе риска возникновения de novo рака молочной железы. Термин "de novo" прежде всего означает отсутствие трансформации или перерождения нормальных клеток молочной железы в раковые или злокачественные клетки. Такая трансформация может происходить по стадиям в тех же самых или дочерних клетках через эволюционный процесс, или может происходить как отдельный центральный процесс. Этот процесс de novo отличается от метастазирования, колонизации или распространения уже трансформированных или злокачественных клеток из первичной опухоли в новые участки локализации.
Человек, который не относится к группе повышенного риска появления рака молочной железы, является тем, у кого может возникнуть de novo рак молочной железы, у кого нет никаких симптомов или сомнений относительно вероятности заболевания вне обычного риска и у кого никогда не было диагностировано заболевание. Наивысшим фактором риска, предполагающим развитие карциномы молочной железы, является анамнез жизни страдающего этим заболевание или наличие предшествующего проявления заболевания, даже если в настоящее время имеется ремиссия без каких-либо симптомов его наличия. Другим фактором риска является наличие заболевания в семейном анамнезе.
Индукция опухолей молочной железы у крыс введением канцерогена N-нитрозо-N-метилмочевины является хорошо известной животной моделью для изучения рака молочной железы и считается подходящей для анализирования действия химиотерапевтических агентов.
В двух отдельных исследованиях самкам крыс Sprague-Dawley в возрасте 55 дней внутривенно (исследование 1) или внутрибрюшинно (исследование 2) вводили дозу 50 мг N-нитрозо-N-метилмочевины на килограмм веса тела за одну неделю до кормления со свободным доступом к пище, в которую примешивали варьирующие количества F-III (Z)-2-[4-(1,2-дифенил-1-бутенил)фенокси]-N,N-диметилэтанамина, основания (основание тамоксифена), или контроль.
В исследовании 1 пищевые дозы 60 мг/кг еды и 20 мг/кг еды переводили к грубо сравнимые дозы 3 и 1 мг/кг веса тела для каждого животного.
В исследовании 2 пищевые дозы 20, 6, 2 и 0,6 мг/кг еды переводили в грубо сравнимые дозы 1; 0,3; 0,1 и 0,03 мг/кг веса тела для опытных животных.
Крыс наблюдали на предмет проявлений токсичности, и раз в неделю взвешивали и пальпировали для определения образования опухоли. Через тринадцать недель (исследование 1) или восемнадцать недель (исследование 2) животных умерщвляли, при аутопсии подтверждали наличие опухоли и взвешивали.
Композиции
Термин "фармацевтический", используемый как прилагательное, по существу означает невредный для реципиента млекопитающего. Под термином "фармацевтическая композиция" имеют в виду, что носитель, разбавитель, наполнители и активный ингредиент(ы) должны быть совместимыми с другими ингредиентами композиции и не быть вредными для реципиента.
Предпочтительно, F-III вносили в композиции до введения. Выбор композиции должен быть сделан наблюдающим врачом с учетом тех же факторов, что включены в определение эффективного количества.
Суммарные активные ингредиенты в такой композиции содержат от 0,1% до 99,9% веса композиции. Предпочтительно не более двух активных ингредиентов включают в названную композицию. Так, предпочтительным является включение в состав композиции F-III вместе с другим активным ингредиентом, выбранным из эстрогена, прогестина, ингибитора ароматазы, аналога LHRH и ингибитора АСnЕ. Наиболее предпочтительными композициями являются такие, в которых F-III оказывается единственным активным ингредиентом.
Фармацевтические композиции данного изобретения готовили с помощью способов, известных в данной области, используя хорошо известные и легко доступные ингредиенты. Например, F-III, либо сам по себе, либо в комбинации с эстрогеном, прогестином, ингибитором ароматазы, аналогом LHRH или ингибитором AChE, готовили с обычными наполнителями, разбавителями или носителями и формировали в таблетки, капсулы, суспензии, растворы, инъецируемые композиции, аэрозоли, порошки и тому подобное.
Фармацевтические композиции этого изобретения для парентерального введения содержат стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки, которые реконструируют непосредственно перед применением в стерильных растворах или суспензиях. Примеры приемлемых стерильных водных и неводных носителей, разбавителей или наполнителей включают в себя воду, физиологический солевой раствор, этанол, полиолы (такие, как глицерин, пропиленгликоль, поли(этиленгликоль) и тому подобное), и их приемлемые смеси, растительные масла (такие как оливковое масло) и инъецируемые органические эфиры, такие как этилолеат. Надлежащую текучесть поддерживали, например, применением покрывающих материалов, таких как лецитин, созданием надлежащего размера частиц в случае дисперсий и суспензий и использования поверхностно-активных веществ.
Парентеральные композиции также могут содержать адъюванты, такие как консерванты, смачивающие агенты, эмульгаторы и диспергаторы. Предотвращение действия микроорганизмов обеспечивали включением антибактериальных и противогрибковых агентов, например, парааминобензойной кислоты, хлорбутанола, фенолсорбиновой кислоты и тому подобного. Также желательно включение изотонических агентов, таких как сахара, хлорид натрия и тому подобного. К пролонгированной абсорбции инъецируемых композиций приводило включение агентов, которые замедляют абсорбцию, таких как моностеарат алюминия и желатин.
В некоторых случаях для пролонгирования действия лекарственного средства желательно замедлить абсорбцию лекарства после подкожной или внутримышечной инъекции. Этого можно достичь использованием жидкой суспензии кристаллического вещества с низкой растворимостью или растворением или суспендированием лекарственного средства в масляном растворителе. В случае подкожной или внутримышечной инъекции суспензии, содержащей форму лекарственного средства с низкой растворимостью в воде, скорость абсорбции лекарства зависит от скорости его растворения.
Инъецируемые "депонируемые" композиции F-III получали формированием микроинкапсулированных матриц лекарственного средства в биодеградируемых полимерах, таких как поли(молочная кислота) поли(гликолевая кислота), сополимеры молочной и гликолевой кислот, поли(ортоэфиры) и поли(ангидриды) этих веществ, описанные в данной области. В зависимости от соотношения лекарственного средства и полимера и свойств отдельного употребляемого полимера, можно контролировать скорость высвобождения лекарственного средства.
Инъецируемые композиции стерилизуют, например, фильтрованием через антибактериальные фильтры или предварительной стерилизацией соединений смеси перед их смешиванием, или во время производства, или непосредственно перед введением (как в двухкамерном шприце-упаковке).
Твердые дозированные формы для перорального введения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах F-III смешивают по крайней мере с одним инертным фармацевтическим носителем, таким, как хлорид натрия или вторичный кислый фосфат кальция, и/или (а) сухими разбавителями, такими как крахмалы, сахара, включая лактозу и глюкозу, маннит и кремниевую кислоту, (b) связывающими агентами, такими как карбоксиметилцеллюлоза и другие производные целлюлозы, альгинаты, желатин, поли(винилпирролидин), сахароза и аравийская камедь, (с) увлажнителями, такими как глицерин, (d) диспергаторами, такими, как агар-агар, углекислый кальций, двууглекислый натрий, картофельный или крупяной крахмал, альгиновая кислота, силикаты и углекислый натрий, (е) увлажняющими агентами, такими как глицерин; (f) агентами, препятствующими растворению, такими как парафин; (g) усиливающими абсорбцию агентами, такими как соединения четвертичной соли аммония; (h) смачивающими веществами, такими как цетиловый спирт и моностеарат глицерина и (j) смазками, такими как тальк, стеарат кальция, твердые поли(этиленгликоли), лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль дозированные формы также могут содержать забуферивающие агенты.
Твердые композиции подобного типа могут также содержать начинку для мягких и твердых желатиновых капсул, используя наполнители, такие как лактоза, а также высокомолекулярные поли(этиленгликоли) и тому подобное.
Твердые дозированные формы, такие как таблетки, драже, капсулы, пилюли и гранулы также можно производить с покрытиями или оболочками, такими как энтерические покрытия или другие покрытия, хорошо известные в области технологии приготовления лекарственных средств. Покрытия могут содержать агенты, делающие вещества непрозрачными, или агенты, которые высвобождают активный ингредиент(ы) в определенном участке пищеварительного тракта как, например, кислоторастворимые покрытия для высвобождения активного ингредиента(ов) в желудке или щелочерастворимые покрытия для высвобождения активного ингредиента(ов) в кишечном тракте.
Активный ингредиент(ы) также может быть микроинкапсулирован в затрудняющем высвобождение покрытии, при этом микрокапсулы оказываются частью таблеточного или капсульного образования.
Жидкие дозированные формы F-III для перорального введения включают в себя раствор, эмульсии, суспензии, сиропы и эликсиры. Кроме активных соединений жидкие композиции могут включать в себя инертные разбавители, обычно используемые в данной области, такие как вода или другие фармацевтические растворители, солюбилизирующие вещества и эмульгаторы, такие, как этанол, изопропанол, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, масло семян, оливковое, касторовое и сезамовое масло), глицерин, тетрагидрофурфуриловый спирт, поли(этиленгликоли), эфиры жирных кислот сорбита и их смеси.
Кроме инертных разбавителей, жидкие пероральные композиции также могут включать в себя адъюванты, такие как смачивающие вещества, эмульгаторы и суспендирующие агенты и подслащивающие, вкусовые и ароматизирующие вещества.
Жидкие суспензии, кроме активного ингредиента(ов) могут содержать суспендирующие агенты, такие как этоксилированные изостеарильные спирты, полиоксиэтиленсорбит и эфиры сорбитана, микрокристаллическую целлюлозу, метагидроокись алюминия, бентонитную глину, агар-агар и трагакант и их смеси.
Композиции для ректального или интравагинального введения получены смешиванием F-III с подходящими не вызывающими раздражения наполнителями, такими как масло какао, полиэтиленгликоль или любой суппозиторный воск, который оказывается твердым при комнатной температуре, но жидким при температуре тела и поэтому плавится в прямой кишке или в полости влагалища с высвобождением активного соединения(ий). Соединения были растворены в расплавленном воске, сформированы в требуемую форму и оставлены для затвердевания в окончательную суппозиторную композицию.
F-III также может быть введен в форме липосом. Как известно в данной области, липосомы обычно получают из фосфолипидов или других липидных веществ. Липосомные композиции образуются посредством моно- и мультислойных гидратированных жидких кристаллов, которые диспергируют в водной среде. Можно использовать любой нетоксичный фармацевтический и метаболизирующий липид, способный образовывать липосомы. Данные композиции в липосомной форме могут содержать, кроме F-III, стабилизаторы, наполнители, консерванты и тому подобное. Предпочтительными липидами являются фосфолипиды и фосфатидилхолины (лецитины) как природные, так и синтетические.
Способы образования липосом известны в данной области и описаны, например, у Prescott, Ed., Methods in Cell Biology, Volume XIV, Academic Press, New York, N.Y. (1976), p. 33 и последующие.
Следующие примеры композиций только иллюстрируют данное изобретение и не предназначены для его ограничения.
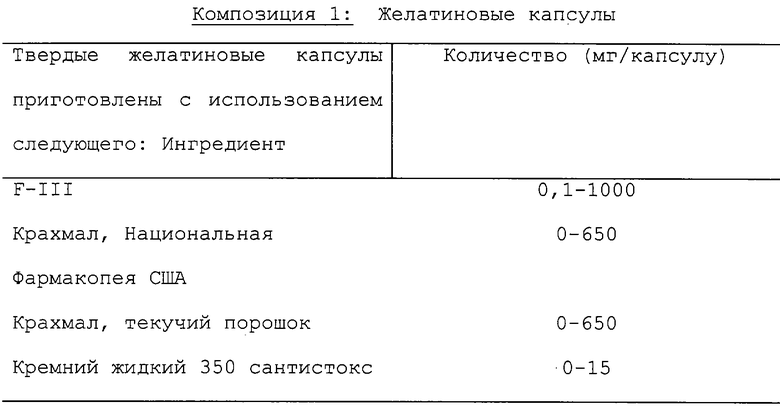
Вышеупомянутая композиция может быть изменена в соответствии с предлагаемыми обоснованными изменениями.
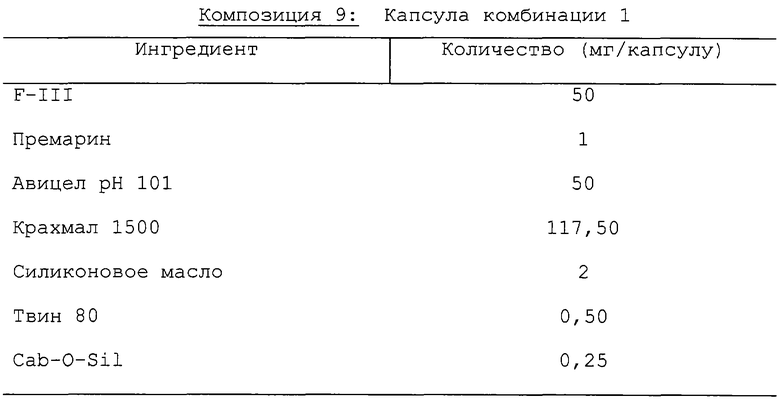
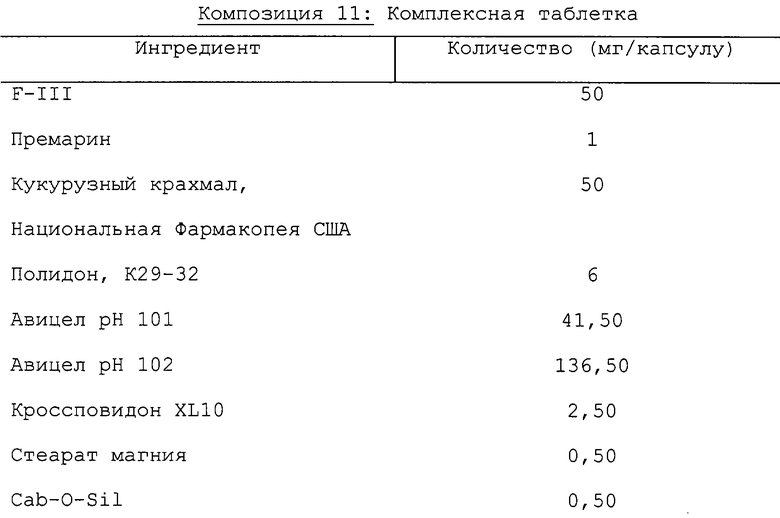
Таблеточная композиция получена с использованием приведенных ниже ингредиентов.

Компоненты смешивают и прессуют с образованием таблеток.

Соединения смешивались и прессовались с образованием таблеток.
Альтернативно, таблетки, каждая содержащая 2,5-1000 мг F-III, составлялись следующим образом:

F-III, крахмал и целлюлоза пропускались через сито US №45 меш. и энергично смешивались. Раствор поливинилпирролидона смешивался с полученными порошками, которые затем пропускались через сито US №14 меш. Полученные так гранулы высушивались при 50-60°С и пропускались через сито US №18 меш. Натрийкарбоксиметил крахмал, стеарат магния и тальк, предварительно пропущенные через сито US №60 меш., затем добавлялись к гранулам, которые, после смешивания, прессовались на машине для изготовления таблеток с образованием таблеток.
Суспензии, каждая содержащая 0,1-1000 мг лекарственного средства на 5 мл дозированной формы, производились следующим образом:
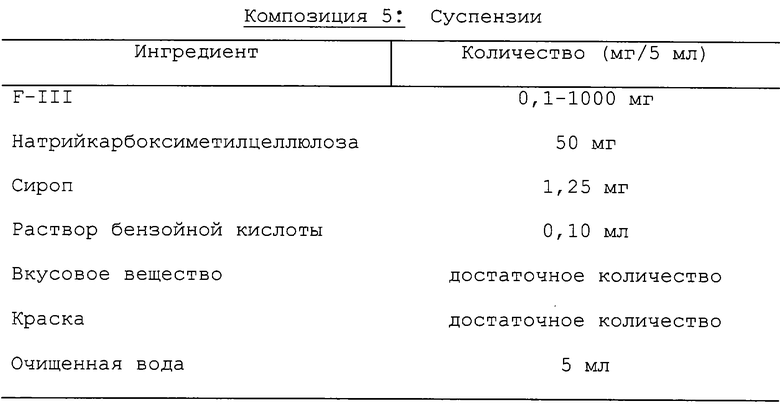
Лекарственное средство пропускалось через сито US №45 меш. и смешивалось с натрийкарбоксиметилцеллюлозой и сиропом с образованием однородной пасты. Раствор бензойной кислоты, вкусовое вещество и краска разбавлялись некоторым количеством воды и добавлялись при перемешивании. Затем добавлялось достаточное количество воды, чтобы получить требуемый объем.
Получали аэрозольные растворы, содержащие следующие ингредиенты.
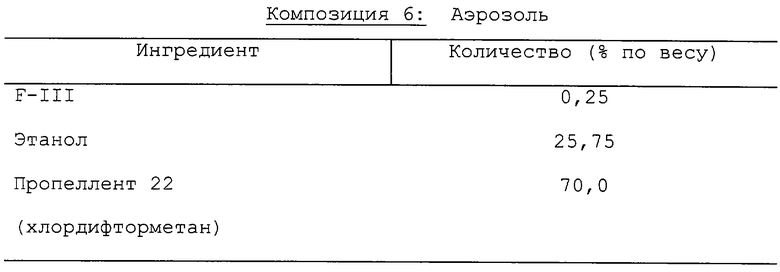
F-III смешивался с этанолом, и смесь добавлялась к порции пропеллента 22, охлаждалась до 30°С и переносилась в заполняющее устройство. Затем требуемое количество подавалось в нержавеющий стальной контейнер и разбавлялось оставшимся пропеллентом. Вентильное устройство затем монтировалось к контейнеру.
Суппозитории готовились следующим образом:

F-III пропускался через сито US №60 меш. И суспендировался в глицеридах насыщенных жирных кислот, предварительно расплавленных, используя минимально необходимое нагревание. Смесь затем заливалась в суппозиторную форму с номинальной емкостью 2 г и оставлялась для охлаждения.
Внутривенная композиция была получена следующим образом.

Раствор вышеупомянутых ингредиентов вводится внутривенно пациенту со скоростью приблизительно 1 мл за минуту.

Система доз
Определенная доза F-III, вводимая согласно изобретению, устанавливается в соответствии с особыми обстоятельствами, сопутствующими каждой ситуации. Эти обстоятельства включают в себя способ введения, предшествующую историю болезни, патологическое состояние или симптом, требующие лечения, тяжесть заболевания/симптома, требующего лечения, и возраст и пол реципиента.
Обычно эффективная минимальная ежедневная доза F-III составляет приблизительно 1, 5, 10, 15 или 20 мг. Эффективная максимальная доза составляет приблизительно 800, 100, 60, 50 или 40 мг. Наиболее типично, доза колеблется между 15 мг и 60 мг. Точная доза может быть установлена в соответствии с стандартным правилом в медицинской практике "дозового титрования" реципиента, которое заключается в первоначальном введении низкой дозы соединения и в постепенном увеличении ее до тех пор, пока не будет наблюдаться желаемое терапевтическое действие.
Хотя может быть необходимым проведение дозового титрования реципиента в отношении обсуждаемых выше комбинированных терапий, типичными дозами активных ингредиентов, помимо F-III, оказываются следующие: Этинилэстроген (0,01-0,03 мг/день), местранол (0,05-0,15 мг/день), конъюгированные эстрогенные гормоны (например, премарин®, Premarin®, Wyeth-Ayerst; 0,3-2,5 мг/день), медроксипрогестерон (2,5-10 мг/день), норэтилнодрел (1,0-10,0 мг/день), нонэтиндрон (0,5-2,0 мг/день), аминоглутемид (250-1250 мг/день, предпочтительно 250 мг четыре раза в день), анастразол (1-5 мг/день, предпочтительно 1,0 мг в день). Летрозол (2,5-10 мг/день, предпочтительно 2,5 мг один раз в день), форместан (250-1250 мг в неделю, предпочтительно 250 мг дважды в неделю), эксеместан (25-100 мг/день, предпочтительно 25 мг один раз в день), госерлин (3-15 мг/три месяца, предпочтительно 3,6-7,2 мг один раз в три месяца) и леупролид (3-15 мг/месяц, предпочтительно 3,75-7,5 мг один раз каждый месяц).
Способ введения
F-III может быть введен с помощью целого ряда способов, включающих в себя пероральный, ректальный, чрескожный, подкожный, внутривенный, внутримышечный и интраназальный.
Способ введения каждого эстроген- и прогестин-содержащего агента соответствует способу, который известен в данной области. F-III, один или в комбинации с эстрогеном, прогестином или ингибитором АСпЕ, обычно вводят в подходящей композиции.
Фармацевтические композиции этого изобретения можно вводить человеку и другим млекопитающим (например, собакам, кошкам, лошадям, свиньям и тому подобным) перорально, ректально, интраназально, парентерально, местно, трансбуккально или подъязычно или назально. Термин "парентеральное введение" относится к способам введения, которые включают в себя внутривенную, внутрибрюшинную, интрастерильную или внутрисуставную инъекцию или инфузию.
Способ/продолжительность введения
Для большинства из способов данного изобретения F-III вводится постоянно от 1 до 3 раз ежедневно или так часто, как необходимо, чтобы обеспечить реципиента эффективным количеством. Циклическая терапия может быть полезной особенно при лечении эндометриоза или может быть высокоэффективной для лечения болезненных приступов заболевания. В случае рестеноза терапия может быть ограничена краткими (1-6 месяцев) интервалами после лечебных манипуляций, таких как ангиопластика.
Данное изобретение относится к новой кристаллической форме 6-гидрокси-3-(4-[2-(пиперидин-1-ил)этокси]фенокси)-2-(4-метоксифенил)бенз[b]тиофена гидрохлорида. Соединение может быть использовано при ингибировании заболеваний, связанных с недостаточностью эстрогена, включая сердечно-сосудистое заболевание, гиперлипидемию и остеопороз; и ингибировании патологических состояний, таких как эндометриоз, фиброз матки, эстроген-зависимый рак (включая рак молочной железы и матки), рак простаты, доброкачественная гиперплазия эндометрия, расстройства ЦНС, включая болезнь Альцгеймера. Соединение получают путем перекристализации арзоксифена из смеси изопропанола и воды. Полученный продукт хорошо кристализуется. 2 c. и 4 з.п. ф-лы, 12 табл., 5 ил.
| НЕСОЛЬВАТИРОВАННЫЙ КРИСТАЛЛИЧЕСКИЙ 6-ГИДРОКСИ-2-(4-ГИДРОКСИФЕНИЛ)-3-[4-(2-ПИПЕРИДИНОЭТОКСИ) БЕНЗОИЛ]-БЕНЗО-[B]-ТИОФЕНГИДРОХЛОРИД, ОБЛАДАЮЩИЙ АНТИЭСТРОГЕННОЙ И АНТИАНРОГЕННОЙ АКТИВНОСТЬЮ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2104278C1 |
Авторы
Даты
2004-11-20—Публикация
2000-07-28—Подача