Настоящее изобретение относится к новой композиции, содержащей пестицидные вещества с хиральным центром, который кооперирован с соседней аминогруппой.
Хотя хиральность обычно является результатом наличия углеродного атома, к которому присоединены четыре различных атома или группы других атомов, включающие серу, также могут быть источником хиральных центров.
Из литературы, например из заявки на Европейский патент ЕР-А-0295117, известно, что некоторые производные N-фенилпиразола могут использоваться для уничтожения членистоногих, растительных нематод, паразитических червей и простейших паразитов. Рассматриваемые соединения включают N-фенилпиразолы, необязательно содержащие в 5-положении кольца замещенную аминогруппу. Указанные замещенные аминогруппы включают аминогруппы, замещенные одной или двумя группами, выбранными из алкила и алканоила. Рассматриваемые соединения включают вещества, содержащие в положении 3 цианогруппу, а в положении 4 группу R-S(O)n, причем R выбирают из алкила и галоалкила. В том случае, когда группа RS(O)n представляет собой сульфоксид, RS(О), полученные в результате производные обычно представляют собой хиральные соединения, существующие в виде смеси двух энантиомеров (известных также как энантиомерные изомеры).
Среди соединений перечисленных в цитированной публикации упомянут 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол, представленный формулой (А).
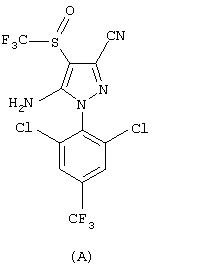
Такое соединение в настоящее время находит коммерческое применение в борьбе с насекомыми-паразитами, например, в области сельского хозяйства, здравоохранения и охраны здоровья животных.
Хотя соединение формулы (А) не содержит каких-либо хиральных углеродных атомов, оно представляет собой смесь энантиомеров в связи с наличием группы -S(O)СF3. Существование таких энантиомеров ранее не описывалось. При пероральном применении на животных рассматриваемое соединение вызывает рвоту.
Для уничтожения членистоногих паразитов у животных желательно, чтобы используемые соединения применялись перорально. Исследование класса N-фенилпиразолов, содержащих необязательно замещенную аминогруппу в положении 5 пиразольного кольца, показало, что степень рвотного эффекта от такого перорального применения зависит от комбинации нескольких параметров: наличия или отсутствия заместителя в положении 5; природы указанного заместителя и хиральности сульфоксидной группы в положении 4.
Введение ацетильной группы в 5-аминогруппу соединения формулы (А) вызывает резкое повышение токсичности и рвоту. При испытании на собаках было установлено, что оба энантиомера при дозе 10 мг/г вызывают рвоту почти у двух третей испытуемых животных. Однако, если смертность от применения энантиомера (S) достигает 100%, то смертность при применении (R) энантиомера составляет лишь 33%. Хотя монозамещение ацетильной группой вызывает повышение рвотной активности и смертности, было обнаружено, что введение в аминогруппу метильного заместителя и замена ацетила на этоксиацетил или тетрагидрофур-2-оил может снизить как рвотную активность, так и смертность.
Однако можно обойтись без указанной химической модификации 5-аминогруппы в результате разделения соединения А на составляющие его (R) и (S) энантиомеры. В отличие от 5-ацетиламино энантиомеров (среди которых (S) энантиомер вызывает 100% смертность) именно (S) энантиомер 5-аминопроизводного является лучшим из двух рассматриваемых энантиомеров и обладает пониженной рвотной активностью. Кроме этого, (S) энантиомер 5-аминопроизводного обладает вторым преимуществом. В результате применения этого соединения может обеспечиваться улучшенное длительное уничтожение клещей. Так, например, при пероральном применении на собаках с дозой 10 мг/кг (S) энантиомер обеспечивает 85% контроль против 71% при использовании (R) энантиомера (что соответствует выживанию только 15% клещей вместо 29%).
Задачей настоящего изобретения является создание композиции, содержащей 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол, который существенно обогащен каким-либо энантиомером.
Другая задача настоящего изобретения заключается в создании композиции, являющейся в целом безопасной при применении в области ветеринарной медицины, сельского хозяйства или здравоохранения.
Следующая задача настоящего изобретения состоит в обеспечении композиции, которая практически не вызывает рвотного эффекта при пероральном введении животным, более предпочтительно, когда при применении такой композиции примерно 70% или более обработанных животных не испытывают позывов к рвоте.
Настоящее изобретение в полной мере или частично обеспечивает решение указанных задач. Настоящее изобретение предусматривает композицию, содержащую (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол и (R)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол, причем рассматриваемая композиция обогащена (S) энантиомером. Под термином “обогащенный” подразумевается, что отношение S/R (вес:вес) составляет, по крайней мере, 1,05 или более.
Предпочтительно, чтобы композиция настоящего изобретения была существенно обогащена S энантиомером. Термин “существенно обогащена” означает, что весовое соотношение S/R составляет, по крайней мере, примерно 1,5 или более.
Согласно еще одному из аспектов настоящего изобретения весовое соотношение S/R составляет, по крайней мере, 2 или более, предпочтительно, по крайней мере, 5 или более, наиболее предпочтительно, по крайней мере, около 10 или более.
Для большей ясности структуры (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола и (R)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола представлены формулами (В) и (С) соответственно. Оптические конфигурации формул (В) и (С) представлены с использованием системы Cahn-Ingold-Prelog, общее описание которой приведено в Advanced Organic Chemistry, J. March, 3-е издание, стр.96-97, Wiley Interscience, NY, 1985. Приведенные формулы, в целом, понятны специалисту в данной области.
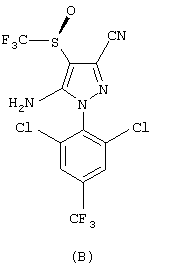
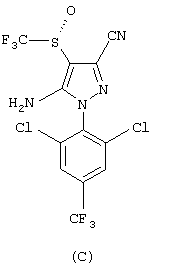
Композиции настоящего изобретения могут дополнительно содержать носитель, используемый в области ветеринарной медицины, защиты здоровья животных, сельского хозяйства или здравоохранения. Рассматриваемые композиции в общих чертах описаны в ЕР-А-0295117.
Кроме этого, настоящее изобретение предусматривает способ борьбы с насекомыми-паразитами в очаге их распространения, причем такой способ заключается в нанесении на указанный очаг композиции настоящего изобретения в пестицидно эффективном количестве.
Соединение А может быть приготовлено согласно способам, описанным в ЕР-А-0295117.
В соответствии с одним из аспектов настоящего изобретения рассматриваемые композиции могут быть получены полным или частичным разделением энантиомеров, например, в результате применения методов колоночной хроматографии или колоночной хроматографии с обращенной фазой с использованием, как это известно специалисту в данной области, существенно оптически активной (или “хиральной”) стационарной фазы.
Согласно другому аспекту настоящего изобретения рассматриваемые энантиомеры могут быть разделены с помощью процесса, который включает
(а) реакцию соединения (А) с соединением (EG), в котором
Е представляет собой органический радикал, который энантиомерно обогащен, например является практически энантиомерно чистой группой, a G представляет собой реакционноспособную группу по отношению к аминогруппе, например группу карбоновой кислоты, ангидрида карбоновой кислоты, галогенида карбоновой кислоты или производного карбоновой кислоты, подходящую для такого применения, как это известно специалисту в данной области; с получением соединений формулы (III-А) и формулы (III-B) (являющихся новыми веществами и вследствие этого составляющих отличительный признак настоящего изобретения)
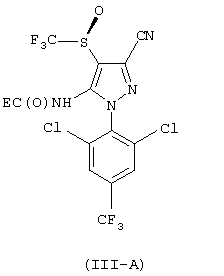
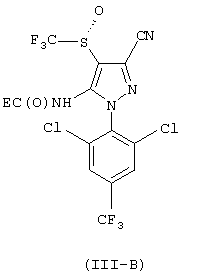
b) разделение соединений формул (III-A) и (III-B);
c) удаление групп ЕС(О) из соединений формулы (III-A) и/или (III-B) с целью раздельного получения (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола и/или (R)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола соответственно.
Продукты, полученные на стадии (а), т.е. соединения формул (III-A) и (III-B), представляют собой два диастереомера, которые, как это известно специалисту, могут быть разделены, например, методами колоночной хроматографии или колоночной хроматографии с обращенной фазой.
В том случае, когда радикал Е включает фрагмент первичного, вторичного или третичного амина, продукты со стадии (а), т.е. соединения формул (III-A) и (III-B) представляют собой два диастереомера, которые могут быть превращены в аддитивные соли соответствующей кислоты и после этого разделены, например, с использованием фракционной кристаллизации, как это известно специалисту в данной области.
В том случае, когда радикал Е включает фрагмент карбоновой кислоты, серной кислоты или другой кислоты, продукты со стадии (а), т.е. соединения формул (III-A) и (III-В), представляют собой два диастереомера, которые могут быть превращены в соответствующие соли и разделены, например, с использованием фракционной кристаллизации, как это известно специалисту в данной области.
Как известно специалисту, удаление амидного фрагмета на стадии (С) включает химический гидролиз.
Согласно еще одному аспекту настоящего изобретения обеспечивается выделенное соединение - (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол.
В соответствии с еще одним аспектом настоящего изобретения композиция изобретения может быть получена селективным окислением 5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола с преимущественным получением (S) энантиомера. Такие способы окисления известны специалисту в области органического синтеза. Также имеется возможность использования таких способов разделения, как описанные ранее, для выделения R-энантиомера фипронила и его превращения с использованием окислительно-восстановительной схемы в S-энантиомер.
Неожиданно было установлено, что (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол обладает существенным преимуществом в борьбе с некоторыми членистоногими паразитами в очаге заражения животных. Другое неожиданное существенное преимущество состоит в том, что (S) энантиомер характеризуется значительным снижением рвотной реакции при пероральном введении животному. Используемый в тексте термин “emesis” обозначает рвоту. Обычно рвотное вещество вызывает рвоту менее чем через 24 часа после его введения, предпочтительно менее чем через 8 часов, более предпочтительно менее чем через 2 часа.
Кроме сказанного выше, настоящее изобретение относится к применению описанной выше композиции для производства ветеринарной композиции, предназначенной для борьбы с членистоногими паразитами в организме или на поверхности животного.
Настоящее изобретение также относится к способу очистки животных с хорошим состоянием здоровья, включающему применение на животном описанной выше композиции.
Способ очистки животных не является терапевтическим методом лечения тела животного per se, поскольку
(a) животное имеет хорошее состояние здоровья и не требует существенного лечения для его корректировки;
(b) указанная чистка животного не предусматривает действий ветеринарного персонала, а осуществляется лишь лицами, заинтересованными в очистке животного;
(с) цель указанной очистки состоит в устранении условий, неприятных для людей и среды их обитания с тем, чтобы исключить инфицирование людей членистоногими паразитами, переносимыми животными.
Кроме этого, настоящее изобретение предусматривает применение описанной выше композиции в качестве активного ветеринарного вещества.
Как правило, композиции, используемые в соответствие с настоящим изобретением, содержат от около 0,001 до 99% активного ингредиента. Остальная часть композиции до 100% представляет собой носитель, а также различные добавки. В тексте описания и формулы изобретения процентные значения даны в весовом выражении.
Разбавленные жидкие рецептуры обычно включают от примерно 0,001 до примерно 20% активного ингредиента, предпочтительно от около 0,1 до около 3%. Твердые рецептуры обычно содержат от около 10 до 99% активного ингредиента, предпочтительно от 40 до 70%.
Композиции, предназначенные для перорального применения, содержат активный ингредиент в комбинации с фармацевтически приемлемым носителями или покрытиями и включают, например, таблетки, пилюли, капсулы, гели, кисели, медицинские корма, медицинскую питьевую воду, медицинские диетические добавки, болюсы пролонгированного действия или другие средства пролонгированного высвобождения, предназначенные для удерживания в желудочно-кишечном тракте. Любые из перечисленных форм могут включать активные ингредиенты, содержащиеся в микрокапсулах, или покрытые кислотно-лабильными или щелочно-лабильными, либо другими фармацевтически приемлемыми энтеросолюбильными покрытиями. Также могут использоваться пищевые премиксы или концентраты, содержащие соединения настоящего изобретения, предназначенные для использования в приготовлении медицинского диетического питания, питьевой воды или других материалов, содержащих лекарственные средства, которые потребляются животными.
В соответствии с настоящим изобретением активный ингредиент (ai) вводится животному в виде пероральной дозы, составляющей обычно от 0,1 до 500 мг/кг ai в расчете на килограмм веса животного (мг/кг), более предпочтительно от 1 до 100 мг/кг, еще более предпочтительно от 1 до 50 мг/кг, наиболее предпочтительно от 1 до 20 мг/кг.
Общее описание примеров насекомых-вредителей, которые могут уничтожаться активным ингредиентом, приведено в заявке на Европейский патент ЕР-А-0295117. Примеры конкретных паразитов различных животных-хозяев, которые могут уничтожаться с помощью настоящего изобретения, включают таких членистоногих, как клещи (например, мезостигматиды, зудни чесоточные (itch, mange), чесоточные клещи (scabies), клещи-тромбикулиды, иксодовые клещи (например, мягкотелые и твердотелые), вши (например, сосущие вши и пухоеды), блохи (например, собачья блоха, кошачья блоха, блоха восточной крысы, человеческая блоха), клопы (например, постельные клопы, триатомидные клопы), кровососущие взрослые мухи (например, жигалка коровья малая, конский овод, жигалка осенняя, тля черная, олений слепень, кровососка, муха цеце, москиты), а также личинки насекомых-паразитов (например, овода, мухи мясной синей, мясной мухи, червовидные личинки, ворсистые гусеницы); такие паразитические черви, как нематоды (например, круглые нематоды, легочные нематоды, кровососы, власоглавки, узелковый червь, кишечная нематода, круглые черви, булавочный червь, сердцевидный гельминт), цестоды (например, ленточные черви) и трематоды (например, печеночная двуустка, кровяная двуустка); такие простейшие организмы, как щитовка, трипаносомы, трихомонады, амебы и плазмодии; акантоцефаланы, такие как колючеголовые черви (например, лингулатулида); а также такие пентастомиды, как пятиустки. С помощью настоящего изобретения особенно хорошо уничтожаются блохи и клещи.
Следует иметь в виду, что используемый термин “животные” относится к млекопитающим, предпочтительно домашним животным, например комнатным животным, или к социальным животным, предназначенным для получения таких коммерческих продуктов, как кожа или шерсть, например к коровам и лошадям; а также млекопитающим, содержащимся в неволе, например, таким, как зебры, львы и медведи. Следует понимать, что термин комнатные животные относится, например, к собакам и кошкам.
Другой аспект настоящего изобретения относится к применению производного R-фипронила в качестве рвотного вещества для борьбы с насекомыми-паразитами когда рвотное действие желательно, например, в качестве защитного средства, повышающего безопасность применения. Как правило, R-фипронил применяют в тех же количествах, что указаны выше для S-фипронила, а композиции, содержащие R-фипронил, используются в тех же формах, количественных соотношениях и содержат те же компоненты, что описаны выше для S-фипронила; также существует возможность регулирования норм и форм применения с целью максимизации рвотного действия.
В следующих ниже примерах иллюстрируются способы реализации настоящего изобретения, не ограничивающие его объема.
ПРИМЕР 1
Примерно 120 мг смеси S-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола и R-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразола в весовом соотношении 1:1 разделяли методом HPLC (жидкостная хроматография высокого давления) с использованием неподвижной фазы Chiracel® с размером частиц 20 микрон (микрометров) в колонке с внешним диаметром 21 мм, длиной 250 мм и подвижной фазы изооктан:изопропанол в объемном соотношении 96:6, с получением каждого из энантиомеров в количестве 60 мг. Скорость элюирования составляла 6 мл в минуту. Соединение С элюировало из колонки через 20 минут, а соединение В примерно через 40 минут.
Из обоих образцов удаляли растворитель, в результате чего получали белые порошки.
Соединение В имело температуру плавления около 204°С, а температура плавления соединения С составляла 201°С.
Абсолютные конфигурации указанных энантиомеров, представленные формулами В и С, определяли путем перекристаллизации обоих веществ из изопропанола с последующим рентгеноструктурным анализом монокристалла.
ПРИМЕР 2
Соединения В и С примера 1 формировали в виде желатиновых капсул и перорально применяли на группе из 10 собак смешанной породы в количестве 20 мг соединения на кг веса тела обрабатываемого животного.
За 1 день до применения указанных соединений всех животных инфицировали кошачьими блохами (Ctenocephalides felis) и иксодовыми собачьими клещами (Rhipicephalus sanguineus). Подсчет членистоногих паразитов проводили через 1 день после применения (ДПП). Сразу после определения эффективности обработки собак очищали от всех членистоногих паразитов. На 8, 15, 22 и 30 дни после обработки животных снова инфицировали членистоногими и на 9, 16, 23 и 31 дни после обработки проводили определение ее эффективности.
Были получены следующие результаты испытания на уничтожение членистоногих, выраженные показателем смертности в процентах (%) (см. табл. 1).
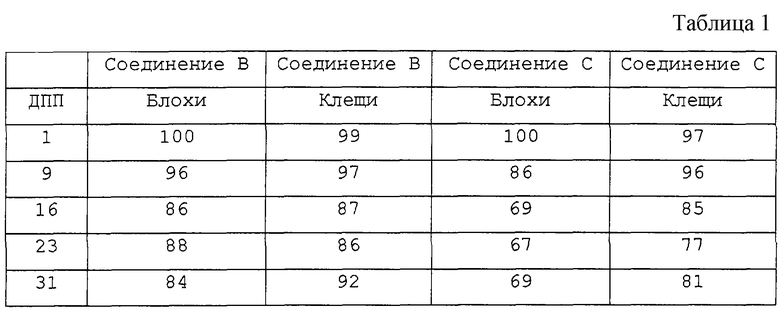
В течение 5 часов после применения рассматриваемых соединений рвотное действие проявлялось у 50% собак, обработанных S-энантиомером, тогда как при обработке R-энантиомером рвотное действие проявлялось у 90% собак.
ПРИМЕР 3
Повторяли тест, описанный в примере 2, используя дозировки, указанные в табл. 2, в которой также представленные полученные результаты.
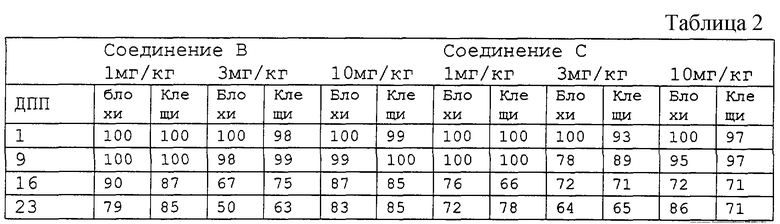
При обработке дозой 1 мг/кг ни одно из испытуемых соединений не проявляло рвотного действия.
При применении дозы в 3 мг/кг 20% животных, обработанных соединением С, проявляли рвотные симптомы через 2 часа.
При дозировке 10 мг/кг 40% животных, обработанных соединением С, проявляли рвотные симптомы через 1 час. Через 3 часа 20% обработанных животных демонстрировали рвотные симптомы.
При обработке соединением В в любой дозировке животные практически не проявляли существенных рвотных симптомов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ N-ФЕНИЛПИРАЗОЛА КАК ИНСЕКТИЦИДЫ | 1990 |
|
RU2026291C1 |
| ПАРАЗИТИЦИДНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ НЕСКОЛЬКО АКТИВНЫХ АГЕНТОВ, СПОСОБЫ И ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2574887C2 |
| ПАРАЗИТИЦИДНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ НЕСКОЛЬКО АКТИВНЫХ АГЕНТОВ, СПОСОБЫ И ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2633751C1 |
| СОСТАВЫ ДЛЯ МЕСТНОГО НАНЕСЕНИЯ, ВКЛЮЧАЮЩИЕ ПРОИЗВОДНОЕ 1-N-АРИЛПИРАЗОЛА И ФОРМАМИДИН | 2004 |
|
RU2361401C2 |
| АРТРОПОЦИДНАЯ ИЛИ РАСТИТЕЛЬНО-НЕМАТОЦИДНАЯ КОМПОЗИЦИЯ | 1987 |
|
RU2080789C1 |
| ПРОИЗВОДНЫЕ 1-ФЕНИЛИМИДАЗОЛА, СПОСОБ БОРЬБЫ С ВРЕДИТЕЛЯМИ СЕЛЬСКОГО ХОЗЯЙСТВА И КОМПОЗИЦИЯ ДЛЯ ПЕСТИЦИДНОЙ ОБРАБОТКИ | 1990 |
|
RU2077201C1 |
| ЭНАНТИОМЕРНОЧИСТЫЙ 2,4-ДИЗАМЕЩЕННЫЙ 2-(2,6-ДИФТОРФЕНИЛ)-4-(4'-ТРИФТОРМЕТИЛБИФЕНИЛ-4-ИЛ)-4,5-ДИГИДРООКСАЗОЛ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ, СПОСОБ БОРЬБЫ С ВРЕДИТЕЛЯМИ, МАТЕРИАЛ ДЛЯ РАЗМНОЖЕНИЯ РАСТЕНИЙ И КОМПОЗИЦИЯ ДЛЯ УНИЧТОЖЕНИЯ ЭКТОПАРАЗИТОВ И ЭНДОПАРАЗИТОВ | 2000 |
|
RU2233838C2 |
| ПРОИЗВОДНЫЕ 5-ЗАМЕЩЕННЫХ АЛКИЛАМИНОПИРАЗОЛОВ В КАЧЕСТВЕ ПЕСТИЦИДОВ | 2003 |
|
RU2308452C2 |
| АМИДОАЦЕТОНИТРИЛЫ, ОБЛАДАЮЩИЕ ПЕСТИЦИДНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2546871C2 |
| ЗАМЕЩЕННЫЕ АРИЛПИРАЗОЛЫ В КАЧЕСТВЕ АГЕНТОВ ДЛЯ УНИЧТОЖЕНИЯ ПАРАЗИТОВ | 2006 |
|
RU2381218C2 |
Изобретение относится к области ветеринариии и предназначено для борьбы с паразитами у животных. Композиция для борьбы с паразитами у животных содержит (S)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол и (R)-5-амино-3-циано-1-(2,6-дихлор-4-трифторметилфенил)-4-трифторметилсульфинилпиразол при различных весовых соотношениях S и R энантиомеров, обеспечивающих возможность регулирования степени рвотного действия композиции. 7 н. и 7 з.п. ф-лы, 2 табл.
Приоритет по пунктам:
| РЕГУЛЯТОР ТЕМПЕРАТУРЫ | 0 |
|
SU295117A1 |
Авторы
Даты
2004-12-10—Публикация
2000-04-12—Подача