Изобретение относится к способам рафинирования галлия и может быть использовано в электронной промышленности, цветной металлургии и других отраслях, занимающихся переработкой галлийсодержащего сырья.
Известен способ рафинирования галлия (Иванова Р.В. Химия и технология галлия. М., "Металлургия", 1973 г., стр.355), включающий перевод чернового галлия в трихлорид GаСl2 (III), действием на металл чистого хлора, разбавленного азотом и тщательно осушенного серной кислотой, с последующей дистилляцией трихлорида галлия при нагревании до температуры 145° С. Основным недостатком способа является использование в качестве реагента хлора - очень токсичного вещества, что приводит к образованию большого количества отходов при операции по его детоксикации.
Наиболее близким по технической сущности к заявляемому объекту является способ (Иванова Р.В. Химия и технология галлия. М., "Металлургия", 1973 г., стр.362), включающий обработку расплава чернового галлия хлором до образования дихлорида галлия GаCl2 (II). Затем дихлорид диспропорционируют, образующийся трихлорид галлия дистиллируют в присутствии хлора под давлением менее 1,01· 105 Па при 180-200° С и 1,33· 104 Па при 160-180° С. Далее трихлорид галлия растворяют в воде и подвергают электролизу с целью выделения галлия в виде металла.
Основными недостатками предлагаемого способа являются следующие:
- низкая степень очистки галлия при дистилляции, так как при хлорировании наряду с образованием дихлорида галлия с последующим диспропорционированием до трихлорида галлия образуются хлориды элементов примесей, имеющие близкие температуры кипения к основному компоненту - трихлориду галлия GаСl3 (III), загрязняющие полученный галлий (таблица 1);
- высокая токсичность технологического процесса, так как обработку чернового галлия ведут хлором - очень токсичным веществом. Кубовый остаток при дистилляции, представляющий собой трихлорид галлия GаСl3 (III) и хлориды элементов примесей, является очень гигроскопичным веществом, на воздухе дымит, притягивает влагу и превращается в агрессивную желеобразную массу, взаимодействует с большинством металлов. При растворении полученного трихлорида галлия GаСl3 (III) в воде и последующем электролизе в анодном пространстве также образуется хлор (Сl2), который очень токсичен и требует дополнительных операций по его детоксикации, что приводит к образованию большого количества отходов;
- кубовый остаток после дистилляции трихлорида галлия требует дополнительных операций по извлечению из него галлия, что тоже приводит к образованию дополнительных отходов и делает процесс дорогостоящим.
Техническим результатом предлагаемого изобретения является увеличение степени очистки галлия, снижение токсичности, уменьшение количества образующихся отходов и удешевление процесса.
Технический результат, обеспечиваемый изобретением, достигается тем, что в данном способе очистки галлия, включающем перевод чернового галлия в химическое соединение и получение металлического галлия, отличающийся тем, что черновой галлий переводят в зоне синтеза в легколетучий оксид галлия Ga2O (I) нагреванием в присутствии оксида галлия Gа2O3 (III) в вакууме при температуре 500-700° С, с образованием кубового остатка, легколетучий оксид галлия Ga2O (I) переводят из зоны синтеза в зону диспропорционирования при этих же условиях и ведут диспропорционирование легколетучего оксида галлия Ga2O (I) при температуре 700-900° С с получением металлического галлия и оксида галлия Gа2O3 (III), а образовавшийся кубовый остаток направляют на повторное использование при добавлении к исходному черновому галлию.
Получение галлия более высокой степени чистоты достигается благодаря тому, что в результате перевода чернового галлия в химическое соединение по реакции 4Ga+Gа2O3→3Gа2О образуется легколетучее соединение оксид галлия Gа2O (I), который в условиях динамического вакуума легко отвести из зоны синтеза, а примеси остаются в реакторе-испарителе. Это возможно благодаря тому, что большинство примесей образуют оксиды, температуры плавления и кипения которых значительно выше, чем у оксида галлия Ga2O (I) (таблица 2).
Для элементов примесей, которые могут присутствовать в исходной смеси чернового галлия и оксида галлия Gа2O3 (III) не в виде оксидов, температуры кипения приведены в таблице 3.
Из таблицы 3 видно, что эти температуры также значительно выше, чем у оксида галлия Ga2O (I).
Таким образом, пары оксида галлия Ga2O (I), очищенные от примесей на этой стадии, проходя через более нагретую зону с температурой 700-900° С, диспропорционируют, образуя галлий более высокой степени чистоты и оксид галлия Gа2О3 (III), который используется многократно для приготовления исходной смеси с черновым галлием. Сравнительные данные степени очистки галлия в заявляемом способе и способе-прототипе приведены в таблице 4.
Использование предлагаемого способа очистки галлия обеспечивает, кроме того, снижение токсичности процесса, уменьшение количества отходов и удешевление процесса.
Снижение токсичности процесса достигается тем, что при переводе чернового галлия в легколетучее соединение в качестве реагента используется менее токсичный оксид галлия Gа2O3 (III), в результате реакции образуется нетоксичный оксид Ga2O (I), а диспропорционирование ведут в нетоксичной среде - в условиях динамического вакуума.
Снижение количества образующихся отходов достигается тем, что кубовый остаток направляется не на утилизацию, а на повторное использование. В кубовом остатке (коллекторе примесей) остается 5-10% по массе от исходной загрузки галлия (берется в избытке). Этот кубовый остаток используется многократно - добавляется к исходной загрузке галлия. По мере накопления примесей больше предела растворимости их в галлии, последний направляется на операцию фильтрации, где отделяются нерастворимые примеси.
Удешевление процесса достигается тем, что основной реагент оксид галлия Gа2О3 (III) используется многократно, исключается операция детоксикации отходов.
Экспериментально получено, что процесс образования легколетучего оксида Ga2O (I) при температуре менее 500° С не происходит. При температуре более 700° С в зоне синтеза в реакторе одновременно с образованием летучего оксида Ga2O (I) начинается обратный процесс - диспропорционирование Ga2O (I) на галлий и оксид галлия Gа2O3 (III), что приводит к резкому снижению выхода годного.
Процесс диспропорционирования происходит при температуре 700-900° С. При температуре менее 700° С процесс диспропорционирования не происходит. Увеличивать температуру более 900° С нецелесообразно, так как возрастает вероятность загрязнения продуктов диспропорционирования контейнерными материалами и возрастают затраты электроэнергии.
Пример конкретного выполнения способа.
На весах взвешивают 1,1 кг чернового галлия (галлий берется в избытке 10% по массе) и помещают в графитовый контейнер. Взвешивают 0,672 кг окиси галлия Ga2O3 (III) и помещают в тот же контейнер. Заполненный контейнер помещают в зону синтеза в кварцевый реактор, который нагревается двухзонной печью сопротивления и подсоединен к откачной системе, состоящей из механического и диффузионного насосов. В зону диспропорционирования помещают специальный конденсатор, на который высаживается галлий и оксид галлия Gа2О3 (III) при диспропорционировании. Включают откачку на вакуум, и после достижения остаточного давления 0,1 Па нагревают двухзонную печь. Задание на нагрев устанавливают таким образом, чтобы в зоне синтеза температура была 500° С, а в зоне диспропорционирования - 700° С. В течение 0,5 часа обе зоны выходят на режим и выдерживаются затем при этих условиях в течение 1 часа. После этого устанавливают задания для зон 700° С и 900° С соответственно, а после выхода зон на режим через 2 часа выдерживают при этих условиях в течение 0,5 часа. Подъем температуры в течение двух часов до температуры 700° С в зоне синтеза и 900° С в зоне диспропорционирования обеспечивает, с одной стороны, полноту реакций синтеза и диспропорционирования, а, с другой - максимальную чистоту образующегося после диспропорционирования галлия, так как при таком медленном подъеме температуры исключается возможность переноса элементов примесей из зоны синтеза в зону диспропорционирования за счет механического захвата их парами оксида галлия Gа2O (I). По окончании процесса печь выключают, производят охлаждение в течение двух часов, отключают вакуумную систему. Реактор заполняют инертным газом азотом. После этого извлекают специальный конденсатор с галлием и оксидом галлия Gа2О3 (III). Галлий сливают во фторопластовый стакан, взвешивают и анализируют на содержание примесей химико-спектральным и полярографическим методами. Gа2О3 (III) собирают в полиэтиленовый пакет, взвешивают и направляют на приготовление исходной смеси.
Остальные примеры на граничные пределы технологических режимов заявляемого способа представлены в таблице 4.
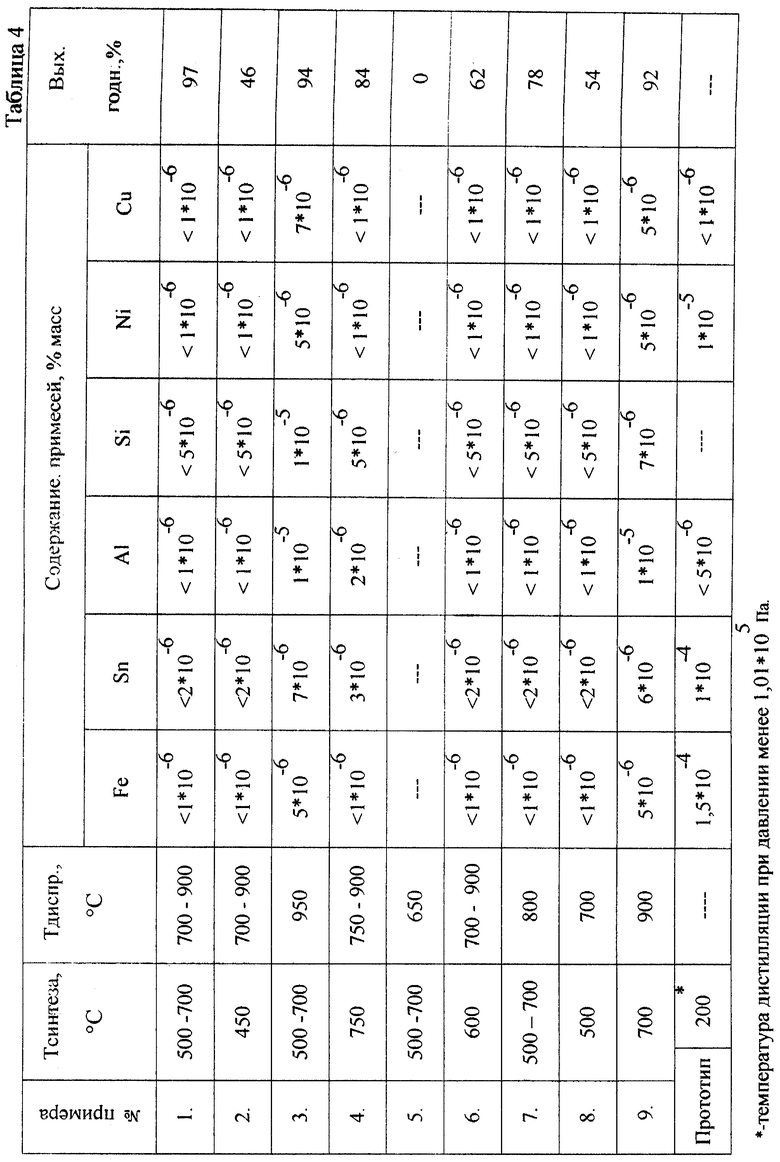
Из таблицы видно, что степень очистки галлия заявляемым способом увеличивается по следующим примесям: Sn, Fe, Al, Si, Ni.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ ГАЛЛИЙМЫШЬЯКСОДЕРЖАЩИХ ОТХОДОВ | 1995 |
|
RU2078842C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПОЛУПРОВОДНИКОВОЙ p-i-n СТРУКТУРЫ НА ОСНОВЕ СОЕДИНЕНИЙ GaAs-GaAlAs МЕТОДОМ ЖИДКОСТНОЙ ЭПИТАКСИИ | 2012 |
|
RU2488911C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСОБО ЧИСТЫХ ХАЛЬКОГЕНИДНЫХ СТЕКОЛ, СОДЕРЖАЩИХ ГАЛЛИЙ | 2021 |
|
RU2770494C1 |
| СПОСОБ БЕСФЛЮСОВОЙ ПАЙКИ РАЗНОРОДНЫХ МАТЕРИАЛОВ | 2010 |
|
RU2442680C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГАЛЛИЯ ИЗ АНОДНОГО ОСАДКА ПРИ ПРОИЗВОДСТВЕ АЛЮМИНИЯ | 2001 |
|
RU2232199C2 |
| Способ получения p-i-n структуры на основе соединений GaAs-GaAlAs методом жидкофазной эпитаксии | 2020 |
|
RU2749501C1 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ДЕГИДРИРОВАНИЯ БУТЕНОВ ИЛИ СМЕСЕЙ БУТАНОВ И БУТЕНОВ С ПОЛУЧЕНИЕМ 1,3-БУТАДИЕНА | 2012 |
|
RU2614977C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЭРОГЕЛЯ ОКСИДА АЛЮМИНИЯ | 1998 |
|
RU2150429C1 |
| СПОСОБ ОЧИСТКИ ВИСМУТА | 2013 |
|
RU2541244C1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ РАССЕЯННЫХ ЭЛЕМЕНТОВ | 2014 |
|
RU2553109C2 |
Изобретение относится к рафинированию галлия. Для получения галлия более высокой степени чистоты черновой галлий переводят в легколетучий оксид галлия Ga2O (I) нагреванием металла в присутствии оксида галлия Ga2O3 (III) в вакууме при температуре 500-700°С с образованием кубового остатка. Легколетучий оксид галлия Ga2O (I) переводят в зону диспропорционирования при этих же условиях с последующим диспропорционированием на металлический галлий и оксид галлия Ga2O3 (III) при температуре 700-900°С, а образовавшийся кубовый остаток направляют на повторное использование при добавлении к исходному черновому галлию. Технический результат заключается в увеличении степени очистки галлия по следующим примесям: Sn, Fe, Al, Si, Ni, снижении токсичности технологического процесса, уменьшении количества образующихся отходов и удешевлении процесса. 4 табл.
Способ рафинирования галлия, включающий перевод чернового галлия в химическое соединение и получение металлического галлия, отличающийся тем, что черновой галлий переводят в зоне синтеза в легколетучий оксид галлия Ga2O(I) нагреванием в присутствии оксида галлия Gа2O3(III) в вакууме при температуре 500-700°С с образованием кубового остатка, легколетучий оксид галлия Ga2O(I) переводят из зоны синтеза в зону диспропорционирования при этих же условиях и ведут диспропорционирование легколетучего оксида галлия Ga2O(I) при температуре 700-900°С с получением металлического галлия и оксида галлия Gа2O3(III), а образовавшийся кубовый остаток направляют на повторное использование при добавлении к исходному черновому галлию.
| ИВАНОВА Р.В | |||
| Химия и технология галлия, М | |||
| Металлургия, 1973, с.362 | |||
| СПОСОБ РАФИНИРОВАНИЯ ГАЛЛИЯ | 1995 |
|
RU2086692C1 |
| Быстрорастворимая фармацевтическая композиция | 2012 |
|
RU2633640C2 |
| WO 00/26422 A1, 11.05.2000 | |||
| US 5458669 А, 17.10.1995 | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
Авторы
Даты
2005-02-20—Публикация
2003-02-04—Подача