Настоящее изобретение относится к способу получения 4-(гетероарилметил)галоген-1(2Н)-фталазинонов.
4-(Гетероарилметил)галоген-1(2Н)-фталазиноны, прежде всего 4-(4-25 пиридилметил)-1(2Н)-фталазинон, являются ценными, образующимися при получении производных фталазина промежуточными продуктами, которые обладают представляющими большой интерес для фармакологии свойствами, такими, например, как ингибирование ангиогенеза (WO 98/35958), ингибирование цГМФ-фосфодиэстеразы (ЕР 0722936) и ингибирующее воспаления и понижающее кровяное давление действие (DE OS 2021195), и которые тем самым открывают новые возможности по терапии различных заболеваний, прежде всего для лечения рака и болезней сердца.
Так, например, 4-(4-пиридилметил)-1(2Н)-фталазинон получают по известному на сегодняшний день методу, основанному на проведении реакции между ангидридом фталевой кислоты и 4-метилпиридином при приблизительно 200°С и на последующем взаимодействии полученного продукта конденсации (γ-пирофталона) с избытком гидразина при 130°С (DE-AS 1061788). К недостаткам этого метода относятся низкий выход (менее 50%) и низкое качество продукта и прежде всего очень высокая температура, необходимая для проведения реакции конденсации, что крайне затрудняет проведение этого метода в промышленном масштабе.
В другом варианте 4-(4-пиридилметил)-1(2Н)-фталазинон можно получать путем конденсации фталида с 4-пиридинальдегидом в присутствии метилата натрия и последующим взаимодействием между полученным 2-(4(1Н)-пиридинилиден)-4,5,6,7-тетрагидроинден-1,3-дионом и используемым в большом избытке (16 экв.) гидразином при 130°С (WO 98/35958). Выход продукта после проведения этих двух стадий составляет приблизительно 40% от теоретического. Серьезные проблемы при осуществлении этого метода связаны с необходимостью использовать большой избыток канцерогенного гидразина и проводить реакцию при температуре, превышающей температуру его разложения (приблизительно 120°С). Одновременно при переработке и выделении продукта практически не удается соблюдать очень низкие предельно допустимые нормы содержания гидразина в воздухе (ПДК, предельно допустимая концентрация, составляет 0,008 част./млн) или в сточных водах.
Из заявки WO 99/32456 известна реакция, которую, однако, проводят с приблизительно 100-кратным избытком гидразина и при температуре, близкой к температуре разложения гидразина (приблизительно 120°С). Поэтому проведение этого способа в промышленном масштабе связано с большими проблемами. Кроме того, выход продукта при этом сравнительно низкий.
С учетом вышеизложенного в основу изобретения была положена задача разработать простой в осуществлении способ получения 4-(гетероарилметил)галоген-1(2Н)-фталазинонов, прежде всего 4-(4-пиридилметил)-1(2Н)-фталазинона, который позволил бы избежать технических и технологических проблем (реакция при 200°С), а также проблем, связанных с техникой безопасности (нагревание гидразина до 130°С) и охраной окружающей среды (большой избыток гидразина), присущих известным способам.
Предлагаемый в изобретении способ позволяет устранить известные недостатки.
Объектом настоящего изобретения в соответствии с этим является способ получения 4-(гетероарилметил)галоген-1(2Н)-фталазинонов общей формулы I
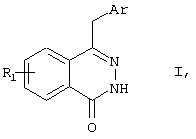
где R1 обозначает фтор, хлор, бром или водород, а Аr обозначает пиридин, пиразин или пиримидин, отличающийся тем, что замещенные соли фталидил-3-трифенилфосфония общей формулы II
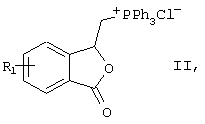
где R1 обозначает фтор, хлор, бром или водород, подвергают взаимодействию с альдегидами общей формулы III
Аr-СНО III,
где Аr обозначает пиридин, пиразин или пиримидин,
в присутствии основания и затем проводят реакцию с гидратом гидразина при необходимости в кислых условиях.
Остаток R1, при условии, что он представляет собой галоген, может находиться в любом положении фенильного кольца в пиназиноновой системе, т.е. в положении 1, 2, 3 или 4. В качестве пригодных для этой цели остатков Аr можно назвать пиридин, пиримидин или пиразин. Пригодными для указанной цели альдегидами являются, например, 2-, 3- или 4-пиридинальдегид, 2-метил-4-пиридинальдегид, 3-метил-4-пиридинальдегид, 4-пиримидинальдегид, 5-пиримидинальдегид, 3-пиразинальдегид или 4-пиразинальдегид.
Таким образом, целевой продукт можно получать, например, взаимодействием соли фталидил-3-трифенилфосфония с 4-пиридинальдегидом в присутствии основания (основное вспомогательное вещество), последующей реакцией с гидратом гидразина и кислотной обработкой реакционной смеси. Поставленная в изобретении задача решается, в частности, с помощью способа, предусматривающего взаимодействие солей фталидил-3-трифенилфосфония с 4-пиридинальдегидом, осуществляемое в соответствующем растворителе в присутствии основания (основное вспомогательное вещество), последующую реакцию с 1-1,1 экв. гидрата гидразина и дальнейшую обработку реакционной смеси 0,1-0,3 экв. ангидрида уксусной кислоты.
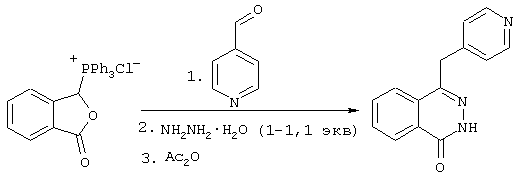
Для выделения продукта реакционную смесь смешивают с водным раствором кислоты, отгоняют растворитель, отфильтровывают выпавший в осадок трифенилфосфин и фильтрат подщелачивают. При этом происходит осаждение целевого продукта, который после фильтрации и сушки получают с высокой степенью чистоты и высоким выходом (95-98% от теоретического).
В качестве растворителей, используемых при проведении реакции, пригодны органические растворители, такие, например, как тетрагидрофуран, диметоксиэтан, метанол, этанол или диметилформамид. В качестве оснований применяют органические основания, такие как амины, например триэтиламин, этилдиизопропиламин, или неорганические основания, такие как карбонат калия, карбонат натрия, карбонат магния либо их гидроксиды. Продолжительность реакции превращения солей фталидил-3-трифенилфосфония составляет 1 ч при 40°С, а реакции взаимодействия с гидразином - от 7 до 14 ч при температуре в интервале от 50 до 70°С.
Применяемые в качестве эдуктов соли фталидил-3-трифенилфосфония (бромиды и хлориды) можно легко получать по известным из литературы методам (J. Organometallic Chem. 1972. 391; J. Org. Chem. 1973. 4164).
К преимуществам предлагаемого в изобретении способа в отличие от способов, известных из уровня техники, относятся более мягкие условия проведения реакции, существенно более высокий выход целевого продукта (более 90%) и прежде всего применение стехиометрических количеств гидразина. При этом реакции протекают до полного завершения и в замкнутой системе, в результате чего перед переработкой гидразин в реакционной смеси практически отсутствует (реакция, осуществляемая по так называемому методу проведения реакций в одном реакционном аппарате). Тем самым исключается опасность работы с этим канцерогенным веществом.
Примеры выполнения
Пример 1
Получение 4-(4-пиридилметил)-фталазинона
500 г хлорида фталидил-3-трифенилфосфония (1,160 моля) суспендируют в 2250 мл тетрагидрофурана (ТГФ). Затем при 5°С добавляют 110,7 мл 4-пиридинальдегида (124,2 г, 1,160 моля), после чего к белой суспензии порциями добавляют 161,7 мл триэтиламина (117,4 г, 1,160 моля). По окончании процесса добавления триэтиламина реакционную смесь в течение 1 ч перемешивают при 40°С, после чего смешивают с 62,0 мл гидрата гидразина (63,9 г, 1,276 моля) и перемешивают в течение 8 ч при 70°С. После этого к смеси добавляют 32,7 мл ангидрида уксусной кислоты (35,5 г, 0,348 моля) и продолжают перемешивать в течение 2,5 ч при 20°С. Затем реакционную смесь вначале смешивают с 1500 мл воды, а затем с 367 мл 4 М раствора серной кислоты. Далее из этой смеси под вакуумом отгоняют приблизительно 2500 мл смеси ТГФ/вода. Полученную суспензию фильтруют через стеклянную фритту. Фильтрат смешивают с 50%-ным раствором гидроксида натрия до достижения рН раствора 8,0 (приблизительно 185 мл). Выпавший в осадок продукт отфильтровывают, промывают 450 мл воды и сушат при 60°С. Таким путем получают 264,2 г (96% от теории) твердого вещества со слегка желтоватой окраской.
tпл: 193-194°С, MC(EI): (M+H)+242.
Другие производные получают аналогичным образом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ИМИДАЗО[4,5-с]ПИРИДИНА, ОБЛАДАЮЩИЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ РЕЦЕПТОРА ГИСТАМИНА 4 (hH4R) | 2012 |
|
RU2628074C2 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2180660C2 |
| КОНДЕНСИРОВАННЫЕ ТРИАЗОЛАМИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ Р2Х7 | 2010 |
|
RU2533122C2 |
| ПИРАЗОЛО[1,5-а]ПИРИМИДИНЫ В КАЧЕСТВЕ ПРОТИВОВИРУСНЫХ СОЕДИНЕНИЙ | 2015 |
|
RU2689788C2 |
| ИНГИБИТОРЫ JAK | 2010 |
|
RU2538204C2 |
| СПИРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2781639C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛИДИНА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КАТЕПСИНА | 2011 |
|
RU2548684C2 |
| ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СУЛЬФОНАМИДНЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ TRPA 1 | 2014 |
|
RU2675792C2 |
| СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕВЫХ КЛЕТОК, ОПОСРЕДОВАННОГО КИНАЗОЙ RAF, ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 1998 |
|
RU2232015C2 |
| ПРОИЗВОДНЫЕ 1-ПИПЕРАЗИН- И 1-ГОМОПИПЕРАЗИНКАРБОКСИЛАТОВ, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ В ТЕРАПИИ | 2004 |
|
RU2356890C2 |
Настоящее изобретение относится к способу получения 4-(гетероарилметил)галоген-1-(2Н)-фталазинонов, прежде всего 4-(4-пиридилметил)1-(2Н)-фталазинона. Предлагаемый способ заключается в том, что замещенные соли фталидил-3-трифенилфосфония подвергают взаимодействию с альдегидами Ar-СНО, где Ar обозначает пиридин, пиразин или пиримидин, в присутствии основания, и затем осуществляют реакцию с гидратом гидразина при необходимости в кислотных условиях. Предлагаемый способ позволяет устранить присущие известным способам проблемы, связанные с техникой безопасности и охраной окружающей среды. 3 з.п. ф-лы.
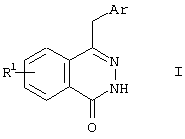
где R1 обозначает фтор, хлор, бром или водород, а
Аr обозначает пиридин, пиразин или пиримидин,
отличающийся тем, что замещенные соли фталидил-3-трифенилфосфония общей формулы II
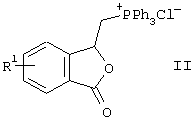
где R1 обозначает фтор, хлор, бром или водород,
подвергают взаимодействию с альдегидами общей формулы III
Аr-СНО III,
где Аr обозначает пиридин, пиразин или пиримидин, в присутствии основания и затем осуществляют реакцию с гидратом гидразина при необходимости в кислых условиях.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| КОНДЕНСИРОВАННЫЙ ПИРИДАЗИН ИЛИ ЕГО ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ ИНГИБИРУЮЩУЮ АКТИВНОСТЬ В ОТНОШЕНИИ ЦИКЛИЧЕСКОЙ ГМФ- ФОСФОДИЭСТЕРАЗЫ | 1995 |
|
RU2128175C1 |
| Коаксиальная нагрузка для штыревых антенн | 1977 |
|
SU634404A1 |
Авторы
Даты
2005-04-27—Публикация
2000-12-20—Подача