Изобретение относится к медицине, а именно к офтальмологии, и может быть использовано для оценки и определения временных фармакокинетических и фармакодинамических параметров лекарственных средств, используемых в офтальмологии для лечения глазного ишемического синдрома, и разработки рационального режима их применения.
Глазной ишемический синдром - сосудистая патология органа зрения, обусловленная нарушением кровообращения в системе внутренней сонной и глазничной артерий. По течению выделяют острый тип, к которому относят окклюзию и спазм центральной артерии сетчатки и ее ветвей, и хронический тип течения, к которому относят диабетическую ретинопатию, гипертоническую ретинопатию, первичную глаукому и ряд других заболеваний.
В последние годы все больше и больше внимания уделяется изучению и поиску новых способов нейроретинопротекторной терапии. Нейроретинопротекция подразумевает защиту сетчатки и волокон зрительного нерва от повреждающего действия различных факторов. При разработке нейроретинопротекторной терапии для рационального выбора способа и режима введения, а также сочетания препаратов необходимо знать особенности распределения лекарственного средства в сетчатке и выраженность его нейроретинопротекторного эффекта.
Известно несколько различных способов оценки фармакокинетики глазных лекарственных форм.
Наиболее простой способ анализа кинетики глазных препаратов состоит в использовании флюоресцирующих веществ в качестве индикаторов, что позволяет произвести замер концентрации во всех прозрачных средах живого глаза человека или животного с помощью специального прибора - флюрометра /1/. Чаще всего используют флюоресцеин, нетоксичное вещество, не имеющее фармакологической активности, не присоединяемое тканями и определяемое даже при очень малых концентрациях. Многие липофобные лекарства подчиняются законам кинетики подобно флюоресцеину. Чтобы оценить особенности фармакокинетики липофильных соединений можно использовать жирорастворимый краситель родамин В. Однако данный способ не применим для оценки особенностей распределения веществ в сетчатке.
Самым распространенным среди способов оценки фармакокинетики глазных лекарственных форм является высокоэффективная жидкостная или газовая хроматография (ВЭЖХ или ВЭГХ), а также радиоизотопные методы количественной оценки содержания препарата в тканях глазного яблока /2/, /3/. Данные методы являются высокоточными, но отличаются высокой стоимостью. Кроме того, для их применения необходим забор тканей и жидкостей глазного яблока, что влечет за собой постоянный забой животных. При этом концентрацию препарата у данного животного можно определить только однократно, т.к. для следующего забора ткани необходимо провести следующий забой животного. В результате получить данные об изменении концентрации препарата в зависимости от времени у одного животного практически невозможно, а использование ряда животных для оценки временной зависимости действия препарата приводит к определенной погрешности из-за отличия различных метаболических процессов у отдельных животных. Применение таких способов исследования для оценки фармакокинетики препаратов, в состав которых входят природные компоненты (пептиды, витамины и т.д.), присутствующие в тканях сетчатки, невозможно, т.к. при хроматографическом анализе пики, соответствующие эндогенному и экзогенному веществу, совпадут.
Наиболее близким по решаемой задаче является известный способ оценки кинетики лекарственного препарата в живом глазу /4/, который так же, как и предложенный, заключается в определении биологической реакции глаза на активные компоненты лекарственного препарата. Данный метод используют для оценки особенностей фармакокинетики препаратов, расширяющих и сужающих зрачок. К недостаткам данного способа следует отнести узкий диапазон его применения, так как он может быть использован, только по отношению к препаратам, оказывающим воздействие на мышцы радужки. Определить фармакокинетические свойства препаратов, относящихся к другим группам, невозможно. Кроме того, способ предполагает необходимость проведения исследований только на здоровых глазах. К тому же измерение временных параметров фармакокинетики миотиков и мидриатиков по реакции сфинктера и дилататора зрачка можно провести только у людей, т.к. у животных их строение и функции отличаются от человека.
Наибольшие сложности возникают при оценке фармакокинетики препаратов, влияющих на функциональную активность сетчатки и зрительного нерва (нейроретинопротекторов). Фактически в настоящее время их концентрацию в тканях сетчатки и зрительного нерва проводят только с помощью ВЭЖХ или радиоизотопных исследований у животных. Проведение данных исследований у людей невозможно, т.к. в этом случае требуется забор биологического материала.
С другой стороны известно, что электроретинография (ЭРГ) представляет собой графическое изображение изменений биоэлектрической активности нейронов сетчатки в ответ на световое раздражение. ЭРГ глаза млекопитающих содержит негативную а-волну и позитивную в-волну. Функциональная активность фоторецепторов обуславливает выраженность амплитуды и времени возникновения (латентность) а-волны. В свою очередь в-волна отражает биоэлектрическую активность в основном клеток Мюллера и биполяров /5/.
Известно также, что при недостаточном поступлении кислорода к тканям сетчатки происходит медленное угасание амплитуды в-волны, вплоть до возникновения негативной в-волны /6/. При этом амплитуда а-волны сохраняется на прежнем уровне или иногда увеличивается /5/. Известные традиционные методики, включающие анализ совокупности амплитуды и латентности а-волны и в-волны, а также их соотношения и сравнение полученных данных со среднестатистической нормой, используют только для диагностики заболевания и для оценки целесообразности хирургического вмешательства. Данная методика является сугубо диагностической, а следовательно, разработка консервативного лечения гипоксических состояний сетчатки, как таковых, с помощью такой методики невозможна. Однако именно консервативное лечение является основным видом терапии данного состояния у большого количества больных.
При этом простым суммированием известных способов оценки фармакокинетики лекарственных препаратов, предназначенных для лечения гипоксических заболеваний сетчатки, и известной методики, позволяющей использовать соотношение амплитуд а-волны и в-волны и сравнения полученных данных со средне-статистической нормой, а также латентности двух волн ЭРГ, невозможно провести одновременную оценку фармакокинетического эффекта (время нарастания и время угасания концентрации лекарственного препарата) и фармакодинамического эффекта (степень выраженности нейроретинопротекторного эффекта) лекарственного препарата в сетчатке живого глаза.
Техническим результатом данного изобретения является расширение возможностей при оценке свойств лекарственных препаратов, предназначенных для лечения глазного ишемического синдрома за счет одновременной динамической оценки их фармакокинетического и фармакодинамического эффектов в сетчатке живого глаза, что стало возможным благодаря экспериментально выявленной взаимосвязи параметров, характеризующих распределение лекарственного вещества в тканях сетчатки, и амплитуды в-волны общей электроретинограммы. При этом имеет место получение более достоверных сведений об особенностях распределения исследуемого препарата в тканях сетчатки и степени выраженности его нейроретинопротекторных свойств. Полученная таким образом комплексная информация в свою очередь приводит к увеличению рациональности нейропротекторной терапии и расширению арсенала лекарственных средств, которые могут быть как известными глазными препаратами, так и вновь используемыми с этой целью, т.к. расширяются представления о временных параметрах фармакокинетики лекарственного средства, а также появляется возможность индивидуального подбора режима дозирования препарата без применения забора биологического материала. Кроме того, данный способ позволяет проводить оценку биоэквивалентности генерических лекарственных средств
Технический результат достигается тем, что в способе оценки фармакокинетических и фармакодинамических свойств лекарственных препаратов, предназначенных для лечения глазного ишемического синдрома, включающем местное введение исследуемого лекарственного препарата в конъюнктивальный мешок или периокулярно, последующее определение параметров, характеризующих распределение препарата в тканях сетчатки производят путем многократной динамической регистрации общей электроретинограммы, причем о максимальной концентрации лекарственного препарата в тканях сетчатки судят по разности времени Тmax eff и Т0,
где Tmax eff - время достижения максимальной амплитуды в-волны,
Т0 - время регистрации начальной амплитуды в-волны,
а период полувыведения лекарственного препарата Ту, вычисляют как разницу между Т1/2 max eff и Т0,
где Т1/2 max eff - время снижения амплитуды в-волны на 50% от максимума,
Т0 - время регистрации начальной амплитуды в-волны,
при этом регистрируют электроретинограмму с одинаковыми интервалами каждые 15-30 минут в течение 3-5 часов.
При этом введение лекарственного препарата осуществляют человеку с глазным ишемическим синдромом или животному с обратимым нарушением кровообращения в сосудах сетчатки. За начальную амплитуду в-волны при этом выбирают первичную величиной амплитуды в-волны, измеренную у человека после приема препарата, а для животного, зарегистрированную через 15-30 минут после нарушения кровообращения в сосудах сетчатки. Для реализации кумулятивного эффекта повторное введение лекарственного препарата производят не ранее, чем через один период полувыведения лекарственного препарата.
Существо способа сводится к следующему.
Экспериментально установлено, что при воздействии препаратов на течение метаболических процессов в сетчатке наблюдается именно увеличение амплитуды в-волны, несмотря на имеющуюся недостаточность кровообращения. Кроме того, наблюдается зависимость между степенью увеличения амплитуды в-волны и временем, а также способом введения лекарственного средства. Поэтому изменение амплитуды в-волны ЭРГ может быть использовано для оценки выраженности нейроретинопротекторных свойств препаратов, применяемых для лечения заболеваний глаз, сопровождающихся гипоксией тканей сетчатки и зрительного нерва (глаукома, диабетическая ретинопатия, дисциркуляторные нарушения в сосудах сетчатки, дистрофии сетчатки и т.д.), которые в целом характеризуются как глазной ишемический синдром.
Кроме того, экспериментально установлено, что при определении параметров, характеризующих распределение препарата в тканях сетчатки, которыми являются максимальная концентрация лекарственного вещества в тканях сетчатки и период полувыведения лекарственного препарата, характерным является то, что многократная динамическая с равными интервалами в течение длительного времени регистрация общей электроретинограммы позволяет судить об их изменении в ту или иную сторону.
Согласно предложенному способу оценивают изменение амплитуды в-волны во времени на фоне действия лекарственного средства, далее регистрируют и анализируют следующие параметры в-волны, по которым в дальнейшем судят о временном распределении препарата в тканях сетчатки:
- Т0 - время регистрации начальной амплитуды в-волны, сразу после применения препарата у человека или через 15-30 минут после нарушения кровообращения у животного,
- Тmax eff - время достижения максимальной амплитуды (возникновения максимального увеличения амплитуды) в-волны.
Далее вычисляют временной интервал между Т0 и Тmах eff. Он соответствует времени достижения максимальной концентрации (Тmах);
- Т1/2 max eff - время снижения амплитуды в-волны на 50% от максимального показателя.
Величину амплитуды в-волны, соответствующую 50% максимального эффекта, вычисляют следующим образом: из величины амплитуды в точке Тmах eff вычитают величину амплитуды в точке Т0, далее полученную величину делят на 2. Затем из максимальной величины амплитуды в-волны вычитают ранее полученную цифру. Затем находят пересечение линии, проведенной через точку, расположенную на кривой, соответствующей вычисленной амплитуде, с осью времени.
После чего вычисляют временной интервал между Т0 и Т1/2 max eff. Он соответствует периоду полувыведения (T1/2).
Существенными признаками предлагаемого изобретения также является использование многократной динамической регистрации общей электроретинограммы с равными интервалами в течение длительного времени, а также подбор указанных временных параметров ЭРГ.
При этом экспериментально установлено, что в качестве минимального интервала времени для регистрации ЭРГ необходимо выбрать 15 минут, так как это время необходимо для создания стабильных физиологических условий и получения максимального скотопического ответа. А в качестве максимального интервала времени для регистрации ЭРГ необходимо выбрать 30 минут, так как при большем временном интервале увеличивается погрешность измерения. И, кроме того, при увеличении заданного интервала более 30 минут, измерения выходят за пределы диапазона периода полуабсорбции.
Далее, в качестве минимального времени, в течение которого проводят регистрации ЭРГ, выбрано 3 часа, так как в этом случае регистрация параметров охватывает как минимум два средних периода полувыведения, что позволяет провести оценку кумулятивных свойств препарата при повторном введении. В свою очередь установлено, что в качестве максимального времени, в течение которого проводят регистрации ЭРГ, необходимо выбрать 5 часов, так как при более длительном сохранении условий ишемии у животных невозможно сохранить обратимость процессов.
Предлагаемый способ осуществляется следующим образом.
Запись электроретинограммы проводят в светонепроницаемой экранированной комнате. Фоновое освещение составляет 17-34 кд/м2. Стимуляцию производят с помощью вспышки, яркость которой на поверхности лампы составляет 3,0 кд/м2. Частота вспышек 1 Гц. Активный электрод представляет собой контактную линзу, которая фиксируется на роговице с помощью вакуумной системы после предварительной поверхностной анестезии. Референтные электроды в виде клипсы располагают на ушах (у животного после предварительного удаления волосяного покрова и обработки 70% этиловым спиртом).
Регистрацию ЭРГ проводят у людей с заболеваниями, сопровождающимися гипоксией тканей сетчатки и зрительного нерва (глаукома, диабетическая ретинопатия, дисциркуляторные нарушения в сосудах сетчатки, дистрофии сетчатки и т.д.).
При исследовании у животных обратимое нарушение кровообращения в сосудах сетчатки создают путем наложения двойных, лигатур на обе общие сонные артерии, которые выделяют в области шеи. Операцию производят под наркозом.
При исследовании у животных первую регистрацию электроретинограммы проводят до перевязки сосудов. Затем затягивают предварительно подведенные под сосуды лигатуры. В течение 1-5 минут после перевязки сосудов необходимо ввести исследуемый препарат. Исследуемый препарат вводят периокулярно (субконъюнктивально или парабульбарно), или закапывают в конъюнктивальный мешок. Далее регистрируют электроретинограмму каждые 15-30 минут в течение 3-5 часов. Для выявления кумулятивного эффекта проводят повторное введение лекарственного средства.
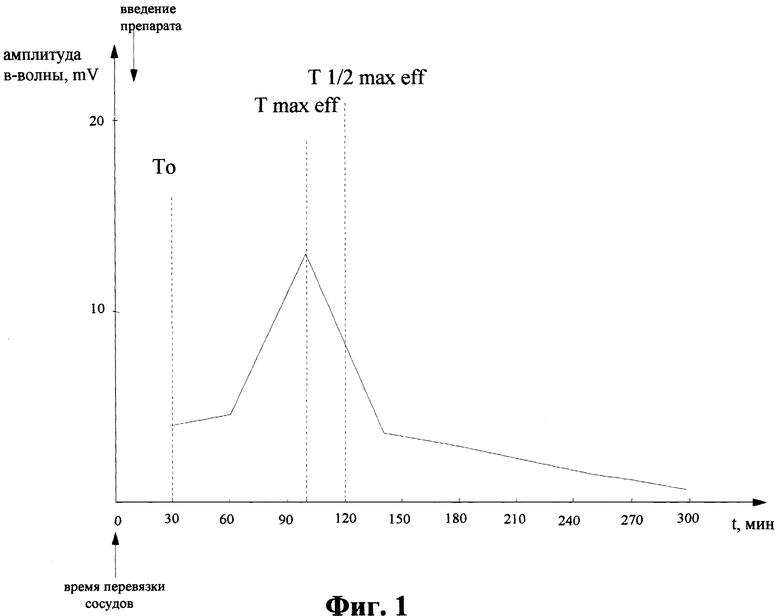
Существо способа поясняется следующим графиком (фиг.1). Согласно представленному графику амплитуда в-волны в точке То составляет 4,0 mV. Максимальная амплитуда в-волны составляет 13,0 mV, a Tmax eff соответствует 100 минутам. Далее из 100 вычитаем 30, получаем, что время достижения максимальной концентрации (Тmах) составляет 70 минут. Далее из 13,0 вычитаем 4,0 и затем делим полученную величину на 2, имеем 4,5. Затем вычитаем из 13,0 ранее полученную цифру, равную 4,5, и получаем величину амплитуды в-волны в точке Т1/2 max eff, равную 8,5 mV. Находим пересечение данной величины по оси ординат с убывающей частью графика. Полученной на графике точке по оси абсцисс соответствует время, равное 120 минутам. Затем из 120 вычитаем 20, получаем, что период полувыведения (Т%) составляет 90 минут.
Таким образом, предложенный способ оценки фармакокинетических и фармакодинамических свойств лекарственных препаратов, предназначенных для лечения глазного ишемического синдрома, благодаря экспериментально выявленной взаимосвязи параметров, характеризующих распределение лекарственного вещества в тканях сетчатки, и амплитуды в-волны общей электроретинограммы, позволит в практической медицине решить вопрос подбора лекарственного средства для лечения патологии сетчатки, вызванной ее гипоксией. При этом получение более достоверных сведений об особенностях распределения исследуемого препарата в тканях сетчатки и степени выраженности его нейроретинопротекторных свойств в свою очередь приведет к увеличению рациональности нейроретинопротекторной терапии и расширению арсенала лекарственных средств, которые могут быть использованы. Кроме того, благодаря использованию предложенного способа на практике также появится возможность индивидуального подбора режима дозирования препарата без применения забора биологического материала, что подтверждается следующими конкретными примерами.
Апробация предлагаемого способа включала сравнение данных, полученных с помощью известной методики (использование хроматографического анализа) и с помощью предлагаемого способа. Провести хроматографический анализ у людей не возможно, поэтому апробация способа была проведена на 187 кроликах (374 глаза).
Исследование проведено для таких препаратов как бетаксолол (селективный бета-адреноблокатор, обладающий свойствами блокатора кальциевых каналов), эмоксипин (антиоксидант), гистохром (антиоксидант), супероксидисмутаза (антиоксидант), цитохром С (антигипоксант), ретиналамин (нейропептид).
Конкретные примеры, выполнения способа
1. Оценка особенностей распространения в тканях сетчатки и выраженности нейроретинопротекторного эффекта селективного бета-адреноблокатора - бетаксолола, применяемого для лечения глаукомы. Способ введения препарата - инстилляции в конъюнктивальный мешок.
На первом этапе были выявлены особенности распространения в тканях сетчатки бетаксолола с помощью традиционных методов хроматографического анализа. Исследование проведено на 12 кроликах (24 глаза).
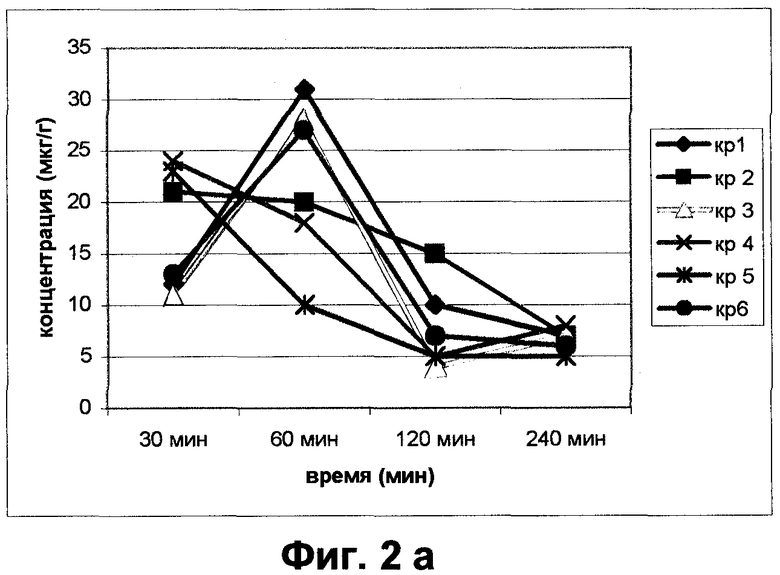
В результате проведенных исследований было получено, что в сетчатке бетаксолол накапливался в значительном количестве. Распределение бетаксолола были следующими: через 30 минут концентрация была равна 18,2±5,89 мкг/г. Через 60 минут она несколько увеличилась и составила 22,33±14,81 мкг/г. Затем она начала снижаться и через 120 и 240 минут была равна 6,57±4,79 мкг/г и 5,7±2,69 мкг/г соответственно. Распределение бетаксолола у испытуемых было недостаточно однородным (фиг.2 а).
Используя математические расчеты, были получены следующие данные:
- время достижения максимальной концентрации (Тmах) составляет 0,91 ч (54,6 мин);
- период полувыведения (T1/2) составляет 1,28 ч (76,8 мин).
На втором этапе было проведено изучение динамики электроретинографии на фоне циркуляторной гипоксии тканей сетчатки после закапывания в конъюнктивальный мешок бетаксолола. Препарат применялся дважды с интервалом 2 часа по 2 капле 0,5% раствора в каждый глаз (сразу после перевязки сосуда и через 120 минут после начала эксперимента). Исследование было проведено у 3 кроликов (6 глаз).
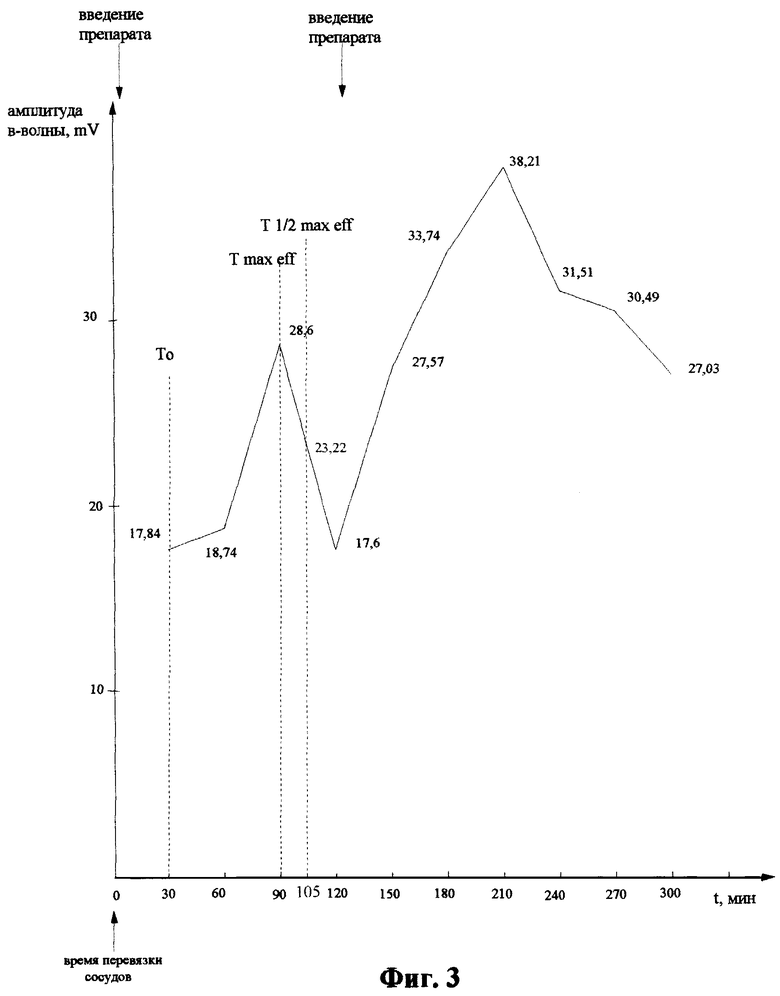
В ходе эксперимента наблюдалось значительное увеличение амплитуды через 90 и 210 мин после применения бетаксолола (фиг.3). Амплитуда в-волны через 30 минут после перевязки сосудов (Т0) составила 17,84 mV. Максимальная амплитуда в-волны, возникшая после первого применения препарата, составляет 28,6 mV, a Tmax eff соответствует 90 минутам. Далее из 90 вычитаем 30, получаем, что время достижения максимальной концентрации (Тmах) составляет 1,0 часа (60 минут). Далее путем вычитания из 28,6 17,84 и последующего деления полученной величины на 2 имеем 5,38. Затем вычитаем из 28,6 ранее полученную цифру равную 5,38 и получаем величину амплитуды в-волны в точке Т1/2 max eff, равную 23,22 mV. Находим пересечение данной величины по оси ординат с убывающей частью графика. Полученной на графике точке по оси абсцисс соответствует время равное 105 минуте. Затем из 105 вычитаем 30, получаем, что период полувыведения (Т%) составляет 1,25 часа (75 минут).
Таким образом, в ходе двух исследований (традиционной методики и предлагаемого способа), были получены практически идентичные величины, характеризующие накопление препарата в тканях сетчатки. Небольшие отличия можно объяснить ограниченным количеством забора биологических проб и определенной погрешностью при математическом моделировании.
Анализируя часть графика, отражающую кумулятивные свойства препарата, можно сделать вывод, что при повторном введении наблюдается аддитивный эффект нейроретинопротекторных свойств бетаксолола, поскольку максимальная амплитуда в-волны после повторного закапывания препарата, превышает первоначальный максимум на 25,15%. Кроме того, имеет место более длительное сохранение нейроретинопротекторного эффекта.
2. Оценка особенностей распространения в тканях сетчатки и выраженности нейроретинопротекторного эффекта 1% раствора эмоксипина (антиоксидант). Способ введения препарата - парабульбарные инъекции.
На первом этапе были выявлены особенности распространения в тканях сетчатки эмоксипина с помощью традиционных методов хроматографического анализа. Исследование проведено у 15 кроликов (30 глаза).
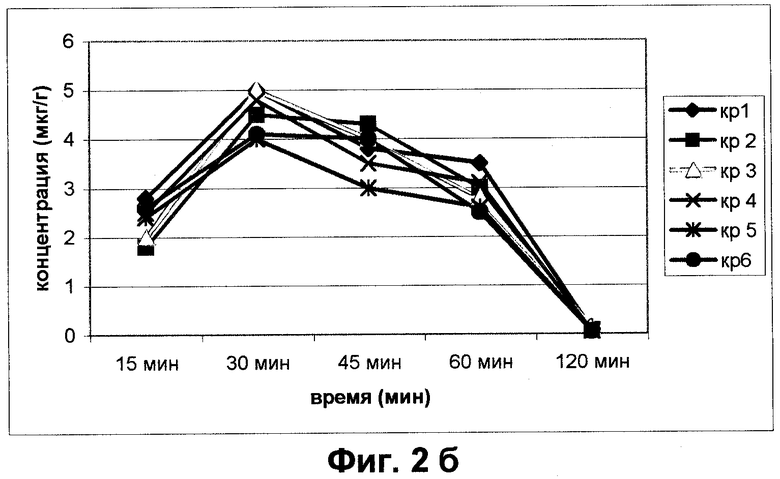
Распределения эмоксипина были следующими: через 15 минут концентрация была равна 2,35±0,38 мкг/г. Через 30 минут она достигла максимального значения и составила 4,56±0,4 мкг/г. Затем она начала снижаться и через 45 и 60 минут была равна 3,27±1,6 мкг/г и 2,92±0,36 мкг/г соответственно. Через 120 минут в сетчатке определялось лишь незначительное количество исследуемого вещества (0,087±0.036 мкг/г). Распределение эмоксипина у испытуемых было однородным (фиг.2 б).
Используя математические расчеты, были получены следующие данные:
- время достижения максимальной концентрации (Тmах) составляет 0,7 ч (42 мин);
- период полувыведения (T1/2) составляет 1,15 ч (69 мин).
На втором этапе было проведено изучение динамики электроретинографии на фоне циркуляторной гипоксии тканей сетчатки после парабульбарного введения раствора эмоксипина. Препарат применялся трижды с интервалом 1,5 часа (сразу после перевязки сосуда и через 90 и 180 минут после начала эксперимента). Исследование было проведено у 3 кроликов (6 глаз),
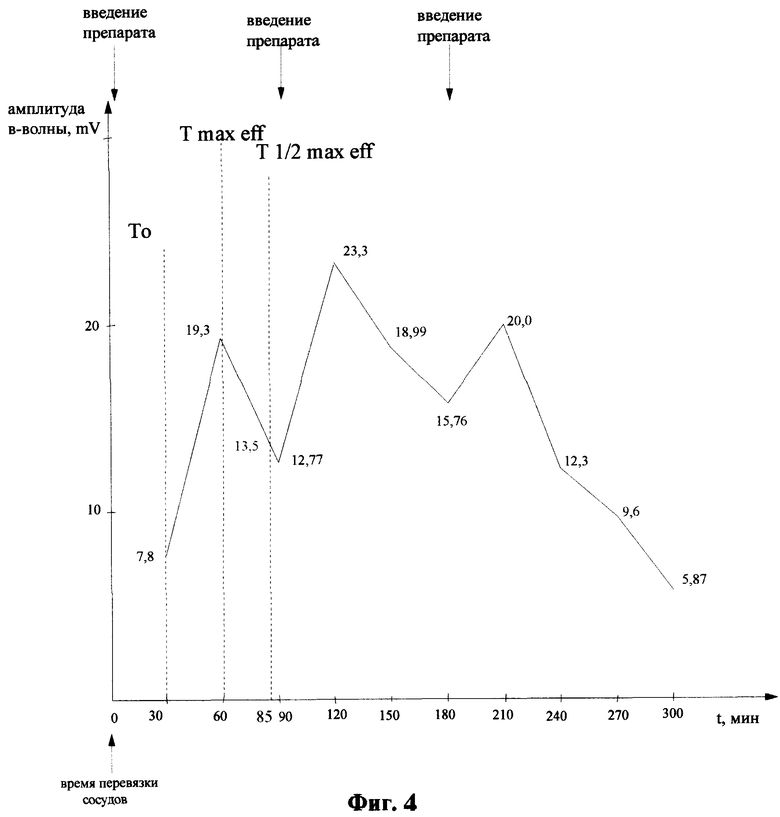
В ходе эксперимента наблюдалось значительное увеличение амплитуды через 60, 120 и 210 мин (фиг.4). Амплитуда в-волны через 30 минут после перевязки сосудов (Т0) составила 7,8 mV. Максимальная амплитуда в-волны, возникшая после первого применения препарата, составляет 19,3 mV, a Tmax eff соответствует 60 минутам. Далее из 60 вычитаем 30, получаем, что время достижения максимальной концентрации (Тmах) составляет 0,5 часа (30 минут). Далее путем вычитания 7,8 из 19,3 и последующего деления полученной величины на 2 имеем 5,75. Затем вычитаем из 19,3 ранее полученную цифру, равную 5,75, и получаем величину амплитуды в-волны в точке Т1/2 max eff, равную 13,5 mV. Находим пересечение данной величины по оси ординат с убывающей частью графика. Полученной на графике точке по оси абсцисс соответствует время, равное 85 минутам. Затем из 85 вычитаем 30, получаем, что период полувыведения (Т1/2) составляет 0,92 часа (55 минут).
Таким образом, данные, полученные предлагаемым способом, соответствуют данным, рассчитанным при математическом моделировании.
Анализирую часть графика, отражающую кумулятивные свойства препарата, можно сделать вывод, что при повторном введении наблюдается увеличение нейроретинопротекторного эффекта эмоксипина, об этом свидетельствует тот факт, что максимальная амплитуда в-волны после повторного введения препарата превышает первоначальный максимум на 17,17%. Кроме того, имеет место более длительное сохранение нейроретинопротекторного эффекта. После третьего применения препарата нейроретинопротекторный эффект практически равен первоначальному.
Необходимо отметить, что предлагаемый способ позволил выявить наличие нарастания выраженности и увеличения периода сохранения нейроретинопротекторного эффекта обоих препаратов. Получить данные сведения традиционными способами невозможно.
Источники информации
1. Araie M., Sawa M., Takase M. Effect of topical indomethacin in the bloodaqueous barrier after intracapsular extraction of senile cataract - a flurophothometric study. //Jpn J Ophthalmol, 1981, 25, p.237-247.
2. Sears M.L. ed. Pharmacology of the eye. // New York, Springer-Verlar, 1984, p.19-116.
3. Bhattacherjee P. Uptake of 3H-noradrenaline by the ocular tissues of rabbit. // Exp Eye Res, 1970, 9, p.73-81.
4. Yoshida S, Mishima S. A pharmacokinetic analysis of the pupil response to topical pilocarpine and tropicamide. //Jpn J Ophthalmol, 1975, 19, p.121-138.
5. Шамшинова A.M., Волков В.В. Функциональные методы исследования в офтальмологию. // M.: Медицина, 1998, с.133-154.
6. Li В., Pang I.H., Barnes G A new method and device to induce transient retinal ischemia in the rat. // Curr Eye Ras, 2002, 24(6), p.458 - 64/.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ТАКТИКИ ЛЕЧЕНИЯ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ | 2004 |
|
RU2262882C1 |
| Способ профилактики ретинальной ишемии-реперфузии миноксидилом в эксперименте | 2016 |
|
RU2643671C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛАУКОМНОЙ ОПТИЧЕСКОЙ НЕЙРОПАТИИ В ПОЖИЛОМ И СТАРОМ ВОЗРАСТЕ | 2009 |
|
RU2411033C1 |
| Способ профилактики ишемической нейропатии зрительного нерва карбамилированным дарбэпоэтином в эксперименте | 2017 |
|
RU2643579C1 |
| СРЕДСТВО, ВОССТАНАВЛИВАЮЩЕЕ ФУНКЦИЮ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА | 1993 |
|
RU2073518C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТАКТИКИ НЕЙРОХИРУРГИЧЕСКОГО ВМЕШАТЕЛЬСТВА ПРИ ХРОНИЧЕСКОЙ СОСУДИСТО-МОЗГОВОЙ НЕДОСТАТОЧНОСТИ | 1998 |
|
RU2141245C1 |
| Способ коррекции ишемической нейропатии зрительного нерва производным диметиламиноэтанола 7-16 в эксперименте | 2017 |
|
RU2663643C1 |
| ТЕТРАПЕПТИД, СТИМУЛИРУЮЩИЙ ФУНКЦИЮ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2000 |
|
RU2161982C1 |
| Способ исследования фармакокинетических свойств лекарственного средства с действующим веществом энисамия йодид | 2022 |
|
RU2802260C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ РЕТИНОПАТИИ | 2004 |
|
RU2260856C1 |
Изобретение относится к медицине и предназначено для исследования фармакокинетических и фармакодинамических свойств лекарственных препаратов, предназначенных для лечения глазного ишемического синдрома. Вводят исследуемый лекарственный препарат в конъюнктивальный мешок или периокулярно. Проводят многократную динамическую регистрацию общей электроретинограммы. О максимальной концентрации лекарственного препарата в тканях сетчатки судят о разности времени Тmaxeff и То, где Тmax eff - время достижения максимальной амплитуды в - волны, а период полувыведения лекарственного препарата Т1/2, вычисляют как разницу между Т1/2 max eff и То, где Т1/2 max eff - время снижения амплитуды в - волны на 50% от максимума. То, - время регистрации начальной амплитуды в - волны. Способ позволяет повысить эффективность оценки фармакокинетических и фармакодинамических свойств лекарственных препаратов, предназначенных для лечения глазного ишемического синдрома. 2 з.п. ф-лы, 4 ил.
| ТЕТРАПЕПТИД, СТИМУЛИРУЮЩИЙ ФУНКЦИЮ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2000 |
|
RU2161982C1 |
| КИСЕЛЕВА Т.Н | |||
| Глазной ишемический синдром (клиника, диагностика, лечение): Автореф | |||
| дисс.д.м.н | |||
| М., 2001, с.10-20 | |||
| ШАМШИНОВА A.M | |||
| и др | |||
| Функциональные методы исследования в офтальмологии | |||
| М.: Медицина, 1999, с.133-154 | |||
| СЕРГЕЕВ П.В | |||
| и др | |||
| Очерки биохимической фармакологии | |||
| М.: РЦ "ФАРМЕДИНФО", с.26-27, 41. | |||
Авторы
Даты
2005-06-10—Публикация
2004-08-16—Подача