Предпосылки создания изобретения
Родственная заявка
Настоящая заявка связана с заявкой на предварительный патент США 60/175658 «Предохранительный клапан и устройство для подачи лекарств при глаукоме», поданной 12 января 2000 г., содержание которой включено в настоящее описание для ссылки.
Область изобретения
Настоящее изобретение относится в целом к системам и способам снижения внутриглазного давления. Один из вариантов настоящего изобретения относится к имплантируемым устройствам для дренажа жидкости для снижения высокого внутриглазного давления при глаукоме.
Предшествующий уровень техники
Глазное яблоко представляет собой по существу сферическую структуру, форма и тонус которой поддерживается эндогенными текучими материалами, которые заполняют внешний пустотелый коллагеновый шар. Внутреннее пространство глазного яблока разделено на две камеры, переднюю и заднюю. Между этими камерами расположен хрусталик глаза и поддерживающие его и связанные с ним ткани. Задняя камера заполнена студенистым материалом, который называется «стекловидное тело», который, как считается, не оказывает существенного влияния на уровень давления в глазном яблоке, которое обозначается термином «внутриглазное давление». Передняя камера в отличие от задней заполнена водянистой жидкостью, которая постоянно вырабатывается и ресорбируется. Эта жидкость оказывает давление на окружающую роговицу и на все окружающие ее структуры. Если организм производит избыточное количество водянистой жидкости, давление в передней камере и внутри глазного яблока повышается. Нормальное внутриглазное давление поддерживается за счет баланса между выработкой и ресорбцией водянистой жидкости.
Водянистая жидкость вырабатывается за основанием радужной оболочки глаза и перетекает в переднюю камеру. Ресорбция происходит через сетчатую систему трабекул, откуда она поступает в сосуды склеры, в которых она смешивается с кровотоком. Нормальным давлением в передней камере считается диапазон от 10 до 21 мм рт.ст. Давление в передней камере определяют по тому, насколько быстро вырабатывается водянистая жидкость и насколько быстро она выводится через сеть трабекул. Причиной повышенного внутриглазного давления может быть закупорка дренажной системы. Длительное повышенное внутриглазное давление приводит к заболеванию, называемому «глаукома», при котором повышенное внутриглазное давление может повредить зрительный нерв и нарушить зрение, что приводит к слепоте, если это заболевание своевременно не лечить.
Известно много способов лечения глаукомы. Терапевтические методы лечения стремятся снизить внутриглазное давление за счет улучшения оттока жидкости или сокращения выработки этой жидкости. Применяются методы, заключающиеся в назначении местных, глазных или общесистемных лекарств. Однако медикаментозное лечение может оказаться неэффективным из-за несоблюдения режима приема лекарств пациентом, высокой стоимости лекарств или может вызвать хорошо известные осложнения и побочные эффекты. Если медикаментозное лечение не помогло, пациенту могут предложить инвазивное лечение, либо изменяющее нормальную анатомию, либо вводящее имплантируемое дренирующее устройство для удаления избытка водянистой жидкости. Например, может быть рекомендована лазерная хирургия для изменения анатомии сетчатки и улучшения дренажа передней камеры. Глаукому лечат и другими процедурами, связанными с применением лазера. Глаза, пораженные глаукомой, могут сохранять повышенное внутриглазное давление несмотря на медикаментозное лечение, а лазерное воздействие может потребовать определенных хирургических процедур.
Например, хирургическое вмешательство обычного типа направлено на создание фистулы или другого дренажного канала, создающего выход из передней камеры. Водянистая жидкость тем самым направляется в созданный хирургическим путем карман под конъюнктивой или карман в склере, который часто называют «пузырь», откуда жидкость может реабсорбироваться в кровоток. Эта операция снижает внутриглазное давление, позволяя избытку жидкости вытекать из передней камеры. Однако такая процедура сопряжена с несколькими известными ограничениями. Во-первых, обычный процесс заживления раны стремится закрыть фистулу и сократить размеры дренажного кармана, поэтому такие операции имеют неприемлемо высокий процент неудач. Для увеличения процента успешных операций врачи могут рекомендовать сопутствующее лечение агентами, которые модулируют нормальный процесс заживления ран. Такое лечение повышает вероятность возникновения проблем второго типа, связанных с этими процедурами: чрезмерный или слишком быстрый отток водянистой жидкости. Хорошо известно, что слишком быстрое удаление слишком большого количества водянистой жидкости может резко понизить внутриглазное давление до опасно низких значений, до состояния, называемого «гипотония», способного вызвать осложнения, угрожающие зрению. Чтобы предотвратить возникновение такой проблемы, хирургическая рана должна заживать достаточно хорошо, чтобы обеспечивать контролируемый дренаж водянистой жидкости. Для этого необходимо, чтобы рана заживала нормально. Методы, препятствующие нормальному заживлению раны, тем самым повышают риск, связанный с избыточным оттоком водянистой жидкости. Третий тип проблем, связанных с этой обычно процедурой дренирования, заключается в повышенном риске инфекции. Дренирование водянистой жидкости в пузырь в склере или в пузырь под конъюнктивой создает риск возникновения инфекции, образуя среду, в которую могут попасть микроорганизмы. Более того, если в кармане, заполненном жидкостью, возникнет инфекция, микроорганизмы смогут через дренажный канал попасть обратно в переднюю камеру глаза и инфицировать ее, что является значительно более серьезным осложнением.
Для решения части проблем, связанных с обычным хирургическим лечением, было предложено несколько имплантируемых устройств, которые предназначены для дренирования избыточного количества жидкости из передней камеры. Однако описанные выше проблемы, сопутствующие хирургии на мягких тканях, также сопутствуют и имплантирующей хирургии. Приходится использовать механизмы заживления ран, несмотря на то, что хирургическое вмешательство заключается в установке внутриглазного имплантата. Действительно, искусственные материалы могут излишне стимулировать локальное заживление раны, что приводит к чрезмерному образованию рубцов. Более того, контроль за поступающим количеством водянистой жидкости продолжает оставаться важной задачей, даже если в процессе используется искусственное устройство. Кроме того, сохраняется риск инфекции. При наличии механического пути проникновения микроорганизмов извне во внутреннюю полость глаза желательно применить некоторый механизм для предотвращения ретроградной инфекции. Наконец глаз, как и большинство тканей тела, имеет ограниченную переносимость долговременного присутствия искусственных материалов. Локально установленный имплантат может раздражать окружающие ткани. Глаз является особо чувствительным органом. Устройство, имплантируемое в поверхность глазного яблока, может восприниматься пациентом как хроническое, постоянно присутствующее и беспокоящее постороннее тело. Наконец, поскольку ткани глаза очень нежны, имплантаты должны конструироваться и имплантироваться так, чтобы они не повреждали уязвимые соседние, нижележащие или вышележащие ткани. Однако имплантаты, даже правильно установленные изначально, могут смещаться под воздействием локальных движений тканей или могут быть вытеснены в процессе стягивающего заживления раны.
Известно много устройств, которые направлены на решение всех этих проблем или некоторых из них. Например, некоторые известные устройства шунтируют водянистую жидкость в резервуар или дренажную зону, которая имплантируется в склеру или под конъюнктиву. Однако, как указывалось выше, такие устройства сталкиваются с проблемами регулирования оттока водянистой жидкости, предотвращения инфекции и локального раздражения тканей и травм. Первая проблема - регулирование оттока водянистой жидкости - возникает потому, что скорость дренирования этой жидкости по существу зависит от механических характеристик имплантата до тех пор, пока рана не заживет в достаточной степени, чтобы ограничивать отток биологически. Эффективный баланс биологического и механического сопротивления оттоку водянистой жидкости остается насущной проблемой при дренажных процедурах, в которых применяются имплантаты. В известных устройствах применяются различные механизмы ограничения оттока водянистой жидкости. Тем не менее каждый из этих механизмов может стать источником проблем после того, как рана заживет. Ограничительные элементы в имплантате в комбинации с ограничительным эффектом заживленной раны могут чрезмерно сократить скорость оттока водянистой жидкости вплоть до неприемлемых с точки зрения терапии уровней. Вторая проблема - возможность внутриглазной инфекции - возникает из-за того, что присутствие имплантата создает путь, через который бактерии могут получить доступ к внутренней полости передней камеры. В некоторых известных дренирующих устройствах установлены фильтры, клапаны или иные проводящие устройства, призванные препятствовать ретроградной передаче инфекции в переднюю камеру. Однако такие механизмы имеют ограничения, даже эффективно препятствуя проникновению микроорганизмов, они оказывают гидравлическое воздействие на отток жидкости, что может снизить эффективность дренажа. Наконец, у некоторых известных устройств возникают проблемы с локальной переносимостью тканей, поскольку эти инородные тела могут инициировать реакцию тканей, приводящую к местному воспалению тканей или вытеснению этих тел и, кроме того, могут ощущаться пациентом и создавать дискомфорт. Такие реакции на присутствие имплантата приводят к клинической неприемлемости его применения.
Устройства, внедряемые через прозрачную роговицу для осуществления дренирования водянистой жидкости, предназначены для устранения некоторых ограничений, сопутствующих имплантации в склере или имплантации под конъюнктиву. Некоторые устройства, например, по патентам США №3788327, №5807302 и №5743868 создают транскорнеальные пути, по которым осуществляется дренаж жидкости из передней камеры на поверхность роговицы, где она смешивается с пленкой слез. Устройства, описанные в вышеуказанных патентах, имеют определенные характеристики, призванные решить проблемы регулирования оттока, ограничения проникновения микроорганизмов, местной тканевой совместимости и стабильности положения. Эти описанные выше проблемы затрагиваются также транскорнеальные устройства. Поэтому сохраняется потребность в биологически совместимом устройстве для дренирования передней камеры, которое обеспечивает хорошо контролируемый отток водянистой жидкости, несмотря на непредсказуемость процесса заживления раны. Кроме того, сохраняется потребность в дренирующих устройствах, которые могут ограничить проникновение микроорганизмов и тем самым защитить полость глаза от инфекции. Помимо этого, сохраняется потребность в офтальмологическом дренирующем устройстве, являющемся хорошо переносимым и комфортабельным для пациента. Наконец, проблема стабильности положения до сих пор удовлетворительно не решена. Существует потребность в дренирующем устройстве, которое можно прочно и надежно установить, не опасаясь его смещения, миграции или вытеснения.
В дополнение к вышеперечисленной потребности в постоянном или долговременном дренаже передней камеры при таких состояниях, как глаукома, имеется дополнительная потребность во временном дренаже или декомпрессии передней камеры. Например, после некоторых офтальмологических процедур, например удаления катаракты и устранения отслоения сетчатки, может наблюдаться кратковременное (от 1 часа до 2 недель) повышение внутриглазного давления. Более того, врач может найти более полезным использовать шунт для временного регулирования внутриглазного давления при глаукоме прежде, чем обратиться к другим хирургическим процедурам для устранения заболевания, которое не требует долгосрочного шунтирования. Существует потребность в устройстве для удовлетворения потребности в кратковременном дренировании передней камеры в таких и подобных ситуациях.
Далее существует потребность в системе доставки, специально приспособленной для атравматического внедрения транскорнеального дренирующего устройства. Преимущественно такая система должна обладать способностью прочно удерживать дренирующее устройство, чтобы хирург мог его позиционировать. Такая система доставки далее должна обеспечивать возможность быстрого освобождения дренирующего устройства, когда его необходимо вставить сквозь роговицу. Далее необходимо, чтобы система доставки была изготовлена так, чтобы не наносить дополнительных повреждений нежным тканям эпителия и стромы роговицы.
Сущность изобретения
Задачей настоящего изобретения является создание систем для снижения внутриглазного давления. Системы по настоящему изобретению могут включать шунт, вставляемый сквозь прозрачную роговицу глаза в переднюю камеру для дренирования из нее водянистой жидкости. Шунт может содержать по существу цилиндрическое тело с каналом, сквозь который обеспечивается дренаж водянистой жидкости из передней камеры на внешнюю поверхность прозрачной роговицы; при этом шунт может далее содержать головку, которая опирается на внешнюю поверхность прозрачной роговицы, основание, которое опирается на внутреннюю поверхность роговицы, и удлиненный фильтр, удерживаемый в канале тела, который регулирует отток водянистой жидкости сквозь этот канал и минимизирует проникновение микроорганизмов. В одном варианте водянистая жидкость имеет возможность вытекать сквозь отверстие в основании для попадания в канал в теле и протекать по нему для выхода сквозь прорезь в головке на поверхность роговицы. В одном варианте головка и основание выполнены заодно с телом. В другом варианте головка, основание или тело могут быть выполнены из обезвоживаемого полимера. В некоторых вариантах внешняя поверхность головки или основания могут иметь такую конфигурацию, чтобы свести к минимуму клеточную адгезию или сцепление. В некоторых вариантах внешняя поверхность тела может иметь такую конфигурацию, чтобы способствовать адгезии тканей или сцеплению, или притягивать их. Основание может иметь особую форму для облегчения внедрения шунта сквозь роговицу. В некоторых вариантах тело имеет меньшую окружность, чем головка или основание. Удлиненный фильтр может удерживаться в канале тела защемлением или любым другим пригодным механизмом. Удлиненный фильтр может устанавливаться на удаленном конце тела или в любом другом положении внутри него.
В других вариантах систем по настоящему изобретению они могут включать в себя имплантат, который может устанавливаться сквозь роговицу для дренирования передней камеры глаза. Имплантат может содержать головку, основание, трубчатый канал между основанием и головкой, в котором выполнен проход, сообщающийся с внутренней камерой, и фильтр который может вставляться в переднюю камеру для регулирования оттока водянистой жидкости и ограничения проникновения микроорганизмов или препятствования их проходу.
В других вариантах системы по настоящему изобретению могут содержать транскорнеальный шунт и могут далее содержать устройство доставки для имплантации шунта в это транскорнеальное положение. В некоторых вариантах имплантируемый с помощью устройства доставки транскорнеальный шунт может иметь головку, основание, по существу цилиндрическое тело между головкой и основанием с выполненным внутри него каналом для регулирования оттока водянистой жидкости и далее ограничения проникновения микроорганизмов. В некоторых вариантах устройство доставки может иметь наконечник, размеры которого приспособлены для удержания шунта и для позиционирования шунта для установки сквозь внешнюю поверхность роговицы, и далее может содержать плунжер, установленный с возможностью перемещения из переднего положения в заднее положение, при этом перемещение поршня освобождает шунт и проводит его сквозь внешнюю поверхность роговицы в транскорнеальное положение.
Еще одной задачей настоящего изобретения является создание способов снижения давления жидкости в передней камере для лечения глаукомы и других заболеваний, характеризующихся повышенным давлением в передней камере. Эти способы могут содержать этапы, при которых используют транскорнеальный шунт, используют устройство доставки для установки шунта в роговице, надрезают пилотное отверстие во внешней поверхности роговицы для обеспечения возможности установки в него шунта, и применяют устройство доставки для того, чтобы вставить шунт в транскорнеальное положение. В одном варианте настоящего изобретения предлагаемый шунт может иметь по существу цилиндрическое тело, головку, основание и фильтр. Следующей задачей настоящего изобретения является создание способов временного снижения давления жидкости в передней камере, тем самым снижая внутриглазное давление. Под временным дренажом понимается кратковременный дренаж, например от одного часа до нескольких недель, с использованием устройства, которое можно извлечь по окончании периода временного дренажа или которое является биоразлагающимся и рассасывается по окончании этого временного периода. Такое устройство может использоваться для имплантации после таких процедур, которые могут повлечь повышение внутриглазного давления или для временного лечения заболеваний, характеризующихся повышением внутриглазного давления.
Шунт по настоящему изобретению предназначен для решения некоторых из упомянутых выше проблем, с которыми сталкивается офтальмология при лечении повышенного внутриглазного давления. Во-первых, шунт, устройство его доставки и способы их использования адаптированы для установки дренажной системы через прозрачную роговицу, тем самым обходя трудности, сопутствующие дренажным системам, устанавливаемым под склерой или под конъюнктивой. Во-вторых, отток водянистой жидкости сообразно регулируется фильтрующей системой, без вовлечения механизмов заживления раны, что позволяет рассчитать прогнозируемую скорость оттока и избежать опасности, с одной стороны, гипотонии, а с другой стороны, недостаточного оттока. В-третьих, фильтр образует извилистый путь, препятствующий проникновению бактерий. Кроме того, щелевое отверстие в головке имеет такую форму и размеры,, которые обеспечивают сопротивление бактериальной инвазии. Более того, сама головка выполнена из материала, который противостоит клеточной адгезии, включая адгезию микроорганизмов. В-четвертых, устройство выполнено из материалов, которые роговица хорошо переносит. Головка и основание сопротивляются клеточной адгезии и препятствуют образованию шрама над устройством, тогда как тело выполнено из материалов, способствующих клеточной адгезии, тем самым позволяя устройству прочно закрепится в транскорнеальном положении. Эти и другие задачи настоящего изобретения будут более понятны из нижеследующего подробного описания со ссылками на прилагаемые чертежи, где сходные детали обозначены одинаковыми позициями.
Краткое описание чертежей
Фиг.1 - вид в перспективе варианта устройства по настоящему изобретению,
Фиг.2 - разнесенный вид варианта устройства по настоящему изобретению, показывающий порядок установки фильтра,
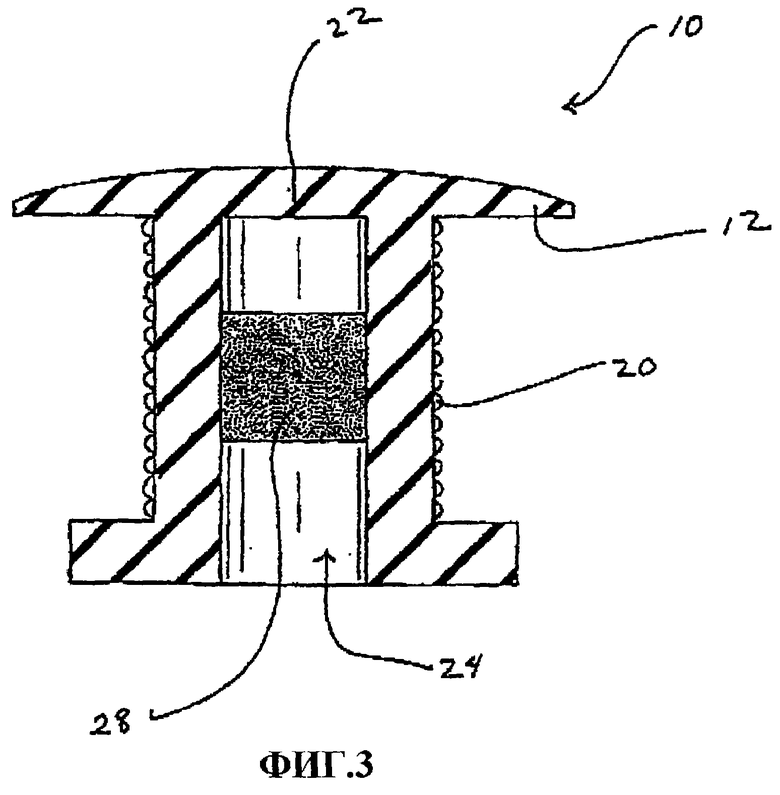
Фиг.3 - поперечное сечение варианта устройства по настоящему изобретению,
Фиг.4 - анатомическое сечение, иллюстрирующее шунт в положении по настоящему изобретению,
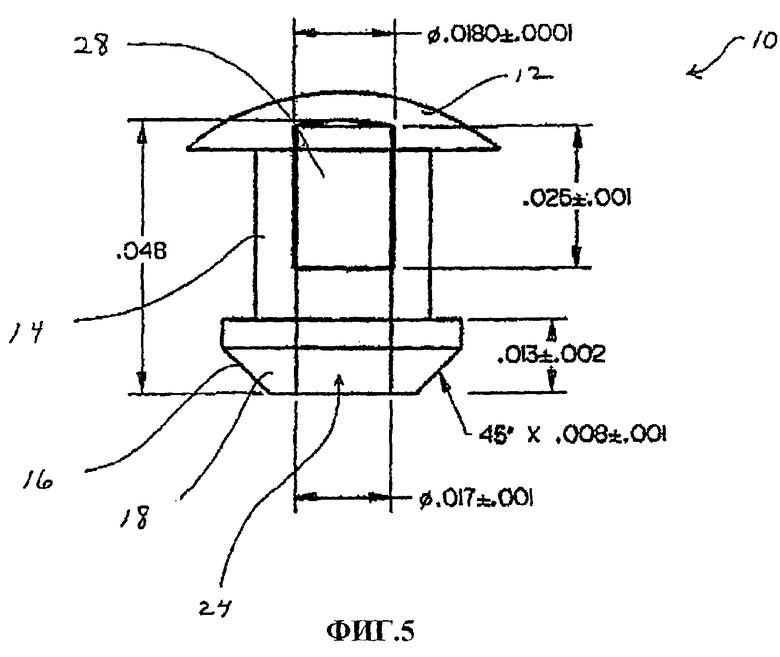
Фиг.5 - схематический чертеж варианта устройства по настоящему изобретению,
Фиг.6А-6D - виды в перспективе и поперечное сечение устройства доставки по настоящему изобретению,
Фиг.7А-7B - виды в перспективе и поперечное сечение альтернативного варианта устройства доставки по настоящему изобретению.
Подробное описание
На фиг.1 в перспективе показан шунт 10 по настоящему изобретению. В представленном варианте шунт 10 может иметь длину приблизительно 1 мм и внешний диаметр приблизительно 0,5 мм. Несмотря на то, что на этом и других чертежах шунт 10 показан имеющим цилиндрическую конструкцию, следует понимать, что могут использоваться и другие формы трубчатого канала. Например, шунт 10 может принимать более овальную или более линзообразную форму. На фиг.1 шунт 10 показан с верхней или внешней стороны. Шунт 10 имеет размеры, адаптированные к транскорнеальной установке. Головка 12 располагается на внешней эллиптической поверхности роговицы, когда шунт 10 устанавливается в рабочее положение. Как показано на фиг.1, головка 12 может быть куполообразной, чтобы создавать непрерывную переходную поверхность от устройства к роговице. Такая форма хорошо переносится веком пациента. Несмотря на то, что такая форма представляется особенно удачной, могут применяться и головки других форм, дающих те же преимущества.
Например, также хорошо может переносится минимально выступающая плоская головка со скругленными кромками. В ходе обычных экспериментов могут быть найдены и другие подходящие конструкции. Нижняя поверхность (не показана) головки 12 может быть плоской или искривленной для того, чтобы она соответствовала форме поверхности роговицы, на которой устанавливается устройство. Головка 12, тело 14 и основание 18 могут быть выполнены заодно, или заодно с телом может быть выполнена либо головка 12 либо основание 18. В другом варианте каждая деталь может отсоединяться от других.
Для изготовления деталей шунта могут использоваться сополимеры гидроксиэтилметакрилата (ГЭМА.). В одном варианте головка 12 выполнена из гладкого материала для устранения тканевого и бактериального сцепления и в значительной степени гидратируется и смачивается слезами. Головка 12 может иметь поверхностный ингредиент, содержащий полимер ГЭМА, например ГЭМА плюс метакриловая кислота, который хорошо известен как вещество, препятствующее клеточной адгезии. Для корпуса шунта может использоваться, например, поли-2-гидроксиэтилметакрилат (ПГЭМА). В одном варианте базовый материал для покрытия поверхности, которая интегрируется с тканью, который притягивает клетки, может содержать ГЭМА и циклогексилметакрилат. В состав корпуса могут включаться ковалентно сшитые гидрогели, используемые в контактных линзах и имеющие равновесное содержание воды по меньшей мере 15 вес.% (и более предпочтительно по меньшей мере 20 вес.%), в частности сополимеры эфиров акриловой и метакриловой кислот с ди- и полигидроксильньшли соединениями. К примерам подходящих полигидроксильных соединений относятся этиленгликоль, диэтиленгликоль, триэтиленгликоль, 1,2-пропандиол, глицерол, глицеролмоноацетат, глюкоза и прочее. Такие эфиры могут быть дополнительно сополимеризованы с винилпирролидоном, акриловой или метакриловой кислотой, акриламидом, N-замещенным акриламидом, и многими другими подобными соединениями, хорошо известными специалистам. Известно несколько конкретных композиций таких гидрогелей, многие из которых могут быть использованы и легко обнаружены опытными специалистами в ходе простых экспериментов. К типичным сшивающим веществам относятся диакрилаты и диметакрилаты указанных диолов и полиолов. В некоторых вариантах настоящего изобретения поверхность тела 14 может содержать слой интеграции с тканью, содержащий сшитый полимер, например соединение, содержащее ГЭМА и алкилметакрилат, в частности циклогексилметакрилат и, в частности, в таких соединениях, где указанный алкилметакрилат используется в более высокой концентрации, чем ГЭМА. Слой интеграции с тканью может быть гладким, пористым или иметь текстурированную поверхность. В иллюстративном примере настоящего изобретения шунт, соответствующий настоящему изобретению, характеризуется определенными физическими свойствами, включая обратимую гидратацию, память формы, локализованные участки поверхности с гидрофильными и гидрофобными свойствами, локализованные поверхности с различными гидратационными свойствами и локализованные поверхности с различными свойствами клеточной адгезии.
Бактериальная инвазия дополнительно предотвращается прорезью 22, пересекающей головку 12. Прорезь 22 обеспечивает отток водянистой жидкости, которая проходит сквозь шунт и вытекает на поверхность прозрачной роговицы, попадая на пленку слез. Хотя прорезь 22 показана на этом чертеже как одно удлиненное отверстие, следует понимать, что отток водянистой жидкости и предотвращение бактериальной инвазии могут обеспечить и другие конфигурации прорези. Например, можно предусмотреть набор из нескольких небольших прорезей. Или, например, прорезь или набор прорезей могут быть менее удлиненными и более круглыми по сравнению с тем, что показано на чертеже. Специалисты могут легко спроектировать и другие формы прорезей.
Основание 18 может быть выполнено из материала, аналогичного материалу головки 12. На чертеже показана верхняя или внешняя поверхность основания 18, выполненная с возможностью контактирования с внутренней эндотелиальной поверхностью роговицы. Как показано на чертеже, основание 18 может быть плоским или оно может быть криволинейным, или иметь форму усеченного конуса для облегчения установки сквозь роговицу. В описанном варианте настоящего изобретения основание 18 шире, чем тело 14. Во внутренней поверхности (не показана) основания 18 выполнено отверстие, сквозь которое водянистая жидкость попадает в шунт 10. Эти и другие признаки основания 18 будут показаны на других чертежах.
Как показано на фиг.1, тело 14 шунта 10 установлено между головкой 12 и основанием 18 и соединено с ними. Тело 14 может быть выполнено из твердого полимера ГЭМА и покрыто гидрогелем, например сополимером ГЭМА, и циклогексилметакрилата, который способствует клеточной адгезии. Покрытие 20 тела 14 является рецептивным для прикрепления тканей, поэтому тело 14 может быть прочно закреплено на месте. Это позволяет шунту 10 сопротивляться движению и смещению in situ. Более того, это позволяет предотвратить направленный внутрь рост бактерий вдоль транскорнеального канала, в котором расположен шунт 10. Чтобы дополнительно стимулировать прорастание тканей и крепление клеток, покрытие 20 тела 14 может подвергаться обработке, меняющей структуру поверхности, например текстурированию, огрублению или нанесению регулярных неровностей. Комбинация полимеров ГЭМА, способствующих клеточной адгезии к телу 14 с полимерами ГЭМА, препятствующими клеточной адгезии на головке 12 и основании 18, позволяет прочно крепить шунт 10 к роговице, когда тело 14 проходит сквозь нее, и одновременно препятствует прикреплению бактерий к головке 12, что могло бы создать потенциальную угрозу инвазии.
Известно, что устройства, изготовленные из ГЭМА, хорошо переносятся глазом. Кроме того, устройство, изготовленное из обезвоженного полимера, такого как ГЭМА, может быть обезвожено для уменьшения его размеров для имплантации сквозь небольшой надрез. Этот признак может облегчить установку шунта сквозь пилотное отверстие или через подобный путь доступа с минимальным разрывом тканей. После надлежащей установки обезвоженного шунта 10 по настоящему изобретению он может насыщаться жидкостью из окружающих тканей и разбухать до заранее определенных размеров. Можно использовать разные степени обезвоживания в зависимости от конкретного состава гидрогеля. Даже если обезвоживание дает лишь небольшое сокращение размеров, оно все равно может облегчить имплантацию. Более того, имплантация обезвоженного устройства в транскорнеальное положение и его насыщение водой и, следовательно, увеличение размеров обеспечивают плотную посадку устройства в нужном положении.
На фиг.2 приведен вид шунта 10 снизу или изнутри в перспективе. В описываемом варианте, когда шунт 10 установлен анатомически, основание 18 лежит на внутренней поверхности или эндотелии роговицы и выступает в переднюю камеру. На этом чертеже также показаны тело 14 и головка 12. Шунт 10 имеет канал 24, который проходит сквозь основание 18 и тело 14 и подходит к внутренней поверхности головки 12. Как показано на предыдущем чертеже, прорезь (не показана) в головке 12 позволяет водянистой жидкости вытекать через канал 24. Фильтр 28 регулирует отток водянистой жидкости из передней камеры на внешнюю сторону глаза и создает извилистый путь в канале 24, чтобы предотвратить проход бактерий. В одном из вариантов фильтр 28 может выполняться из титана. Для фильтра 28 можно использовать такие материалы как керамика и полимеры. В некоторых вариантах настоящего изобретения фильтр 28 вставляется в канал 24 в теле 14. Фильтр 28 может являться постоянной деталью шунта 10. Альтернативно в тех вариантах, где обеспечивается доступ к каналу 24 без нарушения транскорнеального положения шунта 10, фильтр 28 может быть съемным и сменным. Например, доступ к фильтру 28 может обеспечить съемная головка 12, которая позволит его извлекать и заменять. В качестве другого примера головка может иметь порт (не показан), расположенный так, чтобы обеспечивать доступ к фильтру 28 без нарушения положения головки 12. Этот порт и его крепление к головке 12 в некоторых вариантах могут быть интегрированы с системой прорезей, описанной выше. Специалисты в этой области легко найдут и другие решения. Фильтр может устанавливаться в жесткий корпус. Этот корпус может вставляться в тело 14 шунта 10 и извлекаться из него после того, как слой интеграции зафиксирует тело 14 в положении, не нарушая крепление корпуса в глазу.
Как показано на фиг.2, фильтр 28 может иметь форму цилиндра, плотно вставляемого в канал 24 с прессовой посадкой. В показанном варианте канал 24 имеет гладкие стенки 30. Фильтр 28 с размерами приблизительно 0,02×0,02 дюйм (0,5 мм) упирается в стенку канала 24 и прочно крепится на ней. Показанный фильтр 28 содержит систему пор, с размером пор приблизительно 0,5 мкм. Размер пор адаптирован для регулирования потока жидкости на уровне приблизительно два микролитра в минуту. Такой расход, полученный за счет размера пор и длины канала, создающего соответствующее сопротивление потоку, достаточен для снижения избыточного внутриглазного давления, сопровождающего глаукому, и одновременно предотвращает глазную гипотонию. Хотя описанные выше размеры пор и длина канала представляются особенно предпочтительными для систем по настоящему изобретению, следует понимать, что можно использовать и другие величины размера пор и длины канала. Далее следует понимать, что гидравлические характеристики металлов, керамики или полимеров могут изменяться и характеристики фильтров, выполненных из этих материалов, также могут изменяться, не выходя за пределы объема настоящего изобретения, при этом задачей каждого фильтра является создание соответствующих, прогнозируемых и патофизиологически желательных величин оттока водянистой жидкости с одновременным предотвращением ретроградного прохода микроорганизмов.
На фиг.3 показано поперечное сечение шунта 10 по настоящему изобретению. На этом чертеже показан путь водянистой жидкости из передней камеры через канал 24, проходящий в теле 14 для дренирования через прорезь 22 в головке 12. На этом чертеже показана головка 12, тело 14 и основание 18, выполненные заодно. На этом чертеже также показана единственная линейная прорезь 22 сквозь головку 12. Показанная прорезь 22 проходит в осевом направлении сквозь головку 12. Могут использоваться и другие варианты расположения прорези. Например, может быть использовано несимметричное выполнение прорези. Можно также использовать множество прорезей или комбинацию прорезей с отверстиями другой формы. На этом чертеже покрытие 20 с неровной поверхностью нанесено на внешнюю сторону тела 14. Фильтр 28 неподвижно установлен в канале 24. Как показано на этом чертеже, фильтр 28 установлен в центральном участке канала 24.
Фильтр можно устанавливать и в других положениях. Например, фильтр 28 можно установить ближе или дальше по сравнению с положением, показанным на этом чертеже.
На фиг.4 показано сечение шунта 10 в анатомическом положении, в котором он пересекает роговицу 104. Как указано выше, поверхности описываемого устройства могут быть изготовлены из разных материалов, обладающих разными свойствами, в частности с поверхностями, устойчивыми к клеточной адгезии или отложению белка, и с поверхностями, способствующими клеточной адгезии, как описано выше. Головка 12 устройства показана покоящейся на поверхности 118 роговицы. Шунт 10 имеет проход, который позволяет жидкости вытекать из передней камеры 108 через прозрачную роговицу 104 на внешнюю поверхность глаза. Жидкость, попадающая во внутренний проход шунта 10, выходит из устройства и попадает на внешнюю поверхность 118 роговицы, где она смешивается с пленкой слез. На этом чертеже головка 12 шунта 10 показана контактирующей с внешней поверхностью 118 роговицы. На этом чертеже также показано основание 18, контактирующее с внутренней поверхностью 122 роговицы, хотя для правильного позиционирования такой контакт не является необходимым. В показанном положении шунт 10 по настоящему изобретению может устанавливаться выше в прозрачной роговице и закрываться верхним веком в его нейтральном положении. Можно создать варианты шунта 10 по настоящему изобретению для перекрытия стромы роговицы между слезной пленкой на внешней поверхности 118 роговицы и передней камерой 108. В некоторых вариантах шунт 10 может содержать по меньшей мере следующие детали: (а) тело 14, выполненное из гидрогеля, внешняя поверхность которого находится в непосредственном контакте с тканью стромы, (b) головку 12, выступающую над роговицей, внешняя поверхность которой контактирует со слезной пленкой и по меньшей мере периодически контактирует с внутренней стороной века (не показано), (с) основание 18, выступающее в переднюю камеру 108. В описанном варианте по меньшей мере внешняя поверхность тела 14 и головка 12 имеют разные свойства в отношении клеточной адгезии и смачиваемости водой. В конкретном предпочтительном варианте внешняя поверхность головки 12 не связывает клетки, хорошо смачивается слезами и в большой степени гидратирована, тогда как внешняя поверхность тела 14 менее гидратирована и адгезивна для клеток. На фиг.4 также схематически показаны другие анатомические структуры. Хрусталик 100 отделяет переднюю камеру 108 от задней камеры 102. Сбоку от хрусталика показаны реснички 114 мерцательного тела 112, которые отвечают за выработку водянистой жидкости. Перед хрусталиком 100 расположена радужная оболочка 120 глаза.
На фиг.5 показан вариант шунта 10 по настоящему изобретению. В показанном варианте в теле 14 выполнен канал 24 диаметром приблизительно 0,017-0,018 дюйма (0,43-0,45 мм). В показанном варианте канал 24 имеет длину приблизительно 0,048 дюйма (1,2 мм). Внутри канала 24 показан фильтр 28. Вертикальный размер фильтра составляет приблизительно 0,020 дюйма (0,5 мм). Предпочтительно, чтобы фильтр имел конфигурацию, способную удерживать микроорганизмы, например бактерии, грибы и их споры. Основание 18 имеет скошенную кромку 16 для облегчения установки шунта 10 сквозь роговицу. Скошенная кромка 16, показанная на этом чертеже, имеет наклон 45°, и ширину приблизительно 0,008 дюйма (0,2 мм).
Основание 18 может иметь общую высоту приблизительно 0,013 дюйма (0,33 мм). Для облегчения установки шунта через роговицу могут использоваться другие размеры и формы основания 18, которые позволят основанию 18 оставаться в передней камере. Например, основание 18 может иметь складную или гофрированную конструкцию, которая при обезвоживании имеет минимальные размеры, а при поглощении воды расширяется. В других вариантах основание 18 может иметь форму усеченного конуса или форму обратного усеченного конуса и может складываться для облегчения установки. В некоторых вариантах основание 18 имеет больший диаметр, чем тело 14, как показано на этом чертеже. Хотя фильтр 28 показан на этом чертеже на удаленном конце канала 24, для настоящего изобретения можно использовать и другие положения фильтра. Например, фильтр 28 может располагаться не так глубоко в канале 24 или занимать специальное положение в канала 24 или изготавливаться с такими размерами пор и длиной пути для жидкости, чтобы занимать по существу весь канал 24.
В некоторых вариантах настоящего изобретения шунт 10 может изготавливаться из полимера с памятью формы и который можно деформировать для установки сквозь небольшой надрез, и который восстановит свою заранее определенную форму в ответ на гидратацию или в ответ на воздействие температуры тела. Например, шунт 10 в состоянии частичного обезвоживания с температурой размягчения Тs, которая превышает комнатную температуру и предпочтительно приближается к температуре тела, может первоначально устанавливаться в транскорнеальное положение через надрез (например, узкий разрез, вырез, прокол или любой другой вид разреза, доступный специалистам) и после регидратации и повышения температуры расширяется для принятия заранее определенной формы и размеров.
Способы изготовления шунта по настоящему изобретению могут включать изготовление в одноразовой пресс-форме или путем механической обработки, а слой интеграции с тканью наносится в форме отверждаемой композиции. Например, имплантат для роговицы или шунт может отливаться из смеси ГЭМА, метакриловой кислоты, диметакрилатового сшивателя и инициатора свободных радикалов в силиконовой неразъемной пресс-форме с полостью, сформированной штампом, имеющим заранее определенную форму. Альтернативно имплантат для роговицы или шунт может подвергаться механической обработке и затем на внешнюю поверхность шунта наносится слой интеграции с тканью. Слой интеграции с тканью представляет собой отверждаемую композицию, содержащую сополимер ГЭМА с алкилметакрилатом, мономер ГЭМА, диметакриловый сшиватель, инициатор свободных радикалов и летучий растворитель. Специалисты в соответствующих областях, имеющие обычный опыт, легко найдут другие способы изготовления роговичного имплантата или шунта для этих систем и способов.
В системах и способах по настоящему изобретению может применяться устройство доставки, выполненное с возможностью удержания шунта или другого дренирующего устройства, позиционирования шунта или другого дренирующего устройства в заранее выбранном положении, примыкающем к роговице, и введения шунта или другого дренирующего устройства сквозь поверхность роговицы в транскорнеальное положение. В некоторых вариантах устройство доставки может включать в себя вводящий наконечник, выполненный с возможностью удержания и освобождения шунта и для позиционирования шунта для введения сквозь внешнюю поверхность роговицы и может далее содержать вставляющий элемент, выполненный с возможностью перемещения из переднего в заднее положение, при этом перемещение вставляющего элемента из переднего в заднее положение освобождает шунт от вводящего наконечника и вводит его сквозь внешнюю поверхность роговицы в транскорнеальное положение. В поверхности роговицы перед введением шунта или дренажного устройства, для уменьшения сопротивления установке устройства в его заранее определенное транскорнеальное положение предпочтительно можно сформировать пилотное отверстие или другой небольшой надрез, который может затрагивать строму роговицы или проходить сквозь нее. Устройство доставки по настоящему изобретению в некоторых вариантах может быть выполнено с возможностью индикации правильности позиционирования шунта.
На фиг.6А показано устройство 200 доставки, выполненное с возможностью введения шунта по настоящему изобретению в транскорнеальное положение. Устройство 200 доставки, показанное на этом чертеже, имеет эргономичный дизайн с удлиненной рукояткой 206, зоной 210 удержания, вставляющим устройством, которое содержит подвижный наконечник 212 и вставляющий наконечник 214. Рукоятка 206 и зона 210 удержания выполнены на корпусе 202 устройства, предпочтительно изготовленном из легкой пластмассы. Передняя часть устройства 200 доставки содержит пустотелый удаленный кожух 226, в котором вперед и назад может перемещаться подвижный наконечник 212. Зона 210 удержания имеет задний выступ 204 и передний выступ 208, между которыми устройство доставки удерживается наподобие карандаша, что позволяет рукоятке 206 опираться на участок между большим и указательным пальцем кисти хирурга. Такое удержание особенно удобно для точного направления вводящего наконечника 214, однако, по усмотрению хирурга возможны и другие типы удержания устройства 200. На удаленном конце вводящего наконечника 214 выполнено отверстие 218, в которое можно поместить шунт (не показан).
На фиг.6В показано поперечное сечение удаленного конца устройства 200 доставки по настоящему изобретению с подвижным наконечником 212, выдвинутым вперед. Подвижный наконечник 212 перемещается в осевом направлении вместе с плунжером 220. На фиг.6В показан подвижный наконечник 212 в переднем положении относительно фиксированного положения плунжера 220 внутри удаленного корпуса 226. В этом положении образуется камера между удаленным концом 230 плунжера и вставляющим отверстием 218 во вставляющем наконечнике 214, размеры которого подобраны так, чтобы удерживать шунт 10 с возможностью освобождения. На этом чертеже шунт 10 показан во вставляющем наконечнике 214 подвижного наконечника 212 внутри вставляющего отверстия 218. На этом чертеже вставляющий наконечник 214 на удаленном конце подвижного наконечника 212 показан контактирующим с поверхностью роговицы 228. В этом положении передняя грань шунта 10 располагается приблизительно заподлицо с удаленным вставляющим наконечником 214, а задняя грань шунта 10 упирается в удаленный конец 230 плунжера 220. Кроме того, в этом положении за задним торцом 228 подвижного наконечника 212 и перед неподвижным упором 224 образована камера 222. Эта камера 222 образует пространство, в которое может войти подвижный наконечник 212 под воздействием направленного назад усилия. Такое направленное назад усилие может прилагаться к подвижному наконечнику 212, когда хирург подает устройство 200 вперед и когда удаленный вставляющий наконечник 214 находится в контакте с поверхностью 228 роговицы. Поверхность 228 роговицы оказывает сопротивление направленному вперед движению удаленного вставляющего наконечника 214 и выталкивает подвижный наконечник 212 назад. Положение плунжера 220, наоборот, в устройстве 200 является фиксированным. Поэтому, когда подвижный наконечник 212 устремляется назад, плунжер 220 продвигается относительно вперед при продолжении движения устройства 200 вперед в руке хирурга. Плунжер 220 и шунт 10, контактирующий с удаленным концом 230 плунжера 220, продолжает двигаться вперед так, что шунт вталкивается в поверхность 228 роговицы в транскорнеальное положение. Проход шунта 10 сквозь поверхность 228 роговицы можно облегчить, предусмотрев небольшое пилотное или установочное отверстие, в которое может входить основание шунта (не показано). Длина в осевом направлении камеры 222 может приблизительно равняться длине шунта 10. Такая конструкция предохраняет от возможности слишком глубокого введения шунта 10 в глаз.
Степень, с которой подвижный наконечник 212 втягивается назад, показана на фиг.6С. На этом чертеже вставляющий наконечник 214 показан выдвинутым из корпуса 226, а подвижный наконечник 212 введен в корпус 226. На чертеже также показан удаленный конец 230 плунжера, видимый сквозь вставляющее отверстие 218 удаленного вставляющего наконечника 214, что свидетельствует о том, что удаленный конец 230 плунжера находится приблизительно заподлицо с удаленным концом вставляющего наконечника 214, когда подвижный наконечник 212 полностью отведен назад.
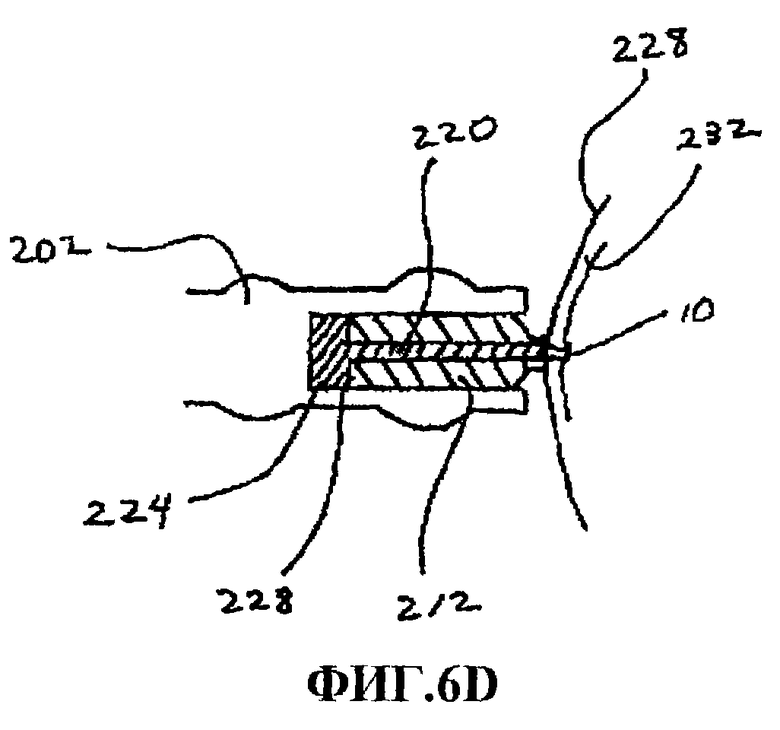
На фиг.6D показано поперечное сечение устройства подачи в положении, когда шунт 10 протолкнут сквозь поверхность роговицы и занял транскорнеальное положение через строму 232 роговицы. Подвижный наконечник 212 полностью отведен назад, а его задний конец 228 упирается в упор 224 плунжера. Сам плунжер 220 неподвижен внутри корпуса 226. Перемещение вперед устройства 200 приводит к вталкиванию подвижного наконечника 212 назад относительно плунжера 220. Шунт 10, остающийся в контакте с удаленным концом 230 плунжера, тем самым проталкивается сквозь поверхность 228 роговицы, преимущественно сквозь пилотное отверстие или надрез, чтобы занять транскорнеальное положение. Дальнейшее направленное вперед давление на устройство 200 встретит сопротивление, когда удаленный вставляющий наконечник 214 более не являющегося подвижным наконечника 212 прижмется к поверхности 228 роговицы. Встретив такое сопротивление, хирург прекращает прилагать усилие к устройству подачи.
Можно предусмотреть другие механизмы информирования хирурга о том, что шунт 10 вставлен правильно. Например, задняя камера 222 может быть оснащена бороздками или язычками (не показаны), которые совмещаются с сопряженными структурами на подвижном наконечнике 212, когда подвижный наконечник 212 полностью смещен назад. Взаимодействие этих сопряженных структур друг с другом могут создавать слышимый или тактильно воспринимаемый щелчок, информирующий хирурга, что произошло полное смещение назад подвижного наконечника 212 и, следовательно, полное выдвижение шунта 10. Взаимодействие сопряженных структур может быть постоянным так, что подвижный наконечник не сможет вернуться в выдвинутое положение, или такое взаимодействие может прерываться под воздействием защелки, кнопки или подобного механизма. Специалисты в данной области легко найдут и другие механизмы, сигнализирующие о положении шунта. В некоторых вариантах весь подвижный наконечник 212 или вставляющий наконечник 214 могут изготавливаться из прозрачных материалов, а плунжер может изготавливаться из непрозрачного или ярко окрашенного материала. Такая конструкция позволит хирургу легко определить положение этих деталей относительно друг друга. Альтернативно все удаленные детали могут изготавливаться из прозрачных материалов так, чтобы хирург мог легко видеть поверхность роговицы сквозь прозрачные участки устройства 200.
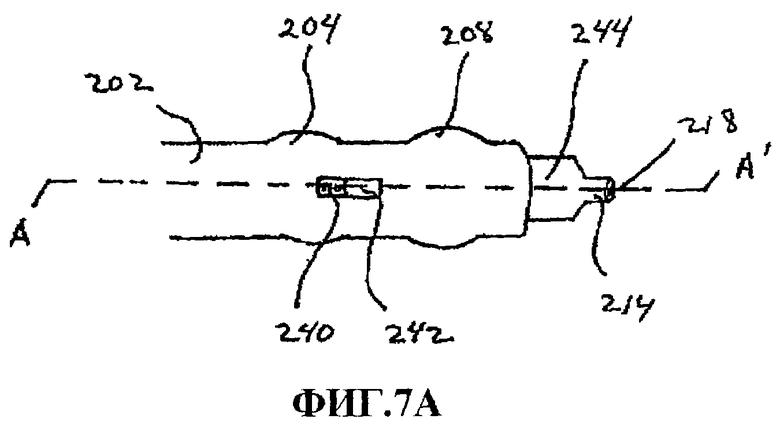
На фиг.7А показан еще один вариант устройства 200 по настоящему изобретению. Внешняя форма этого варианта может быть аналогичной внешней форме устройства 200 по фиг.6А-D, например, имеющей корпус 202, проходящий назад для образования рукоятки (не показана), и зону 210 удержания, эргономично сформированную с выступами 204 и 208. В показанном варианте вставляющее отверстие 218 расположено на удаленном конце вставляющего наконечника 214 и в него вставляется шунт (не показан) с возможностью освобождения. Однако в показываемом варианте фиксированный наконечник 244 и вставляющий наконечник 214 неподвижны относительно устройства 200. Рядом с зоной 210 удержания имеется спусковая кнопка 240. Спусковая кнопка 240 подвижно установлена в вырезе 242 в удаленном конце корпуса 226. Вырез 242 для спусковой кнопки позволяет сместить спусковую кнопку вперед относительно корпуса 226. Как показано на чертеже, спусковая кнопка находится рядом с зоной 210 удержания, хотя для нее можно выбрать любое другое удобное положение. Спусковая кнопка 240 может иметь огрубленную, насеченную или шероховатую поверхность, чтобы хирургу было удобнее ею пользоваться.
На фиг.7В доказано продольное сечение устройства 200 доставки по линии А-А' на фиг.7А. Несмотря на то, что корпус 202 показан пустотелым, этот корпус 202 рядом со спусковой тягой 250 может быть выполнен цельным или иметь любую удобную конфигурацию. Удаленный конец 226 корпуса, однако, по существу выполнен пустотелым, чтобы обеспечить возможность осевого перемещения подвижного плунжера 248. В показанном варианте в удаленном конце 226 корпуса также выполнен вырез 242, сквозь который может проходить спусковая тяга 250. Как показано на этом чертеже, перемещение спусковой тяги 250 вперед также приводит к перемещению подвижного плунжера 248 вперед относительно положения удаленного конца 226 корпуса. На чертеже показана камера 216, выполненная во вставляющем наконечнике 214 неподвижного наконечника 224. Эта камера 216. имеет размеры, позволяющие удерживать с возможностью освобождения шунт (не показан) по настоящему изобретению. Когда показанное на этом чертеже устройство 200 доставки используется для установки и позиционирования шунта, хирург может подать спусковую кнопку 240 вперед до упора, насколько позволяет вырез 242, тем самым перемещая спусковую тягу 250 и связанный с ней подвижный плунжер 248 так, что подвижный плунжер 248 входит в камеру 216 и выталкивает из нее шунт (не показан). Вставляющий наконечник 214 устройства 200 доставки выполнен с возможностью контактирования с внешней поверхностью роговицы во время установки шунта. Хирург прочно удерживает устройство 200 доставки так, что вставляющий наконечник 214 находится в контакте с поверхностью роговицы в заранее выбранном положении, после чего хирург подает спусковую кнопку 240 вперед для установки шунта сквозь роговицу в заданном положении. Как упоминалось ранее, для изготовления устройства 200 доставки могут использоваться различные материалы. В частности, удаленные элементы устройства доставки могут изготавливаться из прозрачных материалов. Подвижный плунжер 248 также может изготавливаться из прозрачного материала так, чтобы позволять видеть шунт. Альтернативно вставляющий наконечник 214 и/или неподвижный наконечник 244 могут быть выполнены из прозрачных материалов, а подвижный плунжер 248 может выполняться из непрозрачного, ярко окрашенного материала, чтобы его положение было хорошо видно.
Из вышеописанных чертежей понятен ряд способов снижения давления в передней камере по настоящему изобретению. В одном из вариантов настоящего изобретения предлагается шунт для дренирования водянистой жидкости и устройство доставки, предназначенное для установки шунта. Шунт может быть выполнен с возможностью дренирования водянистой жидкости с заранее определенным расходом и далее с возможностью сопротивления интрузии микроорганизмов. После адекватной анестезии выбирают место для установки дренирующего шунта. Может делаться пилотный надрез, проходящий по внешней поверхности роговицы и который может проходить сквозь строму роговицы и далее проходить в переднюю камеру. Размеры пилотного отверстия определяются конкретным хирургом на основе хирургических показаний и анатомии конкретного пациента. Для формирования пилотного отверстия или подобного надреза могут использоваться игла, троакар, скальпель или любой другой из множества инструментов, известных офтальмологам. Шунт может устанавливаться в устройство доставки хирургом или шунт может устанавливаться в устройство доставки заранее, на стадии его изготовления. Хотя выше были указаны некоторые иллюстративные размеры шунта, следует понимать, что шунты могут изготавливаться различных размеров в соответствии с индивидуальной анатомией. Далее следует понимать, что могут применяться устройства доставки различных размеров для взаимодействия с шунтами разных размеров или же устройство доставки одного размера может использоваться для имплантации шунтов всех размеров. Когда шунт закреплен во вставляющем наконечнике устройства доставки, хирург подает устройство доставки к внешней поверхности роговицы. Когда устройство доставки достигает заранее определенного положения на роговице, шунт вводят в транскорнеальное положение с использованием механизмов устройства доставки для подачи и перемещения шунта. Когда шунт будет должным образом позиционирован и будет проходить сквозь роговицу, он сможет дренировать водянистую жидкость на поверхность роговицы. Правильное позиционирование шунта может быть подтверждено появлением видимой капельки водянистой жидкости на головке имплантированного устройства.
Следует понимать, что такое устройство может использоваться после таких процедур, которые приводят к повышению внутриглазного давления или могут быть полезны для временного исправления нарушений, характеризующихся повышенным внутриглазным давлением. В случае временного использования при операциях на сетчатке, удалении катаракты или прочих инвазивных офтальмологических операциях устройство имплантируется на срок от двух часов до одного месяца, или до стабилизации внутриглазного давления. Для лечения глаукомы у пациентов, страдающих диабетом, применяются постоянные или долговременные имплантации устройства по настоящему изобретению.
Следует понимать, что вышеприведенное описание с прилагаемыми чертежами является лишь примером настоящего изобретения и некоторых его иллюстративных вариантов. Следует понимать, что в различные компоненты и структуры шунта и устройства его доставки могут быть внесены различные изменения и модификации, не выходящие из объема настоящего изобретения, который определяется прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНТЕРПОЗИЦИОННЫЙ ОФТАЛЬМОЛОГИЧЕСКИЙ ИМПЛАНТАТ | 2016 |
|
RU2721299C2 |
| УСТРОЙСТВА РАСШИРЯЮЩИХСЯ ОФТАЛЬМОЛОГИЧЕСКИХ ИМПЛАНТАТОВ | 2013 |
|
RU2650203C2 |
| УСТРОЙСТВО, КОМПЛЕКТ И СПОСОБ ДЛЯ МАЛОИНВАЗИВНОЙ ХИРУРГИИ ГЛАУКОМЫ | 2021 |
|
RU2775705C1 |
| ШУНТИРУЮЩЕЕ УСТРОЙСТВО И СПОСОБ ЛЕЧЕНИЯ ГЛАУКОМЫ | 2000 |
|
RU2245697C2 |
| СИСТЕМА ДОСТАВКИ ГЛАЗНОГО ИМПЛАНТАТА | 2013 |
|
RU2636859C2 |
| УСТРОЙСТВО ДОСТАВКИ ВНУТРИГЛАЗНОГО ИМПЛАНТАТА И СПОСОБЫ ЕГО ИСПОЛЬЗОВАНИЯ | 2015 |
|
RU2728195C2 |
| ВНУТРИГЛАЗНЫЕ ИМПЛАНТАТЫ, СОДЕРЖАЩИЕ ПРОСТАМИД, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2650614C2 |
| ВНУТРИКАМЕРНЫЕ ИМПЛАНТАТЫ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ТЕРАПЕВТИЧЕСКОГО АГЕНТА | 2011 |
|
RU2565445C2 |
| ВНУТРИГЛАЗНЫЕ ИМПЛАНТАТЫ, СОДЕРЖАЩИЕ ПРОСТАМИДЫ | 2014 |
|
RU2666603C2 |
| СПОСОБ ЛЕЧЕНИЯ ПАТОЛОГИИ ГЛАЗА С ПОМОЩЬЮ ФОКУСИРОВАННОГО УЛЬТРАЗВУКА ВЫСОКОЙ ИНТЕНСИВНОСТИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2501539C2 |






Настоящее изобретение относится в целом к системам и способам снижения внутриглазного давления. Один из вариантов настоящего изобретения относится к имплантируемым устройствам для дренажа жидкости для снижения высокого внутриглазного давления при глаукоме. Предлагаются системы и способы для снижения внутриглазного давления при глаукоме и других заболеваниях. Системы по настоящему изобретению содержат шунт, вставляемый через прозрачную роговицу, и устройство доставки для установки шунта в транскорнеальное положение. Шунт имеет тело с головкой на одном конце и основанием на противоположном конце и канал, обеспечивающий проход водянистой жидкости из передней камеры на внешнюю поверхность роговицы. В канале установлен съемный фильтр для регулирования оттока водянистой влаги и для ограничения попадания микроорганизмов. Шунт, устройство его доставки и способы их использования адаптированы для установки дренажной системы через прозрачную роговицу. Отток водянистой влаги регулируется фильтрующей системой, без вовлечения механизмов заживления раны, что позволяет рассчитать прогнозируемую скорость оттока и избежать опасности, с одной стороны, гипотонии, а с другой стороны, недостаточного оттока. Фильтр образует извилистый путь, препятствующий проникновению бактерий. 7 н. и 23 з.п. ф-лы, 7 ил.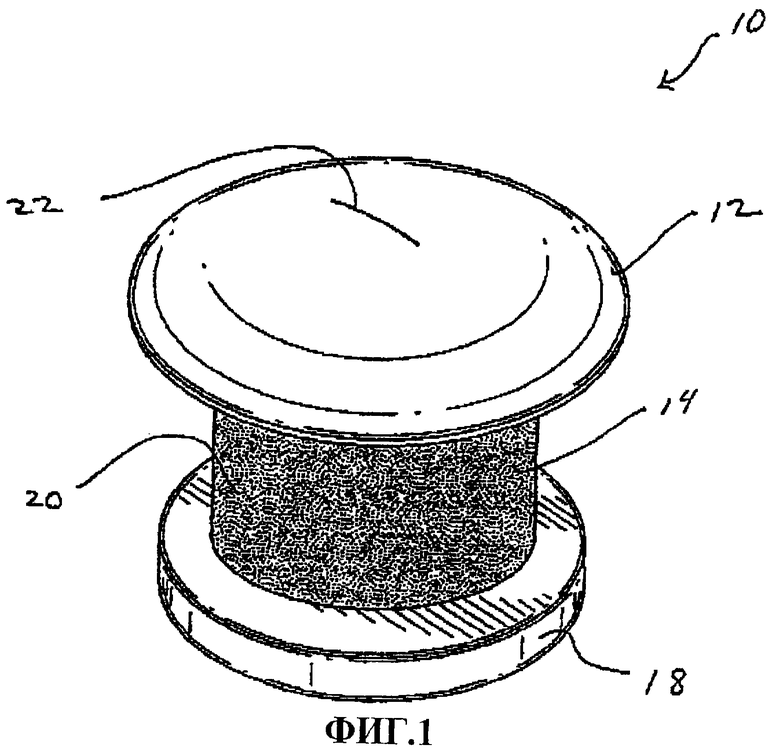
| US 5807302 А, 15.09.1998 | |||
| US 5743868 A, 28.04.1998 | |||
| US 5868697 А, 09.02.1999 | |||
| Имплантируемый магнитоуправляемый шунт | 1983 |
|
SU1159572A1 |
| US 6050999 A, 18.04.2000 | |||
| US 6186974 B1, 13.02.2001. | |||
Авторы
Даты
2005-10-20—Публикация
2001-01-05—Подача