Предпосылки изобретения
Пептиды, родственные бомбезину (Bn) млекопитающих, гастрин-рилизинг-пептид (GRP) и нейромедин В (NMB), обладают широким кругом биологических и фармакологических воздействий. Указанные воздействия включают в себя стимуляцию высвобождения многочисленных желудочно-кишечных гормонов и пептидов, стимуляцию секреции экзокринных желез, хемотаксиса, сокращения гладкой мышцы, эффекты в центральной нервной системе, такие как терморегуляция, поведенческие эффекты, поддержание циркадного ритма, ингибирование высвобождения TSH и чувства насыщения. Пептиды, родственные Bn, также функционируют как факторы роста во многих нормальных клетках (например, бронхиальных клетках, эндометриальных клетках стомы и клетках 3Т3) , а также неопластических клетках, таких как клетки мелкоклеточного рака легкого человека, клетки гепатоклеточной опухоли крыс, клетки простаты и клетки аденокарциномы молочной железы.
Последние исследования структуры-функции и клонирование показали, что по меньшей мере два класса рецепторов опосредуют действие пептидов, родственных Bn. Один класс-подтип, предпочтительно связывающий GRP (рецептор GRP или GRP-R), обладает высоким сродством к GRP и низким сродством к NMB, в то время как другой класс-подтип, предпочтительно связывающий NMB (рецептор NMB или NMB-R), обладает высоким сродством к NMB и низким сродством к GRP. Оба класса рецепторов широко представлены как в центральной нервной системе, так и в желудочно-кишечном тракте. До недавнего времени было неясно физиологическое значение пептидов, родственных Bn, в опосредовании различных процессов, и то, какой подтип рецепторов опосредует различные биологические воздействия пептидов, родственных Bn, о которых сообщалось.
Описано пять разных классов антагонистов Bn-рецептора. Jensen, R.Т. et al. Trends Pharmacol. Sci. 12: 13 (1991). Представители этого ряда классов обладают высокой эффективностью, большой продолжительностью действия и избирательностью по отношению к рецептору GRP и, таким образом, пригодны даже для определения роли GRP или рецепторов GRP в опосредовании различных физиологических явлений in vivo. Однако в настоящее время описано несколько антагонистов рецептора NMB, которые достаточно избирательны или эффективны. (Смотри, например, Coy, D., and Taylor, J., патент США 5462926). Кроме того, NMB был вовлечен в ингибирование рака легкого и глиомы. Cancer Res 1991 Oct 1, 51: 19, 5205-11; J. Cell Biochem. Suppl. 1996, 24: 237-46, Peptides 1995, 16: 6, 1133-40; J. Pharmacol. Exp. Ther. 1992 Oct 263: 1, 311-7), стимуляцию аппетита (Eur. J. Pharmacol. 1994 Dec 12, 271: 1 R7-9; Am. J. Physiol. 1997 Jan. 272: 1 Pt 2 R433-7; Pharmacol. Biochem. Behav. 1996 Aug 54: 4 705-11), стимуляцию секреции TSH (гипотиреоидизм) (Regul. Pept. 1996 Nov 14, 67: 1, 47-53) и ингибирование секреции альдостерона (гиперальдостеронизм) (Histol. Histopathol. 1996 Oct. 11: 4, 895-7). Таким образом, соединения согласно данному изобретению пригодны для исследования физиологической роли, которую играет NMB, и для разработки терапевтических композиций для лечения симптомов, связанных с NMB.
Как известно в данной области, агонисты и антагонисты соматостатина полезны при лечении различных медицинских состояний и заболеваний, таких как ингибирование пролиферации Н. pylori, акромегалия, рестеноз, болезнь Крона, системный склероз, наружная или внутренняя ложная киста поджелудочной железы и асцит, ВИПома, гиперплазия панкреатических островков, гиперинсулинизм, гастринома, синдром Золлингера - Эллисона, диарея, диарея, связанная со СПИДом, диарея, связанная с химиотерапией, склеродермия, синдром раздраженной толстой кишки, панкреатит, непроходимость тонкой кишки, гастроэзофагеальный рефлюкс, дуоденогастральный рефлюкс, и при лечении эндокринологических болезней и/или состояний, таких как синдром Кушинга, гонадотропинома, гиперпаратиреоз, болезнь Грейвса, диабетическая нейропатия, болезнь Педжета и поликистозное заболевание яичника; при лечении различных типов рака, таких как рак щитовидной железы, гепатома, лейкоз, менингиома, и состояний, связанных с раком, таких как раковая кахексия; при лечении таких состояний как гипотензия, такая как ортостатическая гипотензия и постпрандиальная гипотензия, и состояний с реакцией паники; аденом, секретирующих GH (акромегалия) и аденом, секретирующих TSH. Активация рецептора подтипа типа 2, но не типа 5, была связана с лечением аденом, секретирующих пролактин. Другими проявлениями, связанными с активацией подтипов соматостатина, являются ингибирование инсулина и/или глюкагона, и более конкретно - сахарный диабет, гиперлипидемия, нечувствительность к инсулину, синдром X, ангиопатия, пролиферативная ретинопатия, феномен «рассвета» и нефропатия; ингибирование секреции желудочной кислоты, и более конкретно - пептические язвы, кишечно-кожная и кожно-панкретиатическая фистула, демпинг-синдром, синдром водной диареи, острый или хронический панкреатит и опухоли, секретирующие желудочно-кишечные гормоны; ингибирование ангиогенеза, лечение воспалительных заболеваний, таких как артрит; хроническая реакция отторжения аллогенного трансплантата; пластическая операция на сосудах; предотвращение кровотечения при сосудистой трансплантации и желудочно-кишечного кровотечения. Агонисты соматостатина также можно использовать для снижения массы тела пациента. Соответственно, соединения согласно настоящему изобретению пригодны для вышеупомянутых способов.
Недавно сообщалось, что нативный соматостатин (SS), соматостатин-14 (SS-14), ингибировал перекрестное связывание 125I-GRP с белком с М.м. 120 кД в тритоновых экстрактах клеток 3Т3 и клеток мелкоклеточного рака легкого человека, которые, как известно, имеют рецепторы бомбезина. Недавние исследования также показали, что SS-14 также может слабо ингибировать связывание с рецепторами опиата, и последующие исследования взаимосвязи структура-функция привели к идентификации различных замещенных D-аминокислотами и замещенных ограниченными аминокислотами циклических аналогов соматостатина, которые функционируют как эффективные антагонисты опиоидного рецептора mu.
Все упоминаемые здесь патенты и публикации тем самым включены в виде ссылки в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к серии аналогов, обладающих уникальными структурными особенностями, и способу избирательного модулирования биохимической активности клеток, индуцированной соматостатином и/или нейромедином В.
В одном аспекте направлением данного изобретения является соединение формулы (1)

или его фармацевтически приемлемая соль, где α-азот каждой из АА1, AA2, АА3, АА3b, АА4, АА5, АА6, АА7, АА7b и АА8 независимо необязательно замещен (C1-4)алкилом, (С3-4алкенилом, (С3-4)алкинилом или (C1-6)алкил -С(О)-;
АА1 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aac, Aic, Arg, Asn, Asp, Dip, Gln, Glu, Hca, Hyp, Lys, Mac, Macab, Orn, Pro, Ser, Ser(Bzl), Thr, Thr(Bzl), Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, lia, Alla, Aba, Gba, Car, Ipa, laa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua, Рур и необязательно замещенной ароматической α-аминокислоты;
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, CN, (C1-6)алкила, (С2-6)алкенила, (С2-6)алкинила, (C1-6)алкоксигруппы, Bzl, O-Bzl и NR9R10;
АА2 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aic, Arg, Hca, His, Hyp, Pal, F5-Phe, Phe, Pro, Trp, и X0-Phe, Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, lia, Alla, Aba, Gba, Car, Ipa, Iaa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua и Рур;
АА3 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Tpa, Tmpa, Mac, Macab и необязательно замещенной ароматической α-аминокислоты;
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, CN, (C1-4)алкила, (С2-4)алкенила, (C2-4)алкинила, (C1-4)алкоксигруппы, Bzl, O-Bzl, NR9R10, Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, Iia, Alla, Aba, Gba, Car, Ipa, laa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua и Рур; АА3b отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Pal, 4-Pal, His, Arg, Nal, Trp, Bpa, F5-Phe, Phe, X0-Phe, R11, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala и Pala;
АА4 является D- или L- изомером необязательно замещенной аминокислоты или необязательно замещенной ароматической α-аминокислоты ;
где указанная необязательно замещенная аминокислота выбрана из группы, состоящей из Trp, Lys, Orn, hLys, цис-4-Acha, транс-4-Acha, транс-4-Amcha, 4-Pip-Gly, N-Met-Trp, β-Met-Trp, His, hHis, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и 4-Pip-Ala; где аминогруппа боковой цепи указанной необязательно замещенной аминокислоты необязательно замещена R3 и R4;
и где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, CN, (C1-4)алкила, (С2-4)алкенила, (C2-4)алкинила, Bzl, O-Bzl и NR9R10;
АА5 отсутствует, является R11, Aic, А3с, А4с, А5с, А6с, Abu, Aib, β-Ala, Bpa, Cha, Deg, Gaba,Ile, Leu, Nal, Nle, Pro, Sar, Ser, Ser(Bzl), Thr, Thr(Bzl), Trp, Val, Pal, F5-Phe, Phe, X0-Phe или необязательно замещенным D- или L- изомером аминокислоты, выбранный из группы, состоящей из 4-Pip-Gly, 4-Pip-Ala, цис-4-Acha, транс-4-Acha, транс-4-Amcha, hLys, Lys, Orn, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala и Pala; где аминогруппа боковой цепи указанной необязательно замещенной аминокислоты необязательно моно- или дизамещена R3 и R4;
АА6 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, необязательно замещенной ароматической α-аминокислоты, Cys, hCys, Pen, Tpa, Tmpa, Thr, Thr(Bzl), Ser, Ser(Bzl), hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala и Pala;
АА7 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, необязательно замещенной ароматической α-аминокислоты, А3с, А4с, А5с, А6с, Abu, Aib, Aic, β-Ala, Arg, Cha, Deg, Gaba, Ile, Leu, Nle, Pip, Pro, Sar, Ser, Ser (Bzl), Thr, Thr (Bzl), Val, Tic, Htic, Sala, Aala, Thza, Thia, Bal, Fala, Pala, hArg, Bip, Bpa, Dip, Pal, Sala и X0-Phe;
АА7b отсутствует или является D- или L-изомером аминокислоты, выбранной из группы, состоящей из R11, Bpa, Phe, F5-Phe, X0-Phe, Nal, Pro, Ser, Ser (Bzl), Thr, Thr (Bzl), Trp, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala и Pala;
AA8 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Маа, Maaab, Thr, Thr(Bzl), Ser, Ser(Bzl), Tyr, Phe(4-O-Bzl), F5-Phe и X5-Phe, и необязательно замещенной ароматической α- аминокислоты;
каждый из R1 и R2 независимо представляет собой Н, Е-, E(O)2S-, E(O)C-, EOOC-, R13 или отсутствует;
каждый из R3 и R4 независимо представляет собой (С1-12) алкил, (C2-12)алкенил, (C2-12)алкинил, фенил, нафтил, фенил-(С1-6)алкил, фенил-(C2-6)алкенил, фенил-(С2-6)алкинил, нафтил-(C1-6)алкил, нафтил-(С2-6)алкенил, нафтил-(С2-6)алкинил, (цикло(С3-7)алкил)-(C1-6)алкил, (цикло(С3-7)алкил)-(С2-6)алкенил, (цикло(С3-7)алкил)-(С2-6)алкинил, гетероциклил-(C1-4)алкил, гетероциклил-(С2-4)алкенил, гетероциклил-(C2-4)алкинил, 1-адамантил, 2-адамантил, 9-флуоренилметил, дициклопропилметил, диметилциклопропилметил или бензгидрил;
R5 является -OR6, -NR7R8 или отсутствует; где каждый R6, R7 и R8 независимо представляет собой Н, (C1-12)алкил, (С2-12)алкенил, (C2-12)алкинил, фенил, нафтил, фенил-(C1-6)алкил, фенил-(C2-6)алкенил, фенил-(С2-6)алкинил, нафтил-(C1-6)алкил, нафтил-(C2-6)алкенил, нафтил-(С2-6)алкинил, 1-адамантил, 2-адамантил, 9-флуоренилметил, дициклопропилметил, диметилциклопропилметил или бензгидрил;
каждый R9 и R10 независимо представляет собой Н, (C1-6)алкил, (С3-4)алкенил, (С3-4)алкинил, 1-адамантил или 2-адамантил;
R11 независимо для каждого случая является D- или L- аминокислотой формулы:

где каждый из m и n независимо равны 1, 2 или 3, и р равно 0, 1 или 2;
R12 независимо для каждого случая является необязательно замещенным фрагментом формулы
R13 представляет собой фрагмент формулы:

где каждый из q, r, s и t независимо равен 0, 1, 2, 3, 4 или 5;
R19 отсутствует, означает Н, NH2, ОН, (C1-6)гидроксиалкил, N(R27R28), SO3Н или необязательно замещенный фрагмент, выбранный из группы, состоящей из гетероциклила, фенила и нафтила,
где необязательно замещенный фрагмент, определенный для R19, необязательно замещен одним или большим количеством заместителей, выбранных независимо для каждого случая из группы, состоящей из галогена, NO2, ОН, (C1-6)алкила, (С2-6)алкенила, (С2-6)алкинила, (C1-6)алкоксигруппы, NH2, моно- или ди- (С1-6)алкиламиногруппы, Bzl и O-Bzl;
R20 является О или отсутствует;
R21 означает (С1-6)алкил или отсутствует;
R22 является N, О, С или СН;
R23 означает (С1-6)алкил или отсутствует;
R24 является N, СН или С;
R25 является NH, О или отсутствует;
R26 является SO2, CO или СН;
каждый из R27 и R28 независимо является Н или (C1-6)алкилом;
Е независимо для каждого случая представляет собой необязательно замещенный фрагмент, выбранный из группы, состоящей из (С1-12)алкила, (С2-12)алкенила, (C2-12)алкинила, фенила, нафтила, фенил-(C1-6)алкила, фенил-(С2-6)алкенила, фенил-(С2-6)алкинила, нафтил-(C1-6)алкила, нафтил-(С2-6)алкенила, нафтил-(С2-6)алкинила, (цикло(С3-7)алкил)-(C1-6)алкила, (цикло-(С3-7)алкил)-(С2-6)алкенила, (цикло(С3-7)алкил)-(C2-6)алкинила, гетероциклил-(C1-4)алкила, гетероциклил-(С2-4)алкенила, гетероциклил-(С2-4)алкинила, 1-адамантила, 2-адамантила, дициклопропилметила, диметилциклопропилметила, 9-флуоренилметила и бензгидрила;
где необязательно замещенный фрагмент, охарактеризованный для Е, необязательно замещен одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, ОН, Bzl, O-Bzl, NO2, CN, COOH и SH;
X0 означает галоген, NO2, ОН, (C1-6)алкил, (C2-6)алкоксигруппу, моно- или ди- (C1-6)алкиламиногруппу, Bzl, O-Bzl, NR9R10 или CN;
X1 означает Н, (C1-6)алкил, (C2-6)алкенил, (С2-6)алкинил, индолил, имидазолил, 1-нафтил, 3-пиридил, необязательно замещенный в кольце бензил или фрагмент, который соответствует группе боковой цепи Arg, Leu, Gln, Lys, Tyr, His, Thr, Trp, Phe, Val, Ala, Lys или His;
где указанный необязательно замещенный в кольце бензил необязательно замещен одним или большим количеством заместителей, выбранных из группы, состоящей из галогена, ОН, (C1-6)алкоксигруппы, моно- или ди- (C1-6)алкиламиногруппы, (C1-4)алкила, (С2-4)алкенила, (С2-4)алкинила и NR9R10;
каждый из X2 и X3 независимо представляет собой Н, галоген, ОН, =O, =S, (C1-12)алкил, (C2-12)алкенил, (C2-12)алкинил, фенил, нафтил, фенил-(C1-6)алкил, фенил-(С2-6)алкенил, фенил-(С2-6)алкинил, нафтил-(C1-6)алкил, нафтил-(С2-6)алкенил, нафтил-(С2-6)алкинил, (цикло(С3-7)алкил)-(C1-6)алкил, (цикло(С3-7)алкил)-(С2-6)алкенил, (цикло(С3-7)алкил)-(С2-6)алкинил, гетероциклил-(C1-4)алкил, гетероциклил-(С2-4)алкенил, гетероциклил-(C2-4)-алкинил, 1-адамантил, 2-адамантил, дициклопропилметил или диметилциклопропилметил;
X4 означает Н, ОН или NH2 и
X5 означает галоген, NO2, СН3, ОН, Bzl или O-Bzl;
при условии, что
присутствуют, по меньшей мере, шесть аминокислотных остатков;
в том случае, когда АА3 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Тра или Tmpa, и АА6 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Тра или Tmpa, АА3 и АА6 связаны дисульфидной связью;
в том случае, когда АА1 или АА3 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Mac или Macab, АА8 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Маа и Maaab, и когда АА8 является D- или L-изомером аминокислоты, выбранной из группы, состоящей из Маа и Maaab, АА1 или АА3 является D- или L-изомером Mac или Macab, и АА1 или АА3 связаны дисульфидной связью с АА8;
АА2 может быть D- или L-Hca только в том случае, когда АА1 отсутствует;
в том случае, когда один из R1 или R2 является E(O)2S-, Е(O)С-, ЕООС- или R13, другой является Н;
если R5 отсутствует, то один из R1 или R2 также отсутствует, и N - концевая аминокислота и С - концевая аминокислота вместе образуют амидную связь;
если один из X2 или X3 представляет собой С=O или C=S, то другой отсутствует; и указанное соединение формулы (I) не имеет формулу:
D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Ac-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
L-4-NO2-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Ac-L-4-NO2-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Hca-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
D-Dip-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
D-4-NO2-Phe-Phe(4-O-Bzl)-цикло(D-Cys-D-Trp-Lys-Cys)Cha-Nal-NH2 или
D-4-NO2-Phe-цикло(D-Cys-Phe(4-O-Bzl)-D-Trp-Lys-Cys)-Val-Tyr-NH2.
В другом аспекте направлением данного изобретения является фармацевтическая композиция, содержащая одно или большее количество соединений формулы (I), определение которых приведено выше, и фармацевтически приемлемый носитель.
В еще одном аспекте направлением данного изобретения является способ, предназначенный для того, чтобы вызвать агонистическое действие со стороны одного или большего количества подтипов рецепторов соматостатина и/или нейромедина В у субъекта, которому это необходимо, который включает в себя введение соединения формулы (I), которое описано выше, указанному субъекту.
В еще одном аспекте данное изобретение направлено на способ, позволяющий вызвать антагонистическое действие со стороны одного или большего количества подтипов рецепторов соматостатина и/или нейромедина В у субъекта, которому это необходимо, который включает в себя введение соединения формулы (I), которое описано выше, указанному субъекту.
В следующем аспекте данное изобретение направлено на способ связывания одного или большего количества подтипов рецепторов соматостатина и/или нейромедина В у субъекта, который в этом нуждается, который включает в себя введение соединения формулы (I), которое описано выше, указанному пациенту.
В еще одном дополнительном аспекте данное изобретение направлено на применение одного или большего количества соединений формулы I, для связывания с рецептором нейромедина В или с одним или большим количеством рецепторов соматостатина, как при выполнении анализа in vitro, так и in vivo.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Специалист поймет, что некоторые заместители, перечисленные в данном изобретении, могут обладать пониженной химической стабильностью при комбинировании с другим заместителем или с гетероатомами в соединении. Такие соединения с пониженной химической стабильностью не являются предпочтительными.
В общем, соединения формулы (I) можно получить посредством способов, которые включают в себя способы, известные в области химии для получения соединений. Некоторые способы производства соединений формулы (I) предоставлены в качестве дополнительных частей изобретения и иллюстрируются схемами реакций и примерами, включенными в данную работу.
В указанных выше структурных формулах и во всей настоящей заявке следующие термины имеют указанные значения, если не оговорено особо.
Подразумевается что термин «алкил» включает в себя определения алкильных групп указанной длины либо в прямой, либо в разветвленной конфигурации. Примерами таких алкильных групп являются метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, пентил, изопентил, гексил, изогексил и тому подобное. В том случае, когда в определение включен термин С0-алкил, подразумевается, что он означает одинарную ковалентную связь.
Подразумевается, что термин «алкоксигруппа» включает в себя определения алкоксигрупп указанной длины либо в прямой, либо в разветвленной конфигурации. Примерами таких алкоксигрупп являются метокси-, этокси-, пропокси-, изопропокси-, бутокси-, изобутокси-, трет-бутокси-пентокси-, изопентокси-, гексокси-, изогексоксигруппа и тому подобное.
Подразумевается, что термин «галоген» или «атом галогена» включает в себя атомы галогенов: фтора, хлора, брома и йода.
Подразумевается, что термин «циклоалкил» включает в себя моноциклоалкильную группу или бициклоалкильную группу с указанным количеством атомов углерода, известную специалистам в данной области.
Термин «диметилциклопропилметил» относится к структуре

Термин «арил» подразумевает включение ароматических колец, известных в данной области, которые могут быть моноциклическими, бициклическими или трициклическими, такими как фенил, нафтил и антрацил.
Термин «гетероцикл» включает в себя моноциклические и бициклические системы, имеющие один или более гетероатомов, таких как кислород, азот и/или сера. Кольцевые системы могут быть ароматическими, (например, пиридин, индол, хинолин, пиримидин, тиофен (также известный как тиенил), фуран, бензотиофен, тетразол, дигидроиндол, индазол, N-формилиндол, бензимидазол, тиазол и тиадиазол). Кольцевые системы также могут быть неароматическими (например, пирролидин, пиперидин, морфолин и тому подобное).
Специалист химик поймет, что некоторые комбинации заместителей, содержащих гетероатомы, перечисленные в данном изобретении, определяют соединения, которые будут менее стабильны при физиологических условиях. Соответственно такие соединения менее предпочтительны.
Согласно данному здесь определению некоторые остатки или фрагменты в альтернативных случаях отсутствуют в некоторых пептидах согласно изобретению. Там, где связь(зи) с таким остатком или фрагментом указана сплошной линией, понимается, что в том случае, когда остаток или фрагмент отсутствует, связь образована между оставшимся N-концевым остатком или фрагментом(ами) и оставшимся С-концевым остатком или фрагментом(ами). Там, где связь(зи) с таким остатком или фрагментом указана пунктирной линией(ями) понимается, что в том случае, когда остаток или фрагмент отсутствует, не образуется связи между оставшимся N-концевым остатком или фрагментом(ами) и оставшимся С-концевым остатком или фрагментом(ами). Например, в следующей структуре:
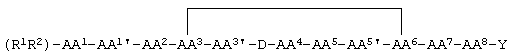
отсутствие АА1 в результате приводит к

и отсутствие АА1' в результате приводит к

В следующей структуре:

отсутствие R23 в результате приводит к

В том случае, когда химическая структура в используемом здесь виде имеет стрелку, выходящую из нее, стрелка указывает точку связывания. Например, структура

является пентильной группой. В том случае, когда линия нарисована проходящей сквозь циклический фрагмент, линия указывает на то, что заместитель может быть связан с циклическим фрагментом в любых доступных точках связывания. Например,

означает, что заместитель X может быть связан в орто-, мета- или пара-положении по отношению к точке связывания. Подобным образом, в том случае, когда линия нарисована проходящей сквозь бициклический или трициклический фрагмент, линия указывает на то, что заместитель может быть связан с бициклическим или трициклическим фрагментом в любых доступных точках связывания в любом из колец.
Для всех изображенных здесь формул N-конец расположен слева и С- конец - справа, в соответствии с традиционным изображением полипептидной цепи.
Символ АА1, АА2 или подобный в последовательности пептида означает аминокислотный остаток, т.е. =N-CH(R)-СО-, когда он расположен на N-конце, или -NH-CH(R)-СО-, когда он находится не на N-конце, где R означает боковую цепь данного аминокислотного остатка. Таким образом, R для Val представляет собой -СН(СН3)2. Также в том случае, когда аминокислотный остаток оптически активен, он находится в форме L-конфигурации, которая подразумевается, если D-форма не указана особо.
Если не оговорено особо, там, где на N-конце появляется ацетильная группа, подразумевается, что ацетильная группа предпочтительнее связана с α-азотом, а не с боковой цепью N-концевой аминокислоты. Например, структура аминокислотной последовательности Ac-4-NO2-Phe-AA2-AAЗ- представляет собой
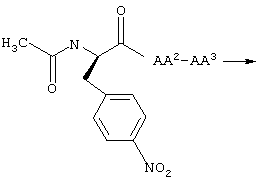
Там, где заместитель Y, например, имеет вид -OR5 на С-конце пептида, подразумевается, что -OR5 связан непосредственно с углеродом карбонила вместо группы -ОН.
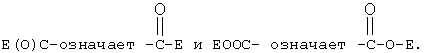
То, что обозначается термином «ароматическая α-аминокислота», представляет собой аминокислотный остаток формулы 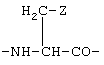
где Z означает фрагмент, содержащий ароматическое кольцо. Примеры Z включают в себя, но не ограничены этим, бензольное или пиридиновое кольцо и следующие структуры без заместителя, или с одним, или большим количеством заместителей Х в ароматическом кольце (где Х независимо для каждого случая является галогеном, NO2, СН3, ОН, Bzl или O-Bzl):
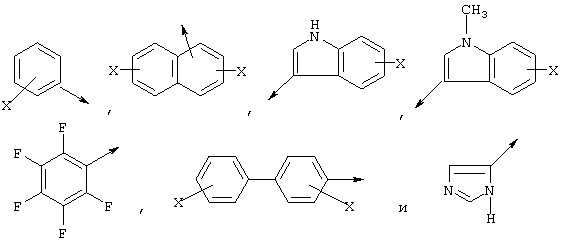
Другими примерами ароматической α-аминокислоты согласно изобретению является замещенный His, такой как MeHis, His(τ-Ме) или His(π-Ме).
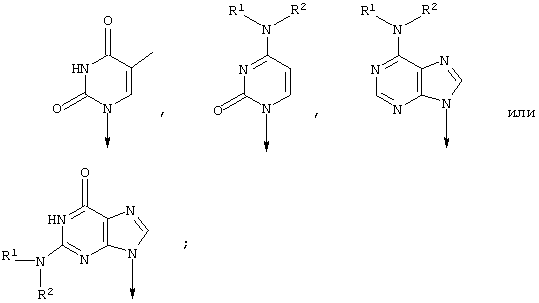
То, что подразумевается под термином «основание нуклеиновой кислоты», является необязательно замещенным фрагментом нуклеиновой кислоты формулы:
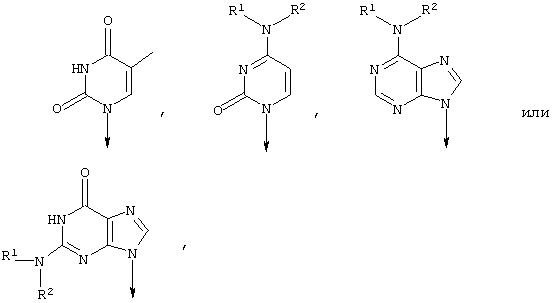
где R1 и R2 представляют собой радикалы, которые определены в формуле изобретения.
В некоторых вариантах изобретения аминогруппа боковой цепи одной или большего количества аминокислот необязательно моно- или дизамещена R3 и R4.
Например, результат введения заместителя R3 в аминогруппу боковой цепи 4-Pip-Gly дал бы следующую структуру:

Соединения согласно настоящему изобретению имеют по меньшей мере один асимметричный центр. В молекуле могут присутствовать дополнительные асимметричные центры, в зависимости от природы разных заместителей в молекуле. Каждый такой асимметричный центр будет давать два оптических изомера, и подразумевается, что все такие оптические изомеры в виде отдельных очищенных или частично очищенных оптических изомеров, их рацемических смесей или диастереометрических смесей включены в рамки настоящего изобретения.
Данные соединения, как правило, можно выделить в форме их фармацевтически приемлемых кислотно-аддитивных солей, таких как соли, полученные с использованием неорганических и органических кислот. Примерами таких кислот являются соляная, азотная, серная, фосфорная, муравьиная, уксусная, трифторуксусная, пропионовая, малеиновая, янтарная, D-винная, L- винная, малоновая, метансульфоновая и тому подобное. Кроме того, некоторые соединения, содержащие кислотную функциональную группу, такую как карбоксильную группу, можно выделить в форме их неорганических солей, в которых противоион может быть выбран из натрия, калия, лития, кальция, магния и тому подобного, а также в форме органических оснований.
Фармацевтически приемлемые соли образуют, используя примерно 1 эквивалент соединения формулы (I) и обеспечивая его контакт примерно с 1 эквивалентом подходящей соответствующей кислоты, соль которой требуется получить. Получение и выделение полученной в результате соли хорошо известны специалистам в данной области.
Соединения согласно данному изобретению можно вводить пероральным, парентеральным (например, внутримышечная, внутрибрюшинная, внутривенная или подкожная инъекция, или имплантат), назальным, вагинальным, ректальным, сублингвальным или местным путями введения, и можно приготовить в композиции с фармацевтически приемлемыми носителями, чтобы обеспечить дозированные лекарственные формы, подходящие для каждого пути введения. Таким образом, в рамки данного изобретения включены фармацевтические композиции, содержащие в качестве активного ингредиента по меньшей мере одно соединение формулы (I) в ассоциации с фармацевтически приемлемым носителем.
Твердые дозированные формы для перорального введения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение смешано по меньшей мере с одним инертным фармацевтически приемлемым носителем, таким как сахароза, лактоза или крахмал. Такие дозированные формы также могут содержать - и это является обычной практикой - дополнительные вещества, отличные от таких инертных разбавителей, например смазывающие агенты, такие как стеарат магния. В случае капсул, таблеток и пилюль дозированные формы также могут содержать буферные средства. Таблетки и пилюли, кроме того, могут быть приготовлены в энтеросолюбильных покрытиях.
Жидкие дозированные формы для перорального введения включают в себя фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры, содержащие инертные разбавители, обычно используемые в данной области, такие как вода. Кроме таких инертных разбавителей, композиции также могут включать в себя адъюванты, такие как увлажняющие средства, эмульгирующие и суспендирующие агенты, и подсластители, корригенты и отдушки.
Препараты для парентерального введения согласно данному изобретению включают в себя стерильные водные и неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или наполнителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и пригодные для инъекции сложные органические эфиры, такие как этилолеат. Такие дозированные формы также могут содержать адъюванты, такие как консерванты, увлажняющие, эмульгирующие и диспергирующие средства. Дозированные формы можно стерилизовать, например, фильтрованием через фильтры, задерживающие бактерии, путем включения стерилизующих средств в композиции, облучением композиций или нагреванием композиций. Дозированные формы также можно производить в виде стерильных твердых композиций, которые можно растворять в стерильной воде, или какой-либо другой стерильной, пригодной для инъекции среде непосредственно перед использованием.
Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые могут содержать кроме активного вещества, наполнители, такие как масло какао или воск для суппозиториев.
Композиции для назального или сублингвального введения также готовят со стандартными наполнителями, хорошо известными в данной области.
Кроме того, соединения согласно данному изобретению можно вводить в виде композиции длительного высвобождения, такой как композиции, описанные в следующих патентах. В патенте США No. 5672659 сообщается о композициях длительного высвобождения, содержащих биоактивное средство и сложный полиэфир. Патент США No. 5595760 знакомит с композициями длительного высвобождения, содержащими биоактивное средство в гелеобразной форме. Заявка на выдачу патента США №08/929363, зарегистрированная 9 сентября 1997 г., знакомит с полимерными композициями длительного высвобождения, содержащими биоактивное средство и хитозан. Заявка на патент США №08/740778, зарегистрированная 1 ноября 1996, знакомит с композициями длительного высвобождения, содержащими биоактивное средство и циклодекстрин. Заявка на патент США №09/015394, зарегистрированная 29 января 1998, знакомит с абсорбируемыми композициями длительного высвобождения биоактивного средства. Сообщения упомянутых выше патентов и заявок включены здесь в виде ссылки.
В общем, эффективная доза активного ингредиента в композициях согласно данному изобретению может варьировать; однако необходимо, чтобы количество активного ингредиента было таким, чтобы была получена подходящая форма дозирования. Выбранная доза зависит от требуемого терапевтического действия, пути введения и от продолжительности лечения, и все это относится к области знаний специалиста в данной области. Как правило, человеку и другим животным, например млекопитающим, вводят уровни доз от 0,0001 до 100 мг/кг массы тела ежедневно.
Предпочтительные пределы дозы составляют от 0,01 до 10,0 мг/кг массы тела ежедневно, которую можно вводить в виде однократной дозы и разделить на многократные дозы или давать при непрерывном введении.
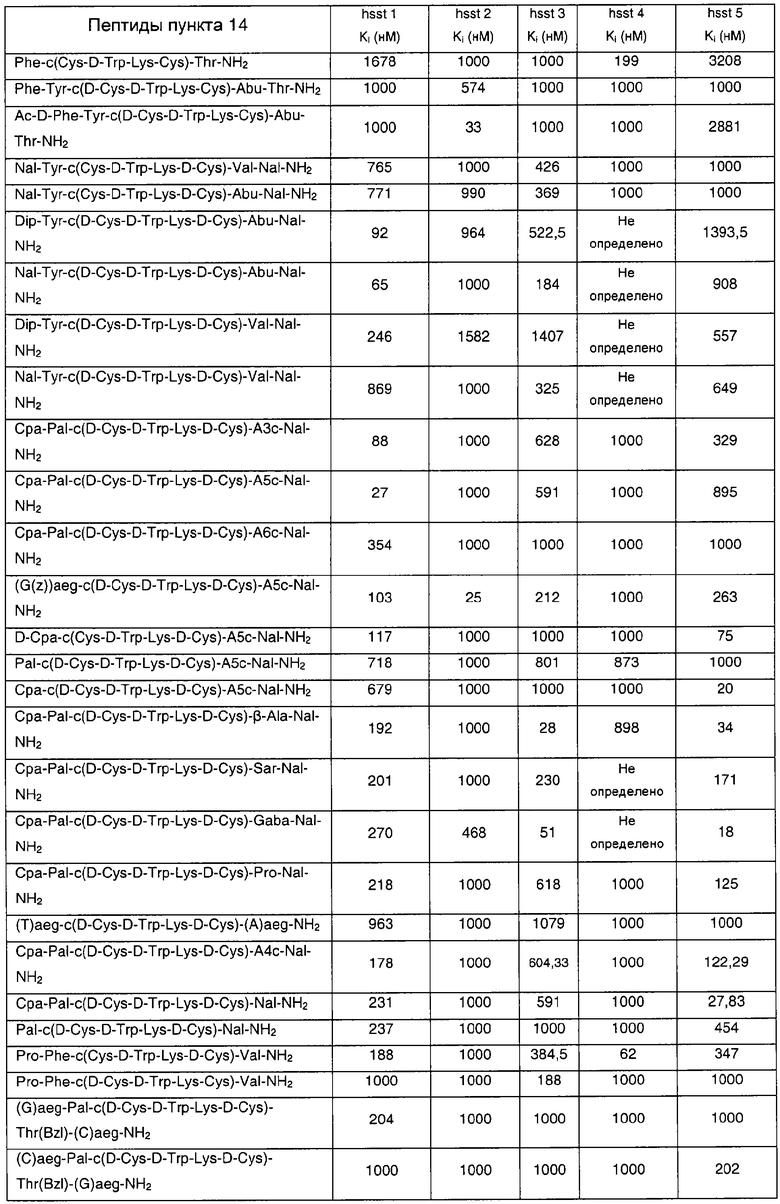
Соединения согласно настоящему изобретению могут быть и были оценены по их способности связываться с рецептором подтипа соматостатина в соответствии со следующими анализами.
Аффинность соединения по отношению к подтипам рецепторов соматостатина человека с 1 по 5 (sst1, sst2, sst3, sst4 и sst5, соответственно) определяли посредством измерения ингибирования связывания [125I-Tyr]SRIF-14 с клетками СНО - К1, трансфицированными подтипом рецептора sst.
Ген рецептора sst1 человека клонировали в виде геномного фрагмента. Фрагмент PstI-XmnI длиной 1,5 т.п.н., содержащий 100 п.н. 5'-нетранслируемого района, 1,17 т.п.н. полного кодирующего района и 230 п.н. 3'-нетранслируемого района, модифицировали добавлением линкера BglII. Полученный в результате фрагмент ДНК субклонировали в сайте BamHI плазмиды pCMV - 81, чтобы получить экспрессирующую плазмиду млекопитающих (предоставлена доктором Graeme Bell, University of Chicago, Chicago, IL). Линию клональных клеток, стабильно экспрессирующих рецептор sst1, получали посредством трансфекции клеток СНО - К1 (Американская коллекция типов культур, Manassas, VA) («АТСС»), используя способ совместной преципитации фосфатом кальция. Плазмиду pRSV-neo (АТСС) включали в качестве селектируемого маркера. Селекцию линий клональных клеток проводили в среде RPMI 1640 (Sigma Chemical Co., St. Louis, МО), содержащей 0,5 мг/мл генетицина (Gibco BRL, Grand Island, NY), клонировали по кольцевой схеме и размножали для получения культуры.
Ген рецептора соматостатина sst2 человека, выделенный в виде BamHI-HindIII-фрагмента геномной ДНК длиной 1,7 т.п.н. и субклонированный в плазмидном векторе pGEM3Z (Promega), был любезно предоставлен Dr. G. Bell (University of Chicago, Chicago, IL). Вектор, экспрессирующий в клетках млекопитающих, конструировали посредством встраивания BamHI-HindIII-фрагмента длиной 1,7 т.п.н. в совместимые сайты рестрикции эндонуклеазами в плазмиде pCMV5. Линию клональных клеток получали путем трансфекции клеток СНО-К1, используя способ совместной преципитации фосфатом кальция. Плазмиду pRSV-neo включали в качестве селектируемого маркера.
Ген sst3 человека выделяли в геномном фрагменте, и полная кодирующая последовательность была заключена в пределах BamHI/HindIII-фрагмента длиной 2,4 т.п.н. Экспрессирующую плазмиду млекопитающих pCMV-h3 конструировали посредством встраивания NcoI-HindIII-фрагмента длиной 2,0 т.п.н. в EcoR1-сайт вектора pCMV после модификации концов и добавления линкеров EcoR1. Линию клональных клеток, стабильно экспрессирующих рецептор sst3, получали путем трансфекции клеток СНО-К1 (АТСС), используя способ совместной преципитации фосфатом кальция. Плазмиду pRSV-neo (АТСС) включали в качестве селектируемого маркера. Селекцию линий клональных клеток проводили в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), клонировали по кольцевой схеме и размножали для получения культуры.
Плазмида pCMV-HX, экспрессирующая рецептор sst4 человека, была предоставлена Dr. Graeme Bell (University of Chicago, Chicago, IL). Вектор содержит геномный NheI-NheI-фрагмент длиной 1,4 т.п.н., кодирующий sst4, 456 п.н. 5'-нетранслируемого района и 200 п.н. 3'-нетранслируемого района, клонированный в сайтах Xbal/EcoRl плазмиды PCMV-HX. Линию клональных клеток, стабильно экспрессирующих рецептор sst4, получали трансфекцией клеток СНО-К1 (АТСС), используя способ совместной преципитации фосфатом кальция. Плазмиду pRSV-пео (АТСС) включали в качестве селектируемого маркера. Селекцию линий клональных клеток проводили в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), клонировали по кольцевой схеме и размножали для получения культуры.
Ген sst5 человека был получен ПЦР с использованием в качестве матрицы геномного клона λ и любезно предоставлен Dr. Graeme Bell (University of Chicago, Chicago, IL). Полученный в результате фрагмент ПЦР длиной 1,2 т.п.н. содержал 21 пару оснований 5'-нетранслируемого района, полный кодирующий район и 55 п.н. 3'-нетранслируемого района. Клон встраивали в EcoR1-сайт плазмиды pBSSK(+). Вставку извлекали в виде HindIII-XbaI-фрагмента длиной 1,2 т.п.н для субклонирования в экспрессирующем векторе млекопитающих pCVM5. Линию клональных клеток, стабильно экспрессирующих рецептор SST5, получали трансфекцией клеток СНО-К1 (АТСС), используя способ совместной преципитации фосфатом кальция. Плазмиду pRSV-neo (АТСС) включали в качестве селектируемого маркера. Селекцию линий клональных клеток проводили в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), клонировали по кольцевой схеме и размножали для получения культуры.
Клетки СНО-К1, стабильно экспрессирующие один из рецепторов sst человека, выращивают в RPMI 1640, содержащей 10% фетальной сыворотки теленка и 0,4 мг/мл генетицина. Клетки собирают с помощью 0,5 мМ ЭДТА и центрифугируют при 500 g в течение примерно 5 минут при температуре около 4°С. Осадок ресуспендируют в 50 мМ гидрохлориде трис [гидроксиметил] аминометана, рН=7,4, при 25°С («трис-буфер») и дважды центрифугируют при 500 g примерно в течение 5 минут при температуре около 4°С. Клетки лизируют обработкой ультразвуком и центрифугируют при 39000 g примерно в течение 10 минут при температуре около 4°С. Осадок ресуспендируют в таком же буфере и центрифугируют при 50000 g примерно в течение 10 минут при температуре около 4°С и мембраны в полученном в результате осадке хранят при -80°С.
Эксперименты по конкурентному ингибированию связывания [125I-Tyr11]SRIF-14 проводят в повторах в 96-луночных полипропиленовых планшетах. Мембраны клеток (10 мкг белка/лунку) инкубируют с [125I-Tyr11]SRIF-14 (Dr. Tom Davis, Univ. Of Arizona, Tuscon, AZ) (0,05 нМ) примерно в течение 60 минут при температуре около 37°С в 50 мМ HEPES, 0,2% БСА, 2,5 мМ MgCl2.
Связанный и свободный [125I-Tyr11]SRIF-14 сразу же разделяют путем фильтрации через фильтровальную пластину из стекловолокна GF/C (Unifilter, Packard, Meriden, CT), предварительно смоченную 0,3% полиэтиленимином (P.E.I), используя устройство для сбора клеток Filtermate 196 (Packard). Фильтры промывают 50 мМ трис-HCl при температуре около 0-4°С примерно в течение 4 секунд и анализируют радиоактивность, используя счетчик Packard Top Count.
Значение специфичного связывания получают вычитанием неспецифичного связывания (определяемого в присутствии 0,1 мкМ SRIF-14) из суммарного связывания. Результаты связывания анализируют посредством анализа нелинейной регрессии с помощью компьютера (Data Analysis Toolbox, v.1.0, Molecular Design Limited, San Leandro, CA), и определяют значения константы ингибирования (Ki).
Является ли соединение данного изобретения агонистом SST или антагонистом соматостатина, определяют при следующем анализе.
Функциональный анализ. Ингибирование внутриклеточной продукции цАМФ.
Клетки СНО-К1, экспрессирующие подтипы рецепторов соматостатина (SRIF-14) человека, высевают в 24-ячеечные чашки для культур ткани в среду RPMI 1640 с 10% фетальной сыворотки теленка (FCS). Среду меняют за день до эксперимента.
Клетки при 105 клеток/лунку 2 раза промывают 0,5 мл среды RPMI 1640. Добавляют свежую среду RPMI 1640 с 0,2% БСА и с добавлением 0,5 мМ 3-изобутил-1-метилксантина («IBMX»), и клетки инкубируют примерно в течение 5 минут при температуре около 37°С. Продукцию циклического АМФ стимулируют добавлением 1 мМ форсколина («FSK») (Sigma Chemical Co., St. Louis, МО) примерно в течение 15-30 минут при температуре около 37°С.
Агонистическое действие соединения измеряют при одновременном добавлении FSK (1 мкМ), SRIF-14 (Bachem, Torrence, CA), (от 10-12 до 10-6 М) и тестируемого соединения (от 10-10 до 10-5 M). Антагонистическое действие соединения измеряют при одновременном добавлении FSK (1 мкМ) , SRIF-14 (от 1 до 10 нМ) и тестируемого соединения (от 10-10 до 10-5 M).
Реакционную среду удаляют и добавляют 200 мл 0,1 N HCl. цАМФ измеряют, используя способ радиоиммуноанализа (набор FlashPlate SMP001A, New England Nuclear, Boston).
Соединения согласно настоящему изобретению могут быть и были оценены по их способности связываться с рецептором нейромедина В, в соответствии со следующим анализом.
Культура клеток. Клетки Balb 3Т3, экспрессирующие рецептор NMB крыс, получили от Dr. R.T. Jensen (National Institutes of Health, Bethesda, MD) и культивировали в среде Игла, модифицированной Дульбекко (DMEM), содержащей 10% фетальной сыворотки теленка, 0,5 мг/мл G418 (Gibco). Клетки поддерживали при 37°С во влажной атмосфере 5% CO2/95% воздуха.
Связывание радиолиганда. Мембраны для исследования связывания радиолиганда получали гомогенизацией клеток в 20 мл ледяного 50 мМ трис-HCl в гомогенизаторе Brinkman Polytron (Westbury, NY) (установка 6, 15 сек). Гомогенаты дважды промывали центрифугированием (39000 g/10 мин), и конечные осадки повторно суспендировали в 50 мМ трис - HCl, содержащем 5,0 мМ MgCl2 и 0,1% БСА. Для анализа аликвоты (0,4 мл) инкубировали с 0,05 нМ [125I-Tyr4]бомбезина (2200 кюри/ммоль, New England Nuclear, Boston, MA) в присутствии и без 0,05 мл немеченных конкурирующих тестируемых пептидов. После инкубации (30 минут, 4°С) , связанный [125I-Tyr4]бомбезин отделяли от свободного быстрым фильтрованием через фильтры GF/C (Brandel, Gaithersburg, MD), которые предварительно были замочены в 0,3% полиэтиленимине. Затем фильтры промывали три раза 5-миллилитровыми аликвотами ледяного 50 мМ трис-HCl, и связанную радиоактивность, захваченную на фильтрах, посчитывали гамма-спектрометрией (Wallac LKB, Gaithersburg, MD). Специфичное связывание определяли как общее связавшееся количество [125I-Tyr4]бомбезина минус количество, связавшееся в присутствии 1000 нМ нейромедина В (Bachem, Torrence, CA).
Один вариант способа включает в себя стадию контактирования клеток с пептидом формулы (2):

или его фармацевтически приемлемой солью,
где АА1 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aac, Aic, Arg, Asn, Asp, Dip, Gln, Glu, Hyp, Lys, Mac, Macab, Orn, Pip, Pro, Ser, Ser(Bzl), Thr, Thr(Bzl), Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, lia, Alla, Aba, Gba, Car, Ipa, laa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua, Рур и необязательно замещенной ароматической α-аминокислоты;
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, выбранных из группы, состоящей из галогена, NO2, ОН, CN, (C1-6)алкила, (С2-6)алкенила, (С2-6)-алкинила и NR9R10;
АА2 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aic, Arg, Нса, His, Hyp, Pal, Fs-Phe, Phe, Pro, Trp, X°-Phe, Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, Iia, Alla, Aba, Gba, Car, Ipa, laa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua и Рур;
АА3 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Тра и Tmpa;
АА4 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Trp, N-Met-Trp, β-Met-Trp, His, hHis, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и необязательно замещенной ароматической α-аминокислоты,
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, (C1-4)алкила, (С2-4)алкенила, (С2-4)алкинила, Bzl, O-Bzl и NR9R10;
АА5 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из 4-Pip-Gly, 4-Pip-Ala, цис-4-Acha, транс-4-Acha, транс-4-Amcha, hLys, Lys, Orn, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala и Pala,
где аминогруппа боковой цепи указанной аминокислоты необязательно моно- или дизамещена R3 и R4;
АА6 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Tpa и Tmpa;
AA7 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aic, А3с, А4с, А5с, А6с, Abu, Aib, β-Ala, Arg, Bpa, Cha, Deg, Gaba, His, Ile, Leu, Nal, Nle, Pal, Phe, F5-Phe, Pro, Sar, Ser, Ser(Bzl), Thr, Thr(Bzl), Trp, N-Me-Trp, Val, N-Me-Val, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и X0-Phe;
АА8 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, необязательно замещенной ароматической α-аминокислоты, Маа, Maaab, Ser, Ser(Bzl), Thr, Thr(Bzl), Tyr, Phe(4-O-Bzl), Fs-Phe и X5-Phe;
R13 представляет собой фрагмент в соответствии с формулой:

где R21 означает (С1-4)алкил и s равно 1, 2, 3 или 4;
Х0 означает галоген, NO2, СН3, ОН, Bzl, O-Bzl или CN;
при условии, что присутствует по меньшей мере одна из АА7 или АА8.
Другой вариант способа включает в себя стадию контактирования клеток с пептидом формулы (III):

или его фармацевтически приемлемой солью,
где АА1 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aac, Aic, Arg, Asn, Asp, Gln, Glu, Hca, His, Hyp, Lys, Mac, Macab, Orn, Pro, Ser, Ser(Bzl), Thr, Thr(Bzl), Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, lia, Alla, Aba, Gba, Car, Ipa, Iaa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua, Рур и необязательно замещенной ароматической α-аминокислоты;
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, выбранных из группы, состоящей из галогена, NO2, ОН, CN, (C1-6)алкила, (С2-6)алкенила, (С2-6)-алкинила и NR9R10;
АА3 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Tpa и Tmpa;
АА3b является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Arg, Bpa, F5-Phe, His, Nal, Pal, 4-Pal, Trp, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и X5-Phe;
АА4 является D- или L-изомером аминокислоты, выбранной из группы, состоящей из Trp, N-Met-Trp, β-Met-Trp, His, hHis, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и необязательно замещенной ароматической α-аминокислоты, где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, CN, (C1-4)алкила, (С2-4)алкенила, (С2-4)алкинила, Bzl, O-Bzl и NR9R10;
АА5 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из 4-Pip-Gly, 4-Pip-Ala, цис-4-Acha, транс-4-Acha, транс-4-Amcha, hLys, Lys и Orn, и hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala,
где аминогруппа боковой цепи указанной аминокислоты необязательно моно- или дизамещена R3 и R4;
АА6 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen, Tpa и Tmpa;
АА7 отсутствует или является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aic, A3с, А4с, А5с, А6с, Abu, Aib, β-Ala, Arg, Bpa, Cha, Deg, Gaba, His, Ile, Leu, Nal, Nle, Pal, Phe, F5-Phe, Pro, Sar, Ser, Ser(Bzl), Thr, Thr(Bzl), Trp, N-Me-Trp, Val, N-Me-Val, hArg, Bip, Tic, Htic, Dip, Sala, Aala, Thza, Thia, Bal, Fala, Pala и X0-Phe;
X0 означает галоген, NO2, СН3, ОН, CN, Bzl или O-Bzl;
каждый из R1 и R2 независимо представляет собой Н, Е-, E(О2)S-, E(О)C-, EOOC-, R13 или отсутствует;
R5 является -OR6 или NR7R8;
R13 представляет собой фрагмент формулы:
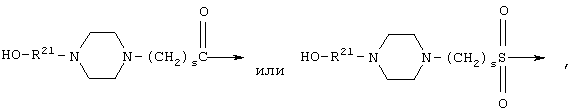
где R21 означает (С1-4)алкил и s равно 1, 2, 3 или 4;
при условии, что присутствует, по меньшей мере, одна из АА1 или АА2;
в том случае, когда АА1 является D- или L- изомером Pro, Hyp, Arg, Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, Iia, Alla, Aba, Gba, Car, Ipa, Iaa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua, Рур или His, АА2 не может быть D- или L- изомером Pro, Hyp, Arg, Pip, hArg, Bip, Bpa, Tic, Cmp, Inc, Inp, Nip, Ppc, Htic, Thi, Tra, Cmpi, Tpr, lia, Alla, Aba, Gba, Car, Ipa, Iaa, Inip, Ара, Mim, Thnc, Sala, Aala, Thza, Thia, Bal, Fala, Pala, Dap, Agly, Pgly, Ina, Dipa, Mnf, Inic, I-Iqc, 3-Iqc, C4c, 5-Iqs, Htqa, 4-Mqc, Thn, α-Chpa, Cit, Nua, Рур или His;
в том случае, когда АА7 является D- или L- изомером Thr или Ser, АА8 не может быть D- или L- изомером Thr или Ser;
по меньшей мере, одна из АА1, АА2, АА3b, АА7, АА7b или АА8 является D- или L-изомером R11 и
в том случае, когда X2 или X3 является =O или =S, другой отсутствует;
или с его фармацевтически приемлемой солью.
Еще один вариант способа включает стадию контактирования клеток с пептидом формулы (4) :

где АА1 отсутствует, является D- или L- изомером аминокислоты, выбранной из группы, состоящей из R11, Aic, Hyp, Pro, Ser, Ser(Bzl), Thr, Thr(Bzl) и необязательно замещенной ароматической α-аминокислоты;
где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, каждый из которых независимо выбран из группы, состоящей из галогена, NO2, ОН, (C1-6)алкила, (C2-6)-алкенила, (С2-6)алкинила, (С1-6)алкоксигруппы, Bzl, O-Bzl и NR9R10;
АА2 отсутствует или является D- или L-изомером аминокислоты, выбранной из группы, состоящей из R11, Arg, F5-Phe, His, Pal, Phe, Trp и X0-Phe;
АА3 является D- или L- изомером необязательно замещенной ароматической α-аминокислоты, где указанная необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или большим количеством заместителей, выбранных из группы, состоящей из галогена, NO2, ОН, (C1-4)алкила, (C2-4)-алкенила, (С2-4)алкинила, Bzl, O-Bzl и NR9R10;
АА4 является D- или L- изомером необязательно замещенной аминокислоты, выбранной из группы, состоящей из Lys, Orn, hLys, цис-4-Acha, транс-4-Acha, транс-4-Amcha, 4-Pip-Gly и 4-Pip-Ala,
где аминогруппа боковой цепи указанной необязательно замещенной аминокислоты необязательно замещена R3 и R4;
АА5 отсутствует или является D- или L- изомером R11, А3с, А4с, А5с, А6с, Abu, Aib, Aic, β-Ala, Bpa, Cha, Deg, F5-Phe, Gaba, Ile, Leu, Nal, Nle, Pal, Phe, Pro, Sar, Ser, Ser(Bzl), Thr, Thr(Bzl), Trp, N-Me-Trp, Val, N-Me-Val или X0-Phe;
АА6 отсутствует, является D- или L- изомером R11, ароматической α-аминоксилоты, F5-Phe, Phe, Thr, Thr(Bzl), Ser, Ser(Bzl) или X0-Phe;
АА7 отсутствует, является D- или L- изомером R11 или D- или L-изомером ароматической α-аминоксилоты;
АА8 является D- или L-изомером R11;
R1 представляет собой Н, Е-, Е(O2)S-, Е(O)С-, ЕООС- или R13;
R13 представляет собой фрагмент формулы:

где R21 означает (С1-4) алкил и s равно 1, 2, 3 или 4;
X0 в определении АА2 и АА5 означает галоген, NO2, ОН, (С1-6)алкил, (С1-6) алкоксигруппу, моно- или ди- (С1-6)алкиламиногруппу, Bzl или O-Bzl;
X0 в определении АА6 означает галоген, NO2, ОН, (C1-6)алкил, (С1-6)алкоксигруппу, моно- или ди- (С1-6)алкиламиногруппу, Bzl, O-Bzl или NR9R10;
при условии, что
присутствует, по меньшей мере, одна из АА1 или АА2;
в том случае, когда АА1 отсутствует, АА2 и АА8 вместе образуют связь;
и присутствуют, по меньшей мере, две аминокислоты из АА5, АА6 и АА7;
или с его фармацевтически приемлемой солью.







Введение фармацевтически приемлемой соли соединения, описываемого формулой (I), пациенту, у которого нарушение является результатом биохимической активности, индуцированной NMB или соматостатином, также входит в рамки данного изобретения. Другими словами пептиды могут быть предоставлены в форме фармацевтически приемлемых солей, например кислотно-аддитивных солей, или комплексов с металлами, например с цинком, железом и тому подобным. Иллюстративными примерами кислотно-аддитивных солей являются соли органических кислот, таких как уксусная, молочная, памовая, малеиновая, лимонная, яблочная, аскорбиновая, янтарная, бензойная, пальмитиновая, субериновая, салициловая, винная, метансульфоновая или толуолсульфоновая кислота, соли полимерных кислот, таких как дубильная кислота или карбоксиметилцеллюлоза, и соли неорганических кислот, таких как соляная кислота, бромистоводородная кислота, серная кислота или фосфорная кислота.
Другие особенности и преимущества данного изобретения будут очевидны из следующего описания предпочтительных вариантов, а также из формулы изобретения. Предполагается, что на основании приведенного здесь описания специалист в данной области использует данное изобретение в самом полном объеме. Поэтому следующие конкретные варианты следует считать только иллюстративными и никоим образом не ограничивающими остальную часть заявки. Все цитированные здесь документы тем самым включены в виде ссылки.
ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ
В предпочтительном варианте особенностью изобретения является соединение согласно формуле 2, где
АА1 отсутствует, является Ac-D-Phe или D- или L- изомером R11, Pip, Pro или Ser, или ароматической а-аминокислоты, выбранной из группы, состоящей из Сра, Dip, Nal, Pal и Phe;
АА2 означает Aic, Pal, Phe, F5-Phe, 4-NO2-Phe, Trp, Tyr, Phe (4-O-Bzl) или отсутствует;
АА3 означает D- или L- изомер аминокислоты, выбранной из группы, состоящей из Pen, Cys, hCys и Tmpa;
АА4 означает D- или L-изомер Trp или His;
АА5 является Lys, hLys, N-Me-Lys, Orn, цис-4-Acha или 4-Pip-Ala;
АА6 является D- или L- изомером аминокислоты, выбранной из группы, состоящей из Cys, hCys, Pen and Tmpa;
АА7 означает А3с, А4с, А5с, А6с, Abu, Aic, β-Ala, Gaba, Nle, F5-Phe, Phe, Pro, Sar, Ser, Thr, Thr(Bzl), Tyr, Val или отсутствует;
АА8 означает R11, Nal, Thr, Thr(Bzl), Tyr, Phe(4-O-Bzl) или отсутствует;
или его фармацевтически приемлемая соль.
В более предпочтительном варианте особенностью изобретения является соединение согласно упомянутому непосредственно выше, где
АА1 отсутствует или является D- или L- изомером R11, Pip или Pro или ароматической α-аминокислоты, выбранной из группы, состоящей из Сра, Dip, Nal, Pal, Phe и Ас-Phe;
АА2 означает Туг, Pal, Phe, 4-NO2-Phe, Trp или отсутствует;
АА3 является D- или L- изомером Cys или Pen;
АА4 означает D-Trp;
АА5 означает Lys, Orn или цис-4-Acha;
АА6 означает D- или L- изомер Cys или Pen;
АА7 означает А3с, А4с, А5с, А6с, Abu, Aic, β-Ala, Gaba, Nle, Phe, Pro, Sar, Thr, Thr(Bzl), Tyr, Val или отсутствует;
АА8 означает R11, Thr, Туг, Nal или отсутствует;
или его фармацевтически приемлемая соль.
В другом предпочтительном варианте особенностью изобретения является соединение согласно формуле III, где АА1 означает R11, Aic, Hca, Pro, Ser, Ser(Bzl), Trp, Tyr или D- или L- изомер ароматической α-аминокислоты, выбранной из группы, состоящей из Сра, Nal, Ac-Nal, Phe, Ac-Phe, 4-NO2-Phe и Ас-4-NO2-Phe;
АА2 означает Pal, Phe, F5-Phe, Tyr или отсутствует;
АА3 является D- или L- изомером Cys, hCys, Pen или Tmpa;
АА3b означает Pal, 4-Pal, His, Trp, Tyr, Phe (4-O-Bzl), Phe или R11;
АА4 является D- или L- изомером Trp или His;
АА5 означает Lys, N-Me-Lys, Orn, hLys, cis-4-Acha или 4-Pip-Ala;
AA6 является D- или L- изомером Cys, hCys, Pen или Tmpa;
АА7 означает R11, A4c, A5c, Abu, β-Ala, Gaba, Phe, F5-Phe, Ser(Bzl), Thr, Thr(Bzl), Phe(4-O-Bzl) или отсутствует;
AA7b означает R11, Nal, F5-Phe, X0-Phe или отсутствует, где X0 является галогеном, NO2, СН3, ОН, Bzl или O-Bzl;
АА8 означает R11, Nal, Туг, Phe(4-O-Bzl) или отсутствует;
или его фармацевтически приемлемая соль.
В более предпочтительном варианте особенностью изобретения является соединение согласно упомянутому непосредственно выше, где
АА1 означает R11, Aic, Hca, Pro, Ser(Bzl) или D- или L- изомер ароматической α-аминокислоты, выбранной из группы, состоящей из Сра, Nal, Ac-Nal, Phe, Ac-Phe, 4-NO2-Phe и Ac-4-NO2-Phe;
АА2 означает Pal, Tyr или отсутствует;
АА3 является D- или L- изомером Cys или Pen;
АА3b означает R11, Pal, 4-Pal, Trp, Туг, Phe(4-O-Bzl) или Phe, где R11 представляет собой (Т)aeg;
АА4 означает D-Trp;
АА5 означает Lys, N-Me-Lys, Orn или цис-4-Acha;
АА6 является D- или L- изомером Cys или Pen;
АА7 означает R11, A5c, Abu, Ser(Bzl), Thr, Thr(Bzl), Phe(4-O-Bzl), Gaba или отсутствует;
АА7b означает Nal, X0-Phe или отсутствует;
АА8 означает Tyr или отсутствует;
или его фармацевтически приемлемая соль.
В еще одном предпочтительном варианте особенностью изобретения является соединение согласно формуле 4, где AA1 означает Aic, Hyp, Cpa, D-Cpa, Nal, Pal, Phe, Pro, R11, Tyr или отсутствует;
AA2 означает Phe, Trp, F5-Phe, His, Tyr, Phe(4-O-Bzl) или R11;
AA3 является D-изомером Trp, His или Pal;
AA4 означает Lys, N-Me-Lys, Orn, hLys, цис-4-Acha или 4-Pip-Ala;
AA5 означает Pal, Phe (4-O-Bzl), Thr(Bzl), Thr, Sar, Gaba, β-Ala, A4c, A5c, A6c, Abu, Aic или отсутствует;
AA6 означает Thr, Tyr, Ser, F5-Phe, Cpa, Nal или D- или L-Phe;
AA7 означает Nal, Pal или отсутствует;
AA8 означает R11;
или его фармацевтически приемлемая соль.
В еще одном предпочтительном варианте особенностью изобретения является соединение согласно упомянутому непосредственно выше, где AA1 означает Cpa, Nal, Pal, Phe, Tyr или отсутствует;
AA2 означает Phe, Tyr, Trp или R11;
AA3 означает D-Trp;
AA4 означает Lys, N-Me-Lys или цис-4-Acha;
AA5 означает Pal, Phe(4-O-Bzl), Aic, Gaba, A5c или отсутствует;
AA6 означает Thr, Nal или D-или L-Phe;
AA7 отсутствует;
АА8 означает R11;
или его фармацевтически приемлемая соль.
В еще одном предпочтительном варианте особенностью изобретения является соединение согласно формуле II, где R1 и R5 отсутствуют и N-концевая аминокислота и С-концевая аминокислота вместе образуют амидную связь; или его фармацевтически приемлемая соль.
В еще одном предпочтительном варианте особенностью изобретения является соединение согласно формуле III, где R1 и R5 отсутствуют и N-концевая аминокислота и С-концевая аминокислота вместе образуют амидную связь; или его фармацевтически приемлемая соль.
В наиболее предпочтительном варианте особенностью изобретения является соединение согласно формуле II, где указанное соединение имеет формулу:
Ac-D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
D-Dip-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
цикло(D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr);
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-АЗс-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A6c-Nal-NH2;
(G(z))aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2 ;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-β-Ala-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Sar-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Pro-Nal-NH2;
или его фармацевтически приемлемая соль.
В еще одном наиболее предпочтительном варианте особенностью изобретения является соединение согласно формуле II, где указанное соединение имеет формулу:
Phe-цикло(Cys-D-Trp-Lys-Cys)-Thr-NH2;
Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Ac-D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A3c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A6c-Nal-NH2;
(G(z))aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
D-Cpa-цикло(Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Сра-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-β-Ala-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Sar-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Aic-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Pro-Nal-NH2;
(Т)aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-(A)aeg-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A4c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nal-NH2;
Pro-Phe-цикло(Cys-D-Trp-Lys-D-Cys)-Val-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-Cys)-Val-NH2;
Pip-4-NO2-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-NIe-NH2;
(G)aeg-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr(Bzl)-(C)aeg-NH2;
(С)aeg-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr(Bzl)-(G)aeg-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nle-Phe-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-Nle-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-Phe-NH2;
Cpa-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-NH2;
Cpa-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Tyr-NH2;
Pip-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-NH2;
Pip-Phe-цикло(Cys-D-Trp-Lys-Cys)-Gaba-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-NH2;
или его фармацевтически приемлемая соль.
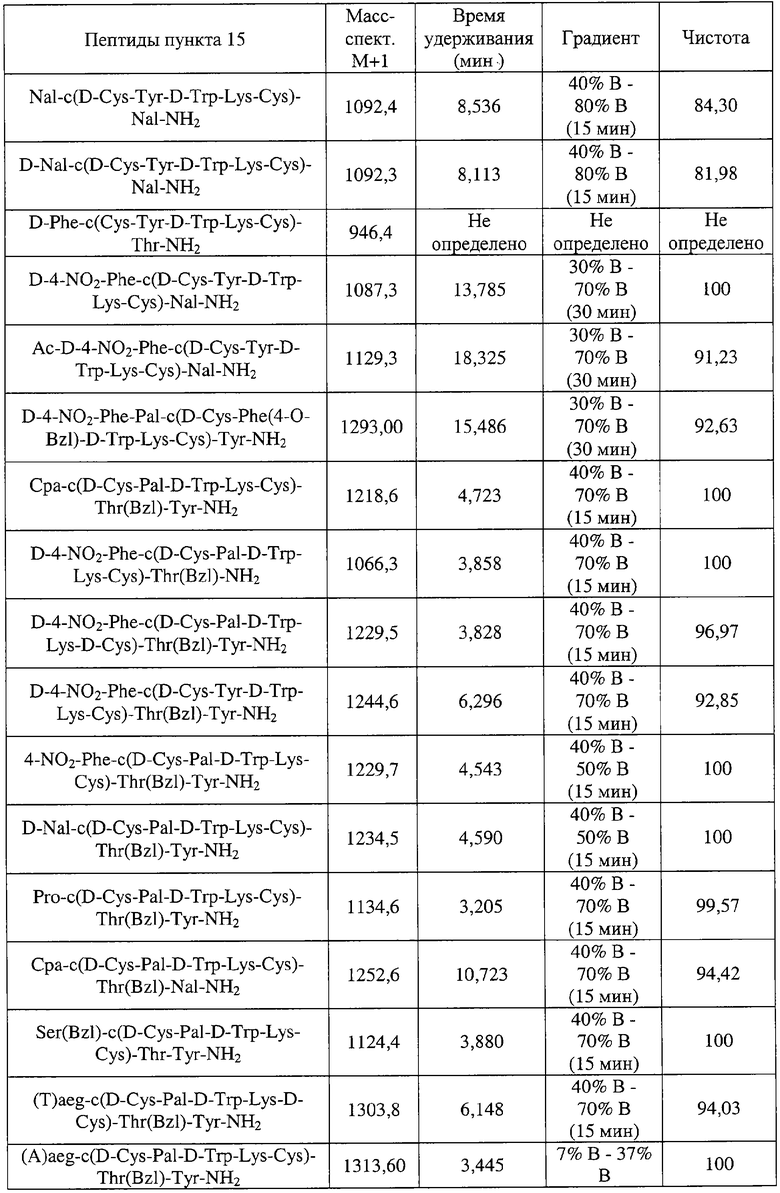
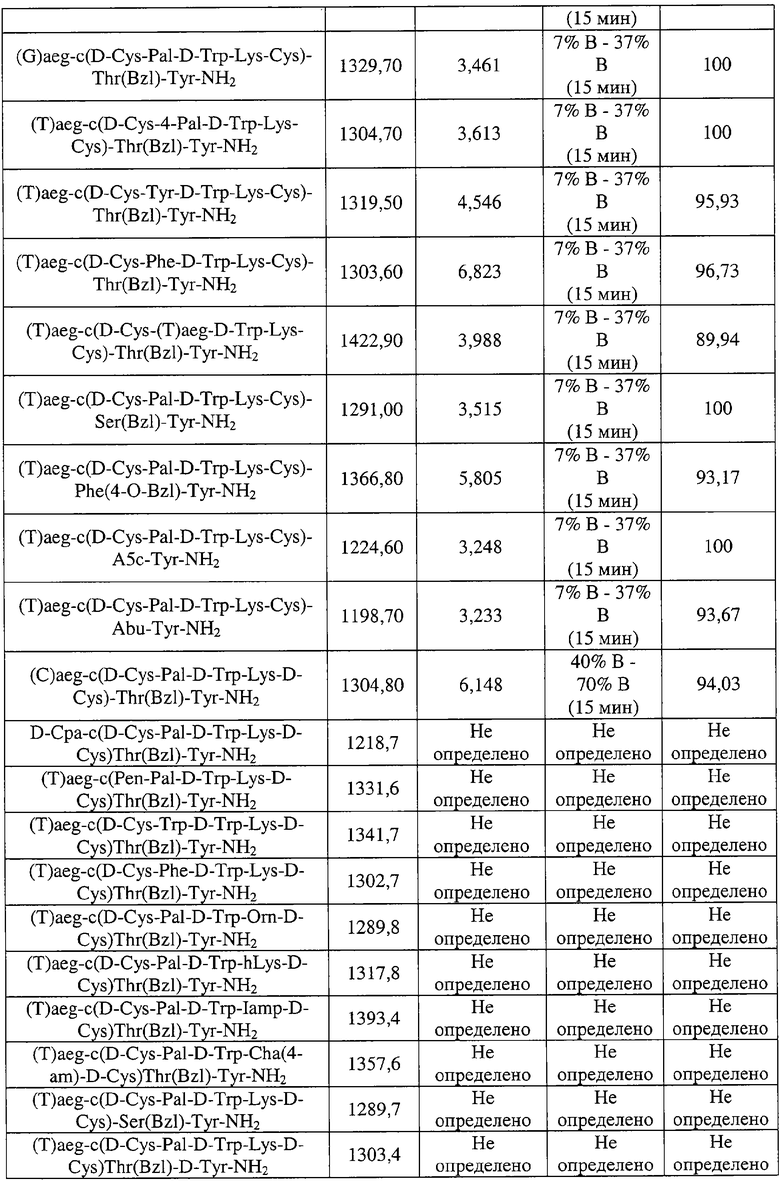
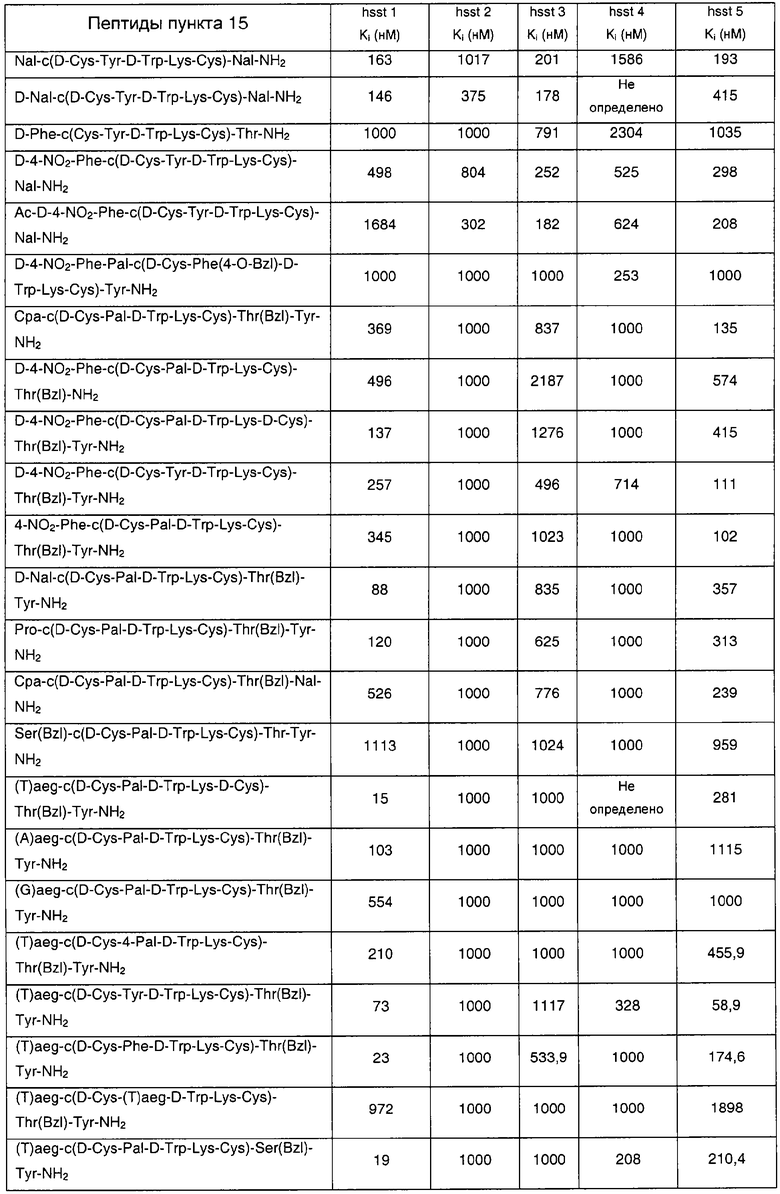
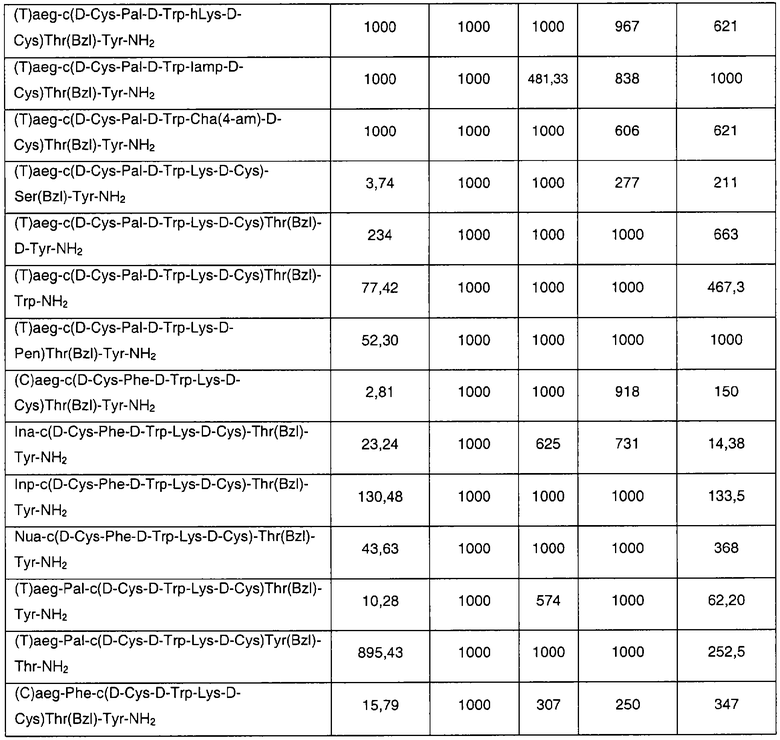
В еще одном наиболее предпочтительном варианте особенностью изобретения является соединение согласно формуле III, где указанное соединение имеет формулу:
Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2
D-Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Cys)-Thr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Ac-D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-4-NO2-Phe-Pal-цикло(D-Cys-Phe(4-O-Bzl)-D-Trp-Lys-Cys)-Tyr-NH2;
Сра-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr-Tyr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2,
D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
D-Nal-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Pro-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Сра-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Nal-NH2;
Ser(Bzl)-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
(А)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(G)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-4-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Phe-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-(T)aeg-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Ser(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Phe(4-O-Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-A5c-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Abu-Tyr-NH2;
D-Cpa-цикло(D-Cys-(T)aeg-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(C)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
D-Cpa-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(Pen-Pal-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Trp-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Orn-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-hLys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Iamp-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Cha(4-am)-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Ser(Bzl)-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)Thr(Bzl)-D-Tyr-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)Thr(Bzl)-Trp-NH2;
(T)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Pen)Thr(Bzl)-Tyr-NH2;
(C)aeg-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
Ina-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
Mnf-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
Inp-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
Nua-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
Рур-цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
цикло(D-Cys-Phe-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
(T)aeg-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(T)aeg-Pat-цикло(D-Cys-D-Trp-Lys-D-Cys)Tyr(Bzl)-Thr-NH2;
(С)aeg-Phe-цикло (D-Cys-D-Trp-Lys-D-Cys)Thr(Bzl)-Tyr-NH2;
(Т)aeg-D-Trp-цикло(D-Cys-Pal-Lys-D-Cys)Thr(Bzl)-Leu-NH2;
или его фармацевтически приемлемая соль.
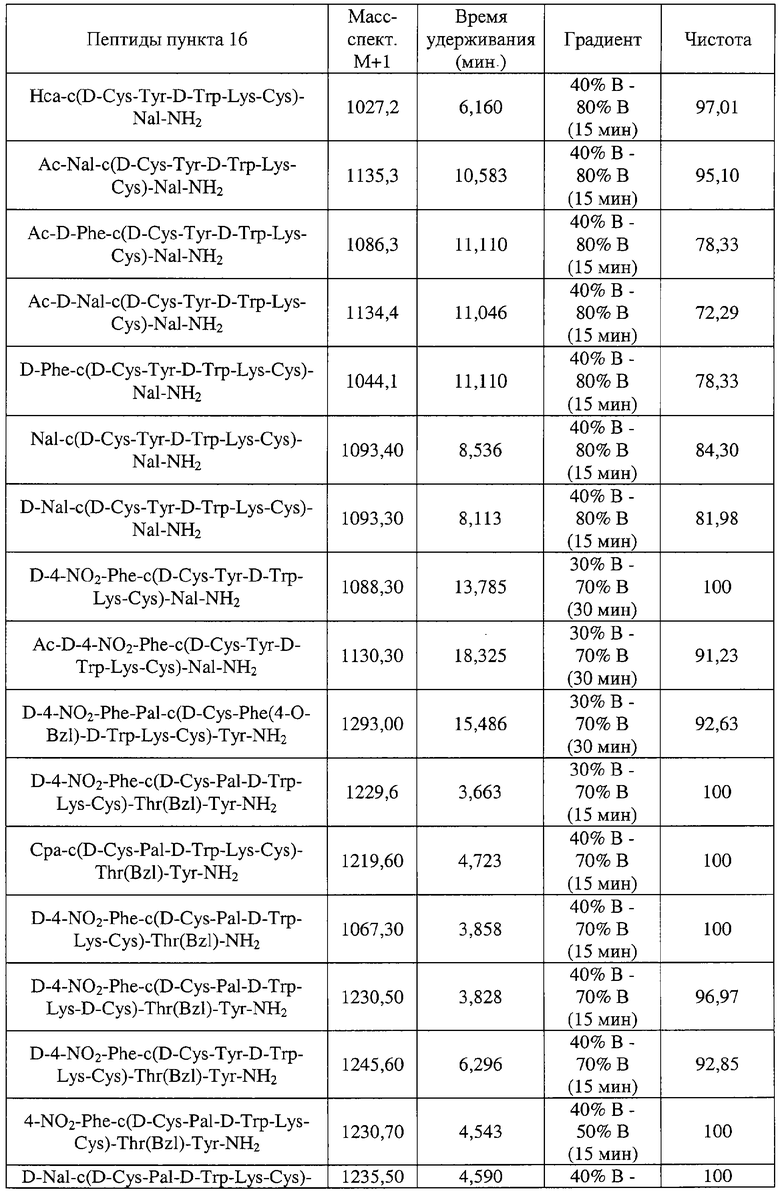
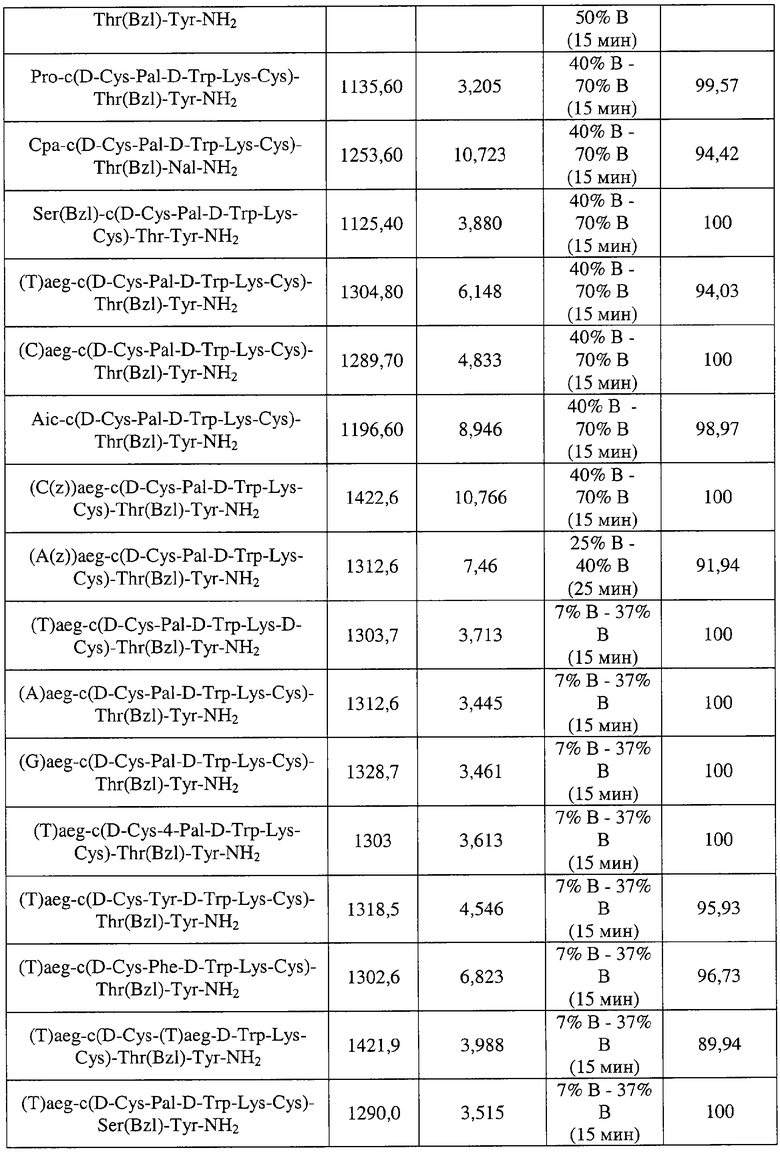
В еще одном наиболее предпочтительном варианте особенностью изобретения является соединение согласно формуле III, где указанное соединение имеет формулу:
Нса-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Ac-Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Ac-D-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Ac-D-Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-Nal-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-Phe-цикло(Cys-Tyr-D-Trp-Lys-Cys)-Thr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
Ac-D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Nal-NH2;
D-4-NO2-Phe-Pal-цикло(D-Cys-Phe(4-O-Bzl)-D-Trp-Lys-Cys)-Tyr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Сра-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-NH2;
D-4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
D-4-NO2-Phe-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
4-NO2-Phe-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
D-Nal-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Pro-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Сра-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Nal-NH2;
Ser(Bzl)-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(С)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
Aic-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(C(z))aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(A(z))aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2:
(А)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(G)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2:
(Т)aeg-цикло(D-Cys-4-Pal-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Tyr-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Phe-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-(T)aeg-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Ser(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Phe(4-O-Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-A5c-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-Cys)-Abu-Tyr-NH2;
D-Cpa-цикло(D-Cys-(T)aeg-D-Trp-Lys-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-p-Me-Phe-NHz;
Ac-(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
(Т)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Nal-NH2;
D-Cpa-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Nal-NH2;
(А)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
(С)aeg-цикло(D-Cys-Pal-D-Trp-Lys-D-Cys)-Thr(Bzl)-Tyr-NH2;
или его фармацевтически приемлемая соль.
В еще одном наиболее предпочтительном варианте особенностью изобретения является соединение согласно формуле 4, где указанное соединение имеет формулу:
цикло(Trp-D-Trp-Lys-Phe(4-O-Bzl)-Phe-(Т)aeg);
цикло(Trp-D-Trp-Lys-Pal-Phe-(Т)aeg);
цикло(Phe-Phe-D-Trp-Lys-Thr-(Т)aeg);
или его фармацевтически приемлемая соль.
ПОЛУЧЕНИЕ ПЕПТИДОВ
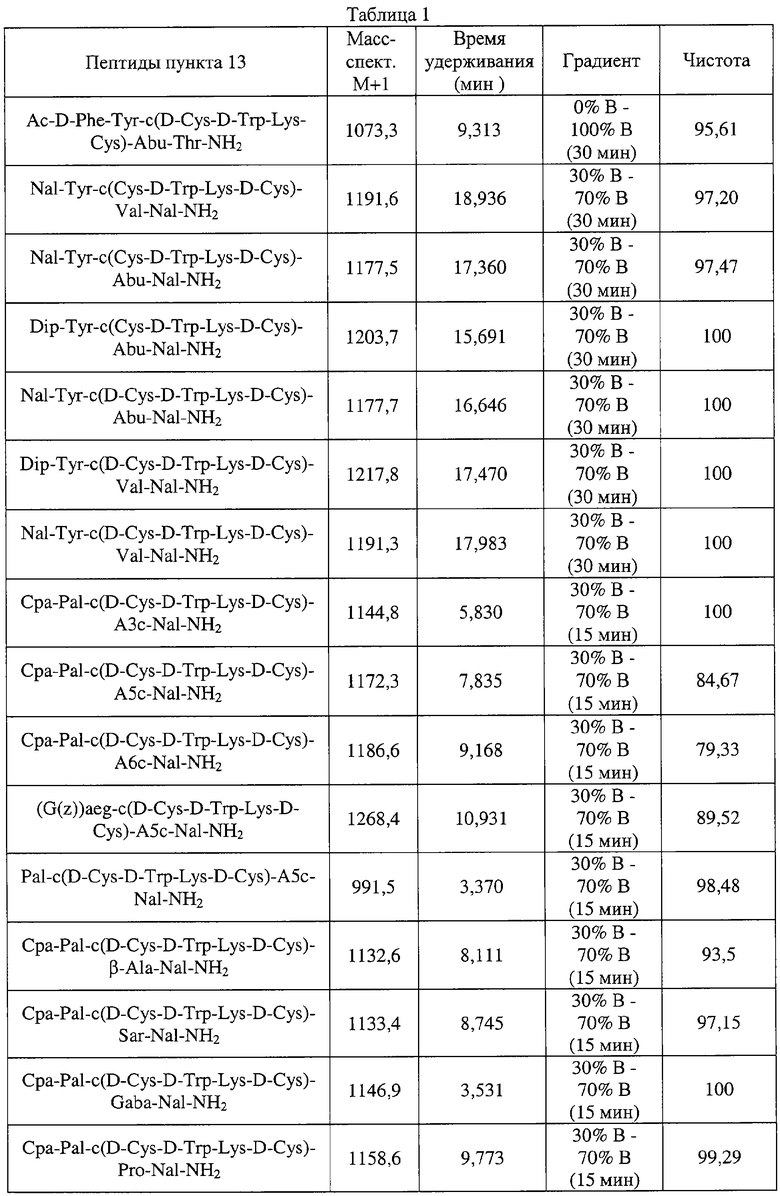
Пептиды синтезировали на амидной смоле Rink МВНА, (4-(2', 4'-диметоксифенил-Fmoc-аминометил)феноксиацетамидонорлейцил-МВНА-смола), используя стандартный протокол твердофазного синтеза, используемый в Fmoc-химии, и отщепляли с помощью смеси ТФУ/фенол/Н2О/триизопропилсилан (83 мл/5 г/10 мл/2 мл). Циклизацию пептидов проводили в СН3CN/Н2О (5 мл/5 мл), используя смолу EKATIOX™ (EKAGEN Corporation, San Carlos, CA) и очищали на колонке C18 с кремнеземом (Rainin Instruments Co., Woburn, MA, теперь Varian Analytical, Walnut Creek, CA), используя буферы ацетонитрил / 0,1% трифторуксусная кислота. Гомогенность оценивали аналитической ВЭЖХ и масс-спектрометрией, и определили, что она составляла >95% для каждого пептида.
Пептиды, имеющие общую структуру
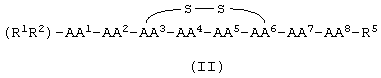
или

то есть имеющие циклическую тетра- или пентапептильную основу, синтезировали на амидной смоле МВНА Rink (4-(2',4'-диметоксифенил-Fmoc-аминометил)феноксиацетамидонорлейцил-МВНА-смола), следуя стандартному протоколу твердофазного синтеза, используемого в Fmoc-химии до тех пор, пока не был собран требуемый пептид. Конечное отщепление/удаление защитных групп достигали обработкой пептида, связанного со смолой, смесью ТФУ/фенол/Н2O/триизопропилсилан (83:5:10:2 мл/г/мл/мл).
Циклизацию (образование S-S-связи) достигали растворением линейного пептида в 50 % смеси СН3CN/Н2O, за исключением тех случаев, которые оговорены особо, после чего добавляли 2,5 экв. смолы EKATHIOXтм , затем перемешивали в течение ночи.
Пептиды очищали на колонке C18 кремнеземом, используя буфер ацетонитрил/0,1% ТФУ. Гомогенность оценивали аналитической ВЭЖХ и масс-спектрометрией и определили, что она составляла >95% для каждого пептида, если не оговорено особо.
Пептиды, имеющие карбоксильную функцию на С-конце, синтезировали на смоле Wang (смола на основе пара-бензилоксибензилового спирта), отщепляли от смолы и удаляли защитные группы смесью В (ТФУ: фенол: Н2O: триизопропилсилан в соотношении 88:5:5:2).
Циклические благодаря образованию связи «голова-хвост» пептиды, имеющие общую структуру
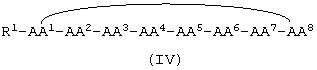
сначала синтезировали в виде полностью защищенного линейного пептида на 2-хлортритилхлоридной смоле.
Первое удаление защитной группы Fmoc выполняли, используя 5% пиперидин в DMF/DCM (1:1) в течение примерно 10 минут, после чего 25% пиперидином в DMF в течение примерно 15 минут. Все последующие процедуры удаления защитных групп выполняли, используя стандартный протокол твердофазного синтеза, используемый в Fmoc-химии.
Защищенные линейные пептиды получали обработкой смолы смесью уксусной кислоты/TFE/DCM (1:1:8 по объему) примерно в течение 60 минут при комнатной температуре.
Циклизацию «голова-хвост» достигали с использованием в качестве связывающего/циклизующего реагента HATU/HOAT/DIPEA. Полностью защищенный циклический пептид обрабатывали смесью ТФУ/фенол/Н2O/триизопропилсилан (83:5:10:2 мл/г/мл/мл) примерно в течение 21/2 часа, чтобы достичь окончательного удаления защитных групп.
Пептиды очищали на колонке C18 с кремнеземом, используя в качестве элюента буфер ацетонитрил/0,1% ТФУ. Гомогенность оценивали аналитической ВЭЖХ и масс-спектрометрией, и определили, что чистота составляла >97% для каждого пептида.
Как указано выше, некоторые соединения согласно изобретению включают в себя один или большее количество аминокислотных фрагментов R11, имеющих структуру

где каждый из R12, X1, X2, X3, X4, m, n и р имеет значение, определенное в формуле изобретения. Специалисту в области химического синтеза будет ясно, что различные аминокислоты R11 легко можно синтезировать, используя подходящие исходные материалы и известные способы синтеза. Примеры подходящих способов можно найти в следующих публикациях, которые, таким образом, включены в виде ссылки: аминоэтилглицин: Tetrahedron, vol.51, pp.6179 (1995); Bioorganic and Medicinal Chemistry Letters, vol.5, No.11, p.1159 (1995); Tetrahedron, vol.53, No.43, p.14671 (1997); Nucleosides, Nucleotides, vol.6 (10 & 11), р.1893 (1997); α,α-диалкилированная аминокислота с боковой цепью, представленной нуклеотидным основанием, Ргос. Natl. Acad. Sci. USA, vol.92, p.12013 (1995); аминоциклогексилглицин, Chem. Eur. J. vol.3, No.6, p.912 (1997); σ-N-Boc-α-N-(тимин-1-илацетил)орнитин, Bioorganic and Medicinal Chemistry Letters, vol.6, No.1, p.793 (1996); замещенный пролин, J. Chem. Soc. Perkin. Trans., vol. 1, pp.539, 547, 555 (1997); N-(аминометил)-β-аланин, Tetrahedron Lett., vol.36, No.38, р.6941 (1995); замещенный орнитин, Nucleosides and Nucleotides, vol. 17 (1-3), pp.219, 339 (1998); структура vi, Tetrahedron Lett., vol.36, No.10, p.1713 (1995); Tetrahedron Lett., vol.38, No.48, p.8363 (1997); структура v, Tetrahedron Lett., vol. 39, p. 4707 (1998); соединение iv, J. Amer. Chem. Soc., vol.119, p.11116 (1997); аминопролин, Bioorganic and Medicinal Chemistry Lett., vol.7, no.6, p.681 (1997); хиральная полинуклеиновая кислота, Tetrahedron Lett., vol.35, No.29, р.5173 (1994); Bioorganic and Medicinal Chemistry Lett., vol.4, no.8. p.1077 (1994).
Ниже приведено подробное описание, касающееся синтеза аналога №1. Другие пептиды согласно изобретению можно получить, сделав соответствующие модификации в пределах возможностей специалиста в области синтеза пептидов.
Стадия 1. Получение Fmoc-Nal-O-трет-бутил-Tyr-S-тритил-D-Cys-N-in-t-Boc-D-Trp-N-ε-t-Boc-Lys-S-тритил-D-Cys-Abu-Nal-4-(2',4'-диметоксфениламинометил)феноксиацетамидонорлейцил-4-метилбензгидриламиновой смолы.
Амидную смолу МВНА Rink (Novabiochem, Inc., San Diego, CA), 1 г (0,53 ммоль), помещали в реакционный сосуд №1 (RV-1) синтезатора пептидов модели 90 (Advanced ChemTech, Louisville, KY). Синтезатор пептидов программировали на выполнение следующего цикла реакции:
а) диметилформамид;
b) 25% пиперидин в диметилформамиде (2 раза в течение 15 минут каждый, с 1 промывкой DMF между ними);
с) промывки DMF (3×10 мл, по 1 минуте каждая).
Смолу перемешивали с Fmoc-Nal (2,12 ммоль), гексафторфосфатом 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (HBUT) (2,01 ммоль) и диизопропилэтиламином (4,24 ммоль) в диметилформамиде в течение примерно 11/2 часа и затем полученную в результате смолу с аминокислотой подвергали циклическим реакциям с (а) по (с) стадии в указанной выше программе. Nal-смолу связывали с Fmoc-Abu, затем подвергали циклу реакций, как описано выше. Смолу сушили в вакууме.
Следующие аминокислоты (1,4 ммоль) последовательно связывали с пептидом на смоле (0,35 ммоль) посредством той же самой процедуры: Fmoc-S-тритил-D-Cys, Fmoc-N-ε-t-Boc-Lys, Fmoc-N-in-t-Boc-D-Trp. После сушки в вакууме смолу с пептидом разделяли и одну часть связывали с Fmoc-S-тритил-О-Cys, Fmoc-O-t-бутил-Tyr. Связанную часть снова разделяли и одну часть связывали с Fmoc-Nal. После промывки DMF (3×10 мл, по 1 минуте каждая) и сушки в вакууме заполненная смола весила 0,242 г.
Стадия 2. Получение 
Смолу с пептидом, полученную на стадии 1 (0,24 г, 0,087 ммоль), смешивали со свежеприготовленным раствором ТФУ (8,8 мл), фенола (0,5 г), Н2О (0,5 мл) и триизопропилсиланом (0,2 мл) при комнатной температуре и перемешивали примерно в течение 21/2 часа. Избыток ТФУ выпаривали при пониженном давлении до маслянистого остатка. Затем к маслянистому остатку добавляли эфир и осаждали свободный линейный пептид, фильтровали, затем промывали осушенным эфиром. Затем неочищенный пептид растворяли в 11 мл СН3CN/Н2О/0,1 N HOAc (5 мл/5 мл/1 мл), после чего добавляли 200 мг смолы EKATHIOX®. Смесь перемешивали в течение ночи и затем фильтровали. Фильтрат упаривали до небольшого объема, затем наносили на колонку (22-250 мм) с микросорбентом оксидом кремния, модифицированным окдадецилсиланом (5 мкМ), с последующим элюированием линейным градиентом (от 30% до 80%, в течение 30 минут) ацетонитрила в воде, при этом оба растворителя содержали 0,1% трифторуксусную кислоту. Фракции оценивали аналитической высоко эффективной жидкостной хроматографией (ВЭЖХ) и объединяли, чтобы получить максимальную чистоту. Лиофилизация растворов для удаления воды давала 10 мг продукта в виде белого, пушистого порошка. Посредством ВЭЖХ на колонке C18 с диоксидом кремния с использованием такого же элюента, который указан непосредственно выше, обнаружено, что продукт является гомогенным (tR=16,646 минут). Инфузионная масс-спектрометрия подтвердила состав циклического октапептида (М.м. 1178,45).
ДРУГИЕ ВАРИАНТЫ
На основании приведенного выше описания специалист в данной области легко установит основные особенности данного изобретения и, не отходя от сути и не выходя за рамки изобретения, может осуществить различные изменения и модификации изобретения, для того чтобы адаптировать его к разным применениям и условиям. Таким образом, другие варианты также входят в формулу изобретения.











Заявлены новые соединения, которые проявляют как высокое сродство, так и избирательность по отношению к рецепторам нейромедина В и соматостатина. Соединения имеют следующую формулу:  где α-азот каждой из АА1, АА2, АА3, АА4, АА5, АА6, АА7 и АА8 независимо необязательно замещен (C1-4)алкилом, (С3-4)алкенилом, (С3-4)алкинилом или (С1-6)алкил-С(O)-; АА1 отсутствует, является Ac-D-Phe или D- или L-изомером R11, Pip, Pro или ароматической α-аминокислотой, выбранной из группы, состоящей из Сра, Dip, Nal и Phe; АА2 отсутствует, является Pal, Phe, Туг; АА3 является D- или L-изомером Cys; АА4 является D- или L-изомером Trp; АА5 означает Lys; АА6 является D- или L- изомером Cys; АА7 является А3с, А4с, А5с, А6с, Abu, Aic, (β-Ala, Gaba, Nle, Pro, Sar, Thr, Thr(Bzl), Val или отсутствует; АА8 является R11, Nal, Thr, Tyr, Phe, Nle или отсутствует; каждый из R1 и R2 независимо представляет собой Н или отсутствует; R5 является -NH2, R11 независимо для каждого случая является D- или L- аминокислотой, АА3 и АА6 связаны дисульфидной связью. 6 н. и 3 з.п. ф-лы, 2 табл.
где α-азот каждой из АА1, АА2, АА3, АА4, АА5, АА6, АА7 и АА8 независимо необязательно замещен (C1-4)алкилом, (С3-4)алкенилом, (С3-4)алкинилом или (С1-6)алкил-С(O)-; АА1 отсутствует, является Ac-D-Phe или D- или L-изомером R11, Pip, Pro или ароматической α-аминокислотой, выбранной из группы, состоящей из Сра, Dip, Nal и Phe; АА2 отсутствует, является Pal, Phe, Туг; АА3 является D- или L-изомером Cys; АА4 является D- или L-изомером Trp; АА5 означает Lys; АА6 является D- или L- изомером Cys; АА7 является А3с, А4с, А5с, А6с, Abu, Aic, (β-Ala, Gaba, Nle, Pro, Sar, Thr, Thr(Bzl), Val или отсутствует; АА8 является R11, Nal, Thr, Tyr, Phe, Nle или отсутствует; каждый из R1 и R2 независимо представляет собой Н или отсутствует; R5 является -NH2, R11 независимо для каждого случая является D- или L- аминокислотой, АА3 и АА6 связаны дисульфидной связью. 6 н. и 3 з.п. ф-лы, 2 табл.
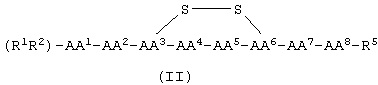
или его фармацевтически приемлемая соль,
где α-азот каждой из АА1, АА2, АА3, АА4, АА5, АА6, АА7 и АА8 независимо необязательно замещен (C1-4)алкилом, (С3-4)-алкенилом, (С3-4)алкинилом или (C1-6)алкил -С(О)-;
АА1 отсутствует, является Ac-D-Phe или D- или L-изомером R11, Pip, Pro или ароматической α-аминокислотой, выбранной из группы, состоящей из Сра, Dip, Nal и Phe;
АА2 отсутствует, является Pal, Phe, Tyr;
АА3 является D- или L-изомером Cys;
АА4 является D- или L-изомером Тгр;
АА5 означает Lys;
АА6 является D- или L- изомером Cys;
АА7 является А3с, А4с, А5с, А6с, Abu, Aic, β-Ala, Gaba, Nle, Pro, Sar, Thr, Thr(Bzl), Val или отсутствует и
АА8 является R11, Nal, Thr, Туг, Phe, Nle или отсутствует;
каждый из R1 и R2 независимо представляет собой Н или отсутствует;
R5 является -NR7R8, где каждый R7 и R8 независимо представляет собой Н,
R11 независимо для каждого случая является D- или L- аминокислотой формулы
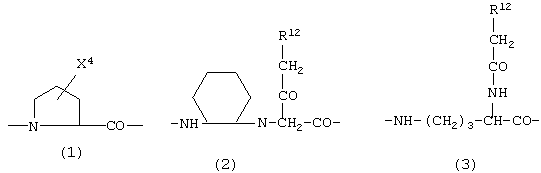
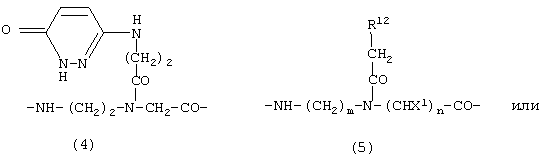
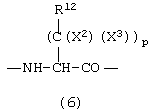
где каждый из m и n независимо равны 1, 2 или 3 и p равно 0, 1 или 2;
R12 независимо для каждого случая является необязательно замещенным фрагментом формулы
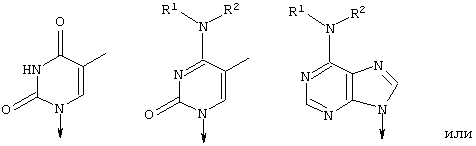
 ;
;
X1 означает Н, (C1-6)алкил или фрагмент, который соответствует группе боковой цепи Arg, Leu, Gin, Lys, Tyr, His, Thr, Trp, Phe, Val, Ala, Lys или His;
каждый из X2 и X3 независимо представляет собой Н, галоген, (C1-12)
алкил, фенил, фенил-(С1-6)алкил;
X4 означает Н, ОН или NH2;
при условии, что присутствуют, по меньшей мере, шесть
аминокислотных остатков;
АА3 и АА6 связаны дисульфидной связью;
и указанное соединение формулы (II) не имеет формулу:
D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Ac-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
L-4-NO2-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Ac-L-4-NO2-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Hca-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
D-Dip-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
D-4-NO2-Phe-Phe(4-O-Bzl)-цикло(D-Cys-D-Trp-Lys-Cys)Cha-Nal-NH2;
или
D-4-NO2-Phe-цикло(D-Cys-Phe(4-O-Bzl)-D-Trp-Lys-Cys)-Val-Tyr-NH2.
Ac-D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
D-Dip-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A3c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A6c-Nal-NH2;
(G(z))aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-β-Ala-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Sar-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Pro-Nal-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nle-Phe-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-Nle-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-Phe-NH2;
Cpa-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-NH2;
Cpa-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Tyr-NH2;
Pip-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-NH2;
Pip-Phe-цикло(Cys-D-Trp-Lys-Cys)-Gaba-NH2 или
Pro-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr-NH2,
или его фармацевтически приемлемая соль.
Phe-цикло(Cys-D-Trp-Lys-Cys)-Thr-NH2,
Phe-Tyr-цикло(D-Cys-D-Tip-Lys-Cys)-Abu-Thr-NH2;
Ac-D-Phe-Tyr-цикло(D-Cys-D-Trp-Lys-Cys)-Abu-Thr-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Tq)-Lys-D-Cys)-Val-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A3c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A6c-Nal-NH2;
(G(z))aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
D-Cpa-цикло(Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-β-Ala-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Sar-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Aic-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Pro-Nal-NH2;
(T)aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-(A)aeg-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A4c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nal-NH2;
Pro-Phe-цикло(Cys-D-Trp-Lys-D-Cys)-Val-NH2;
Pro-Phe-цикло(D-Cys-D-Trp-Lys-Cys)-Val-NH2;
Pip-4-NO2-Phe-цикло(D-Cys-D-Trp-Lys-D-Cys)-Nle-NH2;
(G)aeg-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr(Bzl)-(C)aeg-NH2 или
(C)aeg-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Thr(Bzl)-(G)aeg-NH2,
или его фармацевтически приемлемая соль.
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Abu-Nal-NH2;
Dip-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Nal-Tyr-цикло(D-Cys-D-Trp-Lys-D-Cys)-Val-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A3c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A6c-Nal-NH2;
(G(z))aeg-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
D-Cpa-цикло(Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-цикло(D-Cys-D-Trp-Lys-D-Cys)-A5c-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-β-Ala-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Sar-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Aic-Nal-NH2;
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Gaba-Nal-NH2 или
Cpa-Pal-цикло(D-Cys-D-Trp-Lys-D-Cys)-Pro-Nal-NH2.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2128055C1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Экономайзер | 0 |
|
SU94A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Арматурный каркас железобетонных изделий | 1973 |
|
SU478101A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Способ нанесения шликера на наружные поверхности цилиндрических изделий (труб) и устройство для его осуществления | 1959 |
|
SU127899A1 |
| US 5462926 A, 31.10.1995. | |||
Авторы
Даты
2005-11-10—Публикация
2000-06-05—Подача