Объектом настоящей заявки являются новые производные 4-аминопиперидинов и способы их получения синтезом в жидкой и твердой фазе. Указанные продукты, обладающие хорошим сродством к определенным подтипам рецепторов соматостатина, особенно пригодны для лечения патологических состояний и заболеваний, обусловленных одним (или несколькими) рецепторами соматостатина.
Соматостатин (SST) является циклическим тетрадекапептидом, который впервые был выделен из гипоталамуса как вещество, ингибирующее гормон роста (Brazeau P. et al., 11111,, Science 1973, 179, 77-79). Он действует также в качестве нейротрансмиттера в головном мозге (Reisine Т. et al., Neuroscience 1995, 67, 777-790; Reisine T. et al., Endocrinology 1995, 16, 427-442). В результате молекулярного клонирования было установлено, что биологическая активность соматостатина находится в непосредственной зависимости от семейства пяти мембраносвязанных рецепторов.
Разнообразие биологических функций соматостатина послужило основой для исследований, направленных на идентификацию взаимосвязи между структурой и активностью пептидных аналогов, воздействующих на рецепторы соматостатина, в результате которых было открыто 5 подтипов рецепторов (Yamada et al., Proc. Natl. Acad. Sci. USA, 89, 251-255, 1992; Raynor К. et al., Mol. Pharmacol., 44, 385-392, 1993). В настоящее время ведется активное изучение функций указанных рецепторов. Сродство к разным подтипам рецепторов соматостатина определяет возможность лечения нижеследующих нарушений/заболеваний. Активация подтипов 2 и 5 подавляет гормон роста (GH), в частности, аденомы, секретирующие GH (акромегалия), и аденомы, секретирующие гормон TSH. Активация подтипа 2, не затрагивающая подтип 5, позволяет лечить аденомы, секретирующие пролактин. Другими показаниями для лечения путем активации разных подтипов рецепторов соматостатина являются рецидив стеноза, подавление секреции инсулина и/или глюкагона, в частности сахарный диабет, гиперлипидемия, невосприимчивость к инсулину, синдром X, ангиопатия, пролиферативная ретинопатия, феномен Дауна и нефропатия; подавление секреции желудочного сока, в частности, пептические язвы, тонкокишечные и панкреатические свищи, слизистый колит, демпинг-синдром, водянистый стул, диарея, обусловленная СПИДом, диарея, вызванная химиотерапией, острый или хронический панкреатит и опухоли желудочно-кишечного тракта; рак, такой как гепатома; развитие кровеносных сосудов, воспалительные заболевания, такие как артрит; хроническое отторжение аллотрансплантатов; реконструкция сосудов; профилактика кровотечения из трансплантированных сосудов и желудочно-кишечного тракта. Агонисты соматостатина можно также использовать для снижения массы тела пациента.
Среди патологических нарушений, обусловленных соматостатином (Moreau J.P. et al., Life Science 1987, 40, 419; Harris A.G. et al., The European Journal of Medicine, 1993, 2, 97-105), можно отметить, например, акромегалию, аденому гипофиза, болезнь Кушинга, гонадотропиномы и пролактиномы, катаболические побочные эффекты глюкокортикоидов, инсулинозависимые диабеты, диабетическую ретинопатию, диабетическую нефропатию, гипертиреоз, гигантизм, эндокринные опухоли желудочно-кишечного тракта и поджелудочной железы, включая карциноидный синдром, VIРому, инсулиному, незидиобластому, гиперинсулинемию, глюкагоному, язвенную аденому поджелудочной железы и синдром Цоллингера-Эллисона, GRFoмy как острое кровотечение из варикозно расширенных вен, гастроэзофагеальный рефлюкс, гастродуоденальный рефлюкс, панкреатит, тонкокишечные и панкреатические свищи; диареи, рефрактерные диареи, обусловленные синдромом приобретенного иммунодефицита, хроническую секреторную диарею, диарею, вызванную слизистым колитом, нарушения, обусловленные гастринвысвобождающим пептидом, вторичные патологии кишечных трансплантатов, портальную гипертензию, как кровотечение из варикозно расширенных вен у субъектов, страдающих циррозом, желудочно-кишечное кровотечение, кровотечение из язвы желудка, болезнь Крона, рассеянный склероз, демпинг-синдром, синдром раздраженной тонкой кишки, гипотензию, склеродермию и карциному щитовидной железы, заболевания, обусловленные гиперпролиферацией клеток, такие как злокачественные опухоли, в частности рак молочной железы, рак предстательной железы, рак щитовидной железы, а также рак поджелудочной железы и рак ободочной кишки, фиброзы, в частности фиброз почек, фиброз печени, фиброз легкого, фиброз кожи, фиброз центральной нервной системы, фиброз носоглотки и фиброз, вызванный химиотерапией, и другие заболевания, например сильные головные боли, в том числе сильные головные боли, вызванные опухолями гипофиза, болевым синдромом, приступами страха, химиотерапией, рубцеванием ран, недостаточность функции почек вследствие задержки развития, ожирение и задержку развития, связанную с ожирением, задержку развития матки, дисплазию скелета, синдром Ноонана, приступы апноэ во сне, болезнь Грейвза, поликистозное заболевание яичников, ложную кисту поджелудочной железы и асциты, лейкоз, менингиому, опухолевую кахексию, пилоростеноз, псориаз, а также болезнь Альцгеймера. К таким заболеваниям также относится остеопороз.
Авторы настоящего изобретения обнаружили, что соединения приведенной ниже общей формулы обладают сродством и избирательностью в отношении рецепторов соматостатина. Поскольку саматостатин и его пептидные аналоги часто характеризуются плохой биологической доступностью при пероральном введения и низкой избирательностью (Robinson С., Drugs of the Future, 1994, 19, 992; Reubi J.C. et al., TIPS, 1995, 16, 110), то соединения по настоящему изобретению, являющиеся непептидными агонистами или антагонистами соматостатина, можно эффективно использовать для лечения вышеуказанных патологических состояний или заболеваний, обусловленных одним (или несколькими) рецепторами соматостатина. Указанные соединения можно предпочтительно использовать для лечения акромегалии, аденом гипофиза или эндокринных опухолей желудочно-кишечного тракта и поджелудочной железы, включая карциноидный синдром.
Таким образом, объектом настоящего изобретения являются соединения общей формулы
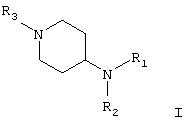
в рацемической, энантиомерной форме или во всех комбинациях указанных форм,
где R1 означает (C1-C6)алкил с линейной или разветвленной цепью, алкенил, алкинил, радикал -(CH2)m-Y-Z11 или -(CH2)m-Z12, в котором
Z11 означает необязательно замещенные (C1-C6)алкил или арил;
Z12 означает циано, циклогексенил, бисфенил, (C3-C7)циклоалкил, необязательно замещенный (С3-С7)гетероциклоалкил, необязательно замещенный арил или необязательно замещенный гетероарил;
или Z12 означает радикал формулы
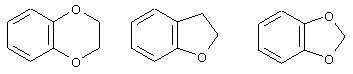
или R1 означает радикал формулы

R2 означает радикал формулы -C(Y)NHX1, -С(O)Х2 или SO2Х3;
R3 означает атом водорода, необязательно замещенный алкил, алкенил, алкинил, необязательно замещенный аралкил, необязательно замещенный гетероарилалкильный радикал или радикал формулы -C(Y)-NHX1, -(СН2)n-С(О)Х2, SO2Х3 или
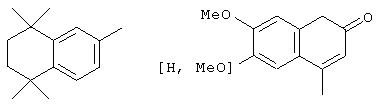
Х1 означает (C1-C15)алкил с линейной или разветвленной цепью, алкенил, алкинил, радикал -(СН2)m-Y-Z21 или -(CH2)pZ22, в котором
Z21 означает (C1-C6)алкил;
Z22 означает циклогексенил, инданил, бисфенил, (C3-C7)циклоалкил, (С3-С7) гетероциклоалкил, моно- или диалкиламино, -С(О)-O-алкил, необязательно замещенные арил или гетероарил
или Z22 означает радикал формулы
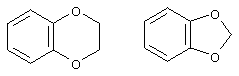
Х2 означает (C1-C10)алкильный радикал с линейной или разветвленной цепью, алкенильный радикал, необязательно замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), алкинильный радикал или радикал формулы -(CH2)m-W-(СН2)q-Z23 или -(СН2)p-U-Z24 у в котором
Z23 означает необязательно замещенные (C1-C6)алкил или арил;
Z24 означает алкил, циклогексенил, бисфенил, необязательно замещенный (C3-C7)циклоалкил, (C3-C7)гетероциклоалкил, циано, амино, моно- или диалкиламино, необязательно замещенные арил или гетероарил;
или Z24 означает радикал формулы
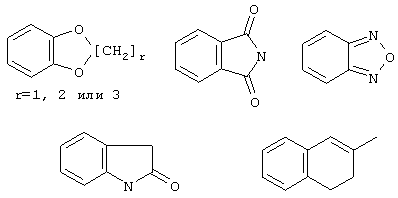
или Х2 означает нижеследующий радикал:
где защитная группа (PG) является Н или трет-бутилоксикарбонилом;
Х3 означает (C1-C10)алкильный радикал с линейной или разветвленной цепью, алкенильный радикал, необязательно замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), CF3 или -(CH2)pZ25, где
Z25 означает необязательно замещенные арил или гетероарил;
или Х3 означает радикал формулы
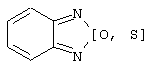
необязательно замещенный одним или несколькими одинаковыми или разными галогенсодержащими радикалами;
Y означает атом кислорода или серы;
W означает атом кислорода или серы или SO2;
U означает ковалентную связь или атом кислорода;
n является целым числом от 0 до 4;
m является целым числом от 1 до 6;
р является целым числом от 0 до 6;
q является целым числом от 0 до 2;
или их аддитивные соли с фармацевтически приемлемыми минеральными или органическими кислотами, за исключением соединений общей формулы I, где R1 означает алкил, алкенил или бензил, R2 означает необязательно замещенный бензилокси и R3 означает аралкил.
Отдельным объектом данного изобретения являются описанные выше продукты общей формулы I, отличающиеся тем, что
i) заместитель или заместители, замещающие арильные радикалы, представленные Z11 и Z12, и гетероарил, представленный Z12, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, -CF3, -OCF3, фенил, фенокси, аминосульфонил;
ii) заместитель или заместители, замещающие гетероциклоалкильный радикал, представленные Z12, независимо выбирают из окси- и алкильных радикалов;
iii) заместитель или заместители, замещающие арильные и гетероарильные радикалы, представленные Z22, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкенил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, аминосульфонил, пиперидиносульфонил, моно- или диалкиламино, -С(О)-O-алкил, -С(О)-алкил или фенил, фенокси, фенилтио, бензилокси, причем фенильный радикал может быть замещен;
iv) заместитель или заместители, замещающие арильные радикалы, представленные Z23 и Z24, циклоалкил или гетероарил, представленные Z24, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, OCHF2, SCF3, нитро, циано, азидо, гидрокси, -С(О)O-алкил, -O-С(О)-алкил, -NH-C(О)-алкил, алкилсульфонил, моно- или диалкиламино, амино, аминоалкил, пирролил, пирролидинил или фенил, фенокси, фенилтио, бензил, бензилокси, причем арильный радикал может быть необязательно замещен одним или несколькими алкильными, CF3 или галогенрадикалами;
v) заместитель или заместители, замещающие арильные или гетероарильные радикалы, представленные Z25, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, OCF3, нитро, циано, -NH-C(О)-алкил, алкилсульфонил, амино, моно- и диалкиламино, фенил, пиридино;
vi) заместитель, замещающий алкильный радикал, представленный R3, является цианорадикалом;
vii) заместитель или заместители, замещающие аралкильный радикал, представленный R3, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, OCF3, OCHF2, SCF3, SCHF2, нитро, циано, -С(О)O-алкил, алкилсульфонил, тиадиазолил или фенил и фенокси, причем фенильный радикал может быть необязательно замещен одним или несколькими галогенрадикалами;
viii) заместитель или заместители, замещающие гетероарилалкильный радикал, представленный R3, независимо выбирают из радикалов, включающих фтор, хлор, бром или нитро.
В приведенных выше определениях "галоген" означает фтор, хлор, бром или иод, предпочтительно хлор, фтор или бром. "Алкил" (за исключением особо оговоренных случаев) предпочтительно означает алкильный радикал с линейной или разветвленной цепью, имеющий 1-6 атомов углерода, такой как метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, втор-бутильный и трет-бутильный, пентильный или амильный, изопентильный, неопентильный, гексильный или изогексильный радикалы. Из алкильных радикалов, содержащих 1-15 атомов углерода, помимо вышеуказанных алкилов можно также назвать гептильные, октильные, нонильные, децильные, додецильные, тридецильные или пентадецильные радикалы.
"Алкенил" за исключением особо оговоренных случаев означает алкильный радикал с линейной или разветвленной цепью, имеющий 1-6 атомов углерода и, по крайней мере, одну ненасыщенность (двойная связь), такой как, например, винил, аллил, пропенил, бутенил или пентенил. "Алкинил" за исключением особо оговоренных случаев означает алкильный радикал с линейной или разветвленной цепью, имеющий 1-6 атомов углерода и по крайней мере одну двойную ненасыщенность (тройная связь), такой как, например, этинил, пропаргил, бутинил или пентинил.
Термин "циклоалкил" означает моноциклическую углеродную систему, имеющую 3-7 атомов углерода и предпочтительно циклопропильное, циклобутильное, циклопентильное или циклогексильное кольцо. "Гетероциклоалкил" означает насыщенный циклоалкил, имеющий 2-7 атомов углерода и по крайней мере один гетероатом. Указанный радикал может содержать несколько одинаковых или разных гетероатомов. Гетероатомы предпочтительно выбирают из кислорода, серы или азота. В качестве примеров гетероциклоалкила можно привести пирролидиновое, пирролидиноновое, имидазолидиновое, пирразолидиновое, изотиазолидиновое, тиазолидиновое, изоксазолидиновое, пиперидиновое, пиперазиновое или морфолиновое кольцо.
Алкоксильные радикалы, такие как, например, метокси, этокси, пропилокси или изопропилоксирадикал, помимо этого, включают вторичный или третичный бутокси, пентилокси с линейной цепью, соответствуют вышеуказанным алкильным радикалам. Термин "низший алкилтио" предпочтительно означает радикалы, в которых алкильный радикал имеет указанные выше значения, например метилтио, этилтио. Термин "алкилсульфонил" предпочтительно означает радикалы, в которых алкильный радикал имеет указанные выше значения.
"Арил" означает ароматический радикал, имеющий одно или несколько конденсированных колец, такой как, например, фенильный или нафтильный радикал. "Гетероарил" означает ароматический радикал, имеющий одно или несколько конденсированных колец, причем, по крайней мере, одно кольцо содержит один или несколько одинаковых или разных гетероатомов, выбираемых из серы, азота или кислорода. В качестве примера гетероарильного радикала можно привести тиенильный, фурильный, пирролильный, имида золильный, пиразолильный, изотиазолильный, тиазолильный, изоксазолильный, оксазолильный, триазолильный, пиридильный, пиразинильный, пиримидильный, хинолильный, изохинолильный, хиноксалинильный, бензотиенильный, бензофурильный, индолильный, бензоксадиазоильный радикалы.
Термины "моно- и диалкиламино" предпочтительно означают радикалы, в которых алкильные радикалы имеют указанные выше значения, такие как, например, метиламино, этиламино, диметиламино, диэтиламино или (метил)(этил)амино.
Символ  соответствует месту присоединения радикала. Если в радикале не указано место присоединения, это значит, что для присоединения использовано одно из мест, имеющихся в данном радикале для указанного присоединения.
соответствует месту присоединения радикала. Если в радикале не указано место присоединения, это значит, что для присоединения использовано одно из мест, имеющихся в данном радикале для указанного присоединения.
Отдельным объектом настоящего изобретения являются описанные выше соединения общей формулы I, в которой
R1 означает (C1-C6)алкильный радикал с линейной или разветвленной цепью, радикал -(СН2)m-Y-Z11 или -(CH2)mZ12, где
Z11 означает (C1-C6)алкил;
Z12 означает бисфенил, (С3-С7)циклоалкил, необязательно замещенный (С3-С7)гетероциклоалкил, арил или гетероарил, необязательно замещенный одним или несколькими заместителями, выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси,
или Z12 означает
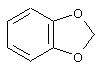
Y означает атом кислорода;
или R1 означает радикал формулы
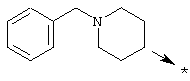
R2 означает радикал формулы -C(Y)NHX1, -C(O)X2 или SO2Х3, где
Х1 означает (С1-С15)алкильный радикал с линейной или разветвленной цепью или -(CH2)pZ22, в котором
Z22 означает циклогексенил, бисфенил, (С3-С7)циклоалкил, (С3-С7)гетероциклоалкил, моно- или диалкиламино, -С(О)-O-алкил, арил или гетероарил, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(О)-O-алкил, -С(О)-алкил или фенил,
или Z22 означает радикал формулы

Х2 означает (С1-С10)алкильный радикал с линейной или разветвленной цепью, алкинил, радикал формулы -(СН2)m-W-(CH2)q-Z23 или -(СН2)p-U-Z24, в которой
W означает SO2;
U означает ковалентную связь;
Z23 означает арильный радикал;
Z24 означает циклогексенил, бисфенил, (С3-С7)циклоалкил, необязательно замещенный аминоалкилом, арильный или гетероарильный радикал, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, SCF3, гидрокси, -С(О)-O-алкил, моно- или диалкиламино, амино,
или Z24 означает радикал формулы

или Х2 означает
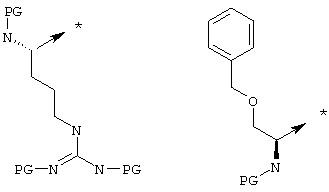
Х3 означает радикал -(CH2)pZ25, где Z25, является арильным радикалом, необязательно замещенным одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3;
R3 означает атом водорода, необязательно замещенный алкильный, алкенильный, гетероарилалкильный радикал или радикал формулы -C(Y)-NHX1, -C(O)X2 или SO2Х3, где
Х1 означает радикал -(CH2)pZ22, в котором
Z22 означает арильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенилом, причем фенильный радикал в свою очередь необязательно замещен одним или несколькими галогенами, или радикал -(СН2)p-U-Z24, где
Z24 означает алкил, (С3-С7)циклоалкил, (С3-С7)гетероциклоалкил, бисфенил, амино, моно- или диалкиламино, арил или гетероарил, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, гидрокси, CF3, нитро, амино, моно- и диалкиламино, пирролил;
или Х2 означает радикал формулы
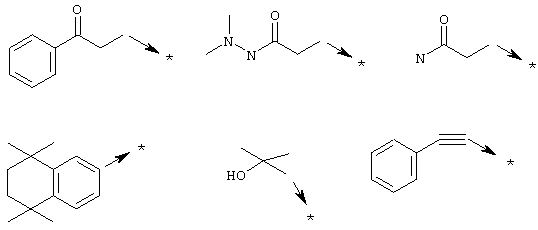
Х3 означает (С1-С10)алкильный радикал с линейной или разветвленной цепью, винильный радикал, замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), CF3 или -(CH2)pZ25, где
Z25 означает арил или гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-C(О)-алкил, моно- и диалкиламино.
R1 предпочтительно означает (C1-C6) алкильный радикал с линейной или разветвленной цепью, радикал -(CH2)m-Y-Z11 или -(CH2)m-Z12, в котором
Z11 означает (C1-C6)алкил;
Z12 означает нафтил, морфолино, бисфенил, пирролидинил, замещенный оксирадикалом, или фенильный, пиперазинильный, пиридинильный и индолильный радикалы, которые необязательно замещены одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих бром, фтор, хлор, алкил, алкокси, -CF3, -OCF3,
или Z12 означает

Y означает атом кислорода;
или R1 означает радикал нижеследующей формулы:
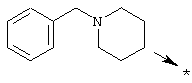
R2 предпочтительно означает радикал формулы -C(Y)NHX1, -С(O)Х2 или SO2Х3, где
X1 означает (С1-С10)алкил с линейной или разветвленной цепью или радикал -(CH2)pZ22, в котором
Z22 означает циклогексил, циклогексенил, бисфенил, морфолино, пиперидино, моно- или диалкиламино, -С(О)-O-алкил либо фенил, нафтил или фурил, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(О)-O-алкил, -С(О)-алкил или фенил,
или Z22 означает радикал формулы

Х2 означает алкил, алкинил, радикал -(СН2)m-W-(CH2)q-Z23 или -(CH2)pZ24, в котором
W означает SO2;
Z23 означает фенильный радикал;
Z24 означает циклогексенил, бисфенил, циклогексил, необязательно замещенный аминоалкилом, либо фенильный, нафтильный, бензотиенильный, тиенильный или индолильный радикал, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, SCF3, гидрокси, -O-С(О)-алкил, -NH-C(О)-алкил, моно- или диалкиламино, амино, или
Z24 означает радикал формулы

или Х2 означает

Х3 означает радикал -(CH2)pZ25, в котором Z25 является фенильным радикалом, необязательно замещенным одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3.
R3 предпочтительно означает атом водорода, алкильный, алкенильный или фурилметильный радикал, замещенный одним или несколькими нитрорадикалами, или радикал формулы -C(Y)-NHX1, -С(O)Х2 или SO2Х3, где
Х1 означает радикал -(CH2)pZ22, в котором
Z22 означает фенильный или нафтильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенильным радикалом, который в свою очередь замещен одним или несколькими галогенами, или радикал -(СН2)p-U-Z24, где
Z24 означает алкил, циклогексил, тетрагидрофурил, бисфенил, амино, моно- или диалкиламино, а также фенил, индолил, тиенил, пиридинил, бензотиенил и фурил, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, амино, моно- и диалкиламино, нитро, гидрокси, пирролил;
или Х2 означает радикал формулы
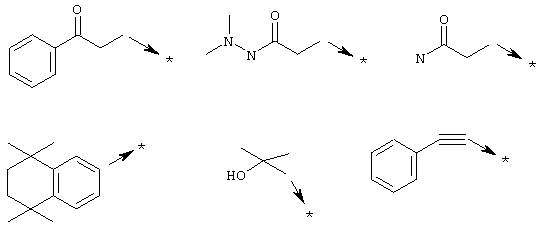
Х3 означает (С1-С10)алкильный радикал с линейной или разветвленной цепью, винильный радикал, замещенный фенилом, CF3 или радикал -(CH2)pZ25, в котором
Z25 означает фенильный, нафтильный, тиенильный, пиразолильный или тиазолильный радикал, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-C(О)-алкил, моно- и диалкиламино;
В наиболее предпочтительном случае R1 означает радикал -(CH2)mZ12, в котором m=2 и Z12 означает бисфенил или индолильный радикал, замещенный одним или несколькими заместителями, независимо выбираемыми из алкильных и алкоксильных радикалов.
В наиболее предпочтительном случае R2 означает радикалы формулы -C(Y)NHX1 и -С(O)Х2, в которой
Y означает S;
X1 означает фенильный радикал, необязательно замещенный одним или несколькими азидорадикалами;
Х2 означает -(CH2)pZ24, где
р равно 1, 2 или 3;
Z24 означает циклогексил, фенил или бензотиенил, необязательно замещенный одним или несколькими радикалами, выбираемыми из фтора, хлора, брома, иода или -CF3.
В наиболее предпочтительном случае R3 означает атом водорода или метильный радикал.
Соединения по данному изобретению могут быть получены в твердой или жидкой фазе.
А) Синтез в жидкой фазе с использованием N-замещенного пиперидона
А1) Восстановительное аминирование
Указанный синтез осуществляют в соответствии со следующей схемой:
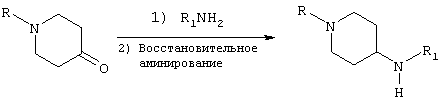
где R означает метил или Boc и R1 имеет приведенные выше значения.
Общий способ состоит в следующем: N-замещенный пиперидон подвергают восстановительному аминированию (Abdel-Magid, A.F.; Maryanoff, C.A.; Carson, K.G., Tetrahedron Lett. 1990, 31, 5595-5598; Abdel-Magid, A.F.; Carson, K.G.; Harris, B.D.; Maryanoff, C.A.; Shah, R.D., J. Org. Chem. 1996, 61, 3849-3862) в безводных хлорированных растворителях, таких как дихлорэтан, в присутствии первичного амина (1,1-1,5 экв.), восстановителя, такого как триацетоксиборогидрид натрия (1,1-1,5 экв.) и уксусной кислоты (10 мас.% в расчете на N-замещенный пиперидон). Реакционную смесь перемешивают в течение 1-4 часов при комнатной температуре. В некоторых случаях добавляют раствор соды (0,1 М раствор) и смесь перемешивают в течение 20-90 минут. Если раствор соды не добавляют, реакционную смесь промывают насыщенным раствором бикарбоната натрия, хлоридом натрия, сушат над сульфатом магния, фильтруют и концентрируют. Требуемый продукт очищают флеш-хроматографией на силикагеле.
Способ получения 1
трет-Бутил-4-[(3,3-дифенилпропил)амино]-1-пиперидинкарбоксилат (С25Н34N2O2, М=394,56)
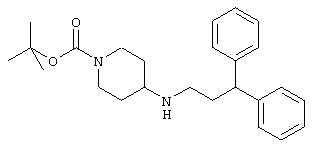
3,3-Дифенилпропиламин (5,8 г, 27,5 ммоль), триацетоксиборогидрид натрия (6,36 г, 30 ммоль) и 0,5 мл уксусной кислоты добавляют к 5 г (25 ммоль) N-Boc-пиперидона в 100 мл безводного дихлорэтана. Мутный желтый раствор перемешивают при комнатной температуре в течение 1 часа. Затем добавляют 50 мл раствора соды (0,1 М раствор) и смесь перемешивают в течение 30 минут. Органическую фазу промывают насыщенным раствором бикарбоната натрия, хлоридом натрия, сушат над сульфатом магния, фильтруют и концентрируют, получая 10 г желтого твердого вещества. Указанное твердое вещество очищают флеш-хроматографией на силикагеле, элюируя смесью гептан/этилацетат (4/1, 3/1, 2/1 и 1/1) и затем чистым этилацетатом. Фракции концентрируют в вакууме, получая при этом 5,6 г (выход 57%) бледно-желтого твердого вещества.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,27 (м, 8Н); 7,16 (м, 2Н); 4 (дд, J=6,4 и 14 Гц, 3Н); 2,73 (м, 2Н); 2,55 (м, 3Н); 2,26 (кв, J=7,6 Гц, 2Н); 1,78 (д, J=12 Гц, 2Н); 1,45 (с, 9Н); 1,15 (квд, J=4,4 и 12,8 Гц, 2Н). МС/ЖХ: m/z=395,2 (М+Н).
Указанным способом получают ряд 4-аминозамещенных-1-пиперидинов с приведенными ниже другими группами R1:

А2а) Введение функциональных групп в пиперидины
А2а) Синтез мочевин и тиомочевин
Мочевины и тиомочевины синтезируют способом, описанным в литературе (Kaldor, S.W.; Siegel, M.G.; Fritz, J.E.; Dressman, B.A.; Hahn, P.J. Tetrahedron Lett 1996, 37, 7193-7196; Kaldor, S.W.; Fritz, J.E.; Tang, J.; McKinney, E.R., Bioorg. Med. Chem. Lett. 1996, 6, 3041-3044; Booth, R.J.; Hodges, J.C. J. Am. Chem. Soc. 1997, 119, 4882-4886; Flynn, D.L.; Crich, J.Z.; Devraj, R.V.; Hockerman, S.L.; Parlow, J.J.; South, M.S.; Woodard, S.; J. Am. Chem. Soc. 1997, 119, 4874-4881), в соответствии со следующей схемой:
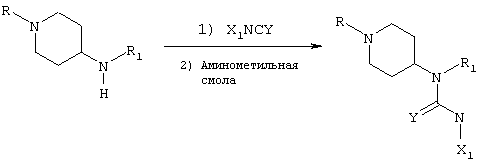
где R означает метил или Вос, Х1 и Y имеют указанные выше значения. Следует отметить, что в том случае, когда R означает Вое, полученное таким образом соединение является конечным продуктом, соответствующим формуле I по настоящему изобретению, который также можно использовать в качестве промежуточного соединения в процессе синтеза.
Общий способ состоит в следующем: изоцианат или изотиоцианат (1,1-1,5 экв.) добавляют к 4-аминозамещенному-1-пиперидину в апротонных растворителях, таких как дихлорметан, тетрагидрофуран или диметилформамид, и смесь перемешивают в течение периода времени от 45 минут до 18 часов при комнатной температуре. Добавляют аминометильную смолу (Novabiochem, 1,33 ммоль/г, 0,2-1 экв.) и смесь перемешивают в течение периода времени от 45 минут до 18 часов. В некоторых случаях добавляют основную ионообменную смолу, такую как IRA-68 (Gayo, L.M.; Suto, M.J. Tetrahedron Lett. 1997, 38, 513-516). Смолы фильтруют и фильтрат концентрируют. Полученный продукт можно очистить другими способами, используя картриджи с силикагелем или основным оксидом алюминия (500 мг, Interchim).
Пример А2а
трет-Бутил-4-((3,3-дифенилпропил)-[[3-(трифторметил)анилино]карбонил}амино)-1-пиперидинкарбоксилат (С33Н38F3N3О3, М=581,68)
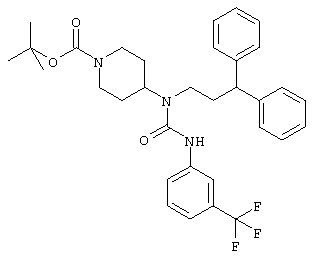
246 мг (1,32 ммоль) 3-(трифторметил)фенилизоцианата добавляют к раствору трет-бутил-4-[(3,3-дифенилпропил)амино]-1-пиперидинкарбоксилата (470 мг, 1,2 ммоль) в 5 мл дихлорметана. Раствор перемешивают в течение 45 минут, добавляют аминометильную смолу (180 мг, 0,36 ммоль) и реакционную смесь снова помещают в ротационный шейкер на 45 минут. Смолу фильтруют и промывают дихлорметаном. Фильтрат концентрируют в вакууме, получая при этом 610 мг (выход 87%) белой пены.
ЯМР 1H (CD3OD, 400 МГц): δ 7,71 (с, 1Н); 7,57 (д, 1Н); 7,43 (т, 1Н); 7,26 (м, 10Н); 7,15 (м, 1Н); 4,1 (м, 3Н); 3,97 (дд, J=7,6 и 10 Гц, 1Н); 3,17 (м, 2Н); 2,75 (м, 2Н); 2,35 (м, 2Н); 1,65 (д, J=12 Гц, 2Н); 1,46 (с, 9Н, трет-бутильная группа); 1,39 (дд, J=2,4 и 10,8 Гц, 2Н); 1,29 (с, 1Н). МС/ЖХ: m/z=582 (M+H).
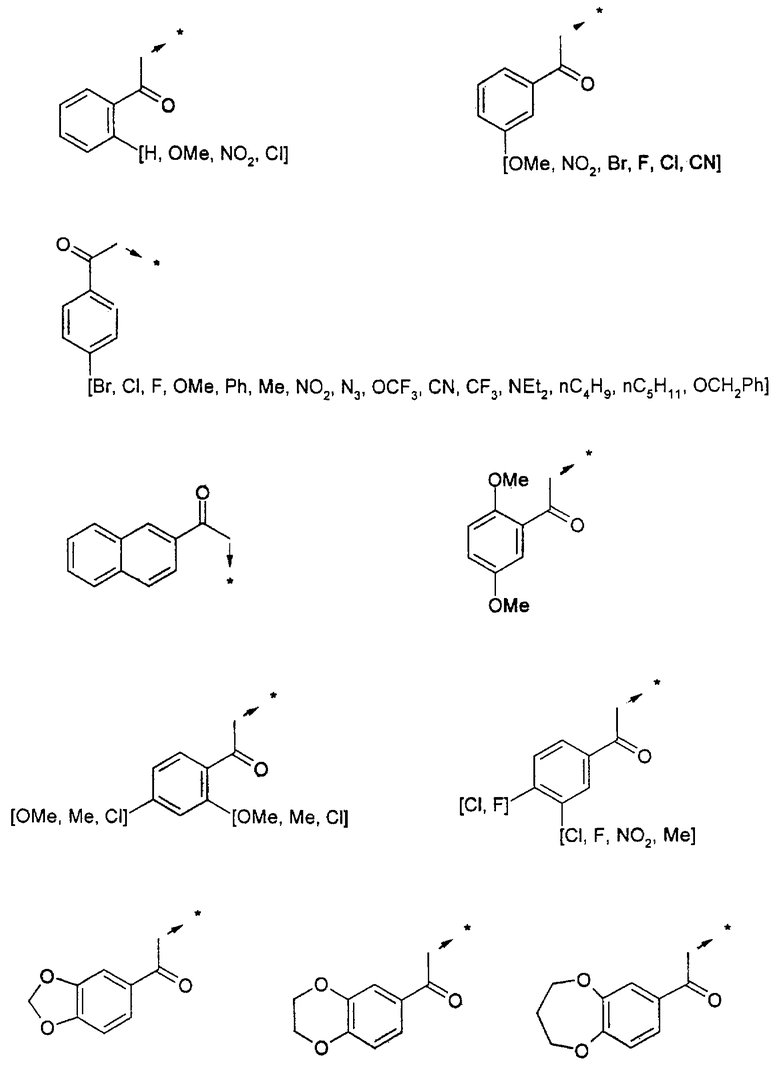
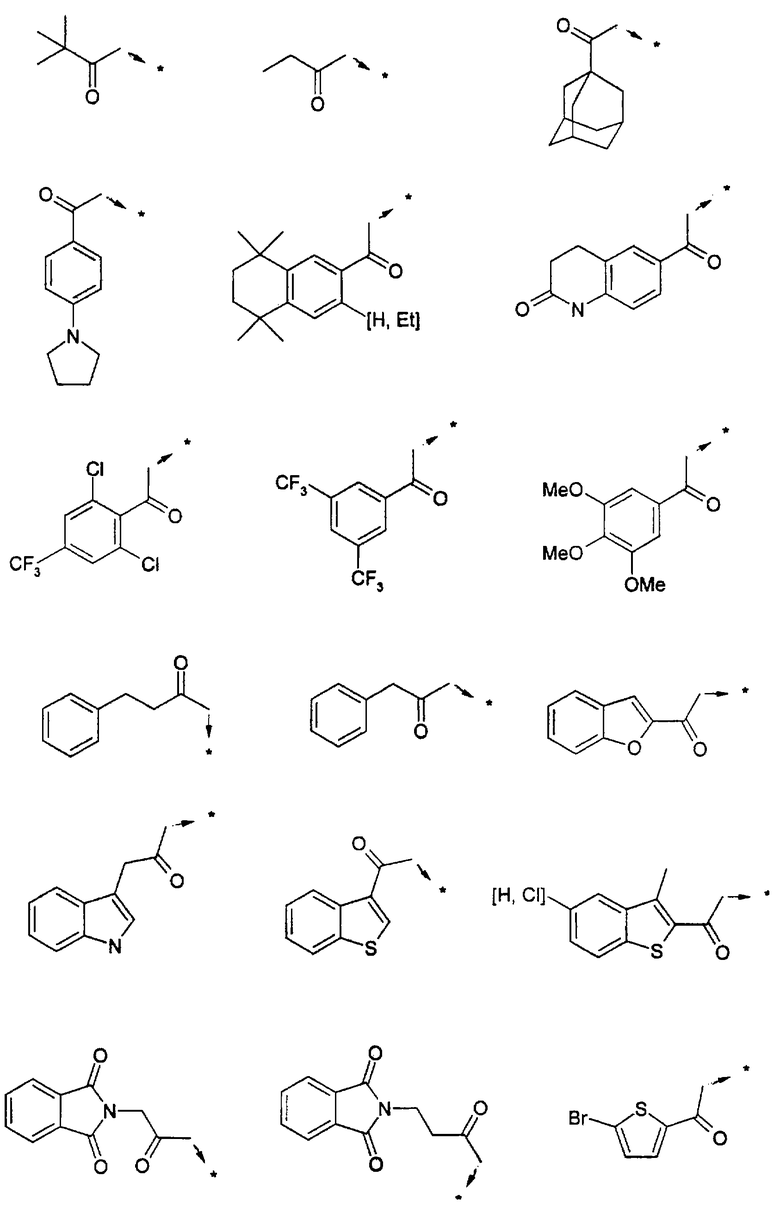
Ниже представлены группы Х1, используемые для синтеза мочевин (Y=О) вышеописанным способом, которые соответствуют группам R1, приведенным в пункте А1:
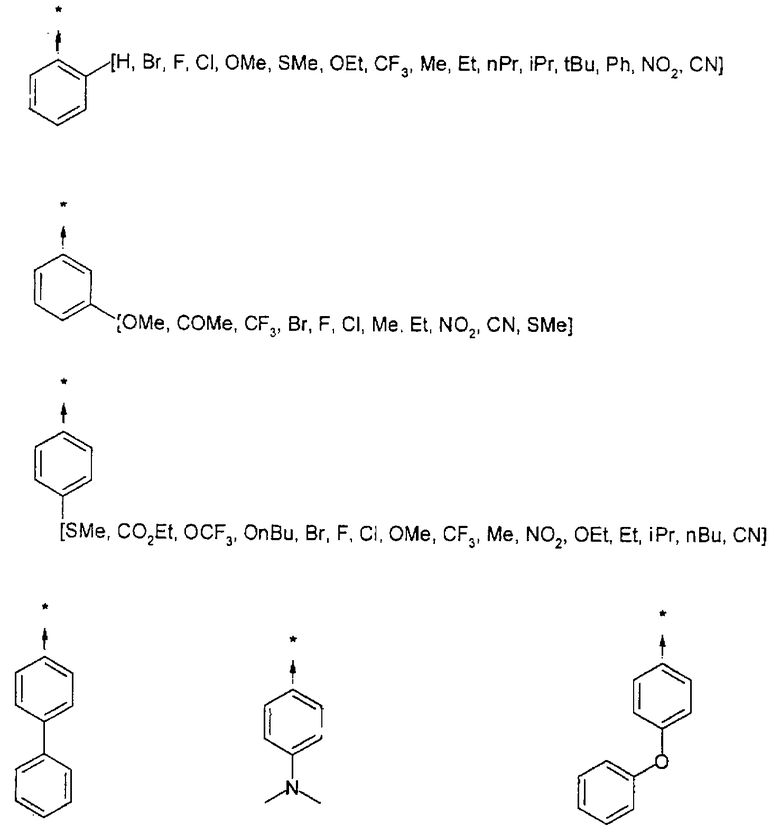
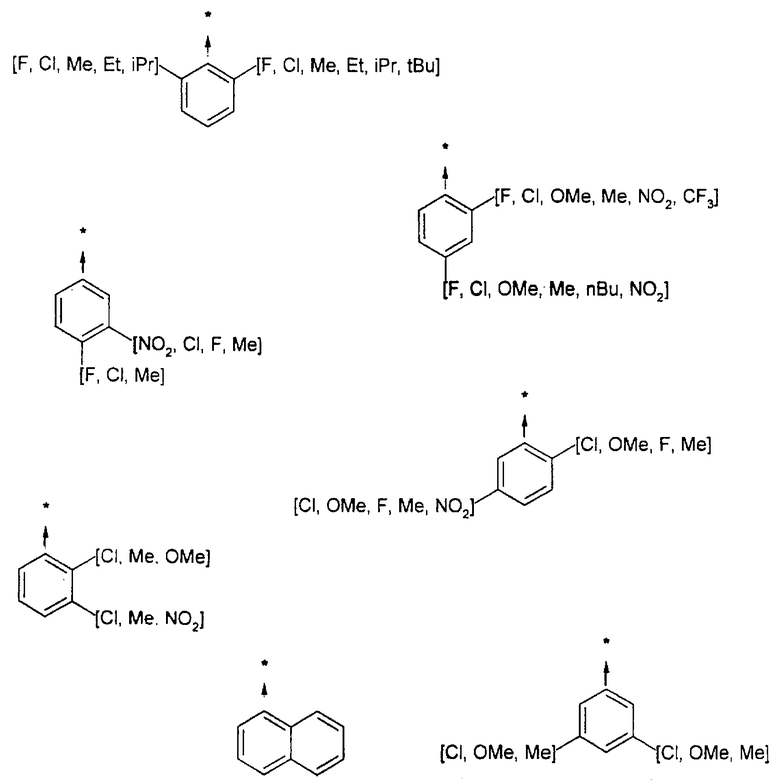
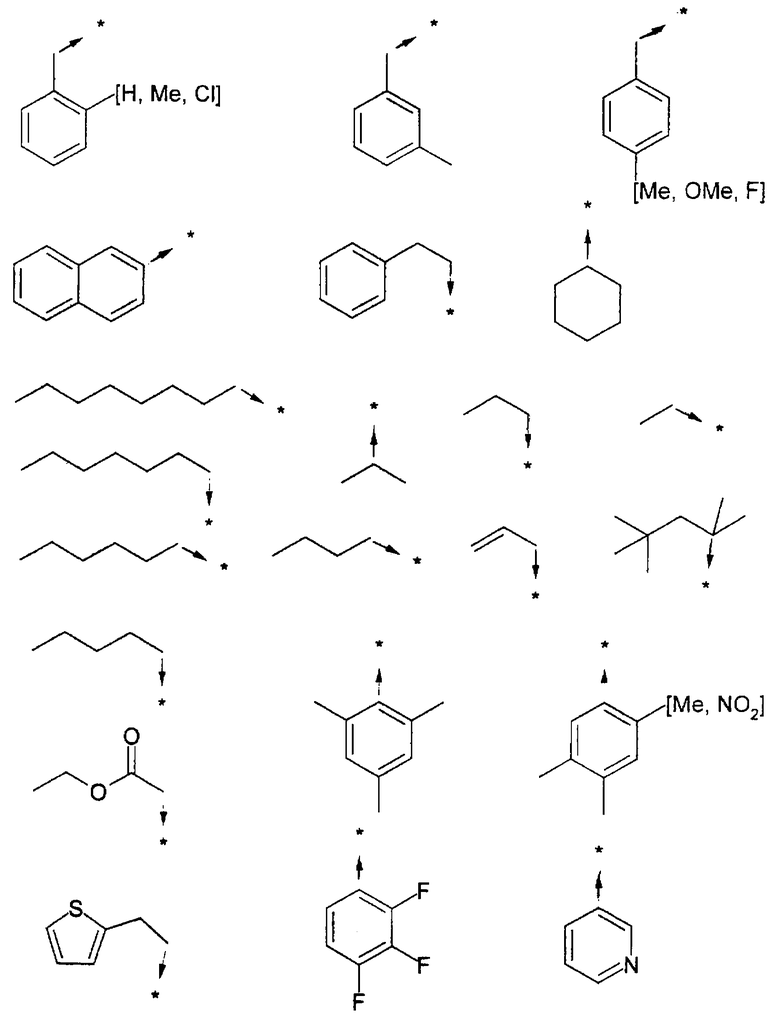
Ниже представлены группы X1, используемые для синтеза тиомочевин (Y=S) вышеописанным способом, которые соответствуют группам R1, приведенным в пункте А1:
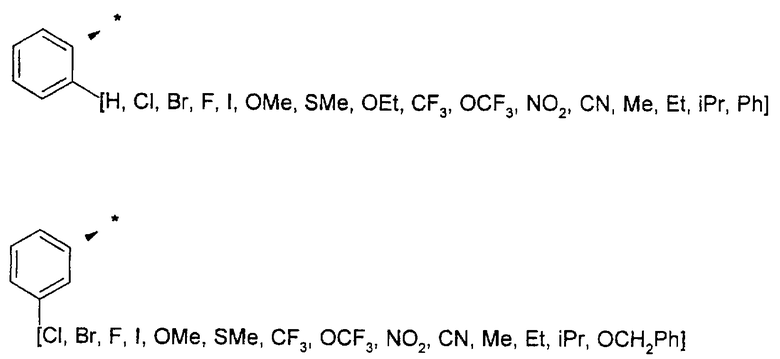

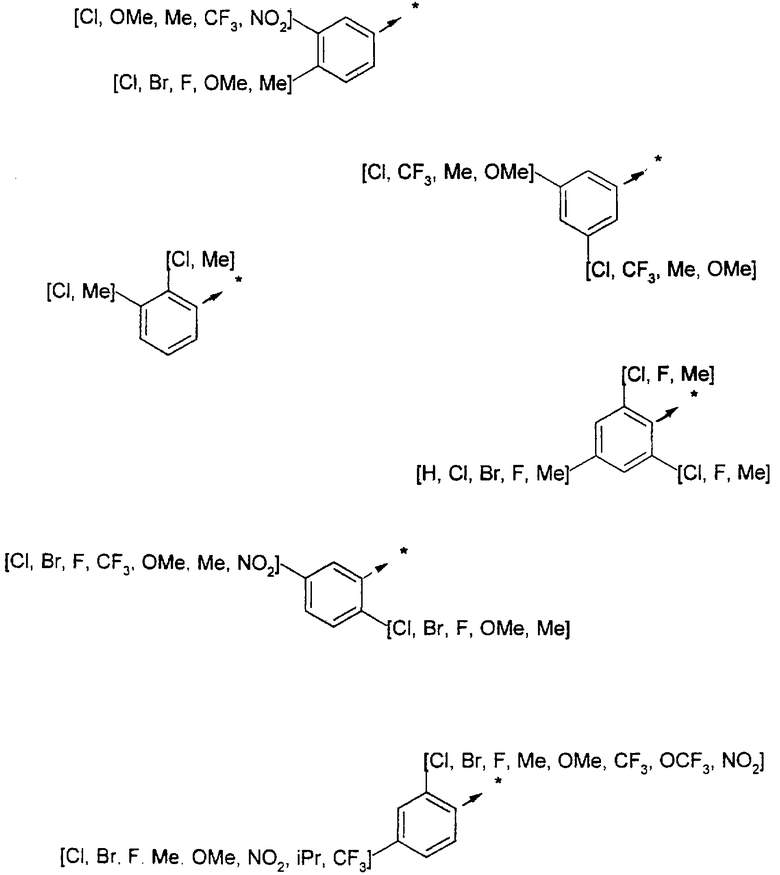

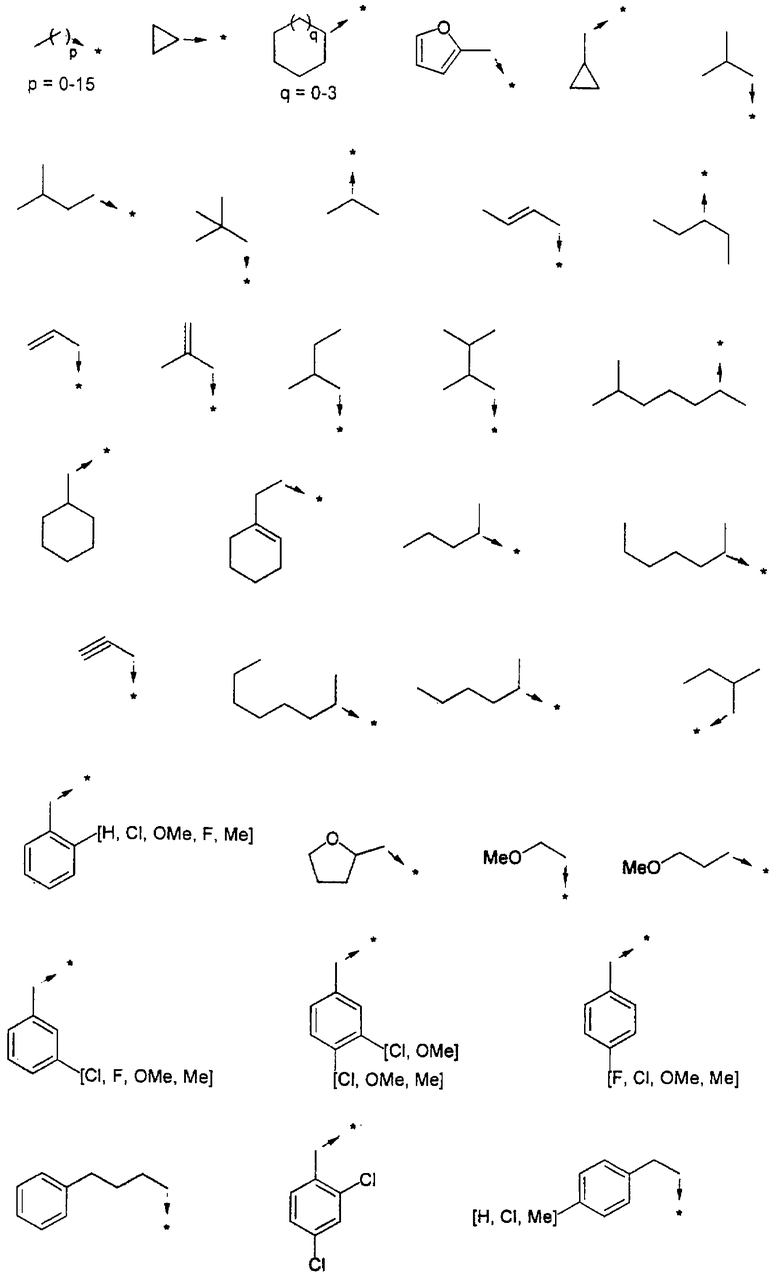
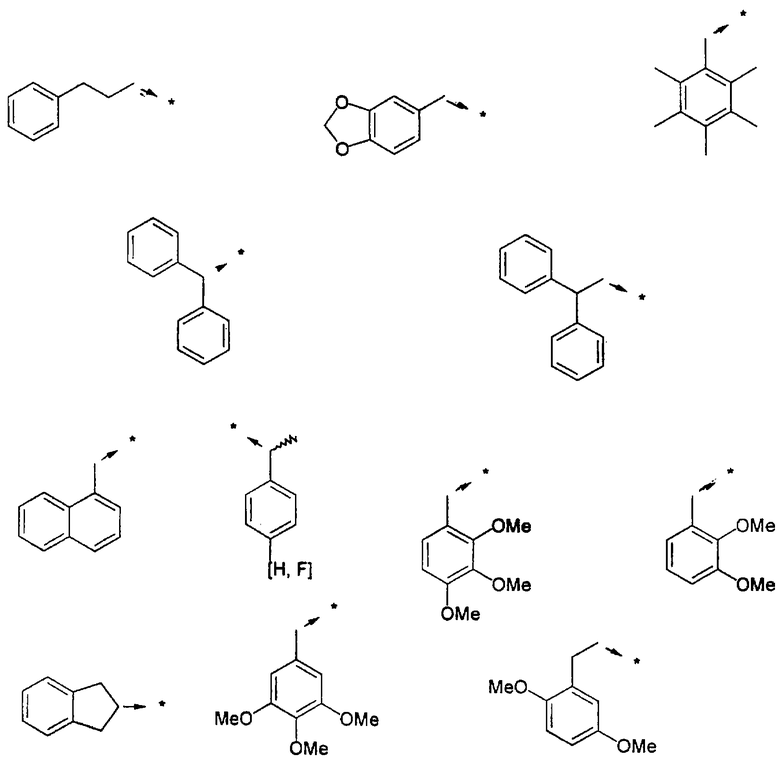
A2b) Синтез амидов из карбоновых кислот
Синтез амидов из карбоновых кислот осуществляют в соответствии со следующей схемой реакций:
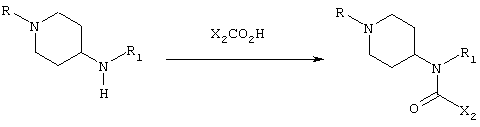
где R означает метил или Boc и Х2 имеет указанные выше значения. Следует отметить, что в том случае, когда R означает Boc, полученное таким образом соединение является конечным продуктом, соответствующим формуле I по настоящему изобретению, который также можно использовать в качестве промежуточного соединения в процессе синтеза.
Общий способ состоит в следующем: карбоновую кислоту (1,1-2,5 экв.), растворенную в безводном апротонном растворителе, таком как дихлорметан, диметилформамид или тетрагидрофуран, активируют 1-этил-3-(3-диметиламинопропил)карбодиимидом, связанным со смолой (P-EDC, Novabiochem, 2,33 ммоль/г, 1,3-3 экв.) (Desai, M.C.; Stephens Stramiello, L.M. Tetrahedron Lett. 1993, 34, 7685-7688). Полученную смесь перемешивают в течение 5-30 минут при комнатной температуре. Затем добавляют 4-аминозамещенный-1-пиперидин, предварительно растворенный в безводном апротонном растворителе, таком как дихлорметан, диметилформамид или тетрагидрофуран, и реакционную смесь перемешивают при комнатной температуре в течение 1-18 часов. В некоторых случаях добавляют основную ионообменную смолу (IRA-68, SAX) и смесь снова перемешивают при комнатной температуре в течение 1-18 часов. Смолы фильтруют через фритту, картридж с основной ионообменной смолой (IRA-68, SAX) или картридж с оксидом алюминия (500 мг, Interchim).
Пример А2b
трет-Бутил-4-{(3,4-диметоксифенетил)[2-(1H-индол-3-ил)ацетил]амино}-1-пиперидинкарбоксилат (С35Н41H3О3, М=551,74)

512 мг (1,12 ммоль, 1,4 экв.) смолы Р-EDC подвергают предварительному набуханию в дихлорметане. Добавляют 2-(1H-индол-3-ил)уксусную кислоту (153 мг, 0,875 ммоль, 1,1 экв.) и смесь перемешивают в течение 10 минут. Добавляют трет-бутил-4-[(3,3-дифенилпропил)амино]-1-пиперидинкарбоксилат (292 мг, 0,8 ммоль) в тетрагидрофуране и реакционную смесь перемешивают в течение ночи. Добавляют 2 шпателя основной ионообменной смолы IRA-68 и реакционную смесь снова перемешивают в течение ночи. Смолы фильтруют и фильтрат концентрируют в вакууме, получая при этом 250 мг (выход 86%) бледно-желтой пены.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,63 (д, J=8 Гц, 1H); 7,44 (д, J=8 Гц, 1H); 7,36 (д, J=8 Гц, 1H); 7,26 (д, J=8 Гц, 1H); 7,2 (м, 6Н); 7,13 (м, 3Н); 7,1 (м, 2Н); 6,68 (с, 1H); 4-3,75 (м, 4Н); 3,65 (с, 1H); 3,2 (м, 1H); 3 (м, 1H); 2,75 (м, 1H); 2,26 (м, 3Н); 1,6 (м, 2Н); 1,44 (с, 9Н); 1,13 (м, 2Н). МС/ЖХ: m/z=552,4 (М+Н).
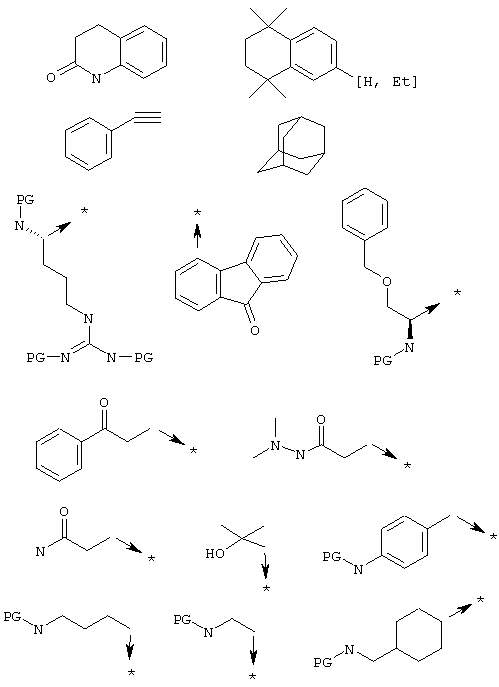
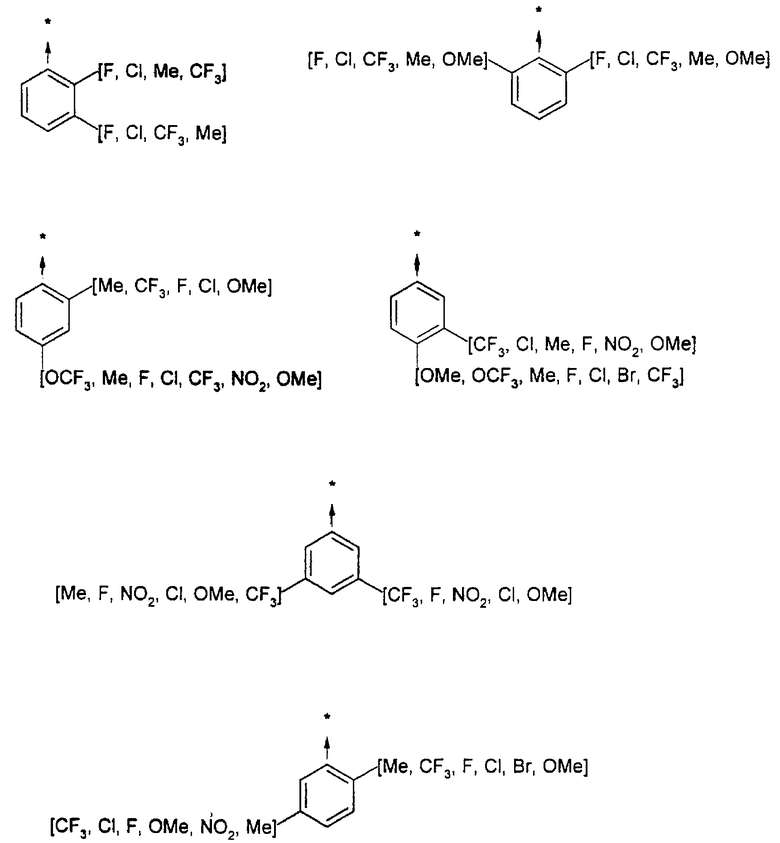
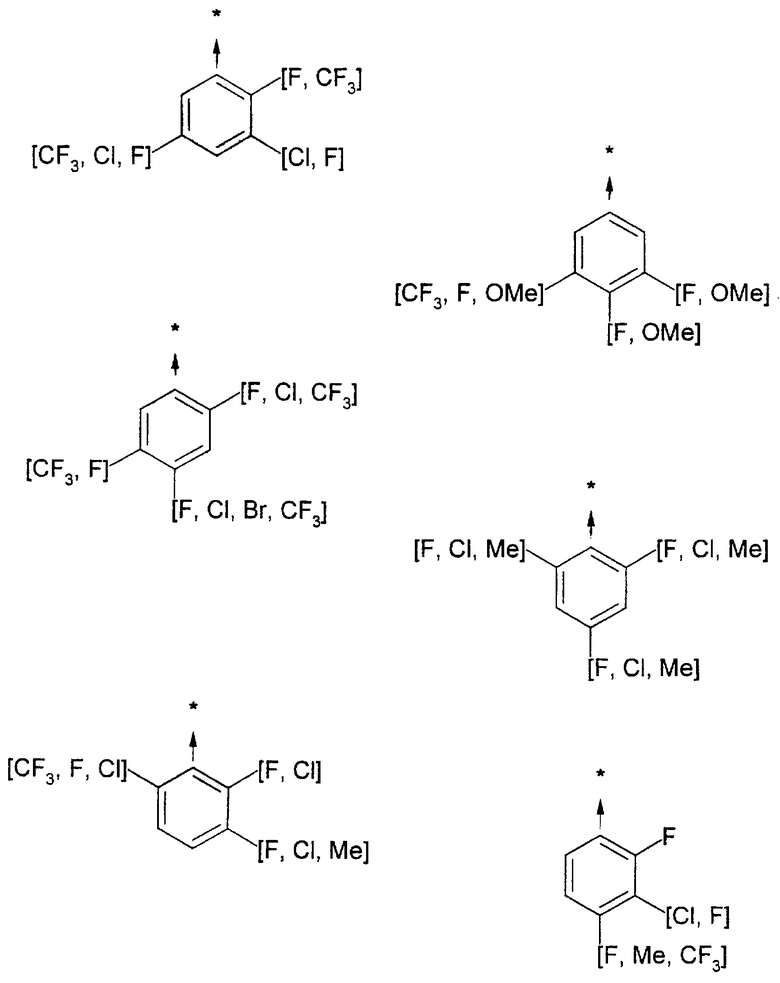
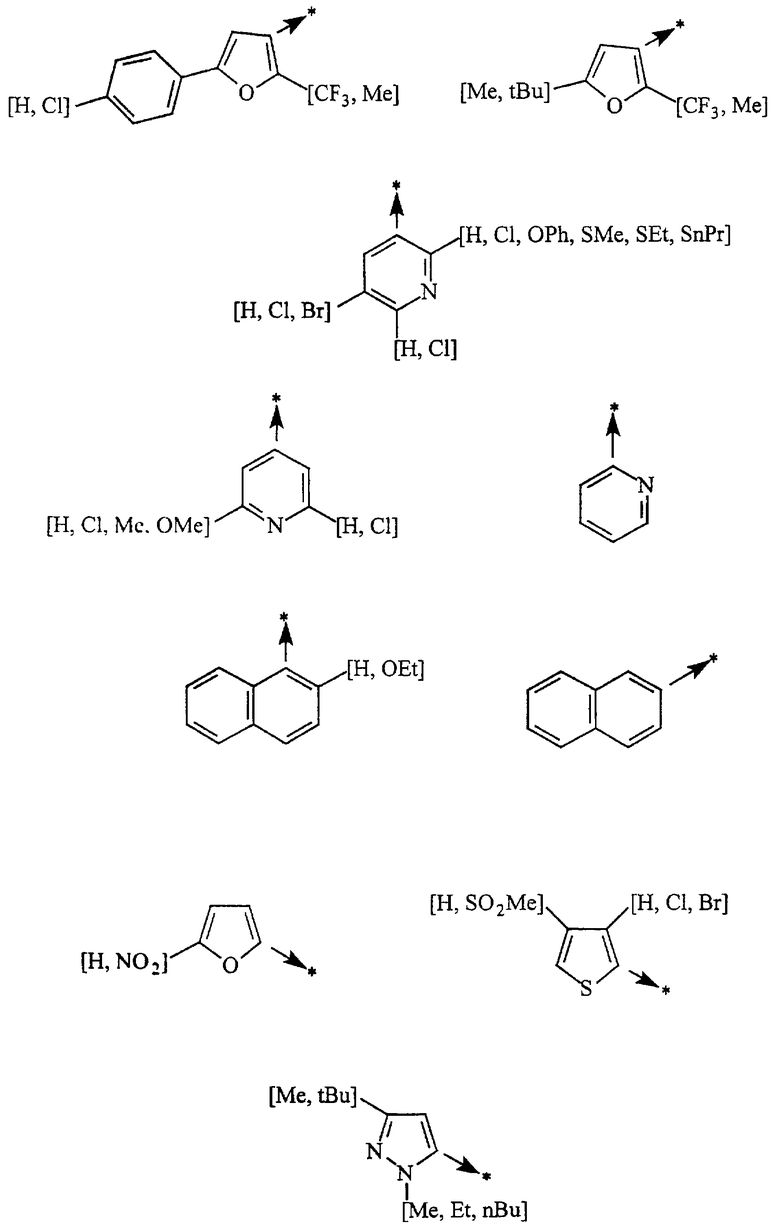
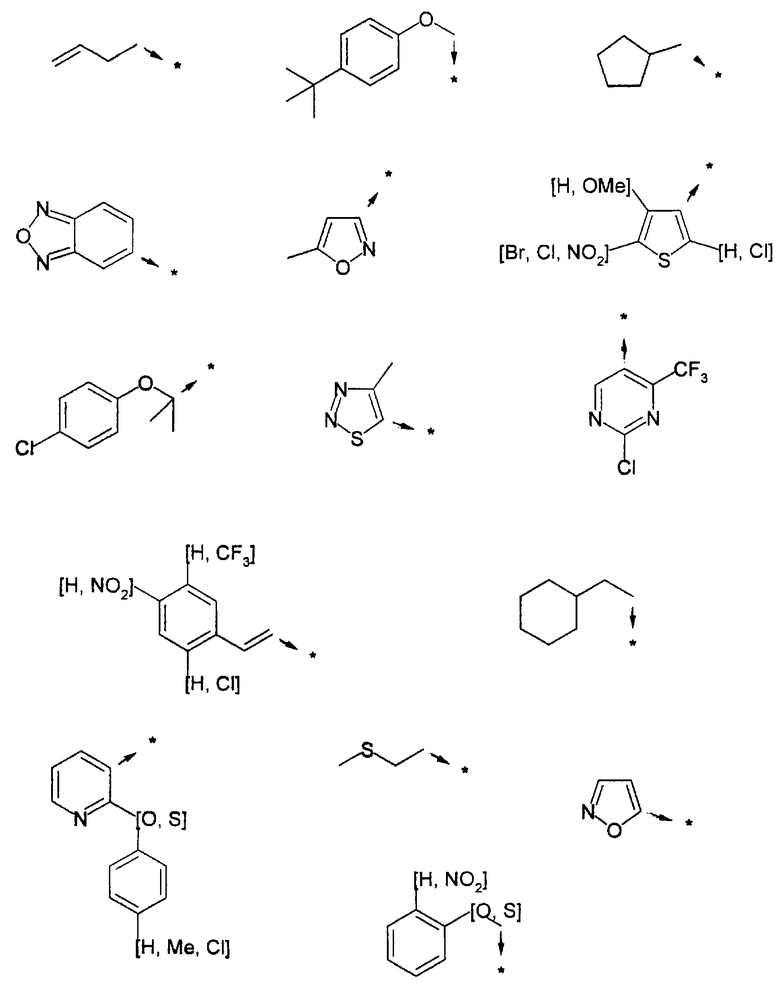
Указанным способом синтезируют ряд амидов. Ниже приведены возможные радикалы Х2:
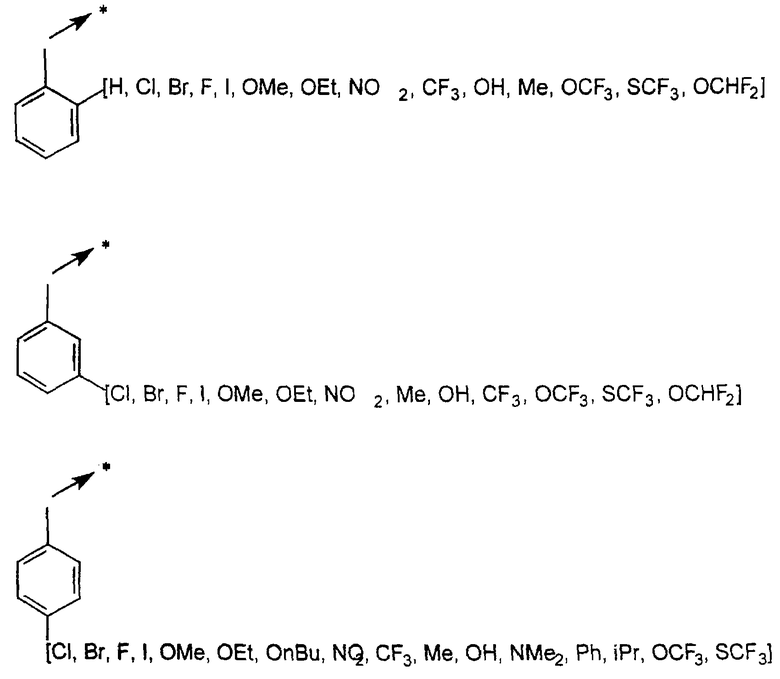

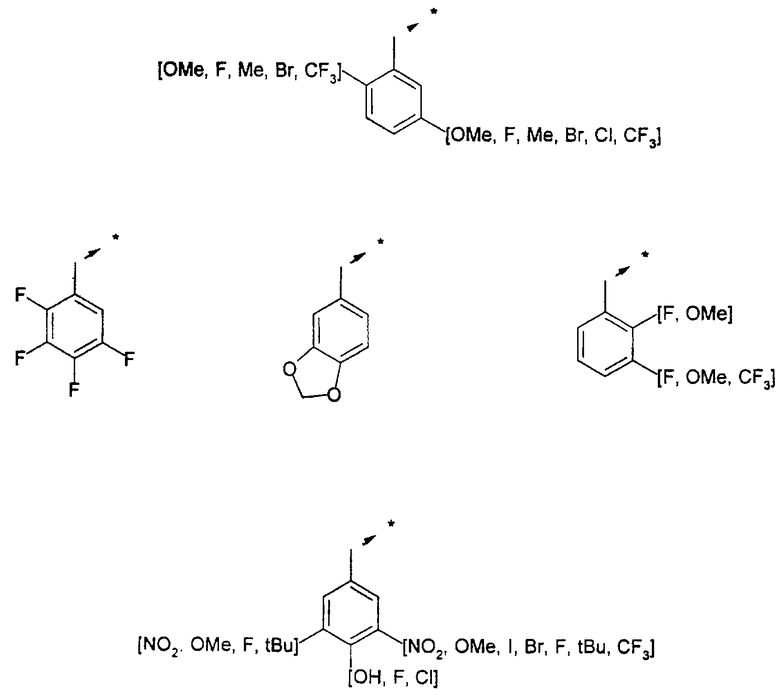
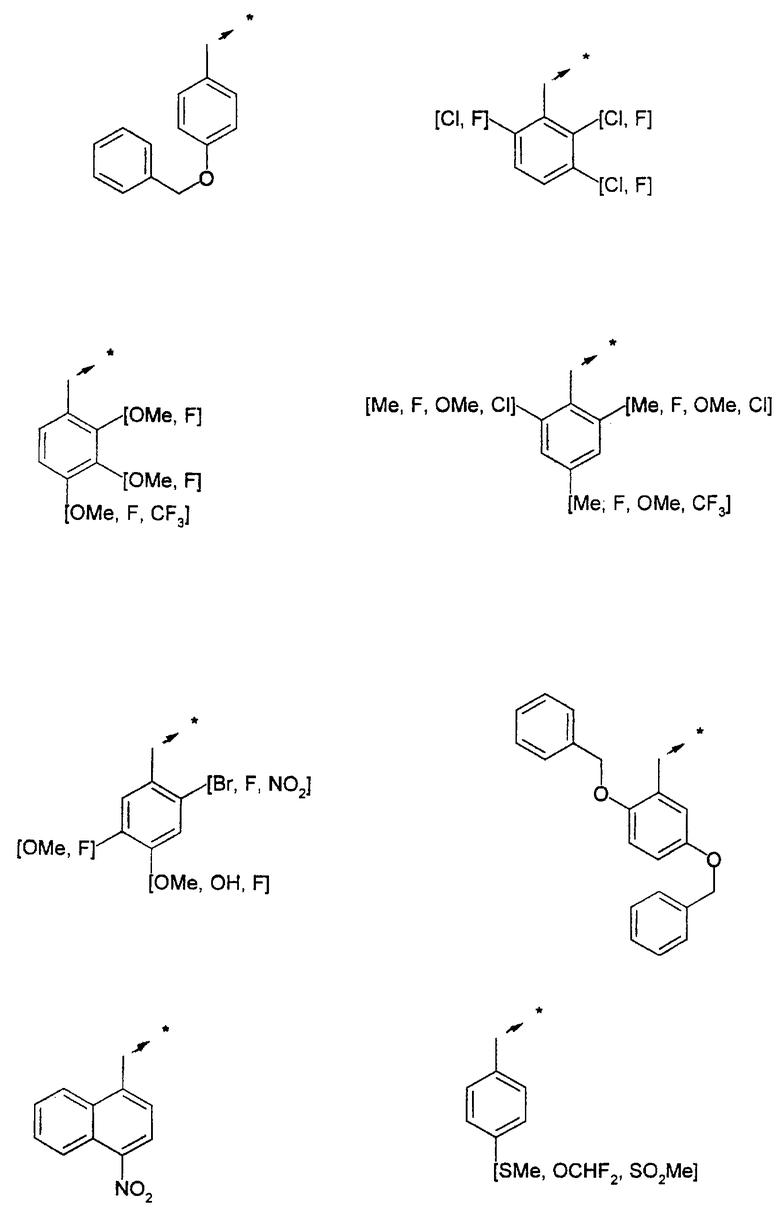
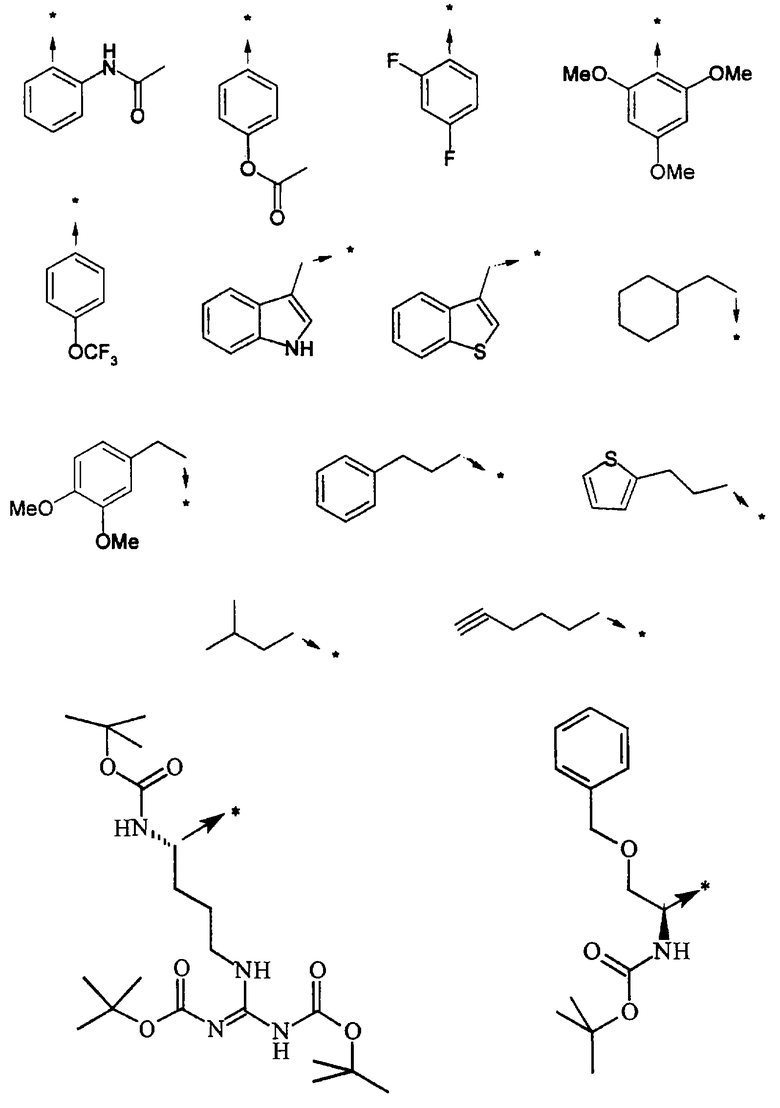
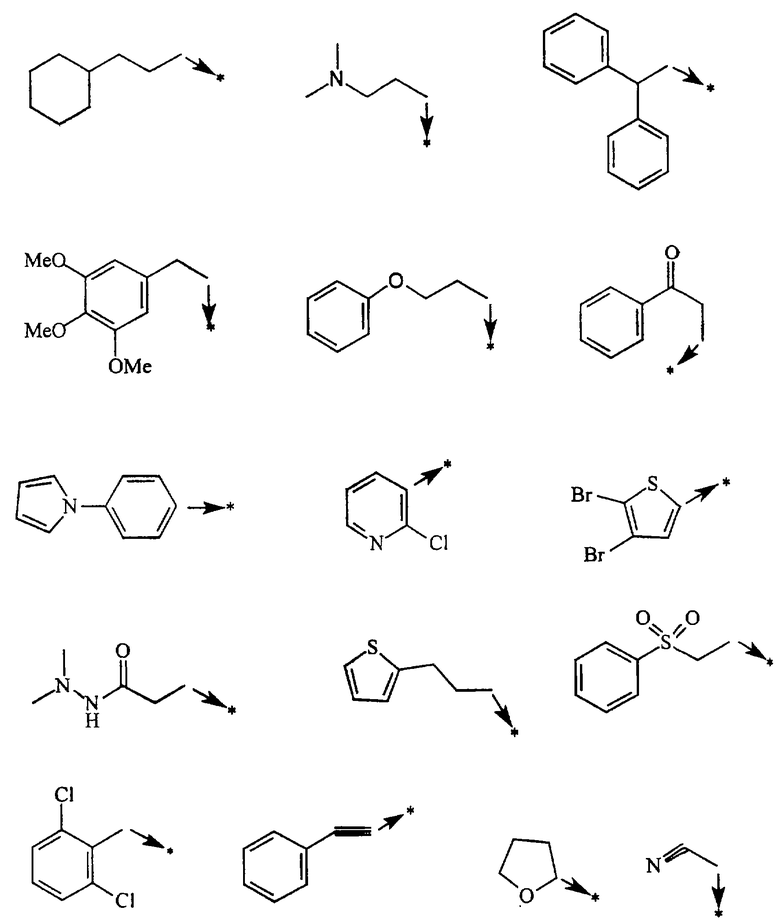

где защитная группа (PG) является Н или трет-бутилоксикарбонилом.
A3) Синтез 4-аминодизамещенных пиперидинов
4-Аминодизамещенные пиперидины по данному изобретению синтезируют, обрабатывая кислотой вышеописанные N-Boc-соединения в соответствии со следующей схемой реакций:

Общий способ: защитные группы из описанных выше мочевин, тиомочевин и амидов можно удалить в кислых средах двумя способами. В соответствии с первым способом соединение растворяют в дихлорметане и добавляют трифторуксусную кислоту (5-20 экв.), а в соответствии со вторым способом используют раствор разбавленной хлористоводородной кислоты в таких растворителях, как этилацетат, диоксан или диэтиловый эфир (5-20 экв.). Реакционную смесь перемешивают в течение 1-4 часов при комнатной температуре. В некоторых случаях добавляют дихлорметан и органическую фазу промывают насыщенным раствором бикарбоната натрия, сушат над сульфатом магния, фильтруют и концентрируют в вакууме, получая таким образом свободное основание.
Пример A3
N-(3,3-Дифенилпропил)-N-(4-пиперидинил)-N'-[3-(трифторметил) фенил] мочевина (С28Н30F3N3О, М=481,57)
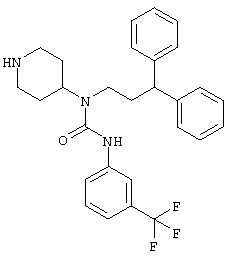
1,6 мл (21 ммоль, 20 экв.) трифторуксусной кислоты добавляют к раствору трет-бутил-4-((3,3-дифенилпропил){[3-(трифторметил)анилино]карбонил}амино)-1-пиперидинкарбоксилата (600 мг, 1,04 ммоль) в дихлорметане. Реакционную смесь перемешивают в течение 90 минут и концентрируют. Добавляют дихлорметан и органическую фазу промывают насыщенным раствором бикарбоната натрия, сушат над сульфатом магния, фильтруют и концентрируют в вакууме, получая при этом 490 мг (выход 98%) белой пены.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,7 (с, 1Н); 7,55 (д, 1Н); 7,44 (т, 1Н); 7,28 (м, 9Н); 7,18 (м, 2Н); 4,05 (м, 2Н); 3,26 (м, 2Н); 3,11 (д, J=10,8 Гц, 2Н); 2,7 (тд, J=2, 4 и 12,4 Гц, 2H); 2,38 (кв, J=8 Гц, 2H); 1,76 (д, J=10 Гц, 2H); 1,63 (квд, J=4 и 12,4 Гц, 2H). МС/ЖХ: m/z=482,2 (М+Н).
Указанным способом синтезируют ряд 4-аминопиперидинов. Возможные радикалы R1, X1 и Х2 проиллюстрированы выше в пунктах А1 и А2.
В) Синтез 4-аминопиперидинов в твердой фазе
4-Аминопиперидины синтезируют в твердой фазе, используя в качестве исходного вещества смолу Вонга.
B1) Получение смолы
B1a) Получение пара-нитрофенилкарбонатной смолы Вонга
Указанный синтез осуществляют в соответствии со следующей схемой реакций:
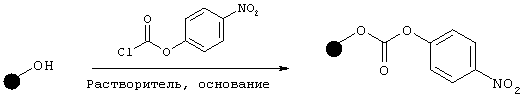
Указанную смолу получают из смолы Вонга (фирмы Bachem или Novabiochem) со степенью наполнения более 0,89 ммоль/г способом, описанным в литературе (Bunin, В.A. The Combinatorial Index, Academic Press, 1998, p. 62-63; Dressman, В.A.; Spangle, L.A.; Kaldor, S.W. Tetrahedron Lett. 1996, 37, 937-940; Hauske, J.R.; Dorff, P. Tetrahedron Lett., 1995, 36, 1589-1592; Cao, J.; Cuny, G.D.; Hauske, J.R. Molecular Diversity 1998, 3, 173-179): N-метилморфолин или пиридин и 4-нитрофенилхлорформиат последовательно добавляют к смоле Вонга, подвергнутой предварительному набуханию в дихлорметане или тетрагидрофуране при комнатной температуре. Смесь перемешивают в течение ночи. Смолу промывают тетрагидрофураном, диэтиловым эфиром и дихлорметаном и затем сушат в вакууме при 50°С в течение ночи.
B1b) Получение пиперидонкарбаматной смолы
Указанный синтез осуществляют в соответствии со следующей схемой:
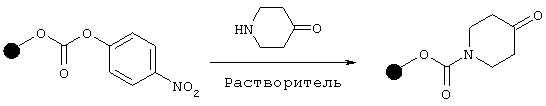
Триэтиламин (1 экв.) и молекулярное сито добавляют к гидратированному пиперидонгидрохлориду, разведенному в диметилформамиде. Смесь нагревают до полного растворения кетона. Полученный раствор добавляют к пара-нитрофенилкарбонатной смоле Вонга (0,05 экв.), которую подвергают предварительному набуханию в диметилформамиде. Смесь перемешивают в течение 24-72 часов при комнатной температуре, смолу фильтруют и затем несколько раз промывают диметилформамидом, тетрагидрофураном, диэтиловым эфиром и дихлорметаном.
Способ получения 2
2,5 г пара-нитрофенилкарбонатной смолы Вонга (степень наполнения 0,88 ммоль/г, 2,2 ммоль) подвергают предварительному набуханию в 100 мл диметилформамида. Одновременно с этим 6,7 г (44 ммоль, 20 экв.) гидратированного пиперидонгидрохлорида, 4,45 г (44 ммоль, 20 экв.) триэтиламина и три шпателя молекулярного сита нагревают в 100 мл диметилформамида до полного растворения. Теплый желтоватый раствор выливают в смолу и смесь перемешивают в течение 40 часов при комнатной температуре. Смолу фильтруют и промывают диметилформамидом, тетрагидрофураном, диэтиловым эфиром и дихлорметаном (трижды каждым растворителем) и затем сушат в вакууме. Получают 2,4 г бледно-желтой смолы со степенью наполнения 0,88 ммоль/г, вычисленной после выполнения элементного анализа азота.
В2) Восстановительное аминирование на твердом носителе
Восстановительное аминирование осуществляют в соответствии со следующей схемой:
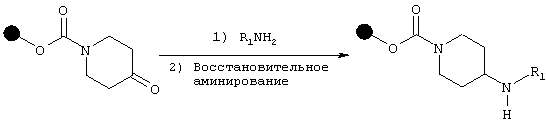
Общий способ состоит в следующем: первичный амин (5-10 экв.) добавляют к кетонной смоле, подвергнутой предварительному набуханию в триметилортоформиате (TMOF), после чего смесь обрабатывают ультразвуком. Затем добавляют комплекс борана с пиридином (8 М, 5-10 экв.) и смесь перемешивают в течение 12-72 часов. Смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и затем сушат в вакууме (Pelter, A.; Rosser, R.M. J. Chem. Soc. Perkin Trans I 1984, 717-720; Bomann, M.D.; Guch, I.C.; DiMare, M. J. Org. Chem. 1995, 60, 5995-5996; Khan, N.M.; Arumugam, V.; Balasubramanian, S. Tetrahedron Lett. 1996, 37, 4819-4822).
Способ получения 3

300 мг (степень наполнения 0,88 ммоль/г, 0,27 ммоль) кетонной смолы подвергают предварительному набуханию в TMOF. Затем добавляют 4-бромфенетиламин (540 мг, 420 мкл, 2,7 ммоль, 10 экв.) и комплекс борана с пиридином (8 М, 338 мкл, 2,7 ммоль, 10 экв.). Смесь перемешивают в течение 56 часов при комнатной температуре. Смолу фильтруют, последовательно промывают дихлорметаном, диметилформамидом, тетрагидрофураном и дихлорметаном и затем сушат в вакууме. Таким образом получают 340 мг бледно-желтой смолы со степенью наполнения 0,81 ммоль/г, вычисленной после выполнения элементного анализа азота.
В3) Введение функциональных групп
В3а) Введение функциональных групп при помощи изоцианатов или изотиоцианатов
Функциональные группы вводят в соответствии со следующей схемой:

Общий способ состоит в следующем: смолу на основе "вторичного амина" подвергают предварительному набуханию в растворителе, таком как дихлорметан или диметилформамид, и добавляют изоцианат или изотиоцианат (3-10 экв.). Смесь перемешивают в течение 1-24 часов при комнатной температуре. Затем смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и сушат в вакууме. Смолу отщепляют в присутствии эквимолярной смеси дихлорметана и трифторуксусной кислоты, перемешивая смесь в течение периода времени от 30 минут до 4 часов. Смолу промывают дихлорметаном и фильтрат концентрируют в вакууме. В некоторых случаях фильтрат снова растворяют в дихлорметане и обессоливают насыщенным раствором карбоната натрия. Органическую фазу упаривают в вакууме, получая таким образом свободное основание.
Пример В3а
N-(4-Бромфенэтил)-N-(4-пиперидинил)-N'-[4-(трифторметил)фенил]мочевина (С21H23BrF3N3О, М=470,3)
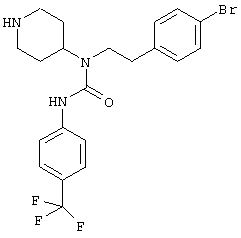
55 мг (50 мкмоль) смолы (см. способ получения 3) подвергают предварительному набуханию в безводном дихлорметане. Затем добавляют 4-трифторфенилизоцианат (28 мг, 150 мкмоль, 3 экв.) и полученную смесь перемешивают в течение ночи. Смолу фильтруют, промывают тетрагидрофураном, диметилформамидом, тетрагидрофураном и дихлорметаном и затем сушат в вакууме. Смесь перемешивают в течение 1,5 часов в присутствии 800 мкл эквимолярной смеси дихлорметана и трифторуксусной кислоты. Смолу фильтруют и промывают дихлорметаном, фильтрат концентрируют, снова разводят в дихлорметане и промывают насыщенным раствором бикарбоната натрия, получая таким образом 6 мг коричневого масла (выход 25%).
ЯМР 1H (CD3OD, 400 МГц) δ: 7,53 (м, 4Н); 7,44 (д, J=6,8 Гц, 2Н); 7,21 (д, J=8,4 Гц, 2Н); 4,1 (м, 1Н); 3,53 (т, J=7,2 Гц, 2Н); 3,12 (д, J=12,8 Гц, 2Н); 2,89 (т, J=8 Гц, 2Н); 2,7 (м, 2Н); 1,73 (м, 4Н). МС/ЖХ: m/z=472,2 (М+Н).
Указанным способом синтезируют ряд мочевин (Y=О) и тиомочевин (Y=S). Ниже приведены возможные радикалы R1:
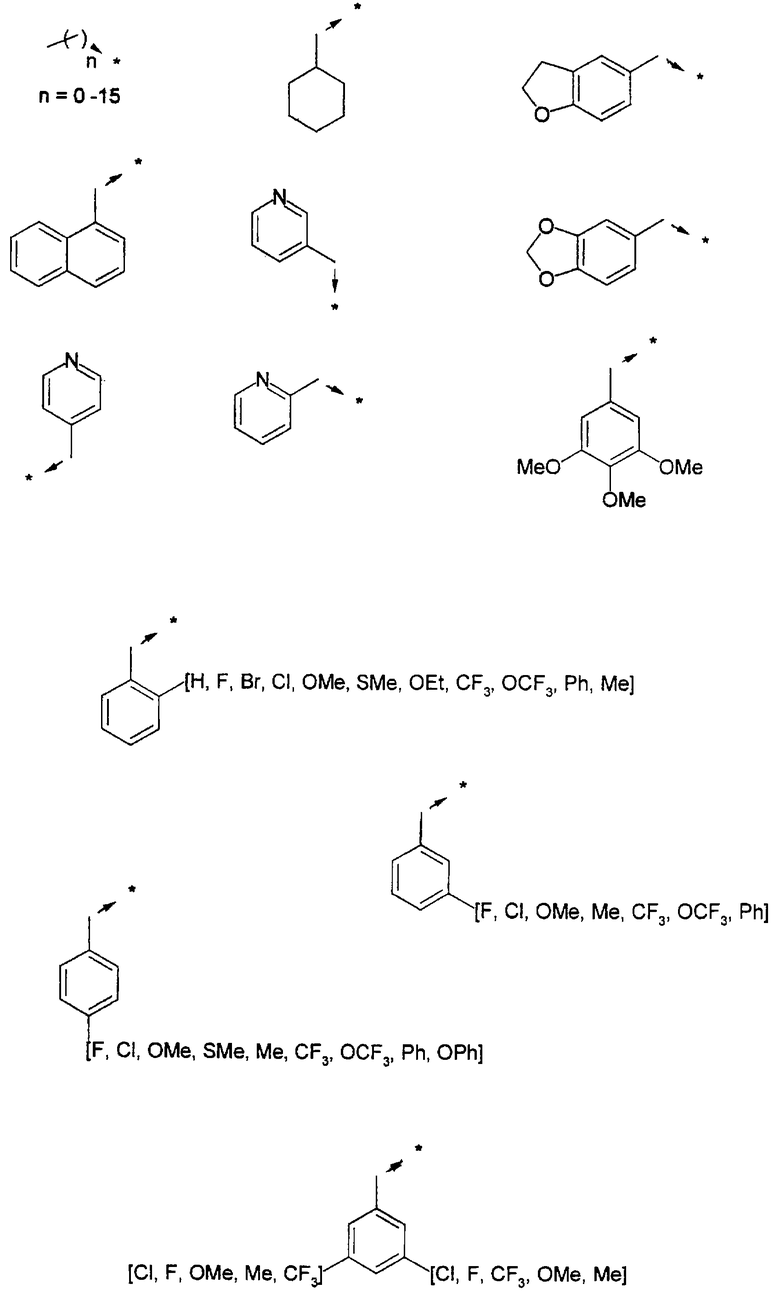
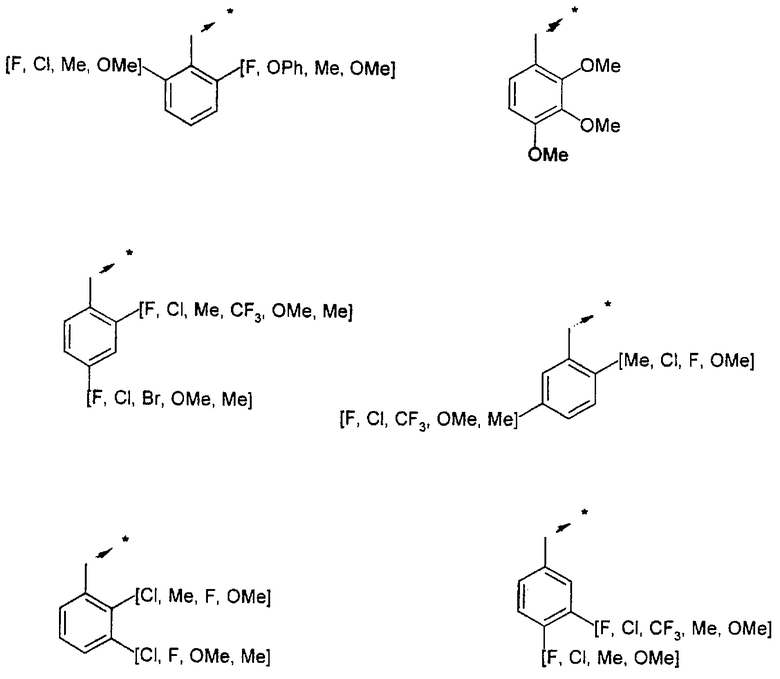
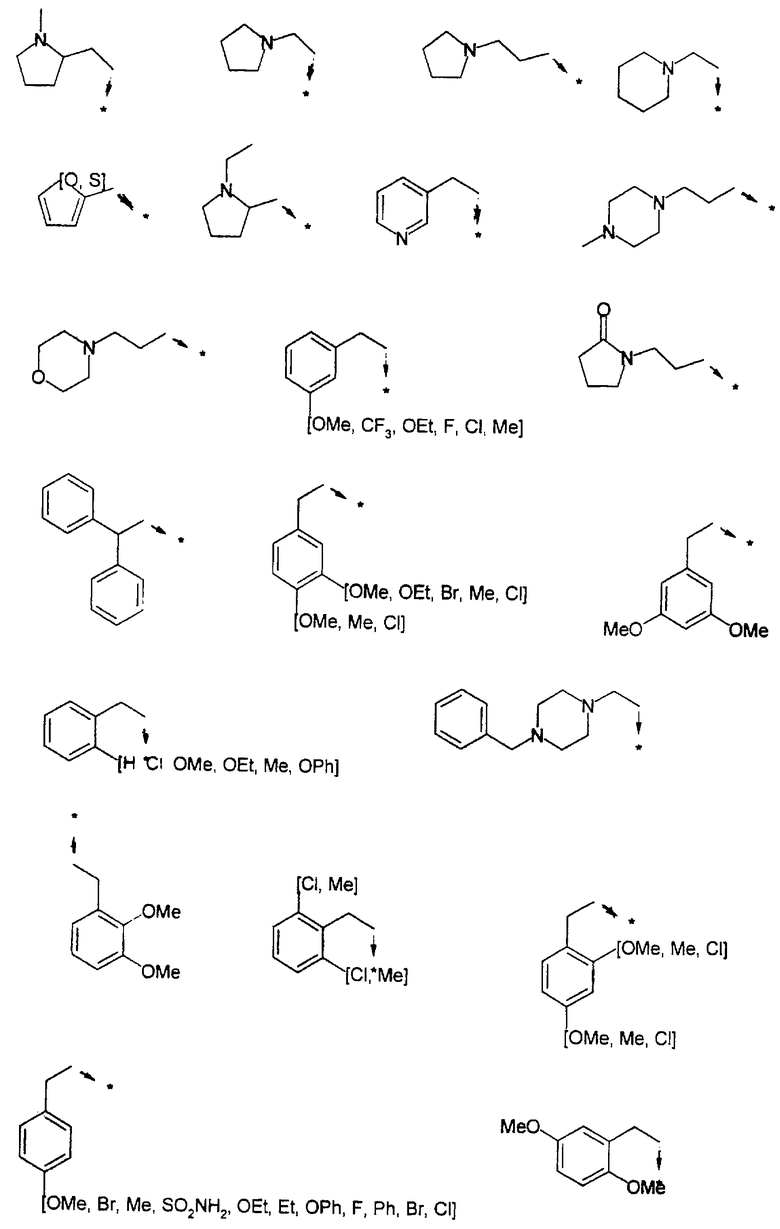
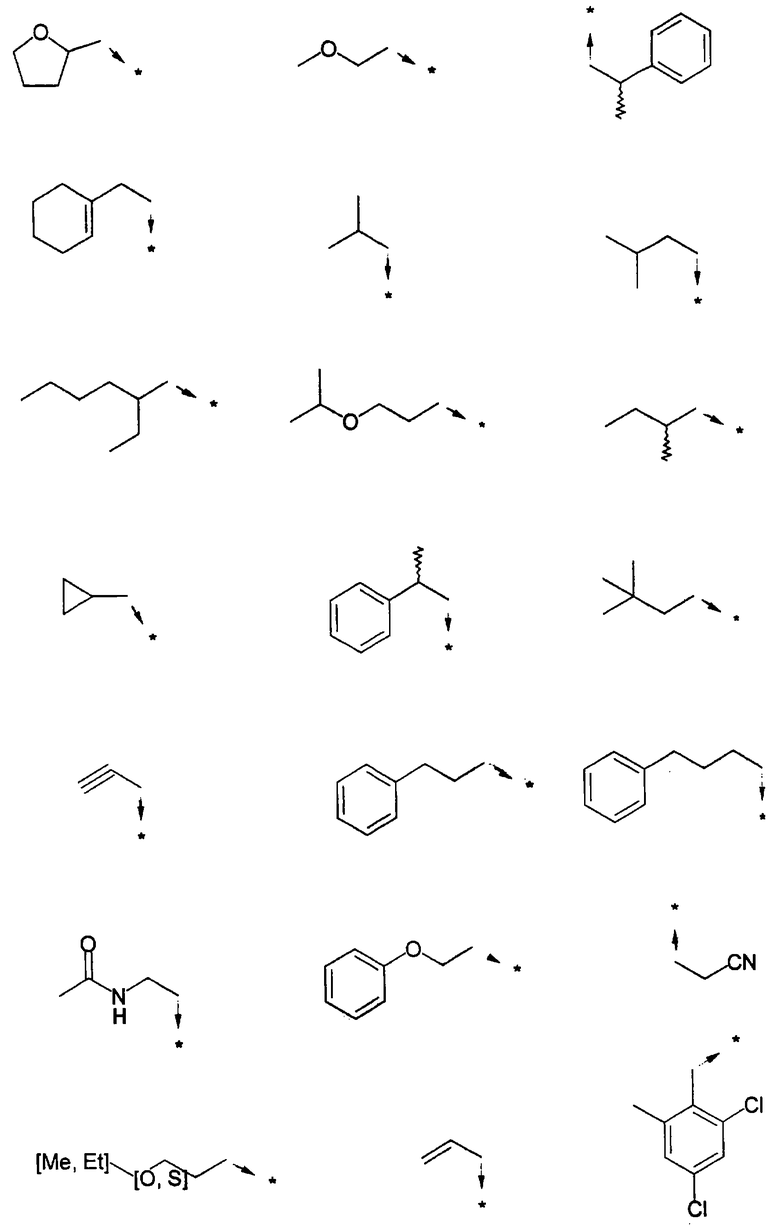
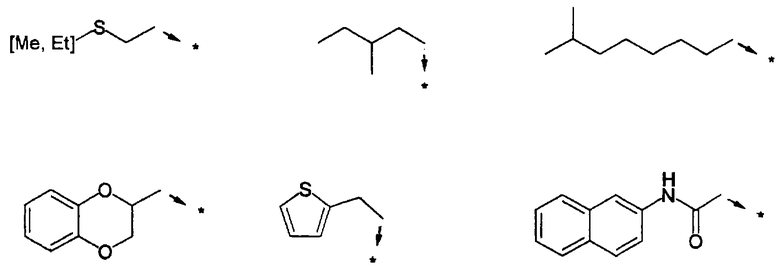
Возможные радикалы Х1 проиллюстрированы выше в пункте А.
В3b) Введение функциональных групп при помощи сульфонилхлоридов
Функциональные группы вводят в соответствии со следующей схемой:

Общий способ: смолу на основе "вторичного амина" подвергают предварительному набуханию в растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран. Затем добавляют сульфонилхлорид (5-10 экв.) и триэтиламин (6-12 экв.) и смесь перемешивают в течение 12-24 часов при комнатной температуре. Смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и сушат в вакууме. Затем смолу перемешивают в течение 1-4 часов в присутствии эквимолярной смеси дихлорметана и трифторуксусной кислоты. Смолу промывают дихлорметаном и фильтрат концентрируют в вакууме. В некоторых случаях фильтрат снова растворяют в дихлорметане и обессоливают насыщенным раствором карбоната натрия. Органическую фазу упаривают в вакууме, получая таким образом свободное основание.
Пример В3b
N-(4-Бромфенэтил)-4-метокси-N-(4-пиперидинил)фенилсульфонамид (C20H25BrN2O3S, M=453,4)
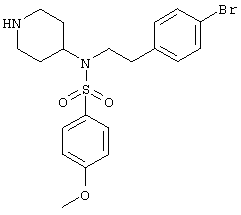
55 мг (50 мкмоль) смолы (см. способ получения 3) подвергают предварительному набуханию в безводном дихлорметане. Затем добавляют триэтиламин (42 мкл, 300 мкмоль, 6 экв.) и 4-метоксибензолсульфонилхлорид (51,5 мг, 250 мкмоль, 5 экв.) и полученную смесь перемешивают в течение ночи. Смолу фильтруют, промывают тетрагидрофураном, диметилформамидом, тетрагидрофураном и дихлорметаном и затем сушат в вакууме. Описанную реакцию выполняют еще раз до полного замещения. Добавляют 800 мкл эквимолярной смеси дихлорметана и трифторуксусной кислоты и перемешивают смесь в течение 1,5 часов при комнатной температуре. Смолу фильтруют и промывают дихлорметаном. Фильтрат концентрируют, снова разбавляют дихлорметаном и промывают насыщенным раствором бикарбоната натрия. Таким образом получают 14 мг коричневого масла (выход 63%).
ЯМР 1H (CD3CD, 400 МГц) δ: 7,8 (дд, J=2,8 и 10 Гц, 2Н); 7,44 (дд, J=1,2 и 6,8 Гц, 2Н); 7,17 (д, J=8,4 Гц, 2Н); 7,07 (дд, J=3,2 и 10 Гц, 2Н); 3,87 (с, 3Н, ОСН3); 3,72 (м, 1Н); 3,3 (м, 2Н); 3,04 (д, J=12,8 Гц, 2Н); 2,92 (т, J=8,4 Гц, 2H); 2,6 (т, J=12,4 Гц, 2H); 1,58 (м, 2H); 1,47 (ушир.д, J=10 Гц, 2H). МС/ЖХ: m/z=455 (М+Н).
Указанным способом синтезируют ряд сульфонамидов. Возможные радикалы R1 проиллюстрированы выше в пунктах А и В3а. Ниже приведены возможные радикалы Х3:
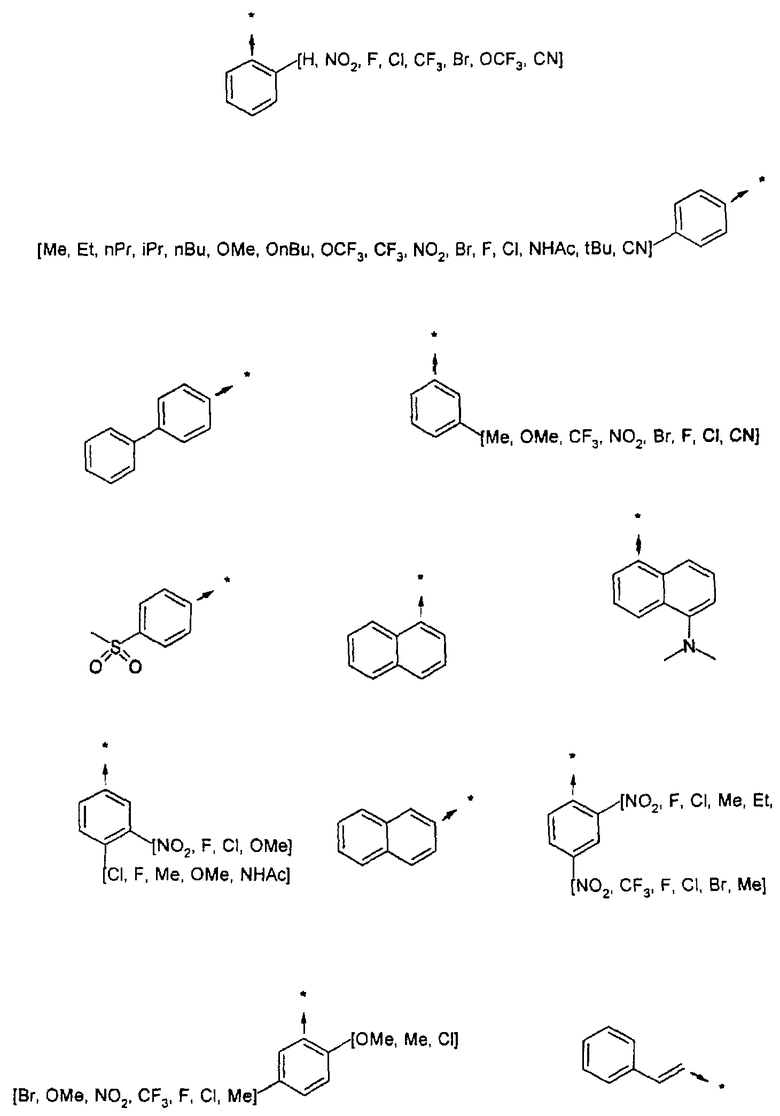

В3с) Введение функциональных групп при помощи хлорангидридов кислот
Функциональные группы вводят в соответствии со следующей схемой:

Общий способ: смолу на основе "вторичного амина" подвергают предварительному набуханию в растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран. Затем добавляют хлорангидрид кислоты (5-10 экв.) и триэтиламин (6-12 экв.) и смесь перемешивают в течение 12-24 часов при комнатной температуре. Смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и сушат в вакууме. Затем смолу перемешивают в течение 1-4 часов в присутствии эквимолярной смеси дихлорметана и трифторуксусной кислоты. Смолу промывают дихлорметаном и фильтрат концентрируют в вакууме. В некоторых случаях фильтрат снова растворяют в дихлорметане и обессоливают насыщенным раствором карбоната натрия. Органическую фазу упаривают в вакууме, получая таким образом свободное основание.
Пример В3с
N-(4-Бромфенетил)-N-(4-пиперидинил)-2-тиофенкарбоксамид (C18H21BrN2OS, M=393,3)
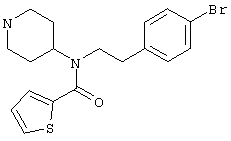
55 мг (50 мкмоль) смолы (см. способ получения 3) подвергают предварительному набуханию в безводном тетрагидрофуране. Затем добавляют триэтиламин (42 мкл, 300 мкмоль, 6 экв.) и 2-тиофенкарбонилхлорид (37 мг, 250 мкмоль, 5 экв.) и полученную смесь перемешивают в течение ночи. Смолу фильтруют, промывают тетрагидрофураном, диметилформамидом, тетрагидрофураном и дихлорметаном и сушат в вакууме. Добавляют 800 мкл эквимолярной смеси дихлорметана и трифторуксусной кислоты и перемешивают смесь в течение 1,5 часов при комнатной температуре. Смолу фильтруют и промывают дихлорметаном. Фильтрат концентрируют, снова разбавляют дихлорметаном и промывают насыщенным раствором бикарбоната натрия, получая при этом 10 мг коричневого масла (выход 50%).
ЯМР 1H (CD3OD, 400 МГц) δ: 7,64 (дд, J=0,8 и 4,8Гц, 1H); 7,44 (д, J=8,4 Гц, 2H); 7,36 (д, J=3,6 Гц, 1H); 7,14 (м, 3Н); 4,11 (м, 1H); 3,61 (т, J=8 Гц, 2H); 3,09 (д, J=12 Гц, 2H); 2,92 (м, 2H); 2,54 (м, 2H); 1,82 (м, 2H); 1,7 (м, 2H). МС/ЖХ: m/z=393,1 (М+Н).
Указанным способом получают ряд амидов. Возможные группы R1 проиллюстрированы выше в пунктах А и В3. Ниже приведены группы Х2.
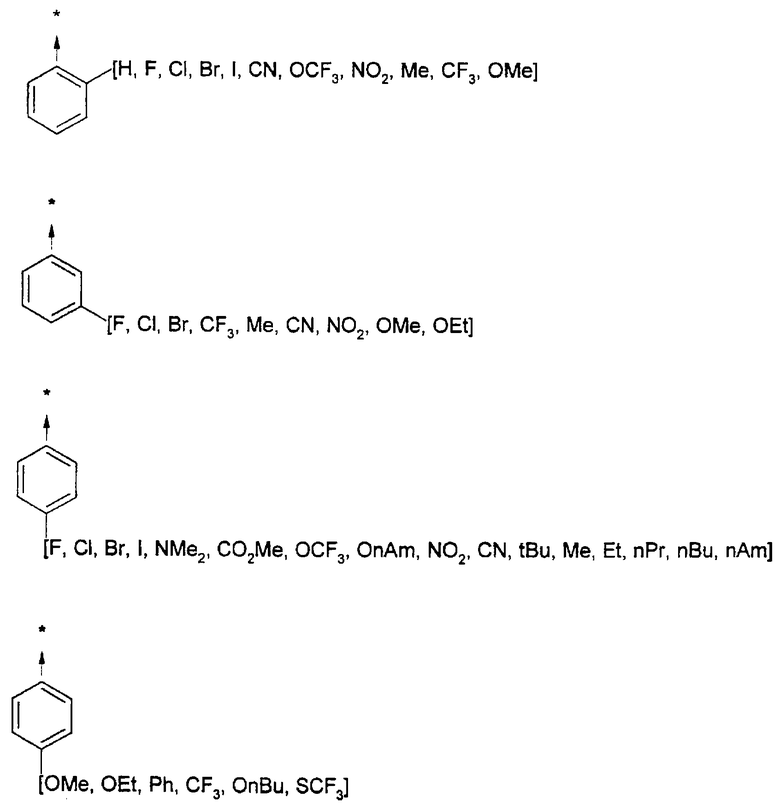
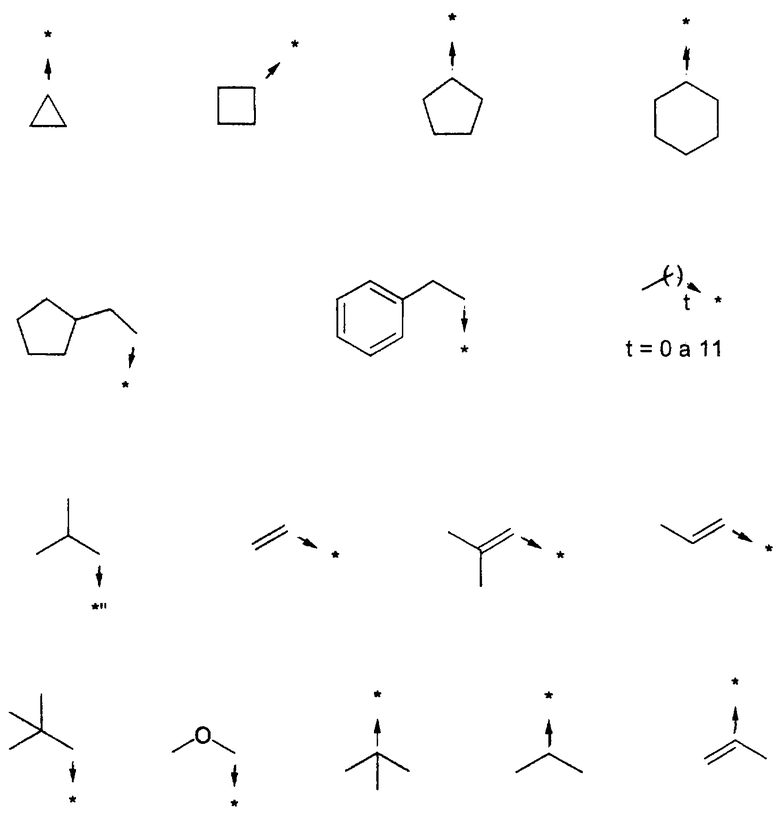
B3d) Введение функциональных групп при помощи карбоновых кислот
Функциональные группы вводят способом, описанным в литературе (Kobayashi, S.; Aoki, Y., J. Comb. Chem. 1999, 1, 371-372), в соответствии со следующей схемой:
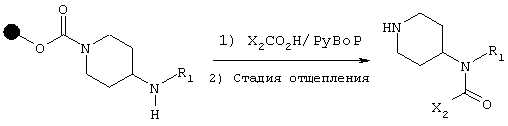
Общий способ: смолу на основе "вторичного амина" подвергают предварительному набуханию в растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран. Затем добавляют карбоновую кислоту (3-5 экв.), гексафторфосфат бензотриазол-1-илокситриспирролидинофосфония (РуВоР, 3-5 экв.) и диизопропилэтиламин (6-10 экв.) и смесь перемешивают в течение 24 часов при комнатной температуре. Смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и сушат в вакууме. Затем смолу перемешивают в течение 1-4 часов в присутствии эквимолярной смеси дихлорметана и трифторуксусной кислоты. Смолу промывают дихлорметаном и фильтрат концентрируют в вакууме. В некоторых случаях фильтрат снова растворяют в дихлорметане и обессоливают насыщенным раствором карбоната натрия. Органическую фазу упаривают в вакууме, получая таким образом свободное основание.
Пример B3d
N-[2-(4-Бромфенил)этил]-N-(4-пиперидинил)ацетамид (С15Н21BrN2О, М=325,25)
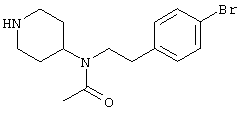
55 мг (50 мкмоль) смолы (см. способ получения 3) подвергают предварительному набуханию в безводном диметилформамиде. Затем добавляют уксусную кислоту (8,8 мг, 150 мкмоль, 3 экв.), РуВоР (76 мг, 150 мкмоль, 3 экв.) и диизопропилэтиламин (38 мг, 300 мкмоль, 6 экв.) и полученную смесь перемешивают в течение ночи. Смолу фильтруют, промывают диметилформамидом, тетрагидрофураном и дихлорметаном и сушат в вакууме. Добавляют 800 мкл эквимолярной смеси дихлорметана и трифторуксусной кислоты и перемешивают смесь в течение 1,5 часов при комнатной температуре. Смолу фильтруют и промывают дихлорметаном. Фильтрат концентрируют, снова разбавляют дихлорметаном и промывают насыщенным раствором бикарбоната натрия, получая таким образом 11 мг коричневого масла (выход 68%).
ЯМР 1H (CD3OD, 400 МГц) δ: 7,44 (м, 2Н); 7,20 (м, 2Н); 4,05 (м, 1Н); 3,45 (м, 2Н); 3,10 (м, 2Н); 2,83 (м, 2Н); 2,64 (м, 2Н); 2,13 (с, 3Н); 1,73 (м, 4Н). МС/ЖХ: m/z=325,2 (М+Н).
Указанным способом синтезируют ряд амидов. Возможные группы R1 проиллюстрированы выше в пунктах А и В3а. Группы Х3 представлены выше в пункте А.
С) Ввведение функциональных групп в пиперидиновую часть в растворе
С1) Получение пиперидина с R3 = C(Y)NHX1
Указанный синтез осуществляют в соответствии со следующей схемой:
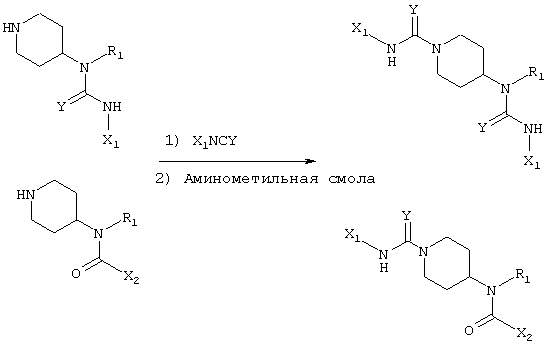
Общий способ: изоцианат или изотиоцианат (1,1-1,5 экв.) добавляют к пиперидину в виде свободного основания, разбавленному дихлорметаном. Смесь перемешивают в течение 1-18 часов при комнатной температуре. Добавляют аминометильную смолу (0,2-1 экв.) и смесь снова перемешивают в течение 2-18 часов. В некоторых случаях добавляют ионообменную смолу, такую как IRA68 или SAX. Смолы фильтруют и фильтрат концентрируют. В некоторых случаях продукт растворяют в дихлорметане или этилацетате и фильтруют через картридж с силикагелем или основным оксидом алюминия (550 мг, Interchim).
Пример С1
4-((3,3-Дифенилпропил){[3-(трифторметил)анилино]карбонил}амино)-N-фенил-1-пиперидинкарбоксамид (C35H35F3N4O2, M=600,68)

N-(3,3-Дифенилпропил)-N-(4-пиперидинил)-N'-[3-(трифторметил)фенил] мочевину (24 мг, 0,05 ммоль) растворяют в дихлорметане. Добавляют фенилизоцианат (9 мг, 0,075 ммоль, 1,5 экв.) и смесь перемешивают в течение 2,5 часов. Добавляют аминометильную смолу (0,02 ммоль) и реакционную смесь снова перемешивают в течение ночи. Смолу фильтруют, промывают дихлорметаном и фильтрат концентрируют. Полученное масло пропускают через картридж с силикагелем, элюируя эквимолярной смесью гептана и этилацетата, и концентрируют, получая при этом 12 мг (выход 40%) желтого масла.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,72 (с, 1Н); 7,58 (д, 1Н); 7,44 (м, 1Н); 7,38 (м, 2Н); 7,29 (м, 12Н); 7,12 (м, 2Н); 7,07 (м, 1Н); 4,2 (д, J=12,4 Гц, 3H); 3,21 (т, J=8 Гц, 2H); 2,9 (т, J=12,4 Гц, 2H); 2,38 (кв, J=8 Гц, 2H); 1,73 (д, J=10 Гц, 2H); 1,54 (квд, J=3,6 и 12 Гц, 2H). МС/ЖХ: m/z=601,4 (М+Н).
Указанным способом синтезируют ряд мочевин (Y=О) и тиомочевин (Y=S). Возможные группы R1, X1 и Х2 проиллюстрированы выше соответственно в пунктах (А и В3а), А и (А и В3с).
С2) Введение функциональных групп при помощи карбоновых кислот
Функциональные группы вводят в соответствии со следующей схемой:
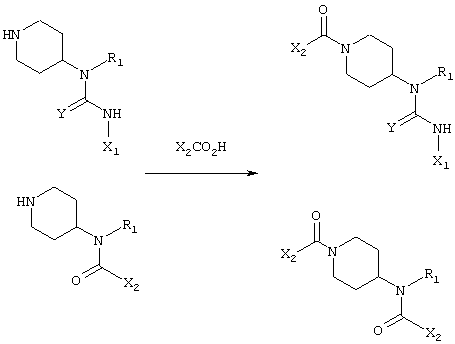
Общий способ: смолу P-EDC (1,3-3 экв.) подвергают предварительному набуханию в безводном дихлорметане. Карбоновую кислоту (1,1-2,5 экв.) растворяют в безводном растворителе, таком как дихлорметан, диметилформамид или тетрагидрофуран, и добавляют к смоле. Смесь перемешивают в течение 5-30 минут при комнатной температуре. Затем к смеси добавляют 4-аминодизамещенный пиперидин в виде свободного основания, растворенного в безводном растворителе, таком как дихлорметан, диметилформамид или тетрагидрофуран, и полученную смесь перемешивают в течение 1-18 часов при комнатной температуре. В некоторых случаях добавляют ионообменную смолу, такую как IRA68 или SAX, и смесь снова перемешивают при комнатной температуре в течение 1-18 часов. Смолы фильтруют через фритту, картридж с ионообменной смолой SAX (500 мг, Interchim) или картридж с основным оксидом алюминия (500 мг, Interchim).
Пример С2
N-(1-Ацетил-4-пиперидинил)-N-(3,3-дифенилпропил)-N'-[3-(трифторметил) фенил] мочевина (С30Н32F3Н3O2, М=523,60)
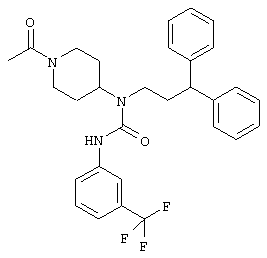
117 мг (175 мкмоль, 3,5 экв.) смолы P-EDC подвергают предварительному набуханию в 1,5 мл безводного дихлорметана. Добавляют уксусную кислоту (7,5 мг, 125 мкмоль, 2,5 экв.) и смесь перемешивают в течение 10 минут. Затем добавляют N-3,3-дифенилпропил)-N-(4-пиперидинил)-N'-[3-(трифторметил)фенил]мочевину (24,3 мг, 50 мкмоль) и смесь перемешивают в течение ночи. Смолу фильтруют и фильтрат концентрируют. Полученное масло пропускают через картридж с силикагелем, элюируя эквимолярной смесью гептана и этилацетата, и концентрируют, получая при этом 16 мг (выход 62%) белой пены.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,71 (с, 1Н); 7,58 (д, J=8,4 Гц, 1Н); 7,43 (т, J=8 Гц, 1Н); 7,28 (м, 9Н); 7,17 (м, 2Н); 4,56 (дд, J=2 и 11,2 Гц, 1Н); 4,17 (м, 1Н); 3,96 (т, J=7,6 Гц, 1H); 3,88 (д, J=12 Гц, 1H); 3,19 (кв, J=4 и 8 Гц, 2Н); 3,1 (т, J=12 Гц, 1H); 2,58 (т, J=12 Гц, 1H); 2,37 (м, 2Н); 2,06 (с, 3Н, CH3); 1,72 (т, J=14,4 Гц, 2Н); 1,43 (квд, J=4 и 12,4 Гц, 2Н). МС/ЖХ: m/z=524,3 (М+Н).
Указанным способом синтезируют ряд амидов. Возможные группы R1, X1 и Х2 проиллюстрированы соответственно в пунктах (А и В3а), А и (А и В3с).
С3) Введение функциональных групп при помощи сульфонилхлоридов
Функциональные группы вводят в соответствии со следующей схемой:
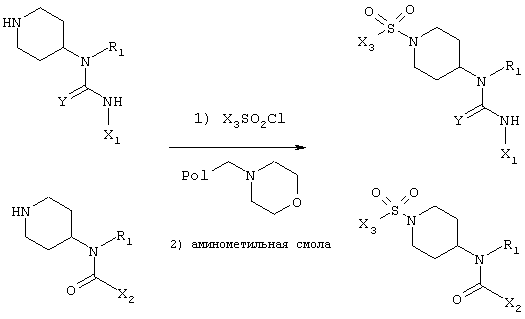
Общий способ: морфолинометильную смолу (Novabiochem, 2-3 экв.) подвергают предварительному набуханию в безводных растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран. Добавляют сульфонилхлорид (1,1-2 экв.), растворенный в безводных растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран, после чего добавляют 4-аминодизамещенный пиперидин. Смесь перемешивают в течение 16-48 часов. Добавляют аминометильную смолу (0,1-1,5 экв.) и реакционную смесь перемешивают в течение ночи. В некоторых случаях добавляют ионообменную смолу, такую как IRA68 или SAX, и смесь перемешивают при комнатной температуре в течение 1-18 часов. Смолы фильтруют через фритту, картридж с ионообменной смолой SAX (500 мг, Interchim) или картридж с основным оксидом алюминия (500 мг, Interchim).
Пример С3
N-(3,3-Дифенилпропил)-N-{1-[(4-метоксифенил)сульфонил]-4-пиперидинил}-N'-[3-(трифторметил)фенил]мочевина (С35Н36F3N3O4S, М=651,75)
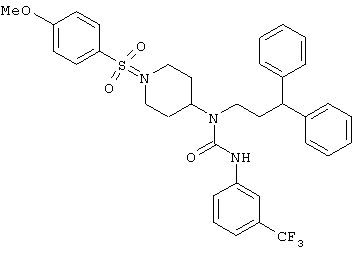
27,5 мг (100 мкмоль, 2 экв.) морфолинометильной смолы подвергают предварительному набуханию в безводном тетрагидрофуране, после чего добавляют 4-метоксифенилсульфонилхлорид (15,5 мг, 0,075 ммоль, 1,5 экв.) и N-(3,3-дифенилпропил)-N-(4-пиперидинил)-N'-[3-(трифторметил)фенил]мочевину (24,3 мг, 0,05 ммоль). Смесь перемешивают в течение ночи. Добавляют аминометильную смолу (20 мг) и ионообменную смолу SAX и смесь перемешивают в течение ночи. Смолы фильтруют и промывают дихлорметаном. Масло, полученное после упаривания смеси, пропускают через картридж с силикагелем (500 мг, Interchim), элюируя этилацетатом, и концентрируют, получая при этом 18 мг (выход 56%) белого твердого вещества.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,71 (д, J=9,2 Гц, 2H); 7,65 (с, 1Н); 7,51 (д, 1Н); 7,41 (т, J=7,6 Гц, 1Н); 7,29 (м, 9Н); 7,20 (м, 2H); 7,11 (дд, J=1,6 и 6,8 Гц, 2H); 3,88 (с, 3Н, ОСН3); 3,77 (д, J=12,4 Гц, 2H); 3,16 (т, J=8 Гц, 2H); 2,33 (м, 4Н); 1,71 (д, J=10 Гц, 2H); 1,62 (квд, J=4 и 12 Гц, 2H); 1,3 (м, 2H). МС/ЖХ: m/z=652,4 (М+Н).
Указанным способом синтезируют ряд сульфонамидов. Возможные группы R1, X1, Х2 и Х3 проиллюстрированы соответственно в пунктах (А и В3а), А, (А и В3с) и В3b.
D) Синтез тризамещенных пиперидинов в твердой фазе
Указанный синтез осуществляют, используя в качестве исходного вещества винилсульфоновую смолу (Kroll, F.E.K.; Morphy, R.; Rees, D.; Gani, D. Tetrahedron Lett. 1997, 38, 8573-8576; Brown, A.R. J. Comb. Chem. 1999, 1, 283-285), в соответствии со следующей схемой.
D1) Получение смолы
Смолу получают в соответствии со следующей схемой:
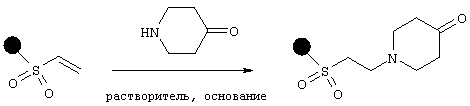
Триэтиламин (1 экв.) добавляют к гидратированному пиперидонгидрохлориду, разбавленному диметилформамидом. Смесь нагревают до полного растворения кетона. Полученный раствор добавляют к винилсульфоновой смоле (0,05 экв.), подвергнутой предварительному набуханию в диметилформамиде. Смолу перемешивают в течение 24-72 часов при комнатной температуре, фильтруют и несколько раз промывают диметилформамидом, тетрагидрофураном, диэтиловым эфиром и дихлорметаном.
Способ получения 4
1,5 г винилсульфоновой смолы (Novabiochem, степень наполнения 1 ммоль/г, 1,5 ммоль) подвергают предварительному набуханию в 50 мл диметилформамида. Одновременно с этим 2,3 г (15 ммоль, 10 экв.) гидратированного пиперидонгидрохлорида и 1,8 г (15 ммоль, 10 экв.) триэтиламина нагревают в 100 мл диметилформамида до полного растворения. Теплый желтоватый раствор выливают в смолу и смесь перемешивают в течение 24 часов при комнатной температуре. Смолу фильтруют, промывают диметилформамидом, тетрагидрофураном, диэтиловым эфиром и дихлорметаном (трижды каждым растворителем) и сушат в вакууме. Получают 1,7 г бледно-желтой смолы со степенью наполнения 1 ммоль/г, вычисленной после выполнения элементного анализа азота.
D2) Восстановительное аминирование на твердом носителе
Восстановительное аминирование на твердом носителе выполняют способом, описанным в литературе (Pelter, A.; Rosser, R.M.; J. Chem. Soc. Perkin Trans I 1984, 717-720; Bomann, M.D.; Guch, I.c.; DiMare, M.; J. Org. Chem. 1995, 60, 5995-5996; Khan, N.M.; Arumugan, V.; Balasubramanian, S.; Tetrahedron Lett. 1996, 37, 4819-4822), в соответствии со следующей схемой:
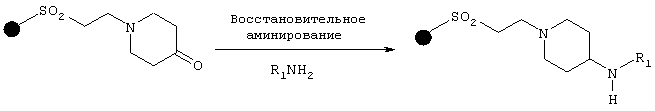
Общий способ: первичный амин (5-10 экв.) добавляют к кетонной смоле, подвергнутой предварительному набуханию в триметилортоформиате (TMOF), после чего смесь обрабатывают ультразвуком. Затем добавляют комплекс борана с пиридином (8 М, 5-10 экв.) и смесь перемешивают в течение 12-72 часов. Смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид, метанол и тетрагидрофуран, и сушат в вакууме.
Способ получения 5
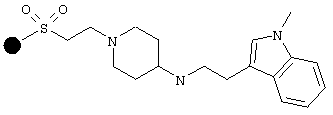
1 г (степень наполнения 1 ммоль/г, 1 ммоль) кетонной смолы подвергают предварительному набуханию в TMOF. Затем добавляют 2-(1-метил-1Н-индол-3-ил)этиламин (1,01 г, 10 ммоль, 10 экв.) и комплекс борана с пиридином (8 М, 1,25 мл, 10 ммоль, 10 экв.). Смесь перемешивают в течение 48 часов при комнатной температуре. Смолу фильтруют, последовательно промывают дихлорметаном, диметилформамидом, метанолом, тетрагидрофураном и дихлорметаном и сушат в вакууме. Таким образом получают 1,05 г бледно-желтой смолы со степенью наполнения 0,91 ммоль/г, вычиленной после выполнения элементного анализа азота.
D3) Введение функциональных групп во вторичный амин
D3a) Введение функциональных групп при помощи изоцианатов
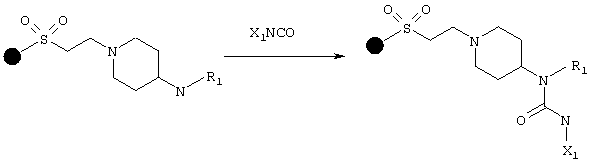
Общий способ: смолу на основе "вторичного амина" подвергают предварительному набуханию в растворителе, таком как дихлорметан или диметилформамид, и добавляют изоцианат (3-10 экв.). Смесь перемешивают в течение 1-24 часов при комнатной температуре. Затем смолу фильтруют, промывают растворителями, такими как дихлорметан, диметилформамид и тетрагидрофуран, и сушат в вакууме.
Способ получения 6
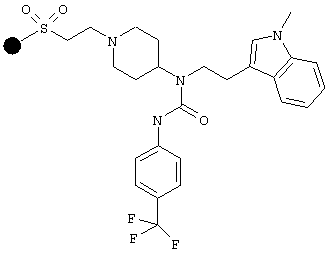
55 мг (50 мкмоль) смолы (см. способ получения 5) подвергают предварительному набуханию в безводном дихлорметане. Затем добавляют 4-трифторфенилизоцианат (28 мг, 150 мкмоль, 3 экв.) и полученную смесь перемешивают в течение 2 часов при комнатной температуре. Смолу фильтруют, промывают тетрагидрофураном, диметилформамидом, тетрагидрофураном и дихлорметаном и сушат в вакууме.
D3b) Введение функциональных групп при помощи сульфонилхлоридов
Данный способ введения функциональных групп аналогичен способу, описанному в пункте В3b.
D3c) Введение функциональных групп при помощи хлорангидридов кислот
Данный способ введения функциональных групп аналогичен способу, описанному в пункте В3с.
D3d) Введение функциональных групп при помощи карбоновых кислот
Данный способ введения функциональных групп аналогичен способу, описанному в пункте B3d.
D4) Стадия отщепления
Описанная ниже стадия отщепления подходит для всех вышеуказанных способов введения функциональных групп во вторичный амин:

Общий способ: дизамещенную смолу подвергают набуханию в растворителях, таких как дихлорметан, диметилформамид или тетрагидрофуран, затем добавляют галогенид R3Х, в котором R3 имеет указанные выше значения и Х означает атом галогена (5 экв.), и смесь перемешивают в течение ночи при температуре от 20 до 60°С. Смолу фильтруют, промывают растворителями, такими как диметилформамид, тетрагидрофуран, метанол и дихлорметан, и сушат в вакууме. Смолу снова подвергают набуханию в дихлорметане и добавляют основную ионообменную смолу (Ouyang, X.; Armstrong, R.W.; Murphy, M.M. J. Org. Chem. 1998, 63, 1027-1032). Полученную смесь перемешивают в течение 48 часов при комнатной температуре. Смолы фильтруют, промывают дихлорметаном и фильтрат концентрируют в вакууме.
Пример D4
N-[2-(1-Метил-1Н-индол-3-ил)этил]-N-(1-метил-4-пиперидинил)-N'-[4-(трифторметил)фенил]мочевина (С25Н29F3N4О, M=458,5)
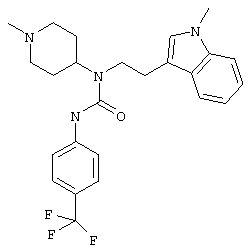
55 мг (50 мкмоль) карбамидной смолы подвергают набуханию в диметилформамиде, добавляют 35 мг (250 мкмоль, 5 экв.) иодметана и смесь перемешивают в течение 18 часов при комнатной температуре. Смолу фильтруют, промывают диметилформамидом, тетрагидрофураном, метанолом и дихлорметаном и сушат в вакууме. Смолу снова подвергают набуханию в дихлорметане, затем добавляют примерно 100 мг ионообменной смолы IRA68 и смесь перемешивают в течение 48 часов. Смолы фильтруют, промывают дихлорметаном и фильтрат концентрируют, получая при этом 18 мг (выход 78%) бесцветного масла.
ЯМР 1H (CD3OD, 400 МГц) δ: 7,65 (м, 2Н); 7,40 (м, 2Н); 7,31 (м, 1Н); 7,20 (т, 1Н); 7,10 (м, 1Н); 7,06 (м, 2Н); 4,04 (м, 1Н); 3,68 (с, 3Н); 3,60 (т, 2Н); 3,04 (т, 2Н); 2,44 (м, 2Н); 2,29 (с, 3Н); 2,14 (м, 2Н); 1,91 (м, 2Н); 1,76 (м, 2Н). МС/ЖХ: m/z=459,3 (М+Н).
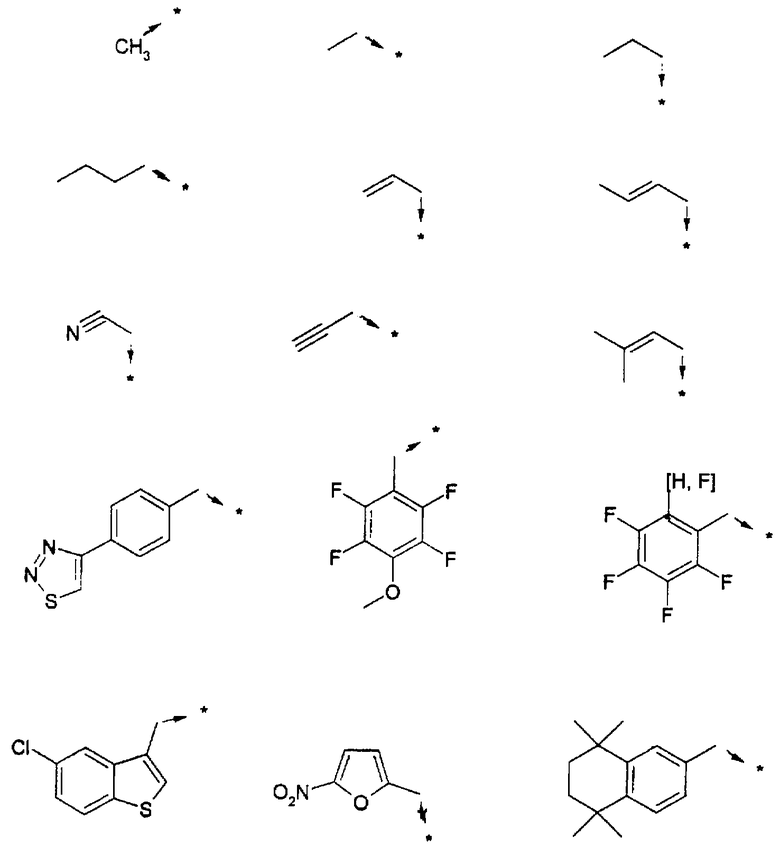
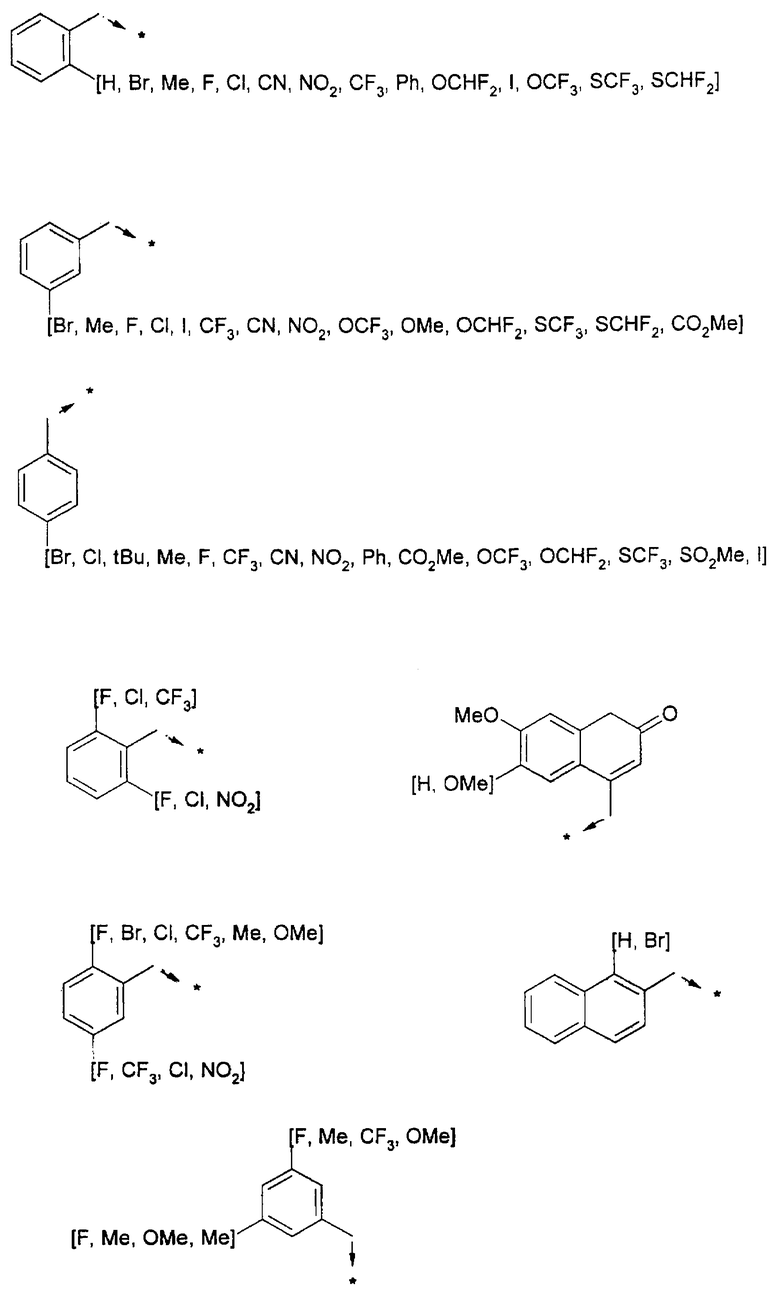
Ниже приведены группы R3, которые можно использовать для синтеза тризамещенных 4-аминопиперидинов вышеописанным способом, при наличии групп R1, Х1, Х2 и Х3, проиллюстрированных выше в пунктах А и В:

Объектом данного изобретения является также способ получения вышеописанных соединений формулы I по настоящему изобретению в твердой или жидкой фазе.
Отдельным объектом настоящего изобретения является способ получения в жидкой фазе описанных выше соединений формулы I, отличающийся тем, что он включает восстановительное аминирование нижеследующего N-замещенного пиперидона
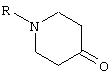
где R означает метильный или Boc радикал, в присутствии амина формулы R1NH3, в которой R1 имеет указанные выше значения, что дает соединение формулы 1
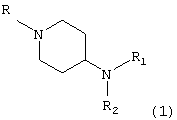
после чего соединение формулы (1) подвергают взаимодействию:
А) с соединением формулы X1NC(Y), где Х1 и Y имеют указанные выше значения, что дает соединение формулы (2)
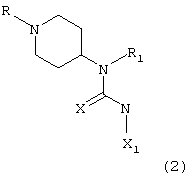
соединение формулы (2) представляет собой соответствующее соединение формулы (I), в которой R3 означает Me или Boc, и, когда R3 означает Boc, данное соединение может быть обработано кислотой, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
полученное таким образом соединение формулы (I) может быть подвергнуто взаимодействию с соединением формулы X1NC(Y), Х2CO2Н или Х3SO2Cl, в которой Х1, Y, Х2 и Х3 имеют указанные выше значения, в результате чего получают соответствующее соединение формулы I, в которой R2 означает радикал формулы -C(Y)NHX1 и R3 соответственно означает радикал -C(Y)NHX1, -С(O)Х2 или SO2Х3;
В) или с соединением формулы Х2СО2Н, в которой Х2 имеет указанные выше значения, что дает соединение формулы (3)
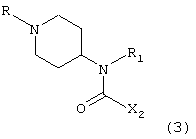
соединение формулы (3) представляет собой соответствующее соединение формулы (I), в которой R3 означает Me или Boc, и, когда R3 означает Boc, данное соединение может быть обработано кислотой, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода,
полученное таким образом соединение формулы (I) может быть подвергнуто взаимодействию с соединением формулы X1NC(Y), Х2СО2Н или Х3SO2Cl, в которой X1, Y, Х2 и Х3 имеют указанные выше значения, в результате чего получают соответствующее соединение формулы I, в котором R2 означает радикал формулы -С(O)Х2 и R3 соответственно означает радикал -C(Y)NHX1, -C(O)X2 или SO2Х3.
Отдельным объектом настоящего изобретения является также способ получения в твердой фазе описанных выше соединений формулы I, отличающийся тем, что он включает
восстановительное аминирование кетонной смолы
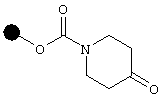
в присутствии амина формулы R1NH2, в которой R1 имеет указанные выше значения, что дает соединение формулы (4)
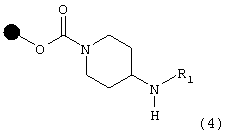
после чего соединение формулы (4) подвергают взаимодействию:
А) с соединением формулы X1NC(Y), в которой Х1 и Y имеют указанные выше значения, что дает соединение формулы (5)
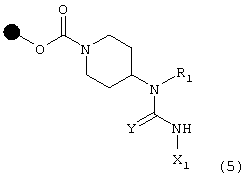
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
B) с соединением формулы Х3SO2Cl, в которой Х3 имеет указанные выше значения, что дает соединение формулы (6)
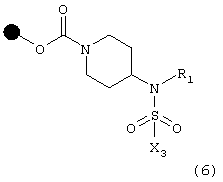
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
C) с соединением формулы Х2CO2Cl, в которой Х2 имеет указанные выше значения, что дает соединение формулы (7)
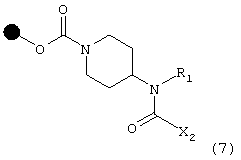
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
D) или с соединением формулы Х2CO2Н, в которой Х3 имеет указанные выше значения, что дает соединение формулы (7), с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода.
И наконец, отдельным объектом настоящего изобретения является способ получения в твердой фазе описанных выше соединений формулы I, отличающийся тем, что он включает:
восстановительное аминирование кетонной смолы
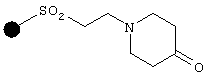
в присутствии амина формулы R1NH2, в которой R1 имеет указанные выше значения, что дает соединение формулы (8)
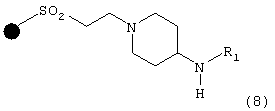
после чего соединение формулы (8) подвергают взаимодействию:
А) с соединением формулы X1NC (О), в которой Х1 имеет указанные выше значения, что дает соединение формулы (9)
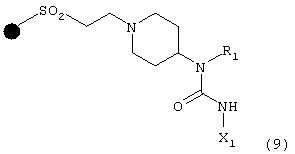
полученное таким образом соединение (9) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет указанные выше значения и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
B) с соединением формулы Х3SO2Cl, в которой Х3 имеет указанные выше значения, что дает соединение формулы (10)
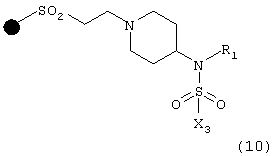
полученное таким образом соединение (10) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет указанные выше значения и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
C) с соединением формулы X2CO2Cl, в которой Х2 имеет указанные выше значения, что дает соединение формулы (11)

полученное таким образом соединение (11) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет указанные выше значения и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
D) или с соединением формулы Х2CO2Н, в которой Х2 имеет указанные выше значения, что дает соединение формулы (11);
полученное таким образом соединение (11) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет указанные выше значения и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I).
Соединения формулы I по настоящему изобретению обладают полезными фармакологическими свойствами. Установлено, что соединения формулы I по настоящему изобретению характеризуются высоким сродством к одному (или нескольким) рецепторам соматостатина. Указанные соединения можно использовать в качестве избирательных или неизбирательных непептидных агонистов или антагонистов соматостатина.
Поэтому соединения по настоящему изобретению можно использовать в разных лечебных целях. Их можно эффективно использовать для лечения вышеуказанных патологических состояний или заболеваний, обусловленных одним (или несколькими) рецепторами соматостатина.
Фармакологические свойства соединений по данному изобретению будут проиллюстрированы ниже в экспериментальной части.
Объектом изобретения по настоящей заявке являются также описанные выше продукты формулы I, аддитивные соли продуктов формулы I с фармацевтически приемлемыми минеральными или органическими кислотами и фармацевтические композиции, содержащие в качестве активного ингредиента по крайней мере одно вышеуказанное лекарственное средство в сочетании с фармацевтически приемлемым носителем.
Фармацевтическая композиция может быть получена в форме твердого вещества, например порошков, гранул, таблеток, желатиновых капсул или суппозиториев. Приемлемыми твердыми носителями являются, например, фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюпоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидин и воск.
Фармацевтические композиции, содержащие соединение по данному изобретению, могут быть также получены в жидкой форме, например, в виде растворов, эмульсий, суспензий или сиропов. Приемлемыми жидкими носителями являются, например вода, органические растворители, такие как глицерин или гликоли, а также их смеси в разных соотношениях в воде, с добавлением фармацевтически приемлемых масел или жиров. Стерильные жидкие композиции можно использовать для внутримышечных, внутрибрюшинных или подкожных инъекций, а также для внутривенного введения.
Некоторые описанные выше соединения общей формулы I представлены в заявке на патент DE 2751138. В указанной заявке на патент Германии описаны соединения, которые являются антагонистами допамина и эндогенных или экзогенных допаминэргических средств и стимулируют серотонинэргический механизм, причем указанная активность существенно отличается от активности соединений по настоящему изобретению.
Кроме того, объектом настоящего изобретения является применение соединений общей формулы Ia
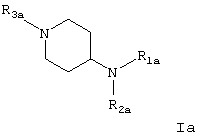
в рацемической, энантиомерной форме или во всех комбинациях указанных форм, где
R1a означает (C1-C16)алкил с линейной или разветвленной цепью, алкенил, алкинил, радикал -(CH2)m-Y-Z11 или -(CH2)mZ12, в котором
Z11 означает необязательно замещенный (C1-C6)алкил или арил;
Z12 означает циано, циклогексенил, бисфенил, (С3-С7)циклоалкил, необязательно замещенный (С3-С7)гетероциклоалкил, необязательно замещенный арил или необязательно замещенный гетероарил;
или Z12 означает радикал формулы

или R1a означает радикал формулы
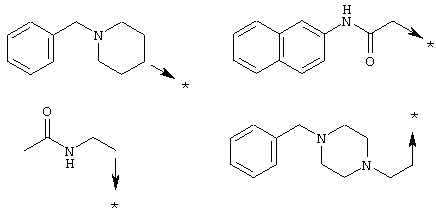
R2a означает радикал формулы -C(Y)NHX1, -C(O)X2 или SO2Х3;
R3а означает атом водорода, необязательно замещенный алкил, алкенил, алкинил, необязательно замещенный аралкил, необязательно замещенный гетероарилалкильный радикал или радикал формулы -C(Y)NHX1, -(CH2)n-C(O)X2 или SO2Х3 или
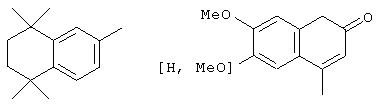
Х1 означает (C1-C15)алкил с линейной или разветвленной цепью, алкенил, алкинил, радикал -(СН2)m-Y-Z21 или -(CH2)pZ22, в котором
Z21 означает (C1-C6)алкил;
Z22 означает циклогексенил, инданил, бисфенил, (С3-С7) циклоалкил, (С3-С7)гетероциклоалкил, моно- или диалкиламино, -С(О)-O-алкил или необязательно замещенный арил или гетероарил;
или Z22 означает радикал формулы

Х2 означает (C1-С10)алкильный радикал с линейной или разветвленной цепью, алкенильный радикал, необязательно замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), алкинильный радикал или радикал формулы -(CH2)m-W-(СН3)q-Z23 или -(СН2)p-U-Z24, в котором
Z23 означает необязательно замещенный (C1-C6)алкил или арил;
Z24 означает алкил, циклогексенил, бисфенил, необязательно замещенный (С3-С7)циклоалкил, (С3-С7) гетероциклоалкил, циано, амино, моно- или диалкиламино, необязательно замещенный арил или гетероарил
или Z24 означает радикал формулы

или Х2 означает нижеследующий радикал:
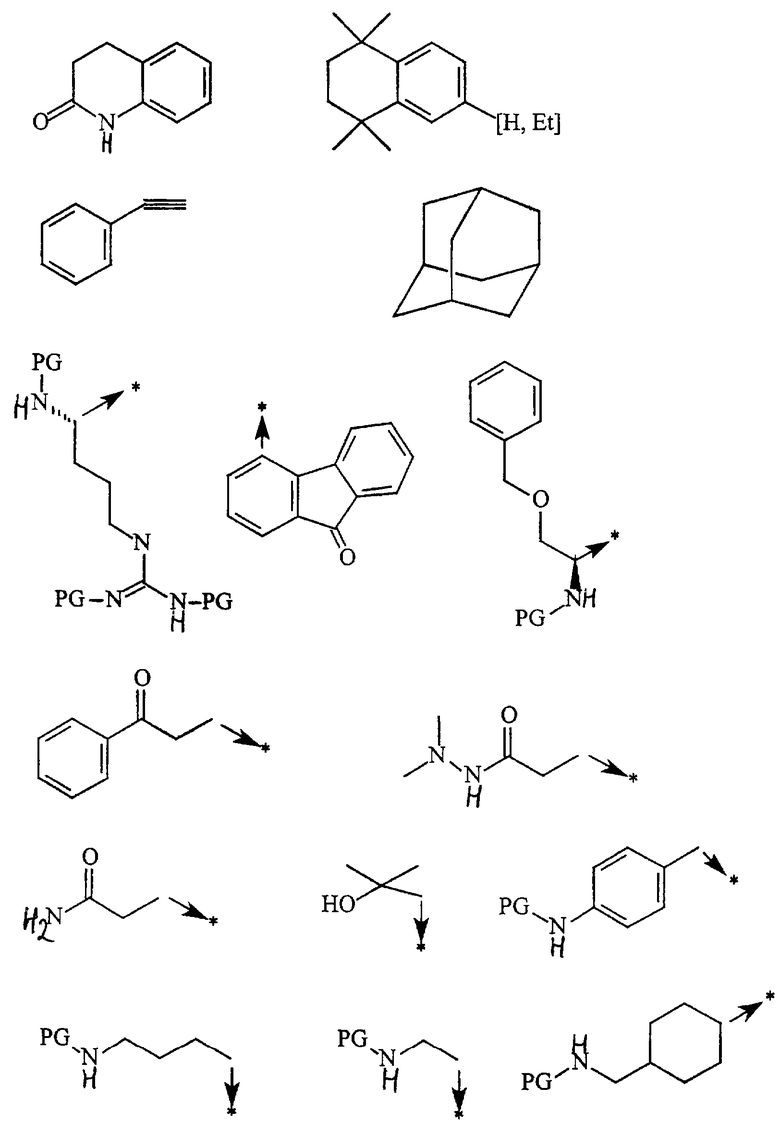
где защитная группа (PG) является Н или трет-бутилоксикарбонилом;
Х3 означает (C1-С10)алкильный радикал с линейной или разветвленной цепью, алкенильный радикал, необязательно замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), CF3 или -(СН2)pZ25, где
Z25 означает необязательно замещенный арил или гетероарил;
или Х3 означает радикал формулы

необязательно замещенный одним или несколькими одинаковыми или разными галогенсодержащими радикалами;
Y означает атом кислорода или серы;
W означает атом кислорода или серы или SO2;
U означает ковалентную связь или атом кислорода;
n является целым числом от 0 до 4;
m является целым числом от 1 до 6;
р является целым числом от 0 до 6;
q является целым числом от 0 до 2,
или их аддитивных солей с фармацевтически приемлемыми минеральными или органическими кислотами для изготовления лекарственных средств, предназначенных для лечения патологических состояний или заболеваний, обусловленных одним (или несколькими) рецепторами соматостатина.
Отдельным объектом данного изобретения является применение описанных выше продуктов общей формулы Ia, отличающихся тем, что
i) заместитель или заместители, замещающие арильные радикалы, представленные Z11 и Z12, и гетероарил, представленный Z12, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, -CF3, -OCF3, фенил, фенокси, аминосульфонил;
ii) заместитель или заместители, замещающие гетероциклоалкильный радикал, представленный Z12, независимо выбирают из окси- и алкильных радикалов;
iii) заместитель или заместители, замещающие арильные и гетероарильные радикалы, представленные Z22, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкенил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, аминосульфонил, пиперидиносульфонил, моно- или диалкиламино, -С(О)-O-алкил, -С(О)-алкил или фенил, фенокси, фенилтио, бензилокси, причем фенильный радикал может быть замещен;
iv) заместитель или заместители, замещающие арильные радикалы, представленные Z23 и Z24, циклоалкил или гетероарил, представленный Z24, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, OCHF2, SCF3, нитро, циано, азидо, гидрокси, -С(О)O-алкил, -O-С(О)-алкил, -NH-C(О)-алкил, алкилсульфонил, моно- или диалкиламино, амино, аминоалкил, пирролил, пирролидинил или фенил, фенокси, фенилтио, бензил, бензилокси, причем арильный радикал может быть необязательно замещен одним или несколькими алкильными, CF3 или галогенрадикалами;
v) заместитель или заместители, замещающие арильные и гетероарильные радикалы, представленные Z25, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, OCF3, нитро, циано, -NH-C(О)-алкил, алкилсульфонил, амино, моно- и диалкиламино, фенил, пиридино;
vi) заместитель, замещающий алкильный радикал, представленный R3, является цианорадикалом;
vii) заместитель или заместители, замещающие аралкильный радикал, представленный R3, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, OCF3, OCHF2, SCF3, SCHF2, нитро, циано, -С(О)O-алкил, алкилсульфонил, тиадиазолил или фенил и фенокси, причем фенильный радикал может быть необязательно замещен одним или несколькими галогенрадикалами;
viii) заместитель или заместители, замещающие гетероарилалкильный радикал, представленный R3, независимо выбирают из радикалов, включающих фтор, хлор, бром или нитро.
Отдельным объектом настоящего изобретения является применение соединений вышеуказанной общей формулы Ia, в которой R1a означает (C1-C6)алкильный радикал с линейной или разветвленной цепью, радикал -(CH2)m-Y-Z11 или -(CH2)mZ12, в котором
Z11 означает (C1-C6)алкил;
Z12 означает бисфенил, (С3-С7)циклоалкил, необязательно замещенный (С3-С7)гетероциклоалкил, арил или гетероарил, необязательно замещенный одним или несколькими заместителями, выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси,
или Z12 означает

Y означает атом кислорода;
или R1a означает радикал формулы
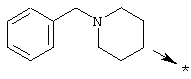
Отдельным объектом настоящего изобретения является применение описанных выше соединений общей формулы Ia, в которой R2a означает радикал формулы -C(Y)NHX1, -С(O)Х2 или SO2Х3, где
Х1 означает (C1-C15)алкильный радикал с линейной или разветвленной цепью или радикал -(CH2)pZ22, в котором
Z22 означает циклогексенил, бисфенил, (С3-С7)циклоалкил, (С3-С7)гетероциклоалкил, моно- или диалкиламино, -С(О)-O-алкил, арил или гетероарил, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(O)-O-алкил, -С(О)-алкил или фенил,
или Z22 означает радикал формулы

Х2 означает (C1-С10)алкил с линейной или разветвленной цепью, алкинил, радикал -(CH2)m-W-(СН2)q-Z23 или -(СН2)p-U-Z24, в котором
W означает SO2;
U означает ковалентную связь;
Z23 означает арильный радикал;
Z24 означает циклогексенил, бисфенил, (С3-С7)циклоалкил, необязательно замещенный аминоалкилом, арильный или гетероарильный радикал, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, SCF3, гидрокси, -С(О)-O-алкил, моно- или диалкиламино, амино,
или Z24 означает радикал формулы

или Х2 означает
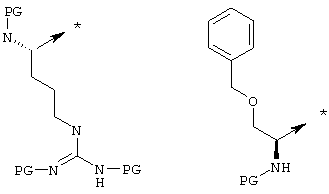
Х3 означает радикал -(СН2)рZ25, где Z25 означает арильный радикал, необязательно замещенный одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3.
Отдельным объектом настоящего изобретения является применение описанных выше соединений общей формулы Ia, в которой R3а означает атом водорода, необязательно замещенный алкильный, алкенильный, гетероарилалкильный радикал или радикал формулы -C(Y)-NHX1, -C(O)X2 или SO2Х3, где
Х1 означает радикал -(СН2)рZ22, в котором
Z22 означает арильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенилом, причем фенильный радикал в свою очередь необязательно замещен одним или несколькими галогенами, или радикал -(СН2)p-U-Z24, где
Z24 означает алкил, (С3-С7)циклоалкил, (С3-С7)гетероциклоалкил, бисфенил, амино, моно- или диалкиламино, арил или гетероарил, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, гидрокси, CF3, нитро, амино, моно- и диалкиламино, пирролил;
или Х2 означает радикал формулы
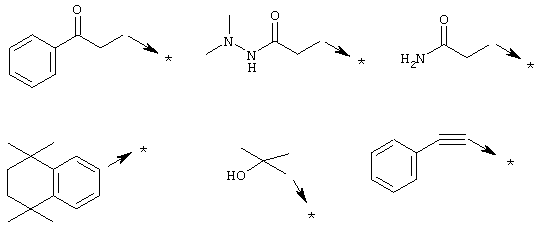
Х3 означает (C1-С10)алкильный радикал с линейной или разветвленной цепью, винильный радикал, замещенный фенильным радикалом (фенильный радикал может быть также необязательно замещен), CF3 или -(CH2)pZ25, где
Z25 означает арил или гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-C(О)-алкил, моно- и диалкиламино.
R1a предпочтительно означает (C1-C6)алкильный радикал с линейной или разветвленной цепью, радикал -(CH2)m-Y-Z11 или -(CH2)m-Z12, в котором
Z11 означает (C1-C6)алкил,
Z12 означает нафтил, морфолино, бисфенил, пирролидинил, замещенный оксирадикалом, или фенильный, пиперазинильный, пиридинильный и индолильный радикалы, которые необязательно замещены одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих бром, фтор, хлор, алкил, алкокси, -CF3, -OCF3,
или Z12 означает

Y означает атом кислорода;
или R1a означает радикал нижеследующей формулы:

R2а предпочтительно означает радикал формулы -C(Y)NHX1, -С(O)Х2 или SO2Х3, где
X1 означает (С1-С10)алкил с линейной или разветвленной цепью или радикал -(CH2)pZ22, в котором
Z22 означает циклогексил, циклогексенил, бисфенил, морфолино, пиперидино, моно- или диалкиламино, -С(О)-O-алкил, либо фенил, нафтил или фурил, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(О)-O-алкил, -С(О)-алкил или фенил,
или Z22 означает радикал формулы

Х2 означает алкил, алкинил, радикал -(CH2)m-W-(СН2)q-Z23 или -(CH2)pZ24, в котором
W означает SO2;
Z23 означает фенильный радикал;
Z24 означает циклогексенил, бисфенил, циклогексил, необязательно замещенный аминоалкилом, либо фенильный, нафтильный, бензотиенильный, тиенильный или индолильный радикал, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, SCF3, гидрокси, -O-С(О)-алкил, -NH-C(О)-алкил, моно- или диалкиламино, амино,
или Z24 означает радикал формулы
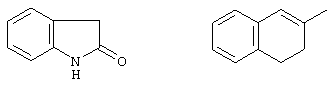
или Х2 означает
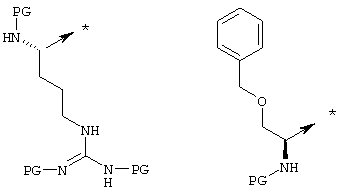
Х3 означает радикал -(СН2)рZ25, в котором Z25 является фенильным радикалом, необязательно замещенным одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3.
R3а предпочтительно означает атом водорода, алкильный, алкенильный или фурилметильный радикал, замещенный одним или несколькими нитрорадикалами, или радикал формулы -C(Y)-NHX1, -С(O)Х2 или SO2Х2, где
Х1 означает радикал -(CH2)pZ22, в котором
Z22 означает фенильный или нафтильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенильным радикалом, который в свою очередь замещен одним или несколькими галогенами, или радикал -(СН2)p-U-Z24, где
Z24 означает алкил, циклогексил, тетрагидрофурил, бисфенил, амино, моно- или диалкиламино, либо фенил, индолил, тиенил, пиридинил, бензотиенил и фурил, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, амино, моно- и диалкиламино, нитро, гидрокси, пирролил;
или Х2 означает радикал формулы
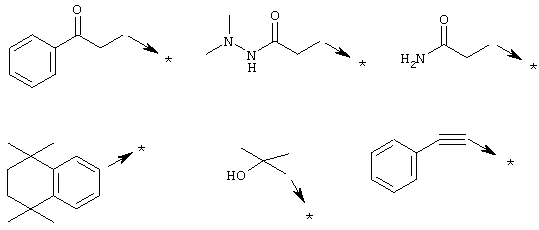
Х3 означает (C1-С10)алкильный радикал с линейной или разветвленной цепью, винильный радикал, замещенный фенилом, CF3 или радикал -(CH2)pZ25, в котором
Z25 означает фенильный, нафтильный, тиенильный, пиразолильный или тиазолильный радикал, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-C(О)-алкил, моно- и диалкиламино;
В наиболее предпочтительном случае R1a означает радикал -(CH2)mZ12, в котором m=2 и Z12 означает бисфенил или индолильный радикал, замещенный одним или несколькими заместителями, независимо выбираемыми из алкильных и алкоксильных радикалов.
В наиболее предпочтительном случае R2a означает радикалы формулы -C(Y)NHX1 и -С(O)Х2, в которой
Y означает S;
Х1 означает фенильный радикал, необязательно замещенный одним или несколькими азидорадикалами;
X2 означает -(CH2)pZ24, где
р равно 1, 2 или 3;
Z24 означает циклогексил, фенил или бензотиенил, необязательно замещенный одним или несколькими радикалами, выбираемыми из фтора, хлора, брома, иода или -CF3.
В наиболее предпочтительном случае R3а означает атом водорода или метильный радикал.
Все технические и научные термины, используемые в описании настоящего изобретения, имеют значения, известные специалистам в данной области. Кроме того, все патенты (или заявки на патент) и другие библиографические данные включены в данное описание изобретения в качестве ссылок.
Экспериментальная часть
Другие соединения по настоящему изобретению, полученные описанными выше способами по примерам А, В, С и D, приведены в нижеследующей таблице.
Соединения охарактеризованы временем удерживания (rt), выраженным в минутах, и молекулярным пиком (М+Н+), определенным масс-спектроскопией (МС).
Масс-спектроскопию выполняют при помощи однолучевого масс-спектрометра ядерного квадрупольного резонанса (модель на платформе Micromass), оснащенного электрораспылительным источником, с разрешением 0,8 Да при 50% понижении. Ниже приведены условия выполнения хроматографии для примеров 1-778.
Условия хроматографии С1 и С2
Элюент - А: вода + 0,02% трифторуксусной кислоты; В: ацетонитрил.
33×4,6 мм (внутренний диаметр)
50×4,6 мм (внутренний диаметр)
Условия хроматографии С3
Элюент - А: вода + 0,02% трифторуксусной кислоты; В: ацетонитрил
Объемный расход 1 мл/мин
Объем пробы 5 мкл
Колонка: Uptisphere ODS 3 мкм, 50×4,6 мм внутренний диаметр
Температура 40°С
Длина волны (% УФ) 220 нм
Ниже приведены условия выполнения хроматографии с указанием примеров:
Приведенные примеры служат только для иллюстрации описанных выше способов и не ограничивают объема настоящего изобретения.
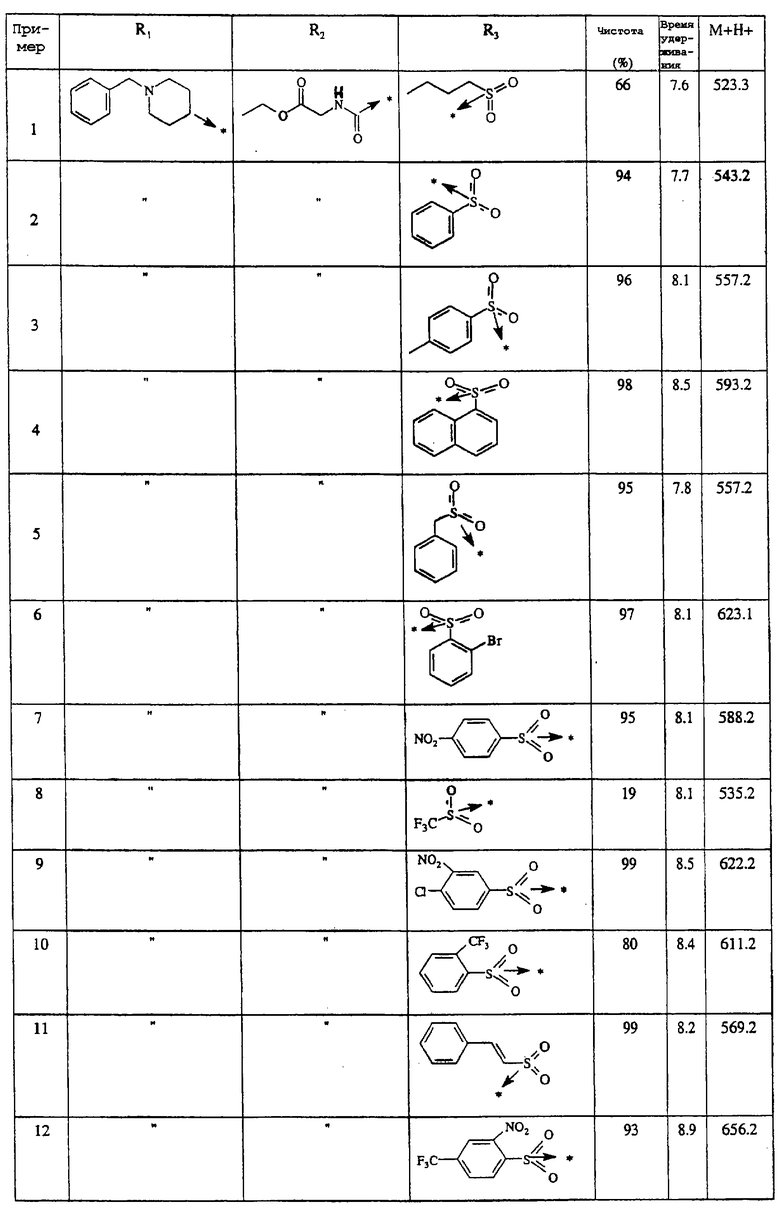
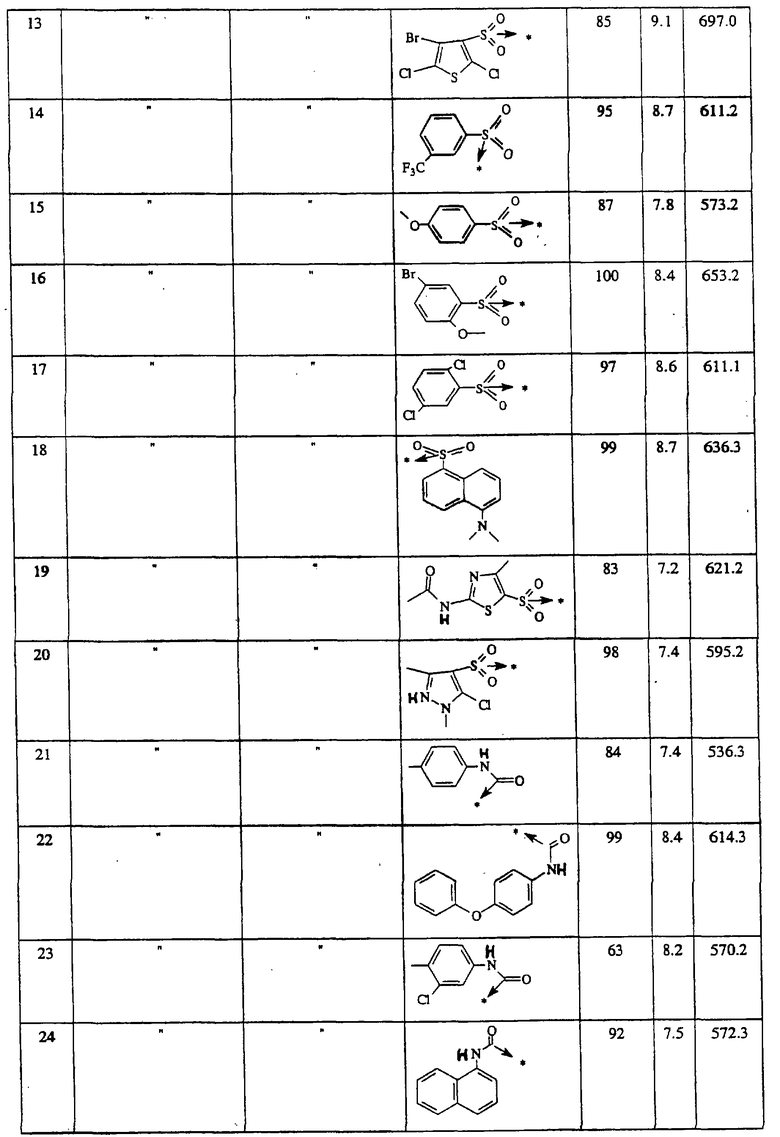
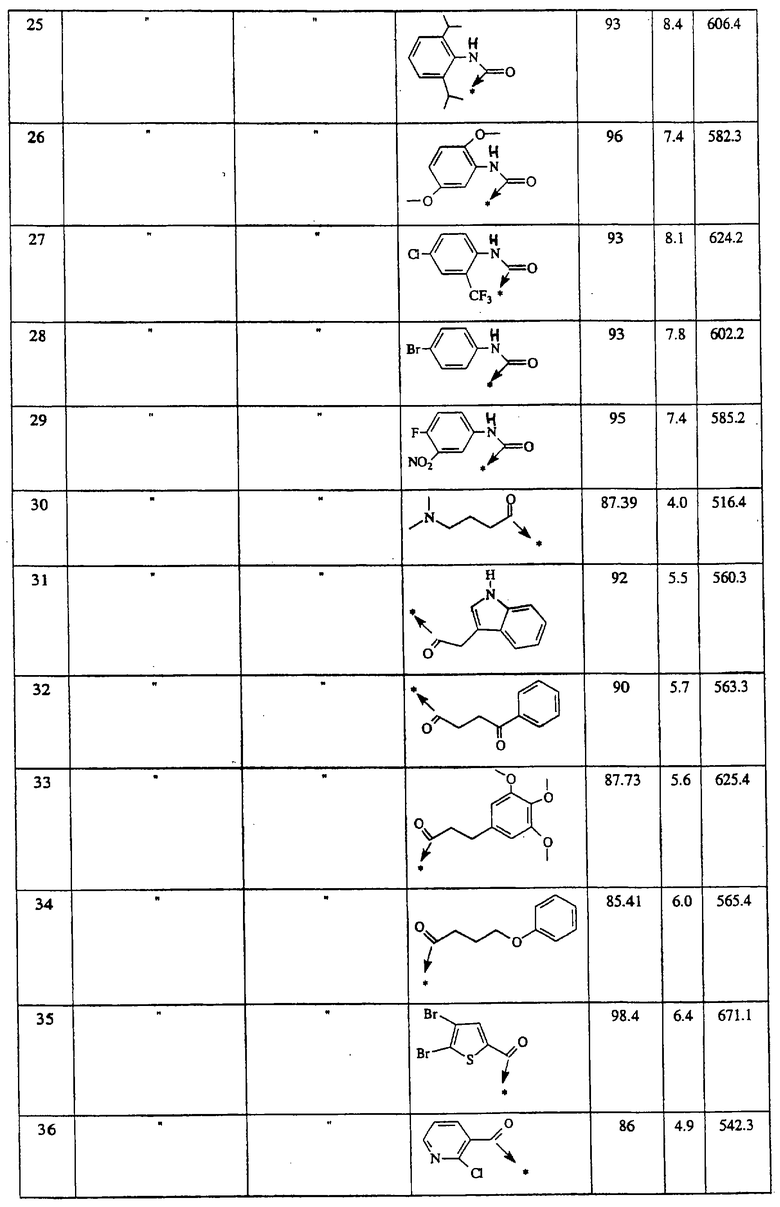
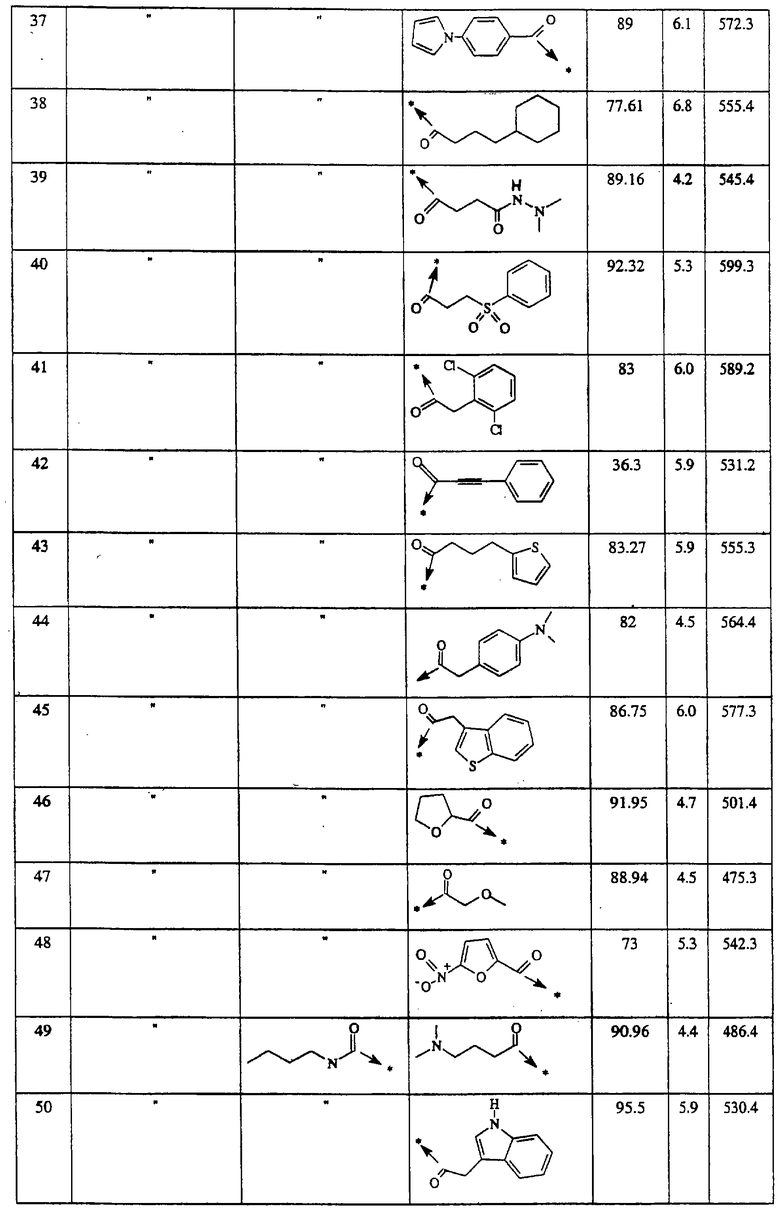
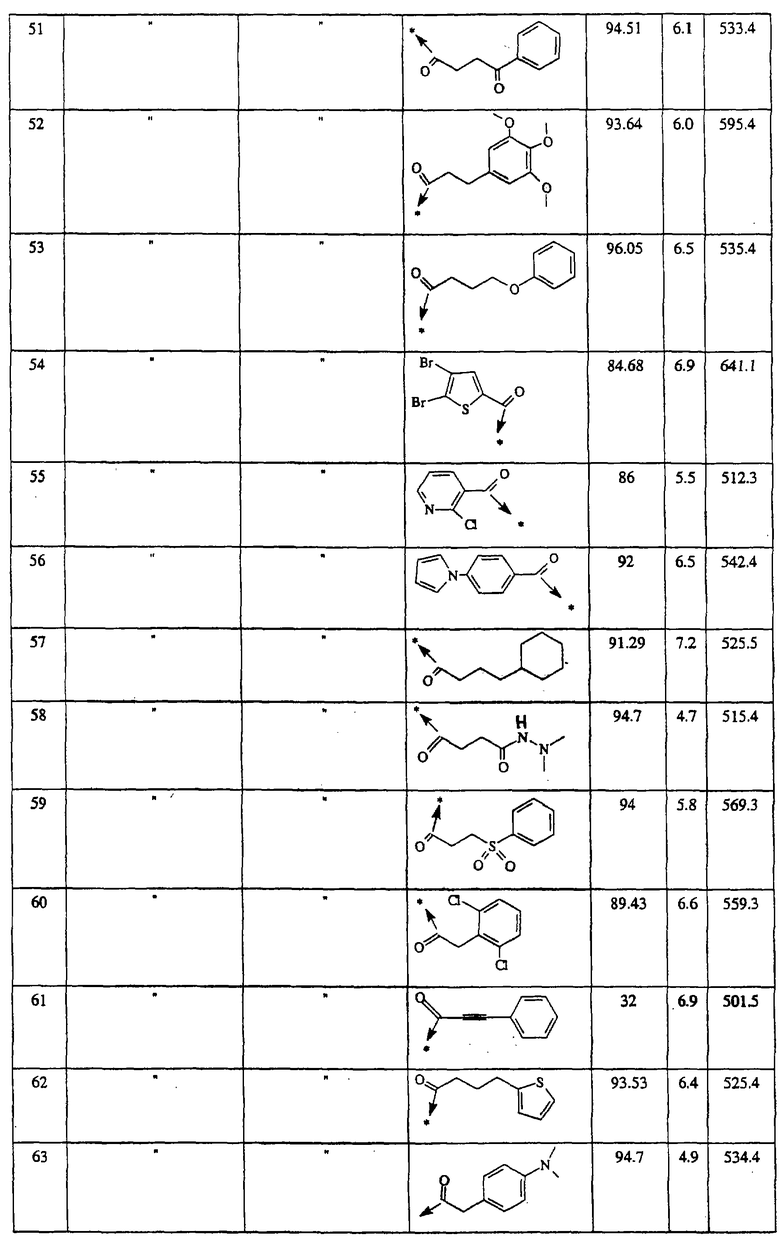
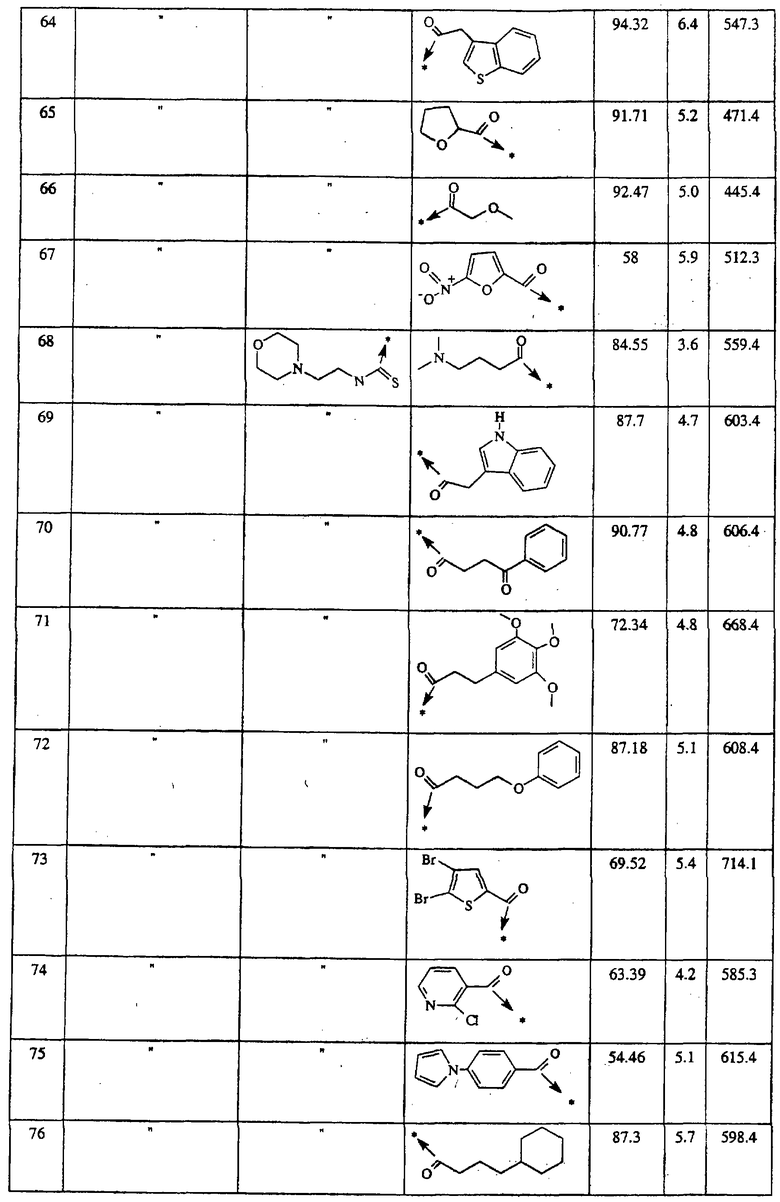

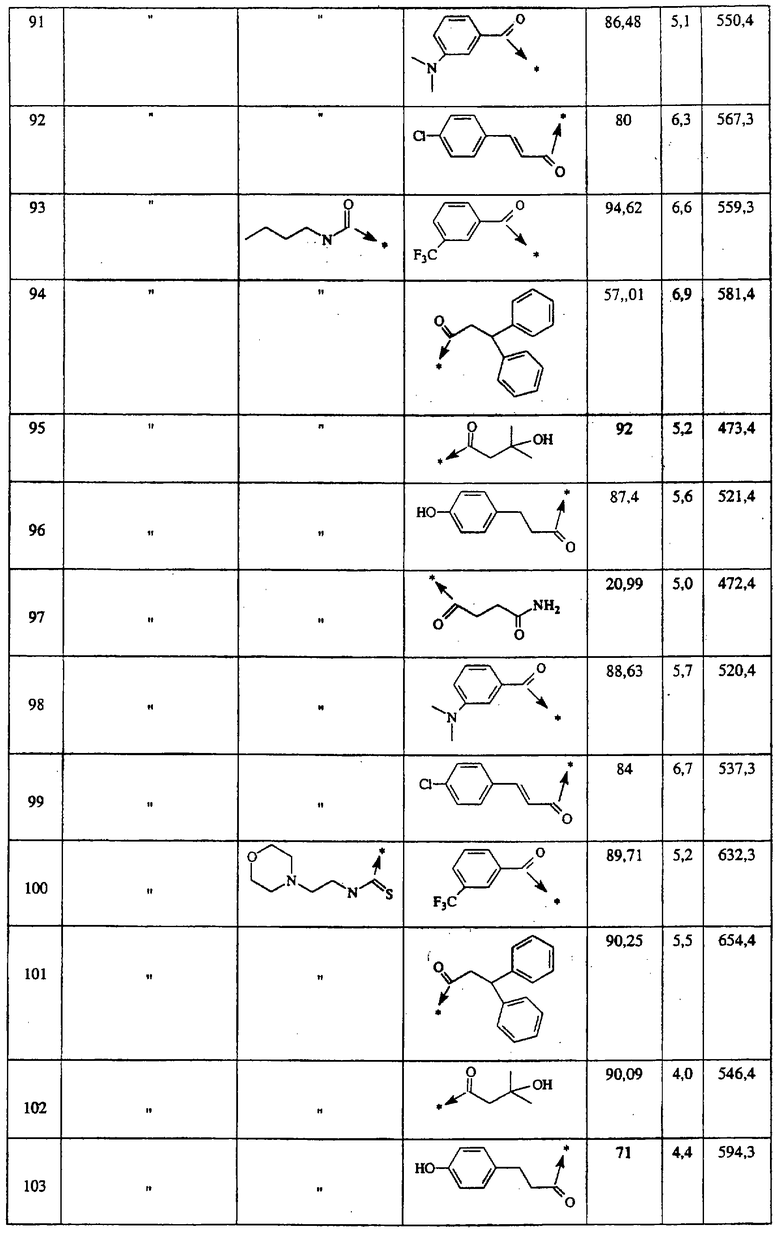
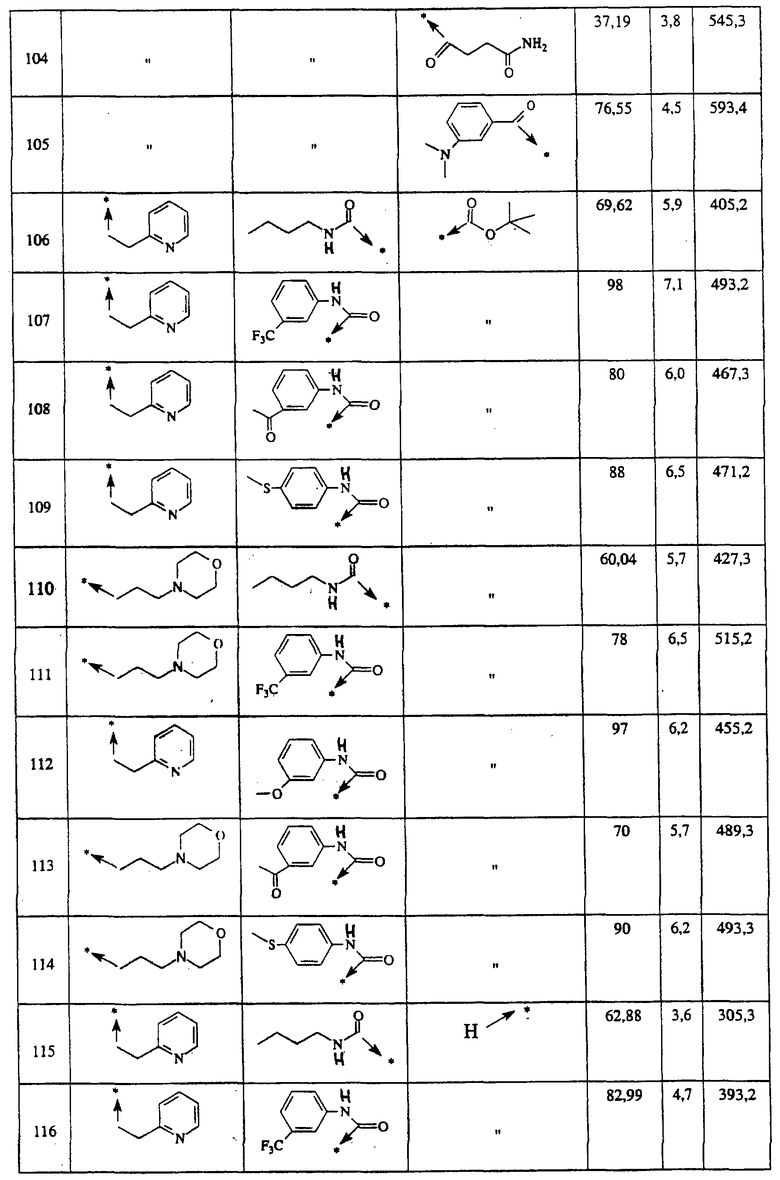
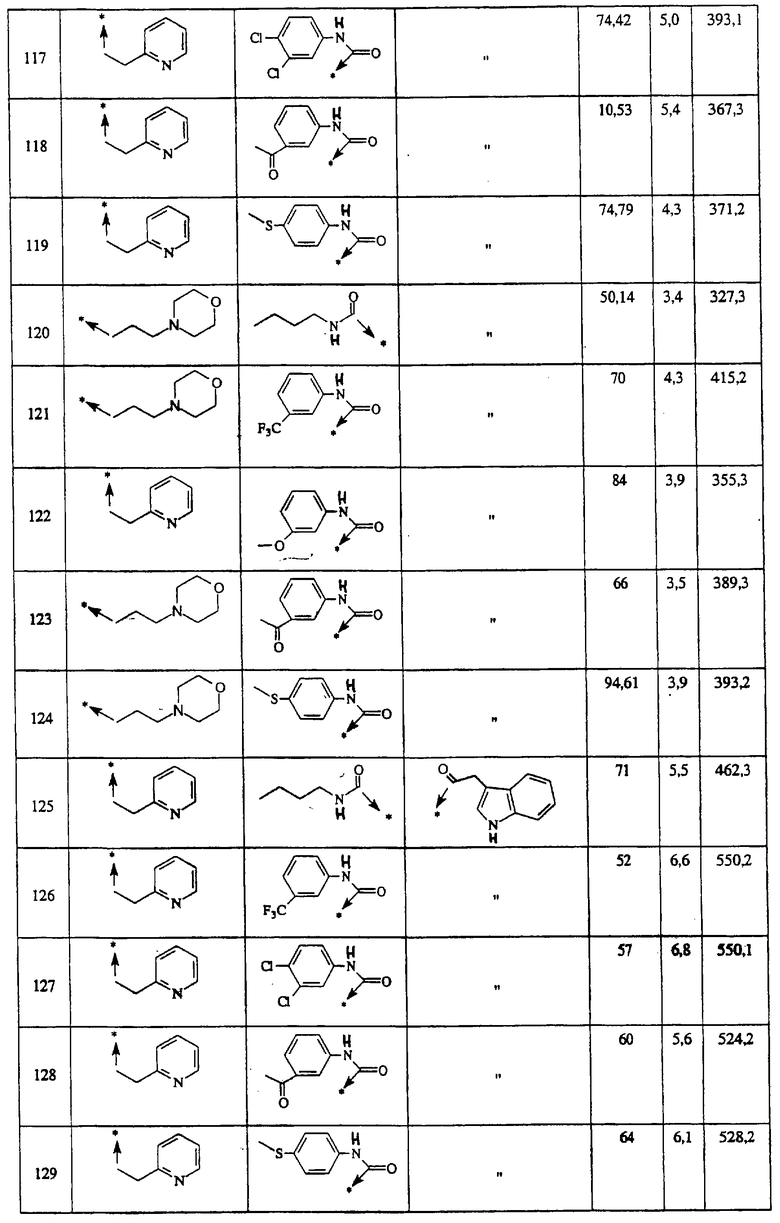
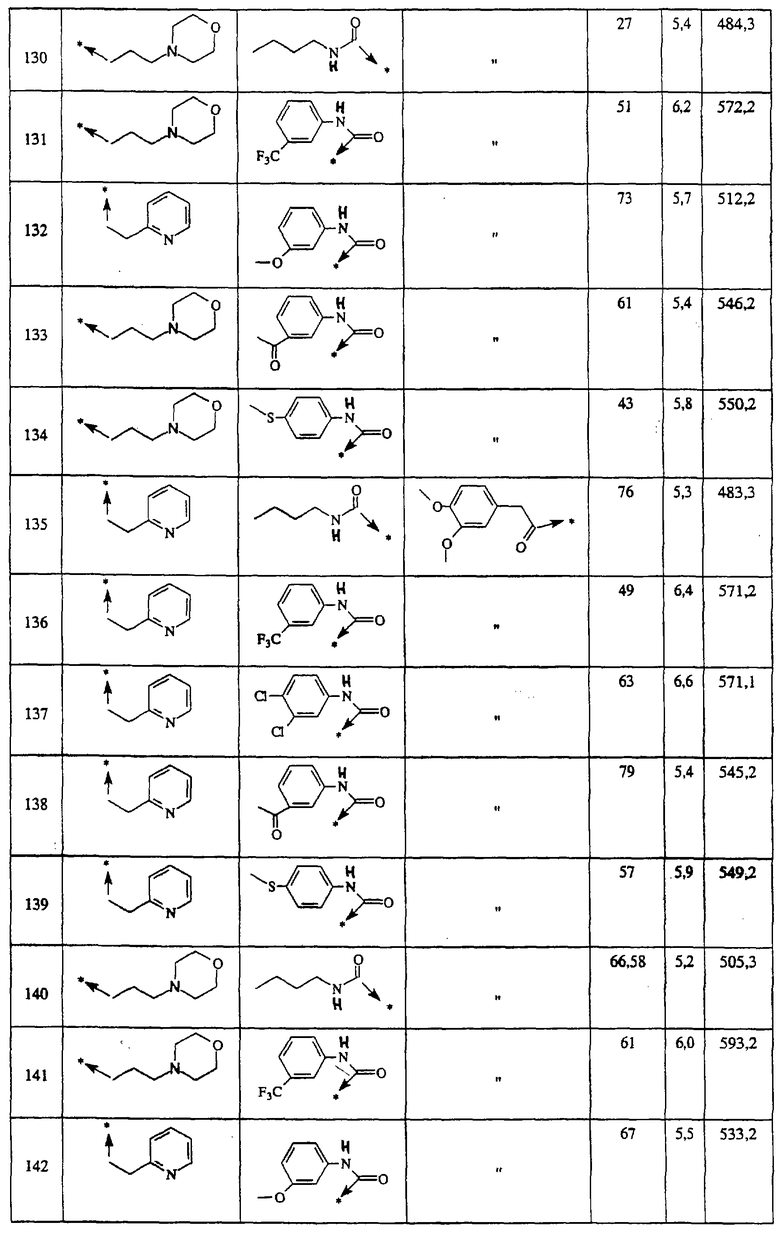
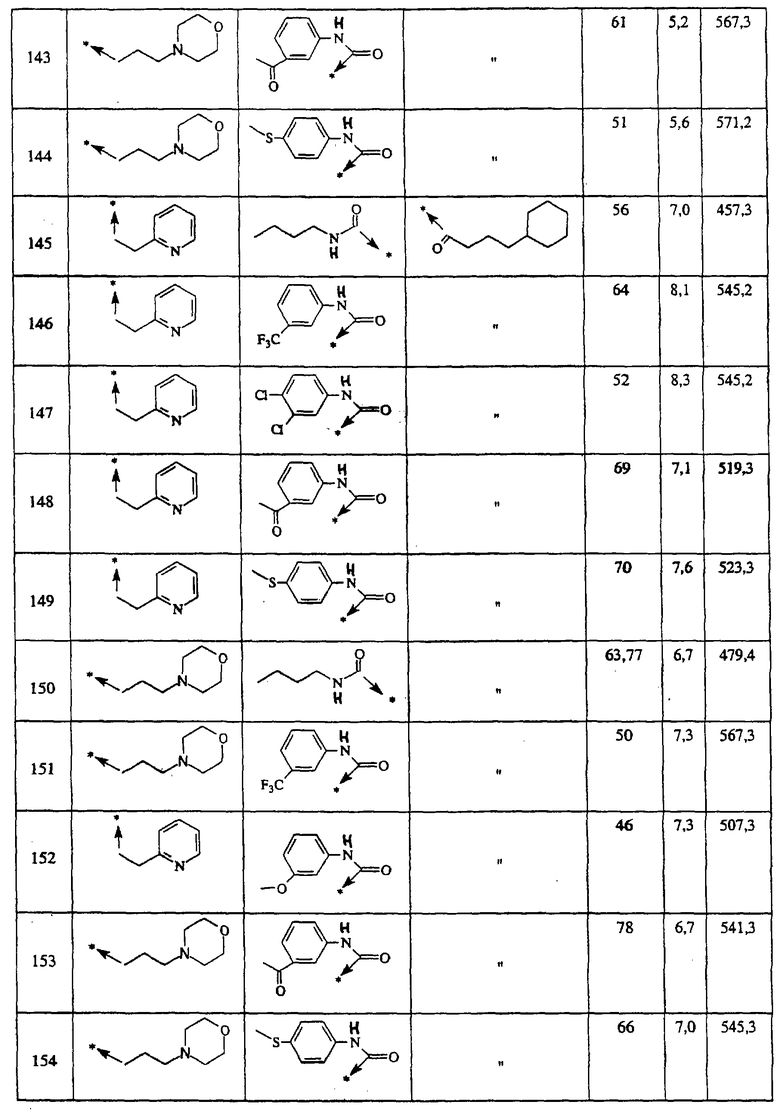
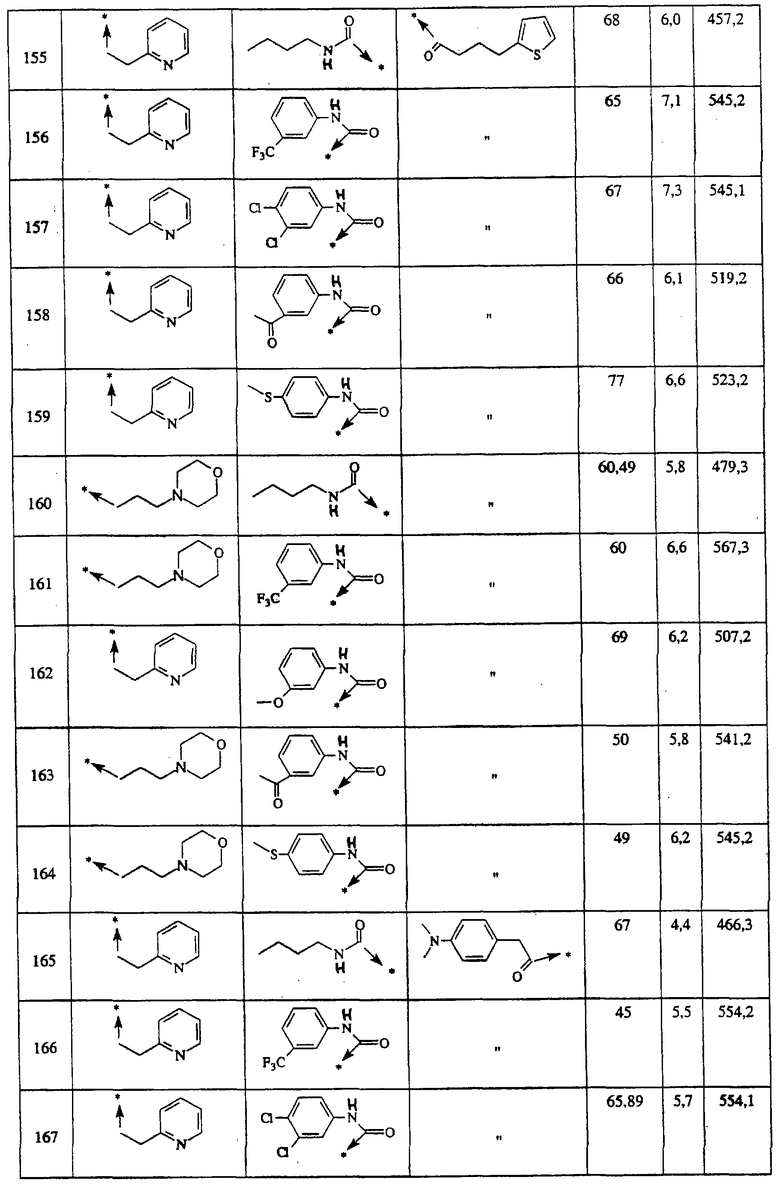
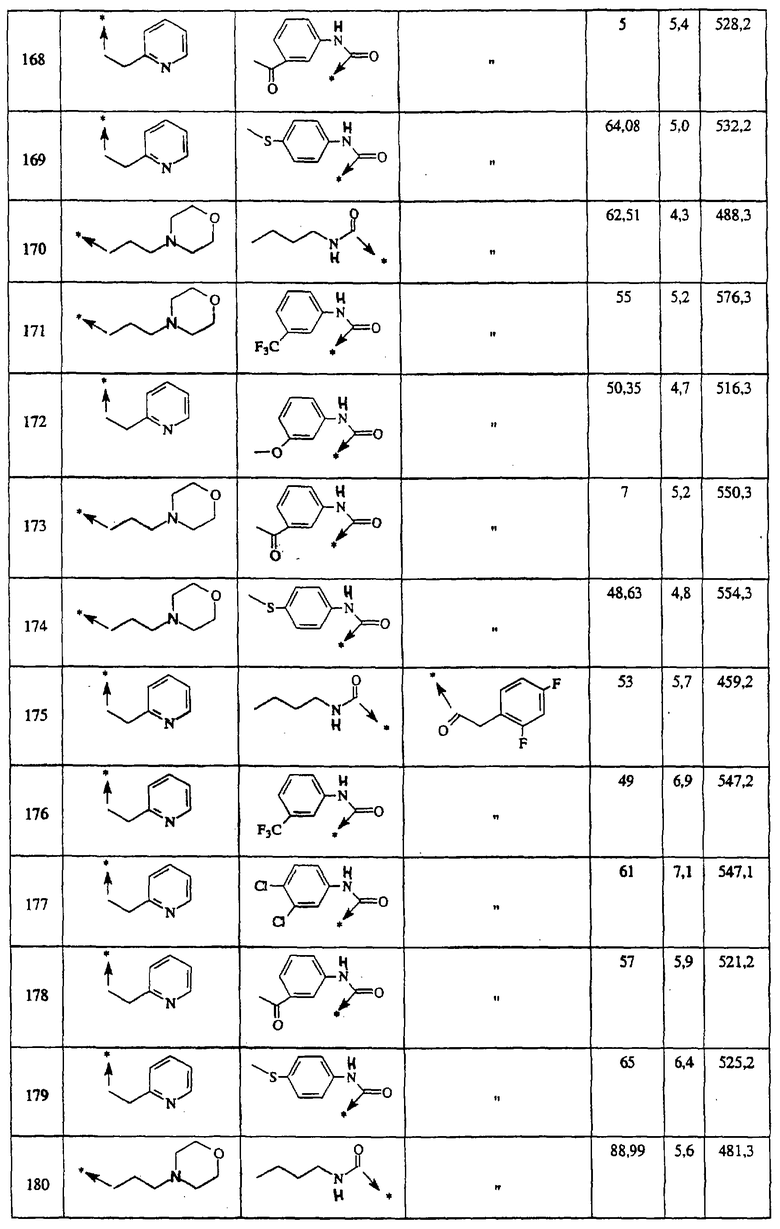
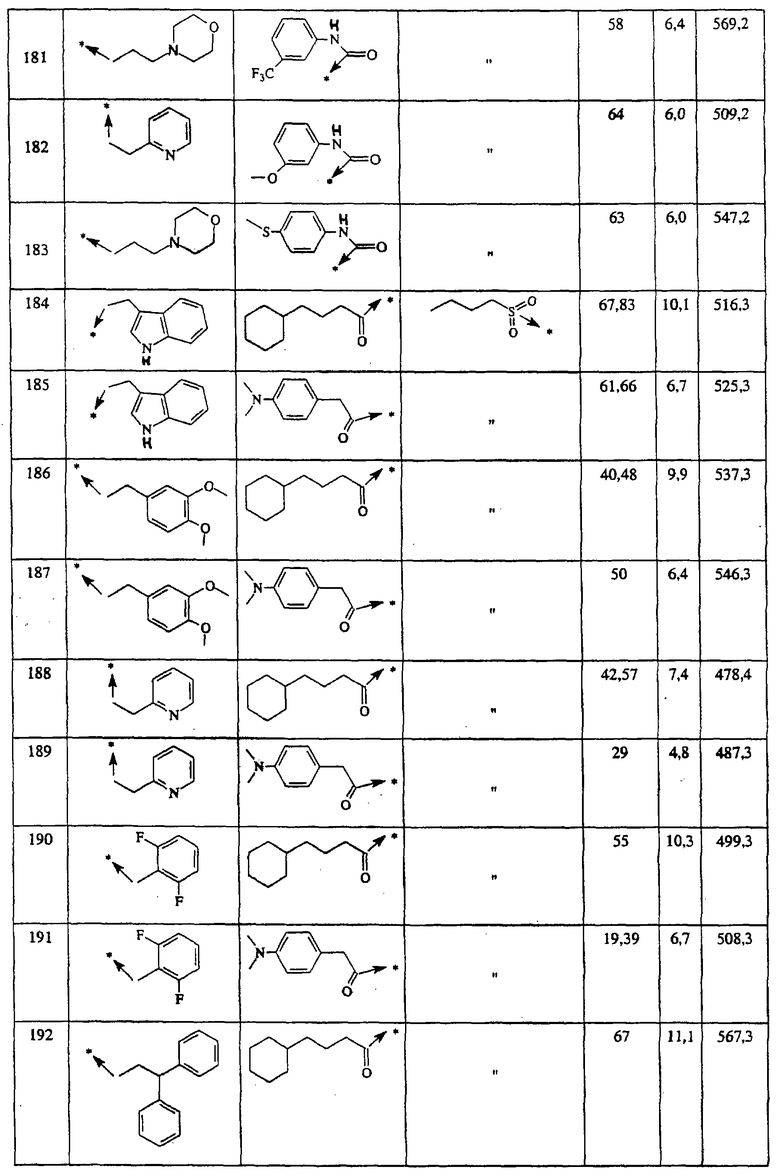

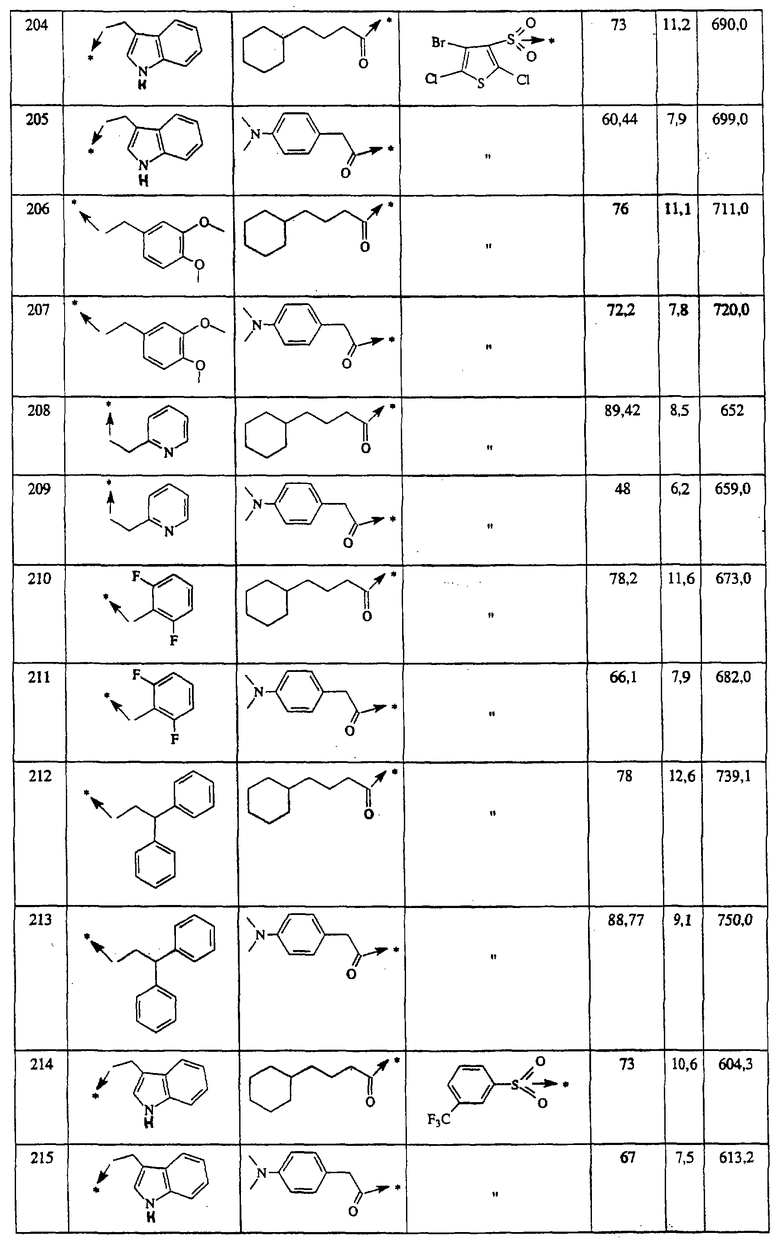
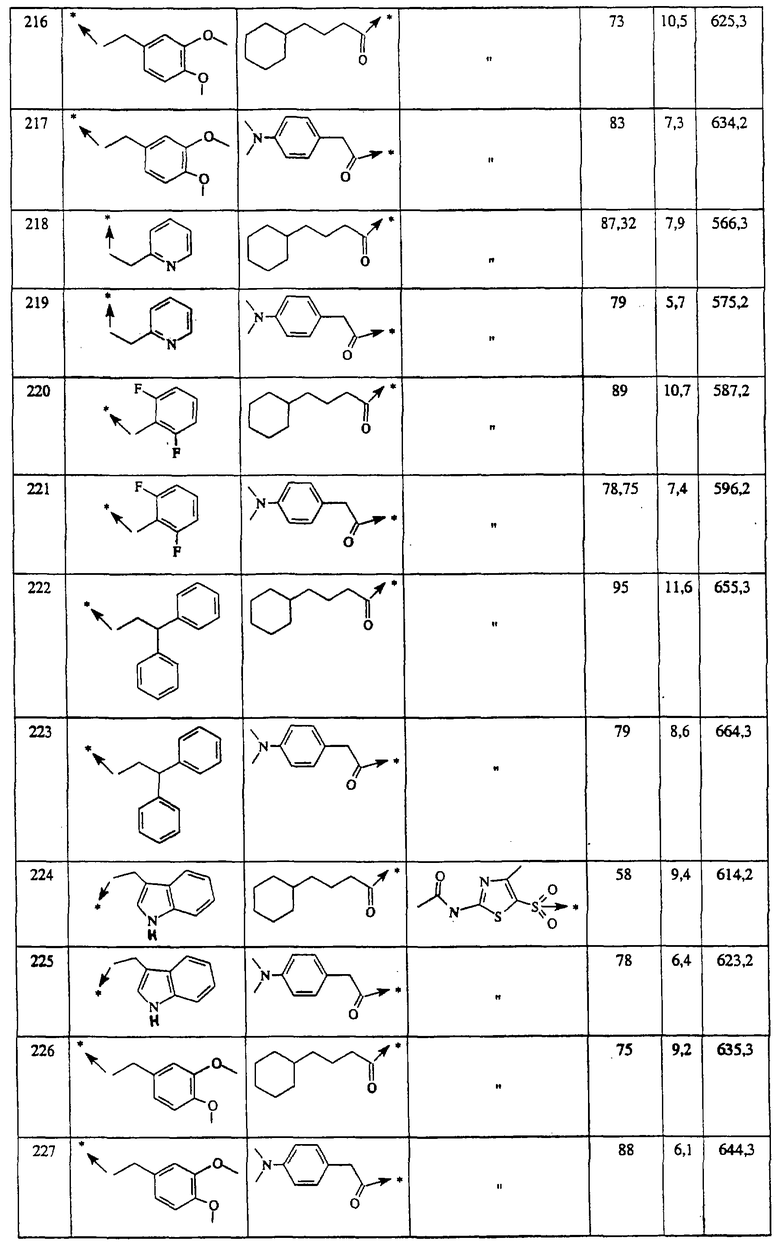
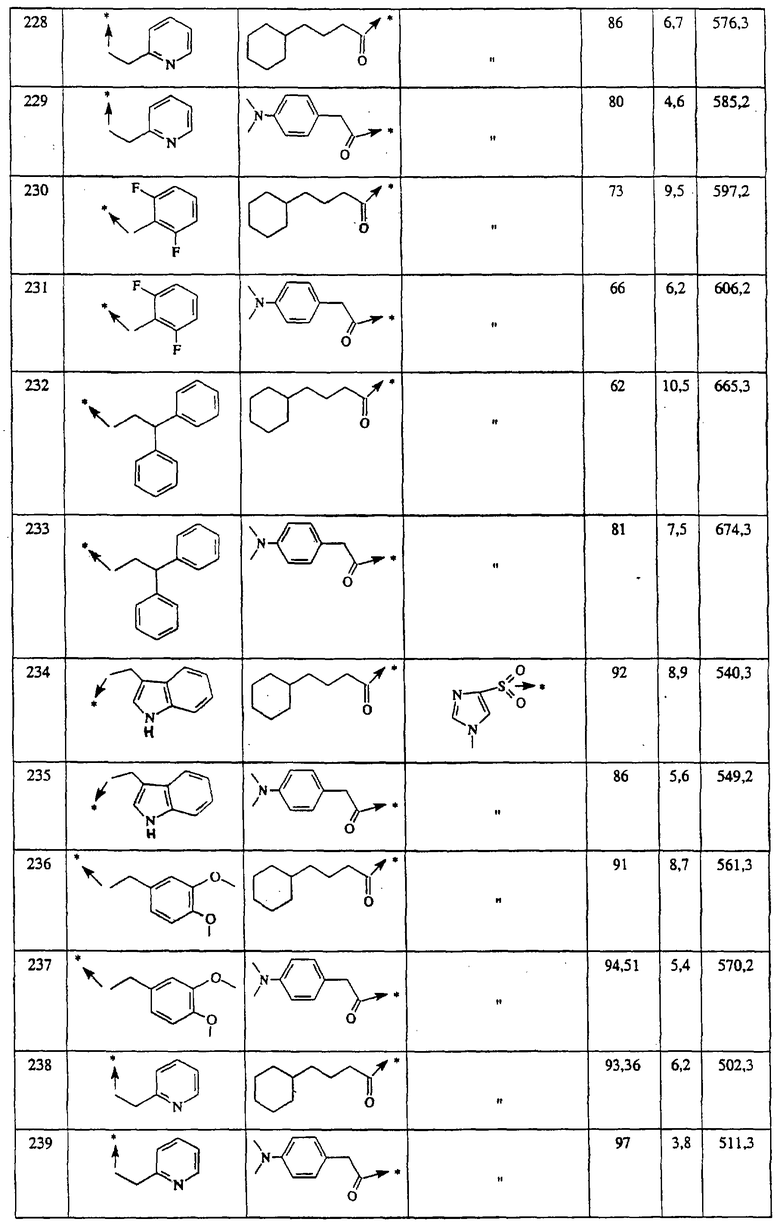
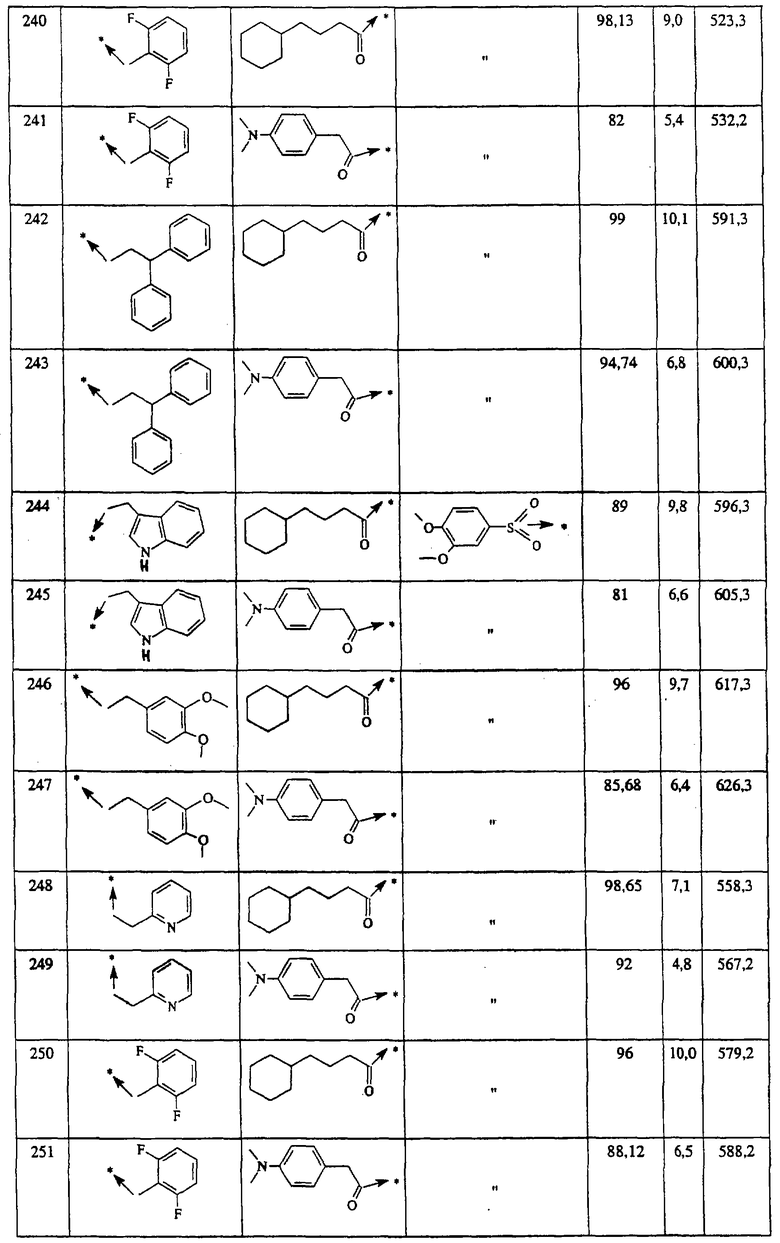

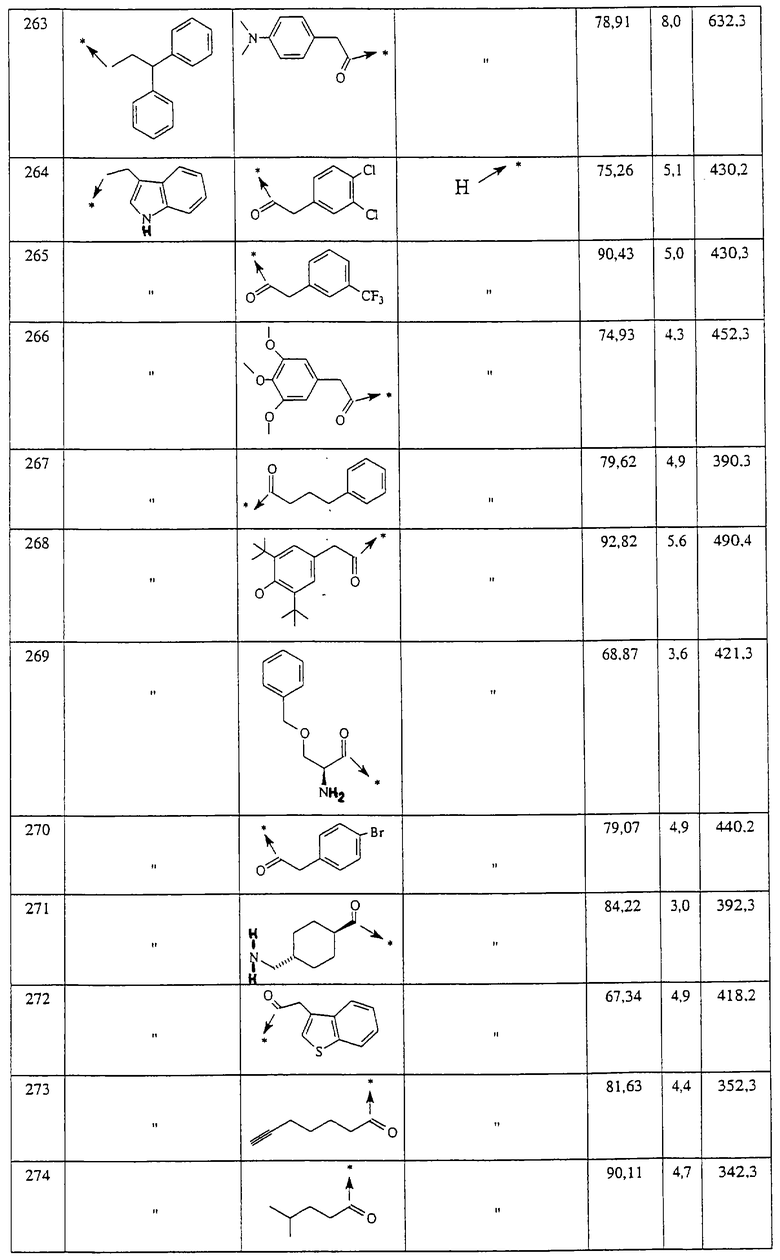
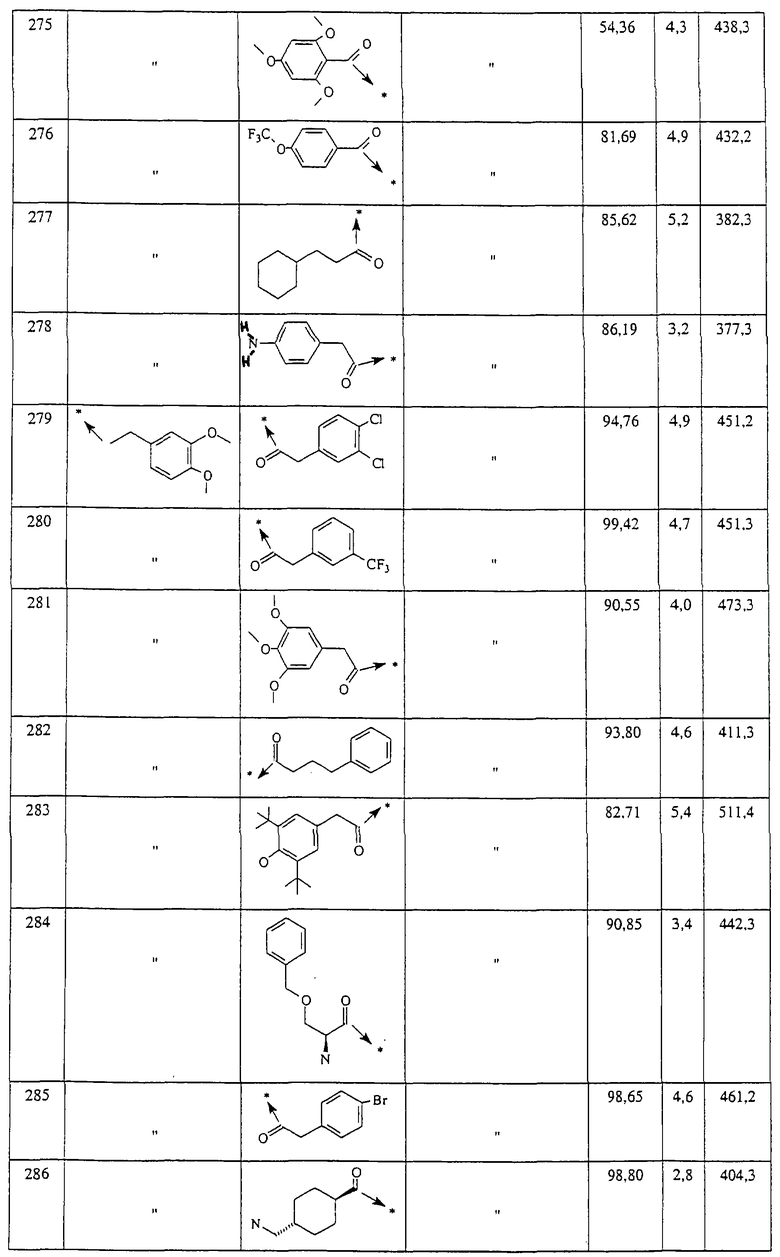
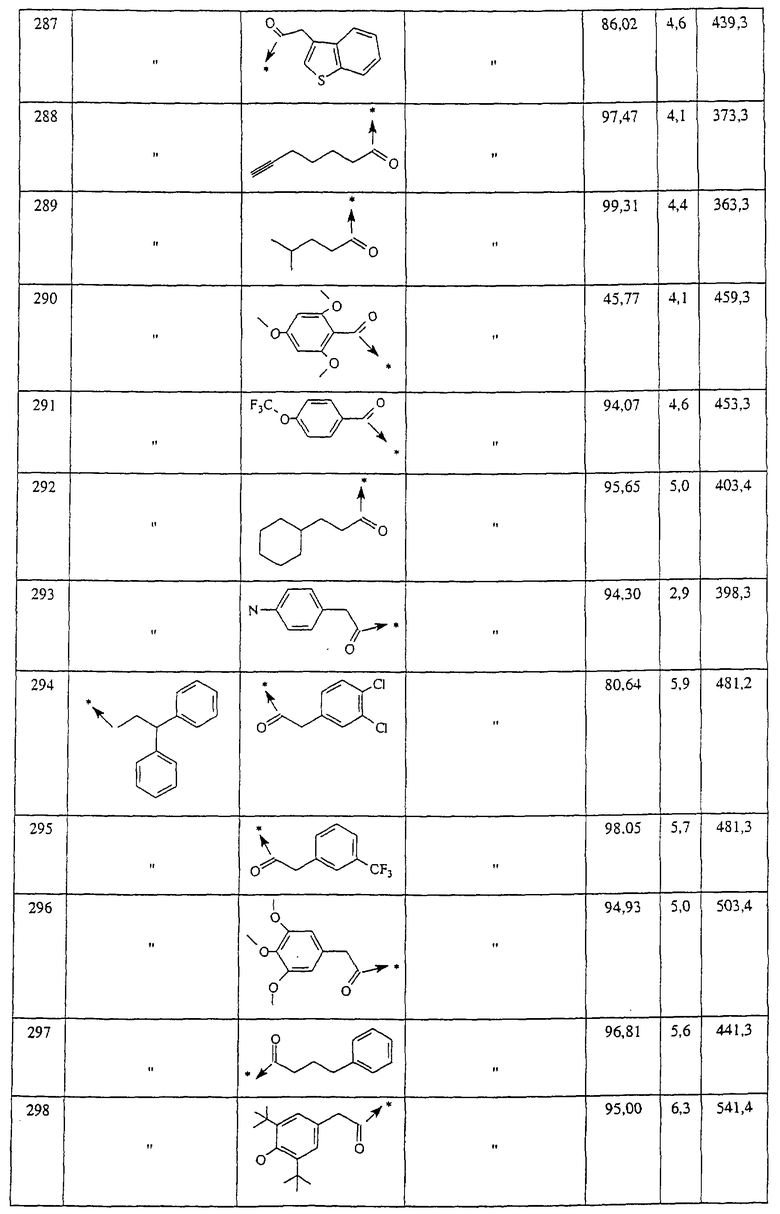
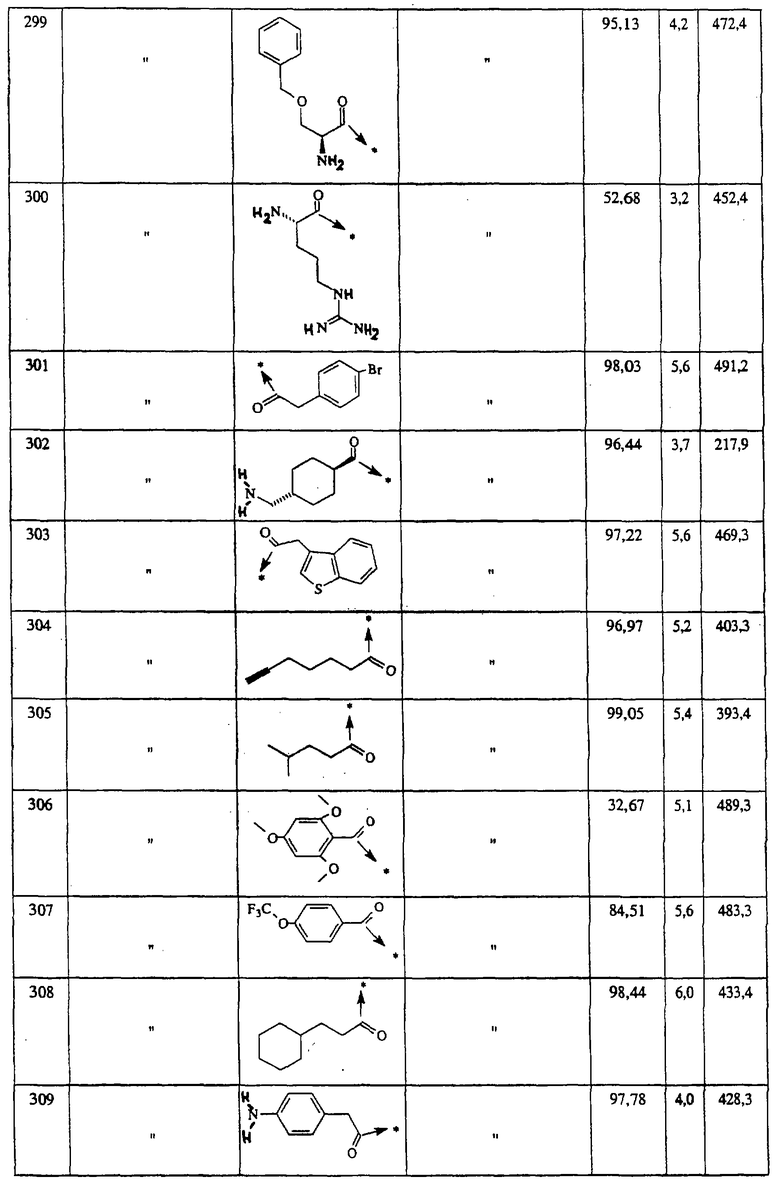
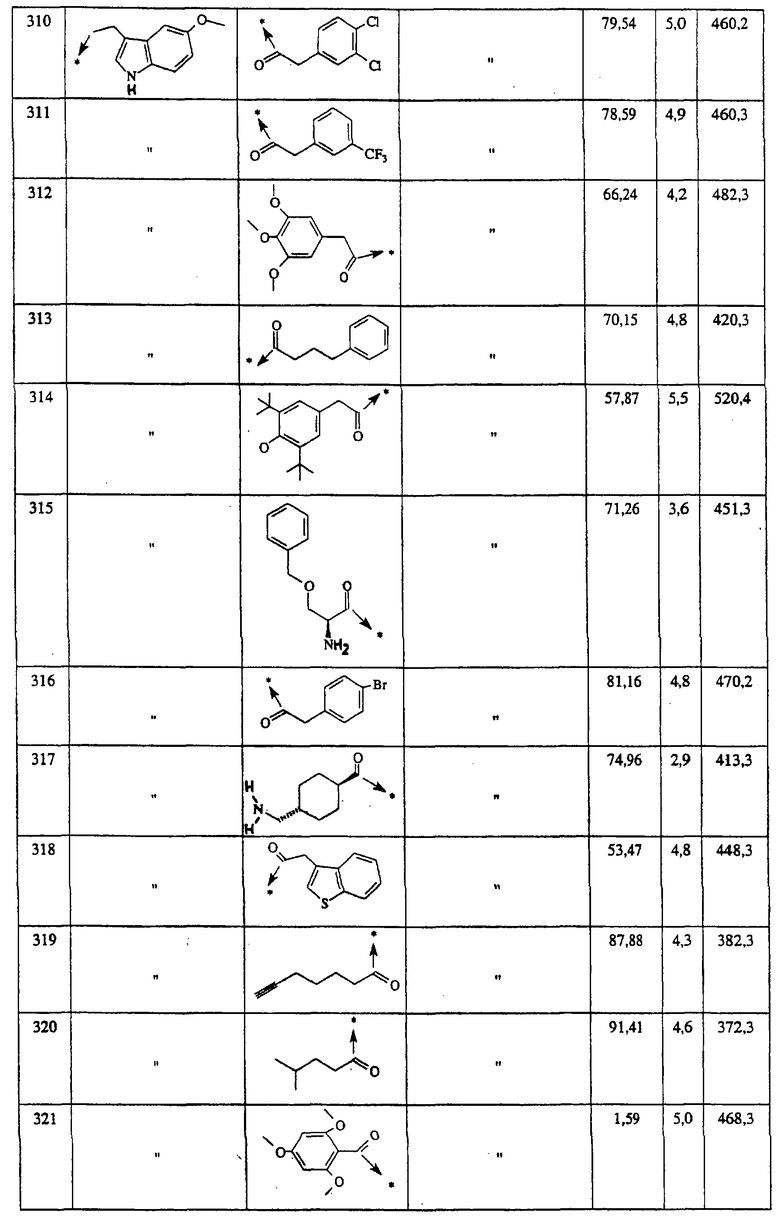
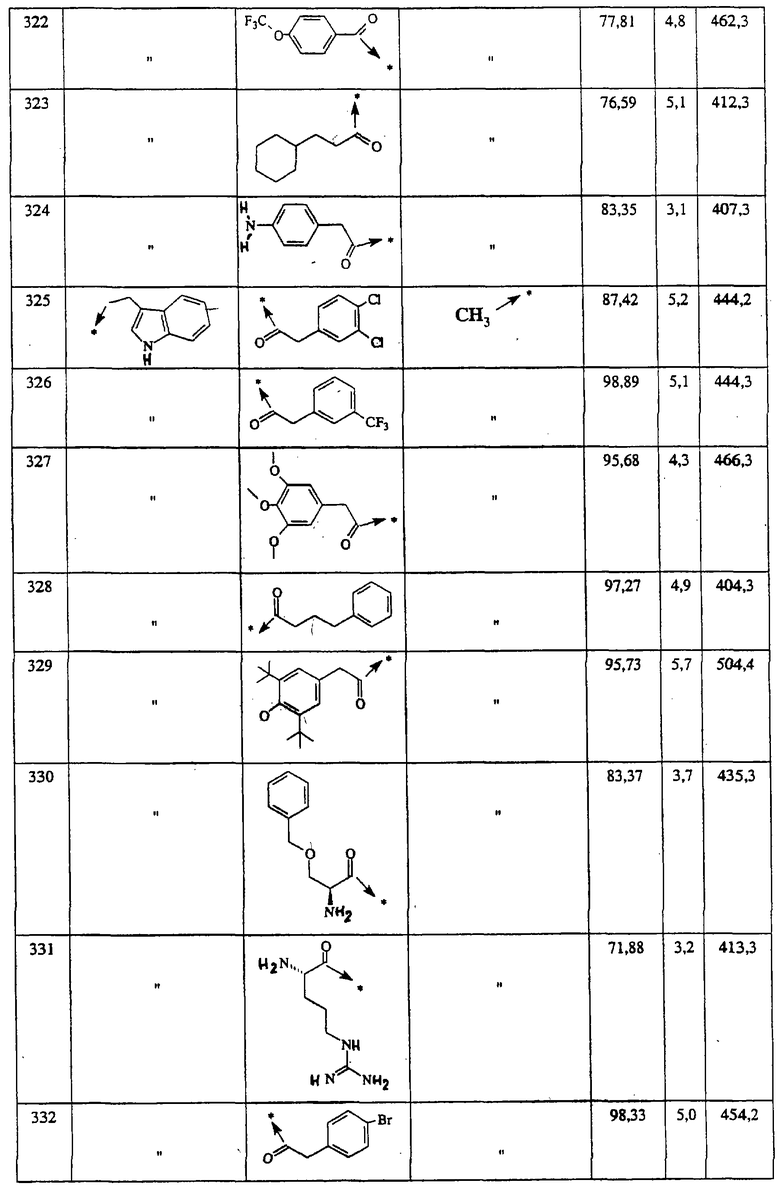
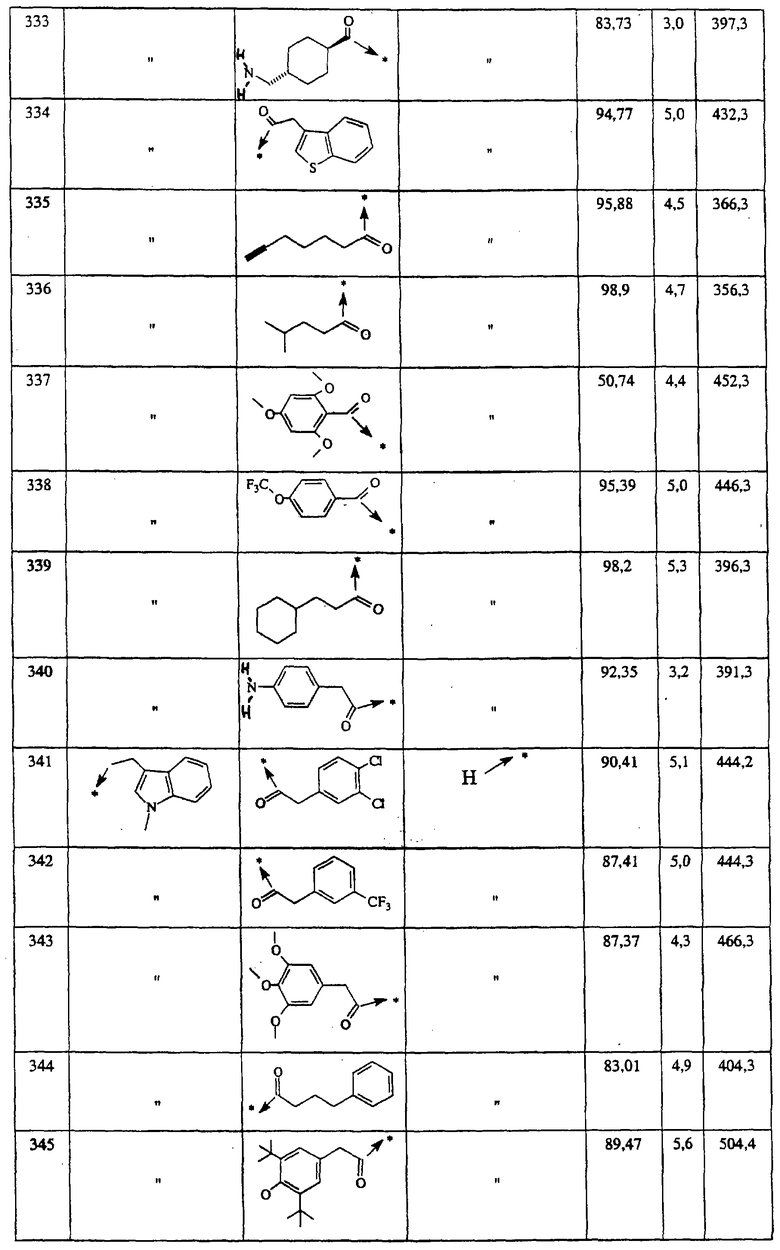
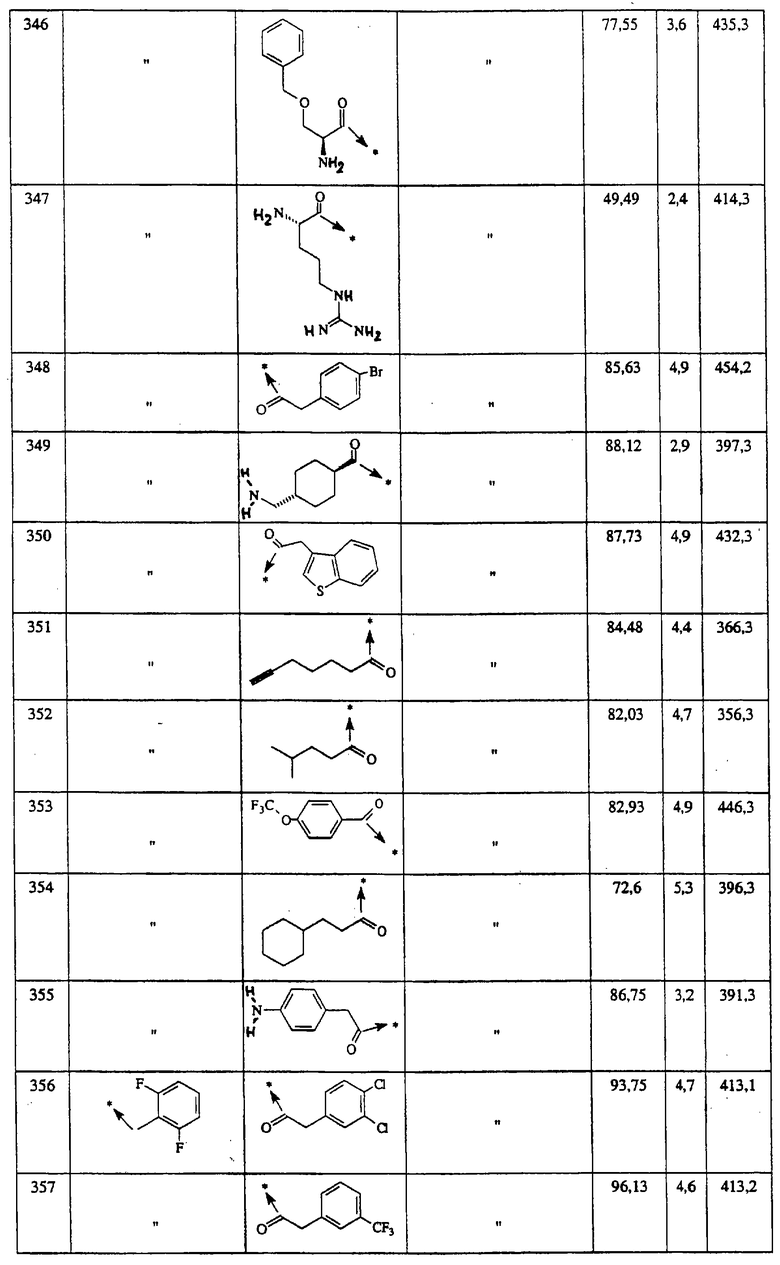
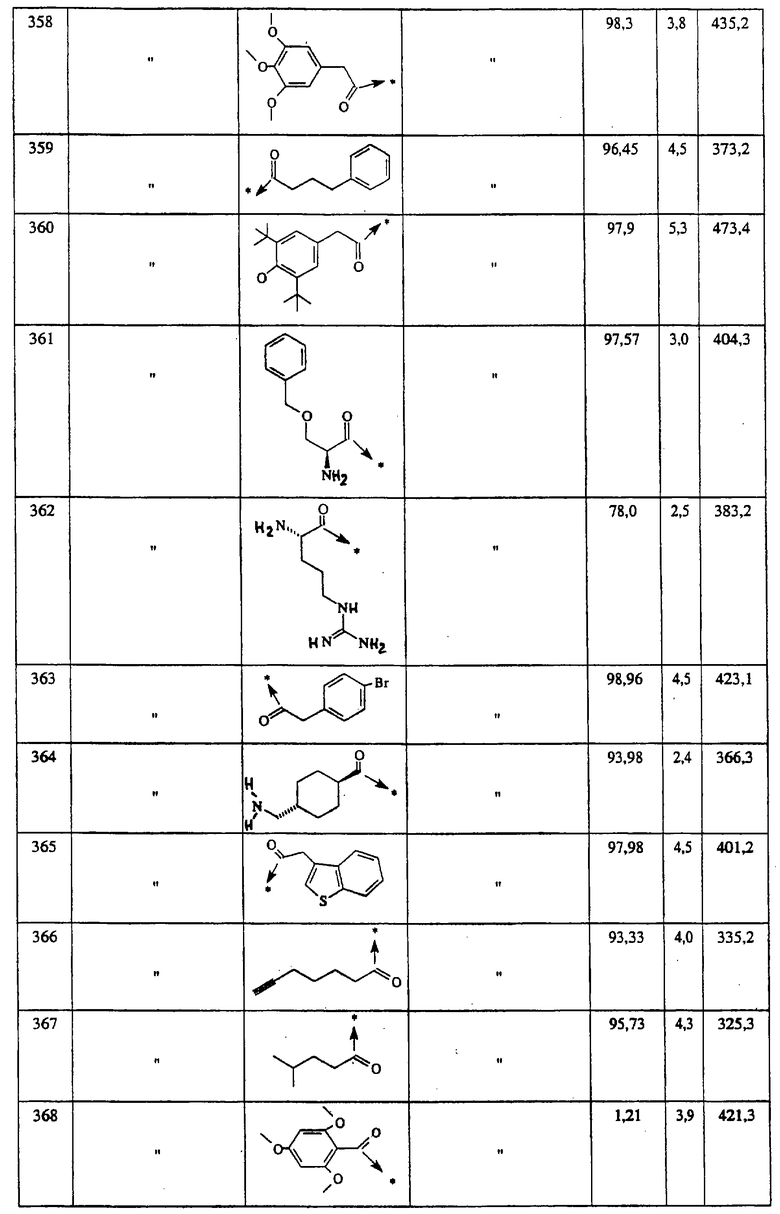
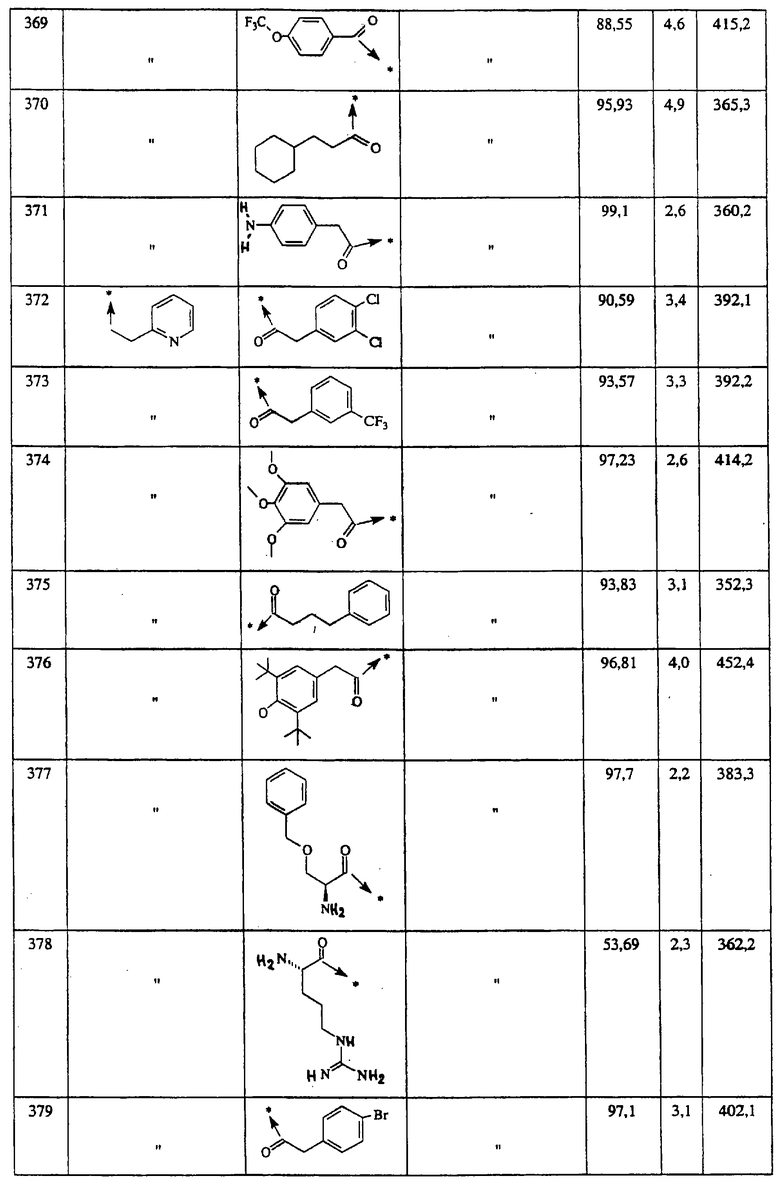
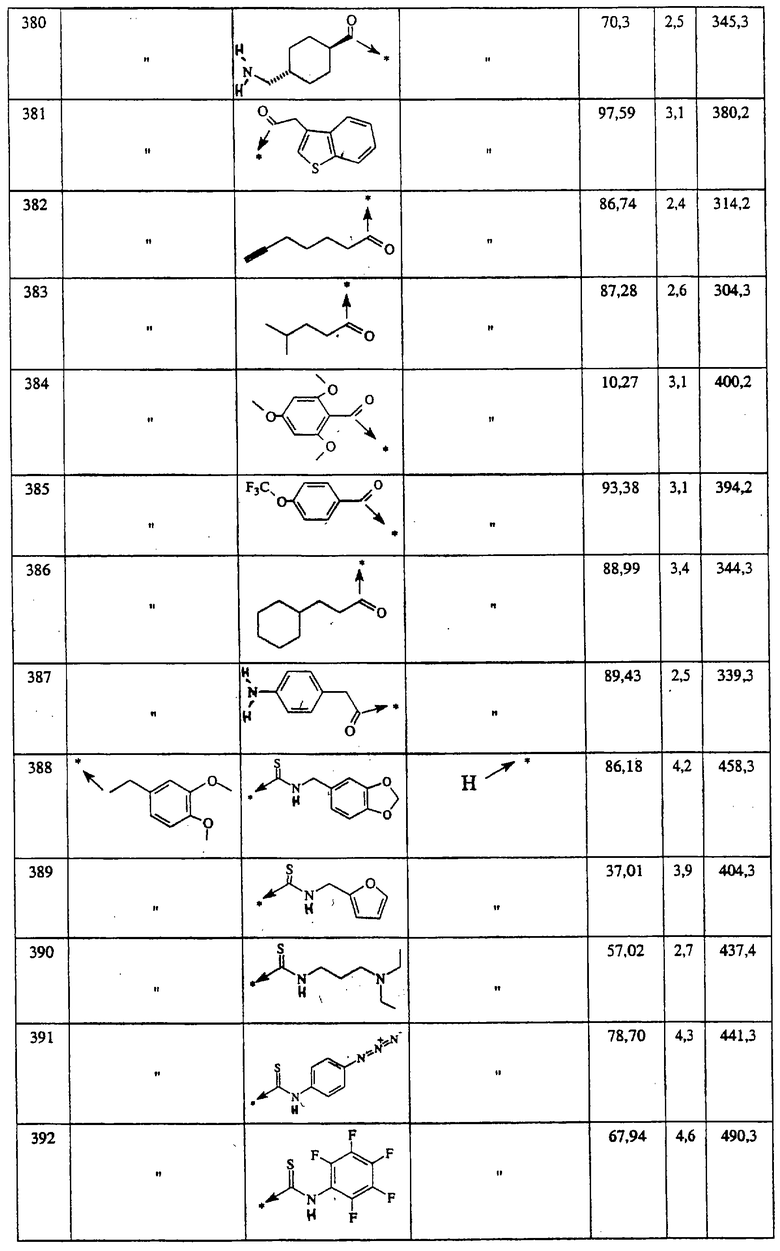
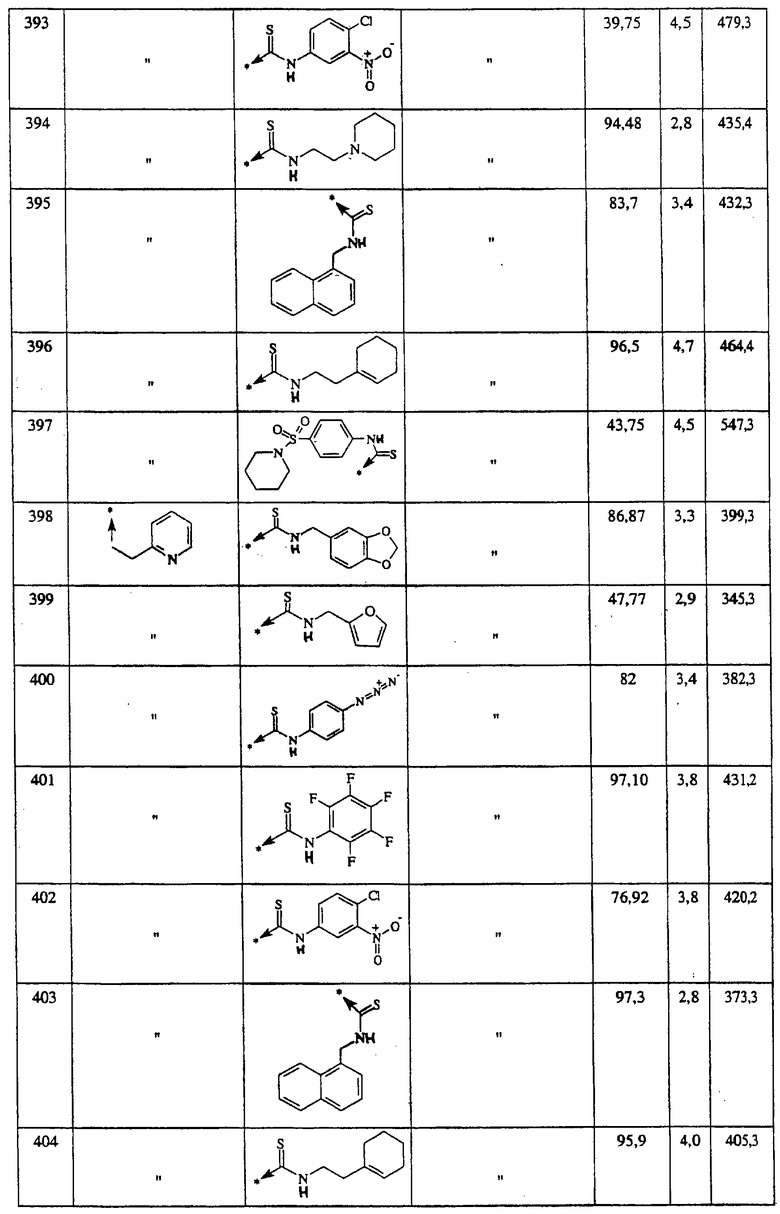
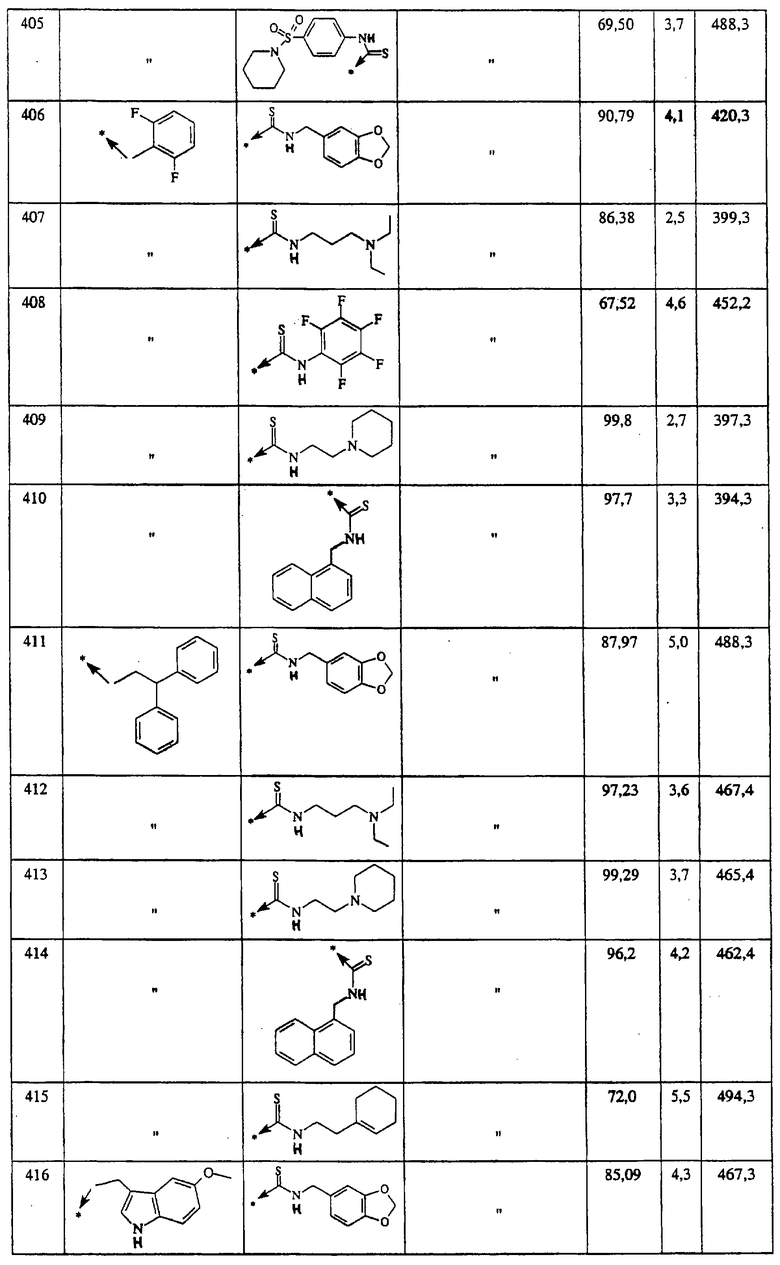
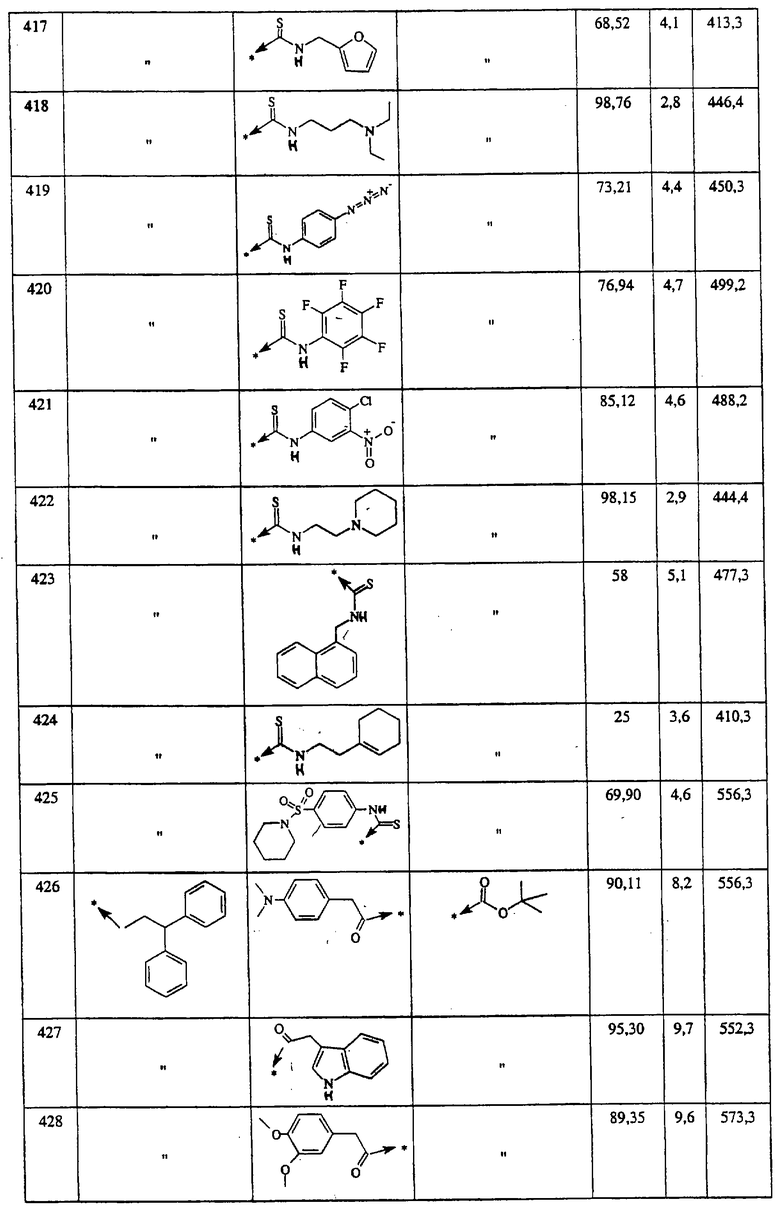
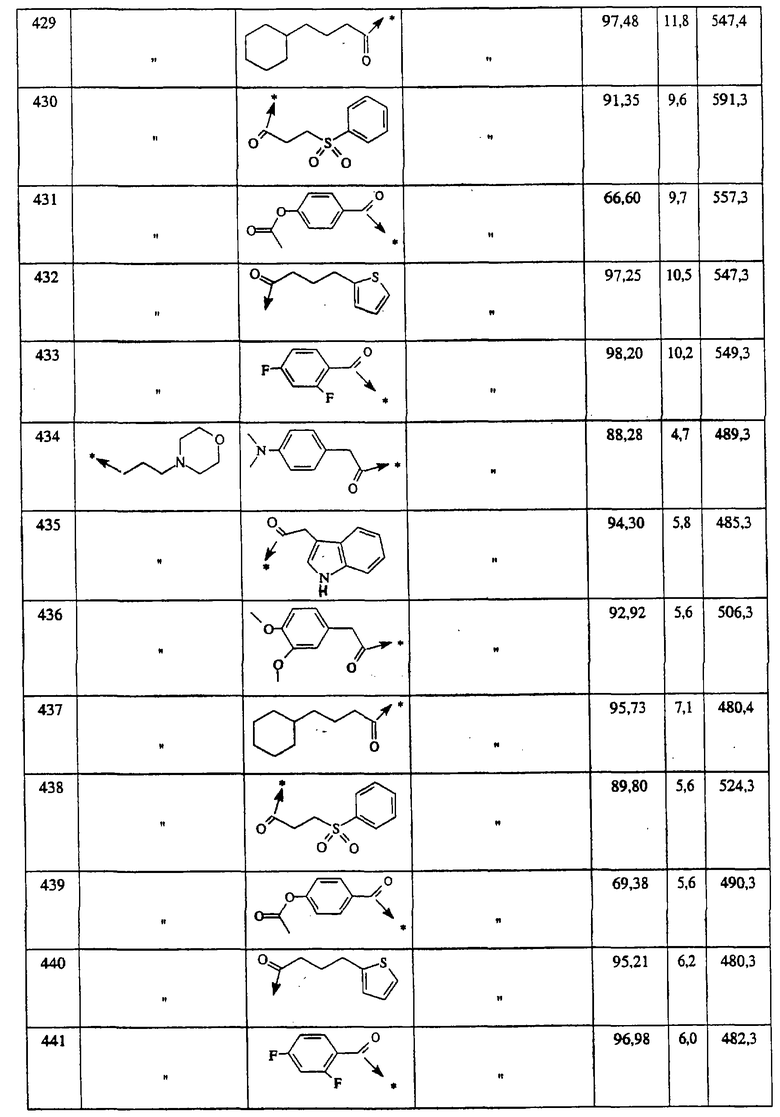
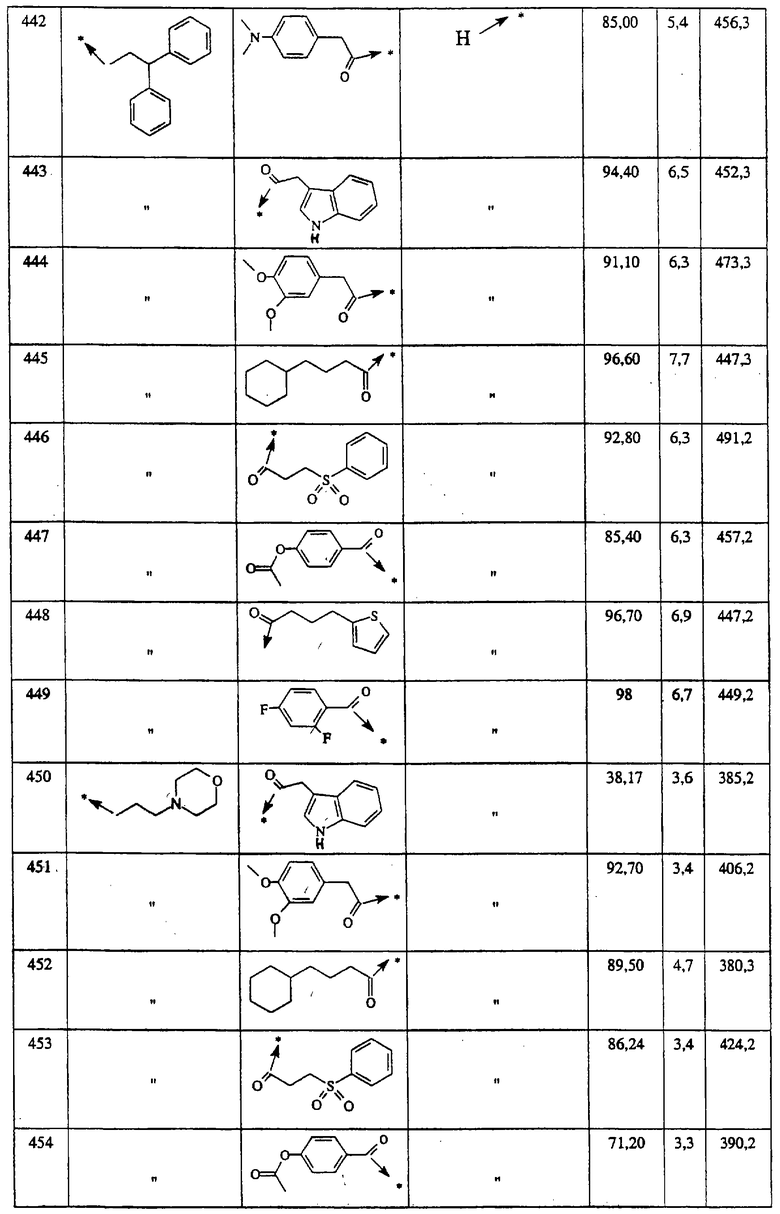
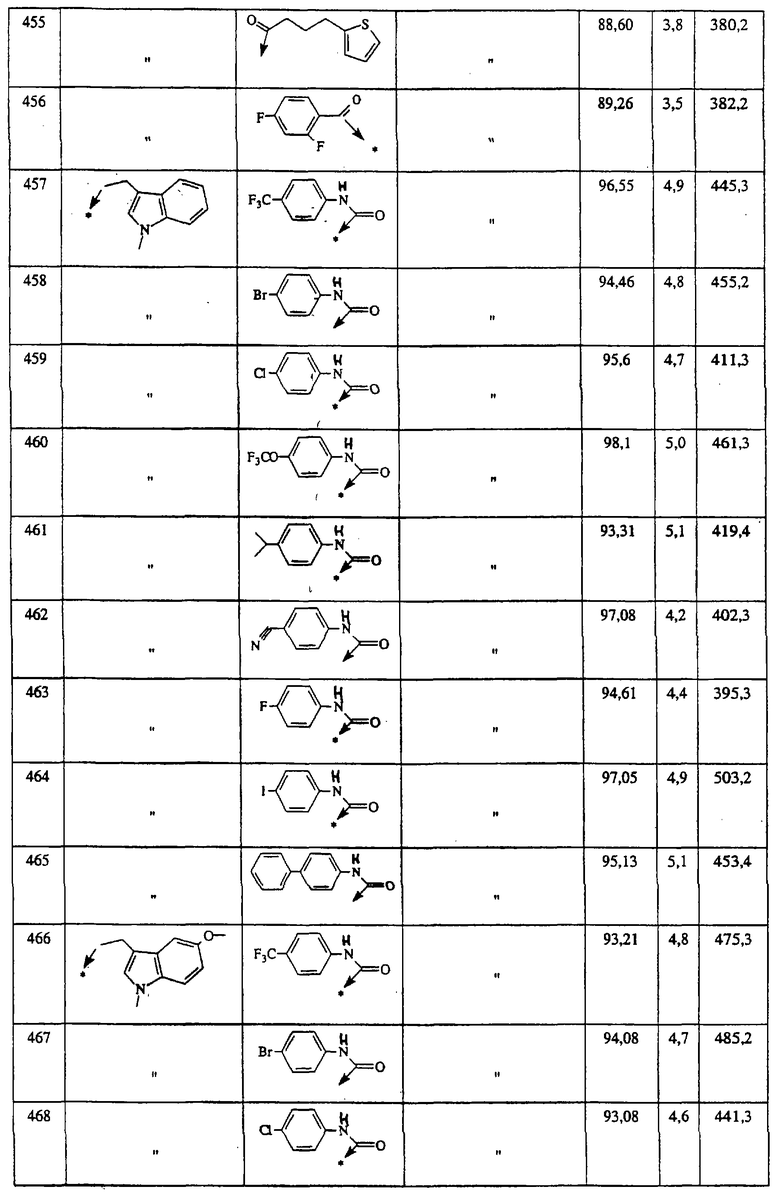
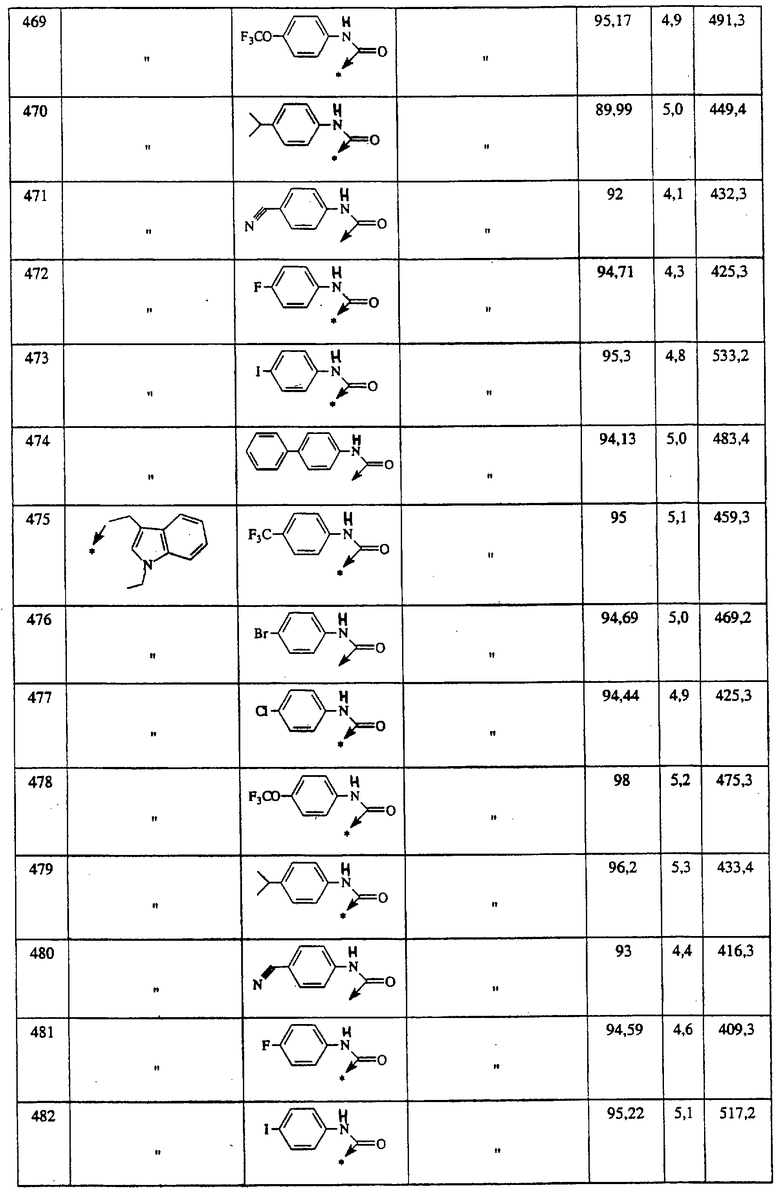
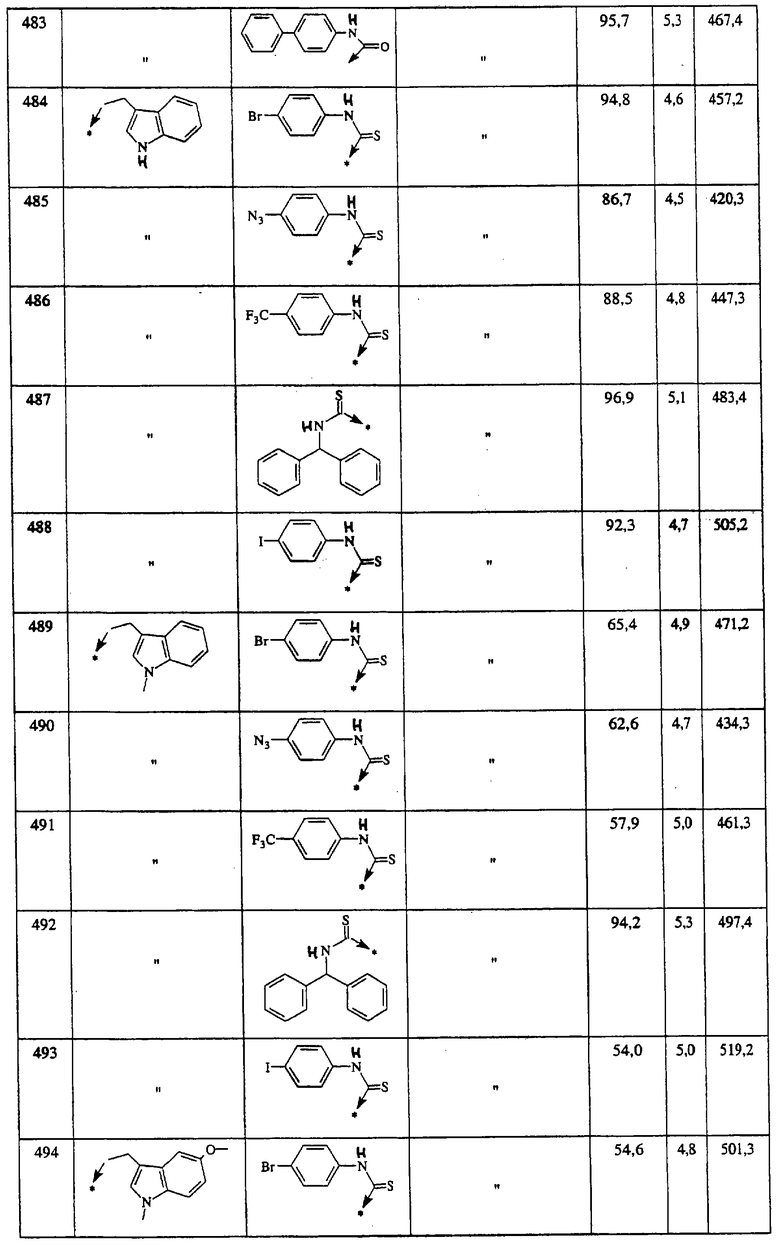
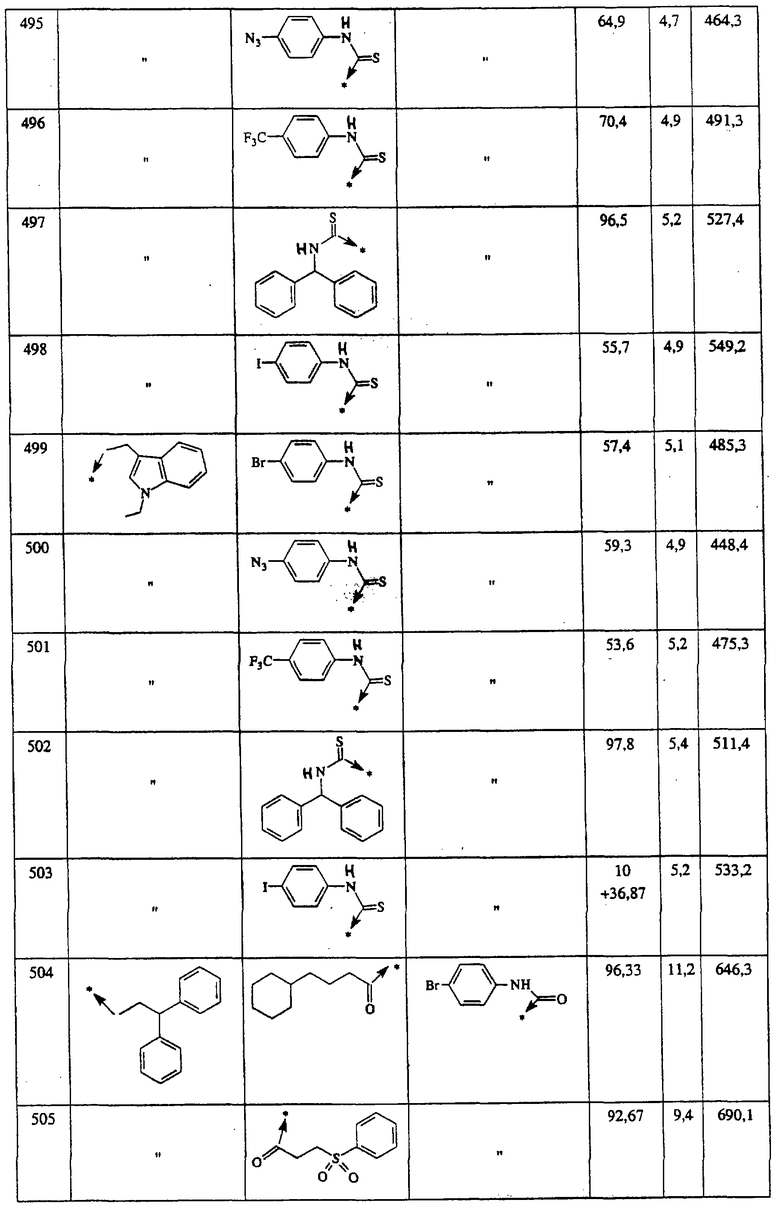

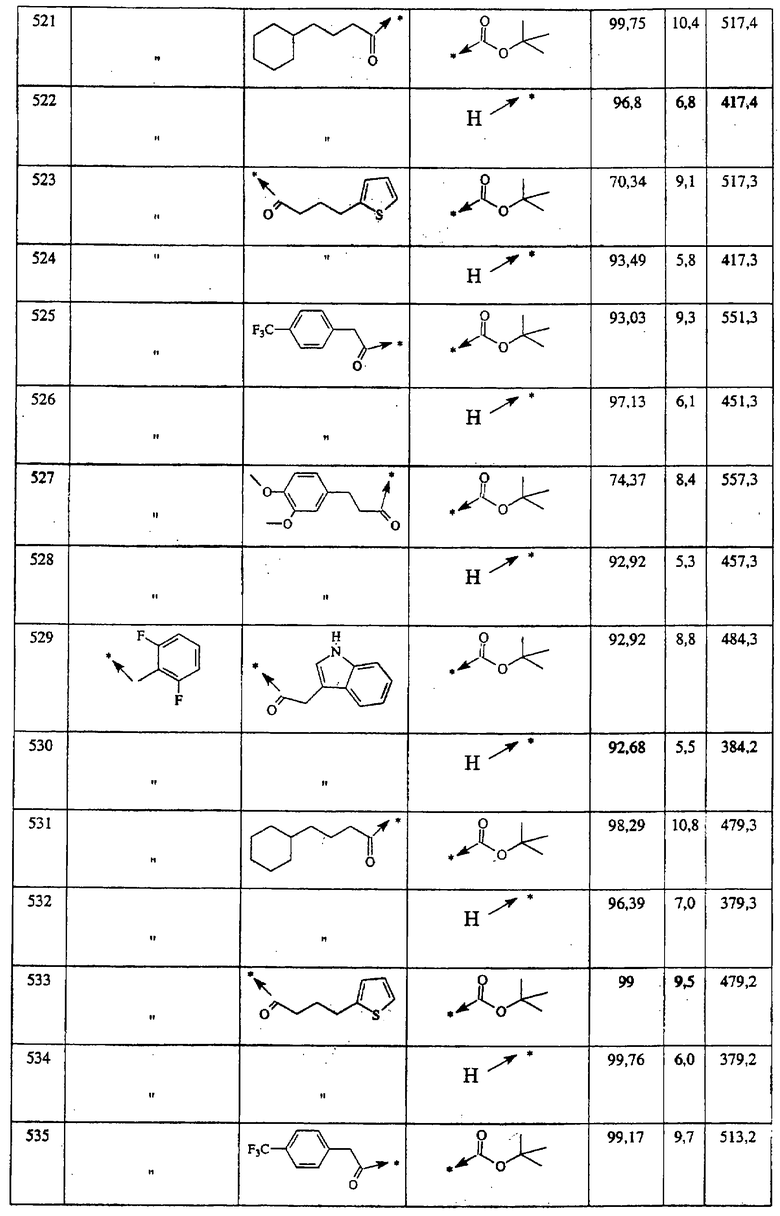
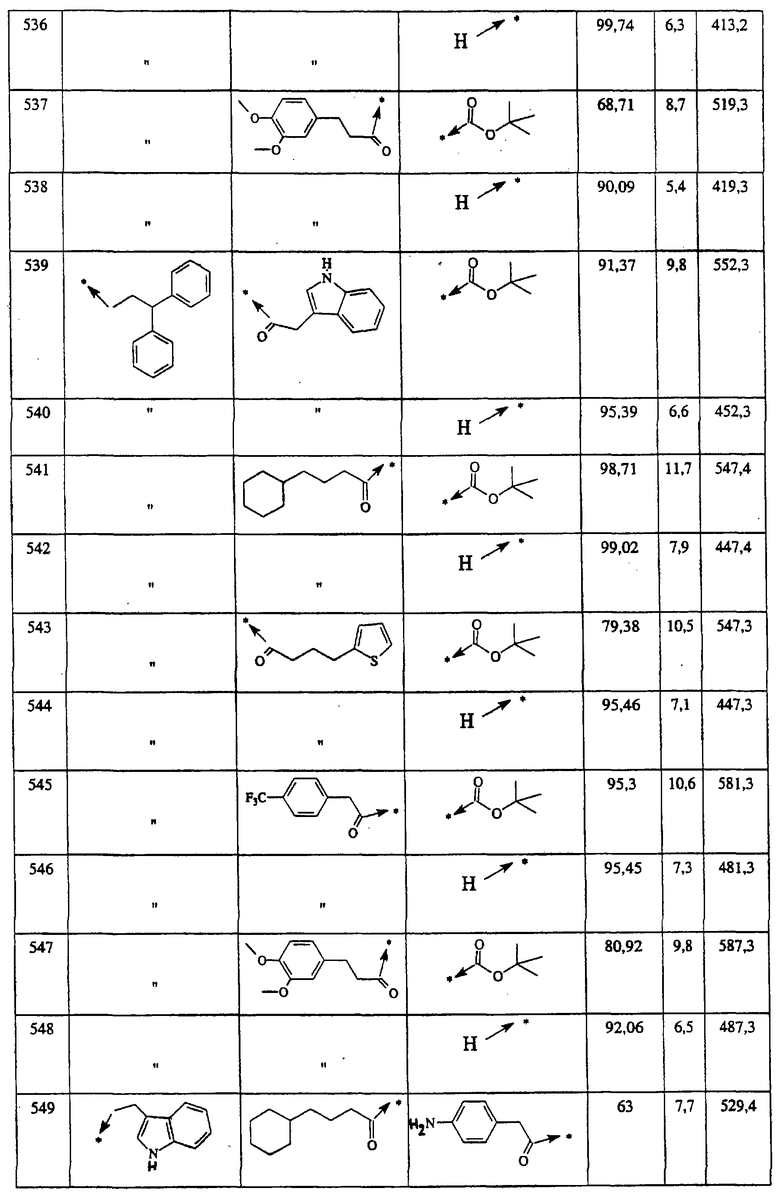
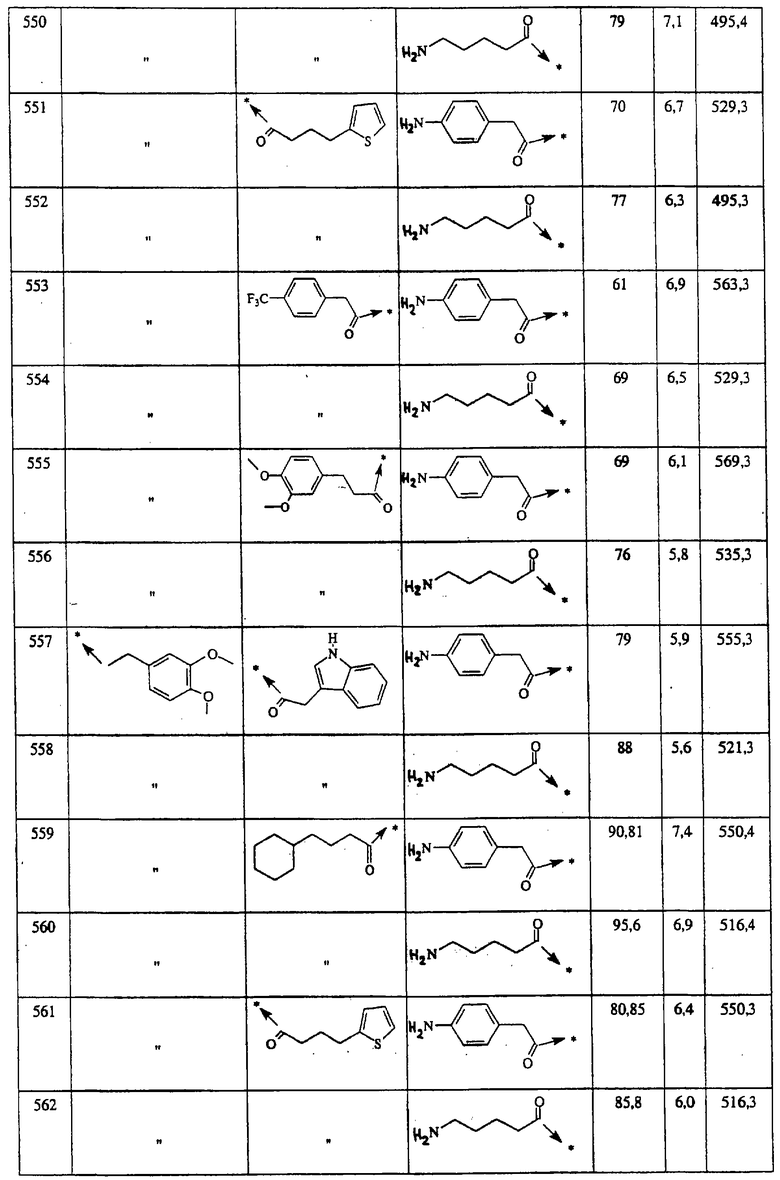
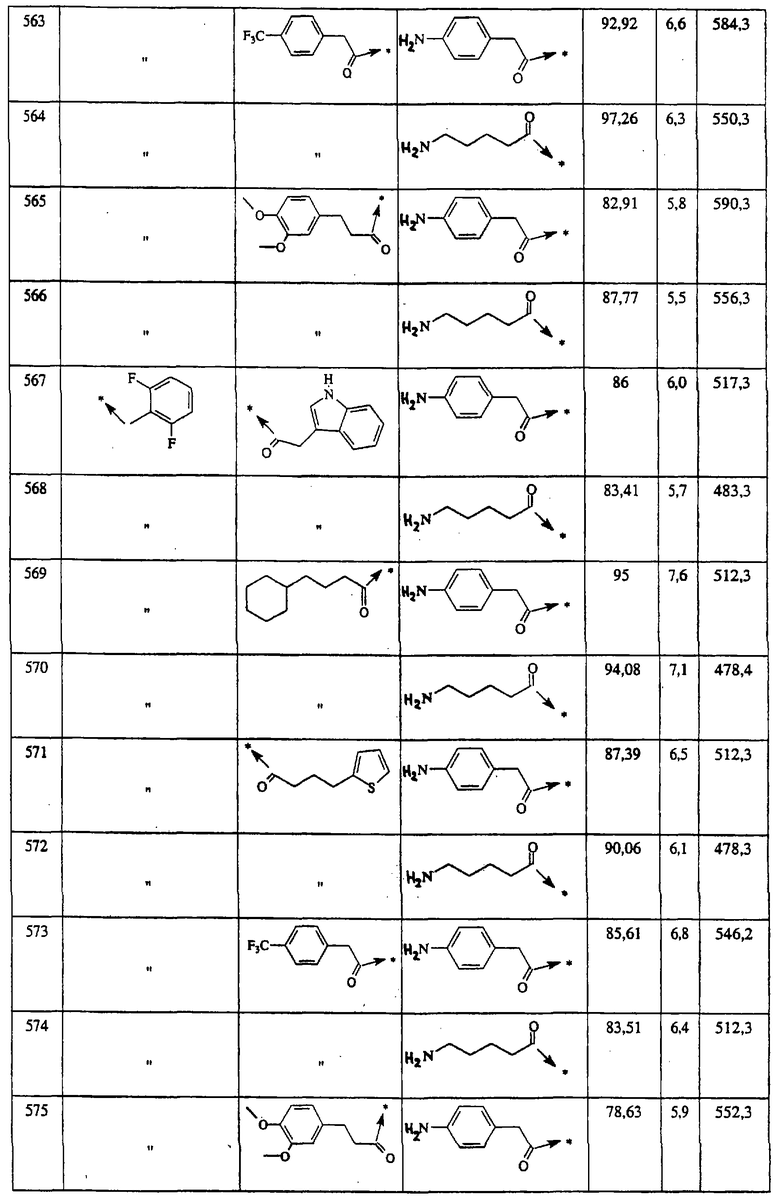
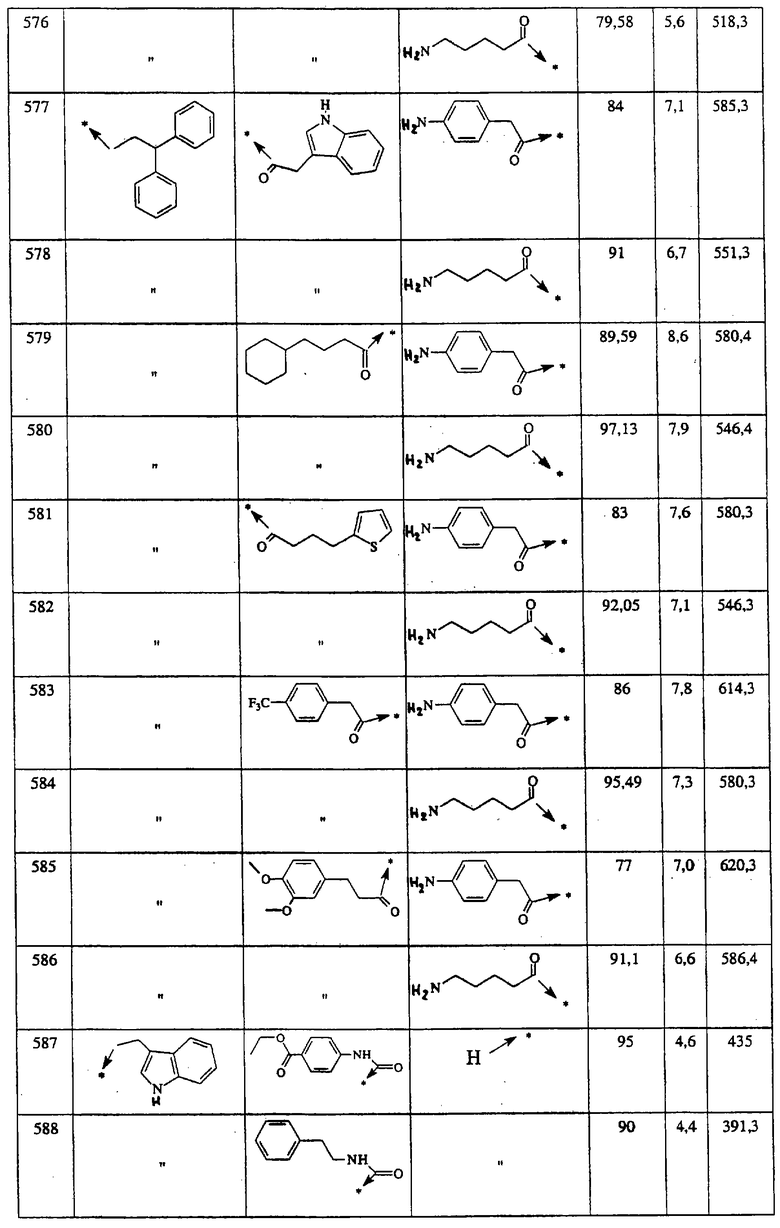

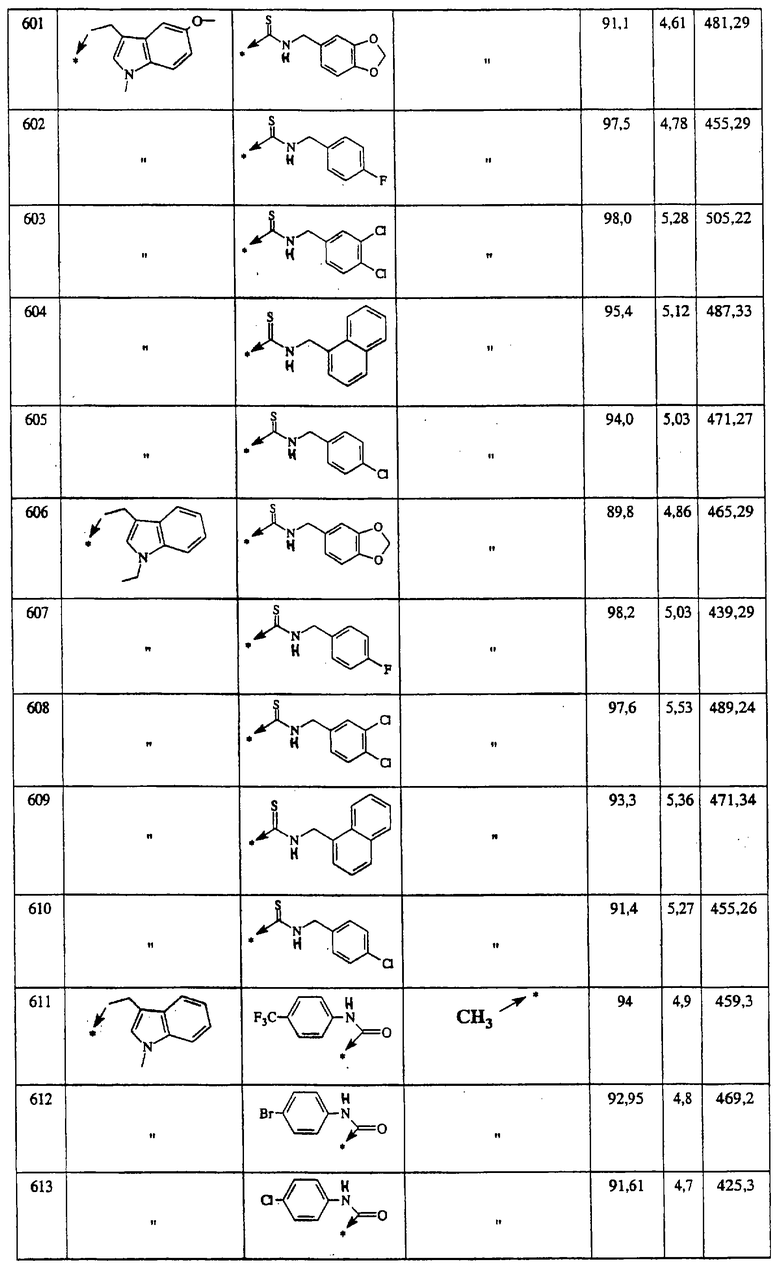
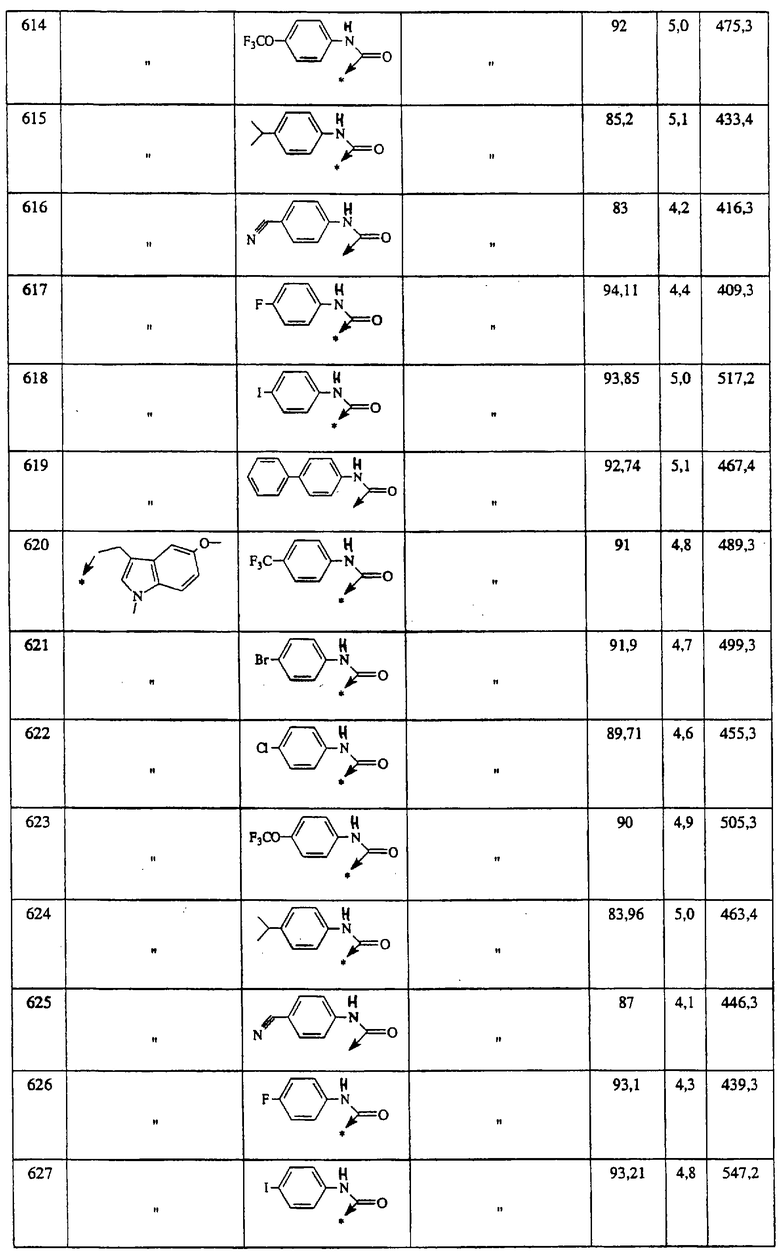
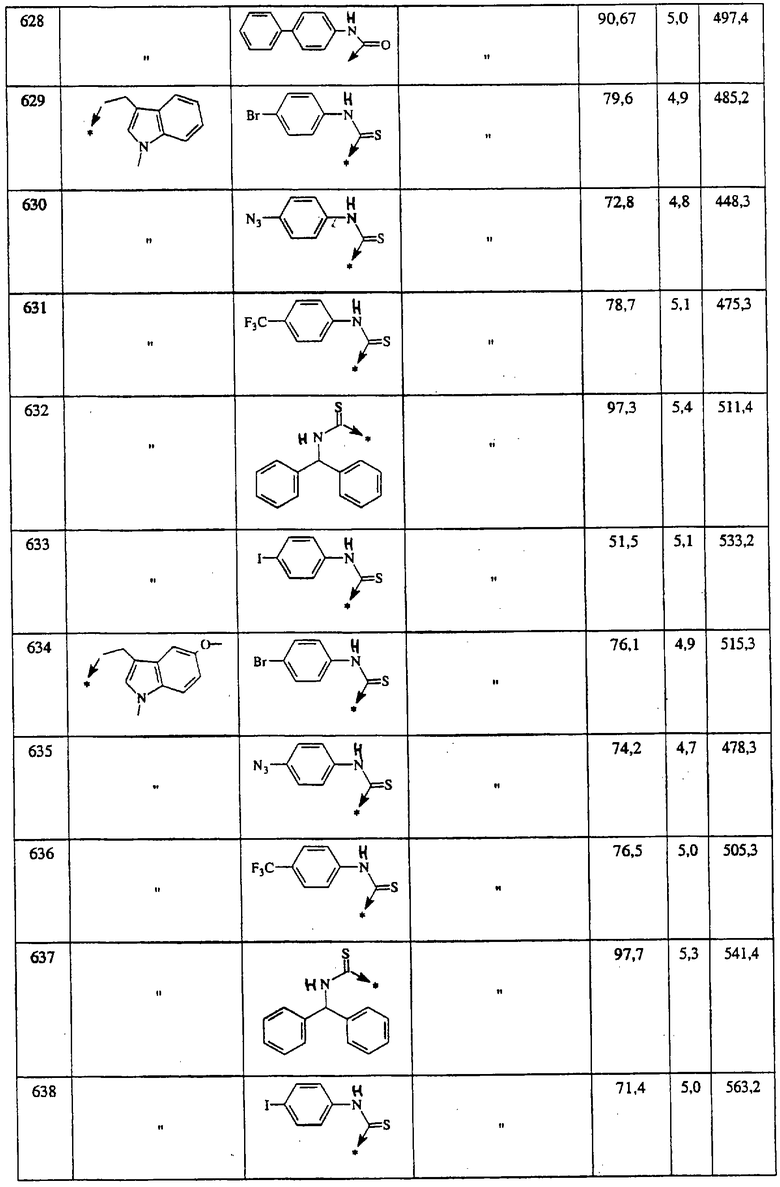
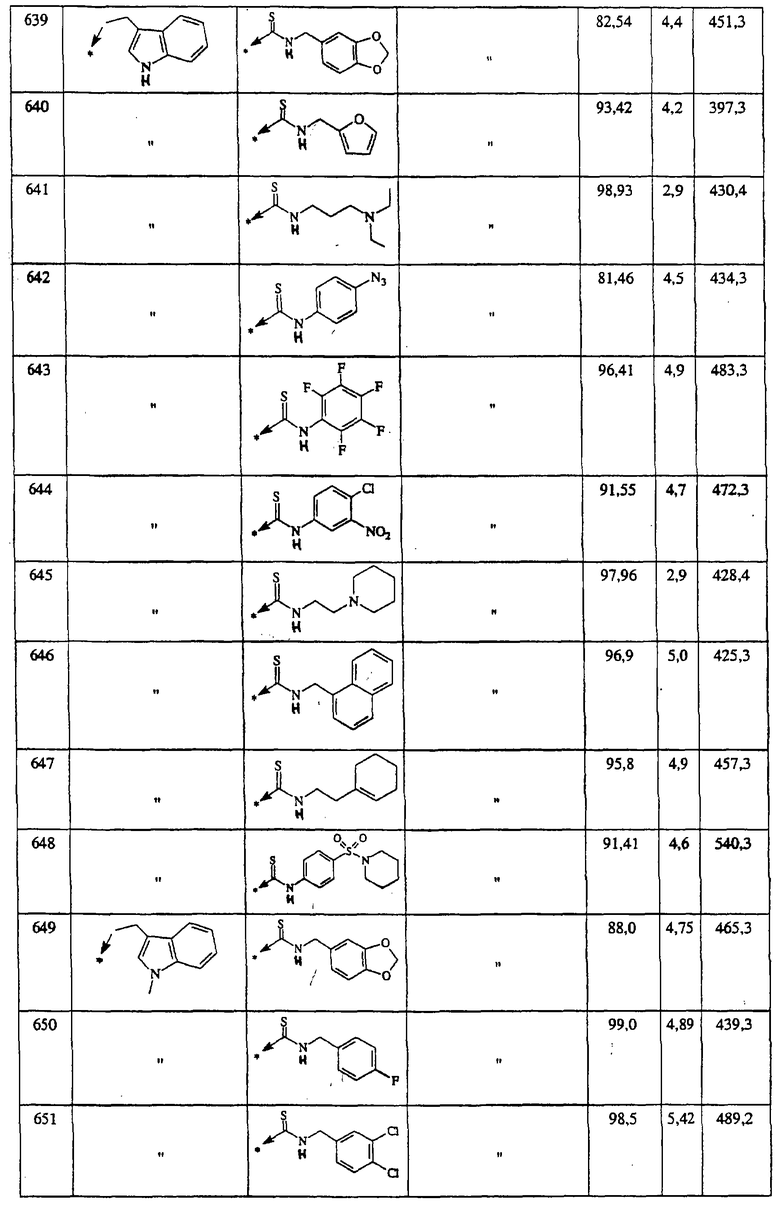
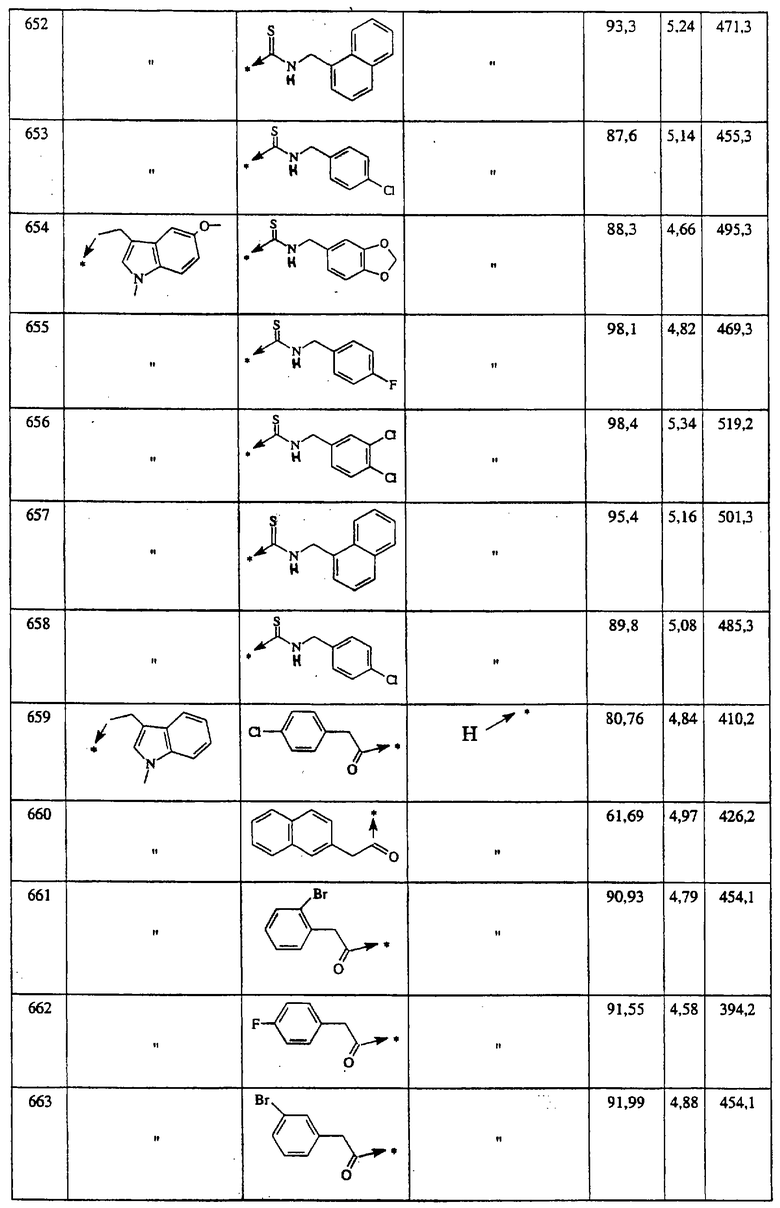
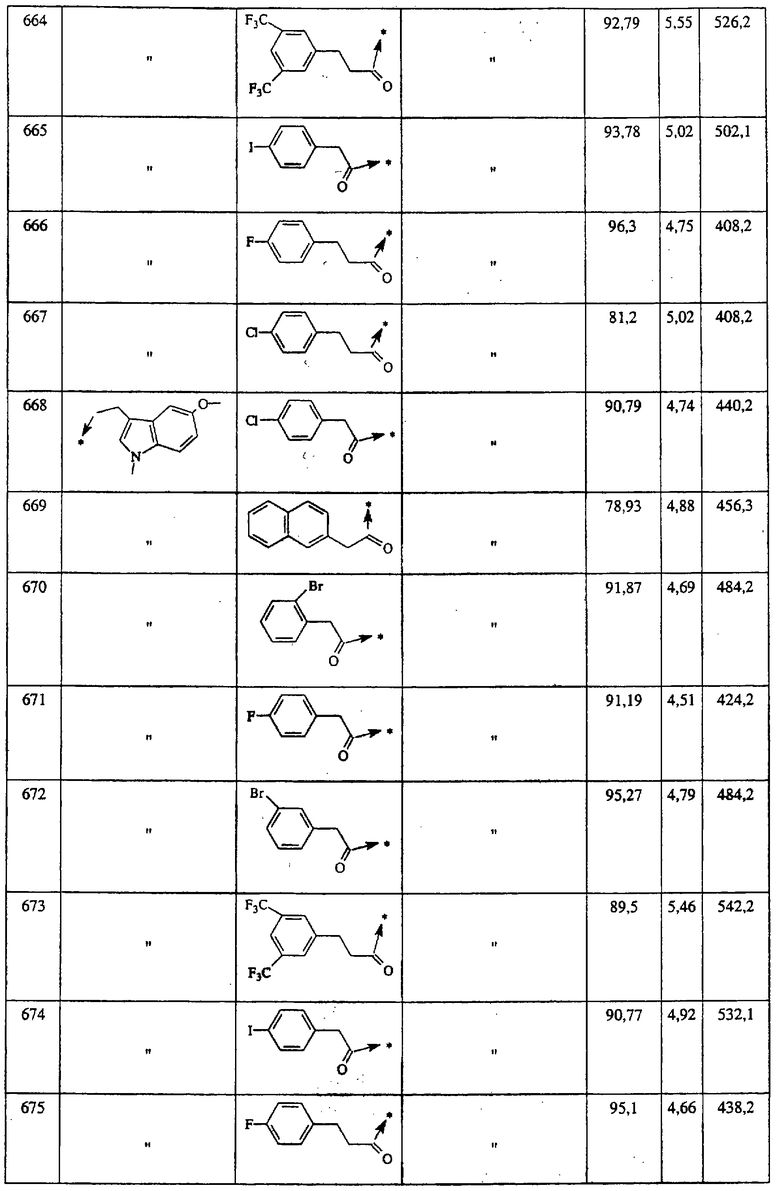
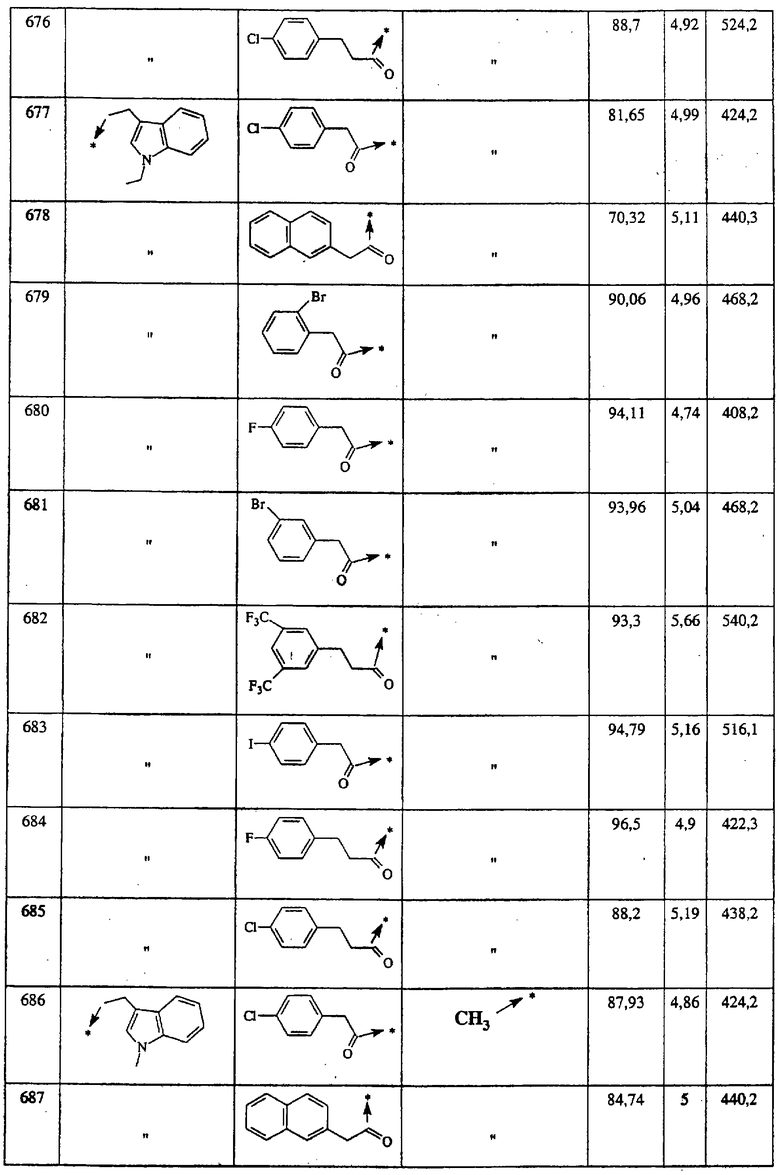
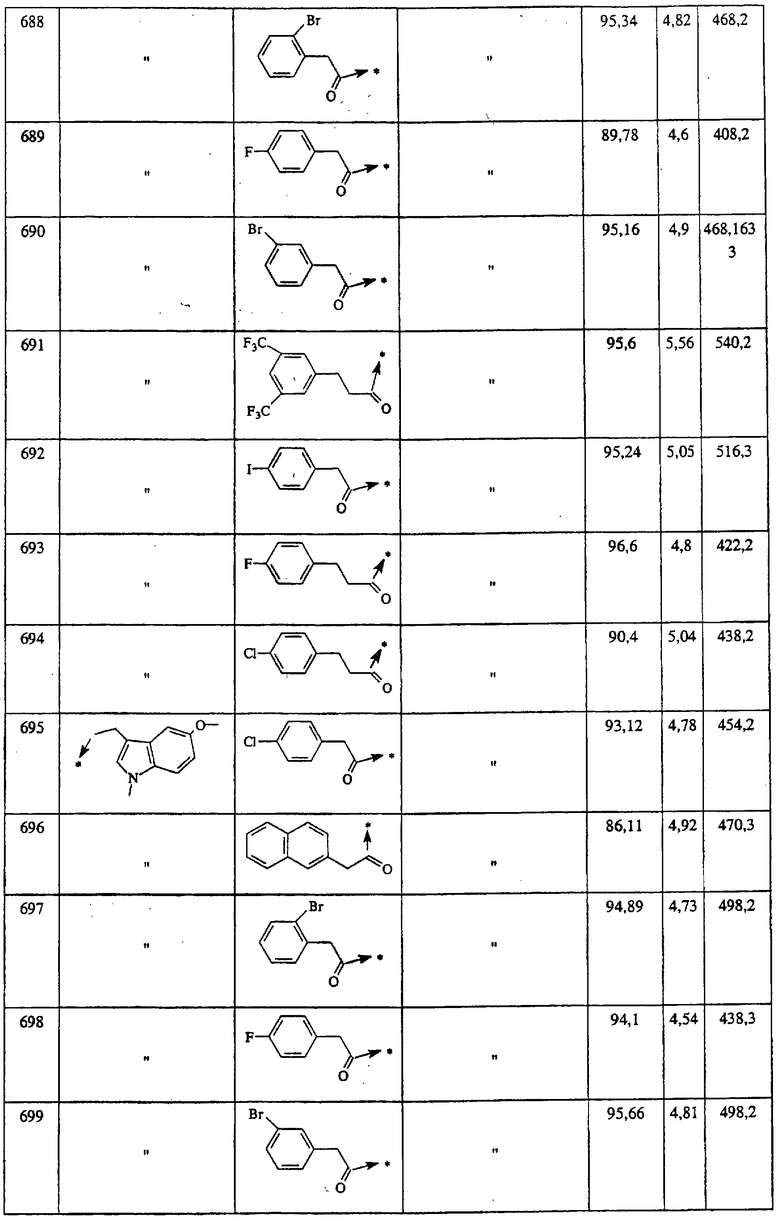
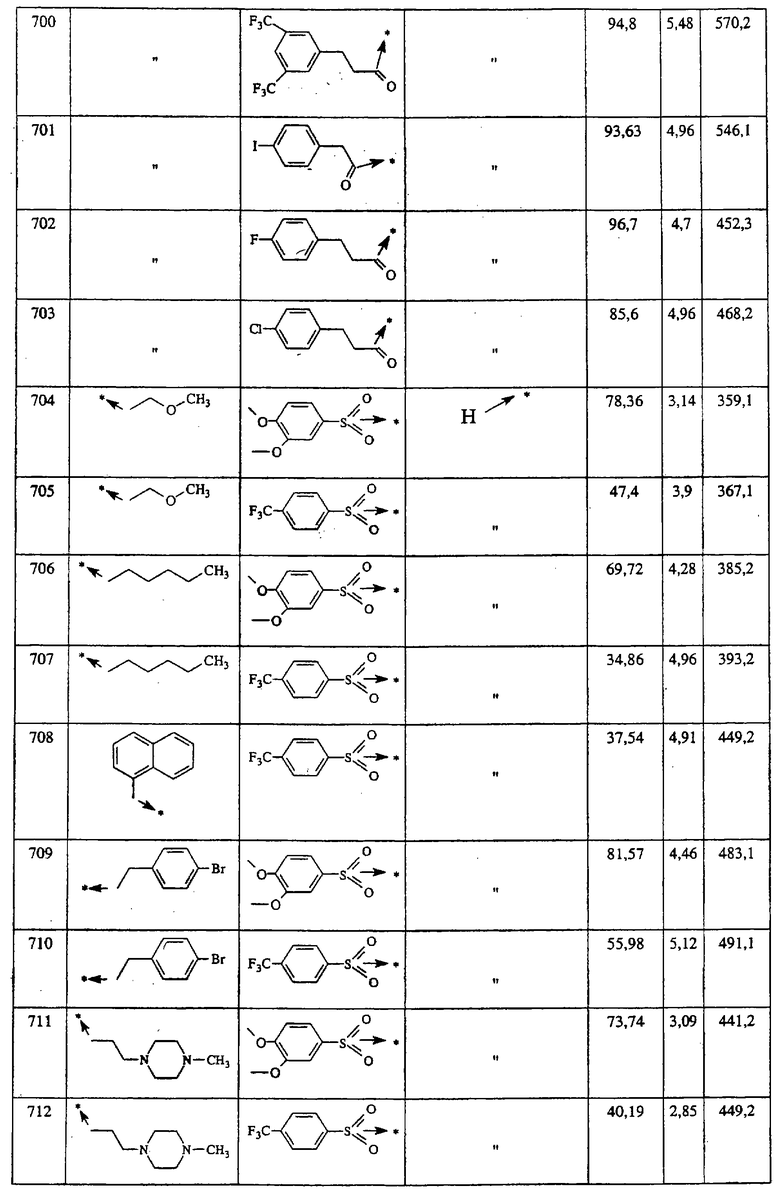
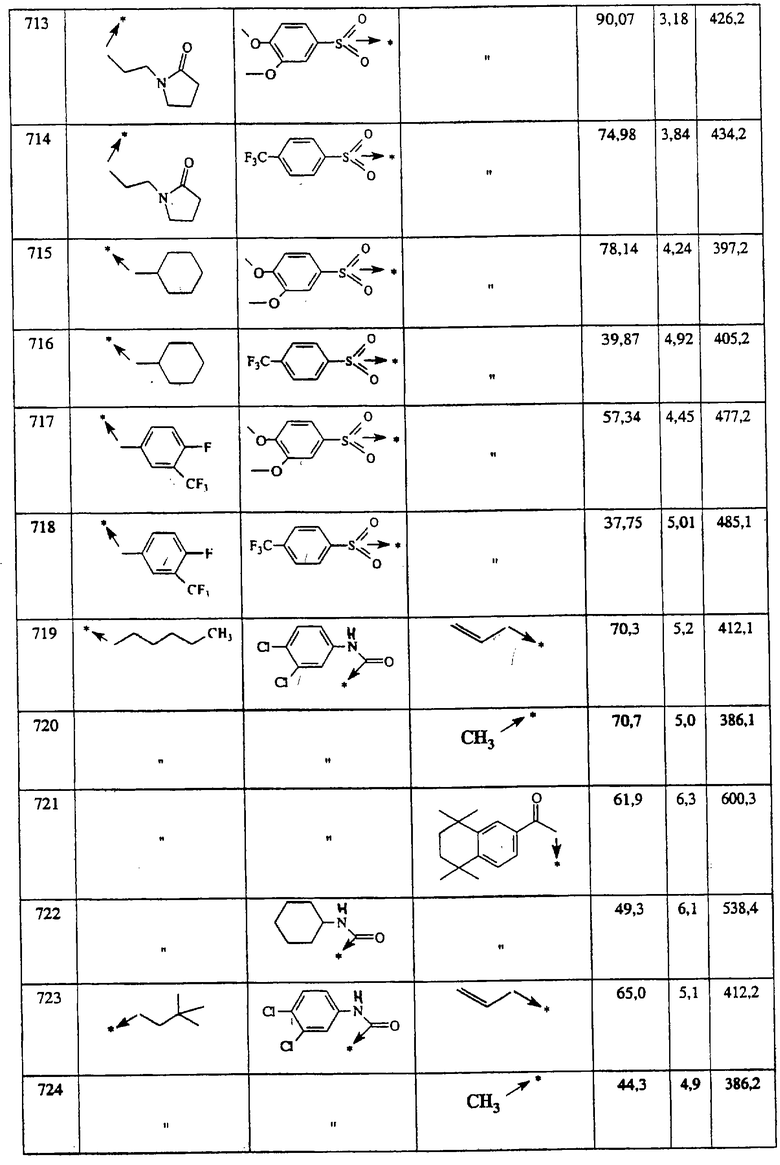
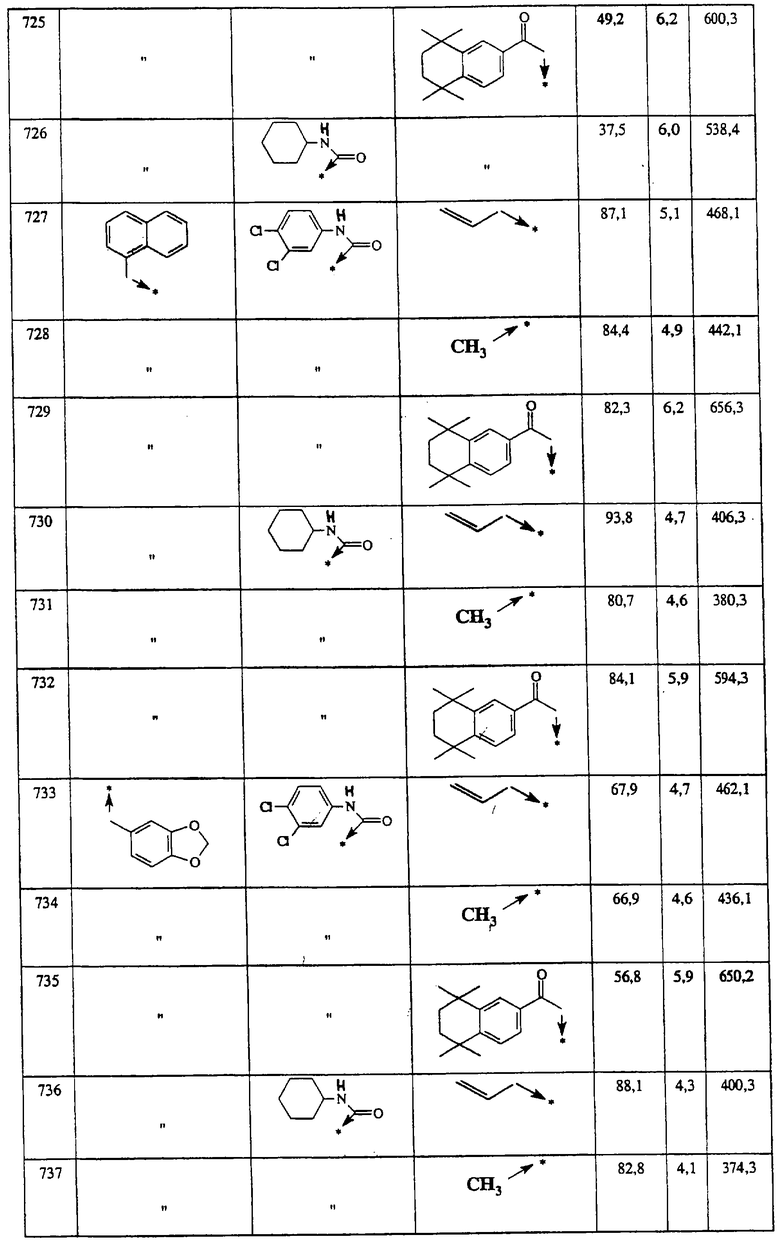
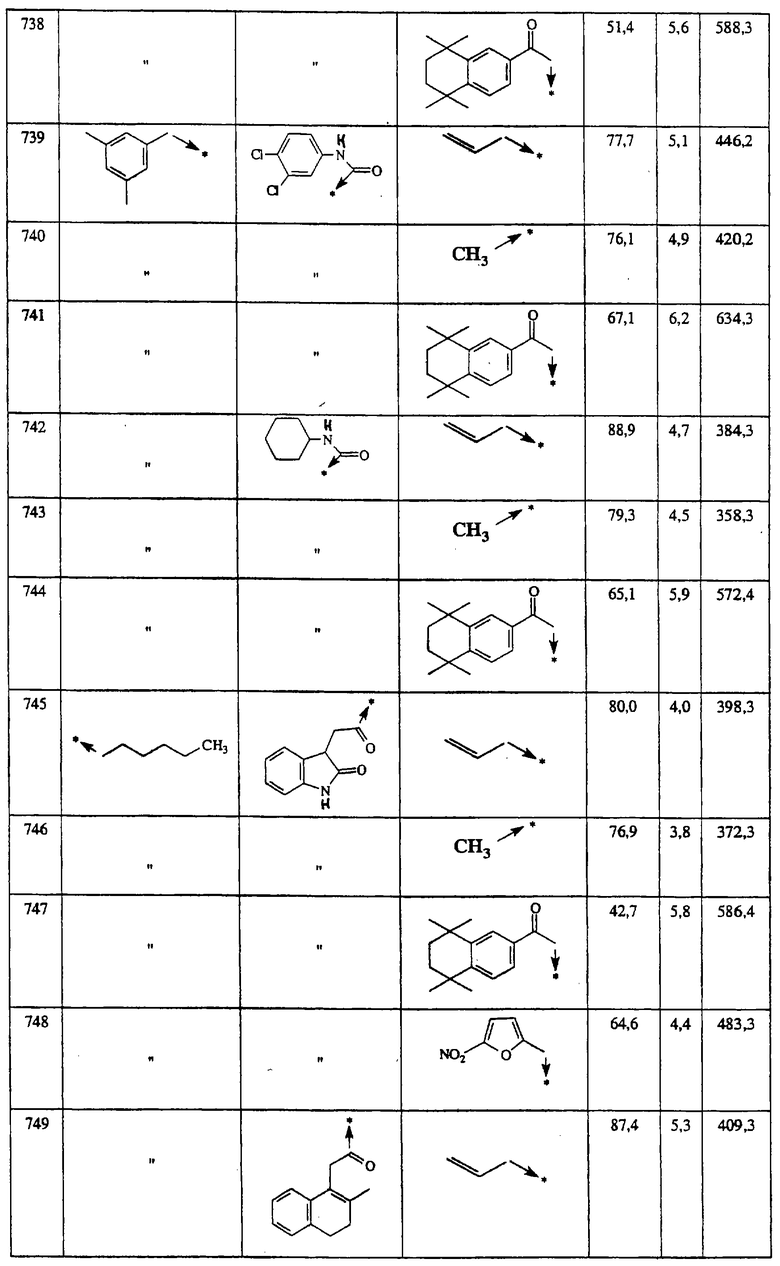
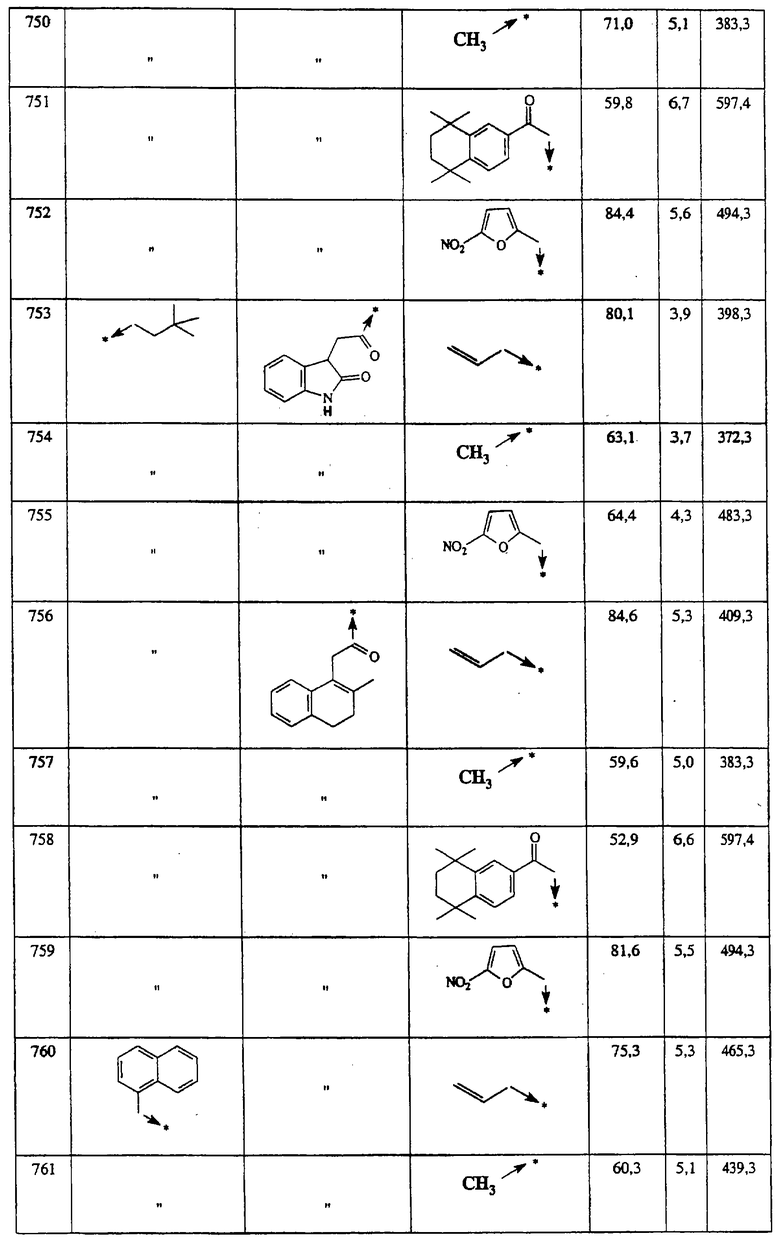
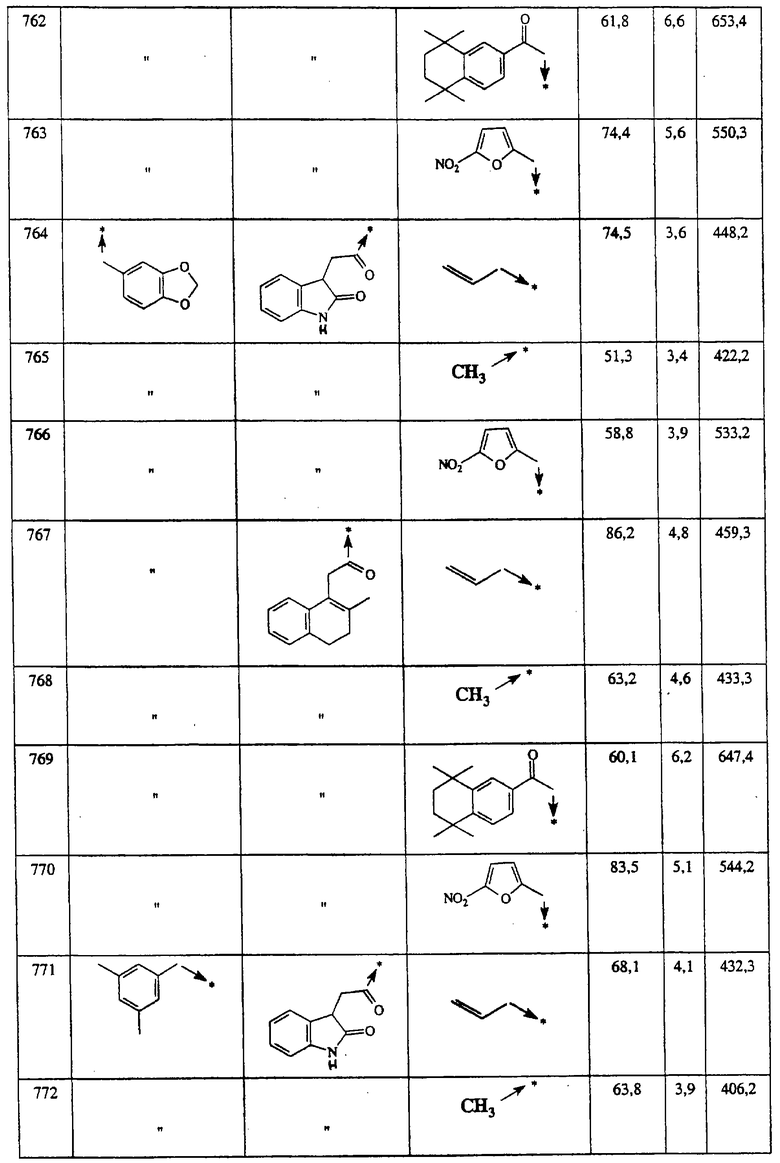
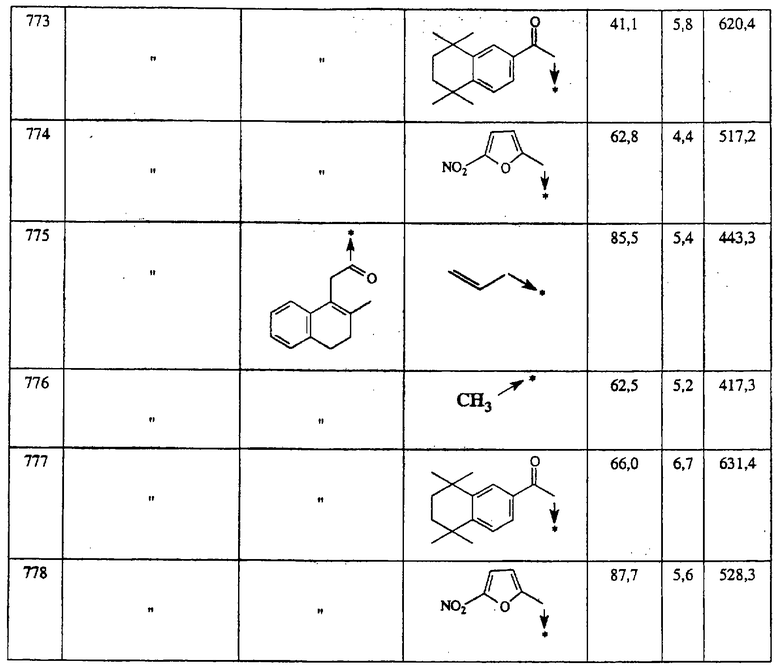
Фармакологическое исследование
Соединения по настоящему изобретению испытаны в отношении их сродства к разным подтипам рецепторов соматостатина описанными ниже способами.
Исследование сродства к подтипам рецепторов соматостатина человека
Сродство соединения по данному изобретению к подтипам рецепторов соматостатина 1-5 (соответственно sst1, sst2, sst3, sst4 и sst5) определяют, измеряя ингибирование связывания [125I-Tyr11] SRIF-14 с трансфецированными клетками яичника китайского хомячка СНО-К1.
Ген рецептора sst1 соматостатина человека клонируют в форме геномного фрагмента. Сегмент PstI-XmnI длиной 1,5 т.п.о., содержащий 100 п.о. нетранскрибированной 5'-концевой области, все 1,17 т.п.о. кодирующей области и 230 п.о. нетранскрибированной 3'-концевой области, модифицируют, добавляя линкер BglII. Полученный фрагмент ДНК субклонируют в сайте BamHI плазмиды pCMV-81, получая экспрессирующую плазмиду у млекопитающих (предоставлена доктором Грэмом Беллом, Чикагский университет). Клонированную линию клеток, устойчиво экспрессирующую рецептор sst1, получают трансфекцией клеток СНО-К1 (АТСС), выполняя копреципитацию фосфатом кальция. Плазмиду pRSV-neo (АТСС) используют в качестве селектирующего маркера. Клонированные линии клеток селектируют в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), с последующим клонированием кольцевых молекул и размножением в культуре.
Ген рецептора sst2 соматостатина человека, выделенный в форме геномного фрагмента ДНК BamHI-HindIII длиной 1,7 т. п.о. и субклонированный в плазмидном векторе pGEM3Z (Promega), предоставлен доктором Г. Беллом (Чикагский университет). Для создания экспрессирующего вектора в клетках млекопитающего фрагмент BamHI-HindIII длиной 1,7 т.п.о. вводят в сайты рестрикции эндонуклеаэы, совместимые с плазмидой pCMV5. Клонированную линию клеток получают трансфекцией клеток СНО-К1, выполняя копреципитацию фосфатом кальция. Плазмиду pRSV-neo используют в качестве селектирующего маркера.
Рецептор sst3 выделяют в виде геномного фрагмента, при этом полная кодирующая последовательность находится во фрагменте NcoI-HindIII длиной 2,4 т.п.о. Для создания экспрессирующей плазмиды в клетках млекопитающего pCMV-h3 фрагмент BamHI-HindIII длиной 2,0 т.п.о. вставляют в сайт EcoR1 вектора pCMV после модификации концов и добавления линкеров EcoR1. Клонированную линию клеток, устойчиво экспрессирующую рецептор sst3, получают трансфекцией клеток СНО-К1 (ATCC), выполняя копреципитацию фосфатом кальция. Плазмиду pRSV-neo (ATCC) используют в качестве селектирующего маркера. Клонированные линии клеток селектируют в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), с последующим клонированием кольцевых молекул и размножением в культуре.
Экспрессирующая плазмида рецептора sst4 человека pCMV-HX предоставлена доктором Грэмом Беллом (Чикагский университет). Указанный вектор содержит геномный фрагмент, кодирующий рецептор sst4 человека NheI-Nhel длиной 1,4 т.п.о., содержащий 456 п.о. нетранскрибированной 5'-концевой области и 200 п.о. нетранскрибированной 3'-концевой области, который клонирован в сайтах XbaI/EcoR1 плазмиды PCMV-HX. Клонированную линию клеток, устойчиво экспрессирующую рецептор sst4, получают трансфекцией клеток СНО-К1 (ATCC), выполняя копреципитацию фосфатом кальция. Плазмиду pRSV-neo (ATCC) используют в качестве селектирующего маркера. Клонированные линии клеток селектируют в среде RPMI 1640, содержащей 0,5 мг/мл G418 (Gibco), с последующим клонированием кольцевых молекул и размножением в культуре.
Ген, соответствующий рецептору sst5 человека, полученный полимеразной реакцией синтеза цепи (PCR) с использованием геномного λ клона в качестве зонда, предоставлен доктором Грэмом Беллом (Чикагский университет). Полученный при помощи PCR фрагмент длиной 1,2 т.п.о. содержит 21 пару оснований нетранскрибированной 5'-концевой области, всю кодирующую область и 55 и.о. нетранскрибированной 3'-концевой области. Полученный клон вводят в сайт EcoR1 плазмиды pBSSK(+). Вставку выделяют в форме фрагмента HindIII-Xbal длиной 1,2 т.п.о. для субклонирования в экспрессирующем векторе млекопитающих pCVM5. Клонированные линии клеток, устойчиво экспрессирующие рецептор sst5, получают трансфекцией клеток СНО-К1 (АТСС), выполняя копреципитацию фосфатом кальция. Плазмиду pRSV-neo (АТСС) используют в качестве селектирующего маркера. Клонированные линии клеток селектируют в среде RPMI 1640, содержащей 0,5 мг/мл G416 (Gibco), с последующим клонированием кольцевых молекул и размножением в культуре.
Клетки СНО-К1, устойчиво экспрессирующие один из рецепторов sst человека, культивируют в среде RPMI 1640, содержащей 10% фетальную телячью сыворотку и 0,4 мг/мл генетицина. Клетки собирают при помощи EDTA в количестве 0,5 мМ и центрифугируют с ускорением 500 g в течение примерно 5 минут при температуре около 4°С. Осадок снова суспендируют в 50 мМ трис-буфера при рН 7,4 и дважды центрифугируют с ускорением 500 g в течение 5 минут при температуре около 4°С. Клетки лизируют ультразвуком и центрифугируют с ускорением 39000 g в течение примерно 10 минут при 4°С. Осадок снова суспендируют в том же буфере и центрифугируют с ускорением 50000 g в течение примерно 10 минут при температуре около 4°С и клеточные мембраны, полученные в осадке, хранят при -80°С.
Испытания по конкурентному ингибированию связывания с [125I-Tyr11] SRIF-14 выполняют с использованием дублируемых образцов на 96-луночных полипропиленовых планшетах. Клеточные мембраны (10 мкг белка/лунку) инкубируют с [125I-Tyr11]SRIF-14 (0,05 нМ) в течение примерно 60 минут при температуре около 37°С в 50 мМ буфера HEPES (рН 7,4), содержащего 0,2% альбумин бычьей сыворотки (BSA), 5 мМ MgCl3, 200 ед/мл тразилола, 0,02 мг/мл бацитрицина и 0,02 мг/мл фенилметилсульфонилфторида.
Связанный [125I-Tyr11]SRIF-14 отделяют от свободного [125I-Tyr11]SRIF-14 фильтрацией через фильтровальные пластины из стекловолокна GF/C (Unifilter, Packard), предварительно пропитанные 0,1% полиэтиленимина (P.E.I.), при помощи фильтрующего устройства Filtermate 196 (Packard). Фильтры промывают 50 мМ буфера HEPES при температуре около 0-4°С в течение примерно 4 секунд и счетчиком определяют их радиоактивность (Packard Top Count).
Для определения специфического связывания из общего значения связывания вычитают величину неспецифического связывания (определяемого в присутствии 0,1 мкМ SRIF-14). Данные, относящиеся к связыванию, анализируют в компьютере методом нелинейной регрессии (MDL) и определяют значения констант ингибирования (Ki).
Агонистический или антагонистический характер соединения по настоящему изобретению определяют при помощи описанного ниже испытания.
Функциональное испытание: ингибирование продуцирования внутриклеточного сАМР
Клетки СНО-К1, экспрессирующие подтипы рецепторов соматостатина человека (SRIF-14), культивируют на 24-луночных планшетах в среде RPMI 1640, содержащей 10% фетальную телячью сыворотку и 0,4 мг/мл генетицина. Среду меняют в день, предшествующий началу эксперимента.
Клетки в количестве 105 клеток/лунку дважды промывают 0,5 мл свежей среды RPMI с 0,2% BSA, содержащей 0,5 мМ 3-изобутил-1-метилксантина (IBMX), и инкубируют в течение примерно 5 минут при температуре около 37°С.
Продуцирование циклического аденозинмонофосфата (АМР) стимулируют, добавляя 1 мМ форсколина (FSK) в течение 15-30 минут при температуре около 37°С.
Ингибирующее действие соматостатина соединения-агониста измеряют, производя одновременное добавление FSK (1 мкМ), SRIF-14 (от 10-12 до 10-6 M) и испытуемого соединения (от 10-10 до 10-5 М).
Антагонистическое действие соединения измеряют, производя одновременное добавление FSK (1 мкМ), SRIF-14 (от 1 до 10 нМ) и испытуемого соединения (от 10-10 до 10-5 М).
Реакционную среду удаляют и добавляют 200 мл 0,1 н. раствора HCl. Количество сАМР измеряют при помощи радиоиммунологического испытания (набор FlashPlate SMP001A, New England Nuclear).
Результаты
Испытания, выполненные описанными выше способами, показывают, что продукты общей формулы (I), представленные в настоящей заявке, обладают хорошим сродством по крайней мере к одному из подтипов рецепторов соматостатина, при этом константа ингибирования Кi ниже микромолярного значения для некоторых испытанных соединений.
Фармацевтическая композиция
Способом, общепринятым в фармакологии, готовят композицию для инъекций, имеющую следующий состав:
Изобретение относится к новым производным 4-аминопиперидинов общей формулы I

где R1 - (C1-С6)алкил, -(CH2)m-Y-Z11 или -(CH2)m-Z12, где Z11-(C1-С6)алкил, Z12-бисфенил, (C3-С7)циклоалкил, (C3-С7)гетероциклоалкил с 1 или 2 гетероатомами, выбранными из N или О, возможно замещенный фенил, нафтил, возможно замещенный (С5-С9)гетероарил, где гетероатомы выбраны из N, или Z12 - 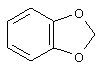 , Y-О, или R1 -
, Y-О, или R1 - 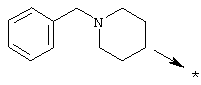
R2 - -C(Y)NHX1, -С(O)Х2 или SO2Х3, R3-Н, (C1-С4)алкил, (С2-С4)алкенил, возможно замещенный гетероарилалкил, или -C(Y)-NHX1, -(СН2)n-С(O)Х2, или SO2Х3, где X1-Х3, Y имеют различные значения. Описаны также способы получения указанных веществ синтезом в жидкой и твердой фазе. Данные продукты, обладающие хорошим сродством к определенным подтипам рецепторов соматостатина, позволяют эффективно лечить патологические состояния или заболевания, обусловленные одним (или несколькими) рецепторами соматостатина. 6 н. и 8 з.п. ф-лы, 5 табл.
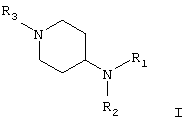
в рацемической, энантиомерной форме или во всех комбинациях указанных форм, где
R1 означает (C1-С6)алкил, радикал -(CH2)m-Y-Z11 или радикал -(СН2)m-Z12, в котором
Z11 означает (C1-С6)алкил;
Z12 означает бисфенил, (C3-С7)циклоалкил, необязательно замещенный (С3-С7)гетероциклоалкил, имеющий 1 или 2 гетероатома, где гетероатомами являются азот или кислород, необязательно замещенный фенил, нафтил, необязательно замещенный (C5-С9) гетероарил, где гетероатом представлен азотом;
или Z12 означает
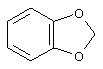 ,
,
Y означает атом кислорода, или
R1 означает радикал формулы
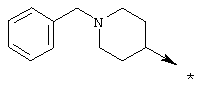
R2 означает радикал формулы -C(Y)NHX1, -С(O)Х2 или SO2Х3,
где
Х1 означает (C1-С8)алкил или -(CH2)pZ22, в котором
Z22 означает циклогексенил, бисфенил, (C3-С7)циклоалкил, (C3-С7) гетероциклоалкил, имеющий 1 или 2 гетероатома, где гетероатомами являются азот или кислород, моно- или диалкиламино, -С(O)-O-алкил, необязательно замещенный фенил, нафтил или необязательно замещенный гетероарил, имеющий 1 или 2 гетероатома, где гетероатомами являются азот или кислород;
или Z22 означает радикал формулы

Y означает атом кислорода или серы;
Х2 означает (C1-С10)алкил, (C2-С8)алкинил, радикал формулы -(CH2)m-W-(CH2)q-Z23 или -(CH2)p-U-Z24, где
W означает SO2;
U означает ковалентную связь;
Z23 означает фенил;
Z24 означает необязательно замещенный (C3-С7)циклоалкил, необязательно замещенный фенил, нафтил, необязательно замещенный гетероарил, имеющий 1 или 2 гетероатома, где гетероатомами являются азот или сера;
или Z24 означает радикал формулы

или Х2 означает

где защитная группа (PG) является Н или третбутилоксикарбонилом;
Х3 означает радикал -(CH2)pZ25, где
Z25 означает необязательно замещенный фенил;
R3 означает атом водорода, (C1-С4)алкил, (C2-С4)алкенил, необязательно замещенный гетероарилалкил или радикал формулы -C(Y)-NHX1, -(CH2)n-C(O)X2 или SO2Х3, где Х1 означает радикал -(CH2)pZ22, в котором Z22 означает необязательно замещенный (C6-С10)арил; Х2 означает (C1-С10)алкил или (C2-С10)алкенил, винил, замещенный фенилом, в котором фенил необязательно замещен одним или более атомами галогена, радикал формулы -(CH2)m-W-(CH2)q-Z23 или -(CH2)p-U-Z24, где W означает SO2; U означает ковалентную связь или атом кислорода; Z23 означает арил; Z24 означает алкил, (C3-С7) циклоалкил, (С3-С7) гетероциклоалкил, бисфенил, амино, моно- или диалкиламино, необязательно замещенный арил или необязательно замещенный гетероарил; или Х2 означает радикал формулы
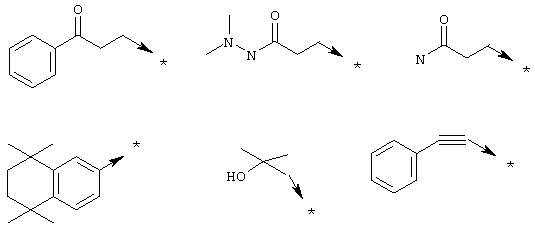
Х3 означает (C1-С10) алкил, винил, замещенный фенилом (фенил может быть также необязательно замещен), CF3 или -(CH2)pZ25, где Z25 означает необязательно замещенный (C6-С10) арил или необязательно замещенный (C3-С6) гетероарил, имеющий 1 или 2 гетероатома, выбранных из серы, кислорода и азота;
n равно р и является целым числом от 0 до 4;
m является целым числом от 1 до 6;
р является целым числом от 0 до 6;
q является целым числом от 0 до 2;
или их аддитивные соли с фармацевтически приемлемыми минеральными или органическими кислотами.
i) заместитель или заместители, замещающие арил, представленный Z12, и гетероарил, представленный Z12, независимо выбирают из фтора, хлора, брома, иода, алкила, алкокси, алкилтио, -CF3, -OCF3, фенила, фенокси, аминосульфонила;
ii) заместитель или заместители, замещающие гетероциклоалкильный радикал, представленный Z12, независимо выбирают из окси- и алкильных радикалов;
iii) заместитель или заместители, замещающие арильные и гетероарильные радикалы, представленные Z22, независимо выбирают из фтора, хлора, брома, иода, алкила, алкенила, алкокси, алкилтио, CF3, ОСРз, нитро, циано, азидо, аминосульфонила, пиперидиносульфонила, моно- или диалкиламино, -С(O)-O-алкила, -С(O)-алкила или фенила, фенокси, фенилтио, бензилокси, причем фенильный радикал может быть также замещен;
iv) заместитель или заместители, замещающие арильные радикалы, представленные Z23 и Z24, циклоалкил или гетероарил, представленный Z24, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, OCHF2, SCF3, нитро, циано, азидо, гидрокси, -С(O)O-алкил, -O-С(O)-алкил, -NH-С(O)-алкил, алкилсульфонил, моно- или диалкиламино, амино, аминоалкил, пирролил, пирролидинил или фенил, фенокси, фенилтио, бензил, бензилокси, причем арильный радикал может быть необязательно замещен одним или несколькими алкильными, CF3 или галогенрадикалами;
v) заместитель или заместители, замещающие арильные или гетероарильные радикалы, представленные Z25, независимо выбирают из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, OCF3, нитро, циано, -NH-С(O)-алкил, алкилсульфонил, амино, моно- и диалкиламино, фенил, пиридино;
vi) заместитель или заместители, замещающие гетероарилалкильный радикал, представленный R3, независимо выбирают из радикалов, включающих фтор, хлор, бром или нитро.
Z12 означает бисфенил, (С3-С7)циклоалкил, необязательно замещенный (C3-С7)гетероциклоалкил или фенил или гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси;
или Z12 означает

в радикале R2
Z22 означает циклогексенил, бисфенил, (C3-С7)циклоалкил, (C3-С7)гетероциклоалкил, моно- или диалкиламино, -С(O)-O-алкил, фенил или гетероарил, необязательно замещенные одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(O)-O-алкил, -С(O)-алкил или фенил;
или Z22 означает радикал формулы
 б
б
Z24 означает циклогексенил, бисфенил, (С3-С7)циклоалкил, необязательно замещенный аминоалкилом, либо фенильный или гетероарильный радикал, необязательно замещенные одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, SCF3, гидрокси, -С(O)-O-алкил, моно- или диалкиламино, амино;
или Z24 означает радикал формулы

Z25 означает фенильный радикал, необязательно замещенный одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3;
В радикале R3
Z22 означает арильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенилом, причем фенильный радикал, в свою очередь, необязательно замещен одним или несколькими галогенами, или радикал -(CH2)p-U-Z24, где
Z24 означает алкил, (C3-С7)циклоалкил, (C3-С7)гетероциклоалкил, бисфенил, амино, моно- или диалкиламино, арил или гетероарил, необязательно замещенные одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, гидрокси, CF3, нитро, амино, моно- и диалкиламино, пирролил;
или Х2 означает радикал формулы
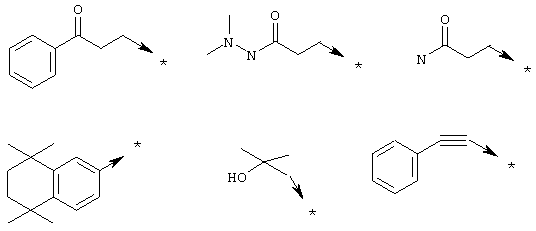
Z25 означает фенил, нафтил или гетероарил, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-С(O)-алкил, моно- и диалкиламино.
Z11 означает (C1-С6)алкил;
Z12 означает нафтил, морфолино, бисфенил, пирролидинил, замещенный оксирадикалом, или фенильный, пиперазинильный, пиридинильный и индолильный радикалы, которые необязательно замещены одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих бром, фтор, хлор, алкил, алкокси, -CF3, -OCF3;
или Z12 означает

Y означает атом кислорода;
или R1 означает радикал нижеследующей формулы:

X1 означает (C1-С10)алкил с линейной или разветвленной цепью или радикал -(CH2)pZ22, в котором
Z22 означает циклогексил, циклогексенил, бисфенил, морфолино, пиперидино, моно- или диалкиламино, -С(O)-O-алкил или фенил, нафтил или фурил, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, алкилтио, CF3, -OCF3, нитро, циано, азидо, пиперидиносульфонил, -С(O)-O-алкил, -С(O)-алкил или фенил;
или Z22 означает радикал формулы

Х2 означает алкил, алкинил, радикал -(CH2)m-W-(CH2)q-Z23 или -(CH2)pZ24, в котором
W означает SO2;
Z23 означает фенильный радикал;
Z24 означает циклогексенил, бисфенил, циклогексил, необязательно замещенный аминоалкилом, либо фенильный, нафтильный, бензотиенильный, тиенильный или индолильный радикал, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей фтор, хлор, бром, иод, алкил, алкокси, -CF3, -OCF3, -SCF3, гидрокси, -O-С(O)-алкил, -NH-С(O)-алкил, моно- или диалкиламино, амино;
или
Z24 означает радикал формулы

или Х2 означает
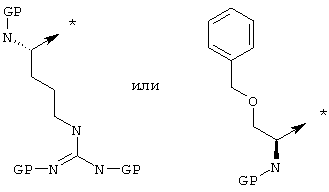
Х3 означает радикал -(CH2)pZ25, в котором Z25 является фенильным радикалом, необязательно замещенным одним или несколькими одинаковыми или разными радикалами, выбираемыми из алкокси и CF3.
X1 означает радикал -(СН2)рZ22, в котором
Z22 означает фенильный или нафтильный радикал, необязательно замещенный одним или несколькими радикалами, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, фенокси;
Х2 означает винильный радикал, замещенный фенильным радикалом, который, в свою очередь, необязательно замещен одним или несколькими галогенами, или радикал -(СН2)р-U-Z24, где
Z24 означает алкил, циклогексил, тетрагидрофурил, бисфенил, амино, моно- или диалкиламино либо фенил, индолил, тиенил, пиридинил, бензотиенил и фурил, необязательно замещенный одним или несколькими радикалами, выбираемыми из группы, включающей алкокси, бром, хлор, фтор, амино, моно- и диалкиламино, нитро, гидрокси, пирролил;
или Х2 означает радикал формулы

Х3 означает (C1-С10)алкильный радикал с линейной или разветвленной цепью, винильный радикал, замещенный фенилом, CF3 или радикал -(CH2)pZ25, в котором
Z25 означает фенильный, нафтильный, тиенильный, пиразолильный или тиазолильный радикал, необязательно замещенный одним или несколькими заместителями, независимо выбираемыми из радикалов, включающих фтор, хлор, бром, иод, алкил, алкокси, CF3, нитро, -NH-C(O)-алкил, моно- и диалкиламин.
Y означает S;
X1 означает фенильный радикал, необязательно замещенный одним или несколькими азидорадикалами;
Х2 означает -(СН2)pZ24, где р равно 1, 2 или 3;
Z24 означает циклогексил, фенил или бензотиенил, необязательно замещенный одним или несколькими радикалами, выбираемыми из фтора, хлора, брома, иода или -CF3.
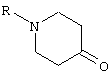
где R означает метильный или Boc радикал, в присутствии амина формулы R1NH2, в которой R1 имеет значения, указанные в п.1, что дает соединение формулы 1
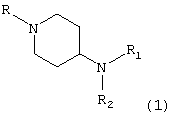
после чего соединение формулы (1) подвергают взаимодействию:
А) с соединением формулы X1NC(Y), где X1 и Y имеют значения, указанные в п.1, что дает соединение формулы (2)
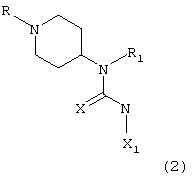
соединение формулы (2) представляет собой соответствующее соединение формулы (I), в которой R3 означает Me или Boc, и, когда R3 означает Boc, обработкой данного соединения кислотой получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
полученное таким образом соединение формулы (I) затем подвергают взаимодействию с соединением формулы X1NC(Y), Х2СО2Н или Х3SO2Cl, в которой X1, Y, Х2 и Х3 имеют значения, указанные в п.1, в результате чего получают соответствующее соединение формулы I, в которой R2 означает радикал формулы -C(Y)NHX1 и R3 соответственно означает радикал -C(Y)NHX1, -C(O)X2 или SO2Х3;
В) или с соединением формулы Х2СО2Н, в которой Х2 имеет значения, указанные в п.1, что дает соединение формулы (3)
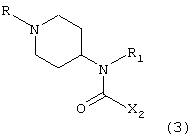
соединение формулы (3) представляет собой соответствующее соединение формулы (I), в которой R3 означает Me или Boc, и, когда R3 означает Boc, обработкой данного соединения кислотой получают соответствующее соединение формулы (I), в которой R3 означает атом водорода,
полученное таким образом соединение формулы (I) затем подвергают взаимодействию с соединением формулы X1NC(Y), Х2СО2Н или Х2SO2Cl, в которой X1, Y, Х2 и Х3 имеют значения, указанные в п.1, в результате чего получают соответствующее соединение формулы I, в которой R2 означает радикал формулы -С(O)Х2 и R3 соответственно означает радикал -C(Y)NHX1, -С(O)Х2 или SO2Х3.
восстановительное аминирование кетонной смолы
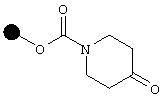
в присутствии амина формулы R1NH2, в которой R1 имеет значения, указанные в п.1, что дает соединение формулы (4)
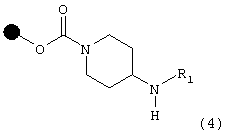
после чего соединение формулы (4) подвергают взаимодействию
A) с соединением формулы X1NC(Y), в которой X1 и Y имеют значения, указанные в п.1, что дает соединение формулы (5)
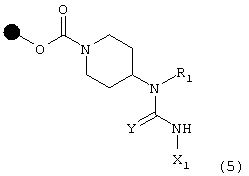
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
B) или с соединением формулы Х3SO2Cl, в которой Х3 имеет значения, указанные в п.1, что дает соединение формулы (6)
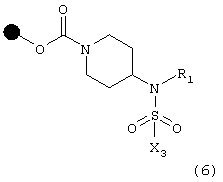
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
C) или с соединением формулы Х2СО2Cl, в которой Х2 имеет значения, указанные в п.1, что дает соединение формулы (7)
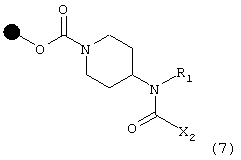
с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода;
D) или с соединением формулы Х2СО2Н, в которой Х2 имеет значения, указанные в п.1, что дает соединение формулы (7), с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I), в которой R3 означает атом водорода.
восстановительное аминирование кетонной смолы
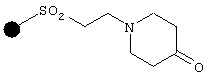
в присутствии амина формулы R1NH2, в которой R1 имеет значения, указанные в п.1, что дает соединение формулы (8)
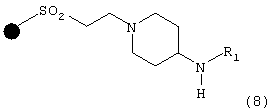
после чего соединение формулы (8) подвергают взаимодействию
A) с соединением формулы X1NC(O), в которой X1 имеет значения, указанные в п.1, что дает соединение формулы (9)

полученное таким образом соединение (9) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет значения, указанные в п.1, и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
B) или с соединением формулы Х2SO2Cl, в которой Х3 имеет значения, указанные в п.1, что дает соединение формулы (10)
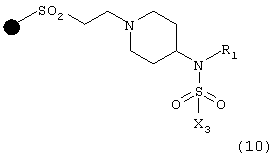
полученное таким образом соединение (10) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет значения, указанные в п.1, и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
С) или с соединением формулы Х2CO2Cl, в которой Х2 имеет значения, указанные в п.1, что дает соединение формулы (11)
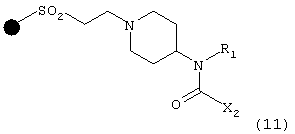
полученное таким образом соединение (11) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет значения, указанные в п.1, и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I);
D) или с соединением формулы Х2СО2Н, в которой Х2 имеет значения, указанные в п.1, что дает соединение формулы (11);
полученное таким образом соединение (11) подвергают взаимодействию с соединением формулы R3Х, в которой R3 имеет значения, указанные в п.1, и Х означает Br или I, с последующим отщеплением смолы, в результате чего получают соответствующее соединение формулы (I).
| Способ получения производных 4-(ароиламино)-пиперидинбутанамида, или их стереоизомеров, или их фармацевтически приемлемых кислотно-аддитивных солей | 1987 |
|
SU1620049A3 |
| WO 9922735, 14.05.1999 | |||
| WO 9844921, 15.10.1998 | |||
| СПОСОБ ОЦЕНКИ КАЧЕСТВА СПЕРМЫ ЖЕРЕБЦОВ ПО УРОВНЮ АКТИВНОСТИ α-АМИЛАЗЫ В СЫВОРОТКЕ КРОВИ | 2020 |
|
RU2751138C1 |
| СТОЛБЧАТЫЕ ЧАСТИЦЫ ОКСИДА ЦИНКА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2530894C2 |
Авторы
Даты
2005-12-20—Публикация
2000-12-13—Подача