Изобретение относится к химической технологии неорганических веществ и материалов.
Известны способы получения ультрадисперсного карбоната кальция СаСО3, основанные на карбонизации водной суспензии гидрооксида кальция Са(ОН)2 [1, 2], однако для проведения таких процессов необходимо использование гидрооксида кальция, который не является природным сырьем и, соответственно, его приготовление требует дополнительных экономических затрат, кроме того, такие способы требуют повышенного расхода двуокиси углерода СО2 ввиду того, что по условиям реакции для образования одного моля СаСО3 требуется 2 моля CO2.
Наиболее близким к предлагаемому изобретению является способ высокоскоростного процесса производства осажденного углекислого кальция с использованием давления проточного СО2, основанный на карбонизации водной суспензии гидрооксида кальция Са(ОН)2 или СаО, проводимой в сосудах высокого давления с механической агитацией и внутренним барботажем СО2 [3]. Однако он требует предварительного получения из природного сырья гидрооксида кальция Са(ОН)2 или СаО, которые применяются в способе в качестве источников ионов кальция, и повышенного расхода углекислого газа, обусловленного сложной схемой химического взаимодействия Са(ОН)2 с CO2, что значительным образом увеличивает себестоимость конечного продукта и технологически усложняет процесс.
Новая техническая задача - повышение простоты и экономичности осуществления способа.
Поставленную задачу решают применением нового способа получения насыщенного водного раствора гидрокарбоната кальция Са(НСО3)2 и ультрадисперсного карбоната кальция СаСО3 из него, включающий карбонизацию водной суспензии исходного сырья в условиях избыточного давления окиси углерода СО2, причем в качестве исходного сырья используют природный карбонат кальция СаСО2 с величиной частиц 10-50 мкм, процесс проводят при Т=0+25°С и избыточном давлении СО2 от 8 до 50 атм без дополнительных стабилизаторов рН среды и далее путем снижения давления до величины атмосферного из получаемого при этом насыщенного водного раствора Са(НСО3)2 осаждают ультрадисперсный СаСО3.
Способ осуществляют следующим образом.
В сосуд высокого давления (автоклав), снабженный механическим агитатором (мешалкой), помещают смесь дистиллированной воды и природного карбоната кальция СаСО3 со средним диаметром частиц 10-50 мкм, в сосуде создается избыточное давление СО2, величиной от 8 до 50 атм, далее, посредствам барботажа СО2 через образовавшуюся суспензию, при этом суспензию подвергают механическому перемешиванию на всем протяжении процесса и обеспечивают поддержание постоянного избыточного давления до установления его постоянства, после чего подачу CO2 прекращают получаемый при этом насыщенный водный раствор Са(НСО3)2, под давлением перекачивают в баллоны высокого давления и используют по назначению, в случае, если конечной целью является получение ультрадисперсного СаСО3, раствор, полученный в сосуде высокого давления (автоклаве), далее подвергают разложению при стравливании избыточного давления CO2 до величины атмосферного, полученную суспензию вторичного СаСО3 выгружают из сосуда, а полученный ультрадисперсный СаСО3 подвергают сушке.
Пример 1.
В сосуд высокого давления объемом 7 л, снабженный механическим перемешивающим устройством (агитатором), заливается 5 литров дистиллированной, либо технической воды и засыпают от 3 до 3,5 кг природного СаСО3 со средним диаметром частиц d=10-50 мкм, определенном из данных по удельной поверхности материала [4], в сосуде создается избыточное давление СО2 от 8 до 50 атм. Водную суспензию выдерживают при избыточном давлении CO2 и постоянном перемешивании до достижения стабилизации давления CO2 в сосуде, при этом протекает процесс превращения нерастворимого СаСО3 в хорошо растворимый Са(НСО3)2 по схеме:

после чего, перемешивание прекращают, а избыточное давление CO2 стравливают до атмосферного, при этом растворенный в воде Са(НСО3)2 разлагается с образованием СаСО3 по схеме:
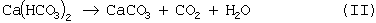
при этом полученный карбонат кальция, образовавшийся в таком процессе характеризуется определенной, как "ультрадисперсная" величиной частиц по данным об удельной поверхности материала [4], на основании чего, можно сделать вывод, что способ обеспечивает получение ультрадисперсного карбоната кальция из природного карбоната кальция, что не требует дополнительных химических операций по приготовлению гидрооксида кальция, а также снижает потребление CO2, необходимого для проведения реакции в 2 раза (при отсутствии необходимости вторичного использования выделяющегося по схеме II углекислого газа).
Теоретические и экспериментальные исследования, включающие теоретическое обоснование и поиск оптимального режима проведения процесса, включали проведение процесса в условиях изменения величин давления, диапазона температур и использования исходного сырья - природного СаСО3 с иными техническими характеристиками (размером частиц менее 10 мкм и более 50 мкм), давления менее 8 атм и более 50 атм, температуры более 25 подтвердили наибольшую оптимальность выбранных значений для наиболее рационального проведения процесса с целью получения насыщенного гидрокарбоната кальция и далее кабоната кальция, имеющего необходимые технические характеристики, а именно требуемую величину частиц. Процесс начинают при величине избыточного давления CO2 8 атмосфер, что соответствует режиму насыщения реакционной смеси, причем увеличение давления до 50 атмосфер способствует увеличению скорости реакции тем самым способствуя сокращению времени ее проведения, используемый температурный режим от 0 до +25° соответствует диапазону максимальной растворимости CO2. Выбранная величина частиц 10-50 мкм является оптимальной для создания наиболее благоприятных условий, а именно способствует сокращению времени проведения процесса с использованием природного сырья и получению достаточного выхода промежуточного и конечного продуктов.
В условиях высокого давления СО2 при механическом перемешивании в водной среде происходит растворение карбоната кальция с образованием гидрокарбоната. Также при контакте дистиллята с СаСО3 происходит хемосорбция агрессивной углекислоты с образованием бикарбоната кальция по схеме

в результате прохождения процесса агрессивная углекислота полностью связывается, а рН повышается до величины 8-8,5, таким образом, осуществляется саморегулируемость процесса, при использовании пропорции 1 г агрессивной углекислоты и 2,5 г СаСО3 при достижении рН величины 8,5 практически, все присутствующие в воде ионы (98%) находятся в форме бикарбонатных ионов.
Ввиду неустойчивости высококонцентрированных водных растворов гидрокарбонат кальция при атмосферном давлении подвергается разложению с образованием нормального карбоната кальция СаСО3 и выделением СО2, остаточная концентрация гидрокарбоната кальция в воде при нормальном давлении не превышает 1 г/л. Поскольку образование карбоната кальция из водных растворов гидрокарбонатов кальция, при стравливании давления протекает довольно быстро, в условиях пониженной концентрации центров кристаллизации, то при таком процессе в объеме раствора образуется огромное количество зародышей кристаллизации, которые и определяют распределение частиц вторичного карбоната кальция по размерам и обуславливают его повышенную, по сравнению с исходным сырьем, дисперсность.
Таким образом применение предлагаемого способа позволяет получать насыщенный раствор гидрокарбоната кальция Са(НСО3)2 и ультрадисперсный карбонат кальция СаСО3 из природного сырья при снижении, как минимум, в 2 раза расхода углекислого газа, что способствует значительному упрощению способа и уменьшению его общей себестоимости.
Источники информации
1. Gomez-Morales J., Torrent-Burgues J., Lopes-Macipe A. et al., J. Cryst. Growth., 1996, v.166, № 1-4, p.1020.
2. Пат. Канады №2203210 АА от 21.10.1998, Porter A.L, Wilson W.J.
3. High speed manufacturing process for precipitated calcium carbonate employing sequential pressure carbonation, № П 2651356, IPC: C 01 F 11/18, 21.07.1999 г. (прототип).
4. Буянова Н.Е., Карнаухов А.П., Алабужев Ю.А., Определение удельной поверхности дисперсных и порошковых материалов, Новосибирск, 1978 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНЫХ ПОРОШКОВ КАРБОНАТОВ | 2006 |
|
RU2374176C2 |
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНЫХ ПОРОШКОВ КАРБОНАТОВ | 2013 |
|
RU2533143C1 |
| СПОСОБ ПОЛУЧЕНИЯ CaCO ИЛИ MgCO | 2005 |
|
RU2389687C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОГО РАСТВОРА БИКАРБОНАТА МАГНИЯ | 2018 |
|
RU2681622C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРТЛАНДЦЕМЕНТА | 2012 |
|
RU2509063C1 |
| СПОСОБ ОЧИСТКИ ПРИРОДНЫХ ВОД | 2013 |
|
RU2524965C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАТЕРИАЛА ДЛЯ НАПОЛНЕНИЯ И МОДИФИЦИРОВАНИЯ ДРЕВЕСНОЙ МАССЫ ПРИ ПРОИЗВОДСТВЕ БУМАГИ | 2024 |
|
RU2830297C1 |
| Способ получения оксида магния из природных рассолов и попутно добываемых вод нефтяных месторождений | 2021 |
|
RU2777082C1 |
| ГРАНУЛИРОВАННОЕ КОМПЛЕКСНОЕ УДОБРЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2702189C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИМИЧЕСКИ ОСАЖДЕННОГО МЕЛА | 2019 |
|
RU2709872C1 |
Изобретение относится к химической технологии неорганических веществ. Способ получения ультрадисперсного карбоната кальция включает карбонизацию водной суспензии исходного сырья в условиях избыточного давления углекислого газа. В качестве исходного сырья используют природный карбонат кальция с величиной частиц от 10 до 50 мкм. Процесс проводят при Т=0÷25°С и избыточном давлении углекислого газа от 8 до 50 атм без дополнительных стабилизаторов рН среды. Далее из полученного насыщенного водного раствора гидрокарбоната кальция путем снижения давления СО2 до величины атмосферного осаждают ультрадисперсный карбонат кальция. Технический результат заключается в повышении простоты и экономичности осуществления способа.
Способ получения ультрадисперсного карбоната кальция, включающий карбонизацию водной суспензии исходного сырья в условиях избыточного давления углекислого газа, отличающийся тем, что в качестве исходного сырья используют природный карбонат кальция с величиной частиц от 10 до 50 мкм, процесс проводят при Т=0÷25°С и избыточном давлении углекислого газа от 8 до 50 атм без дополнительных стабилизаторов рН среды, и далее, из получаемого при этом насыщенного водного раствора гидрокарбоната кальция путем снижения давления СО2 до величины атмосферного осаждают ультрадисперсный карбонат кальция.
| Способ получения химически осажденного мела | 1989 |
|
SU1717541A1 |
| ПНЕВМАТИЧЕСКАЯ ФЛОТАЦИОННАЯ МАШИНА | 2005 |
|
RU2284224C1 |
| CN 1429772 А, 16.07.2003 | |||
| US 4857291 A, 15.08.1989 | |||
| ГНУТЫЙ ПРОФИЛЬ ВЫСОКОЙ ЖЕСТКОСТИ | 2006 |
|
RU2317167C1 |
Авторы
Даты
2006-01-20—Публикация
2004-01-05—Подача