Область техники, к которой относится изобретение
Изобретение относится к способу биологической очистки сточных вод, бактериям и смешанной бактериальной популяции, подходящих для этого способа, и их применению. Кроме того, изобретение относится к биореактору, содержащему указанные бактерии или смешанную популяцию.
Описание уровня техники
Традиционно воду очищают физическими, а также химическими методами, например, путем осаждения, фильтрации или флоккуляции (WO 94/5866, WO 88/5334). Для того чтобы удалить органические вещества и другие вещества, которые трудно очистить, предпочтительно, используют также так называемую биологическую очистку, при которой очищаемую воду приводят в контакт с микроорганизмами, которые разлагают загрязняющие агенты. Способы биологической очистки пригодны для использования как в традиционных установках очистки воды, так и на промышленных установках очистки сточных вод. Биологическая очистка воды также испытана в системах с рециркуляцией воды (FI 964141). Биологическая очистка воды также является необходимой при очистке просачивающейся воды со свалки, например, до сброса этой воды в окружающую среду.
Однако способ биологической очистки труднее регулировать, чем физические или химические способы очистки. Во-первых, необходимо найти микроорганизмы, которые разлагают загрязняющие агенты. Во-вторых, эти микроорганизмы должны обладать способностью легко выживать и воспроизводиться в условиях протекания процесса очистки воды. Иными словами, применяемые для очистки воды микроорганизмы должны выдержать конкуренцию с другими организмами в воде для того, чтобы предотвратить отклонения в культивировании. Кроме того, микроорганизмы, применяемые для очистки воды, не должны обладать чувствительностью к изменениям их среды, что часто происходит в процессе очистки воды при изменении нагрузки.
Для очистки воды применяются многие виды микроорганизмов, включая бактерии и простейшие, такие как жгутиковые. Часто применяемые бактерии включают виды из рода Pseudomas, но также часто используют представителей из родов Alcagenes, Acinetobacter или Rhodococcus. Часто применяются смешанные популяции, отчасти идентифицированные и некоторые не идентифицированные, которые содержат большое число различных микроорганизмов. Лучше всего подходят для очистки воды аэробные микроорганизмы или организмы, способные жить в различных условиях, и в этом случае целесообразно нагнетать воздух в очищаемую воду для того, чтобы повысить эффективность процесса очистки.
При культивировании микроорганизмов обычно среду для выращивания необходимо стерилизовать для того, чтобы предотвратить культивирование от формирований, загрязненных внешними организмами. Поскольку при очистке сточных вод обрабатываются большие количества воды, для биологической очистки также требуются большие количества биомассы. Производство такой биомассы в стерильных условиях является трудоемкой и дорогой операцией; поэтому производство биомассы в нестерильных условиях, при отсутствии какой-либо опасности загрязнения формирований весьма желательно. Настоящее изобретение обеспечивает новую технологию ферментации, в которой отсутствует необходимость в стерилизации. Это возможно, если в способе используются особенно подходящие для этого способа микроорганизмы, причем эти микроорганизмы выращиваются на питательных веществах, подходящих для них.
Краткое изложение сущности изобретения
Настоящее изобретение относится к микроорганизмам, которые необычайно хорошо приспособлены к биологической очистке сточных вод. Эти микроорганизмы особенно хорошо соответствуют упомянутым выше требованиям, предъявляемым к микроорганизмам, подходящим для биологической очистки воды. Кроме того, микроорганизмы этого изобретения настолько специфичны, что их биомассу можно производить в нестерильных условиях, с использованием среды культивирования, в которой другие микроорганизмы неспособны конкурировать. Это обеспечивает большую экономию затрат и потребления энергии в процессе биологической очистки воды, причем результаты очистки воды также являются превосходными. Вода, очищенная согласно данному изобретению, пригодна даже для повторного использования.
Таким образом, изобретение относится к бактериям вида Bacillus DT-1, имеющим номер депонента DSM 12560, и их потомству, вида Pseudomonas DT-2, в последующем идентифицированным как Pseudomonas azelaica, имеющим номер депонента DSM 12561, и их потомству, и к бактериям прежнего вида Pseudomonas, названного теперь видом Rhizobium и имеющего номер депонента DSM 12562, и его потомству. Позднее, анализы 16S rДНК показали, что эта бактерия имеет наибольшее сходство с представителями рода Rhizobium, поэтому в последующем она будет рассматриваться в рамках этого рода. Кроме того, изобретение относится к следующим штаммам бактерий, облегчающим очистку воды: Pseudomonas azelaica DT-6, имеющий номер депонента DSM 13516, вид Azospirillium DT-10, имеющий номер депонента DSM 13517, Ancylobacter aquaticus DT-12, имеющий номер депонента DSM 13518, и Xanthobacter DT-13, имеющий номер депонента DSM 13519, и их потомству. Штаммы DSM 12560-12562 депонированы в Deutsche Saimnlung von Mikroorganismen und Zeilkulturen GmbH на 1 декабря 1998 и DSM 13516-13519 на 29 мая 2000 г.
Кроме того, изобретение относится к смешанной бактериальной популяции, отличающейся содержанием бактерий вида Bacillus DT-1, имеющим номер депонента DSM 12560, Pseudomonas azelaica DT-2, имеющим номер депонента DSM 12561, и/или вида Rhizobium DT-5, имеющего номер депонента DSM 12562, и их потомству.
Кроме того, изобретение относится к применению упомянутых выше бактерий или смешанной бактериальной популяции при очистке сточных вод и к способу очистки сточных вод, отличающемуся тем, что биологическую очистку воды осуществляют с помощью микроорганизмов, принадлежащих к группе вида Bacillus DT-1, имеющего номер депонента DSM 12560, Pseudomonas azelaica DT-2, имеющего номер депонента DSM 12561, и вида Rhizobium DT-5, имеющего номер депонента DSM 12562, и их потомству.
Кроме того, изобретение относится к биореактору, отличающемуся тем, что в нем содержатся микроорганизмы, принадлежащие к группе вида Bacillus DT-1, имеющего номер депонента DSM 12560, Pseudomonas azelaica DT-2, имеющего номер депонента DSM 12561, и вида Rhizobium DT-5, имеющего номер депонента DSM 12562, и их потомству. Биореактор представляет собой реактор, в котором осуществляется процесс биологической очистки.
Чертежи
Фиг.1 - схематический вид системы очистки просачивающейся воды.
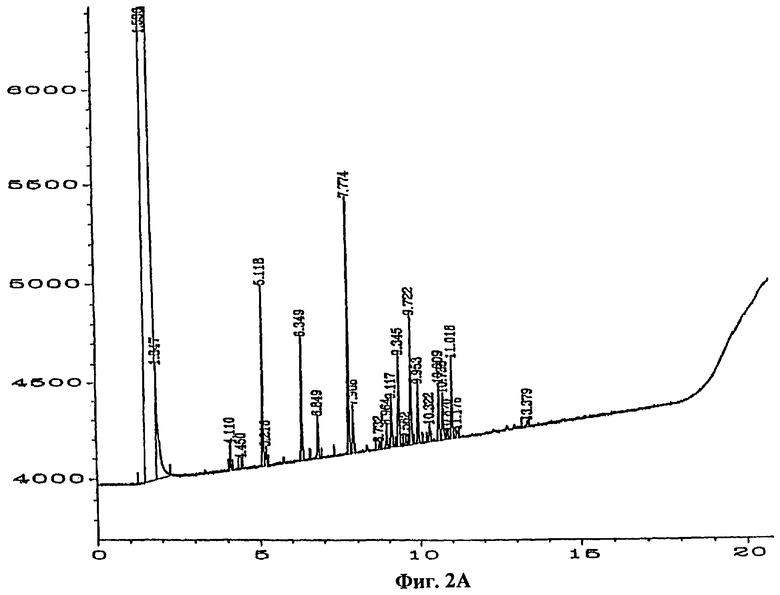
Фиг.2а - профиль жирных кислот бактериального штамма DT-1.
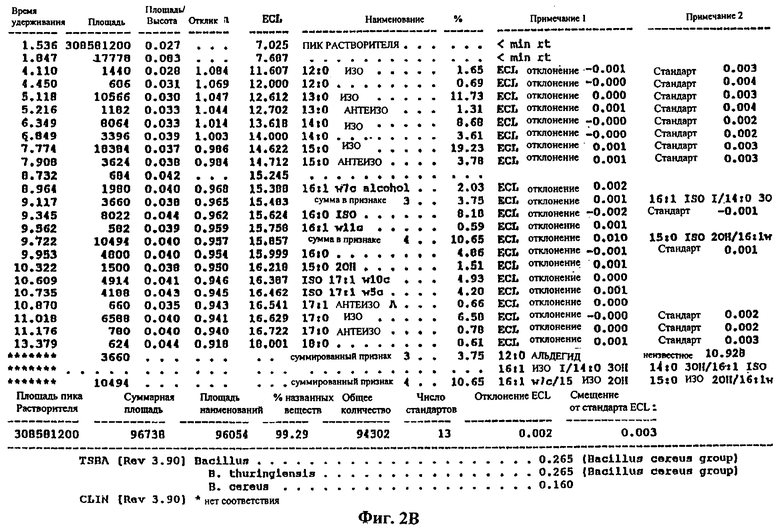
Фиг.2b - распечатка анализа жирных кислот бактериального штамма DT-1.
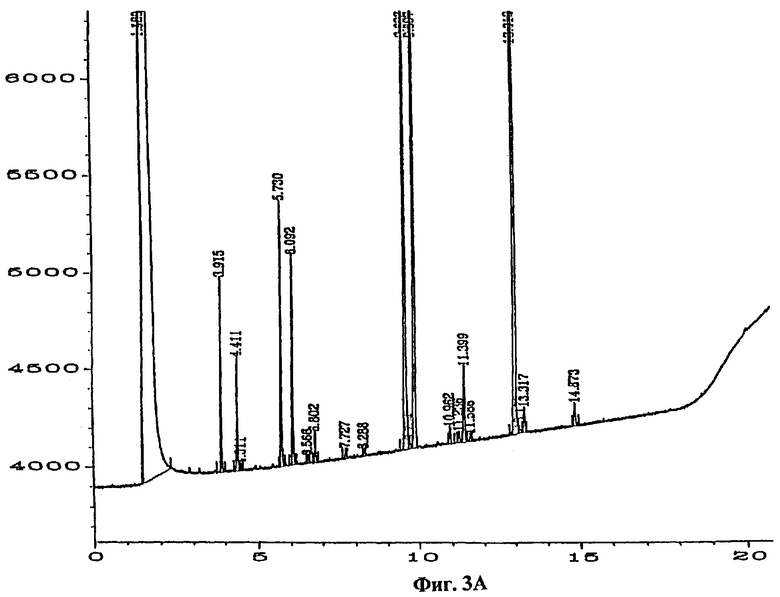
Фиг.3а - профиль жирных кислот бактериального штамма DT-2.
Фиг.3b - распечатка анализа жирных кислот бактериального штамма DT-2.
Фиг.4 - распечатка анализа жирных кислот бактериального штамма DT-5.
Фиг.5 - распечатка анализа жирных кислот бактериального штамма DT-6.
Фиг.6 - распечатка анализа жирных кислот бактериального штамма DT-10
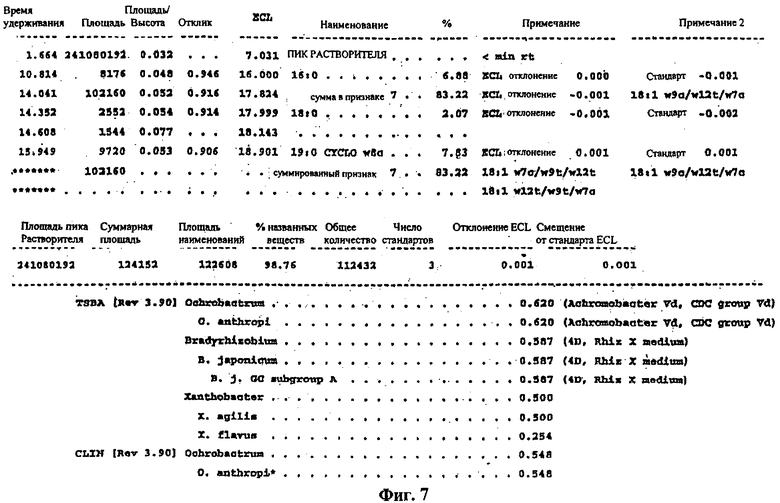
Фиг.7 - распечатка анализа жирных кислот бактериального штамма DT-12.
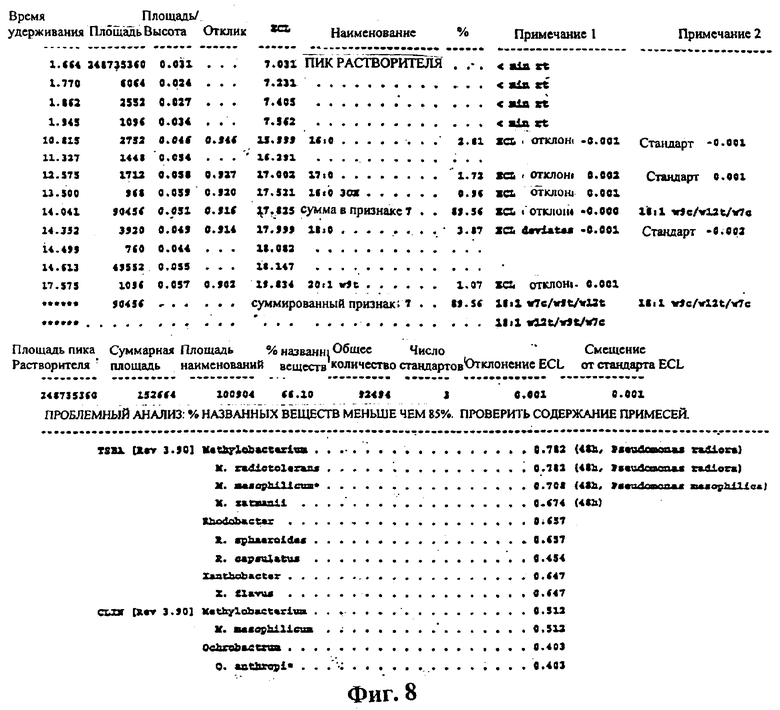
Фиг.8 - распечатка анализа жирных кислот бактериального штамма DT-13.
Подробное описание изобретения
Микроорганизмы, растущие в мыльной смеси, обогащают, удаляя сточную воду промышленной установки, и затем адаптируют их путем культивирования в биореакторе, содержащем сточные воды со свалки. Таким образом, выделяют три штамма бактерий, которые были лучше остальных. Указанные штаммы бактерий представляют собой виды: Bacillus DT-1, имеющий номер депонента DSM 12560, Pseudomonas azelaica DT-2, имеющий номер депонента DSM 12561, и вид Rhizobium DT-5, имеющий номер депонента DSM 12562. Эти бактерии могут культивироваться в водопроводной воде, содержащей 1-4 г/л мыла. В таких условиях могут активно расти только очень немногие микроорганизмы; поэтому эту среду культивирования не нужно стерилизовать при производстве биомассы указанных трех бактерий. Эти штаммы выдерживают весьма высокую концентрацию мыла, приблизительно до 40 г/л. Лучше всего они растут при концентрации мыла около 0,3-0,5 г/л.
Кроме способности расти в среде культивирования, в которой большинство других бактерий неспособны к воспроизводству, указанные штаммы бактерий весьма эффективны при удалении органических веществ из сточных вод. Обычно их содержание оценивают как общее ХПК, что означает общее химическое потребление кислорода (мг О2/л); Выделенные штаммы бактерий могут, в частности, разлагать соединения, которые трудно разлагаются, такие как хлорфенолы, полициклические ароматические углеводороды (соединения ПАУ) и масла. Они также удаляют тяжелые металлы. В объем данного изобретения входит также потомство указанных штаммов, относящееся к такому потомству указанных штаммов, которое обладает практически такой же производительностью при очистке сточных вод, как и депонированные штаммы.
Бактерии вида Bacillus DT-1, Pseudomonas azelaica DT-2, и вида Rhizobium DT-5 дополнительно имеют тенденцию к флоккуляции, и в этом случае они образуют так называемый биологический каркас, который включает комки, содержащие микроорганизмы и другие частицы, и который способствует очистке.
Особенно хорошие результаты при очистке сточных вод достигаются, когда при биологической очистке воды используют смешанную бактериальную популяцию, содержащую один или несколько видов бактерий, выбранных из группы, содержащей бактерии вида Bacillus DT-1, Pseudomonas azelaica DT-2, и вида Rhizobium DT-5 и их потомство. Наилучшие результаты при очистке достигаются при использовании смешанной популяции, которая включает все три штамма бактерий и/или их потомство. Кроме этих трех штаммов, смешанная бактериальная популяция может дополнительно содержать штаммы микроорганизмов, которые эффективны при очистке воды и которые оказывают благоприятное объединенное действие на производительность процесса очистки.
Наилучшие результаты при очистке достигаются, когда штаммы микроорганизмов DT-1, DT-2, и/или DT-5 используют совместно с одним или более штаммами бактерий из группы: Pseudomonas azelaica DT-6, имеющий номер депонента DSM 13516, вид Azospirillium DT-10, имеющий номер депонента DSM 13517, Ancylobacter aquaticus DT-12, имеющий номер депонента DSM 13518, и Xanthobacter DT-13, имеющий номер депонента DSM 13519, и их потомством. Указанные четыре штамма были выделены из биопленки последнего блока четырехкаскадного биореактора для очистки воды, содержащей различные мыла. Они могут быть выращены в той же самой среде культивирования и в тех же условиях, что и DT-1, DT-2, DT-5. Штаммы DT-6, DT-10, DT-12 и DT-13 улучшают иммобилизирующие (фиксирующие) свойства биопленки, которая поддерживает матрицы, когда они смешиваются со штаммами DT-1, DT-2, и DT-5. Объединение штаммов также улучшает процесс очистки сточных вод в результате повышенной стойкости образовавшейся биопленки к отравляющим веществам.
Вид Bacillus DT-1 представляет собой палочку шириной приблизительно 1,0-1,2 мкм и длиной 3,0-6,0 мкм. Определение частичной последовательности 16S rДНК показывает, что подобие с видом В. cereus составляет 99,3% и с видом В. thuringiensis - 100%. В тестах идентификации DT-1 реагирует, как показано ниже:
Pseudomonas azelaica DT-2 представляет собой палочку шириной приблизительно 0,5-0,7 мкм и длиной 1,5-3,0 мкм с 1-3 полярными жгутиками, причем флуоресцирующие пигменты отсутствуют. Определение частичной последовательности 16S rДНК показывает, что подобие с видом Pseudomonas azelaica составляет 99,8%. Штамм DT-2 реагирует, как показано ниже:
Вид Rhizobium DT-5 представляет собой палочку шириной приблизительно 0,5-0,7 мкм и длиной 1,5-3,0 мкм. Определение частичной последовательности 16S rДНК показывает, что подобие с родом R. giardini составляет 98,6% и подобие с родом Phyllobacterium myrisinacearum составляет 98,6%. Ниже приведены результаты физиологического теста, которые не подтверждают ни один из этих родов.
Прочие морфологические, физиологические и биохимические характеристики штаммов бактерий DT-1, DT-2 и DT-5 показаны в табл.1.
Морфологические, физиологические и биохимические характеристики штаммов бактерий DT-1, DT-2 и DT-5
Кроме того, были определены профили жирных кислот для штаммов бактерий DT-1, DT-2 и DT-5, которые показаны на фиг.2-4. Бактерии выращивали 24 ч при температуре 28°С на триптоновом агаре соевого бульона, причем для анализа жирных кислот цельной клетки были приготовлены метиловые эфиры кислот, как описано в публикации ″Структура и состав биологической слизи на машинах по производству бумаги и картона″, Appl. Environ. MicrobioL, т.60, с.641-653 Vaisanen, O.M., E-L.Nurmiaho-Lassila, S.A.Marmo and M.S.Salkinoja-Salonen. (1994). Была использована библиотека аэробного TSBA, версия 3.9 (MIDI Inc. Newark, DE, USA). Время удерживания (в минутах) показано на оси ″х″ фигур 2а и За, а интенсивность пика показана на оси ″у″ тех же самых фигур. Соответствующие распечатки анализов жирных кислот приведены на фиг.2b, 3b и 4. Профиль жирных кислот DT-1 является типичным для группы В. cereus. Профиль DT-2 является типичным для РНК группы 1 псевдомонад, и профиль DT-5 указывает на группу Rhizobium.
Pseudomonas.azelauca DT-6 представляет собой грам-отрицательную подвижную палочку шириной 0,5-0,7 мкм и длиной 1,5-3,0 мкм, имеющую 1-3 полярных жгутика, причем флуоресцирующие пигменты отсутствуют. Распечатка анализа жирных кислот (фиг.5) является типичной для РНК группы I псевдомонад. Определение частичной последовательности 16S rДНК показывает, что подобие с видом Ps. azelaica DT-6 составляет 99,8%. Штамм DT-6 обладает следующими физиологическими реакциями:
Вид Azospirillium DT-10 представляет собой грам-отрицательную палочку шириной 0,8-1,2 мкм и длиной 2,0-4,0 мкм. Распечатка анализа жирных кислот (фиг.6) является типичной для α-подгруппы протеобактерий и указывает на род Azospirillium. Определение частичной последовательности 16S rДНК показывает, что подобие с другими представителями рода Azospirillium составляет между 92% и 97,4%. Наибольшее подобие отмечено для Azospirillium lipoferum. Физиологические реакции штамма DT-10 показаны ниже. Они указывают на род Azospirillium, но не являются типичными для A. Lipoferum. Вероятно, DT-10 является новым видом этого рода.
Вид Ancylobacter aquaticus DT-12, представляет собой грам-отрицательную искривленную палочку шириной 0,5-0,7 мкм и длиной 1,5-2,0 мкм. Определение частичной последовательности 16S rДНК показывает, что подобие с Ancylobacter aquaticus составляет 98,8%, а подобие с Tiobacillus novellus составляет 97,8%. Анализ жирных кислот (фиг.7) указывает на α-протеобактерии. Показанные ниже данные физиологических тестов ясно идентифицируют вид Ancylobacter aquaticus.
Вид Xanthobacter DT-13 представляет собой неправильную грам-отрицательную подвижную палочку шириной 0,8-1,0 мкм и длиной 1,5-3,0 мкм. Определение частичной последовательности 16S rДНК показывает, что подобие с другими представителями рода Xanthobacter составляет от 98,5 до 99,3%, причем максимальное подобие отмечено с X. falvus (99,3%). Профиль жирных кислот является типичным для α-подгруппы протеобактерий. С помощью физиологических тестов не удалось провести надежное различие между видами этого рода (т.е. не обнаружено никакого образования пигмента и слизи). Данные физиологических тестов показаны ниже:
Описанные выше бактерии пригодны для использования при очистке сточных вод. Затем бактерии можно культивировать сначала в минимальной солевой среде (KSN) в шейкере. По желанию, можно добавлять соевый пептон (0,5 г/л), триптон (0,1 г/л), глюкозу (0,2 г/л) и ацетат калия (0,3 г/л). Температура культивирования бактерий составляет приблизительно 20-30°С. После этого увеличивают объем культуры, для того чтобы получить необходимую биомассу для очистки воды. Теперь нет необходимости осуществлять эту стадию в стерильных условиях, и в этом случае в качестве среды для выращивания можно использовать водопроводную воду, в которую добавлено приблизительно 0,5-4 г/л мыла. Предпочтительно применяемое мыло представляет собой смесь, содержащую анионные, катионные, амфотерные и неионные поверхностно-активные вещества. Предпочтительно использовать смесь различных видов мыла, таких как очищающие агенты, кондиционеры тканей и моющие средства для белья и посуды. Бактерии выращиваются в виде погруженной в воду культуры, в которую закачивается воздух. Биомасса культуры может быть получена в периодическом процессе, но предпочтительно ее получают непрерывно, в виде хемостатной культуры. При производстве биомассы предпочтительно используют носитель. Для этой цели подходит любой обычный носитель, например пластиковый. Затем полученную биомассу переносят в реактор для очистки воды, в который подают воду, предназначенную для очистки. В этом реакторе также используют носитель для бактерий, который предпочтительно является таким же, что используют при получении биомассы. Предпочтительно носитель имеет удельную плотность меньше чем 1 г/см3. Обычно носитель удерживается на месте в емкости, например, с помощью сетки (″фиксированный носитель″), но иногда носитель оставляют свободно плавать на поверхности воды в емкости (″плавающий носитель″).
Способ, согласно настоящему изобретению, особенно подходит для очистки воды, просачивающейся со свалки, и далее описан более подробно со ссылкой на фиг.1. Обычно свалка окружена канавой для сбора просачивающейся воды. Просачивающейся водой считается вода, поступающая со свалки из-за дождей и грунтовых вод. Эта просачивающаяся вода, содержащая как поверхностную воду, так и воду котловины, обычно сначала поступает в резервуар, в котором вода проходит через процесс очистки, прежде чем ее выбрасывают в окружающую среду. Вода, просачивающаяся как из глубокого грунта, так и из мелководного грунта, предпочтительно сначала поступает в отстойный бассейн, из которого она фильтруется через входную трубу 1 в колодец фильтрата 2, и из него, через транспортирующую трубу 8, в биореактор 3, содержащий указанные бактерии и носитель 5. Бактерии образуют вокруг носителя так называемую биопленку. Этот носитель вместе с бактериями обычно поддерживают ниже поверхности воды с помощью сетки. Предпочтительно биореактор содержит одну или несколько разделяющих перегородок 6, предназначенных для интенсификации циркуляции воды в реакторе. Эти разделяющие перегородки могут быть расположены на противоположных стенках, как, например, показано на фиг.1. Обычно, реактор дополнительно содержит аэратор 9 для подачи воздуха в реактор через трубу аэрации 4. Кроме того, биореактор содержит выходную трубу, из которой выходит очищенная вода.
Кроме очистки просачивающейся воды настоящее изобретение очень хорошо применимо для очистки бытовой и промышленной ″серой″ воды. Серой водой называют сточные воды, отличающиеся от воды из туалетов, например вода из душевых, рукомойников, ванных и прачечных помещений. Способ очистки, согласно изобретению, также применим для очистки сточных вод из туалетов, которые называют черной водой. Способ изобретения также можно использовать для очистки воды из прачечных и промышленных сточных вод, которые часто содержат большое количество органических загрязнений, таких как масла, полициклические ароматические углеводороды (соединения ПАУ) и/или тяжелые металлы. Данный способ также подходит для очистки сточных вод предприятий пищевой промышленности и для очистки воды в плавательных бассейнах.
Пример 1. Получение биомассы и пуск биореактора
Бактерии вида Bacillus DT-1, Pseudomonas azelaica DT-2, и вида Rhizobium DT-5 отдельно переносят в 200 мл стерилизованной минимальной солевой среды (KSN), имеющей следующий состав (г/л дистиллированной воды): 1,0 К2HPO4х3Н2O, 0,25 Na2HPO4x2H2O, 0,1 (NH4)2SO4, 0,04 MgSO4, 0,01 Са(NO3)2х4Н2O, 0,05 дрожжевого экстракта, рН 7,0 - 7,3 и приблизительно 1 г/л смеси мыла. Смесь мыла содержит приблизительно равные количества следующих моющих средств: хозяйственное мыло, Comfort, Cleani Family - промышленный кондиционер, Cleani Color, Serto Ultra, Bio Luvil, Ariel Futur, Ото Color, Tend Color, Tend Mega, Tend Total и Eko Kompakt (всего около 1 г/л). Бактерии культивируют в шейкере, при скорости 150-200 об/мин и температуре 28°С.
Когда культура становится плотной, все три культуры переносят в один аппарат ферментации емкостью 500 л для того, чтобы получить необходимое количество биомассы. Этот ферментер содержит нестерилизованную водопроводную воду, всего 4 г/л указанной выше смеси мыл, и пластиковый носитель из полиэтилена, имеющий удельную плотность около 0,8 г/см3. Носитель поддерживают ниже поверхности жидкости с помощью сетки. Теперь продолжают культивирование в нестерильных условиях до степени помутнения около 2 (при 600 нм) и затем в виде хемостатной культуры. Затем первый инокулят, полученный из ферментера, вводят в разбавлении 1:10 в биореактор емкостью 6 м3, показанный на фиг.1. Этот биореактор содержит воду, просочившуюся с городской свалки, которую сначала собирают в емкости, из которой ее затем переводят в отстойный бассейн для удаления твердого вещества и затем в колодец фильтрата, из которого ее закачивают в биореактор. Вообще, система работает под действием гравитации, причем требуется единственный погружной насос в колодце фильтрата. Биореактор содержит тот же самый носитель, что и ферментер, используемый для производства биомассы. Носитель поддерживают ниже поверхности жидкости с помощью сетки. В конце биореактора бактерии флоккулируют. Процесс очистки протекает непрерывно с рабочей производительностью около 100 м3/сутки. Воздух закачивают таким образом, чтобы поддерживать содержание кислорода в очищаемой воде более 7 мг/л.
Пример 2. Очистка просачивающейся воды
Для очистки воды, просочившейся с городской свалки, используют биореактор, оснащенный, как указано в примере 1. Среднее значение химического поглощения кислорода (ХПК) в очищаемой сточной воде составляет приблизительно 0,8-6 г О2/л. Эта сточная вода содержит, например, хлорфенолы, полициклические ароматические углеводороды (ПАУ) и масла. Удаление этих веществ из сточной воды контролируется, в соответствии с техническим отчетом Nordtest′s №329 (принят 9603), с помощью газового хроматографа, оборудованного масс-селективным детектором. Результаты приведены в табл.2.
Пример 3. Полномасштабная очистка муниципальных сточных вод
Сточные воды из городской установки сточных вод очищали как традиционным способом, применяемым на этой установке, так и способом, согласно данному изобретению. Традиционно, сточные воды очищают, подавая их сначала в предварительный отстойный бассейн для осаждения твердых веществ на дно. Затем предварительно отстоянную воду подают в бассейн аэробной очистки, куда добавляют сульфат железа (II) для осаждения фосфата и полиамин для осаждения биошлама. Из этого бассейна очистки воду подают далее во второй отстойный бассейн. Система очистки, согласно данному изобретению, включает пять резервуаров (танков) с суммарным объемом 7,5 м3, причем эти танки взаимно связаны следующим образом: два анаэробных танка, в которые добавляют бактерии DT-1, DT-2 и DT-5 без носителя, один аэробный танк, в котором имеется носитель (прикреплен с помощью сетки), на котором фиксируются бактерии DT-1, DT-2 и DT-5, и два танка для осаждения. Температуру процесса поддерживают при 8-15°С, скорость потока сточной воды составляет 7,5 м3/сутки. Аэрация осуществляется путем рециркуляции воды через носитель. Результаты приведены в табл.3.
Результаты очистки, полученные по предлагаемому способу, являются такими же хорошими или превосходят результаты, достигнутые по традиционному способу, а потребление энергии в предлагаемом способе существенно ниже. При очистке одного кубометра воды на городской установке очистки сточных вод потребляется 0,23 кВт-ч энергии, в то время как при использовании способа, согласно данному изобретению, потребляется только 0,05-0,1 кВт-ч энергии.
Пример 4. Полномасштабная очистка бытовой черной воды
Система очистки включает пять танков с суммарным объемом 6,5 м3, причем эти танки взаимно связаны следующим образом: два анаэробных танка, в которые добавляют бактерии DT-1, DT-2 и DT-5, один аэробный танк, в котором имеется носитель, на котором фиксируются бактерии DT-1, DT-2 и DT-5, и два танка для осаждения. Температуру процесса поддерживают при 8-15°С, скорость потока сточной воды составляет 0,5-5 м3/сутки. Аэрация осуществляется путем рециркуляции воды через носитель. Потребление энергии составляет 0,05-0,5 кВт-ч Результаты приведены в табл.4.
Пример 5. Очистка промышленных сточных вод, содержащих мыла и тяжелые металлы (лабораторный масштаб)
Сточные воды промышленной установки металлопокрытий очищают с помощью системы, в которой часть эффективной очистки включает шесть анаэробных и двенадцать аэробных танков. Бактерии DT-1, DT-2, и DT-5, которые зафиксированы на носителе, закрепленном сеткой, добавляют во все анаэробные и аэробные танки. В каждом танке содержатся 2 л. Вся система, состоящая из 23 танков, имеет общий объем 70 л, причем эти танки взаимно связаны следующим образом: шесть анаэробных танков (эффективный объем очистки), один танк для осаждения, шесть аэробных танков (эффективный объем очистки), один танк для осаждения, шесть аэробных танков (эффективный объем очистки), и два танка для обработки хлористым кальцием и гидроксидом натрия для того, чтобы осадить биомассу и тяжелые металлы. До очистки исходную сточную воду разбавляют в пять раз серой водой. После разбавления добавляют следующие минеральные соли: 2-10 мг/л NH4 +, 5-20 мг/л NO3 -, 2-10 мг/л Mg2+, 0,5-2 мг/л Са2+, 1-10 мг/л SO4 2- и 2-20 мг/л PO4 3-. Температуру процесса поддерживают при 20-35°С, скорость потока воды составляет 12 л/сутки. Результаты приведены в табл.5.
Пример 6. Очистка бытовой серой воды для рециркуляции (опытный масштаб)
Эффективная часть системы включает три аэробных танка объемом по 0,2 м3. Вся система содержит шесть танков с суммарным объемом 2,8 м3, причем эти танки взаимно связаны следующим образом: один танк для сбора серой воды, три аэробных танка, содержащих закрепленный носитель, на котором фиксируются бактерии DT-1, DT-2 и DT-5 (эффективный объем очистки), один аэробный танк без носителя и один танк для осаждения и последующая система фильтрации и система обработки ультрафиолетовым излучением. Температуру процесса поддерживают при 20-35°С, скорость потока воды составляет около 1 м3/сутки. Результаты приведены в табл.6.
Пример 7. Очистка серой воды прачечной для рециркуляции (опытный масштаб)
Эффективная часть системы включает два аэробных танка, имеющих объем 1 м3, танки, содержащие плавающий носитель, на котором фиксируются бактерии DT-1, DT-2 и DT-5. Вся система содержит десять танков с суммарным объемом 23 м3, причем эти танки взаимно связаны следующим образом: один танк для сбора серой воды, два аэробных танка, содержащих плавающий носитель (эффективный объем очистки), один танк для осаждения, три аэробных танка, содержащих закрепленный носитель с бактериями (эффективный объем очистки), один аэробный танк без носителя и два танка для осаждения. Температура воды составляет 20-35°С, скорость потока сточной воды составляет 1 м3/сутки. Результаты приведены в табл.7.
Пример 8. Приращение зафиксированной биомассы
Биомассу штаммов DT-1, DT-2, DT-5, DT-6, DT-10, DT-12 и DT-13 получают и фиксируют на носителе, как изложено в примере 1, причем взвешивают количество биомассы на носителе. Вес одного диска носителя составляет 72±1 г. При фиксации штаммов DT-1, DT-2 и DT-5 на носителе вес одного диска носителя составляет 119±13 г, т.е. вес влажной биомассы на одном диске составляет 47±11 г. При фиксации всех семи штаммов бактерий на носителе вес одного диска носителя составляет 172±16 г, т.е. вес влажной биомассы составляет 91±16 г. Эти результаты показывают, что штаммы DT-6, DT-10, DT-12 и DT-13 дают почти двукратный прирост зафиксированной биомассы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм бактерий Pseudomonas monteilii, используемый для очистки сточных вод от одноатомных спиртов, его применение и способ очистки сточных вод от одноатомных спиртов с использованием данного штамма | 2024 |
|
RU2834754C1 |
| Штамм бактерий РSеUDомоNаS меNDосINа, используемый для очистки сточных вод от сульфонола, синтамида и синтанола | 1989 |
|
SU1640155A1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ФЕНОЛЬНЫХ СОЕДИНЕНИЙ | 2011 |
|
RU2476385C1 |
| ШТАММ БАКТЕРИИ THIOBACILLUS THIOPARUS, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ОЧИСТКИ ПРОМЫШЛЕННЫХ ОБОРОТНЫХ ВОД ОТ ТИОЦИАНАТ-ИОНА | 2021 |
|
RU2758291C1 |
| СПОСОБ ОЧИСТКИ КОНЦЕНТРИРОВАННЫХ СТОЧНЫХ ВОД | 2003 |
|
RU2264988C2 |
| Способ биологической очистки сточных вод от легких углеводородов | 2020 |
|
RU2749856C1 |
| Штамм бактерий АеRомоNаS caVIae SK - деструктор капролактама и неионогенных поверхностно-активных веществ | 1990 |
|
SU1740330A1 |
| Штамм бактерий Gordonia desulfuricans, используемый для очистки сточных вод от одноатомных спиртов, его применение и способ очистки сточных вод от одноатомных спиртов с использованием данного штамма | 2024 |
|
RU2834709C1 |
| Способ микробиологической очистки промышленных сточных вод от амфолитных ПАВ | 1987 |
|
SU1463761A1 |
| СПОСОБ МИКРОБНОЙ ОЧИСТКИ СТОЧНЫХ ВОД И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1996 |
|
RU2121459C1 |




Изобретение относится к биологической очистке сточных вод. Предложенный способ биологической очистки предусматривает взаимодействие сточных вод с микроорганизмами, принадлежащими к группе Bacillus DT-1, Pseudomonas azelaica DT-2 и Rhizobium DT-5. Способ обеспечивает экономию энергозатрат, при сохранении качества очистки воды. Также предложено средство и смешанная бактериальная популяция для биологической очистки сточных вод. Предложенная группа изобретений может быть использована для очистки бытовой и промышленной воды. 4 н. и 5 з.п. ф-лы, 8 ил., 7 табл.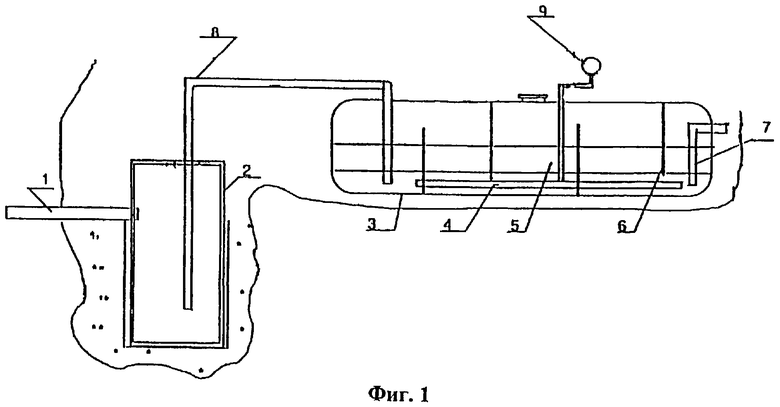
| US 4605502, 12.08.1986 | |||
| 0 |
|
SU290605A1 | |
| СПОСОБ БИОЛОГИЧЕСКОЙ ОЧИСТКИ СТОЧНЫХ ВОД, СОДЕРЖАЩИХ НИТРОЦЕЛЛЮЛОЗУ | 1993 |
|
RU2026830C1 |
| СПОСОБ БИОЛОГИЧЕСКОЙ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ОРГАНИЧЕСКИХ ПРИМЕСЕЙ | 1970 |
|
SU431121A1 |
| Установка для очистки галогенидных солей | 2018 |
|
RU2696474C1 |
| БИОЛОГИЧЕСКИЙ РЕАКТОР | 1989 |
|
SU1736100A1 |
| SU 1686799, 27.06.1997. | |||
Авторы
Даты
2006-03-27—Публикация
2000-07-06—Подача